요산
Uric acid
| | |||
 편광 중의 요산염 결정 | |||
| 이름 | |||
|---|---|---|---|
| 우선 IUPAC 이름 7,9-디히드로-1H-푸린-2,6,8(3H)-트리온 | |||
| 기타 이름 2,6,8-트리옥시푸린, 2,6,8-트리히드록시푸린, 2,6,8-트리옥소푸린, 1H-푸린-2,6,8-트리온 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 3 DMet | |||
| 156158 | |||
| 체비 | |||
| 첸블 | |||
| 켐스파이더 | |||
| 드러그뱅크 | |||
| ECHA 정보 카드 | 100.000.655 | ||
| EC 번호 |
| ||
| 케그 | |||
| 메쉬 | 요산 | ||
PubChem CID | |||
| 유니 | |||
CompTox 대시보드 (EPA ) | |||
| |||
| 특성. | |||
| C5H4N4O3 | |||
| 몰 질량 | 168.112g/160g/표준−1 | ||
| 외모 | 백색 결정 | ||
| 녹는점 | 300 °C (572 °F, 573 K) | ||
| 6 mg/100 mL (20 °C에서) | |||
| 로그 P | −1.107 | ||
| 산도(pKa) | 5.6 | ||
| 기본성(pKb) | 8.4 | ||
자화율(δ) | - 6.62 × 10−53 cm−1 mol | ||
| 열화학 | |||
열용량 (C) | 166.15 J−1 K−1 mol (24.0 °C에서) | ||
표준 어금니 엔트로피 (S | 173.2 J K−1−1 몰 | ||
표준 엔탈피/ 형성 (δHf⦵298) | -619.69 ~ -617.93 kJ−1 몰 | ||
표준 엔탈피/ 연소 (δHc⦵298) | -1921.2 ~ -1919.56 kJ−1 몰 | ||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
요산은 탄소, 질소, 산소, 수소로 이루어진 복소환 화합물이며 공식은5443 CHNO이다.그것은 요산암모늄산 요산염과 산성 요산염으로 알려진 이온과 소금을 형성합니다.요산은 퓨린 뉴클레오티드의 대사 분해 산물로 소변의 정상적인 성분이다.요산의 고농도는 통풍을 일으킬 수 있으며 당뇨병과 요산암모늄산 신장결석의 형성과 같은 다른 질병과 관련이 있습니다.
화학
요산은 1776년 스웨덴의 화학자 칼 빌헬름 [1]쉴레에 의해 신장결석으로부터 처음 분리되었다.1882년 우크라이나 화학자 이반 호르바체프스키가 요소를 글리신에 [2]녹여 요산을 처음 합성했다.
요산은 락탐-락탐 호변이성(케토-에놀 호변이성이라고도[3] 함)을 나타낸다.락팀 형태는 어느 정도 방향성을 가질 것으로 예상되지만 요산은 락탐 [4]형태로 결정되며, 계산화학 또한 호변이체가 가장 [5]안정적이라는 것을 나타낸다.요산은 pKa1 = 5.4, pKa2 = 10.[6]3인 디프로톤산이며, 따라서 생리학적 pH에서는 주로 요산 이온으로 존재한다.
 | 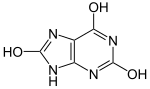 | pKa1 | 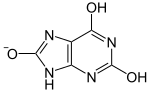 | |
| 락탐 형태 | 락팀 형태 | 요산 이온 |
수용성
일반적으로 요산과 그 알칼리 금속 및 알칼리 토류염의 수용도는 다소 낮다.이 모든 소금은 냉수보다 뜨거운 물에서 용해성이 높아 재결정화가 용이합니다.이 낮은 용해도는 통풍의 병인에 중요하다.에탄올에서 산과 산염의 용해도는 매우 낮거나 무시할 수 있다.에탄올/물 혼합물에서 용해성은 순수한 에탄올과 순수한 물의 최종값 사이에 있습니다.
요산염의 용해성(화합물 1g당 물그램) 컴파운드 차가운 물 끓는 물 요산 15,000 2,000 요산수소암모늄 — 1,600 요산 리튬 370 39 요산수소나트륨 1,175 124 요산수소칼륨 790 75 이수소 마그네슘 3,750 160 이수소이산칼슘 603 276 요산나트륨 77 — 요산2칼륨 44 35 요산칼슘 1,500 1,440 요산 스트론튬 4,300 1,790 요산바륨 7,900 2,700
표시된 수치는 표시된 화합물의 단위 질량을 용해하는 데 필요한 물의 질량을 나타냅니다.수치가 낮을수록 해당 [7][8][9]용매에 용해성이 높은 물질이다.
생화학
크산틴 산화효소(포유동물에서 주로 크산틴 탈수소효소로 발견되고 드물게 산화효소로[10] 발견됨)는 크산틴과 하이포산틴으로부터 요산의 형성을 촉매하는 효소이다.크산틴산화효소는 활성 부위가 유황과 [11]산소에 결합된 금속 몰리브덴으로 구성된 큰 효소이다.세포 내에서 크산틴 산화효소는 크산틴 탈수소효소 및 크산틴 옥시레듀케아제로서 존재할 수 있으며, 크산틴 옥시레듀케아제 또한 소젖 및 비장 [12]추출물로부터 정제되었다.요산은 저산소 상태(산소 [13]포화도 낮음)에서 방출됩니다.
유전적, 생리적 다양성
영장류.인간과 다른 유인원에서 요산(실제로 요산수소 이온)은 푸린 대사의 최종 산화물이며 소변으로 배설되는 반면, 대부분의 다른 포유동물에서 요산 효소는 요산을 알란토인으로 [14]산화시킨다.고등 영장류에서 요산가수분해효소의 손실은 아스코르브산을 합성하는 능력의 손실과 유사하며,[15] 요산가 이러한 종에서 부분적으로 아스코르브산을 대체할 수 있다는 제안을 이끌어낸다.요산과 아스코르브산은 모두 강력한 환원제(전자 공여체)이며 강력한 항산화제이다.사람의 경우 혈장의 항산화 능력의 절반 이상이 요산수소 [16]이온에서 나온다.
사람. 사람 혈액 중 요산(또는 요산수소 이온)의 정상 농도 범위는 남성이 25~80mg/L, 여성이 15[17]~60mg/L이다(단, 값은 약간 다르다).개인은 96mg/L의 혈청값을 가질 수 있으며 [18]통풍에 걸리지 않는다.사람의 경우, 하루 요산 처리의 약 70%가 신장을 통해 발생하며, 사람의 5~25%에서 신장([19]키드니) 배설 장애는 고요산혈증으로 이어진다.소변 내 요산의 정상 배설량은 하루 270~360mg이다(하루 1L의 소변이 생성되는 경우 270~360mg/L 농도 – 용존산 요산염 형태이므로 요산의 용해도보다 높다).https://www.ncbi.nlm.nih.gov/books/NBK562201/
개. 달마시안 개는 간과 신장의 요산 흡수에 유전적 결함이 있어 알란토인으로의 전환이 감소하기 때문에 알란토인이 아닌 요산을 [20]소변으로 배출한다.
새와 파충류.새와 파충류, 그리고 사막에 사는 포유동물(예: 캥거루 쥐)에서 요산은 푸린 대사의 최종 산물이지만, 건조한 덩어리로 대변에 배설됩니다.이는 요소(요소회로)나 암모니아와 같은 다른 질소 폐기물의 처리에 비해 에너지적으로 비용이 많이 들지만 수분 손실을 줄이고 [21]탈수를 방지하는 장점이 있는 복잡한 대사 경로를 포함한다.
무척추동물.해양성 다발충인 Platynereis dumerili는 요산을 성적 페로몬으로 사용한다.이 종의 암컷은 짝짓기 중에 요산을 물에 방출하여 [22]수컷이 정자를 방출하도록 유도한다.
유전학
비록 고기와 해산물과 같은 음식이 혈청 요산 수치를 높일 수 있지만, 유전적 변이는 혈청 요산 수치가 [23][24]높은 데 훨씬 더 큰 기여를 합니다.신장에 의한 요산 배설의 원인이 되는 요산 수송 단백질에 돌연변이가 있는 사람의 비율.혈청 요산염과 연결된 다수의 유전자의 변이가 지금까지 확인되었다. SLC2A9; ABCG2; SLC17A1; SLC22A11; SLC22A12; SLC16A9; GCKR; LRC16A; PD9K1.[25][26][27]
임상적 의의와 연구
사람의 혈장에서 요산의 기준 범위는 일반적으로 남성의 경우 100mL당 3.4~7.2mg(200~430μmol/L), 여성의 경우 100mL당 2.4~6.1mg(140~360μmol/L)[30]이다.혈장 내 요산 농도는 정상범위 이상 및 이하인 것을 각각 고요산혈증 및 저요산혈증으로 알려져 있다.마찬가지로 소변의 요산 농도가 정상보다 높고 낮은 것을 고요도뇨와 저요도뇨라고 합니다.타액의 요산 수치는 혈중 요산 [31]수치와 관련이 있을 수 있다.
고요산
통풍을 유발하는 고요산혈증(고농도 요산)은 다양한 잠재적 원인이 있다.
- 다이어트가 한 요인이 될 수 있다.식이 푸린, 고과당 옥수수 시럽, 수크로스의 높은 섭취는 요산 [32][33]수치를 증가시킬 수 있습니다.
- 혈청 요산은 [34]신장을 통한 배설 감소로 증가할 수 있다.
- 금식이나 급격한 체중 감소는 일시적으로 요산 [35]수치를 높일 수 있다.
- 티아지드 이뇨제와 같은 특정 약물은 신장 [36]청결을 방해함으로써 혈중 요산 수치를 높일 수 있다.
- 종양 용해 증후군은 핵산염기와 칼륨이 혈장으로 방출되어 특정 암이나 화학 요법의 대사 [37]합병증이다.
통풍
2011년 미국의 한 조사에 따르면 인구의 3.9%가 통풍을 앓고 있는 반면,[38] 21.4%는 증상이 없는 고요산혈증을 앓고 있는 것으로 나타났다.
과다한 혈중 요산은 관절, 모세혈관, 피부 및 기타 [40]조직에 침전하는 바늘 모양의 요산 결정으로 인해 발생하는 고통스런 질환인 [39]통풍을 유발할 수 있습니다.통풍은 혈청 요산 수치가 100 mL당 6 mg(357 μmol/L)일 때 발생할 수 있지만, 개인은 100 mL당 9.6 mg(565 μmol/L)의 혈청 값을 가질 수 있으며 [18]통풍은 없다.
인간의 경우 푸린체는 요산으로 대사되고 요산은 소변으로 배출됩니다.푸린체가 풍부한 음식, 특히 육류와 해산물의 대량 섭취는 통풍의 [41]위험을 증가시킨다.푸딩이 풍부한 음식에는 간, 신장, 단빵이 포함되며 멸치, 청어, 정어리, 홍합, 가리비, 송어, 해덕, 고등어,[42] 참치를 포함한 특정 종류의 해산물이 포함됩니다.그러나 푸린체가 풍부한 채소를 적당히 섭취하는 것은 [41]통풍의 위험 증가와 관련이 없다.
19세기 통풍에 대한 한 가지 치료법은 리튬염의 [43]투여였다; 요산리튬은 용해성이 더 높다.오늘날 발작 중의 염증은 NSAIDs, 코르히틴 또는 코르티코스테로이드로 더 일반적으로 치료되고 요산염 수치는 알로푸리놀로 [44]관리된다.크산틴산화효소를 약하게 억제하는 알로푸리놀은 크산틴산화환원효소에 의해 2-위치로 히드록실화되어 옥시푸리놀을 [45]생성하는 히포산틴 유사체이다.
종양용해증후군
혈액암으로 인해 발생할 수 있는 응급상태인 종양용해증후군은 종양세포가 자연적으로 또는 화학요법 [37]후에 혈액으로 내용물을 방출할 때 혈액에서 높은 요산 수치를 생성한다.종양 용해 증후군은 [37]요산 결정이 신장에 축적되면 급성 신장 손상을 초래할 수 있습니다.요산을 소변으로 희석 및 배설하는 과수화, 혈액 중 용해성이 낮은 요산 수치를 감소시키는 라스부리카아제 또는 푸린 이화작용이 요산 [37]수치를 증가시키는 것을 억제하는 알로푸리놀을 포함한다.
레슈니한 증후군
희귀한 유전 질환인 레쉬-나이한 증후군은 높은 혈청 요산 [46]수치와도 관련이 있다.이 [47]증후군에서는 통풍의 증상뿐만 아니라 경련, 무의식적인 움직임, 인지 지체 등이 나타난다.
심혈관 질환
고뇨산혈증은 심혈관 [48]질환의 위험인자를 증가시킬 수 있다.
제2형 당뇨병
고뇨산혈증은 그 [49]전구체라기보다는 당뇨병의 인슐린 저항성의 결과일 수 있다.한 연구는 높은 혈청 요산이 비만, 이상지질혈증, [50]고혈압과 무관하게 제2형 당뇨병에 걸릴 위험이 높다는 것을 보여주었다.고뇨산혈증은 어린이를 [51][52]포함한 대사증후군 성분과 관련이 있다.
요산 결석 형성
신장결석은 요산나트륨 미세결정 [53][54]퇴적물을 통해 형성될 수 있다.
혈중 요산의 포화도는 요산염이 신장에서 결정될 때 신장결석의 한 형태를 초래할 수 있다.이 요산결석은 방사선 투과성이기 때문에 복부 [55]X-ray에는 나타나지 않도록 합니다.요산 결정은 또한 옥살산칼슘 결석의 형성을 촉진하여 "씨 결정"[56] 역할을 합니다.
저요산
저요산(저혈증)은 여러 가지 원인이 있을 수 있다.낮은 식사의 아연 섭취는 요산 수치를 낮추는 원인이 된다.이 효과는 경구 피임약을 [57]복용하는 여성들에게서 더욱 두드러질 수 있다.만성 신부전 환자의 고인산혈증 예방을 위한 약물인 세벨라머는 혈청 요산을 [58]크게 줄일 수 있다.
다발성 경화증
10건의 환자-대조군 연구에 대한 메타 분석 결과, 다발성 경화증 환자의 혈청 요산 수치는 건강한 대조군에 비해 유의미하게 낮았으며, 이는 다발성 [59]경화증에 대한 진단 바이오마커를 나타낼 수 있다.
저요산 정상화
낮거나 부족한 아연 수치를 교정하는 것은 혈청 요산을 [60]높이는 데 도움을 줄 수 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ Scheele, C. W. (1776). "Examen Chemicum Calculi Urinari" [A chemical examiniation of kidney stones]. Opuscula. 2: 73.
- ^ Horbaczewski, Johann (1882). "Synthese der Harnsäure" [Synthesis of uric acid]. Monatshefte für Chemie und Verwandte Teile Anderer Wissenschaften. 3: 796–797. doi:10.1007/BF01516847. S2CID 92323943.
- ^ Lieberman, Michael; Marks, Allan D.; Smith, Colleen M.; Marks, Dawn B. (2007). Marks' Essential Medical Biochemistry. Philadelphia: Lippincott Williams & Wilkins. pp. 47–. ISBN 978-0-7817-9340-7.
- ^ Ringertz, H. (1 March 1966). "The molecular and crystal structure of uric acid". Acta Crystallographica. 20 (3): 397–403. doi:10.1107/S0365110X66000914.
- ^ Jiménez, Verónica; Alderete, Joel B. (November 2005). "Theoretical calculations on the tautomerism of uric acid in gas phase and aqueous solution". Journal of Molecular Structure: THEOCHEM. 755 (1–3): 209–214. doi:10.1016/j.theochem.2005.08.001.
- ^ McCrudden, Francis H. (2008) [1905]. Uric Acid: The Chemistry, Physiology and Pathology of Uric Acid and the Physiologically Important Purin Bodies, with a Discussion of the Metabolism in Gout. Charleston, SC: BiblioBazaar. ISBN 978-0-554-61991-0.
- ^ Weast, Robert C., ed. (1981). CRC Handbook of Chemistry and Physics (62nd ed.). Boca Raton, FL.: CRC Press. OCLC 7842683.
- ^ Windholz, Martha, ed. (1976). Merck Index (9th ed.). Merck. ISBN 978-0-911910-26-1.
- ^ McCrudden, Francis H. Uric acid. p. 58.
- ^ Kimiyoshi, Ichida; Yoshihiro, Amaya; Kumi, Noda; Shinsei, Minoshima; Tatsuo, Hosoya; Osamu, Sakai; Nobuyoshi, Shimizu; Takeshi, Nishino (November 1993). "Cloning of the cDNA encoding human xanthine dehydrogenase (oxidase): Structural analysis of the protein and chromosomal location of the gene". Gene. 133 (2): 279–284. doi:10.1016/0378-1119(93)90652-J. PMID 8224915.
- ^ Hille, R. (2005). "Molybdenum-containing hydroxylases". Archives of Biochemistry and Biophysics. 433 (1): 107–116. doi:10.1016/j.abb.2004.08.012. PMID 15581570.
- ^ Hori, N.; Uehara, K.; Mikami, Y. (1992). "Enzymatic Synthesis of 5-Methyluridine from Adenosine and Thymine with High Efficiency". Biosci. Biotechnol. Biochem. 56 (4): 580–582. doi:10.1271/bbb.56.580. PMID 27280651.
- ^ Baillie, J. K.; Bates, M. G.; Thompson, A. A.; Waring, W. S.; Partridge, R. W.; Schnopp, M. F.; Simpson, A.; Gulliver-Sloan, F.; Maxwell, S. R.; Webb, D. J. (May 2007). "Endogenous urate production augments plasma antioxidant capacity in healthy lowland subjects exposed to high altitude". Chest. 131 (5): 1473–1478. doi:10.1378/chest.06-2235. PMID 17494796.
- ^ Angstadt, Carol N. (4 December 1997). "Purine and Pyrimidine Metabolism: Purine Catabolism". NetBiochem.
- ^ Proctor, P. (November 1970). "Similar functions of uric acid and ascorbate in man?". Nature. 228 (5274): 868. Bibcode:1970Natur.228..868P. doi:10.1038/228868a0. PMID 5477017. S2CID 4146946.
- ^ Maxwell, S. R. J.; Thomason, H.; Sandler, D.; Leguen, C.; Baxter, M. A.; Thorpe, G. H. G.; Jones, A. F.; Barnett, A. H. (1997). "Antioxidant status in patients with uncomplicated insulin-dependent and non-insulin-dependent diabetes mellitus". European Journal of Clinical Investigation. 27 (6): 484–490. doi:10.1046/j.1365-2362.1997.1390687.x. PMID 9229228. S2CID 11773699.
- ^ Braunwald, Eugene, ed. (1987). Harrison's Principles of Internal Medicine (11th ed.). New York: McGraw-Hill. p. A-3. ISBN 978-0-07-079454-2.
- ^ a b Tausche, A. K.; Unger, S.; Richter, K.; et al. (May 2006). "Hyperurikämie und Gicht" [Hyperuricemia and gout: diagnosis and therapy]. Der Internist (in German). 47 (5): 509–521. doi:10.1007/s00108-006-1578-y. PMID 16586130. S2CID 11480796.
- ^ a b Vitart, V.; Rudan, I.; Hayward, C.; et al. (April 2008). "SLC2A9 is a newly identified urate transporter influencing serum urate concentration, urate excretion and gout". Nature Genetics. 40 (4): 437–442. doi:10.1038/ng.106. PMID 18327257. S2CID 6720464.
- ^ Friedman, Meyer & Byers, Sanford O. (1 September 1948). "Observations concerning the causes of the excess excretion of uric acid in the Dalmatian dog". The Journal of Biological Chemistry. 175 (2): 727–735. doi:10.1016/S0021-9258(18)57191-X. PMID 18880769.
- ^ Hazard, Lisa C. (2004). Sodium and Potassium Secretion by Iguana Salt Glands. Iguanas: Biology and Conservation. University of California Press. pp. 84–85. ISBN 978-0-520-23854-1.
- ^ Zeeck, Erich; Harder, Tilman; Beckmann, Manfred (1998). "Uric acid: the sperm-release pheromone of the marine polychaete Platynereis dumerilii". Journal of Chemical Ecology. 24 (1): 13–22. doi:10.1023/A:1022328610423. S2CID 42318049.
- ^ Major TJ, Topless RK, Merriman TR (2018). "Evaluation of the diet wide contribution to serum urate levels: meta-analysis of population based cohorts". The BMJ. 363: k3951. doi:10.1136/bmj.k3951. PMC 6174725. PMID 30305269.
- ^ Keenan RT (2020). "The biology of urate". Seminars in Arthritis and Rheumatism. 50 (35): S2–S10. doi:10.4103/bc.bc_1_19. PMC 6611195. PMID 32620198.
- ^ Aringer, M; Graessler, J. (December 2008). "Understanding deficient elimination of uric acid". Lancet. 372 (9654): 1929–1930. doi:10.1016/S0140-6736(08)61344-6. PMID 18834627. S2CID 1839089.
- ^ Kolz, M.; Johnson, T.; et al. (June 2009). Allison, David B. (ed.). "Meta-analysis of 28,141 individuals identifies common variants within five new loci that influence uric acid concentrations". PLOS Genet. 5 (6): e1000504. doi:10.1371/journal.pgen.1000504. PMC 2683940. PMID 19503597.
- ^ Köttgen, A.; et al. (February 2013). "Genome-wide association analyses identify 18 new loci associated with serum urate concentrations" (PDF). Nature Genetics. 45 (2): 145–154. doi:10.1038/ng.2500. PMC 3663712. PMID 23263486.
- ^ Döring, A.; Gieger, C.; Mehta, D.; et al. (April 2008). "SLC2A9 influences uric acid concentrations with pronounced sex-specific effects". Nature Genetics. 40 (4): 430–436. doi:10.1038/ng.107. PMID 18327256. S2CID 29751482.
- ^ Mandal, Asim K.; Mount, David B. (February 2015). "The molecular physiology of uric acid homeostasis". Annual Review of Physiology. 77: 323–345. doi:10.1146/annurev-physiol-021113-170343. PMID 25422986.
- ^ "Harmonisation of Reference Intervals" (PDF). Pathology Harmony (UK). Archived from the original (PDF) on 2 August 2013. Retrieved 13 August 2013.
- ^ Zhao, J; Huang, Y (2015). "Salivary uric acid as a noninvasive biomarker for monitoring the efficacy of urate-lowering therapy in a patient with chronic gouty arthropathy". Clinica Chimica Acta. 450: 115–20. doi:10.1016/j.cca.2015.08.005. PMID 26276048.
- ^ Cirillo, P.; Sato, W.; Reungjui, S.; et al. (December 2006). "Uric acid, the metabolic syndrome, and renal disease" (PDF). J. Am. Soc. Nephrol. 17 (12 Suppl. 3): S165–S168. doi:10.1681/ASN.2006080909. PMID 17130256.
- ^ Angelopoulos, Theodore J.; Lowndes, Joshua; Zukley, Linda; Melanson, Kathleen J.; Nguyen, Von; Huffman, Anik; Rippe, James M. (June 2009). "The Effect of High-Fructose Corn Syrup Consumption on Triglycerides and Uric Acid". J. Nutr. 139 (6): 1242S–1245S. doi:10.3945/jn.108.098194. PMID 19403709.
- ^ Mayo Clinic staff (11 September 2010). "High uric acid level". Mayo Clinic. Retrieved 24 April 2011.
- ^ Howard AN (1981). "The historical development, efficacy and safety of very-low-calorie diets". Int J Obes. 5 (3): 195–208. PMID 7024153.
- ^ "Diuretic-Related Side Effects: Development and Treatment". Medscape. Retrieved 17 May 2013.
- ^ a b c d Howard, Scott C.; Jones, Deborah P.; Pui, Ching-Hon (12 May 2011). "The Tumor Lysis Syndrome". The New England Journal of Medicine. 364 (19): 1844–1854. doi:10.1056/NEJMra0904569. ISSN 0028-4793. PMC 3437249. PMID 21561350.
- ^ Li R, Yu K, Li C (2018). "Dietary factors and risk of gout and hyperuricemia: a meta-analysis and systematic review". Asia Pacific Journal of Clinical Nutrition. 27 (6): 1344–1356. doi:10.6133/apjcn.201811_27(6).0022. PMID 30485934.
- ^ Heinig, M.; Johnson, R. J. (December 2006). "Role of uric acid in hypertension, renal disease, and metabolic syndrome". Cleveland Clinic Journal of Medicine. 73 (12): 1059–1064. doi:10.3949/ccjm.73.12.1059. PMID 17190309. S2CID 45409308.
- ^ Richette, P.; Bardin, T. (January 2010). "Gout". Lancet. 375 (9711): 318–328. doi:10.1016/S0140-6736(09)60883-7. PMID 19692116. S2CID 208793280.
- ^ a b Choi, H. K.; Atkinson, K.; Karlson, E. W.; Willett, W.; Curhan, G. (March 2004). "Purine-rich foods, dairy and protein intake, and the risk of gout in men". The New England Journal of Medicine. 350 (11): 1093–1103. doi:10.1056/NEJMoa035700. PMID 15014182.
- ^ "Gout diet: What's allowed, what's not". Mayo Clinic. 2 July 2020.
{{cite web}}: CS1 maint :url-status (링크) - ^ Schrauzer, Gerhard N. (2002). "Lithium: Occurrence, Dietary Intakes, Nutritional Essentiality". Journal of the American College of Nutrition. 21 (1): 14–21. doi:10.1080/07315724.2002.10719188. PMID 11838882. S2CID 25752882.
- ^ "NHS Clinical Knowledge Summaries". UK National Health Service. Archived from the original on 4 March 2012.
- ^ Pacher, P; Nivorozhkin, A; Szabó, C (2006). "Therapeutic effects of xanthine oxidase inhibitors: Renaissance half a century after the discovery of allopurinol". Pharmacological Reviews. 58 (1): 87–114. doi:10.1124/pr.58.1.6. PMC 2233605. PMID 16507884.
- ^ Luo, Y. C.; Do, J. S.; Liu, C. C. (October 2006). "An amperometric uric acid biosensor based on modified Ir–C electrode". Biosensors & Bioelectronics. 22 (4): 482–488. doi:10.1016/j.bios.2006.07.013. PMID 16908130.
- ^ Nyhan, W. L. (March 2005). "Lesch-Nyhan Disease". Journal of the History of the Neurosciences. 14 (1): 1–10. doi:10.1080/096470490512490. PMID 15804753. S2CID 37934468.
- ^ Borghi, C.; Verardi, F. M.; Pareo, I.; Bentivenga, C.; Cicero, A. F. (2014). "Hyperuricemia and cardiovascular disease risk". Expert Rev. Cardiovasc. Ther. 12 (10): 1219–1225. doi:10.1586/14779072.2014.957675. PMID 25192804. S2CID 42023170.
- ^ Cappuccio, F. P.; Strazzullo, P.; Farinaro, E.; Trevisan, M. (July 1993). "Uric acid metabolism and tubular sodium handling. Results from a population-based study". J. Am. Med. Assoc. 270 (3): 354–359. doi:10.1001/jama.270.3.354. PMID 8315780.
- ^ Dehghan, A.; van Hoek, M.; Sijbrands E. J., Hofman A.; Witteman, J. C. (February 2008). "High serum uric acid as a novel risk factor for type 2 diabetes". Diabetes Care. 31 (2): 361–362. doi:10.2337/dc07-1276. PMID 17977935.
- ^ De Oliveira, E. P.; et al. (2012). "High plasma uric acid concentration: Causes and consequences". Diabetology & Metabolic Syndrome. 4, 4: 12. doi:10.1186/1758-5996-4-12. PMC 3359272. PMID 22475652.
- ^ Wang, J. Y.; et al. (2012). "Predictive value of serum uric acid levels for the diagnosis of metabolic syndrome in adolescents". The Journal of Pediatrics. 161 (4): 753–6.e2. doi:10.1016/j.jpeds.2012.03.036. PMID 22575243.
- ^ Banach, K.; Bojarska, E.; Kazimierczuk, Z.; Magnowska, L.; Bzowska, A. (2005). "Kinetic Model of Oxidation Catalyzed by Xanthine Oxidase—The Final Enzyme in Degradation of Purine Nucleosides and Nucleotides". Nucleic Acids. 24 (5–7): 465–469. doi:10.1081/ncn-200060006. PMID 16247972. S2CID 42906456.
- ^ "What is Gout: What Causes Gout?". MedicalBug. 6 January 2012. Archived from the original on 2 April 2019. Retrieved 6 May 2012.
- ^ Worcester, Elaine M.; Coe, Fredric L. (2008). "Nephrolithiasis". Primary Care: Clinics in Office Practice. 35 (2): 369–391. doi:10.1016/j.pop.2008.01.005. PMC 2518455. PMID 18486720.
- ^ Pak, C. Y. (September 2008). "Medical stone management: 35 years of advances". The Journal of Urology. 180 (3): 813–819. doi:10.1016/j.juro.2008.05.048. PMID 18635234.
- ^ Hess, F. M.; King, J. C.; Margen, S. (1 December 1977). "Effect of low zinc intake and oral contraceptive agents on nitrogen utilization and clinical findings in young women". The Journal of Nutrition. 107 (12): 2219–2227. doi:10.1093/jn/107.12.2219. PMID 925768.
- ^ Garg, J. P.; Chasan-Taber, S.; Blair, A.; et al. (January 2005). "Effects of sevelamer and calcium-based phosphate binders on uric acid concentrations in patients undergoing hemodialysis: a randomized clinical trial". Arthritis and Rheumatism. 52 (1): 290–295. doi:10.1002/art.20781. PMID 15641045.
- ^ Wang, L.; Hu, W.; Wang, J.; Qian, W.; Xiao, H. (2016). "Low serum uric acid levels in patients with multiple sclerosis and neuromyelitis optica: An updated meta-analysis". Multiple Sclerosis and Related Disorders. 9: 17–22. doi:10.1016/j.msard.2016.05.008. PMID 27645338.
- ^ Umeki, S; Ohga, R.; Konishi, Y.; Yasuda, T.; Morimoto, K.; Terao, A. (November 1986). "Oral zinc therapy normalizes serum uric acid level in Wilson's disease patients". The American Journal of the Medical Sciences. 292 (5): 289–292. doi:10.1097/00000441-198611000-00007. PMID 3777013. S2CID 39995735.