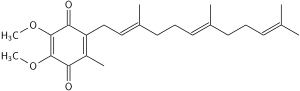
코엔자임10 Q
Coenzyme Q10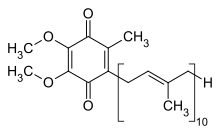 | |
| 이름 | |
|---|---|
| 선호 IUPAC 이름 2-[(2E,6E,10E,14E,18E,22E,26E,30E,34E)-3,7,11,15,19,23,27,31,35,39-Decamethyltetraconta-2,6,10,14,18,22,26,30,34,38-decaen-1-yl]-5,6-dimethoxy-3-methylcyclohexa-2,5-diene-1,4-dione | |
| 기타 이름 유비퀴논, 우비데카레논, 코엔자임 Q, CoQ10, /ˌ코ʊkkkkkk////, CoQ, Q10, 비타민 Q | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 켐벨 | |
| 켐스파이더 | |
| ECHA InfoCard | 100.005.590 |
펍켐 CID | |
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| C59H90O4 | |
| 어금질량 | 863.1987 g·190−1 |
| 외관 | 노란색 또는 주황색 고체 |
| 녹는점 | 48–52°C(118–126°F, 321–325 K) |
| 불용성인 | |
| 약리학 | |
| C01EB09(WHO) | |
| 관련 화합물 | |
관련 퀴노네스 | 1,4-벤조퀴논 플라토키논 유비퀴놀 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
유비쿼터스니온으로도 알려진 코엔자임 Q는 동물과 대부분의 박테리아(유비쿼시논이라는 이름을 가진)에서 어디서나 볼 수 있는 코엔자임 계열이다. 인간에게 가장 흔한 형태는 코엔자임 Q 또는10 유비쿼터스니온-10이다. CoQ는10 미국 식품의약국(FDA)의 승인을 받지 않았지만,[1] 건강 보조식품으로 판매되며 일부 화장품의 원료다.[2][3]
14-벤조퀴논으로 Q는 퀴논 화학군을, 10은 꼬리에 있는 이소프레닐 화학 서브유닛 수를 가리킨다. 천연 유비퀴논에서는 그 수가 6에서 10까지 될 수 있다. 비타민을 닮은 이 지용성 물질군은 주로 미토콘드리아에서 재생되는 모든 진핵 세포에 존재한다. 전자수송체인의 구성요소로서 ATP의 형태로 에너지를 생성하는 유산소 세포호흡에 참여한다. 인체의 에너지의 95%는 이런 식으로 생성된다.[4][5] 심장, 간, 신장 등 에너지 요구량이 가장 높은 장기는 CoQ10 농도가 가장 높다.[6][7][8]
CoQ에는 완전 산화(ubiquinone), 세미키논(ubisemiquinone), 완전 환원(ubiquinol)의 세 가지 redox 상태가 있다. 이 분자가 (퀴노네와 퀴놀형 사이의 이동) 2 전자 캐리어와 (세미키노네와 이 다른 형태들 중 하나에서 이동) 역할을 할 수 있는 역량은 한 번에 한 전자만 받아들일 수 있는 철-설황 군집 때문에 전자 운송망에서 그 역할의 중심이며, 프리라디카로서의 역할을 한다.l-scaving 산화 방지제
결핍과 독성
인간에게 CoQ의10 결핍을 초래하는 두 가지 주요 요인은 생합성 감소와 신체의 사용 증가다. 생합성은 CoQ의10 주요 원천이다. 생합성에는 최소한 12개의 유전자가 필요하며, 그 중 많은 유전자가 돌연변이를 일으켜 CoQ 결핍을 일으킨다. 또한 CoQ10 수준은 다른 유전적 결함(CoQ10 생합성 과정과 직접 관련이 없는 유전자인 미토콘드리아 DNA, ETFDH, APTX, FXN, BRAF의 돌연변이와 같은)에 의해 영향을 받을 수 있다. COQ6의 돌연변이와 같은 일부는 스테로이드 저항성 신드롬과 같은 심각한 질병으로 이어질 수 있으며 센서리노럴 청각장애가 발생할 수 있다.
일부 부작용은 대부분 위장 장애로 매우 높은 섭취량으로 보고된다. 관측된 안전 수준(OSL) 위험 평가 방법은 안전성의 증거가 최대 1200 mg/일 섭취에 강하다는 것을 나타냈으며, 이 수준을 OSL로 식별한다.[9]
평가
비록 CoQ는10 혈장에서 측정될 수 있지만, 이러한 측정은 조직 상태보다는 식이 섭취를 반영한다. 현재 대부분의 임상센터에서는 배양된 피부 섬유질, 근육 생체검사, 혈액 단핵세포에서 CoQ10 수치를 측정하고 있다.[10] 배양 섬유블라스트는 또한 C-라벨로프록시벤조이트의 섭취를 측정하여 내생 CoQ10 생합성률을 평가하는 데 사용될 수 있다.[11]
스타틴스
스타틴의 근독성이 CoQ 생합성 손상 때문이라는 주장이 제기됐으나 이를 뒷받침하는 증거는 2011년 논란이 됐다.[10]
스타틴이 혈액에서 코엔자임 Q를10 감소시킬 수 있지만 근육에서 코엔자임 Q를10 감소시킬지는 불확실하다.[12] 보충제가 스타틴의 부작용을 개선한다는 증거는 없다.[12] 그러나 최근의 한 분석에서는 "CoQ10 보충제는 SAMS를 개선하여 CoQ10 보충제가 아멜리테이트 유도 근병증에 대한 보완적 접근법일 수 있음을 시사했다"[13]고 결론지었다.
식이보조제
규정 및 구성
CoQ는10 많은 관할 지역에서 UbiQ 300 & UbiQ 100이라는 이름으로 식이보충제로 판매되고 있으며, 약제와 동일한 규제를 적용받지 않고 있지만, 어떠한 의학적 질환의 치료에도 승인되지 않고 있다.[1][14] CoQ의10 제조는 규제되지 않으며, 다른 배치와 브랜드는 크게 다를 수 있다.[1] 미국에서 판매 중인 CoQ10 보충제의 2004년 연구실 분석 결과 일부는 제품 라벨에서 식별된 수량을 포함하지 않았다. 양은 "검출 불가능한 CoQ10"부터 명시된 선량의 75%까지, 최대 75% 초과까지 다양했다.[15][16]
일반적으로, CoQ는10 잘 용인된다. 가장 흔한 부작용으로는 위장증상(간증, 구토, 식욕억제, 복통), 발진, 두통 등이 있다.[17]
CoQ의10 이상적인 복용량은 확립되어 있지 않지만, 일반적인 일일 투여량은 100–200mg이다. 다른 공식들은 CoQ와10 다른 성분들의 공시된 양에 따라 다르다.
심장병
2014년 Cochrane 리뷰는 심부전 치료에 CoQ를10 사용하는 것을 "증거할 만한 설득력 있는 증거가 없다"고 밝혔다.[18] 또 다른 2014년 코크란 리뷰는 심장병 예방을 위한 그것의 사용에 대한 결론을 내리기에는 불충분한 증거를 발견했다.[19] 2016년 Cochrane 리뷰는10 CoQ가 혈압에 영향을 주지 않는다고 결론지었다.[20] 2017년 CoQ10 30–100 mg/d의 심부전 환자를 메타분석한 결과 사망률이 31% 감소했다. 운동능력도 높아졌다. 왼쪽 심장 박출률과 뉴욕 심장 협회(NYHA) 분류의 엔드포인트에서 유의미한 차이는 발견되지 않았다.[21]
편두통
편두통 예방협회의 가이드라인은 저품질 증거에 근거하여 300mg의 CoQ가10 예방접종을 위한 선택으로 제공될 것을 권고하고 있다.[22]
스타틴 근병증
CoQ는10 스타틴 약물의 부작용과 관련된 근육파괴를 치료하기 위해 일상적으로 사용되어 왔다. 2015년 무작위 통제 시험의 메타 분석 결과, CoQ는10 스타틴 근병증에는 아무런 영향을 미치지 않았다.[23] 2018년 메타분석 결과 근육통, 근육 약화, 근육경련, 근육피로증상 등 경구10 CoQ 관련 근육 증상 감소에 대한 예비증거가 있었다고 결론 내렸다.[13]
암
2014년[update] 현재 암 치료에 대한 CoQ의10 대규모 임상시험은 실시되지 않았다.[1] 미국 국립 암 연구소는 "연구 방식과 보고되는 정보의 양이 CoQ에10 의한 것인지 아니면 다른 것에 의한 것인지 불분명하게 만들었다"고 말하면서, 수행된 몇 안 되는 소규모 연구의 문제점을 확인했다.[1] 미국암학회는 "CoQ가10 화학요법과 방사선요법의 효과를 떨어뜨릴 수 있으므로 대부분의 종양학자들이 암 치료 중 이를 피하도록 권고할 것"[24]이라고 결론지었다.
치과병
1995년 검토 연구에서는 치주질환 치료에 CoQ를10 사용하는 데 임상적 이점이 없는 것으로 나타났다.[25] 달리 시대에 뒤떨어져 있거나, 체외 시험에 초점을 맞추고 있거나,[26][27][28] 시험 대상 및/또는 잘못된 통계 방법론과 시험 설정을 가지고 있거나,[29][30] 제품 제조업체의 후원을 받은 연구들이 대부분이었다.[31]
만성 신장병
CKD가 있는 사람에게 CoQ10 보충이 미치는 영향에 대한 검토가 2019년에 제안되었다.[32]
추가 용도
코엔자임 Q10은 알츠하이머병, 높은 콜레스테롤, 또는 근위축성 측경화증(루게릭병)을 치료하는 데도 사용되었다. 그러나, 연구는 이것이 이러한 조건들을[33] 치료하는데 효과적이지 않을 수 있다는 것을 보여주었다.
코엔자임 Q10은 코스메슈티컬의 활성 성분으로, 자외선 차단제 제형의 비활성 성분으로도 활용됐다. 때 국소적으로 피부 보호 제품에 적용된 것이 어떤 능력이 본질적인 피부 노화의 skin,[34]지연 간판 등에서 외적 피부의 기미를 산화적 스트레스를 줄이기 위해 특정한 자외선 차단제 actives,[39]증가 dyspigmentation,[37][38]증가 안정은 SPFsunscreens,[40]의 퇴색에고 살 여유가 도와 주aging,[35][36]을 보여 줍니다.sunscr에frared 보호eens.[41][42] 유비퀴논의 피부 이점에 대한 많은 연구는 그것이 피부와 화장품 제형을 향상시키기 위해 다른 국소 항산화제와 시너지 효과를 낸다는 것을 보여준다.
상호작용
Coenzyme10 Q는 항응고제 와파린뿐만 아니라 엽록소의 효과를 억제할 수 있는 잠재력을 가지고 있다; Coenzyme10 Q는 시토크롬 p450 효소와 상호작용을 함으로써 와파린의 작용을 방해할 수 있다. 따라서 혈액 응고의 척도인 INR을 감소시킨다.[43] 코엔자임 Q의10 구조는 와파린의 항응고 효과와 경쟁하고 대항하는 비타민 K의 구조와 매우 유사하다. 코엔자임 Q는10 현재 와파린을 복용하고 있는 환자에게서 응고 위험이 증가하기 때문에 피해야 한다.[17]
화학적 특성
CoQ의10 산화 구조는 위와 같다. 다양한 종류의 Coenzyme Q는 옆면 체인에 있는 이소프레노이드 서브유닛의 수로 구별될 수 있다. 인간 미토콘드리아에서 가장 흔한 코엔자임 Q는 CoQ이다10. Q는 퀴논 머리를 가리키고, 10은 꼬리에 이솝렌이 반복되는 횟수를 가리킨다. 아래의 분자는 3개의 이소프로노이드 단위를 가지고 있으며 Q라고3 불릴 것이다.
순수한 상태에서는 오렌지색 계열의 지방질 분말이며, 맛도 냄새도 없다.[44]: 230
생합성
생합성은 대부분의 인체 조직에서 발생한다. 크게 세 가지 단계가 있다.
초기 두 가지 반응은 미토콘드리아, 소포체 망막, 과록시솜에서 발생하며, 이는 동물 세포에서 복수의 합성 부위를 나타낸다.[45]
이 경로에서 중요한 효소는 HMG-CoA 환원효소인데, 보통 심혈관 합병증에 대한 개입의 대상이다. "statin" 계열의 콜레스테롤 감소 약물은 HMG-CoA 환원효소를 억제한다. 스타틴의 부작용 중 하나는 CoQ의10 생산량 감소인데, 이것은 근병증과 횡문근융해증의 발달과 연관될 수 있다. 하지만, CoQ 결핍에서 스타틴이 하는 역할은 논란의 여지가 있다. 비록 이 약들이 CoQ의 혈중 수치를 감소시키지만, CoQ의 근육 수치의 영향에 대한 연구는 아직 오지 않았다. CoQ 보충제 역시 스타틴 약물의 부작용을 줄이지 않는다.[10][12]
관련된 유전자는 PDSS1, PDSS2, COQ2, ADCK3(COQ8, CABC1)이다.[46]
인간을 제외한 유기체는 벤조퀴논 구조와 이솝렌 구조를 생산하기 위해 다소 다른 원천 화학물질을 사용한다. 예를 들어 대장균 박테리아는 전자를 초리스마이트에서, 후자는 비메오네이트 소스에서 생산한다. 그러나 일반적인 효모 S. 세레비시아는 전자를 초리스마이트나 티로신에서, 후자는 메발로네이트에서 유래한다. 대부분의 유기체는 4-히드록시벤조산염 중간을 공유하지만, 다시 다른 단계를 사용하여 "Q" 구조에 도달한다.[47]
흡수 및 대사
흡수
CoQ는10 물에 용해되지 않는 결정성 분말이다. 흡수는 지질과 같은 과정을 따른다; 흡수 메커니즘은 또 다른 지용성 영양소인 비타민 E와 비슷한 것으로 보인다. 인체의 이 과정은 췌장 효소와 담즙의 소장으로 분비되어 지방질 물질의 흡수에 필요한 유화 및 미셀 형성을 촉진한다.[48] 음식 섭취(및 지질의 존재)는 담즙산의 체내 배설을 자극하고 CoQ의10 흡수를 크게 강화한다. 외생성 CoQ는10 소장에서 흡수되며 식사와 함께 복용하면 가장 잘 흡수된다. Fed 조건에서의 CoQ의10 혈청 농도는 단식 조건보다 높다.[49][50]
신진대사
동물과 인간에서의 CoQ의10 신진대사에 대한 데이터는 제한적이다.[51] 랫드에 C 라벨을 붙인10 CoQ를 사용한 연구는 피크 플라즈마 방사능이 관측된 경구 투여 후 2시간 후 간에서 대부분의 방사능을 보였으나, CoQ9(이소프라닐 단위가 9개에 불과한)는 랫드에 코엔자임Q가 지배적인 형태다.[52] CoQ는10 모든 조직에서 대사되는 반면, 제거의 주요 경로는 담도와 배설이다. CoQ10 보충제 철회 후, 사용한 제형의 종류에 관계없이 수일 이내에 레벨이 정상으로 돌아온다.[53]
약동학
CoQ의10 약동학에 관한 일부 보고서가 발표되었다. 플라즈마 피크는 주로 연구 설계에 따라 경구 투여 후 2-6시간 후에 관찰할 수 있다. 일부 연구에서는 두 번째 혈장 피크가 투여 후 약 24시간 후에 관찰되었는데, 이는 아마도 간에서 순환으로 장내혈액 재활용과 재배포 때문일 것이다.[48] 토모노 외 중수소 라벨 결정 CoQ10을 사용하여 인간의 약동학을 조사했고 제거 반 시간을 33시간으로 결정했다.[54]
CoQ의10 생체이용성 향상
생체이용가능성을 위해 어떻게 약물을 제조하는지의 중요성은 잘 알려져 있다. 구강 투여 후 CoQ의10 생체이용률을 높이기 위한 원칙을 찾기 위해, 몇 가지 새로운 접근법이 취해졌다; 동물과 인간에게 다른 제형과 형태가 개발되고 시험되었다.[51]
입자 크기 감소
나노입자는 흡수 특성이 떨어지는 약물의 경구 생체이용성을 향상시키는 등 다양한 약물의 전달체제로 발굴돼 왔다.[55] 그러나, 보고서는 크게 다르지만, 이것은10 CoQ에서 성공적인 것으로 증명되지 않았다.[56][57] 정제수에 미세 분말된 CoQ의10 수성 정지를 사용하는 것도 미미한 효과만을 드러낸다.[53]
오일 서스펜션에 CoQ가10 들어간 소프트겔 캡슐
성공적인 접근방법은 위장관의 흡수를 촉진하고 생체이용성을 향상시키기 위해 에멀전 시스템을 사용하는 것이다. 콩기름(지질 마이크로스피어) 유화는 레시틴에 의해 매우 효과적으로 안정될 수 있었고 소프트겔 캡슐의 조제에 사용되었다. 오자와 외 연구진은 이러한 첫 시도 중 하나에서 콩기름에 함유된 CoQ의10 에멀젼이 조사된 비글에 대한 약동학 연구를 수행했으며, 지질 미세조직을 투여하는 동안 제어 태블릿 준비의 약 2배인 플라즈마 CoQ10 수준이 결정되었다.[53] 개에 대한 후기 연구에서 Kommuuru et al.에 의해 석유 기반 소프트겔 ucapsules에 의해 거의 무시할 수 있는 수준의 생체이용률 향상이 관찰되었지만,[58] CoQ의10 현저하게 증가한 생체이용률은 대부분의 다른 연구에서 몇 가지 석유 기반 제형에 대해 확인되었다.[59]
수용성이 향상된 CoQ의 새로운10 형태
물 속 용해도를 높여 약품 흡수를 촉진하는 것이 일반적인 의약품 전략이며, CoQ에서도10 성공을 거둔 것으로 나타났다. 이 목표를 달성하기 위해 다양한 접근법이 개발되어 왔으며, 이들 중 다수는 성분 최적화를 위한 많은 시도에도 불구하고 석유 기반의 소프트겔 캡슐보다 훨씬 더 나은 결과를 생산하고 있다.[51] 고체 CoQ10의 중합체 tyloxapol,[60]제제 cyclodextrins과hydrogenated lecithin,[61]과 복합화 등 다양한 solubilising 요원들, 구분으로 이 수성 분산의 그러한 접근법의 예로는 사용하고 그 중 마지막, β-cyclodextrin과 단지 고도로 bioavailability[62][63]이 증가하고 있는 것과 발견되었다. 또한 p.에 사용된다CoQ-증진을10 위한 제약 및 식품 산업.[51]
역사
1950년 영국 리버풀에서 G. N. 페스텐슈타인이 처음으로 소량의 CoQ를10 말의 내장에서 격리시켰다. 이후의 연구에서는 이 화합물을 잠시 물질 SA라고 불렀고, 그것은 퀴논으로 간주되었고, 그것은 많은 동물들의 많은 조직에서 발견될 수 있다는 것에 주목했다.[64]
1957년 프레데릭 L. 크레인(Frederick L. Crane)과 위스콘신대 매디슨 효소연구소 동료들은 쇠고기 심장의 미토콘드리아 막에서 같은 화합물을 분리하고 미토콘드리아 내에서 전자를 운반한다는 점에 주목했다. 그들은 그것이 퀴노네였기 때문에 Q-275라고 불렀다.[65][64] 곧 그들은 영국에서 연구된 Q-275와 물질 SA가 같은 화합물일 수 있다는 점에 주목했다. 이는 그해 말 확인되었고 Q-275/보조 SA는 모든 동물 조직에서 찾을 수 있는 유비쿼터스 퀴논이라 하여 유비쿼시논으로 개칭되었다.[64][44]
1958년, 그것의 완전한 화학 구조는 Rahway의 Merck에서 Karl Forcers 밑에서 일하는 D. E. Wolf와 동료들에 의해 보고되었다.[66][64][44] 그 해 말 D. E. 그린과 위스콘신 연구 그룹에 속한 동료들은 유비쿼시논을 미토콘드리아 전자 전송 체인에 참여하기 때문에 미토키논 또는 코엔자임 Q라고 불러야 한다고 제안했다.[64][44]
1966년 캘리포니아 대학의 A. 멜러스와 A. L. 태플은 감소가6 세포에서 효과적인 산화 방지제라는 것을 처음으로 보여주었다.[67][44]
1960년대에 피터 D. 미첼은 CoQ와10 관련된 전기화학 구배 이론을 통해 미토콘드리아 기능에 대한 이해를 넓혔고, 1970년대 후반 Lars Ernster에 대한 연구는 항산화제로서 CoQ의10 중요성을 확대시켰다. 1980년대에는 CoQ와10 관련된 임상시험의 수가 급격히 증가했다.[44]
식이 농도
2010년 CoQ10 발생과 식이 섭취에 대한 상세한 검토가 발표되었다.[68] 유기체 내의 내생적 합성 외에도, CoQ는10 다양한 식품에 의해 유기체에 공급된다. 그러나 이 화합물에 대한 과학계의 큰 관심에도 불구하고, 식이요법 성분에서 CoQ의10 함량을 결정하기 위한 연구는 극히 제한적이다. 이러한 측면에 대한 첫 보고서는 1959년에 발표되었지만, 특히 농도가 낮은 제품에 대해서는 그 당시 분석 방법의 민감성과 선택성이 신뢰할 수 있는 분석을 허용하지 않았다.[68] 그 이후로 분석 화학의 발달은 다양한 식품에서 CoQ10 농도의 보다 신뢰할 수 있는 결정을 가능하게 했다.
| 음식 | CoQ10 농도(mg/kg) | |
|---|---|---|
| 쇠고기 | 하트 | 113 |
| 간 | 39–50 | |
| 근육의 | 26–40 | |
| 돼지고기 | 하트 | 12–128 |
| 간 | 23–54 | |
| 근육의 | 14–45 | |
| 치킨 | 젖가슴 | 8–17 |
| 허벅지 | 24–25 | |
| 날개짓하다 | 11 | |
| 물고기 | 정어리 | 5–64 |
| 고등어: | ||
| – 붉은 살 | 43–67 | |
| – 흰 살 | 11–16 | |
| 연어 | 4–8 | |
| 참치 | 5 | |
| 오일스 | 콩을 | 54–280 |
| 올리브 | 4–160 | |
| 글자가 있는 | 64–73 | |
| 해바라기 | 4–15 | |
| 카놀라 | 64–73 | |
| 견과류 | 땅콩 | 27 |
| 호두의 | 19 | |
| 참깨 씨 | 18–23 | |
| 피스타치오 | 20 | |
| 헤이즐넛 | 17 | |
| 아몬드 | 5–14 | |
| 야채 | 파슬리 | 8–26 |
| 브로콜리 | 6–9 | |
| 콜리플라워 | 2–7 | |
| 시금치 | 10까지 | |
| 배추 | 2–5 | |
| 과일 | 아보카도 | 10 |
| 블랙커런트 | 3 | |
| 포도를 | 6–7 | |
| 딸기 | 1 | |
| 주황색의 | 1–2 | |
| 자몽 | 1 | |
| 사과 | 1 | |
| 바나나 | 1 | |
고기와 생선은 CoQ의10 가장 풍부한 공급원이다; 50 mg/kg 이상의 레벨은 쇠고기, 돼지고기, 닭 심장과 간에서 발견될 수 있다. 유제품은 동물 조직보다 CoQ의10 공급원이 훨씬 열악하다. 식물성 기름은 또한 CoQ가10 꽤 풍부하다. 채소 내에서는 파슬리와 들깨가 가장 풍부한 CoQ10 공급원이지만, CoQ10 수준에서는 상당한 차이가 문헌에서 발견될 수 있다. 브로콜리, 포도, 콜리플라워는 CoQ의10 적당한 공급원이다. 대부분의 과일과 베리류는 상대적으로 CoQ10 함량이 높은 아보카도를 제외하고, CoQ의10 낮은 공급원에서 매우 낮은 공급원을 나타낸다.[68]
섭취
선진국에서, CoQ의10 일일 예상 섭취량은 주로 육류에서 추출한 일일 3–6mg으로 결정되었다.[68]
열 및 처리의 영향
튀김으로 요리하면 CoQ10 함량이 14~32%[69] 감소한다.
참고 항목
참조
- ^ a b c d e White, J. (14 May 2014). "PDQ® Coenzyme Q10". National Cancer Institute, National Institutes of Health, U.S. Dept. of Health and Human Services. Retrieved 29 June 2014.
- ^ Hojerová, J (May 2000). "[Coenzyme Q10--its importance, properties and use in nutrition and cosmetics]". Ceska a Slovenska Farmacie : Casopis Ceske Farmaceuticke Spolecnosti a Slovenske Farmaceuticke Spolecnosti. 49 (3): 119–23. PMID 10953455.
- ^ "What is coenzyme Q10 (CoQ10) and why is it in skin care products?". WebMD.
- ^ Ernster L, Dallner G (May 1995). "Biochemical, physiological and medical aspects of ubiquinone function". Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1271 (1): 195–204. doi:10.1016/0925-4439(95)00028-3. PMID 7599208.
- ^ Dutton, P. L.; Ohnishi, T.; Darrouzet, E.; Leonard, M. A.; Sharp, R. E.; Cibney, B. R.; Daldal, F.; Moser, C. C. (2000). "4 Coenzyme Q oxidation reduction reactions in mitochondrial electron transport". In Kagan, V. E.; Quinn, P. J. (eds.). Coenzyme Q: Molecular mechanisms in health and disease. Boca Raton: CRC Press. pp. 65–82.
- ^ Okamoto T, Matsuya T, Fukunaga Y, Kishi T, Yamagami T (1989). "Human serum ubiquinol-10 levels and relationship to serum lipids". International Journal for Vitamin and Nutrition Research. Internationale Zeitschrift für Vitamin- und Ernahrungsforschung. Journal International de Vitaminologie et de Nutrition. 59 (3): 288–92. PMID 2599795.
- ^ Aberg F, Appelkvist EL, Dallner G, Ernster L (June 1992). "Distribution and redox state of ubiquinones in rat and human tissues". Archives of Biochemistry and Biophysics. 295 (2): 230–4. doi:10.1016/0003-9861(92)90511-T. PMID 1586151.
- ^ Shindo Y, Witt E, Han D, Epstein W, Packer L (January 1994). "Enzymic and non-enzymic antioxidants in epidermis and dermis of human skin". The Journal of Investigative Dermatology. 102 (1): 122–4. doi:10.1111/1523-1747.ep12371744. PMID 8288904.
- ^ Hathcock JN, Shao A (August 2006). "Risk assessment for coenzyme Q10 (Ubiquinone)". Regulatory Toxicology and Pharmacology. 45 (3): 282–8. doi:10.1016/j.yrtph.2006.05.006. PMID 16814438.
- ^ a b c Trevisson E, DiMauro S, Navas P, Salviati L (October 2011). "Coenzyme Q deficiency in muscle". Current Opinion in Neurology. 24 (5): 449–56. doi:10.1097/WCO.0b013e32834ab528. hdl:10261/129020. PMID 21844807.
- ^ Montero R, Sánchez-Alcázar JA, Briones P, Hernández AR, Cordero MD, Trevisson E, et al. (June 2008). "Analysis of coenzyme Q10 in muscle and fibroblasts for the diagnosis of CoQ10 deficiency syndromes". Clinical Biochemistry. 41 (9): 697–700. doi:10.1016/j.clinbiochem.2008.03.007. PMID 18387363.
- ^ a b c Tan JT, Barry AR (June 2017). "Coenzyme Q10 supplementation in the management of statin-associated myalgia". American Journal of Health-System Pharmacy. 74 (11): 786–793. doi:10.2146/ajhp160714. PMID 28546301. S2CID 3825396.
- ^ a b Qu H, Guo M, Chai H, Wang WT, Gao ZY, Shi DZ (October 2018). "Effects of Coenzyme Q10 on Statin-Induced Myopathy: An Updated Meta-Analysis of Randomized Controlled Trials". Journal of the American Heart Association. 7 (19): e009835. doi:10.1161/JAHA.118.009835. PMC 6404871. PMID 30371340.
- ^ "Mitochondrial disorders in children: Co-enzyme Q10". UK: National Institute for Health and Care Excellence. 28 March 2017.
- ^ "ConsumerLab.com finds discrepancies in strength of CoQ10 supplements". Townsend Letter for Doctors and Patients. August–September 2004. p. 19.
- ^ "ConsumerLab.com finds discrepancies in strength of CoQ10 supplements". ConsumerLab.com. January 2004.
- ^ a b Wyman M, Leonard M, Morledge T (July 2010). "Coenzyme Q10: a therapy for hypertension and statin-induced myalgia?". Cleveland Clinic Journal of Medicine. 77 (7): 435–42. doi:10.3949/ccjm.77a.09078. PMID 20601617. S2CID 26572524.
- ^ Madmani ME, Yusuf Solaiman A, Tamr Agha K, Madmani Y, Shahrour Y, Essali A, Kadro W (June 2014). "Coenzyme Q10 for heart failure". Heart Group. The Cochrane Database of Systematic Reviews (6): CD008684. doi:10.1002/14651858.CD008684.pub2. PMID 24049047.
- ^ Flowers N, Hartley L, Todkill D, Stranges S, Rees K (4 December 2014). "Co-enzyme Q10 supplementation for the primary prevention of cardiovascular disease". The Cochrane Database of Systematic Reviews. 12 (12): CD010405. doi:10.1002/14651858.CD010405.pub2. PMID 25474484.
- ^ Ho MJ, Li EC, Wright JM (March 2016). "Blood pressure lowering efficacy of coenzyme Q10 for primary hypertension". The Cochrane Database of Systematic Reviews. 3 (3): CD007435. doi:10.1002/14651858.CD007435.pub3. PMC 6486033. PMID 26935713.
- ^ Lei L, Liu Y (July 2017). "Efficacy of coenzyme Q10 in patients with cardiac failure: a meta-analysis of clinical trials". BMC Cardiovascular Disorders. 17 (1): 196. doi:10.1186/s12872-017-0628-9. PMC 5525208. PMID 28738783.
- ^ Pringsheim T, Davenport W, Mackie G, Worthington I, Aubé M, Christie SN, et al. (March 2012). "Canadian Headache Society guideline for migraine prophylaxis". The Canadian Journal of Neurological Sciences. 39 (2 Suppl 2): S1-59. PMID 22683887.
- ^ Banach M, Serban C, Sahebkar A, Ursoniu S, Rysz J, Muntner P, et al. (January 2015). "Effects of coenzyme Q10 on statin-induced myopathy: a meta-analysis of randomized controlled trials". Mayo Clinic Proceedings (Systematic Review and Meta-Analysis). Lipid and Blood Pressure Meta-analysis Collaboration Group. 90 (1): 24–34. doi:10.1016/j.mayocp.2014.08.021. PMID 25440725.
- ^ "Coenzyme Q10". American Cancer Society.
- ^ Watts TL (March 1995). "Coenzyme Q10 and periodontal treatment: is there any beneficial effect?". British Dental Journal. 178 (6): 209–13. doi:10.1038/sj.bdj.4808715. PMID 7718355. S2CID 7207070.
- ^ Folkers K, Hanioka T, Xia LJ, McRee JT, Langsjoen P (April 1991). "Coenzyme Q10 increases T4/T8 ratios of lymphocytes in ordinary subjects and relevance to patients having the AIDS related complex". Biochemical and Biophysical Research Communications. 176 (2): 786–91. doi:10.1016/S0006-291X(05)80254-2. PMID 1673841.
- ^ Littarru GP, Nakamura R, Ho L, Folkers K, Kuzell WC (October 1971). "Deficiency of coenzyme Q 10 in gingival tissue from patients with periodontal disease". Proceedings of the National Academy of Sciences of the United States of America. 68 (10): 2332–5. Bibcode:1971PNAS...68.2332L. doi:10.1073/pnas.68.10.2332. PMC 389415. PMID 5289867.
- ^ Nakamura R, Littarru GP, Folkers K, Wilkinson EG (April 1974). "Study of CoQ10-enzymes in gingiva from patients with periodontal disease and evidence for a deficiency of coenzyme Q10". Proceedings of the National Academy of Sciences of the United States of America. 71 (4): 1456–60. Bibcode:1974PNAS...71.1456N. doi:10.1073/pnas.71.4.1456. PMC 388248. PMID 4151519.
- ^ McRee, J. T.; Hanioka, T.; Shizukuishi, S.; Folkers, K. (1993). "Therapy with coenzyme Q10 for patients with periodontal disease". Journal of Dental Health. 43 (5): 659–666. doi:10.5834/jdh.43.659.
- ^ Hanioka T, Tanaka M, Ojima M, Shizukuishi S, Folkers K (1994). "Effect of topical application of coenzyme Q10 on adult periodontitis". Molecular Aspects of Medicine. 15 Suppl (Suppl): s241-8. doi:10.1016/0098-2997(94)90034-5. PMID 7752836.
- ^ Wilkinson EG, Arnold RM, Folkers K (August 1976). "Bioenergetics in clinical medicine. VI. adjunctive treatment of periodontal disease with coenzyme Q10". Research Communications in Chemical Pathology and Pharmacology. 14 (4): 715–9. PMID 785563.
- ^ Xu, Yongxing; Liu, Juan; Han, Enhong; Wang, Yan; Gao, Jianjun (2019). "Efficacy of coenzyme Q10 in patients with chronic kidney disease: protocol for a systematic review". BMJ Open. 9 (5): e029053. doi:10.1136/bmjopen-2019-029053. ISSN 2044-6055. PMC 6530451. PMID 31092669.
- ^ https://neurologycentretoronto.com/wp-content/uploads/2017/06/14-Coenzyme-Q10-Drugs.com_.pdf
- ^ Knott, Anja; Achterberg, Volker; Smuda, Christoph; Mielke, Heiko; Sperling, Gabi; Dunckelmann, Katja; Vogelsang, Alexandra; Krüger, Andrea; Schwengler, Helge; Behtash, Mojgan; Kristof, Sonja (12 November 2015). "Topical treatment with coenzyme Q10‐containing formulas improves skin's Q10 level and provides antioxidative effects". Biofactors. 41 (6): 383–390. doi:10.1002/biof.1239. ISSN 0951-6433. PMC 4737275. PMID 26648450.
- ^ Addor, Flavia Alvim Sant'anna (2017). "Antioxidants in dermatology". Anais Brasileiros de Dermatologia. 92 (3): 356–362. doi:10.1590/abd1806-4841.20175697. ISSN 0365-0596. PMC 5514576. PMID 29186248.
- ^ Blatt, Thomas; Wittern, Klaus-Peter; Wenck, Horst; Staeb, Franz (1 March 2004). "CoQ10, a topical energizer for aging skin". Journal of the American Academy of Dermatology. 50 (3): P76. doi:10.1016/j.jaad.2003.10.628. ISSN 0190-9622.
- ^ Zhang, M.; Dang, L.; Guo, F.; Wang, X.; Zhao, W.; Zhao, R. (June 2012). "Coenzyme Q(10) enhances dermal elastin expression, inhibits IL-1α production and melanin synthesis in vitro". International Journal of Cosmetic Science. 34 (3): 273–279. doi:10.1111/j.1468-2494.2012.00713.x. ISSN 1468-2494. PMID 22339577. S2CID 4664219.
- ^ Hseu, You-Cheng; Ho, Yi-Geng; Mathew, Dony Chacko; Yen, Hung-Rong; Chen, Xuan-Zao; Yang, Hsin-Ling (1 June 2019). "The in vitro and in vivo depigmenting activity of Coenzyme Q10 through the down-regulation of α-MSH signaling pathways and induction of Nrf2/ARE-mediated antioxidant genes in UVA-irradiated skin keratinocytes". Biochemical Pharmacology. 164: 299–310. doi:10.1016/j.bcp.2019.04.015. ISSN 0006-2952. PMID 30991050.
- ^ Afonso, S.; Horita, K.; Sousa e Silva, J. P.; Almeida, I. F.; Amaral, M. H.; Lobão, P. A.; Costa, P. C.; Miranda, Margarida S.; Esteves da Silva, Joaquim C. G.; Sousa Lobo, J. M. (November 2014). "Photodegradation of avobenzone: stabilization effect of antioxidants". Journal of Photochemistry and Photobiology B: Biology. 140: 36–40. doi:10.1016/j.jphotobiol.2014.07.004. ISSN 1873-2682. PMID 25086322.
- ^ Wu, Haiyou; Zhong, Zhangfeng; Lin, Sien; Qiu, Chuqun; Xie, Peitao; Lv, Simin; Cui, Liao; Wu, Tie (19 August 2020). "Coenzyme Q10 Sunscreen Prevents Progression of Ultraviolet-Induced Skin Damage in Mice". BioMed Research International. 2020: 1–8. doi:10.1155/2020/9039843. PMC 7453241. PMID 32923487.
- ^ Grether-Beck, Susanne; Marini, Alessandra; Jaenicke, Thomas; Krutmann, Jean (January 2015). "Effective photoprotection of human skin against infrared A radiation by topically applied antioxidants: results from a vehicle controlled, double-blind, randomized study". Photochemistry and Photobiology. 91 (1): 248–250. doi:10.1111/php.12375. ISSN 1751-1097. PMID 25349107. S2CID 206270691.
- ^ Lim, Henry W.; Arellano-Mendoza, Maria-Ivonne; Stengel, Fernando (March 2017). "Current challenges in photoprotection". Journal of the American Academy of Dermatology. 76 (3S1): S91–S99. doi:10.1016/j.jaad.2016.09.040. ISSN 1097-6787. PMID 28038886.
- ^ Sharma, A; Fonarow, GC; Butler, J; Ezekowitz, JA; Felker, GM (April 2016). "Coenzyme Q10 and Heart Failure: A State-of-the-Art Review". Circulation: Heart Failure. 9 (4): e002639. doi:10.1161/CIRCHEARTFAILURE.115.002639. PMID 27012265. S2CID 2034503.
- ^ a b c d e f Boreková M, et al. (2008). "Nourishing and health benefits of coenzyme Q10". Czech Journal of Food Sciences. 26 (4): 229–241. doi:10.17221/1122-cjfs.
- ^ Bentinger M, Tekle M, Dallner G (May 2010). "Coenzyme Q--biosynthesis and functions". Biochemical and Biophysical Research Communications. 396 (1): 74–9. doi:10.1016/j.bbrc.2010.02.147. PMID 20494114.
- ^ Espinós, Carmen; Felipo, Vicente; Palau, Francesc (2009). Inherited Neuromuscular Diseases: Translation from Pathomechanisms to Therapies. Springer. pp. 122ff. ISBN 978-90-481-2812-9. Retrieved 4 January 2011.
- ^ Meganathan R (September 2001). "Ubiquinone biosynthesis in microorganisms". FEMS Microbiology Letters. 203 (2): 131–9. doi:10.1111/j.1574-6968.2001.tb10831.x. PMID 11583838.
- ^ a b Bhagavan HN, Chopra RK (May 2006). "Coenzyme Q10: absorption, tissue uptake, metabolism and pharmacokinetics". Free Radical Research. 40 (5): 445–53. doi:10.1080/10715760600617843. PMID 16551570. S2CID 39001523.
- ^ 보젠토프트 1991[verification needed]
- ^ Ochiai A, Itagaki S, Kurokawa T, Kobayashi M, Hirano T, Iseki K (August 2007). "Improvement in intestinal coenzyme q10 absorption by food intake". Yakugaku Zasshi. 127 (8): 1251–4. doi:10.1248/yakushi.127.1251. PMID 17666877.[필요하다]
- ^ a b c d Žmitek; et al. (2008). "Improving the bioavailability of CoQ10". Agro Food Industry Hi Tech. 19 (4): 9. Archived from the original on 5 October 2011. Retrieved 21 October 2008.
- ^ Kishi, H.; Kanamori, N.; Nisii, S.; Hiraoka, E.; Okamoto, T.; Kishi, T. (1964). "Metabolism and Exogenous Coenzyme Q10 in vivo and Bioavailability of Coenzyme Q10 Preparations in Japan". Biomedical and Clinical Aspects of Coenzyme Q. Amsterdam: Elsevier. pp. 131–142.
- ^ a b c Ozawa Y, Mizushima Y, Koyama I, Akimoto M, Yamagata Y, Hayashi H, Murayama H (April 1986). "Intestinal absorption enhancement of coenzyme Q10 with a lipid microsphere". Arzneimittel-Forschung. 36 (4): 689–90. PMID 3718593.
- ^ Tomono Y, Hasegawa J, Seki T, Motegi K, Morishita N (October 1986). "Pharmacokinetic study of deuterium-labelled coenzyme Q10 in man". International Journal of Clinical Pharmacology, Therapy, and Toxicology. 24 (10): 536–41. PMID 3781673.
- ^ Mathiowitz E, Jacob JS, Jong YS, Carino GP, Chickering DE, Chaturvedi P, et al. (March 1997). "Biologically erodable microspheres as potential oral drug delivery systems". Nature. 386 (6623): 410–4. Bibcode:1997Natur.386..410M. doi:10.1038/386410a0. PMID 9121559. S2CID 4324209.
- ^ Hsu CH, Cui Z, Mumper RJ, Jay M (2003). "Preparation and characterization of novel coenzyme Q10 nanoparticles engineered from microemulsion precursors". AAPS PharmSciTech. 4 (3): E32. doi:10.1208/pt040332. PMC 2750625. PMID 14621964.[필요하다]
- ^ Joshi SS, Sawant SV, Shedge A, Halpner AD (January 2003). "Comparative bioavailability of two novel coenzyme Q10 preparations in humans". International Journal of Clinical Pharmacology and Therapeutics. 41 (1): 42–8. doi:10.5414/CPP41042. PMID 12564745.[필요하다]
- ^ Kommuru TR, Ashraf M, Khan MA, Reddy IK (July 1999). "Stability and bioequivalence studies of two marketed formulations of coenzyme Q10 in beagle dogs". Chemical & Pharmaceutical Bulletin. 47 (7): 1024–8. doi:10.1248/cpb.47.1024. PMID 10434405.
- ^ Bhagavan HN, Chopra RK (June 2007). "Plasma coenzyme Q10 response to oral ingestion of coenzyme Q10 formulations". Mitochondrion. 7 Suppl (Suppl): S78-88. doi:10.1016/j.mito.2007.03.003. PMID 17482886.[필요하다]
- ^ US 6197349, Westesen, K. & Sieckmann, B, "변형 물리화학 특성을 가진 입자, 그 준비 및 사용" 2001년 발간
- ^ US 4483873, 오하시, H.; 타카미, T. & 코야마, N. 외, "우비데카레논을 포함한 수용액"은 1984년에 출판되었다.
- ^ Zmitek J, Smidovnik A, Fir M, Prosek M, Zmitek K, Walczak J, Pravst I (2008). "Relative bioavailability of two forms of a novel water-soluble coenzyme Q10". Annals of Nutrition & Metabolism. 52 (4): 281–7. doi:10.1159/000129661. PMID 18645245. S2CID 825159.
- ^ Kagan, Daniel; Madhavi, Doddabele (2010). "A Study on the Bioavailability of a Novel Sustained-Release Coenzyme Q10-β-Cyclodextrin Complex". Integrative Medicine. 9 (1).
- ^ a b c d e Morton RA (December 1958). "Ubiquinone". Nature. 182 (4652): 1764–7. Bibcode:1958Natur.182.1764M. doi:10.1038/1821764a0. PMID 13622652.
- ^ Crane FL, Hatefi Y, Lester RL, Widmer C (July 1957). "Isolation of a quinone from beef heart mitochondria". Biochimica et Biophysica Acta. 25 (1): 220–1. doi:10.1016/0006-3002(57)90457-2. PMID 13445756.
- ^ Wolf DE, et al. (1958). "Coenzyme Q. I. structure studies on the coenzyme Q group". Journal of the American Chemical Society. 80 (17): 4752. doi:10.1021/ja01550a096. ISSN 0002-7863.
- ^ Mellors A, Tappel AL (July 1966). "Quinones and quinols as inhibitors of lipid peroxidation". Lipids. 1 (4): 282–4. doi:10.1007/BF02531617. PMID 17805631. S2CID 2129339.
- ^ a b c d e Pravst I, Zmitek K, Zmitek J (April 2010). "Coenzyme Q10 contents in foods and fortification strategies". Critical Reviews in Food Science and Nutrition. 50 (4): 269–80. doi:10.1080/10408390902773037. PMID 20301015. S2CID 38779392.
- ^ Weber C, Bysted A, Hłlmer G (1997). "The coenzyme Q10 content of the average Danish diet". International Journal for Vitamin and Nutrition Research. Internationale Zeitschrift für Vitamin- und Ernahrungsforschung. Journal International de Vitaminologie et de Nutrition. 67 (2): 123–9. PMID 9129255.
외부 링크
- "List of USP Verified CoQ10 Ingredients". U.S. Pharmacopeial Convention. Archived from the original on 9 February 2009.
- "Coenzyme Q10". National Cancer Institute. 23 September 2005.
- Bonakdar, Robert Alan; Guarneri, Erminia (15 September 2005). "Coenzyme Q10". American Family Physician. 72 (6): 1065–1070. PMID 16190504.