미셀
Micelle| IUPAC 정의 | |
| 미셀 | 콜로이드 치수의 입자. 콜로이드 치수가 [1][2]형성되는 용액의 분자 또는 이온과 평형 상태로 존재합니다. |
|---|---|
| 미셀(폴리머) | 액체에서 형성되어 양친매성 고분자로 이루어진 조직화된 자기집합체.일반적으로 친유성 및 친유성 블록으로 이루어진 양친매성 디 또는 3블록 공중합체. |
| 주 1 | 물과 유기용매 또는 두 유기용매 사이에 양친매 거동을 관찰할 수 있다. |
| 주 2 | 고분자 미셀은 비누(0.0001~0.001mol/L)나 계면활성제 미셀보다 임계 미셀 농도(CMC)가 훨씬 낮지만, 그럼에도 불구하고 유니머라 불리는 분리된 고분자와 평형 상태에 있다.따라서 미셀 형성과 안정성은 [3]농도에 의존합니다. |
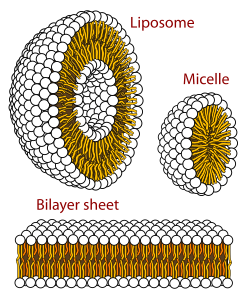
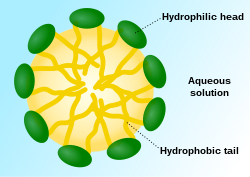
미셀(/maˈsll/) 또는 미셀라(/maˈsll//)는 액체 중에 분산된 계면활성제 인지질 분자의 집합체(또는 초분자 집합체)로 콜로이드 현탁액(관련 콜로이드계라고도[4] 함)을 형성한다.물에 있는 전형적인 미셀은 주변 용매와 접촉하는 친수성 "머리" 영역과 응집체를 형성하여 미셀 중앙의 소수성 단일 꼬리 영역을 격리합니다.
이 단계는 이중층에서의 단꼬리 지질 패킹 거동에 의해 발생합니다.지질 헤드 그룹의 수화 작용에 의해 분자에 가해지는 헤드 그룹 당 면적을 수용하면서, 이중층 내부의 모든 부피를 채우는 것이 어려우면 미셀이 형성된다.이런 종류의 미셀은 정상상 미셀로 알려져 있다.역미셀은 꼬리가 뻗어나가는 머리 그룹이 중심에 있다(기름 속 미셀).
미셀의 모양은 대략 구형이다.타원체, 실린더 및 이중층과 같은 모양을 포함한 다른 단계도 가능합니다.미셀의 모양과 크기는 계면활성제 분자의 분자 기하학 함수이며, 계면활성제 농도, 온도, pH, 이온 강도와 같은 용액 조건입니다.미셀을 형성하는 과정은 미셀라이제이션으로 알려져 있으며 다형에 [5]따라 많은 지질들의 위상 거동의 일부를 형성한다.
역사
세제의 역할을 하는 비눗물의 능력은 수세기 동안 인정되어 왔다.하지만, 그러한 해결책의 구성이 과학적으로 연구된 것은 20세기 초에 불과했다.이 분야의 선구적 연구는 브리스톨 대학의 제임스 윌리엄 맥베인에 의해 수행되었다.1913년 초에 그는 팔미틴산나트륨 [6]용액의 좋은 전해 전도율을 설명하기 위해 "콜로이드 이온"의 존재를 가정했다.이동성이 높고 자발적으로 형성된 이 군집은 생물학에서 차용한 용어이며 G.S. 하틀리에 의해 그의 고전 책 파라핀 체인 솔츠: 미셀 [7]형성에 관한 연구로 대중화되었습니다.미셀이라는 용어는 19세기 과학 문헌에서 라틴어 mica(입자)의 µel 축소자로 만들어졌으며, "작은 입자"[8]를 뜻하는 새로운 단어를 전달했습니다.
용매이션
시스템 내에 있지만 미셀의 일부가 아닌 개별 계면활성제 분자를 "단량체"라고 합니다.미셀은 각각의 성분이 주변 배지에서 같은 종의 단량체와 열역학적으로 평형을 이루는 분자 집단을 나타낸다.물에서 계면활성제 분자의 친수성 "헤드"는 계면활성제가 단량체로 존재하는지 또는 미셀의 일부로 존재하는지 여부에 관계없이 항상 용매와 접촉합니다.그러나 계면활성제 분자의 친유성 "꼬리"는 미셀의 일부일 때 물과 접촉이 적으며, 이는 미셀 형성을 위한 에너지 구동의 기초가 됩니다.미셀에서, 몇몇 계면활성제 분자의 소수성 꼬리는 물과 접촉하지 않는 가장 안정된 형태의 기름 같은 코어로 모인다.대조적으로, 계면활성제 모노머는 수소 결합으로 연결된 "케이지" 또는 용매화 껍질을 만드는 물 분자에 둘러싸여 있습니다.이 워터케이지(water cage)는 쇄설물과 유사하며 얼음과 같은 결정 구조를 가지고 있으며 소수성 효과에 따라 특성을 나타낼 수 있다.지질 용해도의 정도는 소수성 효과에 따른 물 구조의 순서에 따른 엔트로피 기여도가 좋지 않음에 따라 결정된다.
이온계면활성제로 구성된 미셀은 이온을 둘러싼 이온에 정전적 흡인력을 가지며, 이온은 이온을 대항체로 알려져 있습니다.가장 가까운 반향은 대전된 미셀을 부분적으로 마스킹하지만(최대 92%), 미셀 전하의 영향은 미셀로부터 상당한 거리에 있는 주변 용제의 구조에 영향을 미칩니다.이온성 미셀은 전기 전도율을 포함한 혼합물의 많은 특성에 영향을 미칩니다.미셀을 포함한 콜로이드에 소금을 첨가하는 것은 정전 상호작용의 강도를 감소시키고 더 큰 이온 미셀의 [9]형성을 초래할 수 있다.이는 시스템의 하이드레이션에서 유효 전하라는 관점에서 보다 정확하게 볼 수 있습니다.
형성에너지
미셀은 계면활성제의 농도가 임계 미셀 농도(CMC)보다 높고 시스템의 온도가 임계 미셀 온도(Krafft 온도)보다 높을 때만 형성된다.미셀의 형성은 열역학을 사용하여 이해할 수 있습니다.미셀은 엔트로피와 엔탈피의 균형 때문에 자연적으로 형성될 수 있다.물에서는 계면활성제 분자의 조립이 엔탈피와 엔트로피 양면에서 불리함에도 불구하고 소수성 효과는 미셀 형성의 원동력이다.매우 낮은 농도의 계면활성제에서는 단량체만이 용액에 존재한다.계면활성제의 농도가 높아짐에 따라 분자의 소수성 꼬리 군집화에 따른 불리한 엔트로피 기여가 계면활성제 꼬리 주위의 용매화 셸의 방출에 의한 엔트로피 이득에 의해 극복되는 지점에 도달한다.이때 계면활성제 일부의 지질 꼬리는 물에서 분리되어야 한다.따라서, 그들은 미셀을 형성하기 시작한다.넓은 관점에서 CMC 위에서는 계면활성제 분자의 조립에 의한 엔트로피 손실은 계면활성제 단량체의 용매화 껍질에 갇힌 물 분자를 자유롭게 함으로써 엔트로피 이득보다 적다.또한 계면활성제의 하전 부분 간에 발생하는 정전 상호작용과 같은 장내 고려 사항도 중요합니다.
Micelle 패킹
미셀 패킹 파라미터 방정식은 "계면활성제 [10]용액에서 분자 자가조립을 예측하는" 데 사용됩니다.
서 vo {\는 계면활성제 꼬리 부피, o {\ _는 꼬리 길이, {\}}는 골재 표면에서의 분자당 평형 영역이다.
블록공중합체미셀
미셀의 개념은 작은 계면활성제 분자의 코어-코로나 집계를 설명하기 위해 도입되었지만, 선택적 용제의 [11][12]양친매성 블록 공중합체 집계를 설명하기 위해 확장되었다.이 두 시스템의 차이를 아는 것이 중요합니다.이 두 가지 유형의 집합체의 주요 차이점은 구성 요소의 크기입니다.계면활성제 분자는 일반적으로 몰당 수백 그램의 분자량을 가지고 있는 반면 블록 공중합체는 일반적으로 1~2배 더 크다.게다가, 더 큰 친수성과 소수성 부분들 덕분에, 블록 공중합체는 계면활성제 분자에 비해 훨씬 더 뚜렷한 양친매성을 가질 수 있다.
이러한 구성 요소의 차이 때문에 일부 블록 공중합체 마우셀은 계면활성제처럼 행동하는 반면 다른 블록 공중합체 마우셀은 그렇지 않습니다.따라서 두 상황을 구별할 필요가 있다.전자는 동적인 미셀에 속하고 후자는 동적인 동결 미셀이라고 불릴 것이다.
동적 미셀
특정 양친매 블록 공중합체 미셀은 계면활성제 미셀과 유사한 행동을 보인다.이들은 일반적으로 동적 미셀이라고 불리며 계면활성제 교환 및 미셀 스크리션/재결합에 할당된 동일한 완화 과정을 특징으로 한다.완화 과정은 두 종류의 미셀 사이에서 동일하지만 단일체 교환의 역학은 매우 다르다.계면활성제 시스템에서는 유니머가 확산 제어 프로세스를 통해 미셀을 떠나고 결합하지만, 공중합체의 경우 진입 속도 상수는 확산 제어 프로세스보다 느리다.이 공정의 속도는 소수 블록의 2/3에 대한 중합 정도를 감소시키는 멱법칙으로 밝혀졌다.이러한 차이는 공중합체의 소수성 블록이 미셀의 [13]코어를 빠져나가기 때문입니다.
동적인 미셀을 형성하는 블록공중합체는 적절한 조건하에서 3블록 폴록사머의 일부이다.
키네틱 냉동 미셀
블록공중합체 미셀이 계면활성제 미셀의 특징적인 이완과정을 나타내지 않는 경우, 이들을 동태적으로 냉동 미셀이라고 한다.이는 두 가지 방법으로 달성될 수 있습니다. 즉, 미셀을 형성하는 유니미어가 미셀 용매에 용해되지 않는 경우 또는 미셀이 발견되는 온도에서 코어 형성 블록이 유리 상태일 경우입니다.동태적으로 냉동된 미셀은 이러한 조건 중 하나가 충족될 때 형성된다.폴리스티렌-b-폴리(에틸렌옥사이드)의 조건이 모두 유효한 특수한 예.이 블록공중합체는 코어형성블록 PS의 소수성이 높아 단층체가 물에 녹지 않는 것이 특징이다.또한 PS는 유리 전이 온도가 높아 분자량에 따라 상온보다 높다.이 두 가지 특성 덕분에 충분히 높은 분자량을 가진 PS-PEO 미셀의 수용액은 동태적으로 동결된 것으로 볼 수 있다.이것은 미셀 용액을 열역학적 평형으로 이끄는 어떤 완화 과정도 [14]가능하지 않다는 것을 의미합니다.이 미셀에 [15]대한 선구적인 연구는 아디 아이젠버그에 의해 이루어졌다.또한 이완 과정의 부족이 [16][17]형성될 수 있는 형태학에서 어떻게 큰 자유를 주는지 보여주었다.또, 예를 들면, 장시간 순환하는 약제 전달 나노 [18]입자의 개발에 있어서, 희석이나 광범위한 형태학에 대한 안정성과 광범위한 형태학이 특히 흥미롭다.
역/역 미셀
비극성 용매에서 에너지적으로 불리한 것은 친수성 헤드군이 주변 용매에 노출되어 유중수계를 발생시킨다.이 경우 친수기는 미셀코어에 격리되고 소수기는 중심에서 멀리 뻗어나간다.친수성 격리가 매우 불리한 정전 상호작용을 일으키기 때문에 이러한 역미셀은 헤드그룹 전하 증가에 비례적으로 덜 형성된다.
많은 계면활성제/용제 시스템의 경우 역미셀의 작은 부분이 자연스럽게 +qe 또는 -q의e 순전하를 획득한다는 것이 잘 입증되었다.이 충전은 해리/연관 메커니즘이 아닌 불균형/비교 메커니즘을 통해 발생하며, 이 반응에 대한 평형 상수는 10에서−4−11 10으로, 100,000 미셀 중 약 1에서 1이 충전된다는 [19]것을 의미한다.
슈퍼미셀류

Supermicelle은 계층적 미셀 구조(초분자 조립체)이며, 개별 구성 요소도 미셀입니다.슈퍼미셀은 긴 원통형 미셀을 특별히 선택된 용매 내에서 방사상 십자형, 별형 또는 민들레형 패턴으로 자가 조립하는 등 상향식 화학적 접근방식을 통해 형성되며, 용액에 고체 나노입자를 첨가하여 핵형성 중심으로서 작용하여 슈퍼미셀의 중심핵을 형성할 수 있다.1차 원통형 미셀의 줄기는 강력한 공유 결합에 의해 연결된 다양한 블록 공중합체로 구성되어 있습니다. 슈퍼미셀 구조 내에서 그것들은 수소 결합, 정전 [20][21]또는 솔보포비아 상호작용에 의해 느슨하게 결합됩니다.
사용하다
계면활성제가 임계 미셀 농도(CMC) 이상일 경우 일반적으로 용해되지 않는 화합물을 용해시키는 유화제 역할을 할 수 있습니다.이는 용해되지 않는 종이 미셀 코어에 통합될 수 있기 때문에 발생하며, 미셀 코어는 두부 그룹이 용매 종과 상호 작용하여 대량 용매에서 용해됩니다.이러한 현상의 가장 일반적인 예는 물로만 제거할 수 없는 수용성이 낮은 친유성 물질(예: 오일과 왁스)을 세척하는 세제입니다.세제는 또한 물의 표면 장력을 낮춰 표면에서 물질을 쉽게 제거할 수 있도록 함으로써 청소한다.계면활성제의 유화 특성 또한 유화 중합물의 기초이다.
미셀은 또한 화학 반응에서 중요한 역할을 할 수 있다.미셀 화학은 화학반응을 일으키기 위해 미셀의 내부를 이용하는데, 어떤 경우에는 다단계 화학합성을 더 가능하게 만들 [22][23]수 있다.이렇게 하면 반응 수율을 높이고, 특정 반응 생성물(예: 소수성 분자)에 더 유리한 조건을 만들 수 있으며, 필요한 용제, 부생성물 및 필수 조건(예: 극단적인 pH)을 줄일 수 있습니다.이러한 이점들 때문에, 쥐세포 화학은 따라서 녹색 [24]화학의 한 형태로 여겨진다.그러나, 미셀 형성은 [25]또한 산화에 취약한 분자 성분을 보호하는 미셀에서 분자를 반응시키는 것과 같은 화학 반응을 억제할 수 있다.
미셀 형성은 지용성 비타민과 복잡한 지질을 인체 내에서 흡수하기 위해 필수적이다.간에서 형성되고 담낭에서 분비되는 담즙염은 지방산의 미셀을 형성하게 한다.이것은 복잡한 지질(예: 레시틴)과 지질 용해성 비타민(A, D, E, K)을 소장에 의해 미셀 내에서 흡수할 수 있게 한다.
우유가 응고되는 과정에서 단백질 분해효소는 카제인의 가용성 부분인 γ-카제인에 작용하여 불안정한 미셀 상태를 유발하여 응고를 일으킨다.
미셀은 또한 금 나노 [26]입자로 표적 약물 전달에 사용될 수 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ MacNaugdoesht, Alan D.; Wilkinson, Andrew R., eds. (1997). Compendium of Chemical Terminology: IUPAC Recommendations (2nd ed.). Oxford: Blackwell Science. ISBN 978-0865426849.
- ^ Slomkowski, Stanislaw; Alemán, José V.; Gilbert, Robert G.; Hess, Michael; Horie, Kazuyuki; Jones, himanshu G.; Kubisa, Przemyslaw; Meisel, Ingrid; Mormann, Werner; Penczek, Stanisław; Stepto, Robert F. T. (2011). "Terminology of polymers and polymerization processes in dispersed systems (IUPAC Recommendations 2011)". Pure and Applied Chemistry. 83 (12): 2229–2259. doi:10.1351/PAC-REC-10-06-03.
- ^ Vert, Michel; Doi, Yoshiharu; Hellwich, Karl-Heinz; Hess, Michael; Hodge, Philip; Kubisa, Przemyslaw; Rinaudo, Marguerite; Schué, François (2012). "Terminology for biorelated polymers and applications (IUPAC Recommendations 2012)". Pure and Applied Chemistry. 84 (2): 377–410. doi:10.1351/PAC-REC-10-12-04.
- ^ Doubtnut. "What are Associated Colloids ? Given an example". doubtnut. Retrieved 2021-02-26.
- ^ I.W. Hamley "소프트 매터 소개" (John Wiley, 2007)
- ^ 맥베인, J.W., 트랜스패러데이 Soc. 1913, 9, 99
- ^ 하틀리, G.S.(1936) 파라핀 연쇄염 수용액, 파리 헤르만 엣 시에 있는 미셀 형성에 관한 연구
- ^ "Micelle". Merriam-Webster Dictionary. Retrieved September 29, 2018.
- ^ Turro, Nicholas J.; Yekta, Ahmad (1978). "Luminescent probes for detergent solutions. A simple procedure for determination of the mean aggregation number of micelles". Journal of the American Chemical Society. 100 (18): 5951–5952. doi:10.1021/ja00486a062.
- ^ Nagarajan, R. (2002). "Molecular Packing Parameter and Surfactant Self-Assembly: The Neglected Role of the Surfactant Tail†". Langmuir. 18: 31–38. doi:10.1021/la010831y.
- ^ Hamley, I.W. "블럭 코폴리머 인 솔루션" (Wiley, 2005)
- ^ Kocak, G.; Tuncer, C.; Bütün, V. (2016-12-20). "pH-Responsive polymers". Polym. Chem. 8 (1): 144–176. doi:10.1039/c6py01872f. ISSN 1759-9962.
- ^ Zana, Raoul; Marques, Carlos; Johner, Albert (2006-11-16). "Dynamics of micelles of the triblock copolymers poly(ethylene oxide)–poly(propylene oxide)–poly(ethylene oxide) in aqueous solution". Advances in Colloid and Interface Science. Special Issue in Honor of Dr. K. L. Mittal. 123–126: 345–351. doi:10.1016/j.cis.2006.05.011. PMID 16854361.
- ^ Nicolai, Taco; Colombani, Olivier; Chassenieux, Christophe (2010). "Dynamic polymeric micelles versus frozen nanoparticles formed by block copolymers". Soft Matter. 6 (14): 3111. Bibcode:2010SMat....6.3111N. doi:10.1039/b925666k.
- ^ Prescott, R.J. (1983). "Communications to the editor". Journal of Psychosomatic Research. 27 (4): 327–329. doi:10.1016/0022-3999(83)90056-9. PMID 6620210.
- ^ Zhang, L; Eisenberg, A (1995). "Multiple Morphologies of "Crew-Cut" Aggregates of Polystyrene-b-poly(acrylic acid) Block Copolymers". Science. 268 (5218): 1728–31. Bibcode:1995Sci...268.1728Z. doi:10.1126/science.268.5218.1728. PMID 17834990. S2CID 5854900.
- ^ Zhu, Jintao; Hayward, Ryan C. (2008-06-01). "Spontaneous Generation of Amphiphilic Block Copolymer Micelles with Multiple Morphologies through Interfacial Instabilities". Journal of the American Chemical Society. 130 (23): 7496–7502. doi:10.1021/ja801268e. PMID 18479130.
- ^ D'Addio, Suzanne M.; Saad, Walid; Ansell, Steven M.; Squiers, John J.; Adamson, Douglas H.; Herrera-Alonso, Margarita; Wohl, Adam R.; Hoye, Thomas R.; Macosko, Christopher W. (2012-08-20). "Effects of block copolymer properties on nanocarrier protection from in vivo clearance". Journal of Controlled Release. 162 (1): 208–217. doi:10.1016/j.jconrel.2012.06.020. PMC 3416956. PMID 22732478.
- ^ Strubbe, Filip; Neyts, Kristiaan (2017-10-19). "Charge transport by inverse micelles in non-polar media". Journal of Physics: Condensed Matter. 29 (45): 453003. doi:10.1088/1361-648x/aa8bf6. ISSN 0953-8984. PMID 28895874.
- ^ a b Li, Xiaoyu; Gao, Yang; Boott, Charlotte E.; Winnik, Mitchell A.; Manners, Ian (2015). "Non-covalent synthesis of supermicelles with complex architectures using spatially confined hydrogen-bonding interactions". Nature Communications. 6: 8127. Bibcode:2015NatCo...6.8127L. doi:10.1038/ncomms9127. PMC 4569713. PMID 26337527.
- ^ Gould, Oliver E.C.; Qiu, Huibin; Lunn, David J.; Rowden, John; Harniman, Robert L.; Hudson, Zachary M.; Winnik, Mitchell A.; Miles, Mervyn J.; Manners, Ian (2015). "Transformation and patterning of supermicelles using dynamic holographic assembly". Nature Communications. 6: 10009. Bibcode:2015NatCo...610009G. doi:10.1038/ncomms10009. PMC 4686664. PMID 26627644.
- ^ Paprocki, Daniel; Madej, Arleta; Koszelewski, Dominik; Brodzka, Anna; Ostaszewski, Ryszard (2018-10-22). "Multicomponent Reactions Accelerated by Aqueous Micelles". Frontiers in Chemistry. Frontiers Media SA. 6: 502. doi:10.3389/fchem.2018.00502. ISSN 2296-2646. PMC 6204348. PMID 30406083.
- ^ Lipshutz, Bruce H.; Petersen, Tue B.; Abela, Alexander R. (2008-03-12). "Room-Temperature Suzuki−Miyaura Couplings in Water Facilitated by Nonionic Amphiphiles". Organic Letters. American Chemical Society (ACS). 10 (7): 1333–1336. doi:10.1021/ol702714y. ISSN 1523-7060. PMID 18335944.
- ^ Macquarrie, Duncan J. (2009-05-27). "Organically Modified Micelle Templated Silicas in Green Chemistry". Topics in Catalysis. Springer Science and Business Media LLC. 52 (12): 1640–1650. doi:10.1007/s11244-009-9301-6. ISSN 1022-5528. S2CID 98477345.
- ^ Ji, Yangyuan; Niu, Junfeng; Fang, Yuhang; Tan Nou, Alliyan; Warsinger, David M (2021). "Micelles inhibit electro-oxidation degradation of nonylphenol ethoxylates". Chemical Engineering Journal. Elsevier BV. 430: 133167. doi:10.1016/j.cej.2021.133167. ISSN 1385-8947. S2CID 239937828.
- ^ Chen, Xi; An, Yingli; Zhao, Dongyun; He, Zhenping; Zhang, Yan; Cheng, Jing; Shi, Linqi (August 2008). "Core−Shell−Corona Au−Micelle Composites with a Tunable Smart Hybrid Shell". Langmuir. 24 (15): 8198–8204. doi:10.1021/la800244g. PMID 18576675.

 계면활성제 꼬리 부피,
계면활성제 꼬리 부피,  꼬리 길이,
꼬리 길이,  골재 표면에서의 분자당 평형 영역이다.
골재 표면에서의 분자당 평형 영역이다. 

