코엔자임 M
Coenzyme M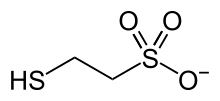 | |
| 이름 | |
|---|---|
| IUPAC 이름 2-술파닐에탄술폰산염 | |
| 시스템 IUPAC 이름 2-술파닐에탄술폰산염 | |
| 기타 이름 2-메르캅토에틸술폰산염, 2-메르캅토에탄술폰산염, 코엔자임M 음이온, H-S-CoM, AC1L1HCY, 2-술파닐에탄-1-술폰산염, CTK8A8912 | |
| 식별자 | |
| |
3D 모델(JSmol) | |
| 체비 | |
| 켐스파이더 | |
PubChem CID | |
| 유니 |
|
| |
| |
| 특성. | |
| C2H5O3S2 | |
| 몰 질량 | 141.18 g/120−1 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
코엔자임 M은 고대 메타노겐의 대사 [1][2]및 박테리아 내 [3]다른 기질의 대사 과정에서 메틸 전달 반응에 필요한 조효소이다.또한 알켄산화세균의 대사 경로에서 필요한 보조인자이다.CoM은 프로필렌과 [4]같은 알케인의 산화로 인해 생성되는 독성 에폭시드를 제거하는 데 도움이 됩니다.이 조효소의 구조는 1974년 CD Taylor와 RS Wolfe가 [5]일부 혐기성 박테리아에서 이산화탄소가 메탄으로 변하는 과정인 메타노제네시스(methanogenesis)를 연구하던 중 발견되었습니다.코엔자임은 HSCHCSO 공식의 음이온으로
2
2−
3 2-mercaptoethanesulfonate로 불리며 HS-CoM으로 약칭됩니다.양이온은 중요하지 않지만 나트륨 소금이 가장 많이 있습니다.메르캅토에탄술폰산염은 반응성의 주요 부위인 티올과 수용성 매체에 용해성을 부여하는 술폰산염기를 모두 포함한다.
생화학적 역할
메타노제네시스
코엔자임은 메타노제네시스에서의 C1 공여체이다.메탄 [6]생성 단계에서는 메틸-코엔자임 M 티오에테르, 티오에테르 CH3SCH2CH2SO-3로 전환된다.메틸-코엔자임 M은 코엔자임 B, 7-티오헵타노일트레오닌인산과 반응하여 헤테로디술피드를 생성하며 메탄을 방출한다.
- CH3 – S – CoM + HS – CoB → CH4 + CoB –S–S–CoM
이 유도 작용은 보철기로서 보조인자 F430을 제한하는 메틸-코엔자임 M 환원효소에 의해 촉매된다.
알켄 대사
코엔자임 M은 또한 CO로부터2 아세토아세테이트를 만들고 호기성 세균에서 프로필렌 또는 에틸렌을 만드는 데 사용된다.특히, 알켄을 에폭시드로 산화시키는 박테리아에서.프로필렌(또는 다른 알켄)이 에폭시화되어 에폭시프로판이 된 후 친전자성 및 독성이 됩니다.이 에폭시드는 DNA와 단백질과 반응하여 세포 기능에 영향을 미칩니다.크산토박터 자가영양균과[4] 같은 알켄산화세균은 CoM이 지방족 에폭시드와 결합하는 대사경로를 이용한다.이 단계는 CO와2 반응할 수 있는 친핵성 화합물을 생성한다.최종적인 카르복실화는 프로필렌을 분해하면서 아세토아세테이트를 [4]생성한다.
「 」를 참조해 주세요.
- 메스나 – 동일한 구조를 가진 암 화학요법 보조제
레퍼런스
- ^ Balch WE, Wolfe RS (1979). "Specificity and biological distribution of coenzyme M (2-mercaptoethanesulfonic acid)". J. Bacteriol. 137 (1): 256–63. doi:10.1128/JB.137.1.256-263.1979. PMC 218444. PMID 104960.
- ^ Taylor CD, Wolfe RS (10 August 1974). "Structure and methylation of coenzyme M(HSCH
2CH
2SO
3)". J. Biol. Chem. 249 (15): 4879–85. doi:10.1016/S0021-9258(19)42403-4. PMID 4367810. - ^ Partovi, Sarah E.; Mus, Florence; Gutknecht, Andrew E.; Martinez, Hunter A.; Tripet, Brian P.; Lange, Bernd Markus; DuBois, Jennifer L.; Peters, John W. (2018-04-06). "Coenzyme M biosynthesis in bacteria involves phosphate elimination by a functionally distinct member of the aspartase/fumarase superfamily". The Journal of Biological Chemistry. 293 (14): 5236–5246. doi:10.1074/jbc.RA117.001234. ISSN 1083-351X. PMC 5892593. PMID 29414784.
- ^ a b c Krishnakumar, Arathi M.; Sliwa, Darius; Endrizzi, James A.; Boyd, Eric S.; Ensign, Scott A.; Peters, John W. (September 2008). "Getting a Handle on the Role of Coenzyme M in Alkene Metabolism". Microbiology and Molecular Biology Reviews. 72 (3): 445–456. doi:10.1128/MMBR.00005-08. ISSN 1092-2172. PMC 2546864. PMID 18772284.
- ^ Parry, Ronald J. (1999-01-01), Barton, Sir Derek; Nakanishi, Koji; Meth-Cohn, Otto (eds.), "1.29 - Biosynthesis of Sulfur-containing Natural Products", Comprehensive Natural Products Chemistry, Oxford: Pergamon, pp. 825–863, doi:10.1016/b978-0-08-091283-7.00031-x, ISBN 978-0-08-091283-7, retrieved 2022-05-10
- ^ Thauer, Rudolf K. (1998-09-01). "Biochemistry of methanogenesis: a tribute to Marjory Stephenson:1998 Marjory Stephenson Prize Lecture". Microbiology. 144 (9): 2377–2406. doi:10.1099/00221287-144-9-2377. ISSN 1350-0872. PMID 9782487.