부티르산
Butyric acid
| | |||
 | |||
| 이름 | |||
|---|---|---|---|
| 선호 IUPAC 이름 부타노산[1] | |||
| 기타 이름 | |||
| 식별자 | |||
| |||
3D 모델(JSmol) |
| ||
| 체비 |
| ||
| 켐벨 |
| ||
| 켐스파이더 | |||
| 드러그뱅크 |
| ||
| ECHA InfoCard | 100.003.212 | ||
| EC 번호 |
| ||
| |||
| 케그 |
| ||
| 메슈 | 부트리크+아시드 | ||
펍켐 CID | |||
| RTECS 번호 |
| ||
| 유니 | |||
| UN 번호 | 2820 | ||
CompTox 대시보드 (EPA) |
| ||
| |||
| |||
| 특성. | |||
| 츄오 3 7 | |||
| 어금질량 | 88.1987 g·messages−1 | ||
| 외관 | 무색액 | ||
| 냄새 | 불쾌함, 구토물 또는 체취와 유사함 | ||
| 밀도 | 1.135 g/cm3(-43 °C)[2] 0.9528 g/cm3(25°C)[3] | ||
| 녹는점 | -5.1°C(22.8°F, 268.0K)[3] | ||
| 비등점 | 163.75°C(326.75°F, 436.90K)[3] | ||
| -35°C에서 서브라임 ΔsublH | |||
| 불능 | |||
| 용해성 | 에탄올, 에테르와 섞이지 않음. CCl에4 약간 용해성 | ||
| 로그 P | 0.79 | ||
| 증기압 | 0.112kPa(20°C) 0.74kPa(50°C) 9.62 kPa(100 °C)[4] | ||
헨리의 법률가 (kH) | 5.35·10−4 L·atm/mol | ||
| 산도(pKa) | 4.82 | ||
자기 감수성(magnetic susibility) | -55.10·10cm−63/192 | ||
| 열전도도 | 1.46·105 W/m·K | ||
굴절률(nD) | 1.398(20°C)[3] | ||
| 점도 | 1.814 cP(15°C)[5] 1.426 cP(25 °C) | ||
| 구조 | |||
| 단핵(-43 °C)[2] | |||
| C2/m[2] | |||
a = 8.01 å, b = 6.82 å, c = 10.14 å[2] α = 90°, β = 111.45°, γ = 90° | |||
| 0.93 D(20°C)[5] | |||
| 열화학 | |||
열 용량 (C) | 178.6 J/몰·K[4] | ||
성 어금니 엔트로피 (S | 222.2 J/몰·K[5] | ||
의 성 엔탈피 대형화 (ΔfH⦵298) | −533.9 kJ/mol[4] | ||
의 성 엔탈피 연소시키다 (ΔcH⦵298) | 2183.5 kJ/mol[4] | ||
| 위험 | |||
| GHS 라벨 표시: | |||
 [6] [6] | |||
| 위험하다. | |||
| H314[6] | |||
| P280, P305+P351+P338, P310[6] | |||
| NFPA 704(화재 다이아몬드) | |||
| 플래시 포인트 | 71~72°C(160~162°F, 344~345K)[6] | ||
| 440°C(824°F, 713K)[6] | |||
| 폭발 한계 | 2.2–13.4% | ||
| 치사량 또는 농도(LD, LC): | |||
LD50(중간 선량) | 2000mg/kg(도덕, 랫드) | ||
| 안전 데이터 시트(SDS) | 외부 MSDS | ||
| 관련 화합물 | |||
관련 카르복실산 | 프로피온산, 펜타노산 | ||
관련 화합물 | 1-부탄올 부티랄데히드 메틸부티레이트 | ||
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |||
| Infobox 참조 자료 | |||
부티르산(고대 그리스어: βούττῡῡρννννννν, '버터'라는 뜻)은 화학식 CHCHCCOH를3222 가진 직선 체인 알킬 카르복실산이다. 그것은 불쾌한 냄새가 나는 기름기가 많고 무색의 액체다. 이소부티르산(Isobutyric acid, 2-methylpropanoic acid)은 이소머이다. 부티릭산의 소금과 에스테르는 부티레이트 또는 부토노아이트로 알려져 있다. 산은 자연에서 광범위하게 발생하지는 않지만 에스테르는 널리 퍼져 있다. 그것은 일반적인 산업 화학[7] 물질이고 포유류 내장의 중요한 성분이다.
역사
부티르산은 1814년 프랑스의 화학자 미셸 외젠 쉐브렐에 의해 불순물 형태로 처음 관찰되었다. 1818년까지 그는 그것을 특징 짓기에 충분할 정도로 정화시켰다. 그러나 쉐브렐은 부티르산에 대한 초기 연구 결과를 발표하지 않고 대신 프랑스 파리의 과학아카데미 서기와 함께 원고 형태로 연구 결과를 기탁했다. 프랑스의 화학자인 앙리 브라콘노도 버터의 성분을 연구하고 있었고, 그의 연구 결과를 발표 중이었는데, 이것이 우선순위에 대한 논쟁으로 이어졌다. 일찍이 1815년에 쉐브렐은 버터 냄새를 일으키는 물질을 발견했다고 주장했다.[8] 1817년까지 부티르산의 성질에 관한 연구 결과를 발표하여 이름을 붙였다.[9] 그러나 1823년에 이르러서야 부티르산의 성질을 상세히 제시했다.[10] 부티르산이라는 이름은 고대 그리스어에서 유래되었다: βύτῡρννννννννν, 처음 발견된 물질인 "버터"를 의미한다. 라틴어 이름 부티럼(또는 부뚜럼)도 비슷하다.
발생
부티르산의 트리글리세리드는 버터의 3~4%를 구성한다. 버터가 썩으면, 부티르산은 가수 분해에 의해 글리세리드로부터 해방된다.[11] 그것은 쇼트 체인 지방산이라고 불리는 지방산 부분군 중 하나이다. 부티르산은 염기와 반응하여 많은 금속들에 영향을 미치는 대표적인 카르복실산이다.[12] 동물성 지방과 식물성 기름, 소젖, 모유, 버터, 파마산 치즈, 체취, 토사물, 혐기성 발효 제품(대장 포함)에서 발견된다.[13][14] 버터와 비슷한 맛과 불쾌한 냄새가 난다. 개와 같이 향기 검출 능력이 좋은 포유류는 10억분의 1로 검출할 수 있는 반면 인간은 10ppm 이상의 농도로만 검출할 수 있다. 식품 제조에서는 향료제로 사용된다.[15]
인간에서 부티르산은 G-커플i/o G 단백질 결합 수용체인 인간 히드록시카르복실산 수용체2(HCA2)의 두 가지 일차 내생 작용제 중 하나이다.[16][17]
부티르산은 파르스닙(파르스티나카 사티바)[18]과 은행나무의 씨앗에 옥틸 에스테르로 존재한다.[19]
생산
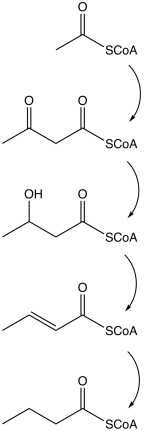
공업
산업계에서는 프로펜과 승라에서 나오는 하이드로폼화하여 부티릭산이 생산되어 부티랄알데히드가 형성되어 최종 산물로 산화된다.[7]
- H2 + CO + CHC3=CH2 → CHCHCHO322 → 부티르산
염화칼슘 등 염분을 포화시켜 수용액과 분리할 수 있다. 칼슘 소금, Ca(CHO472)..2HO는2 차가운 물보다 뜨거운 물에 덜 녹는다.
미생물 생합성
부티레이트(Butyrate)는 의무적인 혐기성 박테리아에 의해 수행되는 여러 발효 과정에 의해 생성된다.[20] 이 발효 경로는 1861년 루이 파스퇴르에 의해 발견되었다. 부티레이트를 생성하는 박테리아 종의 예:
- 클로스트리디움부티쿰
- 클로스트리디움클루이베리
- 클로스트리디움파스퇴리아누스
- 파에칼리박테리움 프라우스니치
- 후소박테리움핵종
- 부티리비브리오 피브리솔벤스
- 에우박테리움 리모숨
이 길은 대부분의 유기체에서 일어나는 것처럼 포도당의 글루코성 갈라짐으로 시작한다. Pyruvate는 아세틸 코엔자임 A에 의해 산화된다. Pyruvate:ferredoxin oxic oxidorductase. 폐기물로서 이산화탄소2(CO)의 두 분자와 원소 수소2(H)의 두 분자가 형성된다. 그 후, 발효의 마지막 단계에서 생산된다. 각 포도당 분자에 대해 비교적 높은 수율인 3개의 ATP 분자가 생성된다. 이 발효를 위한 균형 방정식은
- C6H12O6 → C4H8O2 + 2 CO2 + 2 H2
부티레이트로의 다른 경로로는 굴복성 감소와 크로노네이트 불균형이 있다.
| 액션 | 책임효소 |
|---|---|
| 아세틸 코엔자임 A가 아세토아세틸 코엔자임 A로 변환됨 | 아세틸-코아-아세틸전달효소 |
| Acetoacetyl coenzyme A가 β-hydroxybutyryl CoA로 변환됨 | β-히드록시부티릴-CoA 탈수소효소 |
| 크로토닐 CoA로 변환하는 β-히드록시부티릴 CoA | 크로토나아제 |
| Crotonyl CoA가 Butyryl CoA로 변환(CHCHC322=O-CoA) | 부틸 코아 탈수소효소 |
| 인산염 그룹이 CoA를 대체하여 부티릴 인산염을 형성한다. | 인산염화효소 |
| 인산염 그룹이 ADP와 결합하여 ATP와 Butyrate를 형성함 | 부티레이트키나아제 |
다른 경로에서 아세톤과 n-부탄올을 형성하는 종은 부티레이트 발효로 시작된다. 이러한 종의 일부는 다음과 같다.
- 가장 뛰어난 아세톤과 부탄올 생산지인 클로스트리디움 아세토부틸리쿰도 산업에서 사용된다.
- 클로스트리디움베예린키이
- 클로스트리디움 테타노모르푸스
- 클로스트리디움오란티부티쿰
이들 박테리아는 위에서 설명한 대로 부티레이트 발효로 시작하지만 pH가 5 이하로 떨어지면 pH가 더 이상 낮아지지 않도록 부탄올과 아세톤 생산으로 전환한다. 아세톤의 각 분자에 대해 두 개의 부탄올 분자가 형성된다.
경로의 변화는 아세토아세틸 CoA 형성 후 발생한다. 그러면 이 중간은 두 가지 가능한 경로를 취한다.
- 아세토아세틸 CoA → 아세토아세테이트 → 아세톤
- 아세토아세틸 CoA → 부티릴 CoA → 부티랄데히드 → 부탄올
발효섬유원
내성성 녹말, 귀리겨, 펙틴, 구아 등의 고발효성 섬유 잔류물은 대장균에 의해 부티레이트를 포함한 단사슬 지방산(SCFA)으로 변형되어 셀룰로오스 등 발효성이 낮은 섬유보다 SCFA가 더 많이 발생한다.[14][21] 한 연구는 저항성 녹말이 다른 종류의 식이섬유보다 부티레이트를 지속적으로 더 많이 생산한다는 것을 발견했다.[22] 소와 같은 반추동물에서 섬유로부터 SCFA를 생산하는 것은 우유와 버터의 부티레이트 함량을 책임진다.[13][23]
과당은 부티레이트를 생산하기 위해 소화될 수 있는 전생물학적 가용성 식이섬유의 또 다른 공급원이다.[24] 그것들은 종종 아륨과 십자가형 야채와 같이 황이 많이 함유된 음식의 수용성 섬유에서 발견된다. fructans의 소식통에 따르면 밀(비록 쌀보리와 같은 밀을 변종 소량 포함되어 있)[25]호밀, 보리, 양파, 마늘, 예루살렘과 지구 아티 초크, 아스파라거스, 사탕무,chicory, 민들레 잎이 나오는 것음 파, 적색 치커리, 봄 양파, 브로콜리, brussels 콩나물 양배추, 회향과 프락토 올리고당과 같은 프리 바이오틱스의 하얀 부분을 포함한다.s(FOS, 올리고프룩토스, 이눌린.[26][27]
반응
부티르산은 전형적인 카르복실산으로서 반응한다: 그것은 아미드, 에스테르, 무수화물, 염화 유도체를 형성할 수 있다.[28] 후자의 염화 부틸은 보통 다른 것을 얻기 위한 매개체로 사용된다.
사용하다
부티릭산은 다양한 부티레이트 에스테르를 준비하는데 사용된다. 셀룰로오스 아세테이트 부티레이트(CAB)를 생산하는 데 사용되며, 다양한 도구와 페인트, 코팅에 사용되며 셀룰로오스 아세테이트보다 분해에 더 강하다.[29] CAB는 열과 습기에 노출되면 분해되어 부티르산을 방출할 수 있다.[30]
메틸부티레이트 등 부티르산의 저분자중량 에스테르는 대부분 쾌적한 향이나 맛을 가지고 있다.[7] 그 결과 식품 및 향수 첨가물로 사용된다. EU FAVIS 데이터베이스에서 승인된 식품 향미료(번호 08.005)이다.
강한 냄새 때문에 낚시 미끼 첨가물로도 쓰이고 있다.[31] 잉어(Cyprinus carpio) 미끼에 사용되는 상업적으로 구할 수 있는 많은 맛들은 부티르산을 에스테르 베이스로 사용한다. 생선이 부티산 자체에 끌리는 것인지, 여기에 첨가된 물질에 끌리는 것인지는 분명하지 않다. 부티르산은 텐치와 쓴맛을 모두 느낄 수 있는 몇 안 되는 유기산 중 하나이다.[32] 이 물질은 일본 포경선원들을 교란시키기 위해 씨셰퍼드 보호협회에 의해 악취 폭탄으로 사용되어 왔다.[33]
약리학
| 억제효소 | IC50()nM | 엔트리 노트 |
|---|---|---|
| HDAC1 | 16,000 | |
| HDAC2 | 12,000 | |
| HDAC3 | 9,000 | |
| HDAC4 | 2,000,000 | 하한 |
| HDAC5 | 2,000,000 | 하한 |
| HDAC6 | 2,000,000 | 하한 |
| HDAC7 | 2,000,000 | 하한 |
| HDAC8 | 15,000 | |
| HDAC9 | 2,000,000 | 하한 |
| CA1 | 511,000 | |
| CA2 | 1,032,000 | |
| GPCR 대상 | pEC50 | 엔트리 노트 |
| FFAR2 | 2.9–4.6 | 완전작용제 |
| FFAR3 | 3.8–4.9 | 완전작용제 |
| HCA2 | 2.8 | 작용제 |
약리역학
부티르산(pKa 4.82)은 생리학적 pH에서 완전 이온화되므로 음이온은 주로 생물학적 계통에 관련된 물질이다. 인간 히드록시카르복실산 수용체 2(HCA2, 일명 GPR109A), G-커플i/o G 단백질 결합 수용체(GPCR)의 1차 내생 작용제 중 하나이다.[16][17]
다른 쇼트체인 지방산(SCFA)과 마찬가지로 부티레이트는 자유지방산 수용체 FFAR2와 FFAR3의 작용제로 에너지 균형의 동태적 제어를 용이하게 하는 영양센서 역할을 하지만 SCFA 그룹 중 부티레이트만이 HCA의2 작용제다.[36][37][38] 또한 히스톤 디아세틸라제 효소의 기능을 억제하여 세포 내 히스톤의 아세틸화 상태를 유리하게 하는 [34][35]약인 HDAC1, HDAC2, HDAC3, HDAC8)도 HDAC 억제제다.[38] 히스톤 아세틸화는 히스톤과 DNA 사이의 정전기 흡인력을 감소시킴으로써 염색질의 구조를 느슨하게 한다.[38] 일반적으로 전사 인자는 히스톤이 DNA와 밀접하게 연관되어 있는 영역(즉, 비 아세틸화, 예를 들어 이질화)에 접근할 수 없을 것으로 생각된다.[medical citation needed] 따라서 부티르산은 발기인에서 전사 활동을 강화하는 것으로 생각되는데,[38] 이는 히스톤 제산제 활성으로 인해 일반적으로 침묵되거나 하향 조절된다.
약동학
Butyrate은 결장 안에 식이 섬유의 미생물 발효를 통해 생성된다, 주로 리드미컬하고 대사 colonocytes, ATP생성에 에너지 대사에 liver[노트 1]에 의해, 일부 뷰티 레이트는 문맥에 연결될 수 없는 먼 쪽의 대장,에서의 한 제도적인 경멸하다 허용되는 흡수된다 흡수된다.tributio순환계를 통해 여러 기관 시스템에 부티레이트 n.[38] 체계적 순환에 도달한 부티레이트(Butyrate)는 단카복시화 전달체(즉, SLC16A 전달체 그룹의 특정 구성원)를 통해 혈액뇌 장벽을 쉽게 통과할 수 있다.[39][40] 지질막을 가로지르는 부티레이트 통과를 중재하는 다른 전달체로는 SLC5A8(SMCT1)과 SLC27A1(FATP1) 및 SLC27A4(FATP4)가 있다.[34][40]
신진대사
부티르산은 부티레이트-CoA 리가아제라고도 알려진 다양한 인간 XM(ACSM1, ACSM2B, ASCM3, ACSM4, ACSM5, ACSM6)에 의해 대사된다.[41][42] 이 반응에 의해 생성되는 대사물은 부틸-CoA이며, 다음과 같이 생성된다.[41]
- 아데노신 3인산 + 부티산 + 코엔자임 A → 아데노신 모노인산 + 파이로인산 + 부티릴-코아
단사슬 지방산으로서 부티레이트는 지방산 대사를 통해 미토콘드리아에 의해 에너지(즉 아데노신 삼인산 또는 ATP)원으로 대사된다.[38] 특히 포유류 결장(콜론세포)에 안착하는 세포의 중요한 에너지원이기도 하다.[24] 부티레이트가 없으면 결장세포는 자가소화(즉 자가소화)를 거쳐 죽는다.[43]
인간의 경우 버터에 자연적으로 존재하는 부티레이트 전구체 트리뷰티린은 트리아실글리세롤 리파아제에 의해 다음과 같은 반응을 통해 디부티린과 부티레이트로 대사된다.[44]
- 트리뷰티린 + HO2 → 디부티린 + 부티산
생화학
부티레이트(Butyrate)는 사람의 에너지 홈스태스와 관련 질병(당뇨 및 비만), 염증, 면역 기능(예: 항균 및 항균 유발 효과를 발음함)에 수많은 영향을 미친다. 이러한 영향은 지방산 대사 중에 생성하기 위해 미토콘드리아에 의한 대사 또는 히스톤 수정 효소 대상(즉, 클래스 I 히스톤 디아세틸라제)과 G-단백 결합 수용체 대상(예: FFAR2, FFAR3, HCA2)을 통해 발생한다.[36][45]
포유류 내장에서
부티레이트(Butyrate)는 면역항진증 치료에 필수적이다.[36] 비록 내장에서 부티레이트의 역할과 중요성은 완전히 이해되지는 않았지만, 많은 연구자들은 여러 가지 혈관 질환을 가진 환자들에게 부티레이트를 생성하는 박테리아의 고갈이 이러한 장애의 병원생성에 필수적이라고 주장한다. 내장에서 부티레이트 고갈은 일반적으로 부티레이트 생산박테리아(BPB)의 부재 또는 고갈에 의해 발생한다. BPB의 이러한 고갈은 미생물 이상 증후로 이어진다. 이것은 전반적으로 낮은 생물다양성과 핵심 부티레이트를 생산하는 구성원의 고갈을 특징으로 한다. 부티레이트(Butyrate)는 숙주 내 적절한 면역 기능의 조절자 역할을 하는 필수 미생물 대사물이다. BPB가 부족한 아이들은 알레르기 질환과[46] 제1형 당뇨병에 더 취약한 것으로 나타났다.[47] 부티레이트는 또한 섬유질이 적은 식단에서 감소하는데, 이것은 염증을 유발할 수 있고 이러한 단사슬 지방산이 PPAR-solution을 활성화하는 한 다른 부작용을 일으킬 수 있다.[48]
부티레이트(Butyrate)는 국소적으로나 시스템적으로 (순환 부티레이트를 통해) 면역항진 유지에 중요한 역할을 한다. 규제 T세포의 분화를 촉진하는 것으로 나타났다. 특히 순환 부티레이트는 과민성 규제 T세포의 생성을 촉진한다. 인간 대상체에서 부티레이트의 낮은 수준은 규제 T 세포 매개 통제의 감소에 유리할 수 있으며, 따라서 강력한 면역 병리학적 T 세포 대응을 촉진할 수 있다.[49] 반면, 내트 부티레이트는 국소성 염증성 사이토카인을 억제하는 것으로 보고되었다. 따라서 이러한 BPB가 내장에 없거나 고갈되는 것은 지나치게 적극적인 염증 반응의 가능한 보좌관이 될 수 있다. 내장에 있는 부티레이트 또한 장내 상피 장벽의 무결성을 보호한다. 따라서 부티레이트 수치가 감소하면 장내 상피 장벽이 손상되거나 기능장애로 이어진다.[50]
후루사와 외 연구진이 실시한 2013년 연구에서 쥐의 대장 조절 T세포 분화를 유도하는 데 마이크로비브 유래 부티레이트(microbe-derved butyrate)가 필수인 것으로 나타났다. 규제 T 세포는 염증 및 알레르기 반응을 억제하는 데 중심적인 역할을 하기 때문에 이것은 매우 중요하며 많은 염증성 질환과 관련된 병원체 및 혈관염과 관련이 있을 수 있다.[51] 여러 연구 연구에서 부티레이트가 체외 및 체내 규제 T세포의 분화를 유도했다는 것이 입증되었다.[52] 부티레이트(butyrate)의 항염증 능력은 많은 연구에서 광범위하게 분석되고 지원되어 왔다. 미생물이 생산한 부티레이트는 특정 메커니즘이 불분명하지만 규제 T세포의 생산을 촉진하는 것으로 밝혀졌다.[53] 좀 더 최근에는 부티레이트가 세포독성 T세포의 유전자 발현을 조절하는 데 필수적이고 직접적인 역할을 하는 것으로 나타났다.[54] 부티레이트 또한 중성미자에 항염증 효과가 있어 상처로의 이동을 감소시킨다. 이 효과는 수용체 HCA를1[55] 통해 매개된다.
면역억제 및 염증
부티레이트가 면역체계에 미치는 영향은 HCA2(GPR109A), FFAR2(GPR43) 및 FFAR3(GPR41) 등 G단백질 결합 수용체 대상의 I급 제산 억제와 활성화를 통해 매개된다.[37][56] 부티레이트(butyrate)는 단사슬 지방산 중 체외에서 장내 규제 T세포의 가장 강력한 촉진제로서 HCA2 리간드 그룹 중 유일하게 유일하게 부티레이트(butyrate)[37]가 있다. 대장염증 반응의 결정적 중재자로 나타났다. 그것은 염증 매개 궤양성 대장염과 대장암에 대항할 수 있는 예방과 치료 가능성을 모두 가지고 있다.
부티레이트는 히스톤 H3의 HDAC 억제를 통해 유도하는 항균 펩타이드 LL-37을 통해 매개되는 인간 내 항균 성질을 확립했다.[56][57][58] 시험관내 부티레이트(butyrate)는 FOXP3(의 전사조절기)의 유전자 발현을 증가시키고, 1급 히스톤 제산제의 억제를 통해 대장 조절 T세포(tregs)를 촉진하며,[37][56] 이러한 작용을 통해 항염증 시토카인 인터루킨 10의 발현을 증가시킨다.[56][37] 부티레이트도 히스톤 제산제 억제를 통해 부분적으로 매개되는 IFN-reason–STAT1 신호 경로를 억제하여 대장 염증을 억제한다. 과도성 IFN 신호는 일반적으로 정상적인 호스트 면역 반응과 관련이 있지만, 만성 IFN 신호는 만성 염증과 관련이 있는 경우가 많다. 부티레이트(butyrate)는 T세포에서 FAS 유전자 프로모터에 바인딩된 HDAC1의 활동을 억제하여, FAS 프로모터의 과급화 및 T세포 표면에서 FAS 수용체의 상향 조절을 초래하는 것으로 나타났다.[59]
연구된 다른 HCA2 작용제들과 유사하게, 부티레이트 또한 뇌, 위장, 피부, 혈관 조직을 포함한 다양한 조직에서 두드러진 항염증 효과를 낸다.[60][61][62] FFAR3의 부티레이트 결합은 신경펩타이드 Y 방출을 유도하고 대장 점막과 장내 면역계의 기능적 동점선을 촉진한다.[63]
암
부티레이트는 대장 염증 반응의 결정적인 중재자로 나타났다. 그것은 결장동식세포에서 나오는 약 70%의 에너지를 책임지고 있으며, 결장동맥경화에서 중요한 SCFA가 된다.[64] Butyrate는 염증 매개 궤양성 대장염(UC)과 대장암에 대항할 수 있는 예방과 치료 잠재력을 모두 가지고 있다.[65] 그것은 건강하고 암적인 세포에서 다른 효과를 만들어낸다: 이것은 "버티레이트 역설"이라고 알려져 있다. 특히 부티레이트는 대장종양세포를 억제하고 건강한 대장상피세포의 증식을 자극한다.[66][67] 부티레이트(butyrate)가 정상 대장세포의 에너지원이며 대장암세포의 세포사멸을 유도하는 이유는 암세포의 워버그 효과로 부티레이트(warburg)가 제대로 대사되지 않게 된다. 이 현상은 핵에 부티레이트가 축적되어 히스톤 디아세틸라제(HDAC) 억제제 역할을 하게 된다.[68] 결장 염증 억제에서 부티레이트 기능의 기초가 되는 한 가지 메커니즘은 IFN-medule/STAT1 신호 전달 경로의 억제다. 부티레이트(butyrate)는 T세포에서 FAS 유전자 프로모터에 바인딩된 HDAC1의 활동을 억제하여 FAS 프로모터의 과급화 및 T세포 표면에서 FAS 수용체 상향 조절을 유발하는 것으로 나타났다. 따라서 부티레이트는 대장 조직 내 T세포의 세포사멸을 촉진하여 염증 발생원(IFN-염증 발생원)을 제거하는 것이 제안된다.[69] 부티레이트(Butyrate)는 Sp1 전사 인자 활동을 불활성화하고 혈관 내피 성장 인자 유전자 발현을 억제하여 혈관신생을 억제한다.[70]
요컨대 발효성 섬유로부터 부티레이트 같은 휘발성 지방산의 생산은 대장암에서 식이섬유의 역할에 기여할 수 있다. 부티르산이 함유된 쇼트체인 지방산은 식이섬유를 함유한 식물성 제품인 프리바이오틱스를 먹거나 발효시키는 유익한 대장균(프로바이오틱스)에 의해 생산된다. 이러한 단사슬 지방산은 에너지 생산을 증가시킴으로써 결장세포에 이익을 주고, 세포 증식을 억제함으로써 결장암으로부터 보호할 수 있다.[21]
반대로, 일부 연구자들은 부티레이트를 제거하고 그것을 잠재적인 암 유발자로 간주하려고 노력해왔다.[71] 생쥐에 대한 연구는 MSH2 결핍 대장 상피 세포의 변형을 촉진한다는 것을 보여준다.[72]
부티레이트 복원의 잠재적 치료법
염증 조절기 및 면역 시스템 기여자로서 부티레이트의 중요성 때문에, 부티레이트 감퇴는 많은 혈관조영 조건의 병원생성에 영향을 미치는 주요 요인이 될 수 있다. 그러므로 내장에서 부티레이트의 건강한 수준을 유지하는 것은 필수적이다. 대변 마이크로바이오타 이식(BPB와 장내 공생력을 회복하기 위한 것)은 부티레이트 수준을 보충함으로써 효과적일 수 있다. 이 치료에서는 건강한 개인이 자신의 대변을 기증하여 난이도가 있는 개인에게 이식한다. 덜 침습적인 치료 방법은 구강 보충제나 관장으로서 부티레이트(butyrate)를 투여하는 것으로, 부작용은 최소에서 무(無)로 염증 증상을 종식시키는데 매우 효과가 있는 것으로 나타났다. 궤양성 대장염 환자를 부티레이트 관장으로 치료한 연구에서 염증이 크게 감소했고, 부티레이트 제공 후 출혈이 완전히 멎었다.[73]
중독
부티르산은 인간의 클래스 I HDAC에 선택적인 억제제다.[34] HDAC는 히스톤 탈산화 및 유전자 발현 억제를 유발할 수 있는 히스톤 수정 효소다. HDAC는 시냅스 형성, 시냅스 가소성 및 장기 메모리 형성의 중요한 규제 기관이다. I급 HDAC는 중독의 발달을 중재하는 데 관여하는 것으로 알려져 있다.[74][75][76] 부티릭산 및 기타 HDAC 억제제는 약물에 중독된 동물에서 HDAC 억제가 전사적, 신경적, 행동적 영향을 평가하기 위해 임상 전 연구에 사용되어 왔다.[76][77][78]
부티레이트 소금과 에스테르
부티레이트 또는 부타노산 이온은 부티릭산의 결합 베이스인 CHCOO이다37−. 그것은 생리학적 pH의 생물학적 시스템에서 발견되는 형태다. 부티릭 또는 부타노 화합물은 카르복실산염 또는 부티릭산의 에스테르이다.
예
소금
에스테르스
참고 항목
메모들
참조
이 글에는 현재 공개 도메인에 있는 출판물의 텍스트가 통합되어 있다. Chisholm, Hugh, ed. (1911). "Butyric Acid". Encyclopædia Britannica (11th ed.). Cambridge University Press.
- ^ Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. p. 746. doi:10.1039/9781849733069-00648. ISBN 978-0-85404-182-4.
- ^ a b c d Strieter FJ, Templeton DH (1962). "Crystal structure of butyric acid" (PDF). Acta Crystallographica. 15 (12): 1240–1244. doi:10.1107/S0365110X6200328X.
- ^ a b c d Lide, David R., ed. (2009). CRC Handbook of Chemistry and Physics (90th ed.). Boca Raton, Florida: CRC Press. ISBN 978-1-4200-9084-0.
- ^ a b c d e Linstrom의 Butanoic acid, Peter J.; Mallard, William G. (eds.); NIST 화학 웹북, NIST 표준 참조 데이터베이스 번호 69, 국립 표준 기술 연구소, Gaithersburg (MD), http://webbook.nist.gov(2020년 10월 27일)
- ^ a b c "Butanoic acid". Chemister.ru. 19 March 2007. Retrieved 27 October 2020.
- ^ a b c d e 시그마알드리히 주식회사, 부티릭산 2020년 10월 27일 회수
- ^ a b c Riemenschneider, Wilhelm (2002). "Carboxylic Acids, Aliphatic". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a05_235.
- ^ 쉐브렐 (1815년) "레트레 드 M. 쉐브렐 아 MM. 레 레닥테우르스 데 안날레스 데 치미" (Chevreul씨가 화학실록 편집자에게 보낸 편지), 안날레스 데 치미 94 : 73–79; 75-76페이지에 걸친 각주에서 그는 버터 냄새를 담당하는 물질을 발견했다고 언급하고 있다.
- ^ 쉐브레울(1817) "엑스트라잇 던 레트레 드 M. Chevreul a MM. les Rédacteurs du Journal de Pharmicie" (Chevreul씨가 Journal of Pharmacy의 편집자에게 보낸 편지 추출), Journal de Pharmicie 등 과학 접근권, 3 : 79–81. 페이지 81에 그는 부티르산이라고 이름 지었다: "세프린시페, 퀘이 아펠레 디푸이스산 부테리케, … (이 원칙 [즉, 구성], 그 이후 내가 "부티르산"이라고 이름지은 바 있다.)
- ^ E. Chevreul, Recherchesches sur les crass gras d'origine animale[동물 유래 지방 물질에 대한 화학 연구] (프랑스 파리: F.G. Levrault, 1823), 115–133페이지.
- ^ Woo, A.H.; Lindsay, R.C. (1983). "Stepwise Discriminant Analysis of Free Fatty Acid Profiles for Identifying Sources of Lipolytic Enzymes in Rancid Butter". Journal of Dairy Science. 66 (10): 2070–2075. doi:10.3168/jds.S0022-0302(83)82052-9.
- ^ ICSC 1334 – Butyric acid. 아마존닷컴(1998년 11월 23일). 2020-10-27년에 검색됨.
- ^ a b McNabney, S. M.; Henagan, T. M. (2017). "Short Chain Fatty Acids in the Colon and Peripheral Tissues: A Focus on Butyrate, Colon Cancer, Obesity and Insulin Resistance". Nutrients. 9 (12): 1348. doi:10.3390/nu9121348. PMC 5748798. PMID 29231905.
- ^ a b Morrison, D. J.; Preston, T. (2016). "Formation of short chain fatty acids by the gut microbiota and their impact on human metabolism". Gut Microbes. 7 (3): 189–200. doi:10.1080/19490976.2015.1134082. PMC 4939913. PMID 26963409.
- ^ "Butyric acid". The Good Scents Company. Retrieved 26 October 2020.
- ^ a b Offermanns S, Colletti SL, Lovenberg TW, Semple G, Wise A, IJzerman AP (June 2011). "International Union of Basic and Clinical Pharmacology. LXXXII: Nomenclature and Classification of Hydroxy-carboxylic Acid Receptors (GPR81, GPR109A, and GPR109B)". Pharmacological Reviews. 63 (2): 269–90. doi:10.1124/pr.110.003301. PMID 21454438.
- ^ a b Offermanns S, Colletti SL, IJzerman AP, Lovenberg TW, Semple G, Wise A, Waters MG. "Hydroxycarboxylic acid receptors". IUPHAR/BPS Guide to Pharmacology. International Union of Basic and Clinical Pharmacology. Retrieved 13 July 2018.
- ^ Carroll, Mark J.; Berenbaum, May R. (2002). "Behavioral responses of the parsnip webworm to host plant volatiles". Journal of Chemical Ecology. 28 (11): 2191–2201. doi:10.1023/A:1021093114663. PMID 12523562. S2CID 23512190.
- ^ Raven, Peter H.; Evert, Ray F.; Eichhorn, Susan E. (2005). Biology of Plants. W. H. Freemanand Company. pp. 429–431. ISBN 978-0-7167-1007-3. Retrieved 11 October 2018.
- ^ Seedorf, H.; Fricke, W. F.; Veith, B.; Bruggemann, H.; Liesegang, H.; Strittmatter, A.; Miethke, M.; Buckel, W.; Hinderberger, J.; Li, F.; Hagemeier, C.; Thauer, R. K.; Gottschalk, G. (2008). "The Genome of Clostridium kluyveri, a Strict Anaerobe with Unique Metabolic Features". Proceedings of the National Academy of Sciences. 105 (6): 2128–2133. Bibcode:2008PNAS..105.2128S. doi:10.1073/pnas.0711093105. PMC 2542871. PMID 18218779.
- ^ a b Lupton JR (February 2004). "Microbial degradation products influence colon cancer risk: the butyrate controversy". The Journal of Nutrition. 134 (2): 479–82. doi:10.1093/jn/134.2.479. PMID 14747692.
- ^ Cummings JH, Macfarlane GT, Englyst HN (February 2001). "Prebiotic digestion and fermentation". The American Journal of Clinical Nutrition. 73 (2 Suppl): 415S–420S. doi:10.1093/ajcn/73.2.415s. PMID 11157351.
- ^ Grummer RR (September 1991). "Effect of feed on the composition of milk fat". Journal of Dairy Science. 74 (9): 3244–57. doi:10.3168/jds.S0022-0302(91)78510-X. PMID 1779073.
- ^ a b Rivière, Audrey; Selak, Marija; Lantin, David; Leroy, Frédéric; De Vuyst, Luc (2016). "Bifidobacteria and Butyrate-Producing Colon Bacteria: Importance and Strategies for Their Stimulation in the Human Gut". Frontiers in Microbiology. 7: 979. doi:10.3389/fmicb.2016.00979. PMC 4923077. PMID 27446020.
- ^ "Frequently asked questions in the area of diet and IBS". Department of Gastroenterology Translational Nutrition Science, Monash University, Victoria, Australia. Retrieved 24 March 2016.
- ^ Gibson, Peter R.; Shepherd, Susan J. (1 February 2010). "Evidence-based dietary management of functional gastrointestinal symptoms: The FODMAP approach". Journal of Gastroenterology and Hepatology. 25 (2): 252–258. doi:10.1111/j.1440-1746.2009.06149.x. ISSN 1440-1746. PMID 20136989. S2CID 20666740.
- ^ Gibson, Peter R.; Varney, Jane; Malakar, Sreepurna; Muir, Jane G. (1 May 2015). "Food components and irritable bowel syndrome". Gastroenterology. 148 (6): 1158–1174.e4. doi:10.1053/j.gastro.2015.02.005. ISSN 1528-0012. PMID 25680668.
- ^ Jenkins, P. R. (1985). "Carboxylic acids and derivatives". General and Synthetic Methods. 7. pp. 96–160. doi:10.1039/9781847556196-00096. ISBN 978-0-85186-884-4.
- ^ Lokensgard, Erik (2015). Industrial Plastics: Theory and Applications (6th ed.). Cengage Learning.
- ^ Williams, R. Scott. "Care of Plastics: Malignant plastics". WAAC Newsletter. 24 (1). Conservation OnLine. Retrieved 29 May 2017.
- ^ Freezer Baits 2010년 1월 25일 웨이백 머신에 보관, 너트래빗.그물을 치다
- ^ Kasumyan A, Døving K (2003). "Taste preferences in fishes". Fish and Fisheries. 4 (4): 289–347. doi:10.1046/j.1467-2979.2003.00121.x.
- ^ 2010년 2월 10일 웨이백머신, newser.com에 2010년 6월 8일 보관된 산발화 운동가들에 의해 부상당한 일본 포경선들
- ^ a b c d "Butyric acid". IUPHAR/BPS Guide to Pharmacology. International Union of Basic and Clinical Pharmacology. Retrieved 13 July 2018.
- ^ a b "Butanoic acid and Sodium butyrate". BindingDB. The Binding Database. Retrieved 27 October 2020.
- ^ a b c Kasubuchi M, Hasegawa S, Hiramatsu T, Ichimura A, Kimura I (2015). "Dietary gut microbial metabolites, short-chain fatty acids, and host metabolic regulation". Nutrients. 7 (4): 2839–49. doi:10.3390/nu7042839. PMC 4425176. PMID 25875123.
Short-chain fatty acids (SCFAs) such as acetate, butyrate, and propionate, which are produced by gut microbial fermentation of dietary fiber, are recognized as essential host energy sources and act as signal transduction molecules via G-protein coupled receptors (FFAR2, FFAR3, OLFR78, GPR109A) and as epigenetic regulators of gene expression by the inhibition of histone deacetylase (HDAC). Recent evidence suggests that dietary fiber and the gut microbial-derived SCFAs exert multiple beneficial effects on the host energy metabolism not only by improving the intestinal environment, but also by directly affecting various host peripheral tissues.
- ^ a b c d e Hoeppli RE, Wu D, Cook L, Levings MK (February 2015). "The environment of regulatory T cell biology: cytokines, metabolites, and the microbiome". Front Immunol. 6: 61. doi:10.3389/fimmu.2015.00061. PMC 4332351. PMID 25741338.
그림 1: 미생물에서 유래한 분자는 결장 Treg 분화를 촉진한다. - ^ a b c d e f g Bourassa MW, Alim I, Bultman SJ, Ratan RR (June 2016). "Butyrate, neuroepigenetics and the gut microbiome: Can a high fiber diet improve brain health?". Neurosci. Lett. 625: 56–63. doi:10.1016/j.neulet.2016.02.009. PMC 4903954. PMID 26868600.
- ^ Tsuji A (2005). "Small molecular drug transfer across the blood-brain barrier via carrier-mediated transport systems". NeuroRx. 2 (1): 54–62. doi:10.1602/neurorx.2.1.54. PMC 539320. PMID 15717057.
Other in vivo studies in our laboratories indicated that several compounds including acetate, propionate, butyrate, benzoic acid, salicylic acid, nicotinic acid, and some β-lactam antibiotics may be transported by the MCT at the BBB.21 ... Uptake of valproic acid was reduced in the presence of medium-chain fatty acids such as hexanoate, octanoate, and decanoate, but not propionate or butyrate, indicating that valproic acid is taken up into the brain via a transport system for medium-chain fatty acids, not short-chain fatty acids.
- ^ a b Vijay N, Morris ME (2014). "Role of monocarboxylate transporters in drug delivery to the brain". Curr. Pharm. Des. 20 (10): 1487–98. doi:10.2174/13816128113199990462. PMC 4084603. PMID 23789956.
Monocarboxylate transporters (MCTs) are known to mediate the transport of short chain monocarboxylates such as lactate, pyruvate and butyrate. ... MCT1 and MCT4 have also been associated with the transport of short chain fatty acids such as acetate and formate which are then metabolized in the astrocytes [78]. ... SLC5A8 is expressed in normal colon tissue, and it functions as a tumor suppressor in human colon with silencing of this gene occurring in colon carcinoma. This transporter is involved in the concentrative uptake of butyrate and pyruvate produced as a product of fermentation by colonic bacteria.
- ^ a b "Butyric acid". Human Metabolome Database. University of Alberta. Retrieved 15 August 2015.
- ^ "Butanoate metabolism – Reference pathway". Kyoto Encyclopedia of Genes and Genomes. Kanehisa Laboratories. 1 November 2017. Retrieved 1 February 2018.
- ^ Donohoe, Dallas R.; Garge, Nikhil; Zhang, Xinxin; Sun, Wei; O’Connell, Thomas M.; Bunger, Maureen K.; Bultman, Scott J. (4 May 2011). "The Microbiome and Butyrate Regulate Energy Metabolism and Autophagy in the Mammalian Colon". Cell Metabolism. 13 (5): 517–526. doi:10.1016/j.cmet.2011.02.018. ISSN 1550-4131. PMC 3099420. PMID 21531334.
- ^ "triacylglycerol lipase – Homo sapiens". BRENDA. Technische Universität Braunschweig. Retrieved 25 May 2015.
- ^ Tilg H, Moschen AR (September 2014). "Microbiota and diabetes: an evolving relationship". Gut. 63 (9): 1513–1521. doi:10.1136/gutjnl-2014-306928. PMID 24833634. S2CID 22633025.
- ^ Cait, Alissa; Cardenas, Erick (December 2019). "Reduced genetic potential for butyrate fermentation in the gut microbiome of infants who develop allergic sensitization". Journal of Allergy and Clinical Immunology. 144 (6): 1638–1647. E3. doi:10.1016/j.jaci.2019.06.029. PMID 31279007.
- ^ Vatanen, T.; Franzosa, E.A.; Schwager, R.; et al. (2018). "The human gut microbiome in early-onset type 1 diabetes from the TEDDY study". Nature. 562 (7728): 589–594. Bibcode:2018Natur.562..589V. doi:10.1038/s41586-018-0620-2. PMC 6296767. PMID 30356183.
- ^ Kumar J, Rani K, Datt C (2020). "Molecular link between dietary fibre, gut microbiota and health". Molecular Biology Reports. 47 (8): 6229–6237. doi:10.1007/s11033-020-05611-3. PMID 32623619. S2CID 220337072.
- ^ Consolandi, Clarissa; Turroni, Silvia; Emmi, Giacomo; et al. (April 2015). "Behçet's syndrome patients exhibit specific microbiome signature". Autoimmunity Reviews. 14 (4): 269–276. doi:10.1016/j.autrev.2014.11.009. PMID 25435420.
- ^ Ye, Zi; Zhang, Ni; Wu, Chunyan; et al. (4 August 2018). "A metagenomic study of the gut microbiome in Behcet's disease". Microbiome. 6 (1): 135. doi:10.1186/s40168-018-0520-6. PMC 6091101. PMID 30077182.
- ^ Cait, Alissa; Hughes, Michael R (May 2018). "Microbiome-driven allergic lung inflammation is ameliorated by short chain fatty acids". Mucosal Immunology. 11 (3): 785–796. doi:10.1038/mi.2017.75. PMID 29067994.
- ^ Furusawa, Yukihiro; Obata, Yuuki; Fukuda, Shinji; et al. (13 November 2013). "Commensal microbe-derived butyrate induces the differentiation of colonic regulatory T cells". Nature. 504 (7480): 446–450. Bibcode:2013Natur.504..446F. doi:10.1038/nature12721. PMID 24226770. S2CID 4408815.
- ^ Arpaia, Nicholas; Campbell, Clarissa; Fan, Xiying; et al. (13 November 2013). "Metabolites produced by commensal bacteria promote peripheral regulatory T-cell generation". Nature. 504 (7480): 451–455. Bibcode:2013Natur.504..451A. doi:10.1038/nature12726. PMC 3869884. PMID 24226773.
- ^ Luu, Maik; Weigand, Katharina; Wedi, Fatana; et al. (26 September 2018). "Regulation of the effector function of CD8+ T cells by gut microbiota-derived metabolite butyrate". Scientific Reports. 8 (1): 14430. Bibcode:2018NatSR...814430L. doi:10.1038/s41598-018-32860-x. PMC 6158259. PMID 30258117.
- ^ Cholan, Pradeep Manuneedhi; Han, Alvin; Woodie, Brad R.; Watchon, Maxinne; Kurz, Angela RM; Laird, Angela S.; Britton, Warwick J.; Ye, Lihua; Holmes, Zachary C.; McCann, Jessica R.; David, Lawrence A. (9 November 2020). "Conserved anti-inflammatory effects and sensing of butyrate in zebrafish". Gut Microbes. 12 (1): 1–11. doi:10.1080/19490976.2020.1824563. ISSN 1949-0976. PMC 7575005. PMID 33064972.
- ^ a b c d Wang G (2014). "Human antimicrobial peptides and proteins". Pharmaceuticals (Basel). 7 (5): 545–94. doi:10.3390/ph7050545. PMC 4035769. PMID 24828484.
표 3: 인간 항균 펩타이드 및 제안 대상 선택
표 4: 항균 펩타이드 발현을 유도하는 알려진 요인 - ^ Yonezawa H, Osaki T, Hanawa T, Kurata S, Zaman C, Woo TD, Takahashi M, Matsubara S, Kawakami H, Ochiai K, Kamiya S (2012). "Destructive effects of butyrate on the cell envelope of Helicobacter pylori". J. Med. Microbiol. 61 (Pt 4): 582–9. doi:10.1099/jmm.0.039040-0. PMID 22194341.
- ^ McGee DJ, George AE, Trainor EA, Horton KE, Hildebrandt E, Testerman TL (2011). "Cholesterol enhances Helicobacter pylori resistance to antibiotics and LL-37". Antimicrob. Agents Chemother. 55 (6): 2897–904. doi:10.1128/AAC.00016-11. PMC 3101455. PMID 21464244.
- ^ Zimmerman MA, Singh N, Martin PM, Thangaraju M, Ganapathy V, Waller JL, Shi H, Robertson KD, Munn DH, Liu K (2012). "Butyrate suppresses colonic inflammation through HDAC1-dependent Fas upregulation and Fas-mediated apoptosis of T cells". Am. J. Physiol. Gastrointest. Liver Physiol. 302 (12): G1405–15. doi:10.1152/ajpgi.00543.2011. PMC 3378095. PMID 22517765.
- ^ Offermanns S, Schwaninger M (2015). "Nutritional or pharmacological activation of HCA(2) ameliorates neuroinflammation". Trends Mol Med. 21 (4): 245–255. doi:10.1016/j.molmed.2015.02.002. PMID 25766751.
- ^ Chai JT, Digby JE, Choudhury RP (May 2013). "GPR109A and vascular inflammation". Curr Atheroscler Rep. 15 (5): 325. doi:10.1007/s11883-013-0325-9. PMC 3631117. PMID 23526298.
- ^ Graff EC, Fang H, Wanders D, Judd RL (February 2016). "Anti-inflammatory effects of the hydroxycarboxylic acid receptor 2". Metab. Clin. Exp. 65 (2): 102–113. doi:10.1016/j.metabol.2015.10.001. PMID 26773933.
- ^ Farzi A, Reichmann F, Holzer P (2015). "The homeostatic role of neuropeptide Y in immune function and its impact on mood and behaviour". Acta Physiol (Oxf). 213 (3): 603–27. doi:10.1111/apha.12445. PMC 4353849. PMID 25545642.
- ^ Zeng, Huawei; Lazarova, DL; Bordonaro, M (2014). "Mechanisms linking dietary fiber, gut microbiota and colon cancer prevention". World Journal of Gastrointestinal Oncology. 6 (2): 41–51. doi:10.4251/wjgo.v6.i2.41. PMC 3926973. PMID 24567795.
- ^ Chen, Jiezhong; Zhao, Kong-Nan; Vitetta, Luis (2019). "Effects of Intestinal Microbial–Elaborated Butyrate on Oncogenic Signaling Pathways" (pdf). Nutrients. 11 (5): 1026. doi:10.3390/nu11051026. PMC 6566851. PMID 31067776. S2CID 148568580.
- ^ Klampfer L, Huang J, Sasazuki T, Shirasawa S, Augenlicht L (August 2004). "Oncogenic Ras promotes butyrate-induced apoptosis through inhibition of gelsolin expression". The Journal of Biological Chemistry. 279 (35): 36680–8. doi:10.1074/jbc.M405197200. PMID 15213223.
- ^ Vanhoutvin SA, Troost FJ, Hamer HM, Lindsey PJ, Koek GH, Jonkers DM, Kodde A, Venema K, Brummer RJ (2009). Bereswill S (ed.). "Butyrate-induced transcriptional changes in human colonic mucosa". PLOS ONE. 4 (8): e6759. Bibcode:2009PLoSO...4.6759V. doi:10.1371/journal.pone.0006759. PMC 2727000. PMID 19707587.
- ^ Encarnação, J. C.; Abrantes, A. M.; Pires, A. S.; et al. (30 July 2015). "Revisit dietary fiber on colorectal cancer: butyrate and its role on prevention and treatment". Cancer and Metastasis Reviews. 34 (3): 465–478. doi:10.1007/s10555-015-9578-9. PMID 26224132. S2CID 18573671.
- ^ Zimmerman, Mary A.; Singh, Nagendra; Martin, Pamela M.; et al. (15 June 2012). "Butyrate suppresses colonic inflammation through HDAC1-dependent Fas upregulation and Fas-mediated apoptosis of T cells". American Journal of Physiology. Gastrointestinal and Liver Physiology. 302 (12): G1405–G1415. doi:10.1152/ajpgi.00543.2011. PMC 3378095. PMID 22517765.
- ^ Prasanna Kumar, S.; Thippeswamy, G.; Sheela, M.L.; et al. (October 2008). "Butyrate-induced phosphatase regulates VEGF and angiogenesis via Sp1". Archives of Biochemistry and Biophysics. 478 (1): 85–95. doi:10.1016/j.abb.2008.07.004. PMID 18655767.
- ^ "Low-carb diet cuts risk of colon cancer, study finds University of Toronto Media Room". media.utoronto.ca. Retrieved 4 May 2016.
- ^ Belcheva, Antoaneta; Irrazabal, Thergiory; Robertson, Susan J.; Streutker, Catherine; Maughan, Heather; Rubino, Stephen; Moriyama, Eduardo H.; Copeland, Julia K.; Kumar, Sachin (17 July 2014). "Gut microbial metabolism drives transformation of MSH2-deficient colon epithelial cells". Cell. 158 (2): 288–299. doi:10.1016/j.cell.2014.04.051. ISSN 1097-4172. PMID 25036629.
- ^ Scheppach, W.; Sommer, H.; Kirchner, T.; et al. (1992). "Effect of butyrate enemas on the colonic mucosa in distal ulcerative colitis". Gastroenterology. 103 (1): 51–56. doi:10.1016/0016-5085(92)91094-K. PMID 1612357.
- ^ Robison AJ, Nestler EJ (November 2011). "Transcriptional and epigenetic mechanisms of addiction". Nat. Rev. Neurosci. 12 (11): 623–637. doi:10.1038/nrn3111. PMC 3272277. PMID 21989194.
- ^ Nestler EJ (January 2014). "Epigenetic mechanisms of drug addiction". Neuropharmacology. 76 Pt B: 259–268. doi:10.1016/j.neuropharm.2013.04.004. PMC 3766384. PMID 23643695.
- ^ a b Walker DM, Cates HM, Heller EA, Nestler EJ (February 2015). "Regulation of chromatin states by drugs of abuse". Curr. Opin. Neurobiol. 30: 112–121. doi:10.1016/j.conb.2014.11.002. PMC 4293340. PMID 25486626.
- ^ Ajonijebu DC, Abboussi O, Russell VA, Mabandla MV, Daniels WM (August 2017). "Epigenetics: a link between addiction and social environment". Cellular and Molecular Life Sciences. 74 (15): 2735–2747. doi:10.1007/s00018-017-2493-1. PMID 28255755. S2CID 40791780.
- ^ Legastelois R, Jeanblanc J, Vilpoux C, Bourguet E, Naassila M (2017). "[Epigenetic mechanisms and alcohol use disorders: a potential therapeutic target]". Biologie Aujourd'hui (in French). 211 (1): 83–91. doi:10.1051/jbio/2017014. PMID 28682229.
외부 링크
| 위키미디어 커먼즈에는 부티릭산과 관련된 미디어가 있다. |