프라바돌린
Pravadoline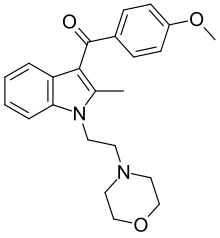 | |
| 임상자료 | |
|---|---|
| ATC 코드 |
|
| 법적현황 | |
| 법적현황 |
|
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 켐스파이더 | |
| 유니 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| 화학 및 물리적 데이터 | |
| 공식 | C23H26N2O3 |
| 어금질량 | 378.472 g·1998−1 |
| 3D 모델(JSmol) | |
| |
| |
| | |
프라바돌린(WIN 48,098)은 인데메타신(Indometacin)과 같은 비스테로이드성 항염증제(NSAIDs)와 구조상 관련이 있는 IC50 4.9μM, CB에서i1 K 2511nM의 항염증제다. 1980년대에 새로운 항염증 및 프로스타글란딘 합성 억제제로 개발되어 효소 사이클록시제네아제(COX)의 억제를 통해 작용하였다.
그러나 프라바돌린은 예상외로 강한 항염증 효과를 보이는 것으로 밝혀졌는데, 이는 유효 항염증 용량보다 10배 작은 용량에서 나타났기 때문에 COX 억제제로서의 작용으로는 설명할 수 없었다. 이러한 효과는 날록손과 같은 오피오이드 길항제들에 의해 차단되지 않았고,[1] 결국 프라바돌린이 카나비노이드 작용제들의 새로운 계급인 아미노칼린돌에서 나온 최초의 화합물을 나타낸다는 것이 밝혀졌다.[2]
Pravadoline 진통제로 사용하기 위해, 부분적으로 독성 우려로 인해 개발되지는 못하였다 카나비노이드 활동의 약 sev이 발견되었다 이 구조적으로 새로운 가족에서 발견(비록 이러한 후 염수 형태의 결과가 이 약의 pravadoline 자체보다 준비했다고 보여 주었다.)[3].시대현재 과학 연구에 널리 사용되고 있는 WIN 55,212-2를 포함한 새로운 카나비노이드 작용제들.[4][5]
동물학
쥐에게 프라바돌린을 투여한 결과는 다음과 같다.[1]
- 55°C 온도에서 뜨거운 물에 꼬리가 잠기면서 유발된 응답 지연 시간 연장(최소 유효 용량 100mg/kg s.c)
- (Randall-Selitto 테스트) 중 (Randall-Selitto 테스트) 동안 양조장 효모 주입으로 랫드에서 고농축 방지(최소 유효 용량 1mg/kg, 페이지)
- 보조 랫드(ED 41 mg/kg50, p.o.)에서 발굽 굴곡에 의해 유도된 nociceptive 반응 방지
- 브래디키닌 유도 머리 및 앞포 굴곡의 nociceptive 반응 방지(ED50 78mg/kg, p.o.)
프라바돌린 유도 항응결 활성은 오피오이드 메커니즘으로 설명할 수 없는데, 이는 프라바돌린 유도 항응결제가 날록손(1mg/kg, s.c)에 의해 반감되지 않았고 프라바돌린은 최대 10μM 농도에서 오피오이드 수용체와 결합되지 않았기 때문이다.[1]
참고 항목
- AM-630 (6-iodopravadoline)
- WIN 54,461(6-브로모프라바돌린)
- WIN 55,212-2
- RCS-4(1-펜틸-3-(4-메톡시벤조일)indole)
참조
- ^ a b c Haubrich DR, et al. (1990). "Pharmacology of pravadoline: a new analgesic agent". J. Pharmacol. Exp. Ther. 255 (2): 511–22. PMID 2243340.
- ^ Bell MR, et al. (1991). "Antinociceptive (aminoalkyl)indoles". J. Med. Chem. 34 (3): 1099–110. doi:10.1021/jm00107a034. PMID 1900533.
- ^ Everett RM, et al. (1993). "Nephrotoxicity of pravadoline maleate (WIN 48098-6) in dogs: evidence of maleic acid-induced acute tubular necrosis". Fundam Appl Toxicol. 21 (1): 59–65. doi:10.1006/faat.1993.1072. PMID 8365586.
- ^ D'Ambra TE, et al. (1992). "Conformationally restrained analogues of pravadoline: nanomolar potent, enantioselective, (aminoalkyl)indole agonists of the cannabinoid receptor". J. Med. Chem. 35 (1): 124–35. doi:10.1021/jm00079a016. PMID 1732519.
- ^ Compton DR, et al. (1992). "Aminoalkylindole analogs: cannabimimetic activity of a class of compounds structurally distinct from delta 9-tetrahydrocannabinol". J. Pharmacol. Exp. Ther. 263 (3): 1118–26. PMID 1335057.


