D형간염
Hepatitis D| D형간염 | |
|---|---|
| 기타이름 | 델타형간염 |
| 전문 | 소화기내과, 전염병 |
| 증상 | 피로감, 메스꺼움, 구토감[1] |
| 합병증 | 간경변증[1] |
| 원인들 | D형[1] 간염 바이러스 |
| 진단방법 | 면역글로불린[2] G |
| 치료 | 항바이러스제, 페길화 인터페론[2] 알파 |
| 약 | 불버타이드 |
D형 간염은 델타형 간염 바이러스(HDV)[4][5]에 의해 발생하는 바이러스성[3] 간염의 한 종류입니다.HDV는 A, B, C, D, E의 다섯 가지 간염 바이러스 중 하나입니다.HDV는 B형 간염 바이러스(HBV)[6]가 있는 경우에만 전파할 수 있기 때문에 위성(아바이러스제의 일종)으로 간주됩니다.HDV의 전파는 HBV와의 동시 감염(coinfection) 또는 만성 B형 간염 또는 B형 간염 매개체 상태(superfection)에 중첩되어 발생할 수 있습니다.
HDV는 합병증의 심각성 때문에 만성 B형 간염(초감염)[7]을 가진 사람을 감염시키는 가장 심각한 유형의 바이러스 간염으로 여겨집니다.이러한 합병증은 급성 감염에서 간부전을 경험할 가능성이 더 높고 간경변증으로 빠르게 진행되며 만성 [8]감염에서 간암이 발생할 위험이 증가합니다.B형 간염 바이러스와 함께 D형 간염은 전체 간염 감염자 중 사망률이 20%로 가장 높습니다.2020년의 최근 추정치에 따르면 현재 4천8백만 명의 사람들이 [9]이 바이러스에 감염되어 있다고 합니다.
| D형간염 | |
|---|---|
| 동의어 | 델타 간염 |
| 바이러스 종류 | ssRNA |
| 잠복기 | 2-12주 |
| 변속기 | 비경구 |
| 통신사 상태 | 네. |
| 면책특권 수동면역 능동면역 | 고면역 글로불린 백신(B형간염) |
바이러스학
| 델타형 간염 바이러스 | |
|---|---|
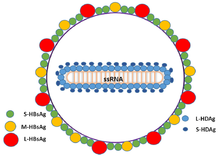 | |
| 델타형 간염 바이러스 바이러스 바이러스의 개략적인 표현 | |
| 바이러스 분류 | |
| (순위 없음): | 바이러스 |
| 영역: | 리보자이비아 |
| 가족: | 콜미오비루스과 |
| 속: | 델타바이러스 |
| 종[10] | |
| |
구조와 게놈
간염 델타 바이러스 또는 HDV는 리보자이비아([11]Ribozyviria) 영역에서 델타바이러스 속(Delta virus)으로 함께 분류되는 음성 의미의 단일 가닥 RNA 바이러스(또는 바이러스 유사 입자)의 8종입니다.HDV 비리온은 지름이 36nm인 구형의 작은 입자로, 바이러스 외피에는 숙주 인지질과 B형 간염 바이러스에서 추출한 3가지 단백질인 대, 중, 소의 B형 간염 표면 항원이 포함되어 있습니다.이 어셈블리는 각 게놈에 대해 약 200 분자의 간염 D 항원(HDAg)으로 둘러싸인 게놈을 포함하는 내부 리보뉴클레오단백질(RNP) 입자를 둘러싸고 있습니다.HDAg의 중심 영역은 RNA를 [12]결합하는 것으로 나타났으며, 여러 상호작용은 또한 HDAg의 [13][14]N 말단에서 코일-코일 영역에 의해 매개됩니다.
HDV 유전체는 음성적인 의미의 단일 가닥의 닫힌 원형 RNA이며, 약 1700 뉴클레오티드의 유전체를 가지고 있으며, HDV는 동물을 감염시키는 것으로 알려진 가장 작은 바이러스입니다.HDV는 [15][16]바이러스보다 훨씬 작은 바이로이드라고 불리는 식물 병원균의 한 종류에서 유래했을 수도 있다고 제안되었습니다.그것의 게놈은 높은 GC 뉴클레오타이드 함량 때문에 동물 바이러스 중에서도 독특합니다.뉴클레오타이드 서열은 약 70%의 자기 보완성을 가지며, 게놈은 부분적으로 이중 가닥의 막대와 같은 [17]RNA 구조를 형성할 수 있습니다.HDV 균주는 매우 발산적입니다. 다양한 균주의 융합이 존재하고 관련된 원형 바이러스 RNA에 대해 서로 다른 시작 부위를 사용하여 공공 데이터베이스에 염기서열이 축적되었습니다.이것은 이 바이러스의 분자 분류와 관련하여 혼란을 야기시켰는데, 이 상황은 최근 제안된 참조 게놈과 균일한 분류 [18]시스템의 채택으로 해결되었습니다.
생애주기
B형 간염처럼, HDV는 타우로콜레이트 소듐 운반 폴리펩타이드(NTCP)[19] 담즙 수송체를 통해 간세포로 진입합니다.HDV는 큰 B형 간염 표면 항원인 HBsAg의 [20]N 말단 도메인을 통해 수용체를 인식합니다.이 도메인의 돌연변이 발생에 의한 매핑은 아미노산 잔기 9-15가 수용체 결합 [21]부위를 구성한다는 것을 보여주었습니다.간세포에 들어간 후 바이러스는 코팅되지 않고 HDAg의[22] 신호에 의해 뉴클레오캡시드가 핵으로 이동합니다. HDV 유전체는 바이러스의 유전체를 복제하기 위해 RNA 중합효소를 코드화하지 않기 때문에, 바이러스는 숙주 세포 RNA 중합효소를 사용합니다.처음에는 RNA 중합효소 [23][24]II만 사용하는 것으로 생각되었으나, 현재는 RNA 중합효소 I과 III도 HDV [25]복제에 관여하는 것으로 나타났습니다.일반적으로 RNA 중합효소 II는 DNA를 주형으로 사용하고 mRNA를 생성합니다. 따라서 복제 중에 HDV가 실제로 RNA 중합효소 II를 사용한다면 DNA 의존 중합효소를 RNA 의존 [citation needed]중합효소로 사용할 수 있는 유일한 동물 병원체가 될 것입니다.
RNA 중합효소는 RNA 게놈이 접힌 막대와 같은 구조로 인해 이중 가닥 DNA로 취급합니다.원형 게놈 RNA, 원형 상보형 항원 RNA, 선형 폴리아데닐화 항원 RNA, HDAg에 대한 개방된 판독 프레임을 포함하는 mRNA.항원 RNA의 합성은 RNA 중합효소 I에 의해 매개되는 뉴클레오퍼스에서 일어나는 반면, 게놈 RNA의 합성은 뉴클레오퍼스에서 이루어지며, 뉴클레오퍼스 [26]II에 의해 매개됩니다.HDV RNA는 먼저 게놈의 많은 복사본을 포함하는 선형 RNA로 합성됩니다.게놈과 항원 RNA는 선형 RNA를 단량체로 스스로 절단하는 리보자임의 역할을 하는 85 뉴클레오티드, 간염 델타 바이러스 리보자임의 배열을 포함합니다.그리고 나서 이 단량체들은 원형 [27][28]RNA를 형성하기 위해 연결됩니다.
델타항원
| 델타형 간염바이러스 델타항원 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 델타형 간염 항원의 올리고머화 도메인 | |||||||||
| 식별자 | |||||||||
| 기호. | HDV_ag | ||||||||
| 피팜 | PF01517 | ||||||||
| 인터프로 | IPR002506 | ||||||||
| SCOP2 | 1a92 / 스코페 / SUPFAM | ||||||||
| |||||||||
바이로이드와 HDV의 중요한 차이점은 바이로이드가 단백질을 생산하지 않는 반면, HDV는 단백질, 즉 HDAg를 생산하는 것으로 알려져 있다는 것입니다.27kDa large-HDAg와 24kDa large-HDAg라는 두 가지 형태로 제공됩니다.두 형태의 N 말단은 동일하며, 큰 HDAg의 [29]C 말단에서 아미노산이 19개 더 다릅니다.두 동형 모두 코돈 196에서 UAG 정지 코돈이 포함된 동일한 판독 프레임에서 생성되며, 이 코돈은 일반적으로 작은 HDAg만 생성됩니다.그러나 세포 효소인 아데노신 탈아미나제-1에 의한 편집은 정지 코돈을 UGG로 변경하여 큰-HDAG를 [29][30]생성할 수 있게 합니다.90%의 동일한 서열을 가지고 있음에도 불구하고, 이 두 단백질은 감염 과정 중에 서로 다른 역할을 합니다.HDAg-S는 감염 초기에 생성되어 핵으로 들어가 바이러스 복제를 지원합니다.반면, HDAg-L은 감염 후기에 생성되고 바이러스 복제의 억제제 역할을 하며 바이러스 [31][32][33]입자의 조립에 필요합니다.따라서 세포 효소에 의한 RNA 편집은 바이러스 복제와 비리온 [citation needed]조립 사이의 균형을 조절하기 때문에 바이러스의 수명 주기에 매우 중요합니다.
항원고리감염성
HDV 외피 단백질에는 3개의 HBV 표면 단백질이 고정되어 있습니다.게놈의 S 영역은 가장 일반적으로 표현되며 주요 기능은 바이러스 하위 입자를 조립하는 것입니다.HDV 항원 단백질은 바이러스 게놈과 결합하여 리보뉴클레오단백질(RNP)을 형성합니다. 리보뉴클레오단백질은 서브바이러스 입자로 둘러싸였을 때 성숙한 HDV와 거의 동일한 바이러스 유사 입자를 형성할 수 있지만 전염성은 없습니다.연구자들은 HDV의 감염성의 결정 요인이 큰 단백질(L)의 N 말단 사전 S1 영역 내에 있다고 결론지었습니다.그것은 세포 수용체에 결합하는 매개체로 밝혀졌습니다.연구원 조르주 아부 자우데와 카미유 슈뢰는 2005년에 HDV 외피 단백질에서 발견되는 항원 고리의 바이러스의 감염성에 대한 역할을 연구한 논문을 발표했습니다.항원 루프는 큰 단백질의 N 말단 pre-S1 도메인과 마찬가지로 비리온 표면에 노출됩니다.Jaudé와 Sureau의 연구는 항원 루프가 숙주 세포로의 HDV 진입에 중요한 요인이 될 수 있다는 증거를 제공했고, 항원 루프의 일부를 변형시킴으로써 HDV의 감염성을 [34]최소화할 수 있습니다.
변속기
D형 간염의 전파 경로는 B형 간염의 전파 경로와 유사합니다.B형 간염 감염 위험이 높은 사람, 특히 약물 사용자와 응고 인자 농축액을 투여하는 사람에게 감염이 크게 제한됩니다.전 세계적으로 1500만 명 이상의 사람들이 공동으로 감염되었습니다.HDV는 대부분의 선진국에서 드물며 대부분 정맥내 약물 사용과 관련이 있습니다.하지만, HDV는 가까운 지중해 지역, 사하라 사막 이남의 아프리카, 중동, 그리고 남아메리카의 [35]북부 지역에서 훨씬 더 흔합니다.모두 합쳐 약 2천만 명의 사람들이 HDV에 [36]감염되었을 수 있습니다.
위험에 처한 사람들
앞서 밝힌 바와 같이 B형 간염으로 진단받은 환자는 D형 간염에 감염될 위험이 있습니다.D형 간염은 주사약을 사용하는 경우, 혈우병인 경우, 혈액투석 환자인 경우, 다른 감염자와의 성적 접촉을 통해 감염 위험이 증가합니다.
예방
D형 간염은 사람에게 [37][38]감염되고 복제되기 위해서는 B형 간염 바이러스 감염이 있어야 하므로 B형 간염 예방접종은 D형 간염 바이러스 감염을 예방합니다.세계보건기구는 B형 간염 바이러스에 대한 보편적인 예방접종을 권고하고 있습니다.B형 간염 백신은 보통 생후 24시간 이내에 B형 간염과 D형 바이러스 [39]감염을 예방하기 위해 투여됩니다.
라텍스나 폴리우레탄 콘돔은 B형 간염, 그리고 아마도 D형 간염 바이러스 [40]감염의 전염을 막는 것으로 나타났습니다.
임신 중이거나 임신을 시도하는 여성은 HBV 검사를 통해 자신이 바이러스를 옮기는지 확인해야 하며, 이를 통해 아이가 태어나는 동안 예방책을 시행할 수 있습니다.CDC는 임신한 모든 여성에게 B형 간염 바이러스 감염 여부를 검사하고, HBV 감염 여성의 모든 유아에게 생후 12시간 이내에 B형 간염 면역글로불린(HBIG)과 B형 간염 백신을 접종해 산모에서 [41]아이로 바이러스가 전염되는 것을 예방할 것을 권고하고 있습니다.
문신이나 신체 피어싱을 한 사람은 감염된 체액을 통해 B형, D형 간염이 전염되는 것을 막기 위해 멸균 장비를 사용해야 합니다.B형과 D형 간염은 오염된 바늘로도 전염될 수 있으므로 약물을 주입하는 사람은 약물 사용을 중단하거나 멸균 바늘을 사용하는 것을 막고 다른 [40]사람과 바늘을 공유하는 것을 피해야 합니다.B형이나 D형 간염에 걸린 사람들은 또한 잠재적으로 전염성이 있는 [40]체액에 의해 오염되었을 수 있는 면도기나 기타 개인 관리 물품을 공유해서는 안 됩니다.
진단.
D형 간염을 검사하려면 항HDV 항체 검사가 필요한데, 이는 바이러스에 대한 과거 노출이나 현재 감염을 나타냅니다.항HDV 항체가 존재하는 경우 간염 DRNA 수치를 [42]측정하여 활성 HDV 감염 여부를 확인합니다.HDV 검사는 사람들을 [42]감염시키기 위해 B형 간염 바이러스 감염이 필요하기 때문에 B형 간염 표면 항원 양성자(B형 간염에 이전 또는 활동적으로 감염된 경험이 있는 사람)에게만 표시됩니다.바이오마커 기반 FibroTest와 같은 간 섬유화의 비침습적 측정 또는 과도 엘라스토그래피(FibroScan이라고도 함)와 같은 비침습적 간 영상은 만성 D형 간염 감염자의 간 섬유화의 정량적 측정으로 검증되지 않았습니다.간섬유화나 간경변증이 의심되는 사람은 대개 간생검이 [42]필요합니다.
치료
만성 D형 간염에 대한 현재 확립된 치료법은 기존의 또는 페길화된 인터페론 알파 [43]요법을 포함합니다.페길화된 인터페론 알파는 약이 투여되는 시간 동안 바이러스 부하와 질병의 영향을 줄이는 데 효과적이지만, [44]약이 중단되면 일반적으로 효과가 중단됩니다.이 치료의 효율은 보통 약 20%를 넘지 않으며, 치료 후 재발이 늦은 것이 [45][46]보고되었습니다.
2020년 5월, 유럽의약품청 인체사용의약품위원회는 [47]D형 간염을 치료하기 위한 항바이러스제 Hepcludex(bulebirtide)를 승인했습니다.B형 간염 바이러스 뿐만 아니라 D형 간염 바이러스가 [48][49]간세포로 들어가는 것을 차단하면서 불레버타이드는 나트륨/바일산 코트랜스포터를 결합시키고 비활성화시킵니다.불버타이드는 페길화된 인터페론 알파와 함께 투여될 수 있는데, 이 둘은 상승작용을 하여 치료 반응률을 [42]높일 수 있다고 생각되기 때문입니다.
HDV 관련 보상성 간경변증과 임상적으로 유의한 문맥압 항진증이 있는 환자의 경우 (bulbirtide)를 사용한 치료는 안전하고 잘 견뎌졌으며 생화학적 변수의 상당한 개선과 간 기능 [50]매개 변수의 증가로 이어졌습니다.
현재 개발 중인 다른 D형 간염 치료제로는 JAK-STAT 신호전달 경로를 통해 세포 내 신호전달 캐스케이드로 이어지는 페길화된 인터페론 람다(pegylated interferon lambda)가 있습니다.[51]프레닐화 억제제인 로나파닙은 L-HDAg의 [52]파르네실화를 억제함으로써 D형 간염 바이러스 입자의 조립을 억제하고, REP2139-Ca는 B형 간염 표면 항원(D형 간염 바이러스 [53]입자의 조립에 필요함)의 방출을 방지하는 핵산 중합체.
예후
만성 B형 간염을 가진 사람에게 D형 간염 바이러스 감염이 일어나는 슈퍼 감염은 만성 D형 간염으로 진행될 가능성이 더 높으며([42]사람이 B형 간염과 D형 간염에 동시에 감염되는 공동 감염과는 반대로) 더 나쁜 예후와 관련이 있습니다.만성 D형 간염 감염 사례의 90%는 이미 [42]B형 간염에 걸린 사람들의 초감염에 의한 것으로 생각됩니다.B형 간염과 D형 간염의 동반 감염은 급성 간염으로 이어질 가능성이 높지만, 보통 D형 [42]간염에 관해서는 자가 제한적입니다.만성 B형 및 D형 간염은 만성 B형 간염 단독보다 [42]더 나쁜 예후와 관련이 있습니다.두 바이러스 모두에 감염되면 만성 D형 간염 환자의 75%가 15년 이내에 간경변증이 발생하고 간암에 [42]걸릴 위험이 훨씬 높을 정도로 예후가 좋지 않은 것이 특징입니다.지속적인 HDV 바이러스혈증은 동시 [42]감염자나 초감염자에서 질병 진행의 가장 중요한 위험인자입니다.만성 D형 간염의 불량한 예후에 책임이 있는 다른 요인으로는 남성 성, 감염 당시의 나이, 알코올 사용, 당뇨병, 비만, 면역 결핍 [42]등이 있습니다.
역학

HDV는 전 세계적으로 널리 보급되어 있습니다.그러나 B형 간염 예방 접종 프로그램으로 인해 많은 고소득 국가에서 유병률이 감소하고 있습니다(약을 주사하는 사람이나 HDV 고유 [42][55]지역 이민자와 같은 일부 그룹에서는 높은 비율이 유지되고 있음).HDV 감염은 HBV의 유병률이 [55]여전히 높은 전 세계 저소득 지역의 주요한 의학적 재앙입니다.현재 아시아와 아프리카의 아마존 유역과 저소득 지역은 HBV 비율이 높아 HDV 비율이 높습니다.전 세계적으로 만성 B형 간염 감염자의 5%가 D형 간염에 걸렸고 HIV 감염자의 12.5%도 [56][42]D형 간염에 함께 감염되었습니다.
역사
D형 간염 바이러스는 1977년 간 [57]질환이 심한 HBV에 감염된 환자에게서 핵항원으로 처음 보고되었습니다.이 핵항원은 그때 B형 간염항원으로 생각되었고 델타항원이라고 불렸습니다.침팬지를 대상으로 한 후속 실험에서 간염 델타 항원(HDAg)은 완전한 바이러스 [58]입자를 생성하기 위해 HBV 감염을 필요로 하는 병원체의 구조적인 부분임을 보여주었습니다.유전체 전체가 1986년에 복제되고 염기서열이 밝혀졌습니다.그 후에 고유속에 속하게 되었습니다.델타 바이러스.[59][60]
라브레아열
| 라브레아열 | |
|---|---|
| 기타이름 | 라브레아 흑열 라브레아 간염 산타마르타 열 |
| 전문 | 전염병 |
| 통상적인 발병 | 갑작스러운 |
| 지속 | 약 1주일 |
| 예방 | HBV 예방접종 |
| 예후 | 죽음. |
라브레아 열병(Labrea fever)은 1950년대 브라질 아마존 유역의 라브레아에서 발견된 치명적인 열대 감염증으로, 아마존 강 남쪽 지역, 아크레, 아마조나스, 론도니아에서 주로 발생합니다.이 병은 콜롬비아와 페루에서도 진단된 바 있습니다.현재 B형 간염(HBV)과 [61]D형 간염의 병용 감염 또는 슈퍼 감염으로 알려져 있습니다.
라브레아열은 황달, 거식증(식욕 부족), 혈연증(피를 토해내는 것), 두통, 발열, 심한 프로파간다와 함께 갑자기 시작됩니다.사망은 급성 간부전(ALF)에 의해 발생합니다.말기에는 동요, 섬망, 경련, 출혈성 혼수 등의 신경학적 증상이 흔히 나타납니다.이 증상들은 1주일 이내에 죽을 수도 있는 심각한 간염에 의해 발생합니다. 그리고 이것은 특징적으로 어린이와 젊은 성인들, 그리고 여성들보다 더 많은 남성들에게 영향을 미칩니다.뇌염도 동반되는 경우가 많습니다.이 질병은 매우 치명적입니다. 1986년 아마존의 보카도 아크레에서 수행된 연구에서 44명의 환자 중 39명이 [61]급성기에 사망했습니다.생존자는 만성 질환에 [citation needed]걸릴 수 있습니다.
델타 바이러스와 HBV 연관성의 주요 발견은 파라 주 벨렘의 에반드로 샤가스 연구소의 길베르타 벤사바스와 그녀의 [62]협력자들에 의해 이루어졌습니다.
감염된 환자는 특정 유형의 지방증(세포 내부의 작은 지방 방울이 특징인 미세 지방증), 주로 델타 바이러스 [63]항원이 포함된 대식세포로 구성된 모룰라 세포라고 불리는 염증성 세포가 대거 침투하는 등 광범위한 간 조직 파괴를 보입니다.
1987년 보카도 아크레 연구에서 과학자들은 역학 조사를 실시하여 무증상 HBV 보균자의 24%, 급성 비진격성 B형 간염 사례의 29%, 전격성 B형 간염 사례의 74%, 만성 B형 간염 [61]사례의 100%에서 델타 바이러스 감염이 보고되었습니다.델타 바이러스는 아마존 [64]지역에서 유행하는 것으로 보입니다.
진화
세 가지 유전자형(I–III)이 원래 기술되었습니다.유전자형 I형은 유럽, 북아메리카, 아프리카 그리고 일부 아시아에 고립되어 있습니다.유전자형 II는 일본, 대만, 그리고 야쿠티아 (러시아)에서 발견되었습니다.유전자형 III는 남아메리카(페루, 콜롬비아, 베네수엘라)에서만 발견되었습니다.대만과 오키나와 섬에서 온 일부 게놈은 타이핑하기 어려웠지만 유전자형 2형에 놓였습니다.그러나 현재 이 바이러스의 유전자형(HDV-1~HDV-8)[65]은 최소 8가지로 알려져 있습니다.계통발생학적 연구는 이 [35]병원체의 아프리카 기원을 시사합니다.
유전자형 3형의 36개 균주를 분석한 결과 이 균주들의 가장 최근의 일반적인 [66]조상은 1930년경에 생긴 것으로 추정되었습니다.이 유전자형은 1950년대 초부터 1970년대까지 남아메리카에서 기하급수적으로 퍼졌습니다.대체율은 연간 부지당 1.07×10개로−3 추정되었습니다.또 다른[67] 연구에서는 연간 사이트당 3.18×10개의−3 대체물이 발생하는 전체적인 진화율을 확인했습니다.위치에 따라 변이율이 달라졌는데, 초가변 영역은 간염 델타 항원 코딩 영역(연간 2.60×10개−3−3 부위별 치환)과 자가 촉매 영역(연간 1.11×10개−3 부위별 치환)보다 더 빠르게 진화했습니다.세 번째 연구에서는 9.5×10에서−3 1.2×10−3 대체/현장/[68]년 사이의 변이율을 제시했습니다.
유전자형은 1형을 제외하고 특정 지역에만 제한적으로 존재하는 것으로 보입니다. 일본, 대만 및 야쿠티아에서 발견되는 HDV-2(이전의 HDV-IIA); 일본 및 대만에서 발견되는 HDV-4(이전의 HDV-IIB); 아마존 지역에서 발견되는 HDV-3; 아프리카에서 [69]발견되는 HDV-5, HDV-6, HDV-7 및 HDV-8.유전자형 8형도 남아메리카에서 분리되었습니다.이 유전자형은 보통 아프리카에서만 발견되며 노예 [70]무역 동안 남아메리카로 수입되었을 수도 있습니다.
HDV 특이 CD8+ T 세포는 바이러스를 제어할 수 있지만 CD8+ T 세포에 의해 감지되지 않도록 [71]HDV 돌연변이가 발견되었습니다.
근연종
HDV와 유사한 몇 가지 다른 바이러스들이 인간 이외의 종에서 기술되었습니다.HDV와 달리, 그들 중 어떤 것도 복제하기 위해 HBV 계열의 바이러스에 의존하지 않습니다.이 약제들은 막대와 같은 구조, 델타 항원, 그리고 [72]리보자임을 가지고 있습니다.HDV와 그와 같은 모든 동족들은 국제 바이러스 [11]분류 위원회에 의해 그들 자신의 영역인 리보지비리아(Ribozyviria)로 분류됩니다.
참고문헌
- ^ a b c "Hepatitis D NIDDK". National Institute of Diabetes and Digestive and Kidney Diseases. Retrieved 10 September 2019.
- ^ a b "Hepatitis D". www.who.int. Retrieved 10 September 2019.
- ^ "Hepatitis (Viral) NIDDK". The National Institute of Diabetes and Digestive and Kidney Diseases. Retrieved 2020-06-19.
- ^ Farci P (2003). "Delta hepatitis: an update". Journal of Hepatology. 39 (Suppl 1): S212–9. doi:10.1016/s0168-8278(03)00331-3. PMID 14708706.
- ^ Magnius L, Taylor J, Mason WS, Sureau C, Dény P, Norder H (December 2018). "ICTV Virus Taxonomy Profile: Deltavirus". The Journal of General Virology. 99 (12): 1565–1566. doi:10.1099/jgv.0.001150. PMID 30311870.
- ^ Makino S, Chang MF, Shieh CK, Kamahora T, Vannier DM, Govindarajan S, Lai MM (1987). "Molecular cloning and sequencing of a human hepatitis delta (delta) virus RNA". Nature. 329 (6137): 343–6. Bibcode:1987Natur.329..343M. doi:10.1038/329343a0. PMID 3627276. S2CID 4368061.
- ^ "Hepatitis D". www.who.int. Retrieved 2020-09-20.
- ^ Fattovich G, Giustina G, Christensen E, Pantalena M, Zagni I, Realdi G, Schalm SW (March 2000). "Influence of hepatitis delta virus infection on morbidity and mortality in compensated cirrhosis type B. The European Concerted Action on Viral Hepatitis (Eurohep)". Gut. 46 (3): 420–6. doi:10.1136/gut.46.3.420. PMC 1727859. PMID 10673308.
- ^ Miao Z, Zhang S, Ou X, Li S, Ma Z, Wang W, Peppelenbosch MP, Liu J, Pan Q (April 2020). "Estimating the Global Prevalence, Disease Progression, and Clinical Outcome of Hepatitis Delta Virus Infection". The Journal of Infectious Diseases. 221 (10): 1677–1687. doi:10.1093/infdis/jiz633. PMC 7184909. PMID 31778167.
- ^ "ICTV 9th Report (2011) Deltavirus". International Committee on Taxonomy of Viruses (ICTV). Archived from the original on 30 January 2019. Retrieved 30 January 2019.
- ^ a b "Virus Taxonomy: 2020 Release". International Committee on Taxonomy of Viruses (ICTV). March 2021. Retrieved 5 August 2021.
- ^ Poisson F, Roingeard P, Baillou A, Dubois F, Bonelli F, Calogero RA, Goudeau A (November 1993). "Characterization of RNA-binding domains of hepatitis delta antigen". The Journal of General Virology. 74 (Pt 11): 2473–8. doi:10.1099/0022-1317-74-11-2473. PMID 8245865.
- ^ Zuccola HJ, Rozzelle JE, Lemon SM, Erickson BW, Hogle JM (July 1998). "Structural basis of the oligomerization of hepatitis delta antigen". Structure. 6 (7): 821–30. doi:10.1016/S0969-2126(98)00084-7. PMID 9687364.
- ^
- ^ Elena SF, Dopazo J, Flores R, Diener TO, Moya A (July 1991). "Phylogeny of viroids, viroidlike satellite RNAs, and the viroidlike domain of hepatitis delta virus RNA". Proceedings of the National Academy of Sciences of the United States of America. 88 (13): 5631–4. Bibcode:1991PNAS...88.5631E. doi:10.1073/pnas.88.13.5631. PMC 51931. PMID 1712103.
- ^ Sureau C (2006). "The role of the HBV envelope proteins in the HDV replication cycle". Hepatitis Delta Virus. Current Topics in Microbiology and Immunology. Vol. 307. pp. 113–31. doi:10.1007/3-540-29802-9_6. ISBN 978-3-540-29801-4. PMID 16903223.
- ^ Saldanha JA, Thomas HC, Monjardino JP (July 1990). "Cloning and sequencing of RNA of hepatitis delta virus isolated from human serum". The Journal of General Virology. 71 (7): 1603–6. doi:10.1099/0022-1317-71-7-1603. PMID 2374010.
- ^ Miao Z, Zhang S, Ma Z, Hakim MS, Wang W, Peppelenbosch MP, Pan Q (January 2019). "Recombinant identification, molecular classification and proposed reference genomes for hepatitis delta virus". Journal of Viral Hepatitis. 26 (1): 183–190. doi:10.1111/jvh.13010. PMC 7379554. PMID 30260538.
- ^ Yan H, Zhong G, Xu G, He W, Jing Z, Gao Z, Huang Y, Qi Y, Peng B, Wang H, Fu L, Song M, Chen P, Gao W, Ren B, Sun Y, Cai T, Feng X, Sui J, Li W (November 2012). "Sodium taurocholate cotransporting polypeptide is a functional receptor for human hepatitis B and D virus". eLife. 1: e00049. doi:10.7554/eLife.00049. PMC 3485615. PMID 23150796.
- ^ Engelke M, Mills K, Seitz S, Simon P, Gripon P, Schnölzer M, Urban S (April 2006). "Characterization of a hepatitis B and hepatitis delta virus receptor binding site". Hepatology. 43 (4): 750–60. doi:10.1002/hep.21112. PMID 16557545. S2CID 23549907.
- ^ Schulze A, Schieck A, Ni Y, Mier W, Urban S (February 2010). "Fine mapping of pre-S sequence requirements for hepatitis B virus large envelope protein-mediated receptor interaction". Journal of Virology. 84 (4): 1989–2000. doi:10.1128/JVI.01902-09. PMC 2812397. PMID 20007265.
- ^ Xia YP, Yeh CT, Ou JH, Lai MM (February 1992). "Characterization of nuclear targeting signal of hepatitis delta antigen: nuclear transport as a protein complex". Journal of Virology. 66 (2): 914–21. doi:10.1128/JVI.66.2.914-921.1992. PMC 240792. PMID 1731113.
- ^ Lehmann E, Brueckner F, Cramer P (November 2007). "Molecular basis of RNA-dependent RNA polymerase II activity". Nature. 450 (7168): 445–9. Bibcode:2007Natur.450..445L. doi:10.1038/nature06290. hdl:11858/00-001M-0000-0015-7EE1-9. PMID 18004386. S2CID 4393153.
- ^ Filipovska J, Konarska MM (January 2000). "Specific HDV RNA-templated transcription by pol II in vitro". RNA. 6 (1): 41–54. doi:10.1017/S1355838200991167. PMC 1369892. PMID 10668797.
- ^ Greco-Stewart VS, Schissel E, Pelchat M (March 2009). "The hepatitis delta virus RNA genome interacts with the human RNA polymerases I and III". Virology. 386 (1): 12–5. doi:10.1016/j.virol.2009.02.007. PMID 19246067.
- ^ Li YJ, Macnaughton T, Gao L, Lai MM (July 2006). "RNA-templated replication of hepatitis delta virus: genomic and antigenomic RNAs associate with different nuclear bodies". Journal of Virology. 80 (13): 6478–86. doi:10.1128/JVI.02650-05. PMC 1488965. PMID 16775335.
- ^ Branch AD, Benenfeld BJ, Baroudy BM, Wells FV, Gerin JL, Robertson HD (February 1989). "An ultraviolet-sensitive RNA structural element in a viroid-like domain of the hepatitis delta virus". Science. 243 (4891): 649–52. Bibcode:1989Sci...243..649B. doi:10.1126/science.2492676. PMID 2492676.
- ^ Wu HN, Lin YJ, Lin FP, Makino S, Chang MF, Lai MM (March 1989). "Human hepatitis delta virus RNA subfragments contain an autocleavage activity". Proceedings of the National Academy of Sciences of the United States of America. 86 (6): 1831–5. Bibcode:1989PNAS...86.1831W. doi:10.1073/pnas.86.6.1831. PMC 286798. PMID 2648383.
- ^ a b Weiner AJ, Choo QL, Wang KS, Govindarajan S, Redeker AG, Gerin JL, Houghton M (February 1988). "A single antigenomic open reading frame of the hepatitis delta virus encodes the epitope(s) of both hepatitis delta antigen polypeptides p24 delta and p27 delta". Journal of Virology. 62 (2): 594–9. doi:10.1128/JVI.62.2.594-599.1988. PMC 250573. PMID 2447291.
- ^ Jayan GC, Casey JL (December 2002). "Inhibition of hepatitis delta virus RNA editing by short inhibitory RNA-mediated knockdown of ADAR1 but not ADAR2 expression". Journal of Virology. 76 (23): 12399–404. doi:10.1128/JVI.76.23.12399-12404.2002. PMC 136899. PMID 12414985.
- ^ Sato S, Cornillez-Ty C, Lazinski DW (August 2004). "By inhibiting replication, the large hepatitis delta antigen can indirectly regulate amber/W editing and its own expression". Journal of Virology. 78 (15): 8120–34. doi:10.1128/JVI.78.15.8120-8134.2004. PMC 446097. PMID 15254184.
- ^ Taylor JM (2006). "Structure and replication of hepatitis delta virus RNA". Hepatitis Delta Virus. Current Topics in Microbiology and Immunology. Vol. 307. pp. 1–23. doi:10.1007/3-540-29802-9_1. ISBN 978-3-540-29801-4. PMID 16903218.
- ^ Chang MF, Chen CJ, Chang SC (February 1994). "Mutational analysis of delta antigen: effect on assembly and replication of hepatitis delta virus". Journal of Virology. 68 (2): 646–53. doi:10.1128/JVI.68.2.646-653.1994. PMC 236498. PMID 8289368.
- ^ Jaoudé GA, Sureau C (August 2005). "Role of the antigenic loop of the hepatitis B virus envelope proteins in infectivity of hepatitis delta virus". Journal of Virology. 79 (16): 10460–6. CiteSeerX 10.1.1.570.4147. doi:10.1128/jvi.79.16.10460-10466.2005. PMC 1182656. PMID 16051838.
- ^ a b Radjef N, Gordien E, Ivaniushina V, Gault E, Anaïs P, Drugan T, Trinchet JC, Roulot D, Tamby M, Milinkovitch MC, Dény P (March 2004). "Molecular phylogenetic analyses indicate a wide and ancient radiation of African hepatitis delta virus, suggesting a deltavirus genus of at least seven major clades". Journal of Virology. 78 (5): 2537–44. doi:10.1128/JVI.78.5.2537-2544.2004. PMC 369207. PMID 14963156.
- ^ Taylor JM (January 2006). "Hepatitis delta virus". Virology. 344 (1): 71–6. doi:10.1016/j.virol.2005.09.033. PMID 16364738.
- ^ "U.S. National Library of Medicine "Delta Agent (hepatitis D)"".
- ^ Tayor JM (2009). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. p. 121. ISBN 978-0-12-375147-8.
- ^ "Hepatitis B". www.who.int.
- ^ a b c "Hepatitis D - American Liver Foundation". liverfoundation.org. 23 May 2022.
- ^ Schillie, Sarah (2018). "Prevention of Hepatitis B Virus Infection in the United States: Recommendations of the Advisory Committee on Immunization Practices". MMWR. Recommendations and Reports. 67 (1): 1–31. doi:10.15585/mmwr.rr6701a1. PMC 5837403. PMID 29939980.
- ^ a b c d e f g h i j k l m Asselah, Tarik; Rizzetto, Mario (6 July 2023). "Hepatitis D Virus Infection". New England Journal of Medicine. 389 (1): 58–70. doi:10.1056/NEJMra2212151. PMID 37407002. S2CID 259354401.
- ^ Yurdaydin C, Idilman R (August 2015). "Therapy of Delta Hepatitis". Cold Spring Harbor Perspectives in Medicine. 5 (10): a021543. doi:10.1101/cshperspect.a021543. PMC 4588130. PMID 26253093.
- ^ Abbas Z, Khan MA, Salih M, Jafri W (December 2011). Abbas Z (ed.). "Interferon alpha for chronic hepatitis D". The Cochrane Database of Systematic Reviews. 2011 (12): CD006002. doi:10.1002/14651858.CD006002.pub2. PMC 6823236. PMID 22161394.
- ^ Heidrich B, Yurdaydın C, Kabaçam G, Ratsch BA, Zachou K, Bremer B, Dalekos GN, Erhardt A, Tabak F, Yalcin K, Gürel S, Zeuzem S, Cornberg M, Bock CT, Manns MP, Wedemeyer H (July 2014). "Late HDV RNA relapse after peginterferon alpha-based therapy of chronic hepatitis delta". Hepatology. 60 (1): 87–97. doi:10.1002/hep.27102. PMID 24585488. S2CID 205892640.
- ^ Pascarella S, Negro F (January 2011). "Hepatitis D virus: an update". Liver International. 31 (1): 7–21. doi:10.1111/j.1478-3231.2010.02320.x. PMID 20880077. S2CID 29142477.
- ^ "Hepcludex". European Medicines Agency. 26 May 2020.
- ^ Francisco EM (2020-05-29). "Hepcludex". European Medicines Agency. Archived from the original on 2020-06-15. Retrieved 2020-08-06.
- ^ "Bulevirtide - MYR Pharma". AdisInsight. Springer Nature Switzerland AG. Retrieved 2020-08-06.
MYR Pharmaceuticals receives Conditional Marketing Authorisation by the European Commission for bulevirtide in the European Union for Hepatitis B and D
- ^ Degasperi E, Anolli MP, Uceda Renteria SC 등HDV 관련 보상성 간경변증 및 임상적으로 유의한 문맥압항진증 환자에서 48주간 Bulebirtide 단독요법.제이 헤파톨.2022;77(6):1525-1531. Doi:10.1016/j.jhep.2022.07.016
- ^ Sandmann, Lisa; Cornberg, Markus (April 2021). "Experimental Drugs for the Treatment of Hepatitis D". Journal of Experimental Pharmacology. 13: 461–468. doi:10.2147/JEP.S235550. PMC 8057838. PMID 33889032.
- ^ Koh, Christopher; Canini, Laetitia; Dahari, Harel; Zhao, Xiongce; Uprichard, Susan L.; Haynes-Williams, Vanessa; Winters, Mark A.; Subramanya, Gitanjali; Cooper, Stewart L.; Pinto, Peter; Wolff, Erin F.; Bishop, Rachel; Ai Thanda Han, Ma; Cotler, Scott J.; Kleiner, David E.; Keskin, Onur; Idilman, Ramazan; Yurdaydin, Cihan; Glenn, Jeffrey S.; Heller, Theo (October 2015). "Oral prenylation inhibition with lonafarnib in chronic hepatitis D infection: a proof-of-concept randomised, double-blind, placebo-controlled phase 2A trial". The Lancet. Infectious Diseases. 15 (10): 1167–1174. doi:10.1016/S1473-3099(15)00074-2. PMC 4700535. PMID 26189433.
- ^ Vaillant, Andrew (10 May 2019). "REP 2139: Antiviral Mechanisms and Applications in Achieving Functional Control of HBV and HDV Infection". ACS Infectious Diseases. 5 (5): 675–687. doi:10.1021/acsinfecdis.8b00156. PMID 30199230. S2CID 52183556.
- ^ Rizzetto M (2020). "Epidemiology of the Hepatitis D virus". WikiJournal of Medicine. 7: 7. doi:10.15347/wjm/2020.001.
- ^ a b Rizzetto M (July 2015). "Hepatitis D Virus: Introduction and Epidemiology". Cold Spring Harbor Perspectives in Medicine. 5 (7): a021576. doi:10.1101/cshperspect.a021576. PMC 4484953. PMID 26134842.
- ^ "Hepatitis D". www.who.int.
- ^ Rizzetto M, Canese MG, Aricò S, Crivelli O, Trepo C, Bonino F, Verme G (December 1977). "Immunofluorescence detection of new antigen-antibody system (delta/anti-delta) associated to hepatitis B virus in liver and in serum of HBsAg carriers". Gut. 18 (12): 997–1003. doi:10.1136/gut.18.12.997. PMC 1411847. PMID 75123.
- ^ Rizzetto M, Canese MG, Purcell RH, London WT, Sly LD, Gerin JL (Nov–Dec 1981). "Experimental HBV and delta infections of chimpanzees: occurrence and significance of intrahepatic immune complexes of HBcAg and delta antigen". Hepatology. 1 (6): 567–74. doi:10.1002/hep.1840010602. PMID 7030907. S2CID 83892580.
- ^ Wang KS, Choo QL, Weiner AJ, Ou JH, Najarian RC, Thayer RM, Mullenbach GT, Denniston KJ, Gerin JL, Houghton M (Oct 9–15, 1986). "Structure, sequence and expression of the hepatitis delta (delta) viral genome". Nature. 323 (6088): 508–14. Bibcode:1986Natur.323..508W. doi:10.1038/323508a0. PMID 3762705. S2CID 4265339.
- ^ Fauquet CM, Mayo MA, Maniloff J, Desselberger U, Ball LA (2005). "Deltavirus". Eight Report of the International Committee on Taxonomy of Viruses. London: 735–8.
- ^ a b c Bensabath G, Hadler SC, Soares MC, Fields H, Dias LB, Popper H, Maynard JE (1987). "Hepatitis delta virus infection and Labrea hepatitis. Prevalence and role in fulminant hepatitis in the Amazon Basin". JAMA. 258 (4): 479–83. doi:10.1001/jama.1987.03400040077025. PMID 3599343.
- ^ Gomes-Gouvêa MS, Soares MC, Bensabath G, de Carvalho-Mello IM, Brito EM, Souza OS, et al. (November 2009). "Hepatitis B virus and hepatitis delta virus genotypes in outbreaks of fulminant hepatitis (Labrea black fever) in the western Brazilian Amazon region". The Journal of General Virology. 90 (Pt 11): 2638–2643. doi:10.1099/vir.0.013615-0. PMID 19605587.
- ^ Tommolino E, Piper MH, Sears D (2021-04-03). Anand BS (ed.). "Fatty Liver: Overview, Etiology, Epidemiology". Medscape.
- ^ Cabezas C, Braga W (September 2020). "Hepatitis B Virus and Delta Infection: Special Considerations in the Indigenous and Isolated Riverside Populations in the Amazon Region". Clinical Liver Disease. 16 (3): 117–122. doi:10.1002/cld.1009. PMC 7508778. PMID 33005393.
- ^ Celik I, Karatayli E, Cevik E, Kabakçi SG, Karatayli SC, Dinç B, et al. (December 2011). "Complete genome sequences and phylogenetic analysis of hepatitis delta viruses isolated from nine Turkish patients". Archives of Virology. 156 (12): 2215–20. doi:10.1007/s00705-011-1120-y. PMID 21984217. S2CID 31356.
- ^ Alvarado-Mora MV, Romano CM, Gomes-Gouvêa MS, Gutierrez MF, Carrilho FJ, Pinho JR (August 2011). "Dynamics of hepatitis D (delta) virus genotype 3 in the Amazon region of South America". Infection, Genetics and Evolution. 11 (6): 1462–8. doi:10.1016/j.meegid.2011.05.020. PMID 21645647.
- ^ Chao YC, Tang HS, Hsu CT (August 1994). "Evolution rate of hepatitis delta virus RNA isolated in Taiwan". Journal of Medical Virology. 43 (4): 397–403. doi:10.1002/jmv.1890430414. PMID 7964650. S2CID 22539505.
- ^ Homs M, Rodriguez-Frias F, Gregori J, Ruiz A, Reimundo P, Casillas R, Tabernero D, Godoy C, Barakat S, Quer J, Riveiro-Barciela M, Roggendorf M, Esteban R, Buti M (2016). "Evidence of an Exponential Decay Pattern of the Hepatitis Delta Virus Evolution Rate and Fluctuations in Quasispecies Complexity in Long-Term Studies of Chronic Delta Infection". PLOS ONE. 11 (6): e0158557. Bibcode:2016PLoSO..1158557H. doi:10.1371/journal.pone.0158557. PMC 4928832. PMID 27362848.
- ^ Le Gal F, Gault E, Ripault MP, Serpaggi J, Trinchet JC, Gordien E, Dény P (September 2006). "Eighth major clade for hepatitis delta virus". Emerging Infectious Diseases. 12 (9): 1447–50. doi:10.3201/eid1209.060112. PMC 3294742. PMID 17073101.
- ^ Barros LM, Gomes-Gouvêa MS, Pinho JR, Alvarado-Mora MV, Dos Santos A, Mendes-Corrêa MC, Caldas AJ, Sousa MT, Santos MD, Ferreira AS (September 2011). "Hepatitis Delta virus genotype 8 infection in Northeast Brazil: inheritance from African slaves?". Virus Research. 160 (1–2): 333–9. doi:10.1016/j.virusres.2011.07.006. PMID 21798297.
- ^ Karimzadeh H, Kiraithe MM, Oberhardt V, Salimi Alizei E, Bockmann J, Schulze Zur Wiesch J, et al. (May 2019). "Mutations in Hepatitis D Virus Allow It to Escape Detection by CD8+ T Cells and Evolve at the Population Level". Gastroenterology. 156 (6): 1820–1833. doi:10.1053/j.gastro.2019.02.003. PMC 6486497. PMID 30768983.
- ^ Paraskevopoulou S, Pirzer F, Goldmann N, Schmid J, Corman VM, Gottula LT, et al. (July 2020). "Mammalian deltavirus without hepadnavirus coinfection in the neotropical rodent Proechimys semispinosus". Proceedings of the National Academy of Sciences of the United States of America. 117 (30): 17977–17983. Bibcode:2020PNAS..11717977P. doi:10.1073/pnas.2006750117. PMC 7395443. PMID 32651267.
서지학
- Specter SC, ed. (1999). Viral Hepatitis: Diagnosis, Therapy, and Prevention. Humana Press. ISBN 0-89603-424-0.
- da Fonseca JC (2004). "[Hepatitis fulminant in Brazilian Amazon]". Revista da Sociedade Brasileira de Medicina Tropical. 37. 37 (Suppl 2): 93–5. doi:10.1590/s0037-86822004000700015. PMID 15586904.
- Bensabath G, Soares M (2004). "[The evolution of knowledge about viral hepatitis in Amazon region: from epidemiology and etiology to the prophilaxy]". Revista da Sociedade Brasileira de Medicina Tropical. 37 (Suppl 2): 14–26. doi:10.1590/S0037-86822004000700003. PMID 15586892.
- Fonseca JC, Souza RA, Brasil LM, Araújo JR, Ferreira LC (2004). "Fulminant hepatic failure in children and adolescents in Northern Brazil". Revista da Sociedade Brasileira de Medicina Tropical. 37 (1): 67–9. doi:10.1590/S0037-86822004000100019. PMID 15042190.
외부 링크
- 세계보건기구 D형 간염에 관한 자료집
- ICTV 보고서: 델타바이러스
- 바이러스 영역:델타바이러스
- "Hepatitis delta virus". NCBI Taxonomy Browser. 12475.


