세포골격
Cytoskeleton| 세포생물학 | |
|---|---|
| 동물 세포도 | |
 |
세포골격은 박테리아와 [1]고세균을 제외한 모든 세포의 세포질에 존재하는 단백질 필라멘트를 연결하는 복잡하고 역동적인 네트워크입니다.그것은 세포핵에서 세포막까지 확장되고 다양한 유기체의 유사한 단백질로 구성되어 있다.진핵생물에서는 마이크로필라멘트, 중간필라멘트, 마이크로튜브 등 3가지 주요 구성 요소로 구성되며, 이들은 모두 세포의 [2]요구에 따라 빠르게 성장하거나 분해할 수 있다.
세포골격은 다양한 기능을 수행할 수 있습니다.세포의 주요 기능은 세포의 형태와 변형에 대한 기계적 저항력을 주는 것이며 세포 외 결합 조직 및 기타 세포와의 연계를 통해 전체 [3][4]조직을 안정시키는 것이다.세포골격은 또한 수축할 수 있으며, 따라서 세포와 세포의 환경을 변형시키고 세포가 이동하도록 [5]한다.게다가, 많은 세포 신호 경로와 세포외 재료의 염색체의 휴대 division,[3]동안 흑인 분리(엔도시토시스)[6]이해가에 연루된 세포 division,[7]의 space[5]고 세포 내 운송에 예를 들어 ves의(, 운동의 셀의 내용이 조직화하기 위해 비계로 세포질 분열 단계이다.icles고 발음하는 o세포 [3]내 rganelles) 및 세포벽을 [3]구축하기 위한 템플릿이 될 수 있습니다.게다가 편모, 섬모, 편모, 편모, 포도솜과 같은 특수한 구조를 형성할 수 있다.세포골격의 구조, 기능 및 동적 거동은 유기체와 [3][7]세포 유형에 따라 매우 다를 수 있습니다.한 세포 내에서조차 세포골격은 다른 단백질과의 연관성과 네트워크의 [5]이전 역사를 통해 변할 수 있다.
세포골격에 의해 수행되는 작용의 대규모 예는 근육 수축이다.이것은 고도로 전문화된 세포들이 함께 일하는 그룹에 의해 수행됩니다.이러한 근육 수축의 진정한 기능을 보여주는 세포골격의 주요 구성요소는 미세 섬유입니다.마이크로필라멘트는 액틴으로 [8]알려진 가장 풍부한 세포 단백질로 구성되어 있습니다.근육이 수축하는 동안, 각 근육 세포 내에서, 미오신 분자 모터는 집합적으로 평행한 액틴 필라멘트에 힘을 가한다.근육 수축은 신경 자극으로부터 시작되는데, 그러면 칼슘이 석회질 망막에서 방출되는 양이 증가한다.세포 내 칼슘의 증가는 트로포미오신과 트로포닌이라는 두 [8]가지 단백질의 도움으로 근육 수축이 시작되도록 합니다.트로포미오신은 액틴과 미오신 사이의 상호작용을 억제하고 트로포닌은 칼슘의 증가를 감지하여 억제 작용을 [9]방출한다.이 작용은 근육 세포를 수축시키고, 많은 근육 세포에서 동기 과정을 통해 전체 근육을 수축시킵니다.
역사
1903년 니콜라이 K. Koltsov는 세포골격이라고 부르는 관망에 의해 세포의 모양이 결정된다고 제안했다.세포질 생화학을 동적으로 조정하는 단백질 모자이크의 개념은 1929년[10] 루돌프 피터스에 의해 제안되었고, 반면 용어 (프랑스어로 cytosquelett)는 1931년 [11]프랑스 태아학자 Paul Wintrebert에 의해 처음 소개되었습니다.
세포 골격이 처음 도입되었을 때, 세포골격은 세포조직이 [12]제자리를 유지하는데 도움을 주는 재미없는 젤 같은 물질로 생각되었다.세포골격과 그 구성 요소의 목적을 이해하기 위해 많은 연구가 이루어졌다.Stuart Hameroff와 Roger Penrose의 도움으로, 뇌 속의 뉴런 안에서 미세관이 진동한다는 것이 밝혀졌는데, 이는 뇌파가 더 깊은 미세관 [13]진동에서 나온다는 것을 암시한다.이 발견은 세포 골격이 단지 겔과 같은 물질이 아니며 실제로 [disputed ]목적이 있다는 것을 증명했다.
처음에 세포골격은 진핵생물의 배타적인 것으로 생각되었지만 1992년에 원핵생물에도 존재하는 것으로 밝혀졌다.이 발견은 박테리아가 진핵 세포 [14]골격의 주요 성분인 튜불린과 액틴과 상동하는 단백질을 가지고 있다는 것을 깨달은 후에 이루어졌다.
진핵세포골격
진핵세포는 세 종류의 세포골격 필라멘트를 포함한다: 미세 필라멘트, 미세관, 그리고 중간 필라멘트를.뉴런에서 중간 필라멘트는 신경 [15]필라멘트로 알려져 있다.각 유형은 다른 유형의 단백질 서브유닛의 중합에 의해 형성되며, 고유한 형태와 세포 내 분포를 가진다.마이크로필라멘트는 단백질 액틴의 중합체이며 지름은 7 nm이다.미세관은 튜브린으로 구성되며 직경은 25nm이다.중간 필라멘트는 발견되는 세포의 유형에 따라 다양한 단백질로 구성되어 있으며,[1] 일반적으로 직경이 8-12 nm입니다.세포골격은 세포에 구조와 모양을 제공하고, 세포 일부에서 고분자를 제외함으로써, [16]이 구획의 고분자 밀집 수준을 증가시킨다.세포골격 요소는 세포막과 [17]광범위하고 밀접하게 상호작용합니다.
파킨슨병, 알츠하이머병, 헌팅턴병, 그리고 근위축성 측삭경화증(ALS)과 같은 신경변성 질환에 대한 연구는 세포 골격이 이러한 [18]질병들에 영향을 받는다는 것을 보여준다.파킨슨병은 떨림, 경직성, 그리고 다른 비운동적 증상을 야기하는 뉴런의 저하로 특징지어진다.연구 결과 미세관 조립과 세포골격의 안정성이 손상되어 뉴런이 시간이 [19]지남에 따라 저하되는 것으로 나타났습니다.알츠하이머병은 미세관을 안정시키는 타우 단백질이 세포골격의 [20]병리를 일으키는 질환의 진행 과정에서 오작동한다.소포를 세포골격에 연결하는 것과 관련된 헌팅턴 단백질의 과잉 글루타민 또한 헌팅턴병 [21]발병의 한 요인으로 제안되었다.근위축성 측삭경화증은 운동신경세포의 저하로 인한 운동 손실을 초래하고 세포골격의 [22]결함도 수반한다.
운동단백질을 포함한 부속단백질은 필라멘트를 조절하고 다른 세포화합물 및 서로 연결하며 특정 위치에서 [23]세포골격 필라멘트의 제어된 조립에 필수적이다.
액틴과 미소관과 상호작용하는 다수의 소분자 세포골격 약물이 발견되었다.이러한 화합물은 세포골격 연구에 유용한 것으로 입증되었으며, 일부는 임상적 응용을 가지고 있다.
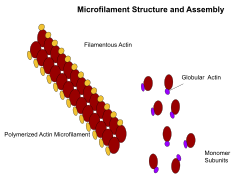
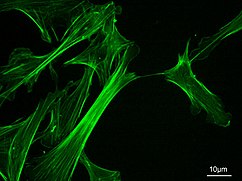
마이크로필라멘트
액틴 필라멘트로도 알려진 미세 필라멘트는 G-액틴 단백질의 선형 중합체로 구성되며 필라멘트의 성장 끝이 세포막과 같은 장벽에 밀릴 때 힘을 발생시킵니다.그것들은 또한 마이크로필라멘트에 부착되어 그것들을 따라 걷는 미오신 분자의 움직임의 흔적으로 작용합니다.일반적으로 마이크로필라멘트의 주요 성분 또는 단백질은 액틴이다.G-액틴 단량체는 결합되어 마이크로필라멘트(액틴 필라멘트)를 계속 형성하는 폴리머를 형성합니다.그리고 나서 이 소단위들은 F-actin [24]사슬이라고 불리는 사슬에 얽히는 두 개의 체인으로 결합됩니다.F-actin 필라멘트를 따라 움직이는 미오신은 근육뿐만 아니라 대부분의 비근육 세포 [25]유형에서도 소위 악토미오신 섬유에서 수축력을 생성합니다.액틴 구조는 수축성 액토미오신 필라멘트("스트레스 섬유")의 경우 Rho 자체, 라멜리포디아의 경우 Rac, 필로포디아의 경우 Cdc42와 같은 작은 GTP 결합 단백질의 Rho 패밀리에 의해 제어된다.
기능은 다음과 같습니다.
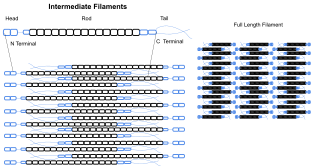
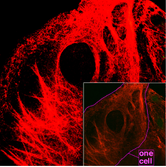
중간 필라멘트
중간 필라멘트는 많은 진핵세포의 세포골격의 일부이다.이러한 필라멘트는 지름이 평균 10나노미터로 미세 필라멘트와 세포골격의 이종 구성 요소보다 안정적입니다(강하게 결합됨).액틴 필라멘트와 마찬가지로, 그들은 장력을 지지함으로써 세포 형태를 유지하는 데 기능합니다(반대로, 미소관은 압축에 저항하지만 또한 유사분열과 중심체의 위치 결정 동안 장력을 견딜 수 있습니다).중간 필라멘트는 세포의 내부 3차원 구조를 구성하며, 세포 조직을 고정하고 핵 라미나의 구조적 구성 요소 역할을 합니다.그들은 또한 세포-세포와 세포-매트릭스 접합에도 참여한다.핵 라미나는 모든 동물과 모든 조직에 존재한다.초파리와 같은 몇몇 동물들은 세포질 중간 필라멘트를 가지고 있지 않다.세포질 중간 필라멘트를 발현하는 동물에서 이것들은 조직 특이적이다.[4]상피 세포의 케라틴 중간 필라멘트는 피부가 견딜 수 있는 다양한 기계적 스트레스를 보호합니다.또한 대사, 산화, 화학적 스트레스로부터 장기를 보호합니다.이러한 중간 필라멘트로 상피세포의 강화는 스트레스 [26]확률을 감소시킴으로써 세포자멸의 시작 또는 세포사멸을 예방할 수 있다.
중간 필라멘트는 세포와 핵에 대한 지지계 또는 "스카폴딩"으로 가장 일반적으로 알려져 있으며, 일부 세포 기능에서도 역할을 한다.단백질과 데스모솜과 결합하여, 중간 필라멘트는 세포 세포 연결을 형성하고 세포의 중요한 기능뿐만 아니라 세포 사이의 메시징에 사용되는 세포 매트릭스 결합을 고정시킵니다.이러한 연결을 통해 세포는 여러 세포의 디스모솜을 통해 통신하여 세포 환경의 신호에 따라 조직의 구조를 조정합니다.IF 단백질의 돌연변이는 조기 노화, 장기를 손상시키는 데스민 돌연변이, 알렉산더병,[27] 그리고 근육위축증과 같은 심각한 의학적 문제를 야기하는 것으로 나타났다.
중간 필라멘트는 다음과 같습니다.
- 비멘틴으로 만들어졌어요비멘틴 중간 필라멘트는 일반적으로 간엽세포에 존재한다.
- 케라틴으로 만들어졌어요케라틴은 일반적으로 상피세포에 존재한다.
- 신경세포의 신경섬유
- 핵 외피를 구조적으로 지탱하는 라민으로 만들어졌다.
- 데스민으로 만들어진, 근육 세포의 [28]구조적이고 기계적인 지지에서 중요한 역할을 한다.
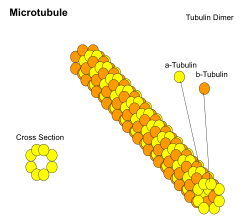
미소관
마이크로튜브는 직경 약 23nm(루멘 직경 약 15nm)의 중공 원통으로, 가장 일반적으로 13개의 프로토필라멘트로 구성되며, 차례로 알파 및 베타 튜브린의 중합체이다.이들은 매우 동적인 행동을 하며 중합하기 위해 GTP와 결합합니다.그것들은 일반적으로 중심체별로 정리되어 있다.
9개의 세쌍둥이 세트(별 모양)는 중심축을 형성하고, 2개의 추가 미소관(바퀴 모양)을 중심으로 하는 9개의 두쌍둥이 세트(별 모양)는 섬모 및 편모를 형성합니다.후자의 형성은 일반적으로 "9+2" 배열이라고 불리며, 여기서 각 더블렛은 단백질 다인(dynein)에 의해 다른 더블렛과 연결됩니다.편모와 섬모는 모두 세포의 구조적 구성 요소이며 미세관에 의해 유지되기 때문에 세포골격의 일부로 간주될 수 있다.섬모에는 두 가지 유형이 있습니다: 운동성 섬모와 비운동성 섬모입니다.섬모는 편모보다 짧고 더 많다.이동성 섬모는 세포에 대한 감각 정보를 받는 비이동성 섬모에 비해 리드미컬한 흔들림 또는 박동 운동을 합니다; 다른 세포나 주변 유체로부터 신호를 처리합니다.또한 미소관은 섬모 및 [29]편모의 박동(이동)을 제어한다.또한 미소관에 부착된 다이네인 암은 분자 모터로서 기능한다.섬모와 편모의 운동은 미세관이 서로 미끄러지면서 생성되는데,[29] 이것은 ATP를 필요로 합니다.이들은 다음과 같은 주요 역할을 수행합니다.
위에서 설명한 역할 외에도 Stuart Hameroff와 Roger Penrose는 미세관이 [30]의식에서 기능한다고 제안했습니다.
비교
| 세포골격 타이프[31] | 직경 (nm)[32] | 구조. | 서브유닛의[31] 예 |
|---|---|---|---|
| 마이크로필라멘트 | 6 | 이중나선 | 액틴 |
| 중간의 필라멘트 | 10 | 2개의 반평행 나선/다이머로 4중합체 형성 | |
| 미소관 | 23 | 프로토필라멘트, 차례로 스타트민과[33] 복합된 튜불린 서브유닛으로 구성됨 | α 및 β-튜브린 |
셉틴스
셉틴은 진핵생물에서 발견되는 고도로 보존된 GTP 결합 단백질의 그룹이다.서로 다른 셉틴이 단백질 복합체를 형성한다.이것들은 필라멘트나 링에 조립할 수 있습니다.따라서 셉틴은 세포골격의 [34]일부로 간주될 수 있다.세포에서 셉틴의 기능은 다른 단백질에 대한 국소적인 부착 부위의 역할을 하고, 특정 [34]분자의 세포 구획 간 확산을 막는 것을 포함한다.효모세포에서는 세포분열 시 구조적인 지지를 제공하기 위해 발판을 만들고 세포의 일부를 구분합니다.인간 세포에 대한 최근의 연구는 셉틴이 박테리아 병원체 주위에 우리를 만들어 해로운 미생물을 고정시키고 다른 [35]세포에 침입하는 것을 막는다는 것을 시사한다.
스펙트린
스펙트린은 진핵세포에서 혈장막의 세포내측에 선을 이루는 세포골격 단백질이다.스펙트린은 오각형 또는 육각형 배치를 형성하여 발판을 형성하고 혈장막 무결성 및 세포골격 [36]구조 유지에 중요한 역할을 한다.
효모세포골격
발아 효모(중요한 모델 생물)에서 액틴은 피질 패치, 액틴 케이블, 사이토키네틱 고리 및 캡을 형성한다.피질 패치는 세포막의 분리된 액틴체이며, 특히 세포벽 합성에 중요한 글루칸 합성효소의 재활용에 필수적이다.액틴 케이블은 액틴 필라멘트의 다발이며 세포 성장을 분극시키기 위해 많은 다른 단백질을 포함하고 있는 캡으로 소포를 운반하는 것과 미토콘드리아의 위치에 관여합니다.세포 분열 [37]부위 주위에서 세포 형성 및 수축합니다.
원핵세포골격
2001년 Jones et al.의 연구 이전에는 세포벽이 막대기와 나선형을 포함한 많은 박테리아 세포 형태의 결정적 요소라고 믿었다.연구했을 때, 많은 기형 박테리아가 세포 [38]외피의 발달과 관련된 돌연변이를 가지고 있는 것으로 밝혀졌다.세포골격은 한때 진핵세포만의 특징으로 생각되었지만, 진핵세포골격의 모든 주요 단백질에 대한 상동성이 원핵세포에서 [39]발견되었다.해롤드 에릭슨은 1992년 이전에는 진핵생물만이 세포골격 성분을 가지고 있는 것으로 생각되었다고 말한다.하지만 90년대 초반의 연구에 따르면 박테리아와 고세균은 액틴과 튜불린의 상동성을 가지고 있으며 이것들은 진핵 미세관이나 미세 필라멘트의 [40]기초라고 합니다.비록 진화적 관계가 너무 멀어서 단백질 배열 비교만으로는 명백하지 않지만, 세포 모양과 극성을 유지하는 3차원 구조와 유사한 기능의 유사성은 진핵세포와 원핵세포 골격체가 진정 [41]동질적이라는 강력한 증거를 제공한다.이미 박테리아 사이토키네시스(cytokinesis)의 핵심으로 알려진 단백질인 FtsZ가 모든 [40]α-, β-, γ-튜브린에 존재하는 "튜브린 시그니처 배열"을 가지고 있다는 것을 3개의 연구소가 독립적으로 발견했다.그러나 박테리아 세포골격의 일부 구조는 [25][42]아직 확인되지 않았을 수 있다.
FTSZ
FtsZ는 확인된 최초의 원핵 세포 골격 단백질이었다.튜브린과 마찬가지로 FtsZ는 구아노신 삼인산(GTP)의 존재 하에서 필라멘트를 형성하지만, 이러한 필라멘트는 튜브로 그룹화되지 않습니다.세포 분열 중에, FtsZ는 분열 부위로 이동하는 첫 번째 단백질이며, 분열 세포 사이의 새로운 세포벽을 합성하는 다른 단백질을 모집하는데 필수적이다.
MreB 및 Parm
MreB와 같은 원핵생물 액틴 유사 단백질은 세포 형태를 유지하는 데 관여합니다.모든 비구면 박테리아는 액틴 유사 단백질을 코드하는 유전자를 가지고 있으며, 이들 단백질은 세포막 아래에 세포벽 [43]생합성에 관여하는 단백질을 이끄는 나선형 네트워크를 형성한다.
일부 플라스미드는 액틴 유사 단백질 ParM을 포함하는 별도의 시스템을 인코딩합니다.ParM의 필라멘트는 동적 불안정성을 나타내며, 진핵세포 유사분열 [25][44]시 미소관에 의해 사용되는 것과 유사한 메커니즘에 의해 플라스미드 DNA를 분할하는 딸세포로 분할할 수 있다.
크레센틴
Caulobacter crescentus 박테리아는 진핵 세포의 중간 필라멘트와 관련이 있는 세 번째 단백질인 crescentin을 포함합니다.Crescentin은 또한 나선형이나 진동형 박테리아의 형태와 같은 세포 형태를 유지하는 데 관여하지만, 이것이 어떻게 하는지는 현재 [45]불분명합니다.또한 곡률은 펩티도글리칸 [46]합성이 중단된 후 초승달 필라멘트의 변위에 의해 설명될 수 있다.
세포골격과 세포역학
세포골격은 변화하는 세포 미세 환경에 대응하여 지속적으로 스스로를 개조하는 고도로 이방성 및 동적 네트워크입니다.네트워크는 구성 필라멘트를 차등적으로 중합 및 탈중합함으로써 세포 역학과 역학에 영향을 미칩니다(주로 액틴과 미오신이지만 미세관 및 중간 필라멘트가 [47]역할을 합니다).이것은 세포에 미세 환경을 알리는 데 중요한 역할을 하는 힘을 발생시킨다.구체적으로 장력, 강성 및 전단력과 같은 힘은 모두 세포 운명, 분화, 이동 [48]및 운동성에 영향을 미치는 것으로 나타났습니다."기계 전달"이라고 불리는 과정을 통해, 세포는 이러한 힘을 감지하고 반응하기 위해 세포 골격을 개조한다.
[기계 전달]은 기본적으로 세포 내 골격과 [세포 외 매트릭스](ECM)를 연결하는 [초점 접착]에 크게 의존한다.[초점접착]을 통해 세포는 초점접착에 존재하는 단백질이 구조변화를 일으켜 시그널링 캐스케이드를 개시함에 따라 세포외력을 세포내 힘에 통합할 수 있다.국소접착인산화효소(FAK)와 Src와 같은 단백질은 증식 및 분화와 같은 세포 활동에 반응하여 힘 신호를 전달하는 것으로 보여졌으며, 기계적 전달 [49]경로의 핵심 센서로 가정되어 있다.기계적 전달의 결과로서 세포골격은 힘 자극을 수용하고 그에 따라 세포가 반응하도록 구성 및/또는 방향을 변경한다.
세포골격은 감지된 힘에 반응하여 세포의 구조를 변화시킨다.예를 들어, 플라즈마막 내에서 장력이 증가하면 이온 채널이 열릴 가능성이 높아져 이온 전도도가 높아지고 세포 변화 이온 유입 또는 유출 가능성이 [50]높아집니다.게다가, 세포의 기계적 특성은 힘이 세포 전체에 얼마나 멀리, 어디로, 그리고 어떻게 세포 [51]역학을 바꿀지를 결정합니다.예를 들어 세포골격에 밀접하게 결합되지 않은 막단백질은 특별히 지시된 힘을 받는다면 피질액틴 네트워크에 큰 영향을 주지 않는다.그러나 세포골격과 더 밀접하게 연관된 막 단백질은 더 중요한 [52]반응을 유도할 것이다.이와 같이 세포골격의 이방성은 세포내 또는 세포외 신호에 대한 세포반응을 보다 예리하게 유도하는 역할을 한다.
장거리 주문
세포 골격이 힘을 감지하고 반응하는 구체적인 경로와 메커니즘은 아직 조사 중이다.그러나 세포골격에 의해 생성된 [장거리 순서]는 기계적 [53]전달에 기여하는 것으로 알려져 있다.지름이 10-50미크론 정도인 세포는 세포 활동을 조정하는 데 필수적인 세포질 내에서 발견되는 분자보다 수천 배 더 크다.세포는 필수 생체 분자에 비해 매우 크기 때문에 조직적인 네트워크가 없으면 세포질의 다른 부분이 [54]소통하는 것이 어렵다.게다가 생체분자는 세포의 길이에 버금가는 길이로 중합해야 하지만, 그 결과 발생하는 고분자는 매우 흐트러지고 세포질의 한 부분에서 다른 부분으로 효과적으로 신호를 전달할 수 없다.따라서, 폴리머를 조직하고 그것들이 세포 전체에 걸쳐 효과적으로 의사소통할 수 있도록 하기 위해 세포 골격이 필요하다.
원핵생물과 진핵생물의 공통 특징과 차이점
정의에 따르면, 세포골격은 모든 유기체에서 세로 배열(섬유)을 형성할 수 있는 단백질로 구성됩니다.이러한 필라멘트 형성 단백질은 4가지 등급으로 분류된다.튜브린 유사, 액틴 유사, 워커 A 세포골격 ATPase(WACA-단백질) 및 중간 필라멘트.[7][25]
튜불린 유사 단백질은 진핵생물에서는 튜불린, 원핵생물에서는 FtsZ, TubZ, RepX이다.액틴 유사 단백질은 진핵생물에서 액틴이고 MreB, FtSA는 원핵생물에서 액틴이다.원핵생물에서 주로 발견되는 WACA-단백질의 예는 MinD이다.동물(즉, 진핵생물)에서 거의 독점적으로 발견되는 중간 필라멘트의 예는 라민, 케라틴, 비멘틴, 신경 필라멘트 및 데스민이다.[7]
튜불린 유사 단백질은 아미노산 배열 유사성을 공유하지만, 단백질 접힘에서의 등가성과 GTP 결합 부위의 유사성은 더욱 두드러진다.액틴 유사 단백질과 그 구조 및 ATP 결합 [7][25]도메인에 대해서도 마찬가지다.
세포골격 단백질은 보통 원핵생물과 진핵생물의 세포 형태, DNA 분리 그리고 세포 분열과 관련이 있다.어떤 단백질이 어떤 작업을 수행하는지 매우 다릅니다.예를 들어, 모든 진핵생물에서 DNA 분리는 튜불린의 사용을 통해 일어나지만, 원핵생물에서는 WACA 단백질, 액틴 유사 단백질 또는 튜불린 유사 단백질을 사용할 수 있다.세포 분열은 진핵생물에서 액틴에 의해 매개되지만, 원핵생물에서는 보통 튜불린과 같은 (종종 FtsZ-고리) 단백질과 때로는 (Thermoproteota) ESCRT-II에 의해, 진핵생물에서는 여전히 [7]분열의 마지막 단계에서 역할을 한다.
세포질 스트리밍
세포질 흐름(cyclosis라고도 함)은 세포골격의 구성 요소를 따라 세포 내용물이 활발하게 움직이는 것입니다.주로 식물에서 볼 수 있는 반면, 모든 종류의 세포는 노폐물, 영양분, 그리고 세포 기관들을 세포의 다른 부분으로 운반하기 위해 이 과정을 사용합니다.[55] 식물과 조류 세포는 일반적으로 다른 많은 세포들보다 크다; 그래서 세포질 흐름은 이러한 종류의 세포에서 중요하다.이것은 세포의 여분의 부피가 [56]세포 전체를 통해 세포 소기관들을 움직이기 위해 세포질 스트리밍을 필요로 하기 때문입니다.유기체는 미오신 모터가 결합하고 액틴 필라멘트 [55]다발을 밀어내는 세포 골격의 미세 필라멘트를 따라 이동합니다.
「 」를 참조해 주세요.
레퍼런스
- ^ a b Hardin J, Bertoni G, Kleinsmith LJ (2015). Becker's World of the Cell (8th ed.). New York: Pearson. pp. 422–446. ISBN 978013399939-6.
- ^ McKinley, Michael; Dean O'Loughlin, Valerie; Pennefather-O'Brien, Elizabeth; Harris, Ronald (2015). Human Anatomy (4th ed.). New York: McGraw Hill Education. p. 29. ISBN 978-0-07-352573-0.
- ^ a b c d e Alberts B, et al. (2008). Molecular Biology of the Cell (5th ed.). New York: Garland Science. ISBN 978-0-8153-4105-5.
- ^ a b Herrmann H, Bär H, Kreplak L, Strelkov SV, Aebi U (July 2007). "Intermediate filaments: from cell architecture to nanomechanics". Nature Reviews. Molecular Cell Biology. 8 (7): 562–73. doi:10.1038/nrm2197. PMID 17551517. S2CID 27115011.
- ^ a b c Fletcher DA, Mullins RD (January 2010). "Cell mechanics and the cytoskeleton". Nature. 463 (7280): 485–92. Bibcode:2010Natur.463..485F. doi:10.1038/nature08908. PMC 2851742. PMID 20110992.
- ^ Geli MI, Riezman H (April 1998). "Endocytic internalization in yeast and animal cells: similar and different". Journal of Cell Science. 111 ( Pt 8) (8): 1031–7. doi:10.1242/jcs.111.8.1031. PMID 9512499.
- ^ a b c d e f Wickstead B, Gull K (August 2011). "The evolution of the cytoskeleton". The Journal of Cell Biology. 194 (4): 513–25. doi:10.1083/jcb.201102065. PMC 3160578. PMID 21859859.
- ^ a b Cooper, Geoffrey M. (2000). "Actin, Myosin, and Cell Movement". The Cell: A Molecular Approach. 2nd Edition. Archived from the original on 2018-04-28.
- ^ Berg JM, Tymoczko JL, Stryer L (2002). "Myosins Move Along Actin Filaments". Biochemistry. 5th Edition. Archived from the original on 2018-05-02.
- ^ Peters RA. "The Harben Lectures, 1929. Reprinted in: Peters, R. A. (1963) Biochemical lesions and lethal synthesis, p. 216. Pergamon Press, Oxford".
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ Frixione E (June 2000). "Recurring views on the structure and function of the cytoskeleton: a 300-year epic". Cell Motility and the Cytoskeleton. 46 (2): 73–94. doi:10.1002/1097-0169(200006)46:2<73::AID-CM1>3.0.CO;2-0. PMID 10891854. S2CID 16728876.
- ^ Hardin J (2015-12-03). Becker's World of the Cell (9th ed.). Pearson. p. 351. ISBN 978-0-321-93492-5.
- ^ Elsevier. "Discovery of Quantum Vibrations in "Microtubules" Inside Brain Neurons Corroborates Controversial 20-Year-Old Theory of Consciousness". www.elsevier.com. Archived from the original on 2016-11-07. Retrieved 2017-11-20.
- ^ Wickstead B, Gull K (August 2011). "The evolution of the cytoskeleton". The Journal of Cell Biology. 194 (4): 513–25. doi:10.1083/jcb.201102065. PMC 3160578. PMID 21859859.
- ^ Taran, AS; Shuvalova, LD; Lagarkova, MA; Alieva, IB (22 June 2020). "Huntington's Disease-An Outlook on the Interplay of the HTT Protein, Microtubules and Actin Cytoskeletal Components". Cells. 9 (6): 1514. doi:10.3390/cells9061514. PMC 7348758. PMID 32580314.
- ^ Minton AP (October 1992). "Confinement as a determinant of macromolecular structure and reactivity". Biophysical Journal. 63 (4): 1090–100. Bibcode:1992BpJ....63.1090M. doi:10.1016/S0006-3495(92)81663-6. PMC 1262248. PMID 1420928.
- ^ Doherty GJ, McMahon HT (2008). "Mediation, modulation, and consequences of membrane-cytoskeleton interactions". Annual Review of Biophysics. 37: 65–95. doi:10.1146/annurev.biophys.37.032807.125912. PMID 18573073. S2CID 17352662.
- ^ Pelucchi, Silvia; Stringhi, Ramona; Marcello, Elena (2020). "Dendritic Spines in Alzheimer's Disease: How the Actin Cytoskeleton Contributes to Synaptic Failure". International Journal of Molecular Sciences. 21 (3): 908. doi:10.3390/ijms21030908. ISSN 1422-0067. PMC 7036943. PMID 32019166.
- ^ Pellegrini L, Wetzel A, Grannó S, Heaton G, Harvey K (February 2017). "Back to the tubule: microtubule dynamics in Parkinson's disease". Cellular and Molecular Life Sciences. 74 (3): 409–434. doi:10.1007/s00018-016-2351-6. PMC 5241350. PMID 27600680.
- ^ Bamburg JR, Bloom GS (August 2009). "Cytoskeletal pathologies of Alzheimer's Disease". Cell Motility and the Cytoskeleton. 66 (8): 635–49. doi:10.1002/cm.20388. PMC 2754410. PMID 19479823.
- ^ Caviston JP, Holzbaur EL (April 2009). "Huntingtin protein is an essential integrator of intracellular vesicular trafficking". Trends in Cell Biology. 19 (4): 147–55. doi:10.1016/j.tcb.2009.01.005. PMC 2930405. PMID 19269181.
- ^ Julien JP, Millecamps S, Kriz J (2005). "Cytoskeletal Defects in Amyotrophic Lateral Sclerosis (motor neuron disease)". Novartis Foundation Symposium. 264: 183–92, discussion 192–6, 227–30. PMID 15773754.
- ^ Alberts, Bruce (2015). Molecular Biology of the Cell. Garland Science. p. 889. ISBN 978-0-8153-4464-3.
- ^ a b Cooper, Geoffrey M. (2000). "Structure and Organization of Actin Filaments". The Cell: A Molecular Approach. 2nd Edition. Archived from the original on 2018-05-02.
- ^ a b c d e Gunning PW, Ghoshdastider U, Whitaker S, Popp D, Robinson RC (June 2015). "The evolution of compositionally and functionally distinct actin filaments". Journal of Cell Science. 128 (11): 2009–19. doi:10.1242/jcs.165563. PMID 25788699.
- ^ Pan X, Hobbs RP, Coulombe PA (February 2013). "The expanding significance of keratin intermediate filaments in normal and diseased epithelia". Current Opinion in Cell Biology. 25 (1): 47–56. doi:10.1016/j.ceb.2012.10.018. PMC 3578078. PMID 23270662.
- ^ Herrmann H, Bär H, Kreplak L, Strelkov SV, Aebi U (July 2007). "Intermediate filaments: from cell architecture to nanomechanics". Nature Reviews. Molecular Cell Biology. 8 (7): 562–73. doi:10.1038/nrm2197. PMID 17551517. S2CID 27115011.
- ^ Paulin D, Li Z (November 2004). "Desmin: a major intermediate filament protein essential for the structural integrity and function of muscle". Experimental Cell Research. 301 (1): 1–7. doi:10.1016/j.yexcr.2004.08.004. PMID 15501438.
- ^ a b Lodish, Harvey; Berk, Arnold; Zipursky, S. Lawrence; Matsudaira, Paul; Baltimore, David; Darnell, James (2 May 2018). "Cilia and Flagella: Structure and Movement". Archived from the original on 2 May 2018. Retrieved 2 May 2018 – via www.ncbi.nlm.nih.gov.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ 해머로프, S, 펜로즈, R.Physical of Life Reviews 2014, 11, 39-78
- ^ a b 상자에 달리 명시되지 않은 한 참조는 다음과 같습니다:Boron WF (2003). Medical Physiology: A Cellular And Molecular Approaoch. Elsevier/Saunders. p. 1300. ISBN 978-1-4160-2328-9.
- ^ Fuchs E, Cleveland DW (January 1998). "A structural scaffolding of intermediate filaments in health and disease". Science. 279 (5350): 514–9. Bibcode:1998Sci...279..514F. doi:10.1126/science.279.5350.514. PMID 9438837.
- ^ Steinmetz MO (May 2007). "Structure and thermodynamics of the tubulin-stathmin interaction". Journal of Structural Biology. 158 (2): 137–47. doi:10.1016/j.jsb.2006.07.018. PMID 17029844.
- ^ a b Mostowy S, Cossart P (February 2012). "Septins: the fourth component of the cytoskeleton". Nature Reviews. Molecular Cell Biology. 13 (3): 183–94. doi:10.1038/nrm3284. PMID 22314400. S2CID 2418522.
- ^ Mascarelli A (December 2011). "Septin proteins take bacterial prisoners: A cellular defence against microbial pathogens holds therapeutic potential". Nature. doi:10.1038/nature.2011.9540. S2CID 85080734.
- ^ Huh GY, Glantz SB, Je S, Morrow JS, Kim JH (December 2001). "Calpain proteolysis of alpha II-spectrin in the normal adult human brain". Neuroscience Letters. 316 (1): 41–4. doi:10.1016/S0304-3940(01)02371-0. PMID 11720774. S2CID 53270680.
- ^ Pruyne D, Bretscher A (February 2000). "Polarization of cell growth in yeast". Journal of Cell Science. 113 ( Pt 4) (4): 571–85. doi:10.1242/jcs.113.4.571. PMID 10652251.
- ^ Jones, Laura J. F.; Carballido-López, Rut; Errington, Jeffery (2001-03-23). "Control of Cell Shape in Bacteria: Helical, Actin-like Filaments in Bacillus subtilis". Cell. 104 (6): 913–922. doi:10.1016/S0092-8674(01)00287-2. PMID 11290328. S2CID 14207533.
- ^ Shih YL, Rothfield L (September 2006). "The bacterial cytoskeleton". Microbiology and Molecular Biology Reviews. 70 (3): 729–54. doi:10.1128/MMBR.00017-06. PMC 1594594. PMID 16959967.
- ^ a b Erickson HP (February 2017). "The discovery of the prokaryotic cytoskeleton: 25th anniversary". Molecular Biology of the Cell. 28 (3): 357–358. doi:10.1091/mbc.E16-03-0183. PMC 5341718. PMID 28137947.
- ^ Michie KA, Löwe J (2006). "Dynamic filaments of the bacterial cytoskeleton" (PDF). Annual Review of Biochemistry. 75: 467–92. doi:10.1146/annurev.biochem.75.103004.142452. PMID 16756499.
- ^ Briegel A, Dias DP, Li Z, Jensen RB, Frangakis AS, Jensen GJ (October 2006). "Multiple large filament bundles observed in Caulobacter crescentus by electron cryotomography". Molecular Microbiology. 62 (1): 5–14. doi:10.1111/j.1365-2958.2006.05355.x. PMID 16987173.
- ^ Popp D, Narita A, Maeda K, Fujisawa T, Ghoshdastider U, Iwasa M, Maéda Y, Robinson RC (May 2010). "Filament structure, organization, and dynamics in MreB sheets". The Journal of Biological Chemistry. 285 (21): 15858–65. doi:10.1074/jbc.M109.095901. PMC 2871453. PMID 20223832.
- ^ Popp D, Narita A, Lee LJ, Ghoshdastider U, Xue B, Srinivasan R, Balasubramanian MK, Tanaka T, Robinson RC (June 2012). "Novel actin-like filament structure from Clostridium tetani". The Journal of Biological Chemistry. 287 (25): 21121–9. doi:10.1074/jbc.M112.341016. PMC 3375535. PMID 22514279.
- ^ Ausmees N, Kuhn JR, Jacobs-Wagner C (December 2003). "The bacterial cytoskeleton: an intermediate filament-like function in cell shape". Cell. 115 (6): 705–13. doi:10.1016/S0092-8674(03)00935-8. PMID 14675535. S2CID 14459851.
- ^ Esue, Osigwe (January 2010). "Dynamics of the Bacterial Intermediate Filament Crescentin In Vitro and In Vivo". PLOS ONE. 5 (1): e8855. Bibcode:2010PLoSO...5.8855E. doi:10.1371/journal.pone.0008855. PMC 2816638. PMID 20140233. Retrieved 12 September 2017.
- ^ Chen, Christopher S. (2008-10-15). "Mechanotransduction – a field pulling together?". Journal of Cell Science. 121 (20): 3285–3292. doi:10.1242/jcs.023507. ISSN 1477-9137. PMID 18843115. S2CID 1287523.
- ^ Chen, Christopher S. (2008-10-15). "Mechanotransduction – a field pulling together?". Journal of Cell Science. 121 (20): 3285–3292. doi:10.1242/jcs.023507. ISSN 1477-9137. PMID 18843115. S2CID 1287523.
- ^ Orr, A. Wayne; Helmke, Brian P.; Blackman, Brett R.; Schwartz, Martin A. (January 2006). "Mechanisms of Mechanotransduction". Developmental Cell. 10 (1): 11–20. doi:10.1016/j.devcel.2005.12.006. PMID 16399074.
- ^ Orr, A. Wayne; Helmke, Brian P.; Blackman, Brett R.; Schwartz, Martin A. (January 2006). "Mechanisms of Mechanotransduction". Developmental Cell. 10 (1): 11–20. doi:10.1016/j.devcel.2005.12.006. PMID 16399074.
- ^ Janmey, Paul A.; McCulloch, Christopher A. (2007-08-15). "Cell Mechanics: Integrating Cell Responses to Mechanical Stimuli". Annual Review of Biomedical Engineering. 9 (1): 1–34. doi:10.1146/annurev.bioeng.9.060906.151927. ISSN 1523-9829. PMID 17461730.
- ^ Orr, A. Wayne; Helmke, Brian P.; Blackman, Brett R.; Schwartz, Martin A. (January 2006). "Mechanisms of Mechanotransduction". Developmental Cell. 10 (1): 11–20. doi:10.1016/j.devcel.2005.12.006. PMID 16399074.
- ^ Fletcher, Daniel A.; Mullins, R. Dyche (January 2010). "Cell mechanics and the cytoskeleton". Nature. 463 (7280): 485–492. Bibcode:2010Natur.463..485F. doi:10.1038/nature08908. ISSN 0028-0836. PMC 2851742. PMID 20110992.
- ^ Mullins, R. D. (2010-01-01). "Cytoskeletal Mechanisms for Breaking Cellular Symmetry". Cold Spring Harbor Perspectives in Biology. 2 (1): a003392. doi:10.1101/cshperspect.a003392. ISSN 1943-0264. PMC 2827899. PMID 20182610.
- ^ a b Woodhouse FG, Goldstein RE (August 2013). "Cytoplasmic streaming in plant cells emerges naturally by microfilament self-organization". Proceedings of the National Academy of Sciences of the United States of America. 110 (35): 14132–7. arXiv:1308.6422. Bibcode:2013PNAS..11014132W. doi:10.1073/pnas.1302736110. PMC 3761564. PMID 23940314.
- ^ Goldstein RE, van de Meent JW (August 2015). "A physical perspective on cytoplasmic streaming". Interface Focus. 5 (4): 20150030. doi:10.1098/rsfs.2015.0030. PMC 4590424. PMID 26464789.
외부 링크
- Cytoskeleton 월간 뉴스 및 블로그
- MBInfo - 세포골격 역학
- 세포골격, 세포운동성 및 운동성 - 생화학, 분자생물학 및 세포생물학 가상 라이브러리
- 세포골격 데이터베이스, 임상시험, 최근 문헌, 실험실 등록부...
- 백혈구 접착 애니메이션(액틴 및 미세관 조립 및 역학 이미지를 이용한 애니메이션)
- http://cellix.imba.oeaw.ac.at/ 비디오를 포함한 세포골격 및 세포운동성
- 세포골격의 출현 복잡성에 대한 공개 접근 검토 기사(물리학의 진보, 2013년)