아미카신
Amikacin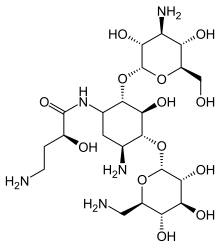 | |
 | |
| 임상자료 | |
|---|---|
| 상명 | 아미킨, 아미글리데V, 아리카이체 등 |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a68261 |
| 라이센스 데이터 | |
| 임신 범주 |
|
| 경로: 행정 | 근육질의 정맥주사. |
| 마약류 | 아미노글리코사이드 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 | |
| 약동학 데이터 | |
| 생체이용가능성 | >90%[3] |
| 단백질 결합 | 0–11% |
| 신진대사 | 대부분 측정되지 않음 |
| 제거 반감기 | 2~3시간 |
| 배설 | 신장 |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.048.653 |
| 화학 및 물리적 데이터 | |
| 공식 | C22H43N5O13 |
| 어금질량 | 585.608 g·1998−1 |
| 3D 모델(JSmol) | |
| |
| |
| (iii) | |
아미카신은 다수의 박테리아 감염에 사용되는 항생제다.[4] 여기에는 관절염, 복막내 감염, 뇌막염, 폐렴, 패혈증, 요로감염 등이 포함된다.[4] 다약 내성 결핵 치료에도 쓰인다.[5] 정맥주사를 이용하여 정맥에 주사하거나 근육에 주사하여 사용한다.[4]
아미카신은 다른 아미노글리코사이드 항생제와 마찬가지로 청력 손실, 균형 문제, 신장 질환 등을 일으킬 수 있다.[4] 다른 부작용으로는 마비가 일어나 호흡이 안 되는 경우도 있다.[4] 임신 중에 사용하면 아기에게 영구적인 귀머거리가 될 수 있다.[4][1] 아미카신은 박테리아의 30S 리보솜 소단위 기능을 차단해 단백질을 생산할 수 없게 하는 작용을 한다.[4]
아미카신은 1971년에 특허를 받았으며, 1976년에 상업적으로 사용되기 시작했다.[6][7] 그것은 세계보건기구의 필수 의약품 목록에 올라 있다.[8] 그것은 카나미신에서 유래되었다.[4]
의학적 용법
아미카신은 다약에 내성이 있고 유산소 그램 음성균으로 중증 감염을 치료하는 데 가장 많이 쓰이며 특히 녹농균, 아시네토박터, 엔테로박터, 대장균, 프로테우스, 클레비엘라, 세라티아 등이 있다.[9] 아미카신이 강하게 영향을 미치는 그램 양성균은 포도상구균과[9] 나초음파뿐이다.[10] 아미카신은 1차 약물이 감염을 억제하지 못할 때 비투혈성 균박테리아 감염과 결핵(감각성 균주로 인한 경우) 치료에도 사용할 수 있다.[4] 혼자 쓰는 경우는 드물다.[11]
그것은 종종 다음과 같은 상황에서 사용된다.[4]
- 기관지확장증[12]
- 뼈 및 관절염
- 그란울로시토페니아는, 티카실린과 결합했을 때, 암에[13] 걸린 사람들에게서,
- 클린다마이신, 메트로니다졸, 피페라실린/타조박탐 또는 앰피실린/술박탐과 같은 다른 약물에 대한 보조제로서의 복막내 감염(예: 복막염)
- 뇌막염:
- 이미페넴의 보조제로서 대장균에 의한 뇌막염의 경우.
- Meropenem의 보조제로서 Phyomonas에 의한 뇌막염의 경우.
- 이미페넴이나 콜리스틴의 보조제로서 아세토박터균에 의한 뇌막염의 경우.
- 앰피실린의 보조제로서 Streptococcus agalactiae 또는 리스테리아 모노키토제네스에 의해 야기된 신생아 뇌막염의 경우
- 3세대 세팔로스포린과 보조제로서 대장균과 같은 그램 음성균에 의한 신생아 뇌막염의 경우
- 활동성 결핵의 2선 요원으로서 포함한 미코박테리아 감염.[14] 또한 마이코박테리움 아비움, M. abcessus, M. chelonae, M. fortuitum에 의한 감염에도 사용된다.
- 결핵을 닮은 감염을 일으키는 로도코커스 에키
- 호흡기 감염(병원성 폐렴의 경우 베타 락탐 또는 카바페넴의 보조제로서 포함)
- 베타락탐이나 카바페넴의 부속물로 [9]신생아에 포함된 패혈증
- 피부 및 봉합 부위 감염[9]
- 덜 독성이 있는 약물에 내성이 있는 박테리아에 의해 발생하는 요로 감염(종종 엔토박테리아과 또는 P. 에어로기노사)
아미카신은 중성미자와 열이 있는 사람들을 위한 경험치료를 위해 베타락탐 항생제와 결합될 수 있다.[4]
사용 가능한 양식
아미카신은 하루에 한두 번 투여할 수 있으며, 분무를 통해 투여할 수 있지만 대개 정맥 또는 근내 경로에 의해 투여된다. 아미카신은 구강으로 흡수되지 않기 때문에 구강 형태가 없다. 신장 장애가 있는 사람의 경우 투여량은 대개 투약 빈도를 줄임으로써 크레아티닌 간극에 따라 조정되어야 한다.[9] 뇌막염과 같은 CNS 감염이 있는 사람에서는 아미카신을 뇌내(척추에 직접 주사)나 심실내(뇌의 심실내 주입)로 투여할 수 있다.[4]
미국에서 마이코박테리움 아비움 복합체(Mac)를 치료하기 위한 지질 흡입 중단도 이용할 수 있고 승인된다.[15][16] 유럽연합(EU)에서 아리카이체 신청이 철회된 것은 아리카이체 의약품위원회(CHMP)가 아리카이스의 혜택이 위험보다 크지 않다는 의견을 냈기 때문이다.[17]
특수인구
아미카신은 신장의 기능 저하를 자주 겪는 노약자와 신장이 아직 완전히 발달하지 않은 소아에서 더 적은 양으로 사용해야 한다. 미국과 호주에서 모두 임신 범주 D로 간주돼 태아에게 해를 끼칠 가능성이 있다는 뜻이다.[4] 아미카신의 약 16%가 태반을 가로지른다; 산모의 아미카신의 반감기는 2시간인 반면 태아는 3.7시간이다.[9] 또 다른 아미노글리코사이드와 함께 아미카신을 복용하는 임산부는 아이에게 선천적인 청각장애를 일으킬 가능성이 있다. 태반을 가로지르는 것으로 알려져 있지만, 아미카신은 모유에 부분적으로만 분비된다.[4]
일반적으로 아미카신은 유아에서 피해야 한다.[18] 유아도 아미노글리코사이드(aminoglycoside)가 있는 세포외액 농도가 높아 분포량이 큰 경향이 있다.[3]
노인들은 아미카신이 체내에 더 오래 머무르는 경향이 있다. 반면에 20세 아미카신의 평균 간격은 6 L/hr이고, 80세에서는 3 L/hr이다.[19]
낭포성 섬유증이 있는 사람들은 더더욱 간격이 높다.[20]
근위병이나 파킨슨병 등 근육장애가 있는 사람에서는 아미카신이 신경근육 접합에 미치는 마비효과가 근육의 허약성을 악화시킬 수 있다.[4]
역효과
아미카신의 부작용은 다른 아미노글리코사이드와 비슷하다. 사용자의 1~10%에서 발생하는 신장 손상과 이투독성(청력 손실로 이어질 수 있음)이 가장 중요한 영향이다.[12] 신장과 이독성은 아미노글리코사이드의 콩팥과 내이에 축적되는 경향 때문인 것으로 생각된다.[3]
아미카신은 복용량이 많거나 권장량보다 긴 경우 신경독성을 유발할 수 있다. 신경독성의 결과적인 효과는 현기증, 무감각, 피부의 따끔거림(마취), 근육 경련, 발작 등이 있다.[4] 8번째 두개골 신경에 대한 독성 효과는 이독성을 유발하여 균형을 잃고, 더 일반적으로 청력 손실을 초래한다.[3] 모세포의 강제적 사멸에 의해 발생하는 콜레아 손상은 고주파 청력 상실로 이어지고 임상 청력 상실을 감지하기 전에 발생한다.[9][21] 귀 전정 손상, 대부분 과도한 산화 활성산소를 생성하여 발생할 수 있음. 선량 의존적 방식이 아닌 시간 의존적 방식으로 그렇게 하는 것으로, 사용 기간을 줄임으로써 위험을 최소화할 수 있다는 것을 의미한다.[22]
아미카신은 근위부 신장 관에 작용하여 신독성(신장에 대한 손상)을 일으킨다. 그것은 쉽게 양이온으로 이온화되며 수용체 매개 피노시토스의 일부로서 근위부 관상세포의 음이온성 부위에 결합된다. 신피질 내 아미카신의 농도는 혈장 내 아미카신의 10배가 된다;[18] 그러면 그것은 라이소솜에서 인산염의 신진대사를 방해할 가능성이 높으며, 이는 리틱 효소가 세포질 속으로 유출되게 한다.[3] 네프로독성은 혈청 크레아티닌, 혈액 요소 질소, 적혈구, 백혈구 증가와 함께 알부미누리아(소변 내 알부민 생산량 증가), 글리코수리아(소변 내 포도당 배출량 증가), 소변 특이중력 감소, 과두리아(전체 소변 배출량 감소)를 초래한다.[9][21] 또한 요로 깁스가 나타나게 할 수도 있다.[3] 신관기능의 변화도 전해질 수준과 체내 산-베이스 밸런스를 변화시켜 저칼륨혈증과 산도증 또는 알칼리증을 유발할 수 있다.[22] 네프로독성은 항트로스타글랜딘을 복용하는 사람뿐만 아니라 기존에 존재하는 저칼륨혈증, 저칼륨혈증, 저칼로네세혈증, 산도증, 저글로머 여과율, 당뇨병, 탈수, 발열, 패혈증 등이 있는 사람들에게서 더 흔하다.[4][18][3][22] 독성은 보통 항생제 과정이 완료되면 되돌아가며,[3] 복용 빈도를 줄임으로써 완전히 피할 수 있다(8시간마다 한 번이 아니라 24시간마다 한 번).[18]
아미카신은 신경근막힘(급성 근육마비 포함)과 호흡마비(무호흡증 포함)를 유발할 수 있다.[4]
희귀 부작용(사용자의 1% 미만에서 발생)은 알레르기 반응, 피부 발진, 발열, 두통, 떨림, 메스꺼움 및 구토, 어시노필리아, 관절염, 빈혈, 저혈압, 저혈소혈증 등이다. (아미카신이 눈에 주입되는 곳) 미간주사에서는 황반경색이 영구적인 시력저하를 일으킬 수 있다.[9][12]
아미카신 지방흡입정지 처방은 과민성 폐염(폐염), 기관지경련(기도의 조임), 기저폐질환 악화, 혈액분해(혈액을 내뿜는 것) 등 호흡기 질환의 위험 증가와 관련한 상자 경고를 포함한다.경우에 따라서는 이온도 있다.[15][16] 아미카신 지방흡입정지를 복용하는 환자에게서 나타나는 다른 일반적인 부작용으로는 난독증(말하기 어려운 말), 기침, 이독성(손상된 청력), 상기도 자극, 근골격계 통증, 피로, 설사, 메스꺼움 등이 있다.[15][16]
콘트라인커뮤니케이션
아미카신은 교차알레르기 때문에 어떤 아미노글리코사이드에 민감한 사람에서는 피해야 한다(즉, 하나의 아미노글리코사이드에 대한 알레르기는 다른 아미노글리코사이드에 대한 과민성을 혼동하기도 한다). 대부분의 아미카신은 보통 알레르기 반응을 일으킬 수 있는 메타비설프산나트륨을 함유하고 있기 때문에 황산염에 민감한 사람(천식 환자들 사이에서 더 많이 나타난다)에서도 피해야 한다.[9][4]
일반적으로 아미카신은 신경독성, 이독성 또는 신독성을 유발할 수 있는 다른 약물과 함께 또는 바로 직전/후에 사용해서는 안 된다. 그러한 약물들에는 다른 아미노글리코사이드, 항바이러스 아키클로비르, 항정신병 암포테리신 B, 항생제 바시트라신, 카프레오마이신, 콜리스틴, 폴리믹신 B, 반코마이신 등이 있다. 그리고 화학요법에 사용되는 시스플라틴도 포함된다.[4]
아미카신은 근육 약화와 마비를 증가시킬 수 있으므로 신경근 차단제와 함께 사용하면 안 된다.[4]
상호작용
아미카신은 다른 아미노글리코사이드로는 아니지만 다른 베타락탐에 의해 비활성화될 수 있으며, 페니실린(베타락탐의 일종)과 일부 그램 양성 박테리아에 대해 시너지 효과를 낼 수 있는 카바페넴과 함께 여전히 자주 사용된다. 또 다른 베타 락탐 그룹인 세팔로스포린은 아미노글리코사이드의 신독성을 증가시킬 수 있을 뿐만 아니라 크레아티닌 수치를 무작위로 상승시킬 수 있다. 클로로페니콜, 클린다마이신, 테트라시클린 항생제는 약리학적 반작용에 의해 아미노글리코시드를 일반적으로 불활성화하는 것으로 알려져 있다.[4]
아미카신의 효과는 보툴리눔 톡신,[12] 마취제, 신경근 차단제 또는 항응고제로 구연산물이 함유된 다량의 혈액에서 유래한 약물과 함께 사용하면 증가한다.[4]
강력한 이뇨제는 스스로 이투독성을 일으킬 뿐만 아니라 혈청과 조직의 아미카신 농도를 높일 수 있어 이투독성을 더욱 높일 수 있다.[4] 키니딘은 또한 체내의 아미카신 수치를 증가시킨다.[12] NSAID Indomethacin은 미숙아의 혈청 아미노글리코사이드 수치를 증가시킬 수 있다.[4] 아이오베르솔과 같은 조영제는 아미카신에 의한 신독성과 난독성을 증가시킨다.[12]
아미카신은 약리학적 대항제 역할을 함으로써 살아있는 BCG 백신(결핵에 사용됨), 콜레라 백신, 살아있는 장티푸스 백신과 같은 특정 백신의 효과를 줄일 수 있다.[12]
약리학
작용기전
아미카신은 원핵산 리보솜 30S 서브유닛의 16S rRNA와 RNA 결합 S12 단백질에 불가역적으로 결합하고, 리보솜의 모양을 바꾸어 mRNA 코돈을 올바르게 읽을 수 없도록 하여 단백질 합성을 억제한다.[9][23] 또한 tRNA 안티코돈의 흔들거리는 베이스와 상호작용하는 영역을 방해한다.[24] 농도에 의존하는 방식으로 작동하며 알칼리성 환경에서 더 좋은 작용을 한다.[3]
정상 용량에서 아미카신에 민감한 박테리아는 24-48시간 이내에 반응한다.[9]
저항
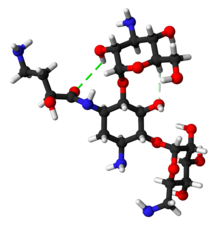
아미카신은 아미노아세틸전달효소와 뉴클레오티딜전달효소를 제외한 박테리아 내 항생제 내성을 담당하는 모든 항생제 불활성화 효소의 공격을 회피한다.[25] 이는 N-1에 부착된 L-하이드록시아미노부테로이드(L-HABA) moiety에 의해 수행되며(단순히 수소가 있는 카나마이신과 비교) 접근을 차단하고 아미노글리코사이드 활성 효소의 친화력을 감소시킨다.[25][26][27] 아미카신은 결국 이들 효소가 공격할 수 있는 부위는 1개뿐이고 겐타미닌과 토브라마이신은 6개다.[11]
스트렙토마이신과 카프레오마이신에 내성이 있는 박테리아는 여전히 아미카신에 취약하다; 카나미신에 내성이 있는 박테리아는 아미카신에 대한 감수성이 다양하다. 아미카신에 대한 저항은 또한 카나미신과 카프레오마이신에 대한 저항성을 내포한다.[28]
결핵의 원인물질인 마이코박테리움에서 아미카신과 카나미신에 대한 저항은 16S rRNA를 암호화하는 rrs 유전자의 돌연변이 때문이다. 이와 같은 돌연변이는 박테리아의 리보솜에 대한 아미카신의 결합 친화력을 감소시킨다.[29] Variations of aminoglycoside acetyltransferase (AAC) and aminoglycoside adenylyltransferase (AAD) also confer resistance: resistance in Pseudomonas aeruginosa is caused by AAC(6')-IV, which also confers resistance to kanamycin, gentamicin, and tobramycin, and resistance in Staphylococcus aureus and S. epidermidis is caused by AAD(4',4), which also 카나미신, 토브라마이신, 그리고 아프라마이신에게 저항을 가한다.[26] S. aureus의 일부 변종은 아미카신을 인산화하여 비활성화할 수도 있다.[13]
약동학
아미카신은 구강으로 흡수되지 않기 때문에 parenteral로 투여해야 한다. 근육내 투여 시 0.5~2시간 만에 혈청 농도가 최고치에 도달한다. 아미카신의 11% 미만이 실제로 혈장 단백질에 결합한다. 심장, 담낭, 폐, 뼈뿐만 아니라 담즙, 가래, 간액, 흉수, 시신액에도 분포한다. 뇌척수액은 대개 심실내 투여를 제외하고 낮은 농도에서 발견된다.[4] 유아에서 아미카신은 보통 척수액 내 혈장수치의 10~20%에서 발견되지만 뇌막염의 경우 그 양이 50%에 이른다.[9] 혈액뇌장벽을 쉽게 넘거나 안구조직으로 들어가지 않는다.[3]
아미카신의 반감기는 보통 2시간인 반면, 말기 신장질환자는 50시간이다.[11]
IM 또는 IV 투여량에서 아미카신의 대부분(95%)은 24시간 이내에 글로머 여과와 소변으로 변경되지 않고 분비된다.[4][11] 아미카신이 소변을 통해 배설되는 요인은 비교적 낮은 분자량, 높은 용해성, 비금속화 상태 등이다.[18]
화학
수의학용
반면 amikacin 개들의 사용만 승인과 말에서 자궁 내 감염을 위한 것이라고 합니다, 그것이 하나의 가장 흔한 aminoglycosides 수의 medicine,[32]에서 사용되고 개, 고양이, 기니 피그, chinchillas, 햄스터, 쥐, 생쥐, 프레리 도그, 가축, 새, 뱀, 거북이 그리고 거북이들, 악어류, 황소 개구리, 다른 생선에 사용되어 왔다.[3][33][34] 뱀의 호흡기 감염, 거북이의 박테리아 껍질 질환, 마코우의 축농증 등에 자주 쓰인다. 일반적으로는 장내 미세플로라의 균형을 해치기 때문에 토끼와 산토끼로 억제된다(아직도 사용되어 왔지만).[3]
개와 고양이에서는 아미카신이 귀염, 각막궤양, 특히 녹농균에 의해 생기는 국소 항생제로 많이 쓰인다. 고름과 세포 찌꺼기는 아미카신의 활동을 감소시키기 때문에 종종 약을 투여하기 전에 귀를 청소한다.[32] 아미카신은 안과 연고나 용액으로 준비했을 때, 또는 부주사를 맞았을 때 눈에 투여된다.[35] 눈의 아미카신은 세파졸린을 동반할 수 있다. 아미카신(및 모든 아미노글리코사이드)은 사용함에도 불구하고 안구 내 구조물에 독성이 있다.[36]
말에서 아미카신은 취약한 박테리아에 의해 야기될 때 자궁내막염(내막증, 피오메트라 등)에 대해 FDA 승인을 받는다.[37] 그것은 또한 눈과 관절경 변기에 대한 국소적인 약에도 사용된다; 세팔로스포린과 결합하면 포도상구균에 의해 야기되는 피하 감염을 치료하는데 사용된다. 팔다리나 관절의 감염에 대해서는 사지 관류를 통해 사지로 직접 투여하거나 관절에 주입하는 경우가 많다.[32][38] 아미카신은 또한 감염을 예방하기 위해 항관절제인 아쿠잔과 관절에 주입된다.[39]
동물의 부작용으로는 신독성, 이독성, IM 주사 현장의 알레르기 반응 등이 있다. 고양이는 이투독성으로 인한 전정 손상에 더 민감하게 반응하는 경향이 있다. 부작용이 덜 빈번하게 나타나는 것은 신경근육 봉쇄, 안면부종, 말초신경증 등이다.[3][32]
대부분의 동물의 반감기는 1~2시간이다.[40]
아미카신의 과다 복용을 치료하려면 신장 투석이나 복막 투석이 필요하며, 혈청 농도를 낮추는 아미카신 및/또는 페니실린 중 일부는 이를 비활성화하는 아미카신과 콤플렉스를 형성할 수 있다.[3]
지질 흡입 서스펜션
아미카신 지방흡입정지는 항균제 및 항균제(LPAD 경로)에 대한 미국 제한적 모집단 경로에 따라 승인된 첫 의약품이다.[15] 또한 가속화된 승인 경로 하에서 승인되었다.[15] 미국 식품의약국(FDA)은 아미카신 지포솜 흡입정지 패스트트랙, 돌파요법, 우선순위 검토, 적격 감염병 제품(QIDP) 지정 신청을 허가했다.[15] FDA는 Arikayce의 승인을 Insmed, Insmed, Inc.에 승인했다.[15]
분무기를 통해 섭취한 흡입 치료제인 아미카신 지방흡입 정지의 안전성과 효능은 두 치료군 중 한 곳에 환자를 배정하는 무작위 조정 임상실험에서 입증됐다.[15] 한 그룹의 환자들은 아미카신 지방흡입 중단과 함께 배경 다의약품 항균성 식이요법을 받았고, 다른 치료 그룹은 배경 다의약품 항균성 식이요법을 단독으로 받았다.[15] 치료 6개월까지 아미카신 지방흡입정지로 치료받은 환자의 29%가 3개월 연속 가래 배양균에서 마이코박테리아 성장을 하지 못한 반면 아미카신 지방흡입정지로 치료받지 못한 환자는 9%에 달했다.[15]
참조
- ^ a b c "Amikacin Use During Pregnancy". Drugs.com. 2 December 2019. Retrieved 13 March 2020.
- ^ "Amikacin 250 mg/ml Injection - Summary of Product Characteristics (SmPC)". (emc). 16 September 2015. Retrieved 13 March 2020.
- ^ a b c d e f g h i j k l m n Plumb, Donald C. (2011). "Amikacin Sulfate". Plumb's Veterinary Drug Handbook (7th ed.). Stockholm, Wisconsin; Ames, Iowa: Wiley. pp. 39–43. ISBN 978-0-470-95964-0.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa "Amikacin Sulfate". The American Society of Health-System Pharmacists. Archived from the original on 20 December 2016. Retrieved 8 December 2016.
- ^ World Health Organization (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). WHO Model Formulary 2008. World Health Organization. p. 137. hdl:10665/44053. ISBN 9789241547659.
- ^ Fischer, Janos; Ganellin, C. Robin (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 507. ISBN 9783527607495. Archived from the original on 20 December 2016.
- ^ Oxford Handbook of Infectious Diseases and Microbiology. OUP Oxford. 2009. p. 56. ISBN 9780191039621. Archived from the original on 24 November 2015.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ a b c d e f g h i j k l m "Amikacin sulfate injection, solution". DailyMed. 10 April 2019. Retrieved 13 March 2020.
- ^ Scholar, Eric M.; Pratt, William B. (22 May 2000). The Antimicrobial Drugs (2nd ed.). Oxford University Press, USA. pp. 15–19. ISBN 978-0-19-975971-2. Archived from the original on 10 September 2017.
- ^ a b c d Cunha, Burke A. (1 November 2006). "New Uses for Older Antibiotics: Nitrofurantoin, Amikacin, Colistin, Polymyxin B, Doxycycline, and Minocycline Revisited". Medical Clinics of North America. Antimicrobial Therapy. 90 (6): 1089–1107. doi:10.1016/j.mcna.2006.07.006. ISSN 0025-7125. PMID 17116438.
- ^ a b c d e f g "amikacin (Rx)". Medscape. WebMD. Archived from the original on 9 August 2017. Retrieved 9 August 2017.
- ^ a b Aronson J. K., ed. (2016). "Amikacin". Meyler's Side Effects of Drugs (16th ed.). Oxford: Elsevier. pp. 207–209. ISBN 978-0-444-53716-4.
- ^ Vardanyan, Ruben; Hruby, Victor (2016). "Chapter 32: Antimicobacterial Drugs". Synthesis of Best-Seller Drugs. Boston: Academic Press. pp. 669–675. ISBN 978-0-12-411492-0.
- ^ a b c d e f g h i j "FDA approves a new antibacterial drug to treat a serious lung disease using a novel pathway to spur innovation". U.S. Food and Drug Administration (FDA) (Press release). Retrieved 12 November 2018.
 이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다..
이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다.. - ^ a b c "Arikayce- amikacin suspension". DailyMed. 30 September 2018. Retrieved 13 March 2020.
- ^ "Arikayce: Withdrawn application". European Medicines Agency (EMA). 14 October 2016. Retrieved 13 March 2020.
- ^ a b c d e Ettinger, Stephen J.; Feldman, Edward C. (24 December 2009). Textbook of Veterinary Internal Medicine. Elsevier Health Sciences. pp. 1976, 523. ISBN 978-1-4377-0282-8. Archived from the original on 10 September 2017.
- ^ Maire, P.; Bourguignon, L.; Goutelle, S.; Ducher, M.; Jelliffe, R. (2017). "Chapter 20 - Individualizing Drug Therapy in the Elderly". Individualized Drug Therapy for Patients. Boston: Academic Press. pp. 373–382. ISBN 978-0-12-803348-7.
- ^ Eghianruwa, Kingsley (2014). Essential Drug Data for Rational Therapy in Veterinary Practice. Author House. p. 16. ISBN 978-1-4918-0000-3. Archived from the original on 10 September 2017.
- ^ a b Morris, Daniel O.; Kennis, Robert A. (11 October 2012). Clinical Dermatology, An Issue of Veterinary Clinics: Small Animal Practice, E-Book. Elsevier Health Sciences. p. 29. ISBN 978-1-4557-7377-0. Archived from the original on 10 September 2017.
- ^ a b c Corti, Natascia; Taegtmeyer, Anne; Imhof, Alexander (1 January 2011). "Miscellaneous antibacterial drugs". Side Effects of Drugs Annual. A worldwide yearly survey of new data in adverse drug reactions. 33: 509–540. doi:10.1016/B978-0-444-53741-6.00026-X. ISBN 9780444537416. ISSN 0378-6080.
- ^ Bauman, Robert W. (2015). Microbiology: with diseases by body system (4th ed.). Boston: Pearson. ISBN 978-0-321-91855-0.
- ^ "Amikacin". DrugBank. 2 August 2017. Archived from the original on 16 August 2017. Retrieved 10 August 2017.
- ^ a b Mudd, Efrain (7 August 2017). "O Aminoglycosides". Pharmacological Sciences. Archived from the original on 16 August 2017. Retrieved 14 August 2017.
- ^ a b Kondo, Shinichi; Hotta, Kunimoto (1 January 1999). "Semisynthetic aminoglycoside antibiotics: Development and enzymatic modifications". Journal of Infection and Chemotherapy. 5 (1): 1–9. doi:10.1007/s101560050001. ISSN 1341-321X. PMID 11810483. S2CID 38981498.
- ^ Park, Je Won; Ban, Yeon Hee; Nam, Sang-Jip; Cha, Sun-Shin; Yoon, Yeo Joon (1 December 2017). "Biosynthetic pathways of aminoglycosides and their engineering". Current Opinion in Biotechnology. Chemical biotechnology: Pharmaceutical biotechnology. 48: 33–41. doi:10.1016/j.copbio.2017.03.019. ISSN 0958-1669. PMID 28365471.
- ^ Caminero, José A; Sotgiu, Giovanni; Zumla, Alimuddin; Migliori, Giovanni Battista (1 September 2010). "Best drug treatment for multidrug-resistant and extensively drug-resistant tuberculosis". The Lancet Infectious Diseases. 10 (9): 621–629. doi:10.1016/S1473-3099(10)70139-0. ISSN 1473-3099. PMID 20797644.
- ^ Ahmad, Suhail; Mokaddas, Eiman (1 March 2014). "Current status and future trends in the diagnosis and treatment of drug-susceptible and multidrug-resistant tuberculosis". Journal of Infection and Public Health. 7 (2): 75–91. doi:10.1016/j.jiph.2013.09.001. ISSN 1876-0341. PMID 24216518.
- ^ Kawaguchi, H.; Naito, T.; Nakagawa, S.; Fujisawa, K. I. (December 1972). "BB-K 8, a new semisynthetic aminoglycoside antibiotic". The Journal of Antibiotics. 25 (12): 695–708. doi:10.7164/antibiotics.25.695. ISSN 0021-8820. PMID 4568692. Archived from the original on 16 August 2017.
- ^ Monteleone, Peter M.; Muhammad, Naseem; Brown, Robert D.; McGrory, John P.; Hanna, Samir A. (1 January 1983). Amikacin Sulfate. Analytical Profiles of Drug Substances. Vol. 12. pp. 37–71. doi:10.1016/S0099-5428(08)60163-X. ISBN 9780122608124. ISSN 0099-5428.
- ^ a b c d Forney, Barbara. "Amikacin for Veterinary Use". Wedgewood Pharmacy. Archived from the original on 16 August 2017. Retrieved 9 August 2017.
- ^ Riviere, Jim E.; Papich, Mark G. (13 May 2013). Veterinary Pharmacology and Therapeutics. John Wiley & Sons. p. 931. ISBN 978-1-118-68590-7. Archived from the original on 10 September 2017.
- ^ Mader, Douglas R.; Divers, Stephen J. (12 December 2013). Current Therapy in Reptile Medicine and Surgery - E-Book. Elsevier Health Sciences. p. 382. ISBN 978-0-323-24293-6. Archived from the original on 10 September 2017.
- ^ Maggs, David; Miller, Paul; Ofri, Ron (7 August 2013). Slatter's Fundamentals of Veterinary Ophthalmology - E-Book. Elsevier Health Sciences. p. 37. ISBN 978-0-323-24196-0. Archived from the original on 10 September 2017.
- ^ Hsu, Walter H. (25 April 2013). Handbook of Veterinary Pharmacology. John Wiley & Sons. p. 486. ISBN 978-1-118-71416-4.
- ^ US National Library of Medicine (9 March 2017). "Amiglyde-V- amikacin sulfate injection". DailyMed. Archived from the original on 16 August 2017. Retrieved 8 August 2017.
- ^ Orsini, James A. (1 August 2017). "Update on Managing Serious Wound Infections in Horses: Wounds Involving Joints and Other Synovial Structures". Journal of Equine Veterinary Science. 55: 115–122. doi:10.1016/j.jevs.2017.01.016. ISSN 0737-0806.
- ^ Wanamaker, Boyce P.; Massey, Kathy (25 March 2014). Applied Pharmacology for Veterinary Technicians - E-Book. Elsevier Health Sciences. p. 392. ISBN 978-0-323-29170-5.
- ^ Papich, Mark G. (October 2015). "Amikacin". Saunders Handbook of Veterinary Drugs: Small and Large Animal (4th ed.). Elsevier Health Sciences. pp. 25–27. ISBN 978-0-323-24485-5. Archived from the original on 10 September 2017.
외부 링크
- "Amikacin". Drug Information Portal. U.S. National Library of Medicine.
- "Amikacin sulfate". Drug Information Portal. U.S. National Library of Medicine.