올란도마이신
Oleandomycin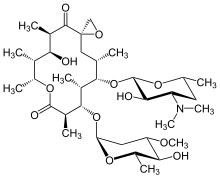 | |
| 임상자료 | |
|---|---|
| AHFS/Drugs.com | 국제 마약 이름 |
| ATC 코드 | |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 켐스파이더 | |
| 유니 | |
| 켐벨 | |
| E 넘버 | E704(항생균제) |
| CompTox 대시보드 (EPA) | |
| ECHA InfoCard | 100.021.360 |
| 화학 및 물리적 데이터 | |
| 공식 | C35H61NO12 |
| 어금질량 | 687.868 g·1998−1 |
| 3D 모델(JSmol) | |
| |
| |
| | |
올레안도마이신은 마크로라이드 항생제다.그것은 스트렙토미세스 항생제의 변종에서 합성된다.에리트로마이신보다 약하다.null
테트라시클린과 결합하여 지그마미신이라는 브랜드명으로 판매되곤 했으며, 프랑스 로사-피로토파마사가 제작하였다.null
의료 사용 및 가용성
올레안도마이신은 에리트로마이신 캔처럼 상부 호흡기에 감염을 일으키는 박테리아의 활동을 억제하기 위해 고용될 수 있다.둘 다 포도상구균과 엔테로코쿠스 생성에 영향을 줄 수 있다.null
올레안도마이신 MIC는 황색포도상구균의 경우 0.3-3µg/ml이다.[1]null
Oleandomycin은 일부 국가에서 수의학 항생제로 승인되었다.그것은 미국에서 돼지 및 가금류 항생제로 승인되었다.그러나 현재 미국에서만 생산용으로 승인되고 있다.[2][3]null
브랜드명
- Mastalone – Oleandomycin, oxatetracycline, neomycin – Zoetis Australia 및 Pfizer Animal Health
- 마스티구아드 – 올란도마이신, 옥사테트라사이클린 – 스톡가드 동물 건강[4]
- 이전에 Pfizer에 의해 지그마미신(Oleandomycin + Tetracycline + 비타민 C)으로 판매되었다.
역사
오리진스
올레안도마이신은 1954년 소빈 박사와 영어, 셀머 박사에 의해 스트렙토미세스 항생제의 산물로 처음 발견되었다.1960년에 호크슈타인은 올레안도마이신의 구조를 성공적으로 결정하는데 성공했다.이 마크로롤라이드는 친척인 에리트로마이신, 스피라마마이신과 비슷한 시기에 발견되었다.[5]null
콤비네이션 약물 지그마미신
올레안도마이신(Oleandomycin)에 대한 대중의 관심은 1956년 화이저가 콤비네이션 약품 지그마미신을 시장에 선보이면서 절정에 달했다.지그마미신은 올레안도마이신(Oleandomycin)과 테트라시클린을 혼합한 약으로 주요 마케팅 캠페인의 지원을 받았다.실제로 테트라사이클린과 올레안도마이신을 2:1로 혼합한 것이 포도상구균에 시너지 효과를 낸다는 주장이었다.또한 이 혼합물이 테트라사이클린이나 올레안도마이신에만 대부분 내성이 있는 유기체에 효과적일 것이라는 주장도 나왔다.이 두 주장 모두 로렌스 P. 가로드의 주장과 같은 조사 결과에 의해 반박되었는데, 그러한 주장이 적절하게 입증되었다는 증거를 찾을 수 없었다.[5]1970년대 초까지 화이저의 콤비네이션 약품은 시장에서 철수되었다.[6] [7] [8]
약리학
작용기전
Oleandomycin은 박테리오스테틱제다.에리트로마이신처럼 올레안도마이신은 박테리아 리보솜의 50년대 서브유닛에 결합해 생존과 복제에 필수적인 단백질의 완성을 억제한다.그것은 번역 활동뿐만 아니라 50년대 서브 유닛 형성을 방해한다.null
그러나 에리트로마이신이나 그 효능이 있는 합성파생물과 달리 12하이드록실 그룹과 3메톡시 그룹이 부족하다.이러한 구조의 변화는 50S 구조와의 상호작용에 악영향을 미칠 수 있으며 왜 그것이 덜 강력한 항생제인지 설명해준다.[9]null
상대 강도
올레안도마이신은 포도상구균이나 장내구균을 포함하는 세균 최소 억제농도 검사에서 에리트로마이신보다 훨씬 덜 효과적이다.[1]그러나, 마크로라이드 항생제는 장기나 세포에 축적될 수 있으며, 이 효과는 혈장 내 농도가 치료 효과가 있다고 여겨지는 것보다 낮더라도 이 종류의 항생제의 생체 활동을 연장시킬 수 있다.null
화학
폴리케티드 합성
OLES(Oleandomycin synthase)는 I형 싱타제의 모듈 구조를 따른다.폴리케타이드 체인은 티오에스터 링크를 통해 ACP 및 KS 도메인의 S-H 그룹에 결합된다(표시되지 않음).null
- 0-2 모듈의 유전자 클러스터 OLES1 코드, 아세틸-CoA 스타터 유닛을 포함하는 모듈 0 및 케토 신타아제 유닛에 부착된 메틸 말론릴-CoA 신장 단위를 포함하는 모든 나머지 모듈.
- 모듈 3 및 4의 OLES2 코드.모듈 3은 탄소 8에 인접한 감소되지 않은 카보닐을 유지하는 역할을 하는 리독스-비활성 케토렐라제를 잠재적으로 운반하는 것으로 유명하다.
- 모듈 5 및 6에 대한 OLES3 코드.
OLES와 6-Deoxyerythronolide B synthase(에리트로마이신 전구체 시네타제)의 아미노산 시퀀스 유사성은 45%의 공통 정체성만을 보여준다.에리트로마이신 전구체 싱타아제와는 달리 OLES 로딩 영역에는 KS가 있다.[10]null
포스트 PKS 테일러링
올레G1과 G2 유전자는 올레안도마이신의 특징적인 당분을 마크로라이드에 부착하는 글리코실전달효소를 담당한다.이 당들은 TDP-글루코오스로부터 유래되었다.OLEG1은 dTDP-D-desoamine을, OleG2는 D-TDP-L-oleandrose를 마크로라이드 링으로 전송한다.이후에 발생하는 에폭시드는 OleP가 인코딩한 효소에서 나온 것으로 P450 효소와 동질적일 수 있다.OleP 에폭시디트가 디하이드록시틸화(dihydroxylation)로 의심받는 방법은 히드록실 그룹을 인산염 그룹으로 변환한 다음 다른 히드록실 그룹에 의한 핵포필 링 폐쇄를 통해 떠난다.[10]null
참조
- ^ a b Semenitz E (September 1978). "The antibacterial activity of oleandomycin and erythromycin--a comparative investigation using microcalorimetry and MIC determination". The Journal of Antimicrobial Chemotherapy. 4 (5): 455–7. doi:10.1093/jac/4.5.455. PMID 690046.
- ^ "Drugs Transitioning from Over‐the‐Counter (OTC) to Veterinary Feed Directive (VFD) Status" (PDF). U.S Food and Drug Administration. 19 Jan 2016. Retrieved 11 May 2016.
- ^ "21 CFR 558.435 - Oleandomycin". Legal Information Institute. Cornell University Law School. 17 Sep 2001. Retrieved 11 May 2016.
- ^ "Oleandomycin". Drugs.com. 16 April 2010. Retrieved 11 May 2016.
- ^ a b Garrod LP (July 1957). "The erythromycin group of antibiotics". British Medical Journal. 2 (5036): 57–63. doi:10.1136/bmj.2.5036.57. JSTOR 25383104. PMC 1961747. PMID 13436854.
- ^ Podolsky SH, Greene JA (August 2011). "Combination drugs--hype, harm, and hope". The New England Journal of Medicine. 365 (6): 488–91. doi:10.1056/NEJMp1106161. PMID 21830965.
- ^ Jones WF, Finland M (September 1957). "Antibiotic combinations; tetracycline, erythromycin, oleandomycin and spiramycin and combinations of tetracycline with each of the other three agents; comparisons of activity in vitro and antibacterial action of blood after oral administration". The New England Journal of Medicine. 257 (12): 536–47 concl. doi:10.1056/NEJM195709192571202. PMID 13464978.
- ^ Pfizer Inc v. L. Richardson c.,434 vF.2D 536, 8(미국 항소법원, 1970년 11월 2일 제2 순회).
- ^ Champney WS, Tober CL, Burdine R (December 1998). "A comparison of the inhibition of translation and 50S ribosomal subunit formation in Staphylococcus aureus cells by nine different macrolide antibiotics". Current Microbiology. 37 (6): 412–7. doi:10.1007/s002849900402. PMID 9806980.
- ^ a b Rawlings BJ (June 2001). "Type I polyketide biosynthesis in bacteria (part B)". Natural Product Reports. 18 (3): 231–81. doi:10.1039/b100191o. PMID 11476481.




