산화아연
Zinc oxide | |
| 이름들 | |
|---|---|
| 기타이름 아연백색, 칼라민, 철학자의 양모, 중국백색, 아연의 꽃 | |
| 식별자 | |
3D 모델(JSMO) | |
| ChEBI | |
| 쳄블 | |
| 켐스파이더 | |
| 드럭뱅크 | |
| ECHA 인포카드 | 100.013.839 |
| EC 번호 |
|
| 13738 | |
| 케그 | |
펍켐 CID | |
| RTECS 번호 |
|
| 유니아이 | |
| UN번호 | 3077 |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| ZnO | |
| 어금니 질량 | 81.406g/mol[1] |
| 외모 | 흰색실체[1] |
| 냄새 | 무취 |
| 밀도 | 5.6g/cm3[1] |
| 융점 | 1,974°C (3,585°F; 2,247K) (붕괴)[1][7] |
| 비등점 | 2,360°C (4,280°F; 2,630K) (분해) |
| 0.0004%(17.8°C)[2] | |
| 밴드갭 | 3.2 eV(직접)[3] |
| 전자이동성 | 180cm2/(V·s)[3] |
| -27.2·10cm−63/mol[4] | |
| 열전도율 | 0.6 W/(cm·K)[5] |
굴절률(nD) | n=2.013, n=2.029 |
| 구조[8] | |
| 워르쯔테 | |
| C6v4-P63mc | |
a = 3.2495 Å, c = 5.2069 Å | |
공식 단위 (Z) | 2 |
| 사면체 | |
| 열화학[9] | |
열용량 (C) | 40.3 J·K몰−1−1 |
어금니 엔트로피 (S⦵298) | 43.65±0.40 J·K−1mol−1 |
스덴탈피 형성 (δ) | -350.46±0.27kJ mol−1 |
깁스 자유 에너지 (δ그) | -320.5 kJ mol−1 |
핵융합 엔탈피 (δ) | 70kJ/mol |
| 약리학 | |
| QA07XA91 (WHO) | |
| 유해성 | |
| GHS 라벨링: | |
 | |
| 경고문 | |
| H400, H401 | |
| P273, P391, P501 | |
| NFPA 704 (파이어다이아몬드) | |
| 플래시 포인트 | 1,436°C (2,617°F; 1,709K) |
| 치사량 또는 농도(LD, LC): | |
LD50(중앙선량) | 240mg/kg (복강intr, 쥐) 7950mg/kg(쥐, 경구)[11] |
LC50(중위농도) | 2500mg/m(mouse) |
LCLo (최저 발행) | 2500mg/m (guinea돼지, 3-4시간) |
| NIOSH(미국 건강 노출 한도): | |
PEL(허용) | TWA 5mg/m3 (흄) TWA 15mg/m3 (총분진) TWA 5mg/m3 (호흡분진)[2] |
REL (권장) | 먼지 : TWA 5mg/mC3 15mg/m3 흄 : TWA 5mg/m ST3 10mg/m3[2] |
IDLH(즉각 위험) | 500mg/m3[2] |
| 안전자료(SDS) | ICSC 0208 |
| 관련화합물 | |
기타 음이온 | 황화아연 셀레나이드 아연 텔루라이드 아연 |
기타 양이온 | 카드뮴 산화물 수성()II) 산화물 |
별도의 언급이 없는 경우를 제외하고, 표준 상태(25 °C [77 °F], 100 kPa에서)의 재료에 대한 데이터가 제공됩니다. | |
산화아연은 화학식이 ZnO인 무기 화합물입니다.이것은 물에 녹지 않는 하얀 가루입니다.ZnO는 화장품, 식품 보조제, 고무, 플라스틱, 세라믹, 유리, 시멘트, 윤활제,[12] 페인트, 자외선 차단제, 연고, 접착제, 실란트, 색소, 식품, 배터리, 페라이트, 난연제, 반도체 및 [13]구급 테이프 등의 다양한 재료 및 제품에 첨가제로 사용됩니다.자연적으로 광물 아연석으로 발생하지만, 대부분의 산화 아연은 합성적으로 생성됩니다.[14]
역사
아연 화합물은 아마도 초기 인류에 의해 가공[14] 및 가공되지 않은 형태로 페인트 또는 약 연고로 사용되었을 것이지만, 그 구성은 불확실합니다.푸쉬판잔, 아마도 산화아연으로 추정되는 눈과 열린 상처를 위한 연고로 사용된 것은 기원전 500년 또는 그 이전의 것으로 생각되는 인도 의학 문헌인 Charaka Samhita에 언급되어 있습니다.[15]산화아연 연고는 그리스 의사 디오스코리데스(Dioscorides, 서기 1세기)에 의해서도 언급됩니다.[16]갈렌은 그의 The Canon of Medicine에서 아비세나가 그랬던 [17]것처럼 산화아연으로 궤양성 암을 치료할 것을 제안했습니다.베이비 파우더, 기저귀 발진 방지 크림, 칼라민 크림, 안티-비듬 샴푸, 방부제 연고 등의 제품에 사용됩니다.[18]
로마인들은 구리가 산화아연과 반응하는 침전 공정에 의해 기원전 200년 초에 상당한 양의 황동(아연과 구리의 합금)을 생산했습니다.[19]산화아연은 아연광을 갱도에서 가열하여 생성된 것으로 추정됩니다.이것은 금속 아연을 증기로 방출했고, 이후 연도를 상승시켜 산화물로 응축시켰습니다.이 과정은 서기 1세기에 디오스코리데스에 의해 기술되었습니다.[20]인도 자와르의 아연 광산에서도 기원전 1천년 후반부터 산화아연이 발견되었습니다.[16]
12세기부터 16세기까지 인도에서는 아연과 산화아연이 직접 합성 과정의 원시적인 형태를 사용하여 인식되고 생산되었습니다.인도에서 아연 제조업은 17세기에 중국으로 옮겨왔습니다.1743년, 최초의 유럽 아연 제련소가 영국 브리스톨에 세워졌습니다.[21]1782년경 Louis-Bernard Guyton de Morveau는 납 백색 안료를 산화아연으로 대체할 것을 제안했습니다.[22]
산화아연(Zinc White)의 주된 용도는 페인트와 연고 첨가제였습니다.아연백색은 1834년까지 유화의 안료로 받아들여졌지만, 그것은 기름과 잘 섞이지 않았습니다.이 문제는 ZnO 합성을 최적화하여 해결하였습니다.1845년, 파리의 Edme-Jean Leclaire는 대규모로 유화 물감을 생산하고 있었고, 1850년까지, 아연 흰색이 유럽 전역에서 생산되고 있었습니다.아연 흰색 페인트의 성공은 전통적인 흰색 납에 비해 장점 때문입니다. 아연 흰색은 햇빛에서 본질적으로 영구적이고, 황을 함유한 공기에 의해 검어지지 않으며, 독성이 없고 경제적입니다.아연 화이트는 매우 "깨끗하기" 때문에 다른 색으로 틴트를 만드는 데 가치가 있지만, 다른 색과 섞이지 않으면 다소 부서지기 쉬운 건조 필름을 만듭니다.예를 들어, 1890년대 후반과 1900년대 초반에 몇몇 예술가들은 그들의 유화를 위한 지면으로 아연 흰색을 사용했습니다.그 모든 그림들은 수년간 금이 갔습니다.[23]
최근 대부분의 산화아연은 부식에 견디기 위해 고무 산업에 사용되었습니다.1970년대에 ZnO의 두 번째로 큰 응용 분야는 복사였습니다.복사용지에 '프랑스 공정'으로 생산된 고품질 ZnO를 충전재로 첨가했습니다.이 애플리케이션은 곧 티타늄으로 대체되었습니다.[24]
화학적 성질
순수한 ZnO는 흰색 분말이지만, 자연에서는 희귀한 광물 아연석으로 발생하는데, 보통 망간과 다른 불순물들이 함유되어 있어 노란색에서 빨간색을 부여합니다.[25]
결정질 산화아연은 열변색을 띠며 공기 중에서 가열하면 흰색에서 노란색으로 변하고 냉각 시 흰색으로 되돌아갑니다.[26]이러한 색상 변화는 고온에서 환경에 산소가 약간 손실되어 비화학량론적 ZnO가 형성되며, 이때 800°C에서는 x = 0.00007입니다.
산화아연은 양성 산화물입니다.물에는 거의 용해되지 않지만 염산과 같은 대부분의 산에는 용해됩니다.[27]
- ZnO + 2 HCl → ZnCl + HO
고체 산화아연은 알칼리에 용해되어 용해성 아연산염을 생성합니다.
- ZnO + 2 NaOH + HO → Na[Zn(OH))]
ZnO는 오일의 지방산과 천천히 반응하여 대응하는 카복실레이트, 예를 들어 올레산 또는 스테아레이트를 생성합니다.염화 아연의 강력한 수용액과 혼합될 때, ZnO는 염화 아연 하이드록시로 가장 잘 묘사되는 시멘트와 유사한 제품을 형성합니다.[28]이 시멘트는 치과에서 사용되었습니다.[29]

ZnO는 또한 인산 처리 시 시멘트와 유사한 물질을 형성합니다; 관련 물질은 치과에서 사용됩니다.[29]이 반응에 의해 생성되는 인산아연 시멘트의 주요 성분은 호프나이트, Zn3(PO4)·24HO입니다2.[30]
ZnO는 표준 산소 압력으로 1975 °C에서 아연 증기와 산소로 분해됩니다.탄소로 가열하면 훨씬 낮은 온도(약 950 °C)에서 산화물이 아연 증기로 변환됩니다.[27]
- ZnO + C → Zn + CO
물리적 특성


구조.
산화아연은 육각형 와르자이트와[31] 입방아연 혼합물의 두 가지 주요 형태로 결정화됩니다.워자이트 구조는 주변 조건에서 가장 안정적이므로 가장 일반적입니다.ZnO를 입방 격자 구조의 기판 위에 성장시킴으로써 아연 블렌드 형태가 안정화될 수 있습니다.두 경우 모두 아연과 산화물 중심은 Zn(II)의 가장 특징적인 기하학인 사면체입니다. ZnO는 약 10 GPa의 비교적 높은 압력에서 암염 모티프로 변환됩니다.[13]ZnO를 함유하는 크림의 많은 놀라운 의학적 특성은 탄성 부드러움으로 설명될 수 있는데, 이것은 팔면체 구조로의 전이에 가까운 사면체 배위 이진 화합물의 특징입니다.[32]
육각형과 아연 혼합 다형은 반전 대칭이 없습니다. (어떤 주어진 점에 대한 결정의 반사는 결정을 그 자체로 변환시키지 않습니다.)이것과 다른 격자 대칭 특성은 육각형과 아연 혼합형 ZnO의 압전성과 육각형 ZnO의 열전성을 야기합니다.
육각형 구조는 점군 6 mm (헤르만-마우긴 표기) 또는6v C (Choenflies 표기)를 가지며, 공간군은 P6mc3 또는 C6v4.격자 상수는 a = 3.25 Å 및 c = 5.2 Å입니다. 이들의 비율 c/a ~ 1.60은 육각형 셀 c/a = 1.633의 이상적인 값에 가깝습니다.대부분의 II-VI 그룹 재료에서와 마찬가지로, ZnO의 결합은 Zn의2+ 경우 0.074 nm, O의2− 경우 0.140 nm의 상응하는 반경을 갖는 대부분 이온성(ZnO2+2−)입니다.이러한 특성은 ZnO의 강한 압전성뿐만 아니라 [34]아연 블렌드 구조보다 wurtzite의 우선적인 형성을 설명합니다.극성 Zn-O 결합 때문에 아연과 산소 면은 전기적으로 대전됩니다.전기적 중립성을 유지하기 위해 ZnO가 아닌 대부분의 상대적인 물질에서는 원자 수준으로 재구성됩니다. ZnO의 표면은 원자적으로 평평하고 안정적이며 재구성되지 않습니다.[35]그러나 wurtzoid 구조를 사용한 연구는 ZnO 평면에서의 전하의 기원 외에 ZnO wurtzite 표면에서의[36] 표면 평탄도의 기원과 재구성의 부재를 설명했습니다.
기계적 성질
ZnO는 II-VI 반도체 그룹의 광대역 갭 반도체입니다.산소결핍이나 아연간질로 인한 반도체의 고유 도핑은 n형입니다.[13]
ZnO는 모스 스케일에서 대략 4.5의 경도를 가진 비교적 부드러운 물질입니다.[12]탄성 상수는 GaN과 같은 관련 III-V 반도체보다 작습니다.ZnO의 높은 열용량과 열전도율, 낮은 열팽창과 높은 용융온도는 세라믹에 유리합니다.[24]ZnO의 E2 광학 포논은 10K에서 133ps의 이례적으로 긴 수명을 보여줍니다.[37]
사면체 접합 반도체들 중에서, ZnO는 가장 높은 압전 텐서, 또는 GaN 및 AlN에 필적하는 적어도 하나를 갖는다고 기술되어 있습니다.[38]이러한 특성으로 인해 대규모 전기 기계적 커플링이 필요한 많은 압전 응용 분야에서 기술적으로 중요한 소재가 됩니다.따라서 박막 형태의 ZnO는 박막 벌크 음향 공진기를 위한 가장 많이 연구된 공진기 재료 중 하나였습니다.
전기적 및 광학적 특성
산화아연의 바람직한 특성으로는 우수한 투명도, 높은 전자 이동도, 넓은 밴드갭, 강한 상온 발광 등이 있습니다.이러한 특성으로 인해 ZnO는 액정 디스플레이의 투명 전극, 에너지 절약 또는 열 보호 윈도우, 박막 트랜지스터 및 발광 다이오드의 전자 장치 등 다양한 새로운 용도에 유용하게 사용됩니다.
ZnO는 상온에서 ~3.3 eV의 비교적 넓은 직접 밴드갭을 갖습니다.넓은 밴드 갭과 관련된 장점으로는 더 높은 항복 전압, 더 큰 전기장을 유지할 수 있는 능력, 더 낮은 전자 노이즈, 그리고 고온 및 고전력 작동이 있습니다.ZnO의 밴드갭은 산화마그네슘 또는 산화카드뮴과 합금화하여 ~3~4eV까지 조정할 수 있습니다.[13]
의도적인 도핑이 없는 경우에도 대부분의 ZnO는 n형 특성을 갖습니다.비화학양론은 일반적으로 n형 문자의 기원이지만, 그 주제는 여전히 논란의 여지가 있습니다.[39]이론적 계산에 근거하여 의도하지 않은 대체 수소 불순물이 원인이라는 대안이 제시되었습니다.[40]제어 가능한 n-형 도핑은 Zn을 Al, Ga, In과 같은 3족 원소로 치환하거나 산소를 7족 원소 염소 또는 요오드로 치환함으로써 쉽게 달성됩니다.[41]
ZnO의 신뢰성 있는 p형 도핑은 여전히 어렵습니다.이 문제는 p형 도펀트의 낮은 용해도와 풍부한 n형 불순물에 의한 보상에서 비롯됩니다.이러한 문제는 GaN과 ZnSe에서 관찰됩니다."본질적으로" n형 물질에서 p형의 측정은 시료의 비균질성으로 인해 복잡합니다.[42]
p-도핑에 대한 현재의 제한은 일반적으로 n-타입 및 p-타입 재료의 접합을 필요로 하는 ZnO의 전자 및 광전자 응용을 제한합니다.공지된 p형 도펀트는 구리 및 은 뿐만 아니라, 기-I 원소 Li, Na, K; 기-V 원소 N, P 및 As; 를 포함합니다.그러나 이러한 것들 중 많은 것들이 깊은 수용체를 형성하고 실온에서 상당한 p형 전도를 일으키지 않습니다.[13]
ZnO의 전자 이동성은 온도에 따라 크게 변하며 80K에서 최대 ~2000cm2/(V·s)를 갖습니다.[43]구멍 이동성에 대한 데이터는 5-30 cm2/(V·s) 범위의 값으로 부족합니다.[44]
대부분의 서지 차단기는 바리스터 역할을 하는 ZnO 디스크가 활성 물질입니다.[45][46]
산화아연은 특히 대량으로 비선형 광학 특성이 강한 것으로 유명합니다.ZnO 나노입자의 비선형성은 크기에 따라 미세조정이 가능합니다.[47]
생산.
산업용으로 ZnO는 세 가지 주요 공정에 의해 연간[25] 10톤5 수준으로 생산됩니다.[24]
간접공정
간접 공정 또는 프랑스 공정에서 금속 아연은 흑연 도가니에서 용융되고 907 °C(일반적으로 약 1000 °C) 이상의 온도에서 기화됩니다.아연 증기는 공기 중의 산소와 반응하여 ZnO를 생성하고 온도 저하와 밝은 발광을 동반합니다.산화아연 입자는 냉각 덕트로 운반되어 백하우스에 수집됩니다.이 간접적인 방법은 1844년 파리의 Edme Jean LeClaire에 의해 대중화되었고 따라서 흔히 프랑스 과정으로 알려져 있습니다.이 제품은 보통 0.1에서 수 마이크로미터의 평균 크기를 가진 산화아연 입자로 구성됩니다.무게로 따지면, 세계의 산화아연의 대부분은 프랑스 공정을 통해 제조됩니다.
직접공정
직접적인 미국 공정은 아연 광석이나 제련소 부산물과 같은 다양한 오염된 아연 복합물에서 시작됩니다.아연 전구체는 무연탄과 같은 탄소 공급원으로 가열하여 아연 증기를 생성함으로써 환원(탄소 환원)되며, 이는 간접 공정에서와 같이 산화됩니다.원료의 순도가 낮기 때문에 간접 공정에 비해 직접 공정에서도 품질이 떨어집니다.
습식화학공정
소량의 산업 생산은 탄산 아연 또는 수산화 아연이 침전되는 아연 염의 수용액으로부터 시작되는 습식 화학 공정을 포함합니다.고체 침전물은 약 800°C의 온도에서 하소됩니다.
실험실 합성

과학 연구 및 틈새 응용을 위한 ZnO 생산을 위한 다양한 전문화된 방법이 존재합니다.이러한 방법은 ZnO 형태(벌크, 박막, 나노와이어), 온도(낮음, 실온에 가깝거나 "높음, 즉 T ~ 1000 °C), 공정 유형(용액으로부터 증착 또는 성장) 및 기타 매개 변수로 분류할 수 있습니다.
큰 단결정(수 입방 센티미터)은 가스 수송(증기상 증착), 수열 [35][48][49]합성 또는 용융 성장에 의해 성장될 수 있습니다.[7]그러나 ZnO의 증기압이 높기 때문에 용융에 의한 성장이 곤란합니다.가스 수송에 의한 성장은 제어하기 어렵고, 수열법을 선호합니다.[7]박막은 화학기상증착법, 금속유기기상에피택시, 전기증착법, 펄스레이저증착법, 스퍼터링법, 졸-겔 합성법, 원자층증착법, 분무열분해법 등에 의해 제조될 수 있습니다.
일반적인 흰색 분말 산화아연은 아연 양극으로 중탄산나트륨 용액을 전기분해함으로써 실험실에서 제조할 수 있습니다.수산화아연과 수소 가스가 생성됩니다.가열하면 수산화아연이 산화아연으로 분해됩니다.
- Zn + 2HO → Zn(OH) + H
- Zn(OH) → ZnO + HO
ZnO 나노구조
ZnO의 나노구조는 나노와이어, 나노로드, 테트라포드, 나노벨트, 나노플라워, 나노입자 등 다양한 형태로 합성될 수 있습니다.나노 구조물은 특정 조건에서, 그리고 증기-액체-고체 방법을 사용하여, 위에서 언급된 대부분의 기술로 얻어질 수 있습니다.[35][50][51]합성은 일반적으로 약 90 °C의 온도에서 질산아연과 헥사민의 동몰 수용액에서 수행되며, 후자는 기본적인 환경을 제공합니다.폴리에틸렌 글리콜 또는 폴리에틸렌에틸렌이민과 같은 특정 첨가제는 ZnO 나노와이어의 종횡비를 향상시킬 수 있습니다.[52]ZnO 나노와이어의 도핑은 성장 용액에 다른 금속 질산염을 첨가함으로써 달성되었습니다.[53]생성된 나노 구조의 형태는 전구체 조성(아연 농도 및 pH 등) 또는 열처리(온도 및 가열 속도 등)와 관련된 파라미터를 변경함으로써 조정될 수 있습니다.[54]
미리 씨드된 실리콘, 유리 및 질화 갈륨 기판 상의 정렬된 ZnO 나노와이어는 기본 환경에서 질산 아연 및 아세트산 아연과 같은 수성 아연 염을 사용하여 성장되어 왔습니다.[55]ZnO를 사용한 프리시드 기판은 합성 동안 ZnO 결정의 균질한 핵생성을 위한 사이트를 생성합니다.일반적인 프리-시딩 방법은 아세트산 아연 결정질의 인-시츄 열 분해, ZnO 나노입자의 스핀 코팅 및 ZnO 박막을 증착하기 위한 물리적 기상 증착 방법의 사용을 포함합니다.[56][57]프리 시드는 성장 전에 핵 생성 부위를 지정하기 위해 전자 빔 리소그래피 및 나노스피어 리소그래피와 같은 하향 패턴 방식과 함께 수행될 수 있습니다.정렬된 ZnO 나노와이어는 염료 감응형 태양 전지 및 전계 방출 장치에 사용될 수 있습니다.[58][59]
적용들
산화아연 분말의 응용분야는 다양하며, 주요한 것은 아래와 같습니다.대부분의 응용 분야는 산화물의 반응성을 다른 아연 화합물의 전구체로 이용합니다.산화아연은 재료 과학 분야에서 높은 굴절률, 높은 열전도율, 결합성, 항균성 및 자외선 차단성을 갖습니다.따라서 플라스틱, 세라믹, 유리, 시멘트,[60] 고무, 윤활제,[12] 도료, 연고, 접착제, 실란트, 콘크리트 제조, 안료, 식품, 배터리, 페라이트, 난연제 등을 포함하는 재료 및 제품에 첨가됩니다.[61]
고무산업
ZnO 사용량의 50~60%가 고무 산업에 사용됩니다.[62]산화아연과 스테아르산은 고무의 황가황에 사용됩니다.[24][63]ZnO 첨가제는 곰팡이(의료용 응용 프로그램 참조)와 자외선으로부터 고무를 보호하기도 합니다.
도자기공업
세라믹 산업은 특히 세라믹 유약과 프릿 조성물에서 산화아연을 상당히 많이 소비합니다.비교적 낮은 팽창 계수와 결합된 ZnO의 비교적 높은 열용량, 열전도도 및 고온 안정성은 세라믹의 생산에 있어서 바람직한 특성입니다.ZnO는 유약, 에나멜 및 세라믹 제형의 융점 및 광학 특성에 영향을 미칩니다.산화아연은 저팽창, 2차 플럭스는 온도에 따라 점도의 변화를 감소시켜 유약의 탄력성을 향상시키고 마멸과 떨림을 방지하는 데 도움을 줍니다.BaO와 PbO를 ZnO로 치환함으로써 열용량이 감소하고 열전도율이 증가합니다.소량의 아연은 광택이 나고 빛나는 표면의 발달을 향상시킵니다.그러나 중간에서 높은 양의 표면에서는 무광택과 결정성이 있습니다.색에 있어서 아연은 복잡한 영향을 줍니다.[62]
약
산화아연은 철(III) 산화물(FeO23)이 약 0.5%인 혼합물로서 칼라민이라 불리며 칼라민 로션에 사용됩니다.역사적으로 광물 칼라민은 산화물 아연석과 헤미모파이트의 혼합물입니다.유게놀과 혼합하면 산화아연 유게놀이 형성되는데, 이는 치과에서 회복제 및 보철제로서의 응용이 있습니다.[29][64]
산화아연 분말은 탈취성과 항균성을 가지고 있습니다.[65]ZnO는 면직물, 고무, 구강 관리 제품,[66][67] 식품 포장에 첨가됩니다.[68][69]벌크 물질과 비교하여 미세 입자의 강화된 항균 작용은 ZnO에만 국한된 것이 아니며 은과 같은 다른 물질에 대해 관찰됩니다.[70]이 특성은 미세 입자의 표면적이 증가함에 따라 발생합니다.
산화아연은 입안의 휘발성 가스와 휘발성 황화합물(VSC)을 감소시켜 플라크와 치석의 형성을 방지하고 [71]입냄새를 조절하기 위해 제안된 항균제로 구강청결제 제품과 치약에 사용됩니다.[72]산화아연 또는 아연염과 함께, 이 제품들은 또한 일반적으로 세틸피리디늄 클로라이드,[73] 자일리톨,[74] 히노키티올,[75] 에센셜 오일 및 식물 추출물과 같은 다른 활성 성분을 포함합니다.[76][77]
산화아연은 아토피 피부염, 접촉성 피부염, 습진으로 인한 가려움증, 기저귀 발진, 여드름 등 다양한 피부 질환 치료에 널리 사용됩니다.[78]기저귀 발진, 칼라민 크림, 안티-비듬 샴푸, 방부제 연고 등을 치료하기 위한 베이비 파우더, 베리어 크림 등의 제품에 사용됩니다.[18][79]흔히 피마자유와 결합하여 용혈성 및 떫은감,[80][81] 아연 및 피마자유 크림을 형성하며, 유아를 치료하는 데 일반적으로 사용됩니다.
운동 중 연조직 손상을 막기 위해 선수들이 붕대로 사용하는 테이프('산화아연 테이프'라고도 함) 속 성분이기도 합니다.[82]산화아연은 자외선 차단제에도 자주 첨가됩니다.[78]
산화아연은 자외선으로 인한 일광 및 기타 피부 손상을 방지하기 위해 연고, 크림 및 로션에 사용할[83] 수 있습니다(자외선 차단제 참조).가장 넓은 스펙트럼의 UVA 및 UVB 흡수제로[84][85] 미국 식품의약국(FDA)에서 자외선 차단제로 사용이 승인되었으며,[86] 완전히 광안정적입니다.[87]산화아연은 자외선 차단제의 성분으로 사용될 경우 자외선 차단제(UVA)(320~400 nm)와 자외선 차단제(UVB, 280~320 nm)를 모두 차단합니다.산화 아연과 다른 가장 일반적인 물리적 자외선 차단제인 이산화 티타늄은 자극적이지 않고, 비알레르기적이며, 희극적이지 않은 것으로 여겨집니다.[88]그러나 산화아연에서 나오는 아연은 피부에 약간 흡수됩니다.[89]
많은 자외선 차단제는 산화아연 나노입자(이산화티타늄 나노입자와 함께)를 사용하는데, 이는 그러한 작은 입자들이 빛을 산란시키지 않기 때문에 흰색으로 보이지 않기 때문입니다.나노 입자는 일반 크기의 산화아연 입자보다 피부에 더 많이 흡수되지 않으며,[90] 피부의 가장 바깥 층에만 흡수될 뿐 체내에는 흡수되지 않습니다.[90]
식품첨가물
산화아연은 아침 시리얼을 포함한 많은 식품에 필수 영양소인 [91]아연의 공급원으로 첨가됩니다.황산 아연도 같은 용도로 사용됩니다.일부 미리 포장된 식품들은 비록 그것이 영양소로 의도되지 않더라도 미량의 ZnO를 포함합니다.
안료
산화아연(아연백색)은 페인트에서 안료로 사용되며, 리소폰보다 불투명하지만 이산화티타늄보다는 불투명하지 않습니다.[14]종이 코팅에도 사용됩니다.차이니즈 화이트는 예술가들의 색소에 사용되는 아연 화이트의 특별한 등급입니다.[92]유화에서 안료로서 아연 흰색의 사용은 18세기 중반에 시작되었습니다.[93]그것은 부분적으로 독이 있는 납을 흰색으로 대체했고 뵈클린, 반 고흐,[94] 마네, 뭉크와 같은 화가들에 의해 사용되었습니다.미네랄 메이크업의 주성분이기도 합니다(CI 77947).[95]
자외선 흡수제
미세화 및 나노화된 산화아연은 자외선(UVA) 및 자외선(UVB)으로부터 강력한 보호 기능을 제공하여 자외선 차단용 자외선 차단 선글라스에 사용되며,[96] 제트추진연구소(JPL) 과학자들의 연구에 따라 우주 공간에서 사용하고 용접 시 보호에도 사용됩니다.[97]
코팅
산화아연 분말을 포함하는 도료는 예로부터 금속의 부식 방지 코팅으로 사용되어 왔습니다.아연도금 철에 특히 효과적입니다.철은 유기 코팅과의 반응성이 취성과 접착력 부족을 초래하기 때문에 보호하기가 어렵습니다.산화아연 페인트는 오랜 세월 동안 이러한 표면에 유연성과 접착력을 유지해 왔습니다.[61]
알루미늄, 갈륨 또는 인듐으로 도핑된 ZnO 하이 n-타입은 투명하고 전도성이 있습니다(투명 ~90%, 최저 저항률 ~10 ω·cm).ZnO:Al 코팅은 에너지 절약 또는 열 보호 윈도우에 사용됩니다.코팅은 스펙트럼의 가시적인 부분을 안으로 들어오게 해주지만 적외선(IR)[25] 방사선을 실내로 다시 반사시키거나(에너지 절약), IR 방사선이 실내로 들어오지 못하게 합니다(열 보호).
폴리에틸렌 나프탈레이트(PEN)와 같은 플라스틱은 산화아연 코팅을 적용하여 보호할 수 있습니다.코팅은 PEN을 통한 산소 확산을 감소시킵니다.[99]산화 아연 층은 또한 야외 응용에서 폴리카보네이트 상에 사용될 수 있습니다.그 코팅은 태양 복사로부터 폴리카보네이트를 보호하고 산화 속도와 광노란색을 감소시킵니다.[100]
원자로 부식방지
Zn(원자 질량 64의 아연 동위 원소)에서 고갈된 산화아연은 원자력 가압수로의 부식 방지에 사용됩니다.Zn은 원자로 중성자의 조사를 받아 방사성 Zn으로 변하기 때문에 고갈이 필요합니다.[101]
메탄 개질
산화아연(ZnO)은 촉매를 독살할 수 있는 메탄 개질기에 앞서 황 화합물을 수소화한 후 천연 가스에서 황화수소(HS2)를 제거하는 전처리 단계로 사용됩니다.약 230~430°C(446~806°F)의 온도에서 HS는2 다음과 같은 반응에 의해 물로 전환됩니다.[102]
- HS + ZnO → HO + ZnS
일렉트로닉스
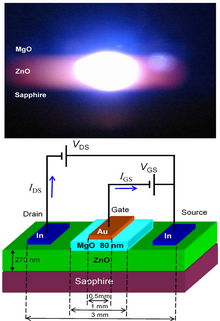

ZnO는 넓은 직접 밴드 갭(실온에서 3.37eV 또는 375nm)을 갖습니다.따라서 가장 일반적인 잠재적 응용 분야는 레이저 다이오드와 발광 다이오드(LED)에 있습니다.[105]또한 ZnO에서 초고속 비선형성과 광전도 기능이 보고되었습니다.[106]ZnO의 일부 광전자 응용은 유사한 밴드 갭(실온에서 ~3.4 eV)을 갖는 GaN의 광전자 응용과 겹칩니다.GaN과 비교하여 ZnO는 더 큰 여기자 결합 에너지(~60meV, 상온 열에너지의 2.4배)를 가지며, 이는 ZnO로부터 밝은 상온 방출을 초래합니다.ZnO는 LED 응용을 위해 GaN과 결합할 수 있습니다.예를 들어, 투명 전도성 산화물 층 및 ZnO 나노 구조물은 우수한 광 아웃커플링을 제공합니다.[107]전자 응용에 유리한 ZnO의 다른 특성으로는 고에너지 방사선에 대한 안정성과 습식 화학 에칭에 의해 패턴화되는 능력이 있습니다.[108]방사선 저항성은[109] ZnO를 우주 응용에 적합한 후보로 만듭니다.ZnO는 전자적으로 펌핑된 UV 레이저 소스를 생산하는 랜덤 레이저 분야에서 가장 유망한 후보입니다.
ZnO 나노로드의 뾰족한 끝은 전기장을 강하게 향상시킵니다.따라서 이들은 전계 방출체로 사용될 수 있습니다.[110]
알루미늄이 도핑된 ZnO 층은 투명 전극으로 사용됩니다.Zn과 Al 성분은 일반적으로 사용되는 인듐 주석 산화물(ITO)에 비해 훨씬 저렴하고 독성이 적습니다.상업적으로 이용 가능하기 시작한 하나의 응용은 태양 전지 또는 액정 디스플레이를 위한 전면 접촉으로서 ZnO를 사용하는 것입니다.[111]
ZnO는 투명 박막 트랜지스터(TTFT)를 제조할 수 있습니다.전계 효과 트랜지스터로서, 이들은 p-n 접합을 필요로 하지 않으므로 [112]ZnO의 p-type 도핑 문제를 피할 수 있습니다.전계 효과 트랜지스터들 중 일부는 심지어 전도 채널로서 ZnO 나노 로드들을 사용합니다.[113]
산화아연 나노로드 센서
산화아연 나노로드 센서는 가스 분자의 흡착에 의한 산화아연 나노와이어를 통과하는 전류의 변화를 감지하는 장치입니다.수소 가스에 대한 선택성은 나노 로드 표면에 팔라듐 클러스터를 스퍼터링함으로써 달성되었습니다.팔라듐의 첨가는 수소 분자를 원자 수소로 촉매 해리하여 센서 장치의 감도를 높이는 데 효과적인 것으로 보입니다.이 센서는 상온에서 100만분의 10까지 수소 농도를 감지하는 반면 산소에는 반응이 없습니다.[114][115]ZnO는 마이크로 전극에 인가된 측정 전기장에 의해 조사된 전체 영역에 걸쳐 항체의 분포를 가능하게 하는 면역 센서에서 고정화 층으로서 사용되어 왔습니다.[116]
압전
ZnO로 코팅된 섬유 섬유의 압전은 바람이나 신체의 움직임으로 인한 일상적인 기계적 스트레스로 "자체 동력 나노 시스템"을 제작할 수 있는 것으로 나타났습니다.[117][118]
2008년 조지아 공과대학교의 나노구조 특성화 센터는 산화아연 나노와이어를 늘려서 방출함으로써 교류를 전달하는 전기 발생 장치(플렉시블 전하 펌프 발전기라고 함)를 생산했다고 보고했습니다.이 미니 발전기는 최대 45밀리볼트의 진동 전압을 생성하여 인가되는 기계적 에너지의 약 7%를 전기로 변환합니다.연구원들은 길이가 0.2-0.3mm이고 직경이 3-5마이크로미터인 와이어를 사용했지만 장치를 더 작은 크기로 줄일 수 있었습니다.[119]

박막 형태의 ZnO는 소형화된 고주파 박막 공진기, 센서 및 필터에서 입증되었습니다.
Li-이온 배터리 및 슈퍼커패시터
ZnO는 값싸고 생체에 적합하며 환경 친화적이기 때문에 리튬 이온 배터리에 유망한 음극 재료입니다.ZnO는 CoO(715 mAhg−1), NiO(718 mAhg−1) 및 CuO(674 mAhg−1)와 같은 많은 다른 전이 금속 산화물보다 높은 이론 용량(978 mAhg−1)을 가지고 있습니다.[120]ZnO는 슈퍼커패시터의 전극으로도 사용됩니다.[121]
안전.
산화아연은 식품첨가물로서 미국 FDA의 일반적으로 안전하다고 인정되는 물질 목록에 포함되어 있습니다.[122]
산화아연 자체는 독성이 없지만, 아연 또는 아연합금이 고온에서 녹아서 산화될 때 발생하는 산화아연 연기를 흡입하는 것은 위험합니다.놋쇠의 녹는점이 아연의 끓는점에 가깝기 때문에 놋쇠를 포함한 합금을 녹이는 동안 이 문제가 발생합니다.[123]아연도금(아연도금) 강철을 용접할 때도 발생하는 공기 중 산화아연에 노출되면 금속 흄열이라는 질병이 발생할 수 있습니다.이러한 이유로, 일반적으로 아연도금강은 용접되지 않거나, 아연이 먼저 제거됩니다.[124][dubious ]
산화아연과 다른 석유화학 자외선 흡수제를 결합한 자외선 차단제에서는 산화아연이 소분자 석유화학 자외선 흡수제의 광분해를 일으킨다는 사실이 밝혀졌는데, 이는 제브라피쉬 배아분석에서 독성을 나타냈습니다.[125]
참고 항목
참고문헌
- ^ a b c d 헤인즈, 페이지 4.95, 12.80
- ^ a b c d NIOSH Pocket Guide to Chemical Hazards. "#0675". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b 헤인즈, 페이지 12.85, 12.89
- ^ 헤인즈, 페이지 4.131
- ^ 헤인즈, 페이지 12.80
- ^ 헤인즈, 페이지 4.138, 10.251
- ^ a b c Takahashi K, Yoshikawa A, Sandhu A (2007). Wide bandgap semiconductors: fundamental properties and modern photonic and electronic devices. Springer. p. 357. ISBN 978-3-540-47234-6.
- ^ 헤인즈, 페이지 4.145
- ^ 헤인즈, 페이지 5.2, 5.42, 6.163
- ^ 산화아연.Chem.sis.nlm.nih.gov .2015-11-17에 검색되었습니다.
- ^ a b c "Zinc oxide". Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ^ a b c Battez AH, González R, Viesca JL, Fernández JE, Fernández JD, Machado A, Chou R, Riba J (2008). "CuO, ZrO2 and ZnO nanoparticles as antiwear additive in oil lubricants". Wear. 265 (3–4): 422–428. doi:10.1016/j.wear.2007.11.013.
- ^ a b c d e Özgür Ü, Alivov YI, Liu C, Teke A, Reshchikov M, Doğan S, Avrutin VC, Cho SJ, Morkoç AH (2005). "A comprehensive review of ZnO materials and devices". Journal of Applied Physics. 98 (4): 041301–041301–103. Bibcode:2005JAP....98d1301O. doi:10.1063/1.1992666.
- ^ a b c De Liedekerke M (2006). "2.3. Zinc Oxide (Zinc White): Pigments, Inorganic, 1". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a20_243.pub2.
- ^ Craddock PT (1998). "Zinc in India". 2000 years of zinc and brass. British Museum. p. 27. ISBN 978-0-86159-124-4.
- ^ a b Craddock PT (2008). "Mining and Metallurgy, chapter 4". In Oleson JP (ed.). The Oxford Handbook of Engineering and Technology in the Classical World. Oxford University Press. pp. 111–112. ISBN 978-0-19-518731-1.
- ^ Winchester DJ, Winchester DP, Hudis CA, Norton L (2005). Breast Cancer (Atlas of Clinical Oncology). PMPH USA. p. 3. ISBN 978-1550092721.
- ^ a b Harding FJ (2007). Breast Cancer: Cause – Prevention – Cure. Tekline Publishing. p. 83. ISBN 978-0-9554221-0-2.
- ^ "Zinc". Encyclopædia Britannica. 10 March 2009.
- ^ Craddock PT (2009). "The origins and inspirations of zinc smelting". Journal of Materials Science. 44 (9): 2181–2191. Bibcode:2009JMatS..44.2181C. doi:10.1007/s10853-008-2942-1. S2CID 135523239.
- ^ National Institute of Health, WHO 및 International Zinc Association의 아연 일반 정보2009년 3월 10일 회수
- ^ "Zinc White".
- ^ "Zinc white: History of use". Pigments through the ages. webexhibits.org.
- ^ a b c d Porter F (1991). Zinc Handbook: Properties, Processing, and Use in Design. CRC Press. ISBN 978-0-8247-8340-2.
- ^ a b c Klingshirn C (April 2007). "ZnO: material, physics and applications". ChemPhysChem. 8 (6): 782–803. doi:10.1002/cphc.200700002. PMID 17429819.
- ^ a b Wiberg E, Holleman AF (2001). Inorganic Chemistry. Elsevier. ISBN 978-0-12-352651-9.
- ^ a b Greenwood NN, Earnshaw A (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ Nicholson JW (1998). "The chemistry of cements formed between zinc oxide and aqueous zinc chloride". Journal of Materials Science. 33 (9): 2251–2254. Bibcode:1998JMatS..33.2251N. doi:10.1023/A:1004327018497. S2CID 94700819.
- ^ a b c Ferracane JL (2001). Materials in Dentistry: Principles and Applications. Lippincott Williams & Wilkins. pp. 70, 143. ISBN 978-0-7817-2733-4.
- ^ Park CK, Silsbee MR, Roy DM (1998). "Setting reaction and resultant structure of zinc phosphate cement in various orthophosphoric acid cement-forming liquids". Cement and Concrete Research. 28 (1): 141–150. doi:10.1016/S0008-8846(97)00223-8.
- ^ Fierro JL (2006). Metal Oxides: Chemistry & Applications. CRC Press. p. 182. ISBN 978-0824723712.
- ^ Phillips JC (1970). "Ionicity of the Chemical Bond in Crystals". Reviews of Modern Physics. 42 (3): 317–356. Bibcode:1970RvMP...42..317P. doi:10.1103/RevModPhys.42.317.
- ^ Rossler U, ed. (1999). Landolt-Bornstein, New Series, Group III. Vol. 17B, 22, 41B. Springer, Heidelberg.
- ^ Klingshirn CF, Waag A, Hoffmann A, Geurts J (2010). Zinc Oxide: From Fundamental Properties Towards Novel Applications. Springer. pp. 9–10. ISBN 978-3-642-10576-0.
- ^ a b c Baruah S, Dutta J (February 2009). "Hydrothermal growth of ZnO nanostructures". Science and Technology of Advanced Materials. 10 (1): 013001. Bibcode:2009STAdM..10a3001B. doi:10.1088/1468-6996/10/1/013001. PMC 5109597. PMID 27877250.
- ^ Abdulsattar MA (2015). "Capped ZnO (3, 0) nanotubes as building blocks of bare and H passivated wurtzite ZnO nanocrystals". Superlattices and Microstructures. 85: 813–819. Bibcode:2015SuMi...85..813A. doi:10.1016/j.spmi.2015.07.015.
- ^ Millot M, Tena-Zaera R, Munoz-Sanjose V, Broto JM, Gonzalez J (2010). "Anharmonic effects in ZnO optical phonons probed by Raman spectroscopy". Applied Physics Letters. 96 (15): 152103. Bibcode:2010ApPhL..96o2103M. doi:10.1063/1.3387843. hdl:10902/23620.
- ^ Posternak M, Resta R, Baldereschi A (October 1994). "Ab initio study of piezoelectricity and spontaneous polarization in ZnO". Physical Review B. 50 (15): 10715–10721. Bibcode:1994PhRvB..5010715D. doi:10.1103/PhysRevB.50.10715. PMID 9975171.
- ^ Look DC, Hemsky JW, Sizelove JR (1999). "Residual Native Shallow Donor in ZnO". Physical Review Letters. 82 (12): 2552–2555. Bibcode:1999PhRvL..82.2552L. doi:10.1103/PhysRevLett.82.2552. S2CID 53476471.
- ^ Janotti A, Van de Walle CG (January 2007). "Hydrogen multicentre bonds". Nature Materials. 6 (1): 44–7. Bibcode:2007NatMa...6...44J. doi:10.1038/nmat1795. PMID 17143265.
- ^ Kato H, Sano M, Miyamoto K, Yao T (2002). "Growth and characterization of Ga-doped ZnO layers on a-plane sapphire substrates grown by molecular beam epitaxy". Journal of Crystal Growth. 237–239: 538–543. Bibcode:2002JCrGr.237..538K. doi:10.1016/S0022-0248(01)01972-8.
- ^ Ohgaki T, Ohashi N, Sugimura S, Ryoken H, Sakaguchi I, Adachi Y, Haneda H (2008). "Positive Hall coefficients obtained from contact misplacement on evident n-type ZnO films and crystals". Journal of Materials Research. 23 (9): 2293–2295. Bibcode:2008JMatR..23.2293O. doi:10.1557/JMR.2008.0300. S2CID 137944281.
- ^ Wagner P, Helbig R (1974). "Halleffekt und anisotropie der beweglichkeit der elektronen in ZnO". Journal of Physics and Chemistry of Solids. 35 (3): 327–335. Bibcode:1974JPCS...35..327W. doi:10.1016/S0022-3697(74)80026-0.
- ^ Ryu YR, Lee TS, White HW (2003). "Properties of arsenic-doped p-type ZnO grown by hybrid beam deposition". Applied Physics Letters. 83 (1): 87. Bibcode:2003ApPhL..83...87R. doi:10.1063/1.1590423.
- ^ 르네 스미츠, 루반 데르 슬루아, 미라드 카페타노비치, 데이비드 F.필로, 안톤 얀센."송배전 시스템의 전환".2014. 페이지 316.
- ^ 무쿤드 R.파텔."전력과 전력전자학 개론", 2012. p. 247
- ^ Irimpan L, Krishnan Deepthy BA, Nampoori VPN, Radhakrishnan P (2008). "Size-dependent enhancement of nonlinear optical properties in nanocolloids of ZnO" (PDF). Journal of Applied Physics. 103 (3): 033105–033105–7. Bibcode:2008JAP...103c3105I. doi:10.1063/1.2838178.
- ^ a b Schulz D, Ganschow S, Klimm D, Struve K (2008). "Inductively heated Bridgman method for the growth of zinc oxide single crystals". Journal of Crystal Growth. 310 (7–9): 1832–1835. Bibcode:2008JCrGr.310.1832S. doi:10.1016/j.jcrysgro.2007.11.050.
- ^ Baruah S, Thanachayanont C, Dutta J (April 2008). "Growth of ZnO nanowires on nonwoven polyethylene fibers". Science and Technology of Advanced Materials. 9 (2): 025009. Bibcode:2008STAdM...9b5009B. doi:10.1088/1468-6996/9/2/025009. PMC 5099741. PMID 27877984.
- ^ Miao L, Ieda Y, Tanemura S, Cao YG, Tanemura M, Hayashi Y, Toh S, Kaneko K (2007). "Synthesis, microstructure and photoluminescence of well-aligned ZnO nanorods on Si substrate". Science and Technology of Advanced Materials. 8 (6): 443–447. Bibcode:2007STAdM...8..443M. doi:10.1016/j.stam.2007.02.012.
- ^ Xu S, Wang ZL (2011). "One-dimensional ZnO nanostructures: Solution growth and functional properties". Nano Res. 4 (11): 1013–1098. CiteSeerX 10.1.1.654.3359. doi:10.1007/s12274-011-0160-7. S2CID 137014543.
- ^ Zhou Y, Wu W, Hu G, Wu H, Cui S (2008). "Hydrothermal synthesis of ZnO nanorod arrays with the addition of polyethyleneimine". Materials Research Bulletin. 43 (8–9): 2113–2118. doi:10.1016/j.materresbull.2007.09.024.
- ^ Cui J, Zeng Q, Gibson UJ (2006-04-15). "Synthesis and magnetic properties of Co-doped ZnO nanowires". Journal of Applied Physics. 99 (8): 08M113. Bibcode:2006JAP....99hM113C. doi:10.1063/1.2169411.
- ^ Elen K, Van den Rul H, Hardy A, Van Bael MK, D'Haen J, Peeters R, et al. (February 2009). "Hydrothermal synthesis of ZnO nanorods: a statistical determination of the significant parameters in view of reducing the diameter". Nanotechnology. 20 (5): 055608. Bibcode:2009Nanot..20e5608E. doi:10.1088/0957-4484/20/5/055608. PMID 19417355. S2CID 206056816.
- ^ Greene LE, Law M, Goldberger J, Kim F, Johnson JC, Zhang Y, et al. (July 2003). "Low-temperature wafer-scale production of ZnO nanowire arrays". Angewandte Chemie. 42 (26): 3031–4. doi:10.1002/anie.200351461. PMID 12851963.
- ^ Wu W (2009). "Effects of Seed Layer Characteristics on the Synthesis of ZnO Nanowires". Journal of the American Ceramic Society. 92 (11): 2718–2723. doi:10.1111/j.1551-2916.2009.03022.x.
- ^ Greene LE, Law M, Tan DH, Montano M, Goldberger J, Somorjai G, Yang P (July 2005). "General route to vertical ZnO nanowire arrays using textured ZnO seeds". Nano Letters. 5 (7): 1231–6. Bibcode:2005NanoL...5.1231G. doi:10.1021/nl050788p. PMID 16178216.
- ^ Hua G (2008). "Fabrication of ZnO nanowire arrays by cycle growth in surfactantless aqueous solution and their applications on dye-sensitized solar cells". Materials Letters. 62 (25): 4109–4111. doi:10.1016/j.matlet.2008.06.018.
- ^ Lee JH, Chung YW, Hon MH, Leu C (2009-05-07). "Density-controlled growth and field emission property of aligned ZnO nanorod arrays". Applied Physics A. 97 (2): 403–408. Bibcode:2009ApPhA..97..403L. doi:10.1007/s00339-009-5226-y. S2CID 97205678.
- ^ Sanchez-Pescador R, Brown JT, Roberts M, Urdea MS (February 1988). "The nucleotide sequence of the tetracycline resistance determinant tetM from Ureaplasma urealyticum". Nucleic Acids Research. 16 (3): 1216–7. doi:10.1093/nar/16.3.1216. PMC 334766. PMID 3344217.
- ^ a b 앰비카 다투 프라이빗 리미티드.ZnO 응용 프로그램.2009년 1월 25일 웨이백 머신 액세스 날짜에 2019년 12월 19일 보관.
- ^ a b Moezzi A, McDonagh AM, Cortie MB (2012). "Review: Zinc oxide particles: Synthesis, properties and applications". Chemical Engineering Journal. 185–186: 1–22. doi:10.1016/j.cej.2012.01.076.
- ^ Brown HE (1957). Zinc Oxide Rediscovered. New York: The New Jersey Zinc Company.
- ^ van Noort R (2002). Introduction to Dental Materials (2d ed.). Elsevier Health Sciences. ISBN 978-0-7234-3215-9.
- ^ Padmavathy N, Vijayaraghavan R (July 2008). "Enhanced bioactivity of ZnO nanoparticles-an antimicrobial study". Science and Technology of Advanced Materials. 9 (3): 035004. Bibcode:2008STAdM...9c5004P. doi:10.1088/1468-6996/9/3/035004. PMC 5099658. PMID 27878001.
- ^ ten Cate JM (February 2013). "Contemporary perspective on the use of fluoride products in caries prevention". British Dental Journal. 214 (4): 161–7. doi:10.1038/sj.bdj.2013.162. PMID 23429124.
- ^ Rošin-Grget K, Peroš K, Sutej I, Bašić K (November 2013). "The cariostatic mechanisms of fluoride". Acta Medica Academica. 42 (2): 179–88. doi:10.5644/ama2006-124.85. PMID 24308397.
- ^ Li Q, Chen S, Jiang W (2007). "Durability of nano ZnO antibacterial cotton fabric to sweat". Journal of Applied Polymer Science. 103: 412–416. doi:10.1002/app.24866.
- ^ Saito M (1993). "Antibacterial, Deodorizing, and UV Absorbing Materials Obtained with Zinc Oxide (ZnO) Coated Fabrics". Journal of Industrial Textiles. 23 (2): 150–164. doi:10.1177/152808379302300205. S2CID 97726945.
- ^ Akhavan O, Ghaderi E (February 2009). "Enhancement of antibacterial properties of Ag nanorods by electric field". Science and Technology of Advanced Materials. 10 (1): 015003. Bibcode:2009STAdM..10a5003A. doi:10.1088/1468-6996/10/1/015003. PMC 5109610. PMID 27877266.
- ^ Lynch, Richard J.M. (August 2011). "Zinc in the mouth, its interactions with dental enamel and possible effects on caries; a review of the literature". International Dental Journal. 61 (Suppl 3): 46–54. doi:10.1111/j.1875-595X.2011.00049.x. PMC 9374993. PMID 21762155.
- ^ Cortelli, José Roberto; Barbosa, Mônica Dourado Silva; Westphal, Miriam Ardigó (August 2008). "Halitosis: a review of associated factors and therapeutic approach". Brazilian Oral Research. 22 (suppl 1): 44–54. doi:10.1590/S1806-83242008000500007. PMID 19838550.
- ^ "SmartMouth Clinical DDS Activated Mouthwash". smartmouth.com.
- ^ "Oxyfresh". Oxyfresh.com.
- ^ "Dr ZinX". drzinx.com.
- ^ Steenberghe, Daniel Van; Avontroodt, Pieter; Peeters, Wouter; Pauwels, Martine; Coucke, Wim; Lijnen, An; Quirynen, Marc (September 2001). "Effect of Different Mouthrinses on Morning Breath". Journal of Periodontology. 72 (9): 1183–1191. doi:10.1902/jop.2000.72.9.1183. PMID 11577950.
- ^ Harper, D. Scott; Mueller, Laura J.; Fine, James B.; Gordon, Jeffrey; Laster, Larry L. (June 1990). "Clinical Efficacy of a Dentifrice and Oral Rinse Containing Sanguinaria Extract and Zinc Chloride During 6 Months of Use". Journal of Periodontology. 61 (6): 352–358. doi:10.1902/jop.1990.61.6.352. PMID 2195152.
- ^ a b Gupta, Mrinal; Mahajan, Vikram K.; Mehta, Karaninder S.; Chauhan, Pushpinder S. (2014). "Zinc Therapy in Dermatology: A Review". Dermatology Research and Practice. 2014: 709152. doi:10.1155/2014/709152. PMC 4120804. PMID 25120566.
- ^ 영국 국립 공식 (2008)."섹션 13.2.2.2 장벽 준비".
- ^ Williams, Cheryll (1 July 2012). Medicinal Plants in Australia Volume 3: Plants, Potions and Poisons. Rosenberg Publishing. p. 309. ISBN 978-1-925078-07-7. Retrieved 8 March 2023.
- ^ Nathan, Alan (2010). Non-prescription Medicines. Pharmaceutical Press. p. 206. ISBN 978-0-85369-886-9. Retrieved 8 March 2023.
- ^ Hughes G, McLean NR (December 1988). "Zinc oxide tape: a useful dressing for the recalcitrant finger-tip and soft-tissue injury". Archives of Emergency Medicine. 5 (4): 223–7. doi:10.1136/emj.5.4.223. PMC 1285538. PMID 3233136.
- ^ Dhatu A (10 October 2019). "Zinc oxide as the chemical for skin care". Retrieved 22 October 2019.
- ^ "Critical Wavelength & Broad Spectrum UV Protection". mycpss.com. Retrieved 15 April 2018.
- ^ More BD (2007). "Physical sunscreens: on the comeback trail". Indian Journal of Dermatology, Venereology and Leprology. 73 (2): 80–5. doi:10.4103/0378-6323.31890. PMID 17456911.
- ^ "Sunscreen". U.S. Food and Drug Administration.
- ^ Mitchnick MA, Fairhurst D, Pinnell SR (January 1999). "Microfine zinc oxide (Z-cote) as a photostable UVA/UVB sunblock agent". Journal of the American Academy of Dermatology. 40 (1): 85–90. doi:10.1016/S0190-9622(99)70532-3. PMID 9922017.
- ^ "What to Look for in a Sunscreen". The New York Times. June 10, 2009.
- ^ Agren MS (2009). "Percutaneous absorption of zinc from zinc oxide applied topically to intact skin in man". Dermatologica. 180 (1): 36–9. doi:10.1159/000247982. PMID 2307275.
- ^ a b Burnett ME, Wang SQ (April 2011). "Current sunscreen controversies: a critical review". Photodermatology, Photoimmunology & Photomedicine. 27 (2): 58–67. doi:10.1111/j.1600-0781.2011.00557.x. PMID 21392107. S2CID 29173997.
- ^ 퀘이커 시리얼 함량.quakeroats.com
- ^ St Clair K (2016). The Secret Lives of Colour. London: John Murray. p. 40. ISBN 9781473630819. OCLC 936144129.
- ^ Kunn, H. (1986) "Zinc White", pp. 169-186 in Artists' Positions. 그들의 역사와 특징에 관한 수첩, Vol. 1. L. Feller (ed.)케임브리지 대학 출판부, 런던.ISBN 978-0521303743
- ^ 빈센트 반 고흐, '사이프러스와 함께한 밀밭, 1889, ColorLex에서 색소 분석
- ^ Bouchez C. "The Lowdown on Mineral Makeup". WebMD. Retrieved January 25, 2009.
- ^ 미국 환경보호청: 자외선 차단제 자외선 차단제의 유효 성분은 무엇일까요 – 신체 성분:"물리적 화합물인 이산화티타늄과 산화아연은 UVA와 UVB 광선을 모두 반사, 산란, 흡수합니다."표에는 UVA 및 UVB에 대한 광범위한 물리적 보호를 제공하는 것으로 나와 있습니다.
- ^ 날카롭게 보는 동안 날카롭게 보세요.NASA 과학 기술 정보 (2006).2009년 10월 17일 회수.JPL 과학자들, 염료와 "자외선을 흡수하는 산화아연"을 이용한 자외선 차단 선글라스 개발
- ^ Schmidtmende L, MacManusdriscoll J (2007). "ZnO – nanostructures, defects, and devices". Materials Today. 10 (5): 40–48. doi:10.1016/S1369-7021(07)70078-0.
- ^ Guedri-Knani L, Gardette JL, Jacquet M, Rivaton A (2004). "Photoprotection of poly(ethylene-naphthalate) by zinc oxide coating". Surface and Coatings Technology. 180–181: 71–75. doi:10.1016/j.surfcoat.2003.10.039.
- ^ Moustaghfir A, Tomasella E, Rivaton A, Mailhot B, Jacquet M, Gardette JL, Cellier J (2004). "Sputtered zinc oxide coatings: structural study and application to the photoprotection of the polycarbonate". Surface and Coatings Technology. 180–181: 642–645. doi:10.1016/j.surfcoat.2003.10.109.
- ^ Cowan RL (2001). "BWR water chemistry?a delicate balance". Nuclear Energy. 40 (4): 245–252. doi:10.1680/nuen.40.4.245.39338.
- ^ Robinson, Victor S. (1978) "높은 표면적 및 향상된 강도의 입자상 산화아연 형상을 이용한 탈황 공정" 미국 특허 4,128,619
- ^ Liu XY, Shan CX, Zhu H, Li BH, Jiang MM, Yu SF, Shen DZ (September 2015). "Ultraviolet Lasers Realized via Electrostatic Doping Method". Scientific Reports. 5: 13641. Bibcode:2015NatSR...513641L. doi:10.1038/srep13641. PMC 4555170. PMID 26324054.
- ^ Zheng ZQ, Yao JD, Wang B, Yang GW (June 2015). "Light-controlling, flexible and transparent ethanol gas sensor based on ZnO nanoparticles for wearable devices". Scientific Reports. 5: 11070. Bibcode:2015NatSR...511070Z. doi:10.1038/srep11070. PMC 4468465. PMID 26076705.
- ^ Bakin A, El-Shaer A, Mofor AC, Al-Suleiman M, Schlenker E, Waag A (2007). "ZnMgO-ZnO quantum wells embedded in ZnO nanopillars: Towards realisation of nano-LEDs". Physica Status Solidi C. 4 (1): 158–161. Bibcode:2007PSSCR...4..158B. doi:10.1002/pssc.200673557.
- ^ Torres-Torres, C.; Castro-Chacón, J. H.; Castañeda, L.; Rojo, R. Rangel; Torres-Martínez, R.; Tamayo-Rivera, L.; Khomenko, A. V. (2011-08-15). "Ultrafast nonlinear optical response of photoconductive ZnO films with fluorine nanoparticles". Optics Express. 19 (17): 16346–16355. Bibcode:2011OExpr..1916346T. doi:10.1364/OE.19.016346. ISSN 1094-4087. PMID 21934998.
- ^ Bakin A (2010). "ZnO – GaN Hybrid Heterostructures as Potential Cost Efficient LED Technology". Proceedings of the IEEE. 98 (7): 1281–1287. doi:10.1109/JPROC.2009.2037444. S2CID 20442190.
- ^ Look D (2001). "Recent advances in ZnO materials and devices". Materials Science and Engineering B. 80 (1–3): 383–387. doi:10.1016/S0921-5107(00)00604-8.
- ^ Kucheyev SO, Williams JS, Jagadish C, Zou J, Evans C, Nelson AJ, Hamza AV (2003-03-31). "Ion-beam-produced structural defects in ZnO" (PDF). Physical Review B. 67 (9): 094115. Bibcode:2003PhRvB..67i4115K. doi:10.1103/physrevb.67.094115.
- ^ Li YB, Bando Y, Golberg D (2004). "ZnO nanoneedles with tip surface perturbations: Excellent field emitters". Applied Physics Letters. 84 (18): 3603. Bibcode:2004ApPhL..84.3603L. doi:10.1063/1.1738174.
- ^ Oh BY, Jeong MC, Moon TH, Lee W, Myoung JM, Hwang JY, Seo DS (2006). "Transparent conductive Al-doped ZnO films for liquid crystal displays". Journal of Applied Physics. 99 (12): 124505–124505–4. Bibcode:2006JAP....99l4505O. doi:10.1063/1.2206417.
- ^ Nomura K, Ohta H, Ueda K, Kamiya T, Hirano M, Hosono H (May 2003). "Thin-film transistor fabricated in single-crystalline transparent oxide semiconductor". Science. 300 (5623): 1269–72. Bibcode:2003Sci...300.1269N. doi:10.1126/science.1083212. PMID 12764192. S2CID 20791905.
- ^ Heo YW, Tien LC, Kwon Y, Norton DP, Pearton SJ, Kang BS, Ren F (2004). "Depletion-mode ZnO nanowire field-effect transistor". Applied Physics Letters. 85 (12): 2274. Bibcode:2004ApPhL..85.2274H. doi:10.1063/1.1794351.
- ^ Wang HT, Kang BS, Ren F, Tien LC, Sadik PW, Norton DP, Pearton SJ, Lin J (2005). "Hydrogen-selective sensing at room temperature with ZnO nanorods". Applied Physics Letters. 86 (24): 243503. Bibcode:2005ApPhL..86x3503W. doi:10.1063/1.1949707.
- ^ Tien LC, Sadik PW, Norton DP, Voss LF, Pearton SJ, Wang HT, et al. (2005). "Hydrogen sensing at room temperature with Pt-coated ZnO thin films and nanorods". Applied Physics Letters. 87 (22): 222106. Bibcode:2005ApPhL..87v2106T. doi:10.1063/1.2136070.
- ^ Sanguino, P.; Monteiro, Tiago; Bhattacharyya, S. R.; Dias, C. J.; Igreja, Rui; Franco, Ricardo (1 December 2014). "ZnO nanorods as immobilization layers for interdigitated capacitive immunosensors". Sensors and Actuators B: Chemical. 204: 211–217. doi:10.1016/j.snb.2014.06.141. ISSN 0925-4005.
- ^ Keim B (February 13, 2008). "Piezoelectric Nanowires Turn Fabric Into Power Source". Wired News. CondéNet. Archived from the original on February 15, 2008.
- ^ Qin Y, Wang X, Wang ZL (February 2008). "Microfibre-nanowire hybrid structure for energy scavenging". Nature. 451 (7180): 809–13. Bibcode:2008Natur.451..809Q. doi:10.1038/nature06601. PMID 18273015. S2CID 4411796.
- ^ "New Small-scale Generator Produces Alternating Current By Stretching Zinc Oxide Wires". Science Daily. November 10, 2008.
- ^ Zheng X, Shen G, Wang C, Li Y, Dunphy D, Hasan T, et al. (April 2017). "Bio-inspired Murray materials for mass transfer and activity". Nature Communications. 8: 14921. Bibcode:2017NatCo...814921Z. doi:10.1038/ncomms14921. PMC 5384213. PMID 28382972.
- ^ Sreejesh, M.; Dhanush, S.; Rossignol, F.; Nagaraja, H. S. (2017-04-15). "Microwave assisted synthesis of rGO/ZnO composites for non-enzymatic glucose sensing and supercapacitor applications". Ceramics International. 43 (6): 4895–4903. doi:10.1016/j.ceramint.2016.12.140. ISSN 0272-8842.
- ^ "Zinc oxide". Database of Select Committee on GRAS Substances (SCOGS) Reviews. U.S. Food and Drug Administration. Archived from the original on 16 April 2014. Retrieved 2009-08-03.
- ^ Gray T. "The Safety of Zinc Casting". The Wooden Periodic Table Table.
- ^ Calvert JB. "Introduction to Zinc and its Uses". Archived from the original on 2006-08-27.
- ^ Ginzburg AL, Blackburn RS, Santillan C, Truong L, Tanguay RL, Hutchison JE (2021). "Zinc oxide-induced changes to sunscreen ingredient efficacy and toxicity under UV irradiation". Photochem Photobiol Sci. 20 (10): 1273–1285. doi:10.1007/s43630-021-00101-2. PMC 8550398. PMID 34647278.
인용 출처
- Haynes, William M., ed. (2016). CRC Handbook of Chemistry and Physics (97th ed.). CRC Press. ISBN 9781498754293.
리뷰
- Özgür Ü, Alivov YI, Liu C, Teke A, Reshchikov M, Doğan S, et al. (2005). "A comprehensive review of ZnO materials and devices". Journal of Applied Physics. 98 (4): 041301–041301–103. Bibcode:2005JAP....98d1301O. doi:10.1063/1.1992666.
- Bakin A, Waag A (29 March 2011). "ZnO Epitaxial Growth". In Bhattacharya P, Fornari R, Kamimura H (eds.). Comprehensive Semiconductor Science and Technology 6 Volume Encyclopaedia. Elsevier. ISBN 978-0-444-53143-8.
- Baruah S, Dutta J (February 2009). "Hydrothermal growth of ZnO nanostructures". Science and Technology of Advanced Materials. 10 (1): 013001. Bibcode:2009STAdM..10a3001B. doi:10.1088/1468-6996/10/1/013001. PMC 5109597. PMID 27877250.
- Janisch R (2005). "Transition metal-doped TiO 2 and ZnO—present status of the field". Journal of Physics: Condensed Matter. 17 (27): R657–R689. Bibcode:2005JPCM...17R.657J. doi:10.1088/0953-8984/17/27/R01. S2CID 118610509.
- Heo YW (2004). "ZnO nanowire growth and devices". Materials Science and Engineering: R: Reports. 47 (1–2): 1–47. doi:10.1016/j.mser.2004.09.001.
- Klingshirn C (2007). "ZnO: From basics towards applications". Physica Status Solidi B. 244 (9): 3027–3073. Bibcode:2007PSSBR.244.3027K. doi:10.1002/pssb.200743072. S2CID 97461963.
- Klingshirn C (April 2007). "ZnO: material, physics and applications". ChemPhysChem. 8 (6): 782–803. doi:10.1002/cphc.200700002. PMID 17429819.
- Lu JG, Chang P, Fan Z (2006). "Quasi-one-dimensional metal oxide materials—Synthesis, properties and applications". Materials Science and Engineering: R: Reports. 52 (1–3): 49–91. CiteSeerX 10.1.1.125.7559. doi:10.1016/j.mser.2006.04.002.
- Xu S, Wang ZL (2011). "One-dimensional ZnO nanostructures: Solution growth and functional properties". Nano Research. 4 (11): 1013–1098. CiteSeerX 10.1.1.654.3359. doi:10.1007/s12274-011-0160-7. S2CID 137014543.
- Xu S, Wang ZL (2011). "Oxide nanowire arrays for light-emitting diodes and piezoelectric energy harvesters". Pure and Applied Chemistry. 83 (12): 2171–2198. doi:10.1351/PAC-CON-11-08-17. S2CID 18770461.
외부 링크
- 아연석속성
- 국제 화학 안전 카드 0208.
- 화학적 위험에 대한 NIOSH 포켓 가이드.
- 농약 특성 데이터베이스(PPDB) 내 산화아연
- ColorLex의 아연 백색 안료


