오자니모드
Ozanimod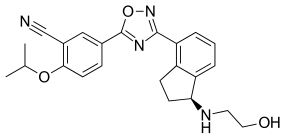 | |
 | |
| 임상자료 | |
|---|---|
| 상명 | 제포시아 |
| 기타 이름 | RPC-1063 |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인플러스 | a620029. |
| 라이센스 데이터 | |
| 임신 범주 |
|
| 경로: 행정 | 입으로 |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 | |
| 약동학 데이터 | |
| 제거 반감기 | 19시간 |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| ECHA InfoCard | 100.247.081 |
| 화학 및 물리적 데이터 | |
| 공식 | C23H24N4O3 |
| 어금질량 | 404.1987 g·messages−1 |
| 3D 모델(JSmol) | |
| |
| |
제포시아라는 상표명으로 판매되는 오자니모드는 다발성 경화증과 궤양성 대장염을 재발견하는 치료를 위한 면역억제제다.[2][3][4][5]그것은 스핑고신-1-인산염(S1P) 수용체 작용제로 작용하여 림프구를 말초 림프구 장기로 격리시키고 만성 염증 부위에서 떨어져 있다.[4]
가장 흔한 이상반응은 상부 호흡기 감염, 간경화합물 고도화, 직교 저혈압, 요로감염, 요통, 고혈압 등이다.[2][6]
오자니모드는 2020년 3월 미국,[6][7][8] 2020년 5월 유럽연합([3]EU), 2020년 7월 호주에서 의료용 허가를 받았다.[1][9]
의학적 용법
미국에서 오즈애니모드는 다발성 경화증의 재발 형태, 임상적으로 격리된 증후군, 재발성 질환, 활성 2차 진행성 질환을 포함하는 성인의 치료, 그리고 적당히 또는 심하게 활성화된 궤양성 대장염에 대해 지시된다.[2]
유럽 연합과 호주에서는 다발성 경화증을 재발시키는 성인의 치료를 위해 오즈애니모드가 표시된다.[9]
약리학
효력 및 선택성
S1P 수용체를 대상으로 하는 자가면역요법의 원리는 비선택적 S1P 모듈레이터인 핑골리모드(무역명 길레냐)의 개발 과정에서 수행된 임상 연구를 통해 확립되었다.[10][4][better source needed]오즈애니모드(Scripps-Receptos 화합물 RPC1063)의 전망은 핑골리모드 및 기타 대조군과 비교해도 비교가능하거나 더 나은 활성도와 선택성의 입증에 따라 달라졌다.[citation needed]그 발달의 발견 단계 동안에, 오자니모드는 S1P1 수용체와 S1P5 수용체의 선택적 작용제인 것으로 나타났다.[4][non-primary source needed]Specifically, in a discovery research report, ozanimod's equal potency and improved selectivity for S1P1 and S1P5 receptor family members were determined though a combination of inhibition, binding, and signalling assays for the S1P1, S1P2, S1P3, S1P4, and S1P5 receptor types alongside the same tests with fingolimod and other compounds.[4][11]
S1P1 수용체 유형의 작용제로서 오즈애니모드에 대한 효력은 GTPsS 결합 및 cAMP 억제 측정에서 관찰된 나노극 EC50 값을 통해, S1P5 유형의 경우 GTPγS 결합 측정에서 관찰된 나노극 EC50 값을 통해 확립되었다.[4]Measured alongside its binding to the S1P2, S1P3, and S1P4 receptor types, these concentration-response results supported a conclusion of an improved selectivity profile, with selectivity of S1P1 over S1P5 receptors at 27‐fold, and selectivity for S1P1 over S1P2, S1P3, and S1P4 receptors greater than 10,000‐fold.[4]
또한, 이 assays 관련 S1적극적인 요원과 fingolimod고 ozanimod S1P1 능력에 이러한 비교 자료와 흡사했다 mocravimod,[12]의phosphorylated(프로드 러그)형태siponimod에 비해서,지만 고가 selectivities 위(된ozanimod 효능에 대한 비교와 S1P1를 위해 다른 S1수용체에 선택성이 허용된다.versus 핑골리모드는 S1P3, S1P4 및 S1P5를 자극하는 데 있어 강력하며, S1P5 형식을 가진 시포니모드 전위제, S1P4 및 S1P5에 대항하여 어떤 식으로든 활성되어 S1P3, S1P4 및 S1P5에 대한 모크라비모드) 선택성을 향상시킨다.[4]
따라서, 이 연구는 "그것이 확립되었다"는 결론을 내렸다.RPC1063 [as] S1P1 활성과 "다른 알려진 S1P 수용체 작용제와 유사하고 덜 선택적인 S1P 수용체 작용제와 S1P5 수용체에 추가 작용제 활성을 갖는 S1P1 수용체의 잠재적 작용제"이다.[4]
약역학 및 약동학
S1P의 작용은 유비퀴틴-단백질 경로를 통해 그 내적화와 열화를 직접적으로 일으킨다.[13][better source needed]S1P의 손실은 특히 CD4+ CCR7+와 CD8+ CCR7+T 세포의 총 림프구 수의 감소를 초래한다.[4][14]
오자니모드는 경구 생체이용률이 높고, 순환 반감기가 약 19시간이며, 약 6시간 후에 혈장 농도가 가장 높다.[4][14]오자니모드는 두 개의 CYP 효소에 의해 두 개의 활성 대사물로 탈수되는데, 모두 유사한 약동학을 가지고 있다.[14]림프구 수 감소는 치료 중단 후 약 14일간 지속된다.[14]핑골리모드와 달리 활성화에 인산화가 필요 없고, 심장 이상이나 간독성을 입증하지도 않는다.[4]
역사
이 섹션은 Scripps의 발견 프로그램에 대한 더 많은 정보와 역사적으로, 오즈애니모드 이전의 납을 식별하는 초기 사건들에 대한 더 많은 정보를 가지고 확장될 필요가 있다.덧셈으로 도와줘도 된다.(2022년 2월) |
오자니모드는 휴 로젠, 에드워드 로버츠, 그리고 더 스크립스 연구소의 동료들에 의해 발명되었고, 이후 스타트업인 콘포스 사의 설립에서 초과 면허를 받았다.[15][16][better source needed][17] 셀젠은 2015년 지적 재산과 함께 콘센토스를 인수했다.[15][18][17]브리스톨 마이어스 스퀴브는 2019년에 셀젠을 인수했다(그리고 그것과 함께, 오즈애니모드와 그것의 나머지 제품과 파이프라인도 인수했다).[19][20][16]
미국 식품의약국(FDA)은 다발성 경화증을 재발견하는 형태를 가진 1767명의 피험자 2명의 임상시험(Trial 1/NCT02294058 및 Trial 2/NCT02047734)의 증거를 바탕으로 오자니모드를 승인했다.[7]이 실험은 미국, 벨라루스, 폴란드, 러시아, 우크라이나의 173개 센터에서 실시되었다.[7]피험자는 ozanimod 또는 대조군(interferon β1a, 다발성 경화증의 형태 재삽입 치료를 위해 승인된 제품)을 최대 1년(1차 시험에서) 또는 최대 2년(2차 시험에서) 동안 받았다.[7]실험이 끝날 때까지 대상자나 의료기관 모두 어떤 치료가 주어지고 있는지 알지 못했다.[7]오즈애니모드의 편익은 인터페론 β1a로 처리된 대상과 비교하여 질병의 재발 감소를 경험한 대상자의 비율을 바탕으로 평가되었다.[7]
2021년 5월, FDA는 온자니모드가 적당히 또는 심하게 활성화된 궤양성 대장염의 치료를 위한 추가 표시를 승인했다.[5]
임상시험
시금석
시금석은 궤양성 대장염 치료를 위한 2상 위약 조절 임상이다.[21][22]위약, 0.5mg 또는 1mg의 구강 오자니모드를 투여한 후 1주일간 복용량을 증가시킨 후 위약, 0.5mg 또는 1mg의 구강 오자니모드를 투여한 18~75세 환자 197명을 모집했다.1mg 복용량은 위약에 비해 궤양성 대장균의 임상적 완화율과 총 림프구 감소율이 약간 증가하였으며, 가장 흔한 부작용은 두통과 빈혈이었다.[21]저자들은 이 연구의 한계에는 짧은 기간과 작은 표본 크기가 포함되어 있어 안전성과 유효성을 평가할 수 없다는 것을 의미한다고 언급했다.[21]
광도
방사광은 다발성 경화증을 재발시키는 치료를 위한 이중 블라인드 위상 복합 임상실험이다.[23][24]2단계 임상시험의 경우, 다발성 경화증(확장 장애 상태 척도 2.9)이 재발한 18-55세의 258명의 환자에게 위약, 0.5mg 또는 1mg의 구강 오자니모드를 투여한 후 1주일의 용량 상승이 이어졌다.[23]Ozanimod는 24주 동안 다발성 경화증을 재발시키면서 참가자들의 MRI 병변 활동을 현저하게 줄였다.[23]두 가지 오즈애니모드 용량 모두 예상 림프구 수의 60-70% 감소에 도달했으며, 건강한 자원 봉사자들의 이전 1단계 연구와 일치하는 안전 프로파일과 함께 잘 허용되었다.[23][citation needed]위약과 비교했을 때 가장 흔한 부작용은 비인두염, 두통, 비뇨기과 감염으로 심각한 감염이나 심장의 부작용이 없었다.[23]이러한 결과를 통해, 두 가지 선량의 오자니모드는 2년 장기 3단계 실험으로 앞당겨졌고 2016년 11월 현재 완료되었지만 발표되지 않았다.[23][24]
선빔
선빔은 최적의 안전성-효익 관계를 가진 선량을 확립하기 위해 다발성 경화 단계 3차 임상시험으로 추정 환자 수가 1200명으로 두 번째다.[23][25]2014년 11월에 시작되었으며, 2017년 2월로 추정되는 완공일이 있다.[25][needs update]
사회와 문화
상업적
2013년 5월에 상장된 후 S1P 면역항암제로 표시된 임상 데이터 오즈애니모드로 주가가 급등했다.[15][26]2015년 8월 콘포스는 셀제네에 수중에 있는 현금과 신규채무를 결합해 [27][17]72억달러에 인수돼 셀제네 주가가 하루 만에 22% 상승했다.[citation needed]
콘포스-셀젠은 2016년 7월 오즈애니모드 합성에 특허를 냈다.[citation needed][28]셀젠의 염증과 면역학 프로필이 확대되면서 오즈애니모드에서 연간 40억~60억달러의 매출을 올릴 것으로 예상돼 왔지만,[29][26] FDA는 2018년 2월 셀젠의 최초 허가 신청을 거절했다.[30][18][31]셀젠은 2019년 3월 리필했다.[31]
이 제품의 새 주인 브리스톨 마이어스 스퀴브는 2020년 3월 26일 성인 표시인 재발성 다발성 경화증, 능동성 2차 진행성 다발성 경화증,[6] 임상적으로 격리된 신드롬에 대해 FDA 승인을 받았다.오자니모드는 2020년 5월 유럽연합([3]EU), 2020년 7월 호주에서 의료용 허가를 받았다[clarification needed].[1]
리서치
오자니모드는 크론병을 포함한 추가적인 면역염증 징후를 위해 개발 중이다.[32]
참조
- ^ a b c d "Zeposia Australian Prescription Medicine Decision Summary". Therapeutic Goods Administration (TGA). July 27, 2020. Retrieved August 16, 2020.
- ^ a b c d "Zeposia (ozanimod) capsules, for oral use" (PDF). Celgene Corporation. March 25, 2020. Retrieved March 26, 2020.
- ^ a b c d "Zeposia EPAR". European Medicines Agency. March 26, 2020. Retrieved August 17, 2020.
- ^ a b c d e f g h i j k l Scott FL, Clemons B, Brooks J, Brahmachary E, Powell R, Dedman H, et al. (June 2016). "Ozanimod (RPC1063) is a potent sphingosine-1-phosphate receptor-1 (S1P1) and receptor-5 (S1P5) agonist with autoimmune disease-modifying activity". British Journal of Pharmacology. 173 (11): 1778–92. doi:10.1111/bph.13476. PMC 4867749. PMID 26990079.
- ^ a b "U.S. Food and Drug Administration Approves Bristol Myers Squibb's Zeposia (ozanimod), an Oral Treatment for Adults with Moderately to Severely Active Ulcerative Colitis". Bristol Myers Squibb (Press release). May 27, 2021. Retrieved June 4, 2021.
- ^ a b c "U.S. Food and Drug Administration Approves Bristol Myers Squibb's Zeposia (ozanimod), a New Oral Treatment for Relapsing Forms of Multiple Sclerosis". Bristol-Myers Squibb Company (Press release). March 26, 2020. Retrieved March 26, 2020.
- ^ a b c d e f "Drug Trials Snapshots: Zeposia". U.S. Food and Drug Administration (FDA). March 25, 2020. Retrieved April 1, 2020.
 이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다..
이 글은 공개 도메인에 있는 이 출처의 텍스트를 통합한다.. - ^ "Drug Approval Package: Zeposia". U.S. Food and Drug Administration (FDA). April 23, 2020. Retrieved October 3, 2020.
- ^ a b Australian Public Assessment Report: Ozanimod hydrochloride (PDF) (Report). November 25, 2020.
- ^ 핑골리모드(Gilenya)를 가리키는 간행물도 발견번호로, FTY720을 가리킨다.예를 들어, 스콧 외 (2016)을 보라.
- ^ Per스콧, 44.1알(2016년),"S1P 수용체 가족을 위해 그 효능 및 RPC1063의 선택도forskolin‐induced cAMP 생산(S1P1 수용체),[35S]‐의 억제를 통해 평가를 받았다.GTPγS 결합 assays, 또는 β‐arrestin, 단순성으로, 인용에서 수용체 하위 유형 아래 첨자 달라졌다(S1P4 수용체)." 에드. 노트 신호(S1P1,2,3,5 수용체).이 글의 스타일에 맞추어
- ^ 시포니모드는 BAF312로 발견 출판물에 등장한다. 스콧 외 (2016) 참조.Mocravimod 발견 간행물에 KRP203로, Pérez-Jeldres T를 참조하십시오. Alvarez-Lobos M&Rivera-Nieves J(6월 2021년)[5월 13일, 2021년까지] 나타난다."물색 Sphingosine-1-Phosphate 신호 Immune-Mediated 질환에:.다중 Sclerosis" 넘어서요약 이지 81(9):985–1002. doi:10.1007/s40265-021-01528-8. 1.8116828.PMID 33983615.Erratum한 마약:에서.2021년 8월;81(12):1451{{ 들고 일기}}:CS1 maint:복수의 이름:작가들(링크)을 열거한다.
- ^ Jo E, Sanna MG, Gonzalez-Cabrera PJ, Thangada S, Tigyi G, Osborne DA, et al. (June 2005). "S1P1-selective in vivo-active agonists from high-throughput screening: off-the-shelf chemical probes of receptor interactions, signaling, and fate". Chemistry & Biology. 12 (6): 703–15. doi:10.1016/j.chembiol.2005.04.019. PMID 15975516.
- ^ a b c d Juif PE, Kraehenbuehl S, Dingemanse J (August 2016). "Clinical pharmacology, efficacy, and safety aspects of sphingosine-1-phosphate receptor modulators". Expert Opinion on Drug Metabolism & Toxicology. 12 (8): 879–95. doi:10.1080/17425255.2016.1196188. PMID 27249325. S2CID 21915268.
- ^ a b c Pollack, Andrew (July 14, 2015). "Celgene Agrees to $7.2 Billion Deal for Receptos". The New York Times (NYTimes.com). Retrieved February 5, 2022.
The biotechnology company Celgene agreed on Tuesday to pay $7.2 billion in cash to acquire Receptos, which is developing a potentially promising drug for autoimmune diseases. ... Receptos, based in San Diego, is developing a drug called ozanimod that is now in late-stage clinical trials as a treatment for multiple sclerosis and ulcerative colitis, with an approval possible for multiple sclerosis as early as 2018 and for ulcerative colitis the year after. / ... / Receptos was formed in 2009 with patents licensed from the Scripps Research Institute. ... ozanimod... was previously called RPC1063. / ... / Ozanimod has the same mechanism of action as Gilenya, a successful multiple sclerosis drug sold by Novartis. But Celgene executives say ozanimod could be safer than Gilenya, which has cardiac side effects.
- ^ a b "FDA approves ozanimod, a drug invented at Scripps Research, for treatment of multiple sclerosis". Scripps.edu (Press release). Retrieved December 5, 2020.
Hugh Rosen, MD, PhD... invented ozanimod along with fellow Scripps Research professor Edward Roberts, PhD, and their laboratory colleagues. / ... / The fundamental discoveries that led to ozanimod were reported by Rosen, Roberts and their Scripps Research colleagues in a series of papers from 2002 to 2008. In 2009, Scripps Research licensed ozanimod to biotechnology startup Receptos, which Celgene purchased in 2015 for $7.3 billion. Celgene was acquired by Bristol Myers Squibb in 2019.
- ^ a b c "Celgene to Acquire Receptos, Advancing Leadership in Immune-Inflammatory Diseases". Celgene Corporation (Press release). July 14, 2015. Archived from the original on June 4, 2021. Retrieved June 4, 2021.
Patents supporting Ozanimod were exclusively licensed to Receptos from The Scripps Research Institute (TSRI).
- ^ a b Taylor, Nick Paul (June 13, 2018). "Biotech: Celgene executive blames Receptos for ozanimod filing fail". Fierce Pharma. Framingham, Mass.: Questex. Retrieved February 5, 2022.
Nadim Ahmed said Celgene’s arm’s-length relationship with the biotech it bought for $7.2 billion three years ago led to a substandard filing and embarrassing refusal-to-file notice. / The FDA hit Celgene with the notice in February after a readthrough of the filing revealed the firm had failed to provide the necessary preclinical and clinical pharmacology information on the multiple sclerosis drug. That delayed approval of a key pipeline prospect with forecast peak sales of around $5 billion a year.
- ^ Liu, Angus (January 6, 2020). "The Top 10 Largest Biopharma M&A Deals in 2019 [1. Bristol-Myers Squibb/Celgene]". Fierce Pharma. Framingham, Mass.: Questex. p. 2. Retrieved February 5, 2022.
On Nov. 20, Bristol-Myers closed the takeover, officially putting an end to Celgene's 34-year run. Along the way, the legacy Celgene portfolio has turned up some positive news. / ...applications for ozanimod in relapsing forms of MS have been accepted by regulators in both the U.S. and Europe, setting up potential approvals next year.
- ^ "Bristol-Myers Squibb Completes Acquisition of Celgene, Creating a Leading Biopharma Company". Bristol Myers Squibb (Press release). April 12, 2019. Retrieved June 4, 2021.
- ^ a b c Sandborn WJ, Feagan BG, Wolf DC, D'Haens G, Vermeire S, Hanauer SB, et al. (May 2016). "Ozanimod Induction and Maintenance Treatment for Ulcerative Colitis". The New England Journal of Medicine. 374 (18): 1754–62. doi:10.1056/NEJMoa1513248. PMID 27144850.
- ^ "Efficacy and Safety Study of Ozanimod in Ulcerative Colitis". ClinicalTrials.gov. July 23, 2012. Retrieved June 4, 2021.
- ^ a b c d e f g Cohen JA, Arnold DL, Comi G, Bar-Or A, Gujrathi S, Hartung JP, et al. (April 2016). "Safety and efficacy of the selective sphingosine 1-phosphate receptor modulator ozanimod in relapsing multiple sclerosis (RADIANCE): a randomised, placebo-controlled, phase 2 trial". The Lancet. Neurology. 15 (4): 373–81. doi:10.1016/s1474-4422(16)00018-1. PMID 26879276. S2CID 3236201.
- ^ a b ClinicalTrials.gov의 "다발성 경화증 환자 재발견 시 RPC1063의 효능 및 안전 연구" 임상시험 번호 NCT01628393
- ^ a b "Study of Ozanimod (RPC1063) in Relapsing Multiple Sclerosis (MS)". ClinicalTrials.gov. November 19, 2014. Retrieved June 4, 2021.
- ^ a b "Celgene 2015 Annual Report" (PDF).
- ^ Rockoff, Jonathan D. (July 14, 2015). "Celgene to Buy Receptos for $7.2 Billion". The Wall Street Journal (WSJ.com). Retrieved February 5, 2022.
Cancer-drug company Celgene Corp. on Tuesday said it will pay $7.2 billion for Receptos Inc. in a bid to move deeper into the multibillion-dollar market for autoimmune diseases.
- ^ US 9388147, Yeager AR, Brahmachary E, Martinborough E, Scott FL, Timony GA, Brooks JL, Tamiya J, Huang L, Moorjani M, Boehm MF, Hanson MA, Peach R, "Selective sphingosine 1 phosphate receptor modulators and methods of chiral synthesis", published 22 October 2015, assigned to Receptos and Celgene International II Sarl
- ^ GE&BN Staff (July 14, 2015). "Celgene to Acquire Receptos for $7.2B". Genetic Engineering & Biotechnology News (GE&BN, GenEngNews.com). Larchmont, N.Y.: Mary Ann Liebert, Inc. Retrieved February 5, 2022.
Celgene has agreed to acquire Receptos for about $7.2 billion, in a deal intended to enhance the buyer’s inflammation and immunology (I&I) portfolio, the companies said today. / The deal will add to Celgene’s pipeline the Phase III compound Ozanimod, an oral, once-daily, selective sphingosine 1-phosphate 1 and 5 receptor modulator (S1P). / Ozanimod is expected to generate annual sales ranging from $4 billion to $6 billion—and expand an I&I franchise whose projected 2020 net product sales Celgene said are expected now to exceed $4 billion, up from the previous target of $3 billion... / Ozanimod is the subject of Phase III trials that include TRUE NORTH in ulcerative colitis (UC)... expected to generate data in 2018; and two trials in relapsing multiple sclerosis (RMS), RADIANCE and SUNBEAM... randomized, controlled, double-blind studies designed to compare... Ozanimod against interferon beta-1a (Avonex®) in patients with RMS.
- ^ Reuters Staff. "U.S. FDA Rejects Filing for Celgene MS Drug, Shares Fall". Reuters.com. Retrieved March 28, 2018.
U.S. health regulators have rejected Celgene Corp’s application seeking approval of a key multiple sclerosis drug due to insufficient data, the company said on Tuesday, a surprise development that will likely delay the entry to market of one of Celgene’s most important pipeline assets. / Celgene shares fell nearly 8 percent after it revealed that it had received a “refusal to file” letter from the ... FDA.. for its ozanimod for the treatment of patients with relapsing multiple sclerosis. / ...it expected U.S. approval of ozanimod by the end of this year and planned to file for European approval during the current quarter. The timeline for a U.S. approval decision is now far less certain. / ... / Upon preliminary review, the FDA determined that the nonclinical and clinical pharmacology sections in the new drug application are insufficient to permit a complete review, the company said.
- ^ a b Staines, Richard (March 27, 2019). "Celgene Refiles Potential MS Blockbuster Ozanimod with FDA". Pharmaphorum.com. West Byfleet, Surrey, England: Pharmaphorum Media Limited. Retrieved February 5, 2022.
Celgene has filed its highly anticipated oral MS drug ozanimod with the US regulator, more than a year after the FDA rejected it... / Last February Celgene received a “Refuse to File” notice from the FDA after finding issues with the dossier submitted by the company’s Receptos unit, which first developed the drug. / ... / Without Celgene overseeing the dossier... Receptos had failed to provide the necessary preclinical and clinical pharmacology information on the MS drug. / Celgene will be hoping the issues are in the past with its new filing for ozanimod in relapsing forms of [MS], which is tipped for annual sales in the region of $5 billion, although a newly-approved... Novartis’ rival pill Mayzent (siponimod) could make this much harder to achieve. / Ozanimod will be particularly important... should the $74 billion merger with Bristol-Myers Squibb go ahead next month.
- ^ Feagan BG, Sandborn WJ, Danese S, Wolf DC, Liu WJ, Hua SY, et al. (September 2020). "Ozanimod induction therapy for patients with moderate to severe Crohn's disease: a single-arm, phase 2, prospective observer-blinded endpoint study". The Lancet. Gastroenterology & Hepatology. 5 (9): 819–828. doi:10.1016/S2468-1253(20)30188-6. PMID 32553149.
외부 링크
- "Ozanimod". Drug Information Portal. U.S. National Library of Medicine.
- "Ozanimod hydrochloride". Drug Information Portal. U.S. National Library of Medicine.
- 임상 시험 번호 NCT02047734(ClinicalTrials.gov)의 "다발경화증 재발 시 오자니모드의 효능 및 안전 연구"
- 중궤양성 대장염에 대한 RPC1063의 안전성과 효능 실험에 대한 임상시험 번호 NCT02435992 ClinicalTrials.gov