백질이 사라지는 백혈구 뇌병증
Leukoencephalopathy with vanishing white matter| 백질이 사라지는 백혈구 뇌병증 | |
|---|---|
| 기타 이름 | 중추신경계 저근혈증을 동반한 소아 아탁시아, 소실백질 백혈구증, 소실백질뇌증, 난소기능장애를 동반한 소실백질백질백질백질혈구증, 포함, 미엘리노패스아중추증 디퓨사 |
 | |
| 이 상태는 자동 열성적 방식으로 유전된다. | |
사라지는 백질(VWM병)에 의한 백혈구뇌증은 자가 열성 신경질환이다.이 질병의 원인은 변환 개시 인자 EIF2B1, EIF2B2, EIF2B3, EIF2B4 또는 EIF2B5의 5개 유전자 부호화 중 어느 하나에서든 돌연변이가 있다.이 병은 백혈병이라고 불리는 질환군에 속한다.
증상 및 징후
발병은 보통 어린 시절에 발생하지만, 일부 성인 사례가 발견되었다.일반적으로 의사들은 어린이들에게서 그 증상들을 찾는다.증상으로는 소뇌 아탁스증, 경련성, 시신경 위축, 간질,[1] 운동기능 상실, 자극성, 구토, 혼수상태,[2] 발열까지 VWM에 묶여 있다.[3]VWM과 함께 발생하는 신경학적 장애와 증상은 국가별로 특별한 것이 아니다. 그들은 전 세계적으로 동일하다.[4]신경학적 이상이 성인으로서 발병을 경험하는 사람들에게 항상 존재하는 것은 아닐 수 있다.증상은 일반적으로 이전에 상당히 정상적으로 발육하던 어린이나 유아에게 나타난다.[citation needed]
원인들
VWM은 독특한 생화학적 이상을 가지고 있는 백혈병이다.[3]VWM의 독특한 특징은 과두정맥과 아스트로사이체만 부정적인 영향을 받는 반면 다른 활엽세포와 뉴런은 영향을 받지 않는 것처럼 보인다는 것이다.이것이 VWM의 핵심 질문이다.이 행동의 진짜 이유는 세포가 뇌에 있고 거의 연구되지 않았기 때문에 알려져 있지 않다.그러나, 그 분야의 대부분의 전문가들에 의해 일반적으로 받아들여지는 이론이 있다.이들 세포의 주요 특징은 단백질을 많이 합성한다는 점이다.이 세포들은 적은 양의 전구체로부터 많은 양의 단백질을 생성하기 때문에 지속적으로 작용하며 상당한 양의 스트레스를 받고 있다.그래서 eIF2B의 돌연변이와 함께 이 세포들이 마주치는 스트레스 양이 약간 증가하여 스트레스로 인해 실패하기 쉽다.[4]세포사멸 특성을 보이고 세포사멸 단백질을 표현하는 많은 양의 과두정맥류는 질병 초기 세포수 감소를 시사한다.[1]조기 난소 부전은 백질을 감소시키는 것과도 관련이 있다.다만 집중 조사를 통해 개인이 조기 난소 장애를 갖고 있다고 해서 반드시 VWM이 있는 것은 아니라고 판단했다.[5]
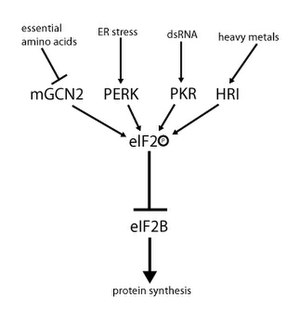
eIF2B의 역할
eIF2B는 eIF2를 위한 구아닌 뉴클레오티드 교환 인자로서 5개의 서브유닛으로 구성된다.가장 큰 서브 유닛인 eIF2B5는 VWM을 위한 가장 많은 돌연변이를 포함하고 있다. eIF2B는 mRNA를 단백질로 변환하는 것에 대한 규정과 매우 관련이 있는 복합체다.[6]eIF2B는 eIF2를 통해 eIF2가 재생되기 때문에 eIF2를 통한 번역 개시 시 구아노신-5'-트리인산염(GTP)에 대한 구아노신 디프인산염(GDP)의 교환에 필수적이다.eIF2B 활동의 감소는 VWM의 시작과 상관관계가 있다.[7]VWM 환자들 사이에서 공통적인 요인은 eIF2B(21개 지금까지 발견된 것)의 5개 서브유닛에서 돌연변이가 나타나며,[6] 이는 환자의 60% 이상에서 나타난다.이러한 돌연변이는 eIF2B의 활동 감소로 이어진다.가장 흔한 돌연변이는 R113H로 히스티딘과 아르기닌의 돌연변이다.돌연변이의 동질성 형태는 가장 심각한 형태다.[4]이 돌연변이는 설치류에도 기록되어 있지만, 인간에게는 VWM을 획득하지 않는다.[6]또 다른 일반적인 돌연변이는 eIF2B5 서브유닛에서 발견된 G584A이다.[8]eIF2B는 스트레스 관리의 중심적 역할(다른 스트레스 조건에서의 하향 조절 단백질 합성에 필수적임)을 하고 VWM 환자들은 스트레스에 매우 민감하기 때문에 스트레스와의 상관관계도 만들어 졌다.[7]단백질 eIF2B는 모든 세포에 존재하며, 이 단백질이 충분히 감소하면 세포에 부정적인 영향을 미치고, 0으로 감소하면 세포는 죽게 된다.영향을 받는 세포에서는 단백질이 약 50%로 감소하여 대부분의 세포에서는 기능성이 허용되지만, 대량의 단백질을 지속적으로 합성하고 그 안에서 가능한 한 많은 기능을 하는 단백질을 필요로 하기 때문에 활엽세포에서는 그렇지 않다.이것은 세포가 처리할 수 있는 스트레스 양의 기준을 낮출 것이고, 따라서 스트레스를 받는 환경에서는 이러한 세포에 해로운 영향을 끼칠 것이다.[4]eIF2B(2,4,&5)의 하위 유니트 중 3개에서의 돌연변이는 VWM과 조기 난소 장애 모두에서 발견되었다.[5]북미 크리족 역시 VWM으로 이어질 수 있는 특이 돌연변이 R195H가 있는 것으로 밝혀졌다.[6]연구를 거친 모든 환자들은 유전자에 하나의 돌연변이가 존재하여 eIF2B가 여전히 활성화되어 VWM으로 이어진다.두 번의 돌연변이가 발생하면, eIF2B 활동은 신체에 의해 중지될 것이다.[9]
신경병학
부검 결과 VWM의 완전한 효과가 입증되었다.회색 물질은 모든 특징에서 정상으로 유지되는 반면 흰 물질은 부드럽고 젤라틴이 된다.백색 물질의 희소반응은 가벼운 현미경으로 관찰되며, 영향을 받은 액손과 유파이버의 적은 숫자도 볼 수 있다.흰 물질에 있는 수많은 작은 충치들 또한 명백하다.VWM을 다른 백혈구들과 차별화하는 주요 특성은 거품 과점포도체의 존재에 있다.이러한 거품성 과두정맥류는 세포질 구조를 증가시키고 불규칙한 미토콘드리아를 더 많이 발생시키며 사멸률이 더 높은 경향이 있다.섬유성 감염을 동반한 비정상적인 형태의 아스트로사이테는 뇌의 모세혈관 전체에 매우 널리 퍼져있다.이상하게도, 아스트로시테는 과두정맥보다 더 많은 영향을 받는다; 아스트로시테의 시조체도 감소하지만, 악센트는 상대적으로 손상되지 않은 채로 남아있다.[10]
진단
대부분의 진단은 생후 2~6세 전후로 초기에 발생한다.[2]발병과 진단이 성년기 후반으로 접어든 사례도 있었다.이 시기에 발병한 사람들은 특히 인지력 저하 부족의 징후가 서로 다르다.전반적으로 성인형 VWM은 진단 당시 MRI가 일반적인 도구가 아니었기 때문에 검출이 어렵다.[3]흔히 볼 수 있는 징후로는 만성 진행성 신경악화 소뇌 경화증, 가소성, 정신적 쇠약, 시력 저하, 가벼운 간질, 손 떨림, 음식을 씹고 삼키는 능력이 어려워지고 머리 외상이나 공포증에 따른 섬유질 감염, 운동 기능 상실, 과민증 등이 있다.행동의 변화, 구토, 심지어 혼수상태까지.혼수상태에 빠진 사람들은, 만약 그들이 밖으로 나온다면, 보통 몇 년 안에 죽는다.[2]의사가 MRI를 찍지 않으면 진단이 어려울 수 있다.[4]
성인용 VWM 진단 사례 보고서
이 개인은 32세에 검사를 받았지만 5년 전부터 차이점을 지적하기 시작했다고 진술했다.그는 성적 충동, 사회적 고립, 설명할 수 없는 공격성과 슬픔, 동기의 상실, 불활성 웃음, 청각 환각, 사상 삽입, 망상, 그리고 명령적 논평에 주목했다.그는 유아용 침대에서도 흔히 볼 수 있는 아주 최소한의 신체적 장애를 보였다.하지만 그의 MRI는 VWM 질환의 특징적인 징후를 보여주었다.[11]
MRI
VWM 환자들의 MRI를 보면 백혈구 위축증이 잘 정의되어 있다.이 MRI들은 뇌의 백색 물질의 신호 강도의 역전을 보여준다.회생 순서와 백색 물질의 구멍도 보인다.[4]시간이 흐르면서 MRI는 흰 물질이 액체로 대체되면서 희소반응과 낭포성 변성을 보이는 데 탁월하다.이러한 변화를 보여주기 위해서는 백질을 높은 신호(T2-가중치), 양성자 밀도, 그리고 FLAIR(Fluid 감쇠된 반전 복구) 영상으로 표시하는 것이 가장 좋은 방법이다.T2-가중 영상에는 뇌척수액과 희소백질도 표시된다.남은 조직을 보고, 손상된 부분(열화율 결정에도 도움이 됨), 양성자 밀도, FLAIR 영상은 퇴화 백색 물질에서 복사 스트라이프 패턴을 보여 주는 것이 이상적이다.MRI 영상의 실패는 아직 뇌가 완전히 발달하지 않았기 때문에 유아에게 효과가 없고 해석이 어려운 것이다.일부 패턴과 징후가 보일 수 있지만 아직 단정적으로 진단하기는 어렵다.특히 MRI가 모호한 패턴을 보이거나 유아 뇌의 수분 함량이 높기 때문에 영유아에게 오진을 유발하는 경우가 많다.이 문제를 해결하는 가장 쉬운 방법은 다음 주에 MRI 후속 촬영이다.백색 물질 이상과 낭포성 변화가 있는 MRI의 잠재적으로 유사한 모습은 이토의 저선화증 환자, 로우의 어떤 형태(oculocerrebroaden) 또는 점막다당류의 일부 환자들에게서 볼 수 있다.[2]
일반적인 오진
종종 VWM과 함께, 그 질병에 대한 지식 부족은 의사들 사이에서 오진을 유발한다.VWM은 백혈구 증후군의 큰 그룹에 속해 있어 전이성 백혈구 등의 또 다른 유형으로 오진되는 경우가 많다.대개는 비특이성 백혈구증후군으로 분류된다.[4]부검 시 뇌의 특성은 종종 비정상적인 확산 경화증과 매우 유사하며, 예를 들어 섬유성 아스트로사이테와 극소량 수단소피지질의 유무와 같다.[2]성인용 VWM병은 정신질환과 함께 나타날 수 있으며 정신분열증과 구별하기 어려울 수 있다.[11]MRI를 잘못 인식하여 발생하는 일반적인 오진은 질식사, 합체감염, 대사질환 등이다.[2]
다발성 경화증은 오진일 경우가 많지만 신경학적 특성, 초창기 발병, MRI 이상 등으로 소아에서만 발병하는 경우가 많다.[1]그러나 두 질병 사이에는 많은 차이점이 있다.글래알 세포는 미엘린의 상실을 나타낸다.이러한 미엘린의 손실은 저산염이 발생하는 다른 질병에서 볼 수 있는 것과 다르다.VWM에서는 세포가 정상적인 양을 만들어내지 못하는 반면 MS와 같은 질병에서는 세포의 정상 양이 악화된다.또한 MS에서는 염증으로 인해 탈염 현상이 발생하는데, VWM에서는 그렇지 않다.[4]세포 차이는 대식세포와 미세글리아 침투율이 낮을 뿐 아니라 VWM에 T세포와 B세포의 부족도 포함한다.[1]마지막으로, MS 환자들은 광범위한 감마 효과를 가지고 있지만, VWM 환자들은 국부적인 영역에서만 감마 효과를 나타낸다.[4]
다발성 경화증(중복성 경화증)의 일부 비정형 형태는 특별히 구별하기 어려울 수 있지만 MRI 영상에는 도움이 될 수 있는 몇 가지 단서가 있다.[12]
치료
주로 머리에 대한 외상을 줄이고 생리적 스트레스를 피하기 위해 취할 수 있는 예방책만 있을 뿐 치료법은 없다.[2]멜라토닌은 엑시토독성, 산화스트레스 등 스트레스 요인에 노출된 글리알 세포에 세포 보호 특성을 제공하는 것으로 나타났다.이러한 스트레스 요인은 유전적으로 감소된 단백질 eIF2B의 활동을 가진 세포에 해로울 수 있다.그러나 이러한 사상을 연결하는 연구는 아직 실시되지 않았다.[4]
역학
광범위한 병리학적, 생화학적 검사를 실시했지만, eIF2B 유전자의 돌연변이가 발견된 소수를 연구해 원인을 밝혀냈다.[10]세계적으로 발병률을 파악하기 위한 효과적인 체계적 연구는 실시되지 않았지만, 지금까지 실시된 연구를 통해 백인 인구에서 더 널리 퍼져 있는 것으로 보인다.[2]VWM은 중동에서 발병 건수가 적은 것으로 보이며, 터키는 아직 보고된 사례가 없다.그 질병의 유병률은 의사의 진단 능력에 의해 제한된다.[4]2006년 현재 200명 이상의 사람들이 VWM으로 확인되었으며, 이 중 많은 사람들은 원래 분류되지 않은 백혈구 증후군으로 진단되었다.[10]
역사
이 질병이 처음으로 기록된 것은 1962년 이클이 36세의 여성을 연구했을 때였다.그녀의 첫 증상인 걸음걸이의 어려움, 그리고 이차적인 아메노르후아(Amerorrhoea)는 그녀가 31살이었을 때 일어났다.그녀는 일생 동안 사소한 신체적 외상에 이어 뇌가 크게 악화되는 만성적인 에피소드를 경험했다.사망과 동시에 뇌백질이 흩어진 낭포성 부위를 표시하는 부검이 실시되었다.이들 지역은 경미한 섬유성 아스트로사이테와 소량수단의 지질만 발견되는 과두정맥의 밀집된 그물로 둘러싸여 있었다.[2]
해가 지날수록 비슷한 증상을 보이는 유사 환자들의 계정이 더 많이 기록되었다. 그러나 아무도 모든 계정을 같은 질병으로 분류하지 않았다.하네펠트 박사와 쉬프만 박사와 그들의 동료들이 이 병을 소아기부터 진행성 백혈구 뇌병증이라고 확인한 것은 1993-94년이 되어서였다.그들은 그것이 자동 열성적이라고 결정했다.그들은 또한 머리 외상이 VWM의 발병의 계기가 되는 것을 보았다.그들이 이 환자들을 연결시킬 수 있게 한 주요 요인은 정상적인 백색 물질 신호가 사라지고 종종 젖산염과 포도당을 나타내는 공명기로 대체되는 자기저항 분광법의 결과였다.그들은 그 원인이 저산염이라는 것을 알아냈다.1997-98년, 마르조 S. 반 데르 크나프 박사와 동료들은 다른 환자 세트에서도 같은 특성을 보였지만, 이 환자들 또한 열감염증을 나타냈다.판데르 크나프 박사는 자기저항 분광학뿐만 아니라 MRI를 사용했으며 뇌백질[2] 및 물질[7] 희석작용의 진행 중인 낭포성 변성이 저염증보다는 병을 더 잘 묘사하고 있다고 판단하고 그 이름을 소멸하는 백질이라고 제안했다.[2]박사님이 제안한 이름.1994년 쉬프만, 중앙 저절제술(CACH)이 있는 소아 아탁시아(Ataxia)는 또 다른 일반적으로 통용되는 이름이다.[7]
참고 항목
- 스테니스 재단
- CADASIL(하구경색 및 백혈구 뇌병증 포함 추간 자가 우성 동맥병)
- 진행성 다초점 백혈구 뇌병증
- 전이성 백혈구증
- 일반백혈뇌증
참조
- ^ a b c d Kuhlmann, T.; Lassmann, H.; Bruck, W (2008). "Diagnosis of inflammatory demyelination in biopsy specimens: a practical approach". Acta Neuropathol. 115 (3): 275–287. doi:10.1007/s00401-007-0320-8. PMC 2668559. PMID 18175128.
- ^ a b c d e f g h i j k van der Knaap, M.S.; Pronk, J.C.; Scheper, G.C. (2006). "Vanishing White Matter Disease". Lancet Neurology. 5 (5): 413–423. doi:10.1016/S1474-4422(06)70440-9. PMID 16632312. S2CID 44301370.
- ^ a b c Baumann, N.; Turpin, J-C (2000). "Adult-onset leukodystrophies". Journal of Neurology. 247 (10): 751–9. doi:10.1007/s004150070088. PMID 11127529. S2CID 6817046.
- ^ a b c d e f g h i j k 라파엘 쉬프만 박사(텍사스 댈러스 베일러 연구소장).전화 인터뷰 2008-11-08
- ^ a b Goswami, D.; Conway, G.S. (2005). "Premature ovarian failure". Human Reproduction Update. 11 (4): 391–410. doi:10.1093/humupd/dmi012. PMID 15919682. S2CID 23396413.
- ^ a b c d Abbott, C.M.; Proud, C.G. (2004). "Translation factors: in sickness and in health". Trends in Biochemical Sciences. 29 (1): 25–31. doi:10.1016/j.tibs.2003.11.006. PMID 14729329.
- ^ a b c d Pronk, J.C.; van Kollenburg, B.; Scheper, G.C.; van der Knaap, M.S. (2006). "Vanishing White Matter Disease: A Review with Focus on Its Genetics". Mental Retardation and Developmental Disabilities Research Reviews. 12 (2): 123–8. doi:10.1002/mrdd.20104. PMID 16807905.
- ^ Laberge, A-M.; Michaud, J.; Richter, A.; Lambert, M.; Brais, B.; Mitchell G.A. (2005). "Population history and its impact on medical genetics in Quebec". Clinical Genetics. 68 (4): 287–301. doi:10.1111/j.1399-0004.2005.00497.x. PMID 16143014. S2CID 26368522.
- ^ Scheper, G.C.; Proud, C.G.; van der Knaap, M.S. (2006). "Defective translation initiation causes vanishing of cerebral white matter". Trends in Molecular Medicine. 12 (4): 159–166. doi:10.1016/j.molmed.2006.02.006. PMID 16545608.
- ^ a b c Schiffmann, R.; Elroy-Stein, O. (2006). "Childhood ataxia with CNS hypomyelination/vanishing white matter disease – A common leukodystrophy caused by abnormal control of protein synthesis". Molecular Genetics and Metabolism. 88 (1): 7–15. doi:10.1016/j.ymgme.2005.10.019. PMID 16378743.
- ^ a b Denier C, Orgibet A, Roffi F, Jouvent E, Buhl C, Niel F, Boespflug-Tanguy O, Said G, Ducreux D (2007). "Adult-onset vanishing white matter leukoencephalopathy presenting as psychosis". Neurology. 68 (18): 1538–9. doi:10.1212/01.wnl.0000260701.76868.44. PMID 17470759. S2CID 28752485.
- ^ Ayrignac 등.뇌 자기공명영상촬영은 뇌하수체 병변과 사라지는 백질병과의 비정형 다발성 경화증 분화에 도움이 된다, 유럽 신경학술지 제23권 제6호, 2016년 1월 04호, doi:10.111/ene.12931호
외부 링크
- "Leukoencephalopathy with vanishing white matter". Neurographics. 2 (1). March 2012.