황체화호르몬
Luteinizing hormone| 융모성 고나도트로핀 알파 | |||||||
|---|---|---|---|---|---|---|---|
| 식별자 | |||||||
| 기호. | CGA | ||||||
| Alt. | HCG, GPHA, GPHA1 | ||||||
| NCBI유전자 | 1081 | ||||||
| HGNC | 1885 | ||||||
| 옴 | 118850 | ||||||
| 참조 | NM_000735 | ||||||
| 유니프로트 | P01215 | ||||||
| 기타 데이터 | |||||||
| 궤적 | 제6장 Q14-q21 | ||||||
| |||||||
| 황체화호르몬β폴리펩티드 | |||||||
|---|---|---|---|---|---|---|---|
| 식별자 | |||||||
| 기호. | LHB | ||||||
| NCBI유전자 | 3972 | ||||||
| HGNC | 6584 | ||||||
| 옴 | 152780 | ||||||
| 참조 | NM_000894 | ||||||
| 유니프로트 | P01229 | ||||||
| 기타 데이터 | |||||||
| 궤적 | 19장 문제 13.3 | ||||||
| |||||||
황체화 호르몬(LH, 황체화 호르몬[1], 루트로핀, 때로는 루트로핀으로도[2] 알려져 있음)은 뇌하수체 전엽의 성선 자극 세포에 의해 생성되는 호르몬이다.LH의 생산은 시상하부에서 나오는 성선 방출 호르몬(GnRH)[3]에 의해 조절된다.여성의 경우, LH의 급격한 상승("LH 급증")은 배란과[4] 황체 발달을 유발한다.LH가 간질세포자극호르몬(ICSH)[5]이라고도 불렸던 남성의 경우, LH는 [4]테스토스테론의 레이디지 세포 생성을 자극한다.그것은 모낭자극호르몬(FSH)과 상승작용을 한다.
구조.
LH는 헤테로 이합체 당단백질이다.각각의 단량체는 당단백질 분자이며, 하나의 알파와 하나의 베타 서브유닛은 완전한 기능성 단백질을 만든다.
그것의 구조는 다른 당단백질 호르몬, 모낭자극호르몬, 갑상선자극호르몬, 인간 융모성 성선자극호르몬과 유사하다.단백질 이합체에는 비공유적으로 연관된 [6]2개의 글리코펩티드 서브유닛(알파 서브유닛 및 베타 서브유닛으로 표시됨)이 포함되어 있다.
- LH, FSH, TSH 및 hCG의 알파 서브유닛은 동일하며 인간에게는 92개의 아미노산이 있지만 다른 거의 모든 척추동물 종에는 96개의 아미노산이 포함되어 있습니다(당단백질 호르몬은 무척추동물에는 존재하지 않습니다).
- 베타 서브유닛은 다양합니다.LH는 120개의 아미노산(LHB)으로 구성된 베타 서브유닛을 가지고 있어 특정 생물학적 작용을 하며 LH 수용체와의 상호작용의 특이성을 담당합니다.이 베타 서브유닛은 hCG의 베타 서브유닛과 큰 호몰로지를 나타내며 둘 다 동일한 수용체를 자극하는 아미노산 배열을 포함한다.단, hCG 베타 서브유닛은 24개의 아미노산을 추가로 포함하고 있으며, 두 호르몬의 당분 구성이 다르다.
이들 올리고당의 다른 조성은 생물 활성과 분해 속도에 영향을 미친다.LH의 생물학적 반감기는 20분으로 FSH(3-4시간)와 hCG(24시간)[citation needed]보다 짧다.LH의 생물학적 반감기는 피하 23시간[7] 또는 10-12시간의 말기 반감기 10-12시간이다.[8]
유전자
알파 서브유닛의 유전자는 6q12.21 염색체에 위치한다.
황체화 호르몬 베타 서브유닛 유전자는 염색체 19q13.32의 LHB/CGB 유전자 클러스터에 국재되어 있다.알파 유전자 활성과 대조적으로 베타 LH 서브유닛 유전자 활성은 뇌하수체 성선 자극 세포로 제한된다.시상하부에서 나오는 성선 분비 호르몬에 의해 조절됩니다.인히빈, 액티빈 및 성호르몬은 LH의 베타 서브유닛 생산을 위한 유전자 활동에 영향을 미치지 않는다.
기능.
수컷과 암컷 모두에서 LH는 안드로겐을 생성하기 위해 생식선의 내분비세포에 작용합니다.
여성의 영향
LH는 에스트라디올 생산을 위해 안드로겐과 호르몬 전구체를 제공하는 난소에서 테카 세포를 지지합니다.월경 시에 FSH는 모낭 성장을 시작하며, 특히 과립상세포에 [9]영향을 미친다.에스트로겐이 증가함에 따라 성숙된 모낭에서도 LH 수용체가 발현되어 에스트라디올이 더 많이 생성된다.결국 모낭이 완전히 성숙하면 모낭에 의한 17α-히드록시프로게스테론 생성의 스파이크가 에스트로겐 생성을 억제하고 시상하부의 GnRH에 대한 에스트로겐 매개 음성피드백의 감소를 초래하여 뇌하수체 [10]전엽으로부터의 LH 방출을 촉진한다.그러나 LH 피크의 또 다른 이론은 에스트라디올로부터의 양의 피드백 메커니즘입니다.이 수치는 엽상 단계를 통해 계속 상승하며, 알 수 없는 임계값에 도달하면 [11]LH의 정점이 됩니다.이 효과는 낮은 수준에서 나타나는 일반적인 음성 피드백 메커니즘과는 반대입니다.즉, 메커니즘은 아직 명확하지 않습니다.LH 생산 증가는 24시간에서 48시간 동안만 지속된다.이 "LH 급증"은 배란을 유발하고, 따라서 난포에서 난자를 방출할 뿐만 아니라, 가능한 착상을 위한 자궁 내막을 준비하기 위해 프로게스테론을 생성하는 말뭉치 황체로의 잔여포의 전환을 시작합니다.LH는 생리 주기의 두 번째 2주 동안 황체 기능을 유지하기 위해 필요하다.임신이 되면 LH 수치가 낮아지고 대신 LH와 매우 비슷하지만 새로운 태반에서 분비되는 호르몬인 hCG(인간 융모성 성선 자극 호르몬)의 작용으로 황체 기능이 유지된다.
성선 스테로이드(에스트로겐과 안드로겐)는 일반적으로 시상하부 수준과 성선 자극에서 GnRH-1 방출에 부정적인 피드백 효과를 가지며 GnRH에 대한 민감도를 감소시킨다.에스트로겐에 의한 양성 피드백은 암컷 포유류의 생식선 축에서도 발생하며 배란을 자극하는 LH의 중간 주기 급증을 일으킨다.에스트로겐은 ARC의 kiss1 뉴런에서 키스펩틴(Kp) 방출을 억제하지만, 에스트로겐은 AVPV의 Kp 뉴런에서 Kp 방출을 자극합니다.에스트로겐의 수치가 점차 상승함에 따라 긍정적인 효과가 우세해지면서 LH의 급등으로 이어집니다.GnRH-1 뉴런을 자극하는 GABA 분비 뉴런도 GnRH-1 방출을 자극할 수 있다.이러한 GABA 뉴런은 또한 ER을 가지고 있으며 GnRH-1 급증을 일으킬 수 있다.GnRH-1 방출에 대한 엔도르핀의 억제 작용의 일부는 이러한 GABA 뉴런의 억제를 통해 이루어진다.배란 시 난포의 파열은 에스트로겐 합성의 급격한 저하와 난소 내 황체에 의한 프로게스테론 분비의 현저한 증가를 야기하며, GnRH-1의 [12]시상하부 분비에 대한 지배적인 부정적인 피드백을 회복시킨다.
남성의 영향
LH는 고환의 레이디지 세포에 작용하고 고나도트로핀 방출 호르몬(GnRH)[13]에 의해 조절됩니다.레이디지 세포는 LH의 통제 하에 테스토스테론을 생성한다. LH는 레이디지 세포의 막 표면에 있는 LH 수용체에 결합한다.이 수용체에 결합하면 콜레스테롤이 미토콘드리아로 전이되도록 하는 2차 메신저인 고리형 아데노신 일인산(cAMP)이 증가한다.미토콘드리아 내에서 콜레스테롤은 CYP11A1에 [14]의해 프레그네놀론으로 전환된다.그리고 나서, 피그네놀론은 데히드로에피안드로스테론(DHEA)[15]으로 전환된다.DHEA는 3β-히드록시스테로이드탈수소효소(3β-HSD)[16]에 의해 안드로스테디온으로 전환되고, 17β-히드록시스테로이드탈수소효소(HSD17B)에 의해 최종적으로 테스토스테론으로 전환된다.사춘기의 시작은 두 가지 주요 호르몬에 의해 제어된다: FSH는 정자 형성을 시작하고 LH는 정자 형성에 내분비 활성과 자궁 내 활동을 모두 하는 안드로겐인 테스토스테론의 [17]방출을 신호한다.
LH는 뇌하수체에서 방출되어 고나도트로핀 방출 호르몬의 펄스에 의해 제어된다.혈류 테스토스테론 수치가 낮으면 뇌하수체가 자극돼 [13]LH를 방출하고 테스토스테론 수치가 높아지면 음의 피드백 루프를 통해 뇌하수체에 작용해 [citation needed]GnRH와 LH의 방출을 억제한다.안드로겐(테스토스테론 및 디히드로테스토스테론 포함)은 송과선에서 모노아민산화효소(MAO)를 억제하여 멜라토닌에 의해 고나도트로핀-억제호르몬(GnIH)[18] 합성 및 분비를 증가시켜 멜라토닌을 증가시키고 LH 및 FSH를 감소시킨다.테스토스테론은 또한 LH를 억제하기 위해 에스트라디올(E2)로 방향족화할 수 있다. E2는 시상하부에서 뇌하수체로 [19]가는 GnRH에 대한 펄스 진폭과 반응을 감소시킨다.
LH와 테스토스테론 혈중 수치의 변화와 맥박 분비는 남성의 성적 [20]각성의 변화에 의해 유발된다.
정상 수준
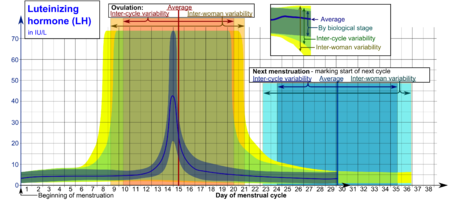
- 생물학적 단계로 표시된 범위는 생물학적 진행의 다른 지표와 관련하여 면밀하게 모니터링되는 생리 주기에서 사용될 수 있으며, 시간 척도는 각각 평균 주기에 비해 얼마나 빨리 또는 얼마나 느리게 진행되는지 압축 또는 연장된다.
- 주기 간 변동으로 표시된 범위는 생리 시작만 알려진 비감시 사이클에서 사용하기에 더 적합하지만, 여성이 배란기의 평균 주기 길이와 시간을 정확히 알고 있고, 시간 척도가 압축되거나 연장되어 여성의 평균 평균 주기이다.연령 주기 길이가 모집단의 평균보다 각각 짧거나 길다.
- 여성간 변동으로 표시된 범위는 배란의 평균 주기 길이와 시간을 알 수 없을 때 사용하기에 더 적합하지만 월경의 시작만 제시된다.
LH 수치는 보통 어린 시절과 여성의 경우 낮고, 폐경 이후 높다.LH는 맥박으로 분비되기 때문에 충분한 시간 동안 농도를 따라가야 혈중 수치에 대한 적절한 정보를 얻을 수 있다.
생식기 동안, 일반적인 수치는 1 ~ 20 IU/L 사이이다.생리적으로 높은 LH 수준은 LH 서지(v.s.) 동안 나타나고 일반적으로 48시간 동안 지속됩니다.
18세 이상의 남성에서 기준 범위는 1.8-8.6 IU/[22]L로 추정되었다.
LH는 국제 단위(IU)로 측정됩니다.표본에 포함된 LH의 양을 IU 단위로 수량화할 때는 LH의 로트가 해마다 크게 다를 수 있으므로 어떤 국제 표준에 따라 보정되었는지 아는 것이 중요합니다.사람의 비뇨기 LH의 경우, 가장 최근에 IU 1개가 96/602로 표시된 앰풀의 1/189분의 1로 정의되고 NIBSC에 의해 분포되며, 단일 IU의 LH 단백질 약 0.04656μg에 해당하지만, 이전 표준 버전은 여전히 널리 [23][24]사용되고 있다.
배란 예측
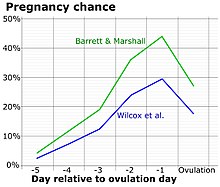
황체화 호르몬의 급격한 방출은 배란이 임박했음을 나타낸다.LH는 배란이 [26]예상되는 시기에 일반적으로 매일 수행되는 배뇨 예측 키트(OPK, LH 키트)에 의해 검출될 수 있습니다.음수에서 양수 판독치로 전환하면 배란이 24-48시간 내에 일어나 임신하려는 [27]의도로 이틀 동안 성관계나 인공수정을 할 수 있다는 것을 암시할 수 있다.
권장되는 테스트 빈도는 제조업체마다 다릅니다.예를 들어 Clearblue 테스트는 매일 수행되며 주파수가 증가해도 LH [28]서지를 놓칠 위험이 감소하지 않습니다.반면 중국 기업 난퉁 에겐스 바이오테크놀로지는 하루에 [29]두 번 테스트를 사용할 것을 권장하고 있다.하루에 한 번 검사를 하는 경우, 임신률과 [30]관련하여 아침과 저녁 사이에 LH 검사 사이에 유의한 차이가 발견되지 않았으며, 하루 중 몇 시에 검사를 받을 것인지의 권장 사항은 제조업체와 의료 [31]종사자 간에 차이가 있다.테스트는 색상 변경용지 스트립을 사용하여 수동으로 읽거나 전자 기기의 도움을 받아 디지털 방식으로 읽을 수 있습니다.
황체화 호르몬 검사는 클리어블루 불임 [medical citation needed]모니터와 같은 검사에서 에스트라디올 검사와 결합될 수 있다.
LH 테스트의 민감도는 밀리 국제 단위로 측정되며 일반적으로 10 - 40 m.i.u. 범위에서 사용할 수 있다(숫자가 작을수록 [citation needed]민감도가 높다).
정자는 며칠 동안 여성에게서 생존할 수 있기 때문에, LH 검사는 피임 시술에 권장되지 않는다. 왜냐하면 LH의 급증은 일반적으로 가임 기간이 시작된 후에 발생하기 때문이다.
질병 상태
초과
뇌하수체 또는 중추 기원의 성조숙증을 가진 아동의 경우, LH 및 FSH 수치는 연령에 따라 낮은 수준이 아닌 생식 범위에 있을 수 있다.
생식기 동안, 상대적으로 높은 LH는 다낭포성 난소 증후군 환자에게서 자주 볼 수 있지만, 정상 생식 범위를 벗어난 LH 수치를 갖는 것은 드문 일이다.
지속적으로 높은 LH 수치는 생식선으로부터의 정상적인 제한 피드백이 없는 상황을 나타내며, 이로 인해 LH와 FSH가 모두 뇌하수체로 생성됩니다.폐경기에서는 이것이 전형적이지만, 생식기에는 비정상이다.다음과 같은 징후가 있을 수 있습니다.
- 조기 폐경
- 생식선 이상, 터너 증후군, 클라인펠터 증후군
- 거세
- 스와이어 증후군
- 다낭성 난소 증후군
- 선천성 부신 과형성의 특정 형태
- 고환 기능 상실
- 임신 - 베타HCG는 LH를 모방할 수 있으므로 테스트에서 LH가 상승한 것으로 나타날 수 있습니다.
주의: 황체화 호르몬 분비를 억제하는 약물은 부티나조신이다.[32]
부족.
LH의 분비가 감소하면 생식선 기능이 저하될 수 있습니다(고나디즘).이 상태는 일반적으로 남성들에게서 정상적인 수의 정자를 생산하지 못하는 것으로 나타난다.여성들에게서는 무월경이 흔하게 관찰된다.좌측 분비량이 매우 낮은 조건은 다음과 같습니다.
약으로
LH는 메노트로핀의 형태로 FSH와 혼합되어 사용 가능하며, 다른 형태의 요로 고나도트로핀도 사용할 수 있습니다.보다 정제된 형태의 뇨중 성선(gonadotropin)[36]은 FSH에 비해 LH 부분을 감소시킬 수 있다.이 모든 약들은 비경구적으로 투여되어야 한다.그것들은 난포 발달을 촉진하기 위해 불임 치료에 일반적으로 사용되며, 주목할 만한 것은 체외수정 치료이다.
종종 HCG 약물은 동일한 수용체를 활성화하기 때문에 LH 대체제로 사용됩니다.의학적으로 사용되는 hCG는 임산부의 소변에서 추출되며, 비용이 적게 들고, LH보다 반감기가 길다.
인산화에서의 역할
인산화란 유기화합물에 인산염을 첨가하는 생화학적 과정이다.스테로이드 생성은 콜레스테롤이 생물학적으로 활성화된 스테로이드 호르몬으로 전환되는 과정을 수반한다.최근의 연구는 PKA 신호 경로를 통한 LH가 [37]난소의 스테로이드 생성 세포의 미토콘드리아 내에서 DRP1의 인산화와 국재화를 조절한다는 것을 보여준다.
레퍼런스
- ^ GCSE Science Revision Biology "The Menstrual Cycle", retrieved 2022-03-23
- ^ Ujihara M, Yamamoto K, Nomura K, Toyoshima S, Demura H, Nakamura Y, et al. (June 1992). "Subunit-specific sulphation of oligosaccharides relating to charge-heterogeneity in porcine lutrophin isoforms". Glycobiology. 2 (3): 225–31. doi:10.1093/glycob/2.3.225. PMID 1498420.
- ^ Stamatiades, George A.; Kaiser, Ursula B. (2018-03-05). "Gonadotropin regulation by pulsatile GnRH: Signaling and gene expression". Molecular and Cellular Endocrinology. Signaling Pathways Regulating Pituitary Functions. 463: 131–141. doi:10.1016/j.mce.2017.10.015. ISSN 0303-7207. PMC 5812824. PMID 29102564.
- ^ a b Nosek, Thomas M. "Section 5/5ch9/s5ch9_5". Essentials of Human Physiology. Archived from the original on 2016-03-24.
- ^ Louvet JP, Harman SM, Ross GT (May 1975). "Effects of human chorionic gonadotropin, human interstitial cell stimulating hormone and human follicle-stimulating hormone on ovarian weights in estrogen-primed hypophysectomized immature female rats". Endocrinology. 96 (5): 1179–86. doi:10.1210/endo-96-5-1179. PMID 1122882.
- ^ Jiang X, Dias JA, He X (January 2014). "Structural biology of glycoprotein hormones and their receptors: insights to signaling". Molecular and Cellular Endocrinology. 382 (1): 424–451. doi:10.1016/j.mce.2013.08.021. PMID 24001578.
- ^ Ezcurra D, Humaidan P (October 2014). "A review of luteinising hormone and human chorionic gonadotropin when used in assisted reproductive technology". Reproductive Biology and Endocrinology. 12 (1): 95. doi:10.1186/1477-7827-12-95. PMC 4287577. PMID 25280580.
- ^ le Cotonnec JY, Porchet HC, Beltrami V, Munafo A (February 1998). "Clinical pharmacology of recombinant human luteinizing hormone: Part I. Pharmacokinetics after intravenous administration to healthy female volunteers and comparison with urinary human luteinizing hormone". Fertility and Sterility. 69 (2): 189–94. doi:10.1016/S0015-0282(97)00501-3. PMID 9496327.
- ^ Bowen R (13 May 2004). "Gonadotropins: Luteinizing and Follicle Stimulating Hormones". Colorado State University. Retrieved 12 March 2012.
- ^ Mahesh VB (January 2012). "Hirsutism, virilism, polycystic ovarian disease, and the steroid-gonadotropin-feedback system: a career retrospective". American Journal of Physiology. Endocrinology and Metabolism. 302 (1): E4–E18. doi:10.1152/ajpendo.00488.2011. PMC 3328092. PMID 22028409.
- ^ 가이튼과 홀 의학 생리학 교과서 2006년 1021페이지
- ^ Norris DO, Carr JA (2013). Vertebrate Endocrinology. Academic Press. p. 126. ISBN 978-0-12-396465-6.
- ^ a b "Male Medical Fertility Treatment: HCG + LH + Recombinant FSH To Increase Sperm Count Through Spermatogenisis". Archived from the original on February 19, 2015. Retrieved 6 April 2015.[어쩔 수 없는 의료원?]
- ^ Zirkin BR, Papadopoulos V (July 2018). "Leydig cells: formation, function, and regulation". Biology of Reproduction. 99 (1): 101–111. doi:10.1093/biolre/ioy059. PMC 6044347. PMID 29566165.
- ^ Akhtar MK, Kelly SL, Kaderbhai MA (November 2005). "Cytochrome b(5) modulation of 17{alpha} hydroxylase and 17-20 lyase (CYP17) activities in steroidogenesis". The Journal of Endocrinology. 187 (2): 267–74. doi:10.1677/joe.1.06375. PMID 16293774.
- ^ Liu L, Kang J, Ding X, Chen D, Zhou Y, Ma H (2015). "Dehydroepiandrosterone-Regulated Testosterone Biosynthesis via Activation of the ERK1/2 Signaling Pathway in Primary Rat Leydig Cells". Cellular Physiology and Biochemistry. 36 (5): 1778–92. doi:10.1159/000430150. PMID 26184424. S2CID 13816368.
- ^ Oduwole OO, Peltoketo H, Huhtaniemi IT (2018). "Role of Follicle-Stimulating Hormone in Spermatogenesis". Frontiers in Endocrinology. Nutrients. 9: 763. doi:10.3389/fendo.2018.00763. PMC 6302021. PMID 30619093.
- ^ Ubuka T, Son YL, Tobari Y, Narihiro M, Bentley GE, Kriegsfeld LJ, Tsutsui K (2014). "Central and direct regulation of testicular activity by gonadotropin-inhibitory hormone and its receptor". Frontiers in Endocrinology. 5: 8. doi:10.3389/fendo.2014.00008. PMC 3902780. PMID 24478760.
- ^ Pitteloud N, Dwyer AA, DeCruz S, Lee H, Boepple PA, Crowley WF, Hayes FJ (March 2008). "Inhibition of luteinizing hormone secretion by testosterone in men requires aromatization for its pituitary but not its hypothalamic effects: evidence from the tandem study of normal and gonadotropin-releasing hormone-deficient men". The Journal of Clinical Endocrinology and Metabolism. 93 (3): 784–91. doi:10.1210/jc.2007-2156. PMC 2266963. PMID 18073301.
- ^ Stoléru SG, Ennaji A, Cournot A, Spira A (1993). "LH pulsatile secretion and testosterone blood levels are influenced by sexual arousal in human males". Psychoneuroendocrinology. 18 (3): 205–18. doi:10.1016/0306-4530(93)90005-6. PMID 8516424. S2CID 23595343.
- ^ Häggström M (2014). "Reference ranges for estradiol, progesterone, luteinizing hormone and follicle-stimulating hormone during the menstrual cycle". WikiJournal of Medicine. 1 (1). doi:10.15347/wjm/2014.001. ISSN 2002-4436.
- ^ Mayo Medical Laboratory - 테스트 ID : LH, Luteinizing Hormon (LH), Serum Archived at the Wayback Machine 2016-09-25, 2012년 12월 취득
- ^ 세계보건기구, 황체화호르몬 국제표준제안WHO 생물 표준화 전문가 위원회세계보건기구제네바.2003.
- ^ WHO 국제표준, 황체호르몬, 인간, 재조합.국립 생물 표준 및 방제 연구소.
- ^ Dunson DB, Baird DD, Wilcox AJ, Weinberg CR (July 1999). "Day-specific probabilities of clinical pregnancy based on two studies with imperfect measures of ovulation". Human Reproduction. 14 (7): 1835–9. doi:10.1093/humrep/14.7.1835. PMID 10402400.
- ^ Nielsen MS, Barton SD, Hatasaka HH, Stanford JB (August 2001). "Comparison of several one-step home urinary luteinizing hormone detection test kits to OvuQuick". Fertility and Sterility. 76 (2): 384–7. doi:10.1016/S0015-0282(01)01881-7. PMID 11476792.
- ^ "Ovulation Predictor Kit Frequently Asked Questions". Fertility Plus. Archived from the original on March 12, 2012. Retrieved 12 March 2012.[어쩔 수 없는 의료원?]
- ^ "Clear Blue Ovulation Test Instructions". Ovulation Guide. Retrieved 2018-01-19.
- ^ "Advanced Ovulation Test" (PDF). Homehealth-UK. Retrieved 2018-01-19. 버전 1.1 2/11/15
- ^ Martinez AR, Bernardus RE, Vermeiden JP, Schoemaker J (March 1994). "Time schedules of intrauterine insemination after urinary luteinizing hormone surge detection and pregnancy results". Gynecological Endocrinology. 8 (1): 1–5. doi:10.3109/09513599409028450. PMID 8059611.
- ^ 67 인치 페이지:
- ^ 미국 특허 4,406,904
- ^ Weiss J, Axelrod L, Whitcomb RW, Harris PE, Crowley WF, Jameson JL (January 1992). "Hypogonadism caused by a single amino acid substitution in the beta subunit of luteinizing hormone". The New England Journal of Medicine. 326 (3): 179–83. doi:10.1056/NEJM199201163260306. PMID 1727547.
- ^ Valdes-Socin H, Salvi R, Daly AF, Gaillard RC, Quatresooz P, Tebeu PM, et al. (December 2004). "Hypogonadism in a patient with a mutation in the luteinizing hormone beta-subunit gene". The New England Journal of Medicine. 351 (25): 2619–25. doi:10.1056/NEJMoa040326. PMID 15602022.
- ^ Valdes-Socin H, Daly AF, Beckers A (2017). "Luteinizing Hormone Deficiency: Historical Views and Future Perspectives" (PDF). Austin Andrology. 2 (1): 1015.
- ^ Luveris 정보[unreliable medical source?] 2006년 6월 18일 Wayback Machine에서 아카이브
- ^ Plewes MR, Hou X, Talbott HA, Zhang P, Wood JR, Cupp AS, Davis JS (February 2020). "Luteinizing hormone regulates the phosphorylation and localization of the mitochondrial effector dynamin-related protein-1 (DRP1) and steroidogenesis in the bovine corpus luteum". FASEB Journal. Federation of American Societies for Experimental Biology. 34 (4): 5299–5316. doi:10.1096/fj.201902958R. PMC 7136153. PMID 32077149.