흉선
Thymus| 흉선 | |
|---|---|
 흉선 | |
흉선의 기능에 대한 설명 | |
| 세부 사항 | |
| 전구체 | 세 번째 인두 주머니 |
| 시스템 | 면역체계의 일부인 림프계 |
| 림프 | 기관절개술, 파라소외부 |
| 함수 | 기능성 T세포 개발 지원 |
| 식별자 | |
| 라틴어 | 흉선 |
| 메슈 | D013950 |
| TA98 | A13.1.02.001 |
| TA2 | 5152 |
| FMA | 9607 |
| 해부학적 용어 | |
흉선은 면역체계의 특화된 1차 림프종 기관이다.흉선 내에서는 흉선세포 림프구 또는 T세포가 성숙한다.T세포는 인체가 특히 외국 침략자에 적응하는 적응 면역체계에 중요하다.흉선은 가슴의 앞쪽 윗부분, 앞쪽 윗부분, 흉골 뒤, 심장 앞에 위치한다.그것은 두 개의 로브로 이루어져 있으며, 각각 중앙 메둘라와 외피질로 구성되어 있으며 캡슐로 둘러싸여 있다.
흉선은 흉선세포라고 불리는 미성숙 T세포와 흉선세포의 발달을 돕는 상피세포라고 불리는 안감세포로 구성되어 있다.발육에 성공한 T세포는 신체의 MHC 면역 수용체(양성 선택체라고 함)와 적절히 반응하며, 신체의 단백질(음성 선택체라고 함)에 대해서는 반응하지 않는다.흉선은 신생아 및 성인 전 기간 동안 가장 크고 가장 활동적이다.10대 초반에 이르러 흉선의 크기와 활동이 감소하기 시작하고 흉선의 조직은 지방 조직으로 점차 대체된다.그럼에도 불구하고 일부 T세포의 발달은 성인의 생활 전반에 걸쳐 계속된다.
흉선의 이상은 T세포의 수가 감소하고 자가면역질환인 자가면역결핍증 1형, 마이스테니아 그라비스와 같은 자가면역질환을 유발할 수 있다.이것들은 흔히 흉선이라 불리는 흉선의 조직의 암이나, 임파종이라 불리는 T세포와 같은 미성숙 림프구에서 생기는 조직과 관련이 있다.흉선을 제거하는 것을 흉선 절제술이라고 한다.고대 그리스 시대부터 흉선이 몸의 일부로 확인되었지만, 면역체계의 흉선의 기능이 더욱 뚜렷해진 것은 1960년대 이후다.
구조
흉선은 가슴 앞 윗부분의 흉골 아래에 앉아 목 쪽으로 위로 뻗어나가는 기관이다.어린이들에게 흉선은 분홍빛이 도는 회색이며, 부드럽고, 표면에 돌출되어 있다.[1]태어날 때 그것은 길이가 약 4-6cm, 너비가 2.5~5cm, 두께가 약 1cm이다.[2]그것은 사춘기까지 크기가 증가하는데, 사춘기까지는 크기가 약 40–50 g의 크기를 가질 수 있고,[3][4] 그 후에 비자발이라고 알려진 과정에서 크기가 감소한다.[4]
흉선은 전방에 위치한다.[5]윗 중간선에서 만나는 두 개의 로브로 이루어져 있으며, 목의 갑상선 아래에서 네 번째 갈비뼈의 연골만큼 낮게 뻗어 있다.[1]로브는 캡슐로 덮여 있다.[3]흉선은 흉골 아래에 있고 심막 위에 놓여 있으며, 근막 층에 의해 대동맥 아치 및 대혈관으로부터 분리된다.왼쪽 뇌수두 정맥은 흉선 안에 박혀 있을 수도 있다.[1]목에는 스테로히이드와 선갑상선 기능 부전근 뒤에 기관 앞과 옆면에 놓여 있다.[1]
미세조영술
흉선은 중앙에 합쳐진 두 개의 로브로 이루어져 있으며, 내부로 혈관과 함께 확장되는 캡슐에 둘러싸여 있다.[2]로브는 세포가 풍부한 외피질과 내부가 덜 밀집된 중피질로 구성되어 있다.[4]로브는 직경 0.5~2mm의 작은 로브들로 나뉘는데, 그 사이로 캡슐에서 셉타를 따라 돌출된 복사 삽입물이 나온다.[1]
피질은 주로 흉선세포와 상피세포로 이루어져 있다.[3]미숙한 T세포인 흉선세포는 정교하게 갈린 상피세포의 네트워크로 지탱되고 있는데, 이는 메둘라에서 유사한 네트워크로 계속된다.이 네트워크는 혈관에 대한 어드벤티시아를 형성하는데, 혈관은 메둘라와의 접합점 부근의 셉타를 통해 피질로 들어간다.[1]다른 세포들도 흉선에 존재하는데, 대식세포, 덴드리트 세포, 소량의 B세포, 중성미세포, 어시노필 등이 있다.[3]
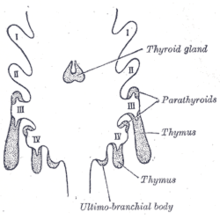
메둘라에서 상피세포의 네트워크는 피질보다 응고되어 있고, 림프세포의 수는 상대적으로 적다.[1]해솔의 말뭉치(심혈 말뭉치라고도 한다)라고 불리는 동심원형의 둥지 같은 몸체는 중상피세포의 집합에 의해 형성된다.[3]이것들은 일생동안 수가 증가하는 상피세포의 동심층적인 외침이다.[1]그것들은 상피관의 잔해로서, 배아의 세 번째 인두 주머니에서 자라 흉선을 형성한다.[6]
흉선의 로블을 보여주는 마이크로그래프.피질(더 낮은 보라색 영역)은 밀도가 낮고 가벼운 중수체를 둘러싸고 있다.
혈액 및 신경 공급
흉선을 공급하는 동맥은 내흉부와 하갑상선동맥의 가지로서, 상갑상선동맥의 가지가 간혹 보이는 경우가 있다.[2]나뭇가지들은 흉선에 닿아 캡슐의 9분의 1과 함께 피질과 메둘라 사이의 영역으로 이동하는데, 거기서 그들은 흉선 자체에 들어가거나 혹은 그 대신에 직접 캡슐에 들어간다.[2]
흉선의 정맥은 좌뇌수두정맥, 내흉정맥, 하갑상선정맥에서 끝난다.[2]때때로 정맥은 직접 윗정맥에서 끝난다.[2]
림프관은 동맥과 정맥을 동반한 흉선으로부터만 이동한다.이것들은 뇌수두, 기관지 및 기생충 림프절로 배수된다.[2]
흉선을 공급하는 신경은 질신경과 자궁경부 교감 사슬에서 발생한다.[2]흉선의 신경에서 나온 가지들은 흉선의 캡슐에 닿지만 흉선 자체에 들어가지 않는다.[2]
변형
두 개의 로브는 크기가 약간 다르며, 보통 왼쪽 로브는 오른쪽보다 높다.흉선 조직은 갑상선 위나 주변에 흩어져 있을 수 있으며, 때로는 갑상선 안에서 발견되기도 한다.[2]어린이들의 흉선은 때때로 갑상선만큼 높은 위쪽으로 가변적으로 뻗어 있다.[2]
개발
흉선세포와 흉선의 상피는 발달 기원이 다르다.[4]흉선의 상피는 먼저 발달하여 양쪽에 하나씩 세 번째 인두 주머니의 두 개의 외생물로 나타난다.[4]그것은 또한 때때로 네 번째 인두 주머니를 포함한다.[3]이것들은 외측과 후방으로 주변 중간으로 확장되며 복측 대동맥 앞에 있는 신경 볏에서 파생된 중핵으로 확장된다.여기서 흉선세포와 상피는 결합조직과 만나 결합한다.각 게실의 인두개방은 곧 없어지지만 플라스크의 목은 세포줄로서 얼마간 지속된다.플라스크에 줄지어 있는 세포의 더 많은 증식에 의해 세포의 싹이 형성되고, 세포는 침입하는 중간자에 의해 둘러싸이고 격리된다.[7]
상피는 미세한 로브를 형성하고, 스폰지 같은 구조로 발전한다.이 단계에서 조혈모세포는 흉선으로 이동한다.[4]정상 발육은 상피와 조혈성 흉선세포 사이의 상호작용에 의존한다.요오드는 흉선의 발달과 활동에도 필요하다.[8]
비자발적
흉선은 출산 후 사춘기가 되면 상대적인 최대 크기에 도달한 후 계속 성장한다.[2]태아와 신생아 생활에서 가장 활발하다.[9]사춘기가 되면 20~50g의 질량으로 늘어난다.[3]그리고 나서 흉선의 비자발이라 불리는 과정에서 크기와 활동량이 감소하기 시작한다.[4]생후 1년이 지나면 T세포의 생산량이 감소하기 시작한다.[4]지방과 결합조직은 흉선의 일부를 채운다.[2]무의식 중에 흉선은 크기와 활동량이 감소한다.[4]지방세포는 태어날 때는 존재하지만, 사춘기 이후에는 크기와 수가 현저하게 증가하여, 먼저 전두엽 사이의 벽에서 분비선을 침범한 다음, 피질과 메둘라로 침입한다.[4]이 과정은 현미경으로 보든 사람의 눈으로 보든 간에 흉선은 일반적으로 5-15그램의 무게가 나가지만 감지하기 어려울 수 있는 노년기까지 계속된다.[4][3]
위축은 성호르몬의 순환수치가 증가하기 때문이며, 성인의 화학적 또는 물리적 거세는 흉선의 크기와 활동량이 증가하는 결과를 초래한다.[10]심각한 질병이나 인체 면역결핍 바이러스 감염은 또한 비자발적인 결과를 초래할 수 있다.[3]
함수
T세포 성숙
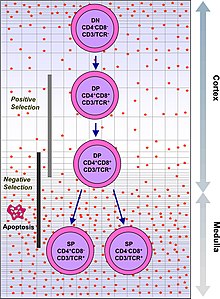
흉선은 세포 매개 면역력을 제공하는 면역체계의 중요한 부분인 T세포의 성숙을 촉진한다.[11]T세포는 뼈마름에서 조혈전구로 시작하여 흉선으로 이동하는데, 여기서 흉선세포라고 한다.흉선에서는 세포가 항원에 대해 반응하도록 하는 성숙 과정을 겪지만, 신체 조직에서 발견되는 항원에 대해서는 반응하지 않는다("부정 선택").[11]일단 성숙되면, T세포는 면역체계에 중요한 기능을 제공하기 위해 흉선에서 이주한다.[11][12]
각각의 T세포는 항원이라 불리는 특정 물질에 적합한 뚜렷한 T세포 수용체를 가지고 있다.[12]대부분의 T세포 수용체는 신체의 세포에 있는 주요 조직적합성 복합체에 결합한다.MHC는 T세포 수용체에 항원을 제시하는데, 이것이 특정 T세포 수용체와 일치하면 활성화가 된다.[12]제대로 기능하기 위해서는 성숙한 T세포가 MHC 분자("양성 선택")에 결합할 수 있어야 하며, 실제로 신체의 조직에서 나오는 항원("음성 선택")[12]에 대해 반응하지 않아야 한다.양선택은 피질에서 일어나고 음선택은 흉선의 중절에서 일어난다.[13]이 과정 후에 살아남은 T 세포는 스핑고신-1-인산염에 의해 조절된 흉선을 떠난다.[13]말초 순환에서 더 성숙하게 된다.[13]이 중 일부는 흉선 내 세포에 의해 분비되는 호르몬과 사이토카인 때문인데, 흉선 내에는 흉선, 흉선, 흉선, 흉선 등이 있다.[4]
포지티브 선택
T세포는 뚜렷한 T세포 수용체를 가지고 있다.이러한 뚜렷한 수용체들은 RAG1과 RAG2 유전자에 의해 자극된 V(D)J 재조합 유전자의 재배열 과정에 의해 형성된다.[13]이 과정은 오류가 발생하기 쉬우며, 일부 흉선세포는 기능적인 T-세포 수용체를 만들지 못하는 반면, 다른 흉선세포는 자동소거하는 T-세포 수용체를 만든다.[14]기능성 T세포 수용체가 형성되면 흉선세포는 세포표면 단백질 CD4와 CD8을 동시에 발현하기 시작할 것이다.[13]
그러면 T세포의 생존과 성질은 주변의 흉선 상피세포와의 상호작용에 달려 있다.여기서 T세포 수용체는 상피세포 표면에서 MHC 분자와 상호작용한다.[13]반응하지 않거나 약하게 반응하는 수용체를 가진 T세포는 세포사멸에 의해 죽게 된다.반응하는 T세포는 살아남아 증식할 것이다.[13]성숙한 T 셀은 CD4나 CD8만 표현하지만 둘 다 표현하지는 않는다.[12]이는 TCR과 MHC 등급1 또는 등급2 사이의 결합 강도에 따라 달라진다.[13] MHC 등급1 또는 등급2에 주로 결합하는 T세포 수용체 I는 성숙한 "세포독성" CD8 양성 T 셀을 생성하는 경향이 있고, MHC 등급 II에 대부분 결합하는 T세포 수용체는 CD4 양성 T 셀을 생성하는 경향이 있다.[14]
음선택
몸 자체의 단백질을 공격하는 T세포는 흉선에서 제거되는데, 이를 '부정적 선택'이라고 한다.[12]흉선의 상피세포와 흉선의 덴드리트 세포는 신체의 다른 곳에서 온 주요 단백질을 표현한다.[13]이를 자극하는 유전자는 AIRE이다.[12][13]자기 항원에 강하게 반응하는 흉선세포는 살아남지 못하고, 사멸에 의해 죽는다.[12][13]자기 항원에 노출된 일부 CD4 양성 T세포는 T 규제세포로서 지속된다.[12]
임상적 유의성
면역결핍증
흉선이 T세포가 발달하는 곳인 만큼 흉선의 발달에 따른 선천성 문제는 흉선의 발달에 문제가 있거나 흉선세포 발달에 특유한 문제 때문인지 면역결핍으로 이어질 수 있다.면역결핍은 심오할 수 있다.[9]유전적 돌연변이를 통해 어린 나이에 흉선을 상실하면(DiGeorge syndrome, COUNGE 증후군, 또는 머리카락과 흉선의[15] 부재를 유발하는 매우 희귀한 "nude" 흉선에 의해) 면역결핍이 심해지고 그 후에 바이러스, 원생동물, 곰팡이에 의한 감염 가능성이 높아진다.[16]FOXN1 돌연변이의 결과로 매우 희귀한 "누드" 결핍을 가진 누드 생쥐는 T세포 결핍의 모델로서 연구 생쥐의 일종이다.[17]
흉선과 관련된 면역 결핍의 가장 흔한 선천적 원인은 디조지 증후군이라고 불리는 22번째 염색체의 삭제에서 비롯된다.[15][16]이로 인해 제3기, 제4기 인두부위의 발육에 실패하여 흉선의 발육에 실패하게 되고 선천성 심장질환과 구강 이상(구개구개열, 구개열입술 등), 부갑상선발육의 실패, 기혈의 유무 등 가변적인 기타 관련 문제들이 발생하게 된다.기관과 외소파거스 사이의 [16]기둥매우 적은 수의 순환 T세포가 보인다.[16]그 상태는 상황 교배에서 형광에 의해 진단되고 흉선 이식으로 치료된다.[15]
중증 복합면역결핍증(SCID)은 희귀 선천성 유전질환의 집단으로 T, B, NK세포 결함을 유발할 수 있다.[16]이러한 신드롬은 B세포와 T세포의 전구인 조혈모세포의 성숙에 영향을 미치는 돌연변이에 의해 발생한다.[16]IL-2 수용체 유전자 기능 상실을 비롯한 여러 유전적 결함이 SCID를 유발할 수 있고, 돌연변이를 일으켜 효소 아데닌 제아미노효소가 결핍될 수 있다.[16]
자가면역병
자가면역성 다항분비증후군
자가면역성 다항분비증후군 1형은 흉선조직의 유전적 결함으로 발생하는 희귀 유전적 자가면역증후군이다.[18]구체적으로 이 병은 흉선의 명수 내 상피세포에서 자기 항원의 발현을 자극하는 자가면역조절기(AIRE) 유전자의 결함에 기인한다.이 상태의 결함으로 인해 자기 항원이 발현되지 않아 T세포가 신체의 조직을 견디도록 조건화되지 않고 이물질로 취급되어 면역반응을 자극하여 자가면역성을 유발할 수 있다.[18]APECED에 걸린 사람들은 갑상선의 갑상선 기능 저하증, 부신의 애디슨병, TH17 세포의 기능장애로 인한 입안과 손톱의 안쪽 안감 등 신체 표면의 칸디다 감염, 여러 내분비 조직에 영향을 주는 자가면역질환이 발병한다.ms는 종종 어린시절에 시작한다.많은 다른 자가면역 질환도 발생할 수 있다.[18]치료는 환자에 걸린 장기를 대상으로 한다.[18]
흉선 관련 다항 자가면역
백선종과 연관된 다선종 자가면역증은 백선종 환자에게서 발생할 수 있다.이 상태에서 흉선에서 발달한 T세포는 신체의 조직에 대하여 향하게 된다.악성 흉선은 자기반응 T세포를 제거하기 위해 흉선세포의 발달을 적절하게 교육할 수 없기 때문이다.이 질환은 사실상 이식 대 숙주 질환과 구별할 수 없다.[19]
마이스테니아 그라비스
마이스테니아 그라비스는 아세틸콜린 수용체를 차단하는 항체로 인해 가장 자주 발생하는 자가면역질환으로 신경과 근육 사이의 신호전달에 관여한다.[20]비정상적으로 발달한 T세포 때문에 아마도 생성된 항체와 함께 [20]흉선 비대증이나 흉선종과 관련되는 경우가 많다.[21]마이스테니아 그라비스는 젊은 나이와 중년 나이 사이에 발달하여 근육의 움직임을 쉽게 피로하게 한다.[20]조사에는 항체(아세틸콜린 수용체 또는 근육 특이 키나아제 등)를 입증하는 것과 흉선종이나 흉선절제술을 검출하기 위한 CT 스캔이 포함된다.[20]흉선에 관해서는 특히 흉선종이 발견되면 흉선 절제술이라 불리는 흉선의 제거가 치료로 간주될 수 있다.[20]다른 치료법으로는 신경 시냅스에서의 아세틸콜린 작용의 지속시간을 증가시켜 고장률을 감소시키는 것도 있다.이것은 피리도스티그민 같은 아세틸콜린세테라제 억제제에 의해 이루어진다.[20]
암
티모마스
흉선 상피세포에서 비롯된 종양을 시모마라고 한다.[3]그것들은 대부분 40세 이상의 성인들에게서 발생한다.[3]종양은 일반적으로 목질량이나 상정맥과 같은 인근 구조물에 영향을 미치는 등의 증상을 유발할 때 검출되며,[21] 흉부 X선과 같은 영상에 부수적인 소견으로 검출되는 마이스테니아 그라비스를 가진 환자에게서 검진을 받기 때문에 검출된다.[3][21]흉선에서 발원한 과대증상과 종양은 저혈구글로불린혈증, 그레이브스병, 순수 적세포아플라스아, 악성빈혈증, 피부염과 같은 다른 자가면역질환과 관련이 있는데, 이는 증식 T세포의 음성선택의 결함 때문일 가능성이 높다.[3][22]
흉선은 양성일 수 있다; 양성이지만 확장에 의해 흉선의 캡슐 너머에 침입하거나, 악성(암)이다.[3]이 분류는 세포의 외관에 근거한다.[3]WHO 분류도 존재하지만 표준 임상 관행의 일부로 사용되지 않는다.[3]흉선에 국한된 양성 종양은 가장 흔하다; 국부적으로 침습적인 종양, 그리고 암이 그 뒤를 잇는다.[3]일부 출처에서는 악성 종양이 더 흔하다고 보고하는 등 보고에 차이가 있다.[22]침습성 종양은 기술적으로 악성 종양은 아니지만 여전히 신체의 다른 부위로 퍼질 수 있다.[3]흉선세포가 상피세포에서 발생하더라도 흉선세포도 포함할 수 있다.[3]흉선을 치료하려면 흉선 전체를 제거하는 수술이 필요한 경우가 많다.[22]이것은 또한 관련된 자가면역 조건의 일시적 해소를 초래할 수 있다.[22]
림프종
흉선의 T세포에서 발생한 종양은 급성 림프성 백혈병(ALL)의 일부를 형성한다.[23]이들은 증상, 조사 접근법 및 관리가 다른 형태의 ALL과 유사하다.[23]ALL의 다른 형태와 마찬가지로 발병하는 증상은 혈소판의 결핍으로 인해 멍이 들거나 출혈이 생기거나, 감염을 일으키는 면역억제 또는 세포에 의한 신체 일부 침투로 간, 비장, 림프절 또는 기타 부위가 확대되는 것과 관련이 있다.[23]혈액검사에서 백혈구나 림프관 등이 다량 발견될 수 있으며 혈소판이나 빈혈 등 다른 세포 라인의 결핍이 나타날 수 있다.[23]면역항암제는 T세포에서 발견되는 단백질인 CD3인 세포를 밝혀내고 T세포의 성숙도를 더욱 구분하는데 도움을 줄 것이다.카리오타이핑을 포함한 유전자 분석은 필라델피아 번역과 같이 예후나 치료에 영향을 미칠 수 있는 특정한 이상을 밝혀낼 수 있다.[23]관리에는 항암화학요법, 줄기세포 이식, 항생제 감염 치료, 수혈 등 관련 문제 관리 등 여러 과정이 포함될 수 있다.매우 높은 백혈구 수치는 또한 세포와 세포의 전도를 필요로 할 수 있다.[23]
흉선에 존재하는 B세포의 적은 개체군에서 발생하는 종양은 일차적(혈액)대 B세포 림프종으로 이어진다.[24]이것들은 희귀한 비호지킨 림프종의 아형이지만, 유전자의 활동성과 때때로 미세한 모양에 의해 특이하게도 호지킨스 림프종의 특성도 가지고 있다.[25]젊은 층과 중년층에서 가장 흔하게 발생하는 것으로 여성층에서 더 두드러진다.[25]가장 흔히 증상이 발생할 때 그것은 상정맥이나 상부 호흡기와 같은 흉선 근처의 구조물의 압축 때문이다; 림프절에 영향을 받았을 때 그것은 종종 중격막과 목의 그룹에 있다.[25]이러한 종양은 면역항화학의 영향을 받는 조직검사에서 종종 발견된다.이것은 CD19, CD20, CD22, CD15가 없는 상태에서 분화성, 즉 세포 표면 단백질, 즉 CD30의 존재를 보여줄 것이다.다른 마커도 진단을 확인하는 데 사용할 수 있다.[25]치료에는 일반적으로 SOP 또는 EPOCH 또는 기타 요법이 포함된다. 일반적으로 사이클로인산염, 안트라시클린, 프레드니손 및 기타 화학요법을 포함하는 요법, 그리고 잠재적으로 줄기세포 이식도 포함된다.[25]
흉낭종
흉선은 보통 지름 4cm 미만의 낭종을 포함할 수 있다.흉선 낭종은 보통 우발적으로 발견되며 일반적으로 증상을 일으키지 않는다.[3]흉막낭은 목이나 흉부(중격자)를 따라 발생할 수 있다.[26]낭종은 보통 액체를 포함하고 있으며 평평한 세포의 많은 층이나 기둥 모양의 세포에 의해 정렬되어 있다.[26]그럼에도 불구하고 낭종이 존재하면 인근 구조물을 압축해 시모마와 비슷한 문제를 일으킬 수 있고,[3] 일부는 내부 벽(세파)에 접촉해 종양과 구별이 어려울 수 있다.[26]낭종이 발견되었을 때, 조사에는 종양에 대한 검사가 포함될 수 있으며, 여기에는 낭종이 있는 것으로 의심되는 부위에 대한 CT나 MRI 스캔이 포함될 수 있다.[3][26]
외과적 제거
흉선 절제술은 흉선의 외과적 제거술이다.[2]통상적인 제거 사유는 신생아기에 선천성 심장 결함을 교정하기 위한 수술을 위해 심장에 접근하기 위함이다.[27]흉막절제술에 대한 다른 징후로는 흉막제거와 마이스테니아 그라비스의 치료가 있다.[2]신생아의 경우 흉선의 상대적 크기가 심장 및 주변 혈관에 대한 외과적 접근을 방해한다.[27]유아기에 흉선을 제거하면 종종 치명적인 면역결핍을 초래하는데, 기능 T세포가 발달하지 않았기 때문이다.[2]성숙한 T세포가 다른 림프구에 위치하는 기능적인 림프계를 가진 어린이와 성인의 경우 효과가 감소하고, 새로운 항원에 대한 면역반응을 탑재하지 못하는 것으로 제한된다.[2]
사회와 문화
인간의 먹이로 사용될 때, 동물의 흉선은 달콤한 빵의 종류 중 하나로 알려져 있다.[28]
역사
그 흉선 고대 그리스인들은 하고, 그리고 그것의 이름은 희랍어 단어 θυμός(thumos)에서"분노"또는"심장, 영혼, 소망, 삶"을 의미하며, 가슴에 감정을 주관적으로 미치고 있 가깝다는 위치, 아마,[29]또는 다른 이름을 "이상을 된 이름이 약초 양념하여(그리스어로 또한 θύμος 또는 θυμάρι),에서 나온다 알려져 있었다.rty백리향 한 다발과 닮았기 때문일 것이다.[30]
갈렌은 사람의 일생 동안 장기의 크기가 변했다는 것을 가장 먼저 주목했다.[31]
19세기에는 림프조직의 증가와 확대된 흉선에 의해 정의된 상태 흉선염으로 조건이 확인되었다.갑작스러운 영아 사망 증후군의 원인으로 생각되었으나 지금은 구식 용어다.[32]
면역체계에 있어서 흉선의 중요성은 1961년 자크 밀러에 의해 발견되었는데, 외과적으로 하루 된 생쥐로부터 흉선을 제거하고, 이후 림프구 개체군의 결핍을 관찰함으로써, 그 기원의 기관의 이름을 따서 T세포라고 명명되었다.[33][34]면역학적 역할이 발견되기 전까지 흉선은 기능적 중요성이 없는 '진화적 사고'로 치부되어 있었다.[14]이식된 흉선의 T세포가 쥐에게 이식된 흉선의 T세포가 기증된 생쥐의 조직에 대한 내성을 보인다는 발견과 함께 성숙한 T세포가 신체의 조직을 견딜 수 있도록 하는 데 있어 흉선의 역할은 1962년에 밝혀졌다.[14]1968년 B세포와 T세포가 서로 다른 종류의 림프구로 확인되었고, T세포가 흉선의 성숙을 필요로 한다는 사실이 이해되었다.[14]T세포의 하위 유형(CD8과 CD4)은 1975년까지 식별되었다.[14]이러한 T세포의 하위 분류인 MHC 수용체와 기능적으로 결합되는 양의 세포 선택에서 성숙하는 방법은 1990년대에 알려졌다.[14]AIRE 유전자의 중요한 역할, 그리고 자동소거 T세포가 성숙하는 것을 막는 데 있어서 음성선택의 역할은 1994년까지 이해되었다.[14]
최근 면역학의 발달로 T세포 성숙기에 있는 흉선의 기능이 더욱 완전하게 이해될 수 있게 되었다.[14]
다른동물
흉선은 모든 턱이 있는 척추동물에게 존재하며, 나이와 함께 같은 수축을 겪으며 다른 척추동물과 같은 면역학적 기능을 한다.최근, 2011년, 흉선이라고 불리는 이산 흉선 모양의 림프구-이피델리 구조물이 유충의 아가미에서 발견되었다.[35]하그피쉬는 인두종륜근과 관련된 갑상선근육을 가지고 있는데, 이것은 다양한 면역 반응을 담당한다.[36]
흉선은 인간의 흉선과 유사한 구조와 기능을 가진 대부분의 다른 척추동물에도 존재한다.목에 두번째 흉선은 때때로 mouse[37]에 인간에서 발생하는 동물지만 무흉선의. 털 없는 기니 피그(는 자발적인 실험실 돌연변이에서 일어났다)도무지 흉선 조직을 보유하고 있고 오르간 공동 낭포로 대체됩니다 adulthood,[38]에 이르게 되면, 기니 피그의 흉선 자연스럽게 퇴화된 것으로 알려졌다. spaces.[39]
추가 이미지
태아의 흉선
참조
![]() 이 기사는 20일자 1273페이지의 공공영역의 텍스트를 통합하고 있다. 그레이스 아나토미 (1918)
이 기사는 20일자 1273페이지의 공공영역의 텍스트를 통합하고 있다. 그레이스 아나토미 (1918)
- ^ a b c d e f g h Standring S, et al., eds. (2008). Gray's Anatomy: The Anatomical Basis of Clinical Practice (40th ed.). London: Churchill Livingstone. ISBN 978-0-8089-2371-8.
- ^ a b c d e f g h i j k l m n o p q Standring S, Gray H, eds. (2016). Gray's Anatomy: The Anatomical Basis of Clinical Practice (41st ed.). Philadelphia. pp. 983–6. ISBN 9780702052309. OCLC 920806541.
- ^ a b c d e f g h i j k l m n o p q r s t u v Kumar V, Abbas AK, Fausto N, Aster JC (2014-08-27). "Chapter 13. Diseases of White Blood Cells, Lymph Nodes, Spleen, and Thymus: Thymus.". Robbins and Cotran Pathologic Basis of Disease (9th (online) ed.). ISBN 9780323296397.
- ^ a b c d e f g h i j k l Young B, O'Dowd G, Woodford P (2013). Wheater's functional histology: a text and colour atlas (6th ed.). Philadelphia: Elsevier. pp. 204–6. ISBN 9780702047473.
- ^ Nasseri, Farbod; Eftekhari, Farzin (March 2010). "Clinical and Radiologic Review of the Normal and Abnormal Thymus: Pearls and Pitfalls". RadioGraphics. 30 (2): 413–428. doi:10.1148/rg.302095131. ISSN 0271-5333.
- ^ Larsen W (2001). Human Embryology (3rd ed.). Elsevier. pp. 366–367. ISBN 978-0-443-06583-5.
- ^ 스위스 발생학(UL, UB, UF) qblood/limphat03
- ^ Venturi S, Venturi M (September 2009). "Iodine, thymus, and immunity". Nutrition. 25 (9): 977–9. doi:10.1016/j.nut.2009.06.002. PMID 19647627.
- ^ a b 데이비드슨의 2018년, 페이지 67.
- ^ Sutherland JS, Goldberg GL, Hammett MV, Uldrich AP, Berzins SP, Heng TS, et al. (August 2005). "Activation of thymic regeneration in mice and humans following androgen blockade". Journal of Immunology. 175 (4): 2741–53. doi:10.4049/jimmunol.175.4.2741. PMID 16081852.
- ^ a b c Hall JE (2016). Guyton and Hall textbook of medical physiology (13th ed.). Philadelphia: Elsevier. pp. 466–7. ISBN 978-1-4557-7016-8.
- ^ a b c d e f g h i Kumar V, Abbas AK, Fausto N, Aster JC (2014-08-27). "Chapter 6. Diseases of the immune system. The normal immune system.". Robbins and Cotran Pathologic Basis of Disease (9th (online) ed.). ISBN 9780323296397.
- ^ a b c d e f g h i j k Hohl TM (2019). "6. Cell mediated defence against infection: Thymic selection of CD4+ and CD8+ T Cells". In Bennett JE, Dolin R, Blaser MJ (eds.). Mandell, Douglas, and Bennett's principles and practice of infectious diseases (9th (online) ed.). Elsevier. ISBN 9780323482554.
- ^ a b c d e f g h i Miller JF (May 2011). "The golden anniversary of the thymus". Nature Reviews. Immunology. 11 (7): 489–95. doi:10.1038/nri2993. PMID 21617694. S2CID 21191923.
- ^ a b c 해리슨의 2015년 페이지 2493.
- ^ a b c d e f g 데이비드슨의 2018년, 페이지 79-80.
- ^ Fox JG (2006). The Mouse in Biomedical Research: Immunology. Elsevier. p. 277. ISBN 978-0-08-046908-9.
- ^ a b c d 해리슨의 2015년판 2756-7페이지.
- ^ Wadhera A, Maverakis E, Mitsiades N, Lara PN, Fung MA, Lynch PJ (October 2007). "Thymoma-associated multiorgan autoimmunity: a graft-versus-host-like disease". Journal of the American Academy of Dermatology. 57 (4): 683–9. doi:10.1016/j.jaad.2007.02.027. PMID 17433850.
- ^ a b c d e f 데이비드슨의 2018년판 1141-43쪽
- ^ a b c Engels EA (October 2010). "Epidemiology of thymoma and associated malignancies". Journal of Thoracic Oncology. 5 (10 Suppl 4): S260-5. doi:10.1097/JTO.0b013e3181f1f62d. PMC 2951303. PMID 20859116.
- ^ a b c d 해리슨의 2015년 페이지 2759.
- ^ a b c d e f Larson RA (2015). "Chapter 91: Acute Lymphoblastic Leukemia". Williams hematology (online) (9th ed.). McGraw-Hill Education. ISBN 978-0071833004.
- ^ Dabrowska-Iwanicka A, Walewski JA (September 2014). "Primary mediastinal large B-cell lymphoma". Current Hematologic Malignancy Reports. 9 (3): 273–83. doi:10.1007/s11899-014-0219-0. PMC 4180024. PMID 24952250.
- ^ a b c d e Smith SD, Press OW (2015). "Chapter 98. Diffuse Large B-Cell Lymphoma and Related Diseases". Williams hematology (online) (9th ed.). McGraw-Hill Education. ISBN 978-0071833004.
- ^ a b c d Goldstein, Alan J.; Oliva, Isabel; Honarpisheh, Hedieh; Rubinowitz, Ami (1 February 2015). "A Tour of the Thymus: A Review of Thymic Lesions with Radiologic and Pathologic Correlation". Canadian Association of Radiologists Journal. 66 (1): 5–15. doi:10.1016/j.carj.2013.09.003. PMID 24736228. S2CID 33986973.
- ^ a b Eysteinsdottir JH, Freysdottir J, Haraldsson A, Stefansdottir J, Skaftadottir I, Helgason H, Ogmundsdottir HM (May 2004). "The influence of partial or total thymectomy during open heart surgery in infants on the immune function later in life". Clinical and Experimental Immunology. 136 (2): 349–55. doi:10.1111/j.1365-2249.2004.02437.x. PMC 1809033. PMID 15086401.
- ^ "Sweetbread recipes – BBC Food". BBC Food. Retrieved 2019-12-12.
- ^ Liddell HG, Scott R. "θυμός". A Greek-English Lexicon. Retrieved 2019-12-10.
- ^ "thymus Origin and meaning of thymus by Online Etymology Dictionary". www.etymonline.com. Retrieved 2019-12-10.
- ^ Nishino M, Ashiku SK, Kocher ON, Thurer RL, Boiselle PM, Hatabu H (2006). "The thymus: a comprehensive review". Radiographics. 26 (2): 335–48. doi:10.1148/rg.262045213. PMID 16549602.
- ^ Sapolsky RM (2004). Why zebras don't get ulcers (3rd ed.). New York: Henry Hold and Co./Owl Books. pp. 182–185. ISBN 978-0805073690.
- ^ Miller JF (July 2002). "The discovery of thymus function and of thymus-derived lymphocytes". Immunological Reviews. 185 (1): 7–14. doi:10.1034/j.1600-065X.2002.18502.x. PMID 12190917. S2CID 12108587.
- ^ Miller JF (June 2004). "Events that led to the discovery of T-cell development and function--a personal recollection". Tissue Antigens. 63 (6): 509–17. doi:10.1111/j.0001-2815.2004.00255.x. PMID 15140026.
- ^ Bajoghli B, Guo P, Aghaallaei N, Hirano M, Strohmeier C, McCurley N, et al. (February 2011). "A thymus candidate in lampreys". Nature. 470 (7332): 90–4. Bibcode:2011Natur.470...90B. doi:10.1038/nature09655. PMID 21293377. S2CID 4417477.
- ^ Riviere HB, Cooper EL, Reddy AL, Hildemann WH (1975). "In Search of the Hagfish Thymus" (PDF). American Zoologist. 15 (1): 39–49. doi:10.1093/icb/15.1.39. JSTOR 3882269.
- ^ Terszowski G, Müller SM, Bleul CC, Blum C, Schirmbeck R, Reimann J, et al. (April 2006). "Evidence for a functional second thymus in mice". Science. 312 (5771): 284–7. Bibcode:2006Sci...312..284T. doi:10.1126/science.1123497. PMID 16513945. S2CID 24553384.
- ^ Suckow, Mark A.; Stevens, Karla A.; Wilson, Ronald P. (2012). The Laboratory Rabbit, Guinea Pig, Hamster, and Other Rodents. Academic Press. p. 583. ISBN 978-0-12-380920-9.
- ^ Gershwin, M. Eric; Merchant, Bruce (2012). Immunologic Defects in Laboratory Animals 1. Springer Science & Business Media. p. 289. ISBN 978-1-4757-0325-2.
책들
- Ralston SH, Penman ID, Strachan MW, Hobson RP, eds. (2018). Davidson's principles and practice of medicine (23rd ed.). Elsevier. ISBN 978-0-7020-7028-0.
- Kasper D, Fauci A, Hauser S, Longo D, Jameson J, Loscalzo J (2015). Harrison's Principles of Internal Medicine (19th ed.). McGraw-Hill Professional. ISBN 9780071802154.
외부 링크
| 위키미디어 커먼즈에는 사이머스(기관)와 관련된 미디어가 있다. |
- 흉선에서 T세포가 발달한다.Janice Yau의 비디오, 스트롬 신호와 허용오차를 묘사한다.토론토 대학의 면역학 및 바이오메디컬 커뮤니케이션학과Master's Research Project, Master of Science in Biomedical Communications. 2011.