지질다당류
Lipopolysaccharide
지질다당류(LPS)는 지질과 박테리아 독소인 다당류로 구성된 큰 분자입니다. 이들은 모두 공유결합으로 연결된 O-항원, 외핵, 내핵으로 구성되어 있으며, 대장균, 살모넬라 등 그람 음성균의 세포 외피의 가장 바깥쪽 막인 세균 캡슐에서 발견됩니다.[1] 오늘날 내독소라는 용어는 LPS와 동의어로 사용되는 경우가 많지만,[2] Bacillus turingiensis가 생산하는 소위 델타 내독소 단백질과 같이 LPS와 관련이 없는 내독소(원래 의미로는 세포가 분해될 때 방출되는 독소)가 몇 개 있습니다.[3]
지질다당류는 주로 면역계와의 상호작용을 통해 인간의 건강에 상당한 영향을 미칠 수 있습니다. LPS는 면역계의 강력한 활성화제이자 발열을 일으키는 약제입니다.[4] 심할 경우 LPS가 패혈성 쇼크를 일으키는 역할을 할 수 있습니다.[5] 낮은 수치와 더 오랜 시간에 걸쳐 LPS가 자가면역, 비만, 우울증, 세포노년에 중요하고 해로운 역할을 할 수 있다는 증거가 있습니다.[6][7][8][9]
디스커버리
LPS의 독성 활성은 Richard Friedrich Johannes Piffer에 의해 처음 발견되고 내독소라고 불렸습니다. 그는 박테리아에 의해 주변 환경으로 방출되는 독소인 외독소와 박테리아 세포 내에 "안에" 있다가 박테리아 외막이 파괴된 후에야 방출되는 독소인 내독소를 구별했습니다.[10] 후속 연구에서는 그람 음성 미생물로부터 LPS의 방출이 반드시 박테리아 세포벽의 파괴를 필요로 하는 것은 아니며, 오히려 LPS가 박테리아 외막 소포(OMV)의 형태로 막 소포 밀매의 정상적인 생리적 활동의 일부로서 분비된다는 것을 보여주었습니다. 다른 독성 인자와 단백질을 포함할 수도 있습니다.[11][1]
세균내의 기능
LPS는 그람 음성 박테리아의 외막의 주요 구성 요소로 박테리아의 구조적 무결성에 크게 기여하고 특정 종류의 화학적 공격으로부터 막을 보호합니다. LPS는 대부분의 그람 음성균의 세포 표면에 가장 풍부한 항원으로 대장균과 살모넬라 외막의 80%까지 기여합니다.[1] LPS는 세포막의 음전하를 증가시키고 전체 막 구조를 안정화하는 데 도움을 줍니다. 그것은 많은 그람음성균들에게 매우 중요한데, 그것을 코딩하는 유전자가 변형되거나 제거되면 죽게 됩니다. 그러나 Neisseria meningitidis, Moraxella catarhalis 및 Acineobter baumannii와 같은 적어도 일부 그람 음성 박테리아에서는 LPS가 필수적이지 않은 것으로 보입니다.[12] 또한 표면 부착, 박테리오파지 민감도 및 아메바와 같은 포식자와의 상호 작용을 포함하여 박테리아 생태학의 비병원성 측면과 관련이 있습니다. LPS는 또한 박테리아 단백질분해효소의 한 종류인 omptins의 기능에 필요합니다.[13]
구성.
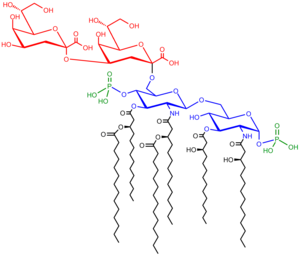
지질다당류는 세 가지 부분으로 구성됩니다. O 항원(또는 O 다당류), 코어 올리고당 및 지질 A.
O-항원
LPS 내에 포함된 반복적인 글리칸 중합체는 박테리아의 O 항원, O 다당류 또는 O 측쇄로 지칭됩니다. O 항원은 코어 올리고당에 부착되며, LPS 분자의 가장 바깥쪽 영역을 포함합니다. O 사슬의 구성은 균주마다 다릅니다. 서로 다른 대장균 균주에 의해 생성되는 160개 이상의 서로 다른 O 항원 구조가 있습니다.[14] O 사슬의 유무에 따라 LPS가 "거친" 것으로 간주되는지 또는 "평활한" 것으로 간주되는지 여부가 결정됩니다. 전체 길이의 O-체인은 LPS를 매끄럽게 만드는 반면, O-체인의 부재 또는 감소는 LPS를 거칠게 만듭니다.[15] 거친 LPS가 더 소수성이기 때문에 거친 LPS를 가진 박테리아는 보통 소수성 항생제에 대해 더 많은 세포막을 가지고 있습니다.[16] O항원은 세균 세포의 가장 바깥쪽 표면에 노출되어 결과적으로 숙주 항체에 의한 인식의 표적이 됩니다.
코어
코어 도메인은 항상 지질 A에 직접 부착되는 올리고당 성분을 포함하고 일반적으로 헵토스 및 3-데옥시-D-만노-옥트-2-울로손산(KDO, keto-deoxyoctulosonate)과 같은 당을 포함합니다.[17] 많은 박테리아의 LPS 코어에는 인산염, 아미노산 및 에탄올아민 치환기와 같은 비탄수화물 성분도 포함되어 있습니다.
지질A
지질 A는 정상적인 상황에서 여러 지방산으로 장식된 인산화된 글루코사민 이당류입니다. 이 소수성 지방산 사슬은 LPS를 박테리아 막에 고정시키고 나머지 LPS는 세포 표면에서 돌출합니다. 지질 A 도메인은 그람 음성 박테리아의 독성의 대부분을 담당합니다. 세균 세포가 면역계에 의해 용해되면 지질 A를 포함한 막의 파편이 순환계로 방출되어 발열, 설사, 치명적인 내독성 쇼크(패혈성 쇼크라고도 함)를 일으킵니다. 지질 A 부분은 LPS의 매우 보존된 구성 요소입니다.[18] 그러나 지질 A 구조는 박테리아 종에 따라 다릅니다. 지질 A 구조는 전체적인 숙주 면역 활성화의 정도와 성질을 크게 정의합니다.[19]
리포올리고당
LPS의 "거친 형태"는 O 다당류의 부재로 인해 분자량이 더 낮습니다. 그 대신에 짧은 올리고당이 있습니다: 이 형태는 리포올리고당(LOS)으로 알려져 있으며, 나이세리아 종 및 헤모필루스 종과 같은 일부 유형의 그람 음성 박테리아의 외막에서 발견되는 당지질입니다.[6][20] LOS는 그람 음성 세포 외피의 외막의 무결성과 기능을 유지하는 데 중심적인 역할을 합니다. LOS는 면역자극제 및 면역조절제 역할을 할 수 있기 때문에 특정 세균 감염의 발병기전에서 중요한 역할을 합니다.[6] 또한 LOS 분자는 일부 박테리아 균주가 분자 모방 및 항원 다양성을 나타내는 능력을 담당하여 숙주 면역 방어를 회피하는 데 도움이 되어 이러한 박테리아 균주의 독성에 기여합니다. Neisseria meningitidis의 경우, 분자의 지질 A 부분은 대칭 구조를 가지며 내부 코어는 3-디옥시-D-만노-2-옥툴로손산(KDO)과 헵토스(Hep) 부분으로 구성됩니다. 외부 코어 올리고당 사슬은 박테리아 균주에 따라 다릅니다.[6][20]
LPS 해독
아실옥시아실 가수분해효소(AOAH)라고 불리는 고도로 보존된 숙주 효소는 LPS가 동물의 조직에 들어가거나 생산될 때 그것을 해독할 수 있습니다. 또한 장내 LPS를 LPS 억제제로 전환시킬 수도 있습니다. 이 리파아제는 호중구, 대식세포 및 수지상세포에 의해 생성되며, 리파아제는 지질 A에서 2차 아실 사슬을 제거하여 테트라아실 LPS를 생성함으로써 LPS를 비활성화합니다. 쥐에게 비경구적으로 LPS를 투여하면 AOAH가 결핍된 쥐는 높은 역가의 비특이적 항체가 발생하고 간비대가 길어지며 내독소 내성이 길어집니다. 동물이 비경구 LPS 노출 후 항상성을 회복하려면 LPS 비활성화가 필요할 수 있습니다.[21] 쥐는 LPS 신호전달을 억제하는 다른 많은 메커니즘을 가지고 있지만 AOAH가 부족한 동물에서는 이러한 변화를 막을 수 없습니다.
장내 알칼리성 인산분해효소에 의한 LPS의 탈인산화는 정상적인 장내 미생물군을 회복시키는 Salmonella tryphimurium 및 Clostridioides difficile 감염의 중증도를 감소시킬 수 있습니다.[22] 알칼리성 포스파타제는 LPS의 지질 A 부분을 탈인산화시킴으로써 박테리아로부터의 장 염증(및 "누출된 내장")을 방지합니다.[23][24][25]
생합성 및 수송
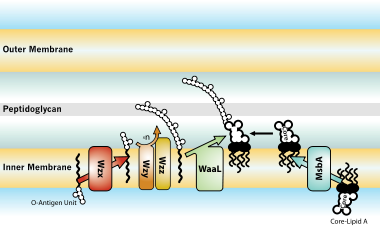
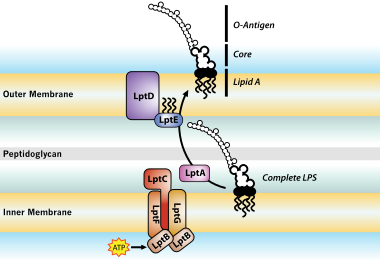
LPS를 만드는 모든 과정은 세포 내막 표면에서 처음 생성되는 지질 A-Kdo2라는 분자에서 시작됩니다. 그런 다음 MsbA라는 단백질의 도움으로 내막과 외막 사이의 공간으로 이동하기 전에 내막 위의 이 분자에 추가 당이 첨가됩니다. LPS의 또 다른 부분인 O-항원은 내막의 특별한 효소 복합체에 의해 만들어집니다. 그런 다음 세 가지 다른 시스템을 통해 외막으로 이동됩니다. 하나는 Wzy 의존적이고, 다른 하나는 ABC 수송체에 의존적이며, 세 번째는 합성효소 의존적 과정을 포함합니다.[28]
그람음성균에 감염된 숙주에 대한 생물학적 영향
면역반응
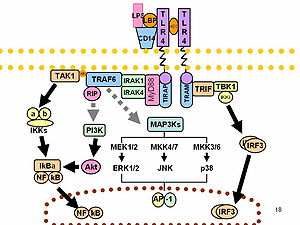
LPS는 많은 세포 유형에서 CD14/TLR4/MD2 수용체 복합체에 결합하기 때문에 원형 내독소로 작용하지만, 특히 단핵구, 수지상 세포, 대식세포 및 B 세포에서 친염증성 사이토카인, 산화질소 및 에이코사노이드의 분비를 촉진합니다.[29] 브루스 뷰틀러(Bruce Beutler)는 TLR4가 LPS 수용체임을 입증한 공로로 2011년 노벨 생리학·의학상의 일부를 수상했습니다.[30][31]
과산화물은 세포 스트레스 반응의 일환으로 TLR(toll-like receptor)을 발현하는 다양한 세포 유형에서 LPS에 의해 유도되는 주요 활성 산소 종 중 하나입니다.[32] LPS는 외인성 발열물질이기도 합니다.[4]
LPS 기능은 많은 전사 인자를 활성화시키는 역할로 인해 몇 년 전부터 실험적인 연구를 진행해 왔습니다. LPS는 또한 패혈성 쇼크와 관련된 여러 유형의 매개체를 생성합니다. 인간은 다른 동물(예: 쥐)보다 LPS에 훨씬 더 민감합니다. 1 µg/kg의 용량은 사람에게 쇼크를 유발하지만 쥐는 최대 천 배 이상의 용량을 견딜 수 있습니다. 이것은 두 종 사이의 순환하는 천연 항체 수준의 차이와 관련이 있을 수 있습니다.[34][35] Said et al.은 LPS가 PD-L1에 의한 PD-1의 결합 후 단핵구에 의한 IL-10 생산을 유도하는 단핵구 상에서 PD-1 수준을 상향 조절함으로써 CD4 T-세포 확장 및 기능의 IL-10 의존적 억제를 유발한다는 것을 보여주었습니다.[36]
내독소는 대부분 수막구균혈증, 워터하우스-프리데리히센 증후군 및 수막염을 포함한 수막구균 질환을 유발하는 병원체인 Neisseria meningitidis와 같은 병원성 그람 음성 박테리아 감염의 극적인 임상 징후에 책임이 있습니다.
여러 박테리아 균주의 LPS의 일부는 인간 숙주 세포 표면 분자와 화학적으로 유사한 것으로 나타났습니다. 일부 박테리아가 일부 유형의 숙주 세포 표면 분자와 화학적으로 동일하거나 유사한 분자를 표면에 제시하는 능력을 분자 모방이라고 합니다.[37] 예를 들어, Neisseria meningitidis L2,3,5,7,9에서 올리고당(lacto-N-neotetraose)의 말단 사당류 부분은 인간 적혈구에서 발견되는 ABH 당지질 항원의 전구체인 paragloboside에서 발견되는 것과 동일한 사당류입니다.[6] 다른 예에서, 병원성 나이세리아 종으로부터의 올리고당의 말단 삼당류 부분(lactotriaose). LOS는 인간 세포의 락토네오스 계열 글리코스핑고지질에서도 발견됩니다.[6] 임균뿐만 아니라 그룹 B와 C의 대부분의 수막구균은 LOS 구조의 일부로 이 삼당류를 가지고 있는 것으로 나타났습니다.[6] 이러한 인간 세포 표면 '모방'의 존재는 면역계의 '카모' 역할을 할 뿐만 아니라 HLA-B35와 같은 특정 인간 백혈구 항원(HLA) 유전자형을 가진 숙주를 감염시킬 때 면역 내성을 없애는 역할을 할 수 있습니다.[6]
LPS는 TLR4와의 결합을 통해 조혈모세포(HSCs)에 의해 직접 감지되어 전신 감염에 대한 반응으로 증식할 수 있습니다. 이러한 반응은 HSC 내에서 TLR4-TRIF-ROS-p38 신호전달을 활성화하고 지속적인 TLR4 활성화를 통해 증식 스트레스를 유발하여 경쟁적인 재집계 능력을 손상시킬 수 있습니다.[38] S. typhimurium을 사용한 쥐의 감염도 유사한 결과를 보여 생체 내에서도 실험 모델을 검증했습니다.
변이성이 면역반응에 미치는 영향
O-항원(외부 탄수화물)은 LPS 분자에서 가장 가변적인 부분으로 항원 특이성을 부여합니다. 대조적으로 지질 A는 가장 보존된 부분입니다. 그러나 지질 A 조성은 또한 다양할 수 있습니다(예를 들어, 속 내 또는 속 간에도 아실 사슬의 수 및 특성). 이러한 변형 중 일부는 이러한 LPS에 길항 특성을 부여할 수 있습니다. 예를 들어, Rhodobacter sphaeroides (RsDPLA)의 디포스포릴 지질 A는 인간 세포에서 LPS의 강력한 길항제이지만 햄스터 및 말 세포에서는 작용제입니다.[39]
Porphyromonas gingivalis와 같은 원추형 지질 A는 더 작용적인 반면, Porphyromonas gingivalis와 같은 덜 원추형 지질 A는 다른 신호(TLR4 대신 TLR2)를 활성화할 수 있으며, Rodobacter sphaeroides와 같은 완전히 원통형 지질 A는 TLR에 길항적이라고 추측되었습니다.[40][41] 일반적으로 LPS 유전자 군집은 다른 균주, 아종, 식물 및 동물의 박테리아 병원체 종 간에 매우 다양합니다.[42][43]
정상적인 사람의 혈액 혈청은 살균성이 있는 항-LOS 항체를 포함하고 있으며 혈청형으로 구별되는 균주에 의해 감염된 환자는 정상 혈청과 비교하여 특이성이 다른 항-LOS 항체를 가지고 있습니다.[44] 다른 LOS 유형에 대한 체액성 면역 반응의 이러한 차이는 주로 LOS 분자의 올리고당 부분의 구조 내에서 LOS 분자의 구조에 기인할 수 있습니다.[44] Neisseria gonorrhoeae에서 LOS 분자의 항원성은 이 박테리아가 한 가지 이상의 LOS를 합성하는 능력으로 인해 감염 중에 변할 수 있음이 입증되었으며,[44] 이는 위상 변이로 알려져 있습니다. 또한, 나이세리아 고노르호에에(Neisseria gonorrhoeae) 및 나이세리아 수막염(Neisseria meningitidis) 및 헤모필루스 인플루엔자([6]Hemophilus influenzae)는 예를 들어, 시알화(sialic acid residue에 의한 변형)를 통해 시험관 내에서 LOS를 추가로 변형시킬 수 있습니다. 그리고 결과적으로 보체 매개 사멸 또는 심지어 다운 regulate 보체 활성화에 대한 내성을 증가시키거나 살균 항체의 영향을 회피할 수 있습니다. 시알릴화는 또한 감소된 산화 폭발뿐만 아니라 면역계 세포에 의한 호중구 부착 및 식균 작용을 방해하는 데 기여할 수 있습니다.[6] 소의 병원체인 Hemophilus somnus도 LOS 단계 변이를 나타내는 것으로 나타났는데, 이는 소 숙주 면역 방어의 회피에 도움이 될 수 있는 특징입니다.[45] 종합하면, 이러한 관찰은 LOS와 같은 박테리아 표면 분자의 변화가 병원체가 체액성(항체 및 보체 매개) 및 세포 매개(예를 들어, 호중구에 의한 사멸) 숙주 면역 방어 모두를 회피하는 데 도움이 될 수 있음을 시사합니다.
LPS 인식의 비정규 경로
최근에는 TLR4 매개 경로 외에도 일시적 수용체 전위 이온 채널군의 특정 구성체가 LPS를 인식하는 것으로 나타났습니다.[46] 마우스와[47] Drosophila melanogaster 파리에서 TRPA1의 LPS 매개 활성화가 나타났습니다.[48] 고농도에서, LPS는 TRPV1, TRPM3 및 어느 정도 TRPM8과 같은 감각 TRP 채널 패밀리의 다른 구성체도 활성화합니다.[49] LPS는 상피 세포에서 TRPV4에 의해 인식됩니다. LPS에 의한 TRPV4 활성화는 살균 효과와 함께 산화질소 생성을 유도하기 위해 필요하고 충분했습니다.[50]
테스트
지질다당류는 세균을 유해하게 만드는 중요한 요소이며, 세균의 구조와 기능에 따라 다른 그룹으로 분류하는 데 도움이 됩니다. 이를 통해 LPS는 다양한 그람 음성 박테리아를 구별하는 데 유용한 마커가 됩니다. 감염을 신속하게 관리하고 치료하기 위해서는 관련 병원체의 종류를 신속하게 파악하고 이해하는 것이 중요합니다. LPS는 우리 세포에서 면역 반응의 주요 유발 인자이기 때문에 급성 감염의 초기 신호로 작용합니다. 따라서 LPS 검사는 다른 많은 혈청학적 검사보다 더 구체적이고 의미가 있습니다.[51]
현재 LPS를 테스트하는 방법은 매우 민감하지만 많은 방법이 서로 다른 LPS 그룹을 구별하는 데 어려움을 겪고 있습니다. 또한, LPS는 물을 끌어당기는 특성과 물을 튕기는 특성(양친매성)을 모두 가지고 있어 민감하고 사용자 친화적인 테스트를 개발하기가 어렵습니다.[52]
일반적인 검출 방법은 LPS의 지질 A 부분을 식별하는 것에 의존합니다. 그러나 이 방법은 지질 A가 다른 박테리아 종과 혈청형 사이에서 매우 유사하기 때문에 한계가 있습니다. LPS 검사 기법은 생체 내 검사, 체외 검사, 변형 면역 검사, 생물학적 검사, 화학적 검사의 6가지 범주로 분류됩니다.[53]
병태생리학
LPS는 체내에서 세포 수용체와 결합하여 염증을 유발하는 강력한 독소입니다. 혈중 LPS가 과다하면 내독소혈증을 일으켜 잠재적으로 패혈성 쇼크라는 유해한 상태를 유발할 수 있습니다. 이 질환은 급격한 심장 박동, 빠른 호흡, 온도 변화, 혈액 응고 문제 등의 증상을 포함하며, 이로 인해 혈관이 확장되고 혈액량이 감소되어 세포 기능 장애가 발생합니다.[54]
최근 연구에 따르면 작은 LPS 노출도 자가면역질환 및 알레르기와 관련이 있다고 합니다. 혈중 LPS 수치가 높으면 대사증후군이 발생해 당뇨병, 심장질환, 간질환 등의 위험이 높아질 수 있습니다.[55]
또한 LPS는 워터하우스-프리데리히센 증후군, 수막구균혈증, 수막염과 같은 심각한 질환을 포함한 유해균 감염으로 인한 증상에 중요한 역할을 합니다. 특정 박테리아는 LPS를 적응시켜 호흡기와 소화기에 오래 지속되는 감염을 일으킬 수 있습니다.[56]
최근 연구에 따르면 LPS는 세포막 지질을 교란시켜 콜레스테롤과 대사에 영향을 미쳐 잠재적으로 높은 콜레스테롤, 비정상적인 혈중 지질 수치, 비알코올성 지방간 질환을 유발한다고 합니다. 경우에 따라서는 LPS가 독소 제거를 방해할 수 있으며, 이는 신경학적 문제와 관련이 있을 수 있습니다.[57]
건강영향
일반적으로 LPS의 건강 영향은 면역계의 강력한 활성화제 및 조절제로서의 능력, 특히 염증 유발에 기인합니다.
내독소혈증
혈액에 내독소가 존재하는 것을 내독소혈증이라고 합니다. 내독소혈증이 높으면 패혈성 쇼크가 올 수 있는 [58]반면, 혈중 내독소 농도가 낮아지면 대사성 내독소혈증이라고 합니다.[59] 내독소혈증은 비만, 식이,[60] 심혈관 질환 [60]및 당뇨병과 관련이 [59]있으며 숙주 유전학도 영향을 미칠 수 있습니다.[61]
더욱이, 특히 숙주-병원체 계면에서 장내 기원의 내독소혈증은 알코올성 간염의 발병에 중요한 요인으로 여겨지며,[62] 이는 소장 세균 과증식 증후군 및 장 투과성 증가에 근거하여 발병할 가능성이 있습니다.[63]
지질 A는 패혈성 쇼크를 유발할 수 있는 염증성 매개체의 생성으로 포유류 면역계의 조절되지 않은 활성화를 유발할 수 있습니다.[20] 이 염증 반응은 면역계 세포 활성화를 담당하는 Toll-like receptor 4에 의해 매개됩니다.[20] 이러한 염증매개물질로 인한 혈관 내피층 손상은 모세혈관 누출증후군, 혈관 확장, 심장기능 저하 등을 유발하고 패혈성 쇼크를 유발할 수 있습니다.[64] 뚜렷한 보체 활성화는 박테리아가 혈액에서 증식함에 따라 과정 후반에 관찰될 수도 있습니다.[64] 파괴적인 내피 손상을 유발하는 높은 박테리아 증식은 혈액 공급의 손상으로 인해 신장, 부신 및 폐와 같은 특정 내부 기관의 기능을 상실한 파종성 혈관 내 응고(DIC)를 유발할 수도 있습니다. 피부는 종종 페티시아, 자반병 및 에키모스의 형태로 응고 인자의 고갈과 함께 혈관 손상의 영향을 보여줄 수 있습니다. 사지도 영향을 받을 수 있으며, 때때로 괴저가 발생하는 등의 파괴적인 결과를 초래하여 후속 절단이 필요합니다.[64] 부신의 기능 상실은 부신 기능 부전을 유발할 수 있고 부신으로의 추가 출혈은 생명을 위협할 수 있는 워터하우스-프리데리히센 증후군을 유발할 수 있습니다.
임균 LOS는 인간 나팔관에 손상을 일으킬 수 있다는 보고도 있습니다.[44]
자가면역질환
일부 LOS 분자의 분자 모방은 다발성 경화증의 발적과 같은 자가면역 기반 숙주 반응을 일으키는 것으로 생각됩니다.[6][37] LOS를 통한 숙주 구조의 박테리아 모방의 다른 예는 인간의 위장 질환을 유발하는 유기체인 헬리코박터 파일로리균 및 캄필로박터 제주니 박테리아 및 샹크로이드를 유발하는 Hemophilus ducrey에서 발견됩니다. 특정 C. jejuni LPS 혈청형(핵심 올리고당의 특정 테트라- 및 펜타사카라이드 부분에 기인함)은 길랭-바레 증후군 및 밀러-피셔 증후군이라고 하는 길랭-바레 변종과도 관련이 있습니다.[6]
비만과의 연관성
역학 연구에 따르면 장내 내독소 생성 박테리아의 개체 수 증가의 결과로 발생할 수 있는 내독소 부하 증가는 특정 비만 관련 환자군과 관련이 있습니다.[7][65][66] 다른 연구들은 대장균에서 정제된 내독소가 무균 마우스 모델에 주입되었을 때 비만과 인슐린 저항성을 유도할 수 있다는 것을 보여주었습니다.[67] 보다 최근의 연구는 인간 환자의 비만과 인슐린 저항성에 대한 Enterobacter cloacae B29의 잠재적인 기여 역할을 밝혀냈습니다.[68] 내독소와 비만의 연관성에 대한 추정된 메커니즘은 내독소가 관찰된 비만과 인슐린 저항성을 설명하는 염증 매개 경로를 유도한다는 것입니다.[67] 내독소 관련 비만 효과와 관련된 박테리아 속에는 Escherichia와 Enterobacter가 있습니다.
우울증.
LPS가 우울증에 역할을 할 수 있다는 실험적, 관찰적 증거가 있습니다. 쥐에게 LPS를 투여하면 우울한 증상이 나타날 수 있고, 우울증이 있는 일부 사람들에게서는 LPS 수치가 상승하는 것으로 보입니다. 염증은 때때로 우울증의 발병에 역할을 할 수 있으며 LPS는 전염증입니다.[8]
세포노년증
LPS에 의해 유도된 염증은 폐 상피세포와 미세아교세포(후에 신경변성으로 이어지는 것)에서 보여진 바와 같이 세포노화를 유도할 수 있습니다.[9]
생명공학 및 연구에서 오염물질로서의 역할
지질다당류는 세균 또는 세균으로부터 발현된 단백질로부터 제조된 플라스미드 DNA에서 빈번한 오염물질로서, 오염 실험을 회피하고 산업용 발효를 이용하여 제조된 제품의 독성을 피하기 위해 DNA 또는 단백질로부터 제거되어야 합니다.[69]
오브알부민은 종종 내독소에 오염됩니다. 오브알부민은 동물 모델에서 광범위하게 연구된 단백질 중 하나이며 기도 과반응(AHR)에 대한 확립된 모델 알레르겐입니다. LPS에 오염된 시판되는 난형부민은 단백질 항원이 동물 생리에 미치는 영향을 정확히 반영하지 못해 연구 결과를 위조할 수 있습니다.[70]
의약품 생산에 있어서는 소량의 내독소라도 사람에게 병을 일으킬 수 있기 때문에 의약품 용기에 있는 미량의 내독소를 모두 제거할 필요가 있습니다. 이를 위해 탈수소 오븐을 사용합니다. LPS를 완전히 분해하려면 300°C가 넘는 온도가 필요합니다.[71]
내독소의 존재를 검출하기 위한 표준 분석법은 말굽게(Limulus polyphemus)의 혈액을 이용한 LAL(Limulus Amebocyte Lysate) 분석법입니다.[72] 매우 낮은 수준의 LPS는 효소 캐스케이드를 통한 강력한 증폭으로 인해 리물루스 용해물의 응고를 유발할 수 있습니다. 그러나 편자게의 개체수가 감소하고 LAL 분석을 방해하는 요인이 있다는 사실로 인해 대체 분석법을 개발하려는 노력이 이루어졌는데, 가장 유망한 것은 LAL 분석에서 단백질의 재조합 버전인 Factor C를 사용한 ELISA 테스트입니다.[73]
[74]1.지질다당류 [74]테스트는 박테리아를 해롭게 만드는 중요한 요소이며, 박테리아를 구조와 기능에 따라 다른 그룹으로 분류하는 데 도움이 됩니다. 이를 통해 LPS는 다양한 그람 음성 박테리아를 구별하는 데 유용한 마커가 됩니다. 감염을 신속하게 관리하고 치료하기 위해서는 관련 병원체의 종류를 신속하게 파악하고 이해하는 것이 중요합니다. LPS는 우리 세포에서 면역 반응의 주요 유발 인자이기 때문에 급성 감염의 초기 신호로 작용합니다. 따라서 LPS 검사는 다른 많은 혈청학적 검사보다 더 구체적이고 의미가 있습니다. 현재 LPS를 테스트하는 방법은 매우 민감하지만 많은 방법이 서로 다른 LPS 그룹을 구별하는 데 어려움을 겪고 있습니다. 또한, LPS는 물을 끌어당기는 특성과 물을 튕기는 특성(양친매성)을 모두 가지고 있어 민감하고 사용자 친화적인 테스트를 개발하기가 어렵습니다. 일반적인 검출 방법은 LPS의 지질 A 부분을 식별하는 것에 의존합니다. 그러나 이 방법은 지질 A가 다른 박테리아 종과 혈청형 사이에서 매우 유사하기 때문에 한계가 있습니다. LPS 검사 기법은 생체 내 검사, 체외 검사, 변형 면역 검사, 생물학적 검사, 화학적 검사의 6가지 범주로 분류됩니다.
[75]2.[75]병태생리 LPS는 체내에서 세포 수용체와 결합하여 염증을 유발하는 강력한 독소입니다. 혈중 LPS가 과다하면 내독소혈증을 일으켜 잠재적으로 패혈성 쇼크라는 유해한 상태를 유발할 수 있습니다. 이 질환은 급격한 심장 박동, 빠른 호흡, 온도 변화, 혈액 응고 문제 등의 증상을 포함하며, 이로 인해 혈관이 확장되고 혈액량이 감소되어 세포 기능 장애가 발생합니다. 최근 연구에 따르면 작은 LPS 노출도 자가면역질환 및 알레르기와 관련이 있다고 합니다. 혈중 LPS 수치가 높으면 대사증후군이 발생해 당뇨병, 심장질환, 간질환 등의 위험이 높아질 수 있습니다. 또한 LPS는 워터하우스-프리데리히센 증후군, 수막구균혈증, 수막염과 같은 심각한 질환을 포함한 유해균 감염으로 인한 증상에 중요한 역할을 합니다. 특정 박테리아는 LPS를 적응시켜 호흡기와 소화기에 오래 지속되는 감염을 일으킬 수 있습니다. 최근 연구에 따르면 LPS는 세포막 지질을 교란시켜 콜레스테롤과 대사에 영향을 미쳐 잠재적으로 높은 콜레스테롤, 비정상적인 혈중 지질 수치, 비알코올성 지방간 질환을 유발한다고 합니다. 경우에 따라서는 LPS가 독소 제거를 방해할 수 있으며, 이는 신경학적 문제와 관련이 있을 수 있습니다.
참고 항목
참고문헌
- ^ a b c Avila-Calderón ED, Ruiz-Palma MD, Contreras-Rodríguez A (2021). "Outer Membrane Vesicles of Gram-Negative Bacteria: An Outlook on Biogenesis". Frontiers in Microbiology. 12: 557902. doi:10.3389/fmicb.2021.557902. PMC 7969528. PMID 33746909.
- ^ Rietschel ET, Kirikae T, Schade FU, Mamat U, Schmidt G, Loppnow H, Ulmer AJ, Zähringer U, Seydel U, Di Padova F (1994). "Bacterial endotoxin: molecular relationships of structure to activity and function". FASEB J. 8 (2): 217–25. doi:10.1096/fasebj.8.2.8119492. PMID 8119492. S2CID 28156137.
- ^ Höfte, H.; de Greve, H.; Seurinck, J.; Jansens, S.; Mahillon, J.; Ampe, C.; Vandekerckhove, J.; Vanderbruggen, H.; van Montagu, M.; Zabeau, M. (1 December 1986). "Structural and functional analysis of a cloned delta endotoxin of Bacillus thuringiensis berliner 1715". European Journal of Biochemistry. 161 (2): 273–280. doi:10.1111/j.1432-1033.1986.tb10443.x. ISSN 0014-2956. PMID 3023091.
- ^ a b Roth, Joachim; Blatteis, Clark M. (October 2014). "Mechanisms of fever production and lysis: lessons from experimental LPS fever". Comprehensive Physiology. 4 (4): 1563–1604. doi:10.1002/cphy.c130033. ISSN 2040-4603. PMID 25428854.
- ^ Dellinger, R. Phillip; Levy, Mitchell M.; Rhodes, Andrew; Annane, Djillali; Gerlach, Herwig; Opal, Steven M.; Sevransky, Jonathan E.; Sprung, Charles L.; Douglas, Ivor S.; Jaeschke, Roman; Osborn, Tiffany M. (February 2013). "Surviving sepsis campaign: international guidelines for management of severe sepsis and septic shock: 2012". Critical Care Medicine. 41 (2): 580–637. doi:10.1097/CCM.0b013e31827e83af. ISSN 1530-0293. PMID 23353941. S2CID 34855187.
- ^ a b c d e f g h i j k l m n Moran AP, Prendergast MM, Appelmelk BJ (1996). "Molecular mimicry of host structures by bacterial lipopolysaccharides and its contribution to disease". FEMS Immunol. Med. Microbiol. 16 (2): 105–15. doi:10.1016/s0928-8244(96)00072-7. PMID 8988391.
- ^ a b Moreno-Navarrete JM, Ortega F, Serino M, Luche E, Waget A, Pardo G, Salvador J, Ricart W, Frühbeck G, Burcelin R, Fernández-Real JM (2012). "Circulating lipopolysaccharide-binding protein (LBP) as a marker of obesity-related insulin resistance". Int J Obes (Lond). 36 (11): 1442–9. doi:10.1038/ijo.2011.256. PMID 22184060.
- ^ a b Lasselin, Julie; Schedlowski, Manfred; Karshikoff, Bianka; Engler, Harald; Lekander, Mats; Konsman, Jan Pieter (August 2020). "Comparison of bacterial lipopolysaccharide-induced sickness behavior in rodents and humans: Relevance for symptoms of anxiety and depression". Neuroscience and Biobehavioral Reviews. 115: 15–24. doi:10.1016/j.neubiorev.2020.05.001. ISSN 1873-7528. PMID 32433924. S2CID 218665128.
- ^ a b Wei W, Ji S (2018). "Cellular senescence: Molecular mechanisms and pathogenicity". Journal of Cellular Physiology. 233 (12): 9121–9135. doi:10.1002/jcp.26956. PMID 30078211. S2CID 51924586.
- ^ Parija SC (1 January 2009). Textbook of Microbiology & Immunology. India: Elsevier. ISBN 978-8131221631.
- ^ Kulp A, Kuehn MJ (2010). "Biological functions and biogenesis of secreted bacterial outer membrane vesicles". Annu. Rev. Microbiol. 64: 163–84. doi:10.1146/annurev.micro.091208.073413. PMC 3525469. PMID 20825345.
- ^ Zhang G, Meredith TC, Kahne D (2013). "On the essentiality of lipopolysaccharide to Gram-negative bacteria". Curr. Opin. Microbiol. 16 (6): 779–785. doi:10.1016/j.mib.2013.09.007. PMC 3974409. PMID 24148302.
- ^ Kukkonen, Maini; Korhonen, Timo K. (July 2004). "The omptin family of enterobacterial surface proteases/adhesins: from housekeeping in Escherichia coli to systemic spread of Yersinia pestis". International Journal of Medical Microbiology. 294 (1): 7–14. doi:10.1016/j.ijmm.2004.01.003. ISSN 1438-4221. PMID 15293449.
- ^ Raetz CR, Whitfield C (2002). "Lipopolysaccharide endotoxins". Annu. Rev. Biochem. 71: 635–700. doi:10.1146/annurev.biochem.71.110601.135414. PMC 2569852. PMID 12045108.
- ^ Rittig MG, Kaufmann A, Robins A, Shaw B, Sprenger H, Gemsa D, Foulongne V, Rouot B, Dornand J (2003). "Smooth and rough lipopolysaccharide phenotypes of Brucella induce different intracellular trafficking and cytokine/chemokine release in human monocytes". J. Leukoc. Biol. 74 (6): 1045–55. doi:10.1189/jlb.0103015. PMID 12960272.
- ^ Tsujimoto H, Gotoh N, Nishino T (1999). "Diffusion of macrolide antibiotics through the outer membrane of Moraxella catarrhalis". J. Infect. Chemother. 5 (4): 196–200. doi:10.1007/s101560050034. PMID 11810516. S2CID 2742306.
- ^ Hershberger C, Binkley SB (1968). "Chemistry and metabolism of 3-deoxy-D-mannooctulosonic acid. I. Stereochemical determination". J. Biol. Chem. 243 (7): 1578–84. doi:10.1016/S0021-9258(18)93581-7. PMID 4296687.
- ^ Tzeng YL, Datta A, Kolli VK, Carlson RW, Stephens DS (May 2002). "Endotoxin of Neisseria meningitidis composed only of intact lipid A: inactivation of the meningococcal 3-deoxy-D-manno-octulosonic acid transferase". J. Bacteriol. 184 (9): 2379–88. doi:10.1128/JB.184.9.2379-2388.2002. PMC 134985. PMID 11948150.
- ^ Khan, Mohd M.; Ernst, Orna; Sun, Jing; Fraser, Iain D. C.; Ernst, Robert K.; Goodlett, David R.; Nita-Lazar, Aleksandra (24 June 2018). "Mass Spectrometry-based Structural Analysis and Systems Immunoproteomics Strategies for Deciphering the Host Response to Endotoxin". Journal of Molecular Biology. 430 (17): 2641–2660. doi:10.1016/j.jmb.2018.06.032. ISSN 1089-8638. PMID 29949751. S2CID 49481716.
- ^ a b c d Kilár A, Dörnyei Á, Kocsis B (2013). "Structural characterization of bacterial lipopolysaccharides with mass spectrometry and on- and off-line separation techniques". Mass Spectrom Rev. 32 (2): 90–117. Bibcode:2013MSRv...32...90K. doi:10.1002/mas.21352. PMID 23165926.
- ^ Munford R, Lu M, Varley AW (2009). Kill the Bacteria...and Also Their Messengers?. Advances in Immunology. Vol. 103. pp. 29–48. doi:10.1016/S0065-2776(09)03002-8. ISBN 9780123748324. PMC 2812913. PMID 19755182.
- ^ Bilski J, Mazur-Bialy A, Wojcik D, Zahradnik-Bilska J, Brzozowski B, Magierowski M, Mach T, Magierowska K, Brzozowski T (2017). "The Role of Intestinal Alkaline Phosphatase in Inflammatory Disorders of Gastrointestinal Tract". Mediators of Inflammation. 2017: 9074601. doi:10.1155/2017/9074601. PMC 5339520. PMID 28316376.
- ^ Bates JM, Akerlund J, Mittge E, Guillemin K (2007). "Intestinal alkaline phosphatase detoxifies lipopolysaccharide and prevents inflammation in zebrafish in response to the gut microbiota". Cell Host & Microbe. 2 (6): 371–382. doi:10.1016/j.chom.2007.10.010. PMC 2730374. PMID 18078689.
- ^ Alam SN, Yammine H, Moaven O, Ahmed R, Moss AK, Biswas B, Muhammad N, Biswas R, Raychowdhury A, Kaliannan K, Ghosh S, Ray M, Hamarneh SR, Barua S, Malo NS, Bhan AK, Malo MS, Hodin RA (April 2014). "Intestinal alkaline phosphatase prevents antibiotic-induced susceptibility to enteric pathogens". Annals of Surgery. 259 (4): 715–22. doi:10.1097/sla.0b013e31828fae14. PMC 3855644. PMID 23598380.
- ^ Lallès JP (February 2014). "Intestinal alkaline phosphatase: novel functions and protective effects". Nutrition Reviews. 72 (2): 82–94. doi:10.1111/nure.12082. PMID 24506153.
- ^ Wang X, Quinn PJ (2010). "Lipopolysaccharide: Biosynthetic pathway and structure modification". Prog. Lipid Res. 49 (2): 97–107. doi:10.1016/j.plipres.2009.06.002. PMID 19815028.
- ^ Ruiz N, Kahne D, Silhavy TJ (2009). "Transport of lipopolysaccharide across the cell envelope: the long road of discovery". Nat. Rev. Microbiol. 7 (9): 677–83. doi:10.1038/nrmicro2184. PMC 2790178. PMID 19633680.
- ^ Romano, K. P., & Hung, D. T. (2023). 다제내성 시대에 그람 음성균에서 LPS 생합성 및 수송을 목표로 합니다. Biochimica et biophysica acta. 분자세포 연구, 1870(3), 119407. https://doi.org/10.1016/j.bbamcr.2022.119407
- ^ Abbas, Abul (2006). Basic Immunology. Elsevier. ISBN 978-1-4160-2974-8.
- ^ Poltorak A, He X, Smirnova I, Liu MY, Van Huffel C, Du X, Birdwell D, Alejos E, Silva M, Galanos C, Freudenberg M, Ricciardi-Castagnoli P, Layton B, Beutler B (1998). "Defective LPS signaling in C3H/HeJ and C57BL/10ScCr mice: mutations in Tlr4 gene". Science. 282 (5396): 2085–8. Bibcode:1998Sci...282.2085P. doi:10.1126/science.282.5396.2085. PMID 9851930.
- ^ "The 2011 Nobel Prize in Physiology or Medicine - Press Release". www.nobelprize.org. Archived from the original on 23 March 2018. Retrieved 28 April 2018.
- ^ Li, Yao; Deng, Shou-Long; Lian, Zheng-Xing; Yu, Kun (12 June 2019). "Roles of Toll-Like Receptors in Nitroxidative Stress in Mammals". Cells. 8 (6): 576. doi:10.3390/cells8060576. ISSN 2073-4409. PMC 6627996. PMID 31212769.
- ^ Warren HS, Fitting C, Hoff E, Adib-Conquy M, Beasley-Topliffe L, Tesini B, Liang X, Valentine C, Hellman J, Hayden D, Cavaillon JM (2010). "Resilience to bacterial infection: difference between species could be due to proteins in serum". J. Infect. Dis. 201 (2): 223–32. doi:10.1086/649557. PMC 2798011. PMID 20001600.
- ^ Reid RR, Prodeus AP, Khan W, Hsu T, Rosen FS, Carroll MC (1997). "Endotoxin shock in antibody-deficient mice: unraveling the role of natural antibody and complement in the clearance of lipopolysaccharide". J. Immunol. 159 (2): 970–5. doi:10.4049/jimmunol.159.2.970. PMID 9218618.
- ^ Boes M, Prodeus AP, Schmidt T, Carroll MC, Chen J (1998). "A critical role of natural immunoglobulin M in immediate defense against systemic bacterial infection". J. Exp. Med. 188 (12): 2381–6. doi:10.1084/jem.188.12.2381. PMC 2212438. PMID 9858525.
- ^ Said EA, Dupuy FP, Trautmann L, Zhang Y, Shi Y, El-Far M, Hill BJ, Noto A, Ancuta P, Peretz Y, Fonseca SG, Van Grevenynghe J, Boulassel MR, Bruneau J, Shoukry NH, Routy JP, Douek DC, Haddad EK, Sekaly RP (2010). "Programmed death-1-induced interleukin-10 production by monocytes impairs CD4+ T cell activation during HIV infection". Nat. Med. 16 (4): 452–9. doi:10.1038/nm.2106. PMC 4229134. PMID 20208540.
- ^ a b Chastain EM, Miller SD (2012). "Molecular mimicry as an inducing trigger for CNS autoimmune demyelinating disease". Immunol. Rev. 245 (1): 227–38. doi:10.1111/j.1600-065X.2011.01076.x. PMC 3586283. PMID 22168423.
- ^ Takizawa, Hitoshi; Fritsch, Kristin; Kovtonyuk, Larisa V.; Saito, Yasuyuki; Yakkala, Chakradhar; Jacobs, Kurt; Ahuja, Akshay K.; Lopes, Massimo; Hausmann, Annika (3 August 2017). "Pathogen-Induced TLR4-TRIF Innate Immune Signaling in Hematopoietic Stem Cells Promotes Proliferation but Reduces Competitive Fitness". Cell Stem Cell. 21 (2): 225–240.e5. doi:10.1016/j.stem.2017.06.013. ISSN 1875-9777. PMID 28736216.
- ^ Lohmann KL, Vandenplas ML, Barton MH, Bryant CE, Moore JN (2007). "The equine TLR4/MD-2 complex mediates recognition of lipopolysaccharide from Rhodobacter sphaeroides as an agonist". Journal of Endotoxin Research. 13 (4): 235–242. doi:10.1177/0968051907083193. PMID 17956942. S2CID 36784237.
- ^ Netea MG, van Deuren M, Kullberg BJ, Cavaillon JM, Van der Meer JW (2002). "Does the shape of lipid A determine the interaction of LPS with Toll-like receptors?". Trends Immunol. 23 (3): 135–9. doi:10.1016/S1471-4906(01)02169-X. PMID 11864841.
- ^ Seydel U, Oikawa M, Fukase K, Kusumoto S, Brandenburg K (2000). "Intrinsic conformation of lipid A is responsible for agonistic and antagonistic activity". Eur. J. Biochem. 267 (10): 3032–9. doi:10.1046/j.1432-1033.2000.01326.x. PMID 10806403.
- ^ Reeves PP, Wang L (2002). "Genomic Organization of LPS-Specific Loci". In Hacker J, Kaper J (eds.). Pathogenicity Islands and the Evolution of Pathogenic Microbes. Current Topics in Microbiology and Immunology. Vol. 2. pp. 109–35. doi:10.1007/978-3-642-56031-6_7. ISBN 978-3-540-42682-0. PMID 12014174. 264.
- ^ Patil PB, Sonti RV (2004). "Variation suggestive of horizontal gene transfer at a lipopolysaccharide (lps) biosynthetic locus in Xanthomonas oryzae pv. oryzae, the bacterial leaf blight pathogen of rice". BMC Microbiol. 4: 40. doi:10.1186/1471-2180-4-40. PMC 524487. PMID 15473911.
- ^ a b c d e Yamasaki R, Kerwood DE, Schneider H, Quinn KP, Griffiss JM, Mandrell RE (1994). "The structure of lipooligosaccharide produced by Neisseria gonorrhoeae, strain 15253, isolated from a patient with disseminated infection. Evidence for a new glycosylation pathway of the gonococcal lipooligosaccharide". J. Biol. Chem. 269 (48): 30345–51. doi:10.1016/S0021-9258(18)43819-7. PMID 7982947.
- ^ Howard MD, Cox AD, Weiser JN, Schurig GG, Inzana TJ (2000). "Antigenic diversity of Haemophilus somnus lipooligosaccharide: phase-variable accessibility of the phosphorylcholine epitope". J. Clin. Microbiol. 38 (12): 4412–9. doi:10.1128/JCM.38.12.4412-4419.2000. PMC 87614. PMID 11101573.
- ^ Boonen, Brett; Alpizar, Yeranddy; Meseguer, Victor; Talavera, Karel; Boonen, Brett; Alpizar, Yeranddy A.; Meseguer, Victor M.; Talavera, Karel (11 August 2018). "TRP Channels as Sensors of Bacterial Endotoxins". Toxins. 10 (8): 326. doi:10.3390/toxins10080326. PMC 6115757. PMID 30103489.
- ^ Meseguer, Victor; Alpizar, Yeranddy A.; Luis, Enoch; Tajada, Sendoa; Denlinger, Bristol; Fajardo, Otto; Manenschijn, Jan-Albert; Fernández-Peña, Carlos; Talavera, Arturo; Kichko, Tatiana; Navia, Belén; Sánchez, Alicia; Señarís, Rosa; Reeh, Peter; Pérez-García, María Teresa; López-López, José Ramón; Voets, Thomas; Belmonte, Carlos; Talavera, Karel; Viana, Félix (20 January 2014). "TRPA1 channels mediate acute neurogenic inflammation and pain produced by bacterial endotoxins". Nature Communications. 5: 3125. Bibcode:2014NatCo...5.3125M. doi:10.1038/ncomms4125. PMC 3905718. PMID 24445575.
- ^ Soldano, Alessia; Alpizar, Yeranddy A; Boonen, Brett; Franco, Luis; López-Requena, Alejandro; Liu, Guangda; Mora, Natalia; Yaksi, Emre; Voets, Thomas; Vennekens, Rudi; Hassan, Bassem A; Talavera, Karel (14 June 2016). "Gustatory-mediated avoidance of bacterial lipopolysaccharides via TRPA1 activation in Drosophila". eLife. 5. doi:10.7554/eLife.13133. PMC 4907694. PMID 27296646.
- ^ Boonen, Brett; Alpizar, Yeranddy A.; Sanchez, Alicia; López-Requena, Alejandro; Voets, Thomas; Talavera, Karel (July 2018). "Differential effects of lipopolysaccharide on mouse sensory TRP channels". Cell Calcium. 73: 72–81. doi:10.1016/j.ceca.2018.04.004. PMID 29689522. S2CID 13681499.
- ^ Alpizar, Yeranddy A.; Boonen, Brett; Sanchez, Alicia; Jung, Carole; López-Requena, Alejandro; Naert, Robbe; Steelant, Brecht; Luyts, Katrien; Plata, Cristina; De Vooght, Vanessa; Vanoirbeek, Jeroen A. J.; Meseguer, Victor M.; Voets, Thomas; Alvarez, Julio L.; Hellings, Peter W.; Hoet, Peter H. M.; Nemery, Benoit; Valverde, Miguel A.; Talavera, Karel (20 October 2017). "TRPV4 activation triggers protective responses to bacterial lipopolysaccharides in airway epithelial cells". Nature Communications. 8 (1): 1059. Bibcode:2017NatCo...8.1059A. doi:10.1038/s41467-017-01201-3. PMC 5651912. PMID 29057902.
- ^ 페이지, M.J., 켈, DB., & 프레토리우스, E. (2022) 만성 염증에서 지질다당류에 의한 세포 신호전달의 역할 만성 스트레스 (California, Thousand Oaks), 6,24705470221076390 https://doi.org/10.1177/24705470221076390
- ^ 페이지, M.J., 켈, DB., & 프레토리우스, E. (2022) 만성 염증에서 지질다당류에 의한 세포 신호전달의 역할 만성 스트레스 (California, Thousand Oaks), 6,24705470221076390 https://doi.org/10.1177/24705470221076390
- ^ 페이지, M.J., 켈, DB., & 프레토리우스, E. (2022) 만성 염증에서 지질다당류에 의한 세포 신호전달의 역할 만성 스트레스 (California, Thousand Oaks), 6,24705470221076390 https://doi.org/10.1177/24705470221076390
- ^ 페이지, M.J., 켈, DB., & 프레토리우스, E. (2022) 만성 염증에서 지질다당류에 의한 세포 신호전달의 역할 만성 스트레스 (California, Thousand Oaks), 6,24705470221076390 https://doi.org/10.1177/24705470221076390
- ^ 페이지, M.J., 켈, DB., & 프레토리우스, E. (2022) 만성 염증에서 지질다당류에 의한 세포 신호전달의 역할 만성 스트레스 (California, Thousand Oaks), 6,24705470221076390 https://doi.org/10.1177/24705470221076390
- ^ 페이지, M.J., 켈, DB., & 프레토리우스, E. (2022) 만성 염증에서 지질다당류에 의한 세포 신호전달의 역할 만성 스트레스 (California, Thousand Oaks), 6,24705470221076390 https://doi.org/10.1177/24705470221076390
- ^ 페이지, M.J., 켈, DB., & 프레토리우스, E. (2022) 만성 염증에서 지질다당류에 의한 세포 신호전달의 역할 만성 스트레스 (California, Thousand Oaks), 6,24705470221076390 https://doi.org/10.1177/24705470221076390
- ^ Opal SM (2010). "Endotoxins and other sepsis triggers". Endotoxemia and Endotoxin Shock. Contributions to Nephrology. Vol. 167. pp. 14–24. doi:10.1159/000315915. ISBN 978-3-8055-9484-4. PMID 20519895.
- ^ a b Gomes, Júnia Maria Geraldo; Costa, Jorge de Assis; Alfenas, Rita de Cássia Gonçalves (March 2017). "Metabolic endotoxemia and diabetes mellitus: A systematic review". Metabolism. 68: 133–144. doi:10.1016/j.metabol.2016.12.009. PMID 28183445.
- ^ a b Kallio, K. A. Elisa; Hätönen, Katja A.; Lehto, Markku; Salomaa, Veikko; Männistö, Satu; Pussinen, Pirkko J. (April 2015). "Endotoxemia, nutrition, and cardiometabolic disorders". Acta Diabetologica. 52 (2): 395–404. doi:10.1007/s00592-014-0662-3. ISSN 0940-5429. PMID 25326898. S2CID 24020127.
- ^ Leskelä, Jaakko; Toppila, Iiro; Härma, Mari‐Anne; Palviainen, Teemu; Salminen, Aino; Sandholm, Niina; Pietiäinen, Milla; Kopra, Elisa; Pais de Barros, Jean‐Paul; FinnGen; Lassenius, Mariann I. (20 October 2021). "Genetic Profile of Endotoxemia Reveals an Association With Thromboembolism and Stroke". Journal of the American Heart Association. 10 (21): e022482. doi:10.1161/JAHA.121.022482. ISSN 2047-9980. PMC 8751832. PMID 34668383.
- ^ Ceccanti M, Attili A, Balducci G, Attilia F, Giacomelli S, Rotondo C, Sasso GF, Xirouchakis E, Attilia ML (2006). "Acute alcoholic hepatitis". J. Clin. Gastroenterol. 40 (9): 833–41. doi:10.1097/01.mcg.0000225570.04773.5d. PMID 17016141.
- ^ Parlesak A, Schäfer C, Schütz T, Bode JC, Bode C (2000). "Increased intestinal permeability to macromolecules and endotoxemia in patients with chronic alcohol abuse in different stages of alcohol-induced liver disease". J. Hepatol. 32 (5): 742–7. doi:10.1016/S0168-8278(00)80242-1. PMID 10845660.
- ^ a b c Stephens DS, Greenwood B, Brandtzaeg P (2007). "Epidemic meningitis, meningococcaemia, and Neisseria meningitidis". Lancet. 369 (9580): 2196–210. doi:10.1016/S0140-6736(07)61016-2. PMID 17604802. S2CID 16951072.
- ^ Lepper PM, Schumann C, Triantafilou K, Rasche FM, Schuster T, Frank H, Schneider EM, Triantafilou M, von Eynatten M (2007). "Association of lipopolysaccharide-binding protein and coronary artery disease in men". J. Am. Coll. Cardiol. 50 (1): 25–31. doi:10.1016/j.jacc.2007.02.070. PMID 17601541. S2CID 12136094.
- ^ Ruiz AG, Casafont F, Crespo J, Cayón A, Mayorga M, Estebanez A, Fernadez-Escalante JC, Pons-Romero F (2007). "Lipopolysaccharide-binding protein plasma levels and liver TNF-alpha gene expression in obese patients: evidence for the potential role of endotoxin in the pathogenesis of non-alcoholic steatohepatitis". Obes Surg. 17 (10): 1374–80. doi:10.1007/s11695-007-9243-7. PMID 18000721. S2CID 44494003.
- ^ a b Cani PD, Amar J, Iglesias MA, Poggi M, Knauf C, Bastelica D, Neyrinck AM, Fava F, Tuohy KM, Chabo C, Waget A, Delmée E, Cousin B, Sulpice T, Chamontin B, Ferrières J, Tanti JF, Gibson GR, Casteilla L, Delzenne NM, Alessi MC, Burcelin R (2007). "Metabolic endotoxemia initiates obesity and insulin resistance". Diabetes. 56 (7): 1761–72. doi:10.2337/db06-1491. PMID 17456850.
- ^ Fei N, Zhao L (December 2012). "An opportunistic pathogen isolated from the gut of an obese human causes obesity in germfree mice". ISME J. 7 (4): 880–4. doi:10.1038/ismej.2012.153. PMC 3603399. PMID 23235292.
- ^ Wicks, Ian P.; Howell, Meredith L.; Hancock, Tuesday; Kohsaka, Hitoshi; Olee, Tsaiwei; Carson, Dennis A. (March 1995). "Bacterial Lipopolysaccharide Copurifies with Plasmid DNA: Implications for Animal Models and Human Gene Therapy". Human Gene Therapy. 6 (3): 317–323. doi:10.1089/hum.1995.6.3-317. PMID 7779915.
- ^ Watanabe, Junji; Miyazaki, Yasunari; Zimmerman, Guy A.; Albertine, Kurt H.; McIntyre, Thomas M. (24 October 2003). "Endotoxin contamination of ovalbumin suppresses murine immunologic responses and development of airway hyper-reactivity". The Journal of Biological Chemistry. 278 (43): 42361–42368. doi:10.1074/jbc.M307752200. ISSN 0021-9258. PMID 12909619.
- ^ 16 December 2014. "The Detection of Endotoxins Via the LAL Test, the Chromogenic Method". Archived from the original on 29 March 2015. Retrieved 14 March 2015.
{{cite web}}: CS1 main: 숫자 이름: 저자 목록 (링크) - ^ Iwanaga S (2007). "Biochemical principle of Limulus test for detecting bacterial endotoxins". Proc. Jpn. Acad., Ser. B, Phys. Biol. Sci. 83 (4): 110–9. Bibcode:2007PJAB...83..110I. doi:10.2183/pjab.83.110. PMC 3756735. PMID 24019589.
- ^ Ding JL, Ho B (2001). "A new era in pyrogen testing" (PDF). Trends Biotechnol. 19 (8): 277–81. doi:10.1016/s0167-7799(01)01694-8. PMID 11451451. Archived from the original (PDF) on 2 January 2014. Retrieved 2 January 2014.
- ^ 페이지, M.J., 켈, DB., & 프레토리우스, E. (2022) 만성 염증에서 지질다당류에 의한 세포 신호전달의 역할 만성 스트레스 (California, Thousand Oaks), 6,24705470221076390 https://doi.org/10.1177/24705470221076390
- ^ 페이지, M.J., 켈, DB., & 프레토리우스, E. (2022) 만성 염증에서 지질다당류에 의한 세포 신호전달의 역할 만성 스트레스 (California, Thousand Oaks), 6,24705470221076390 https://doi.org/10.1177/24705470221076390


