자나미비르
Zanamivir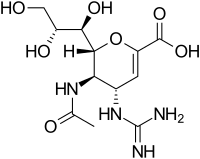 | |
| 임상 데이터 | |
|---|---|
| 발음 | /zz-ném v-r/ |
| 상호 | 레렌자 |
| AHFS/Drugs.com | 모노그래프 |
| 임신 카테고리 |
|
| 루트 행정부. | 흡입, IV |
| ATC 코드 | |
| 법적 상태 | |
| 법적 상태 | |
| 약동학 데이터 | |
| 바이오 어베이러빌리티 | 2%(구강) |
| 단백질 결합 | 10 % 미만 |
| 대사 | 무시할 수 있다 |
| 반감기 제거 | 2.5~5.1시간 |
| 배설물 | 신장 |
| 식별자 | |
| |
| CAS 번호 | |
| PubChem CID | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 체비 | |
| 첸블 | |
| PDB배위자 | |
| CompTox 대시 보드 (EPA ) | |
| ECHA 정보 카드 | 100.218.632 |
| 화학 및 물리 데이터 | |
| 공식 | C12H20N4O7 |
| 몰 질량 | 332.313g/120−1 |
| 3D 모델(JSmol) | |
| |
| |
| (표준) | |
자나미비르는 인플루엔자 A와 B 바이러스에 의한 인플루엔자 치료와 예방에 사용되는 약이다.이것은 뉴라미니다아제 억제제이며 호주의 바이오타 홀딩스에 의해 개발되었다.1990년 글락소에 허가되었고 1999년 미국에서 인플루엔자 치료제로만 사용되도록 승인되었다.2006년에는 인플루엔자 A와 [1]B의 예방을 위해 승인되었다. Zanamivir는 상업적으로 개발된 최초의 뉴라미니다아제 억제제이다.현재 GlaxoSmithKline에서 Relenza라는 상표명으로 경구흡입용 분말로 판매되고 있습니다.
의료 용도
Zanamivir는 인플루엔자 A와 인플루엔자 B 바이러스에 의한 감염 치료에 사용되지만, 그렇지 않으면 건강한 사람에게는 전반적으로 혜택이 적은 것으로 보인다.그것은 사람이 증상에 걸릴 위험을 줄여주지만, 무증상 인플루엔자는 아니다.진단의 불확실성, 바이러스 균주 내성의 위험성, 가능한 부작용과 재정적인 비용의 조합은 건강한 [2]개인의 예방과 치료를 위한 자나미비르의 작은 이점보다 더 크다.
이후 자나미비르 [3]치료 과정에서 조류인플루엔자 A형 H7N9에 감염된 중국인에게서 자나미비르 내성 유전자가 발견됐다.
치료
그렇지 않으면 건강한 개인에게는 전반적으로 혜택이 [2]적은 것으로 보인다.자나미비르는 인플루엔자와 유사한 질병의 증상 기간을 하루 미만으로 단축한다.천식이 있는 아이들의 경우 첫 [4]증상 완화 시간에 뚜렷한 효과가 없었다.그것이 입원해야 할 위험성에 영향을 미치는지 아니면 사망 위험에 영향을 미치는지 [2]명확하지 않다.자나미비르가 입원이나 폐렴, 기관지염, 중이염,[4][5] 축농증 등 인플루엔자의 다른 합병증을 줄였다는 증거는 없다.Zanamivir는 조사관이 직접 보고한 폐렴이나 성인의 방사능 확인 폐렴의 위험을 줄이지 않았다.소아 폐렴에 대한 영향 또한 [6]크지 않았다.
예방
낮은 증거에서 중간 증거는 그것이 [2]노출된 사람들에게서 1에서 12%까지 인플루엔자에 걸릴 위험을 감소시킨다는 것을 보여준다.예방 실험에서는 자나미비르가 개인과 가정에서 증상 인플루엔자의 위험을 줄였지만, 무증상 인플루엔자나 다른 인플루엔자 유사 질환에 대한 영향의 증거는 없었다.또한 인플루엔자 바이러스의 사람 [4]대 사람 확산 위험이 감소했다는 증거는 없었다.인플루엔자 예방의 유익성에 대한 증거는 [7]문헌의 출판 편향에 대한 우려와 함께 어린이에게 약하다.
저항
2009년 현재 미국에서는 [8]내성의 징후를 보이는 인플루엔자는 없었다.2011년 메타분석 결과 자나미비르 내성이 거의 [9]보고되지 않은 것으로 나타났다.항바이러스 내성은 특정 사람에게 항바이러스제를 투여하는 치료 중 또는 치료 후에 나타날 수 있습니다(예:[10] 면역 억제).2013년 조류 인플루엔자 A H7N9에 [3]감염된 중국인 환자에서 자나미비르(및 오셀타미비르)에 대한 내성을 발현하는 유전자가 발견되었다.
부작용
투여는 흡입 경로로 제한된다.이것은 천식을 치료하면 기관지 [11]경련을 유발할 수 있기 때문에 사용을 제한한다.2006년 미국 식품의약국(FDA)은 Relenza의 최초 승인 후 일부 환자에서 사망을 포함한 호흡 문제(브론코스마)가 보고되었음을 발견했다.이 환자들 대부분은 천식이나 만성폐쇄성폐질환을 앓고 있었다.따라서 천식이나 만성폐쇄성 [12]폐질환이 있는 사람의 계절성 인플루엔자 치료나 예방에는 릴렌자가 권장되지 않았다.2009년 자나미비르 패키지 삽입물에는 호흡기 [13]질환 환자의 기관지 경련 위험에 대한 예방 정보가 포함되어 있습니다.글락소스미스클라인(GSK)과 FDA는 가용화 및 기계적 [14]환기로 투여된 자미비르 흡입 분말을 투여받은 인플루엔자 환자의 사망 보고를 의료 전문가에게 통보했다.
성인의 경우 임상시험에서 보고된 부작용의 위험이 증가하지 않았다.자나미비르에 [4]걸린 아이들의 치료와 관련된 가능한 해악에 대한 증거는 거의 없었다.자나미비르는 독성을 유발하는 것으로 알려져 있지 않고 인체에 [15]대한 신체 노출이 낮다.
작용 메커니즘
자나미비르는 뉴라미니다아제 단백질의 활성 부위에 결합함으로써 인플루엔자 바이러스가 숙주 세포를 빠져나오지 못하게 하고 [16]다른 사람들을 감염시키는 역할을 한다.또한 체외 및 체내 인플루엔자 바이러스 복제 억제제이다.임상 시험에서 자나미비르는 증상 시작 후 48시간 이내에 치료를 시작하면 증상 해결 시간을 1.5일 단축하는 것으로 밝혀졌다.
자나미비르의 생물학적 가용성은 2%이다.흡입 후, 자나미비르는 폐와 구인두에 농축되어 최대 15%의 용량이 흡수되고 [17]소변으로 배설된다.
역사
자나미비르는 1989년 호주 CSIRO의 피터[18][19] 콜먼과 조셉 바르헤스가[20] 이끄는 과학자들이 빅토리아 약대 및 모나시 대학과 공동으로 처음 만들었다.자나미비르는 뉴라미니다아제 억제제 중 첫 번째였다.이 발견은 처음에는 호주의 생명공학 회사인 Biota가 자금을 지원했으며 합리적인 약물 설계를 통해 항바이러스제를 개발하는 Biota의 진행 중인 프로그램의 일부였다.그 전략은 X선 결정학에 의한 인플루엔자 뉴라미니다아제 구조의 가용성에 의존했다.또한 1974년까지 시알산 유사체인 2-디옥시-2,3-디데히드로-N-아세틸뉴라민산(DANA)이 뉴라미니다아제 [21]억제제라는 사실이 알려져 있었다.
계산 화학 기술은 효소의 활성 부위를 조사하기 위해 사용되었으며, 촉매 부위의 아미노산 잔기에 단단히 결합하는 DANA의 유도체를 설계하기 위해 시도되었다. 따라서 효소의 강력하고 특이적인 억제제가 될 것이다.Molecular Discovery의 GRID 소프트웨어는 다양한 기능군과 촉매 부위 협곡의 잔류물 사이의 에너지적으로 바람직한 상호작용을 결정하기 위해 사용되었다.이 조사 결과, DANA의4 C 하이드록실기와 일치하는 뉴라미니다아제 활성 부위에서 음전하 구역이 발생하는 것으로 나타났다.따라서 활성 부위에서 보존된 글루탐산(119)과 소금 브릿지가 형성되었기 때문에 4-아미노 DANA는 양전하 아미노기로 대체되었다.글루 119는 또한 더 크지만 더 기본적인 구아니딘 [22]기능군을 수용할 수 있을 만큼 충분히 큰 활성 부위의 보존된 주머니의 바닥에 있는 것으로 확인되었다.그 결과 [23]뉴라미니다아제의 전이 상태 아날로그 억제제인 자나미비르가 나왔다.
Biota는 작은 회사였기 때문에, Zanamivir를 단독으로 시장에 투입할 수 있는 자원이 없었다.1990년 자나미비르 특허권은 글락소(현 글락소스미스클라인)에 라이선스됐다.라이센스 계약서에 따르면 Biota는 Glaxo의 Zanamivir 판매에 대해 7%의 로열티를 받을 수 있습니다.
1999년, 이 제품은 인플루엔자 A와 B의 치료를 위해 미국과 유럽에서의 시판 허가를 받았습니다.FDA 자문위원회는 13 대 4의 표결에서 환자들이 파라세타몰과 같은 다른 약물을 복용했을 때 효과가 부족하고 위약보다 더 효과적이지 않기 때문에 승인해서는 안 된다고 권고했다.그러나 FDA 지도부는 위원회를 무시하고 위원회의 검토자인 생물통계학자 마이클 엘라쇼프를 비난했다.그 당시 승인 절차 중이었던 oseltamivir에 대한 심사는 그에게서 빼앗겨 [24]다른 사람에게 위임되었다.2006년 미국과 유럽에서는 A와 [1]B 인플루엔자 예방을 위해 자나미비르가 승인되었다.
자나미비르는 첫 번째 뉴라미니다아제 억제제였지만, 경구 캡슐 제제를 사용한 두 번째 진입자인 오셀타미비르(타미플루)보다 불과 몇 개월 앞서 있었다.
1999/2000년에 미국에서 처음 판매되었을 때, Zanamivir는 대규모 판촉 캠페인에도 불구하고 인플루엔자 항바이러스 시장의 25%만을 점유했습니다.그 시즌이 끝날 무렵, 타미플루는 자나미비르를 3:1로 앞지르고 있었다.그 시즌 동안, 자나미비르는 기관지 경련과 사망의 위험과 관련된 세계적인 안전 경고를 경험했다.그 후 글락소는 자나미비르의 판매를 줄였고 타미플루의 지배력은 증가했다.첫 번째 시즌에서 Glaxo가 판매한 2000만 달러 이상의 Zanamivir는 환자에 대한 매출이 예상보다 훨씬 낮았기 때문에 다음 두 시즌 동안 회사에 반환되었습니다.
비오타는 글락소가 자나미비르의 판매를 줄인 것이 계약 위반이라고 주장하며 2004년 법적 절차를 시작했다.바이오타는 글락소로부터 약 7억 호주달러를 요구했다.Biota는 소송을 진행하기 위해 4년간 노력하여 5천만 호주달러의 소송 비용을 부담한 후 2008년 7월에 청구를 포기했으며 조정에서의 해결로 인한 소송 비용을 포함하여 2천만 호주달러만 회수했습니다.Biota는 Glaxo로부터 7500만 호주달러와 소송비용을 더 받는 전술적 제안을 거절했었다.
2006년 8월 독일은 조류독감 대비 전략의 일환으로 170만 도스의 자나미비르를 구입할 것이라고 발표했다."독일의 구매는 국가들이 인플루엔자 대비에 대해 균형 잡힌 시각을 갖기 시작했음을 보여줍니다,"라고 자나미비어가 원래 [16]개발되었던 멜버른 소재 바이오타의 연구 책임자인 사이먼 터커는 말했다.
2009년 4월에는 미국과 멕시코에서 신종플루(H1N1형 바이러스) 환자가 다수 보고되었다.자나미비르는 그것을 치료하기 위해 처방된 두 가지 약 중 하나이다.2009년 6월에 발표된 연구는 2009년 H1N1 돼지 플루 뉴라미니다아제(NA)가 타미플루 내성(His274Tyr)을 획득하는 시나리오에서 이러한 약물의 성능 평가에 기초해 자나미비어를 포함한 추가적인 항바이러스제와 함께 오셀타미비르 비축량의 증대가 시급하다고 강조했다.테스트된 모든 계절 H1N1 [25]균주의 99.6%에 광범위하게 분포합니다.
2011년 1월 GSK는 북반구와 남반구 [26]20개국에 걸친 연구에서 자나미비르 정맥주사 임상시험 3단계를 시작할 것이라고 발표했다.
레퍼런스
- ^ a b "FDA Approves a Second Drug for the Prevention of Influenza A and B in Adults and Children FDA press release March 29, 2006". FDA.
- ^ a b c d Michiels, B.; Van Puyenbroeck, K.; Verhoeven, V.; Vermeire, E.; Coenen, S. (2013). "The value of neuraminidase inhibitors for the prevention and treatment of seasonal influenza: a systematic review of systematic reviews". PLOS ONE. 8 (4): e60348. Bibcode:2013PLoSO...860348M. doi:10.1371/journal.pone.0060348. PMC 3614893. PMID 23565231.
- ^ a b Hu, Y.; Lu, S.; Song, Z.; Wang, W.; Hao, P.; Li, J.; Zhang, X.; Yen, H. L.; Shi, B.; Li, T.; Guan, W.; Xu, L.; Liu, Y.; Wang, S.; Zhang, X.; Tian, D.; Zhu, Z.; He, J.; Huang, K.; Chen, H.; Zheng, L.; Li, X.; Ping, J.; Kang, B.; Xi, X.; Zha, L.; Li, Y.; Zhang, Z.; Peiris, M.; Yuan, Z. (2013). "Association between adverse clinical outcome in human disease caused by novel influenza a H7N9 virus and sustained viral shedding and emergence of antiviral resistance". The Lancet. 381 (9885): 2273–2279. doi:10.1016/S0140-6736(13)61125-3. PMID 23726392. S2CID 7537862.
- ^ a b c d Jefferson, T; Jones, MA; Doshi, P; Del Mar, CB; Hama, R; Thompson, MJ; Spencer, EA; Onakpoya, I; Mahtani, KR; Nunan, D; Howick, J; Heneghan, CJ (10 April 2014). "Neuraminidase inhibitors for preventing and treating influenza in healthy adults and children" (PDF). The Cochrane Database of Systematic Reviews. 4 (4): CD008965. doi:10.1002/14651858.CD008965.pub4. PMC 6464969. PMID 24718923.
- ^ Heneghan, CJ; Onakpoya, I; Thompson, M; Spencer, EA; Jones, M; Jefferson, T (Apr 9, 2014). "Zanamivir for influenza in adults and children: systematic review of clinical study reports and summary of regulatory comments". BMJ (Clinical Research Ed.). 348: g2547. doi:10.1136/bmj.g2547. PMC 3981976. PMID 24811412.
- ^ Heneghan, C. J.; Onakpoya, I.; Thompson, M.; Spencer, E. A.; Jones, M.; Jefferson, T. (9 April 2014). "Zanamivir for influenza in adults and children: systematic review of clinical study reports and summary of regulatory comments". BMJ. 348 (apr09 2): g2547. doi:10.1136/bmj.g2547. PMC 3981976. PMID 24811412.
- ^ Wang, K; Shun-Shin, M; Gill, P; Perera, R; Harnden, A (Apr 18, 2012). "Neuraminidase inhibitors for preventing and treating influenza in children (published trials only)". Cochrane Database of Systematic Reviews. 4 (4): CD002744. doi:10.1002/14651858.CD002744.pub4. PMC 6599832. PMID 22513907.
- ^ "2008-2009 Influenza Season Week 32 ending August 15, 2009". Flu Activity & Surveillance. Centers for Disease Control and Prevention (CDC). August 21, 2009.
- ^ Thorlund, Kristian; Awad, Tahany; Boivin, Guy; Thabane, Lehana (2011). "Systematic review of influenza resistance to the neuraminidase inhibitors". BMC Infectious Diseases. 11 (1): 134. doi:10.1186/1471-2334-11-134. PMC 3123567. PMID 21592407.
- ^ "Influenza Antiviral Medications: Summary for Clinicians". CDC. 2018-05-11. Retrieved 21 April 2014.
- ^ Hayden FG (December 2001). "Perspectives on antiviral use during pandemic influenza". Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 356 (1416): 1877–84. doi:10.1098/rstb.2001.1007. PMC 1088564. PMID 11779387.
- ^ "FDA Approves a Second Drug for the Prevention of Influenza A and B in Adults and Children". FDA press release.
- ^ "Safe and Appropriate Use of Influenza Drugs". Public Health Advisories (Drugs). U.S. Food and Drug Administration (FDA). April 30, 2009. Archived from the original on 2009-11-04. Retrieved 2009-11-11.
- ^ "Relenza (zanamivir) Inhalation Powder". Archived from the original on 2009-10-12.
- ^ Freund, B; Gravenstein, S; Elliott, M; Miller, I (Oct 1999). "Zanamivir: a review of clinical safety". Drug Safety. 21 (4): 267–81. doi:10.2165/00002018-199921040-00003. PMID 10514019.
- ^ a b Cyranoski D (September 2005). "Threat of pandemic brings flu drug back to life". Nature Medicine. 11 (9): 909. doi:10.1038/nm0905-909. PMID 16145557.
- ^ Moscona A (September 2005). "Neuraminidase inhibitors for influenza". The New England Journal of Medicine. 353 (13): 1363–73. doi:10.1056/NEJMra050740. PMID 16192481. S2CID 17162678.
- ^ Varghese, J. N.; Laver, W. G.; Colman, P. M. (1983). "Structure of the influenza virus glycoprotein antigen neuraminidase at 2.9 a resolution". Nature. 303 (5912): 35–40. doi:10.1038/303035a0. PMID 6843658. S2CID 4363648.
- ^ "Archived copy". Archived from the original on October 4, 2013. Retrieved October 2, 2013.
{{cite web}}: CS1 maint: 제목으로 아카이브된 복사(링크) - ^ "Archived copy". Archived from the original on October 5, 2013. Retrieved October 2, 2013.
{{cite web}}: CS1 maint: 제목으로 아카이브된 복사(링크) - ^ Meindl P, Bodo G, Palese P, Schulman J, Tuppy H (April 1974). "Inhibition of neuraminidase activity by derivatives of 2-deoxy-2,3-dehydro-N-acetylneuraminic acid". Virology. 58 (2): 457–63. doi:10.1016/0042-6822(74)90080-4. PMID 4362431.
- ^ Laver, Graeme (1 March 2007). "Flu drugs - pathway to discovery". Education in Chemistry. Vol. 44, no. 2. Royal Society of Chemistry. pp. 48–52. ISSN 0013-1350. Retrieved 19 June 2018.
- ^ von Itzstein, M; Wu, WY; Kok, GB; Pegg, MS; Dyason, JC; Jin, B; Van Phan, T; Smythe, ML; White, HF; Oliver, SW (3 June 1993). "Rational design of potent sialidase-based inhibitors of influenza virus replication". Nature. 363 (6428): 418–23. Bibcode:1993Natur.363..418V. doi:10.1038/363418a0. PMID 8502295. S2CID 4359333.
- ^ Cohen, D.; Carter, P. (3 June 2010). "WHO and the pandemic flu "conspiracies"". BMJ. 340 (jun03 4): c2912. doi:10.1136/bmj.c2912. PMID 20525679. S2CID 35959611.
- ^ Soundararajan V, Tharakaraman K, Raman R, Raguram S, Sasisekharan V, Sasisekharan R (June 2009). "Extrapolating from sequence--the 2009 H1N1 'swine' influenza virus". Nature Biotechnology. 27 (6): 510–3. doi:10.1038/nbt0609-510. PMID 19513050. S2CID 22710439.
- ^ Hirschler, Ben (2011-01-19). "GSK tests intravenous flu drug vs Roche's Tamiflu". Reuters.
외부 링크
- 인플루엔자 치료를 위한 Relenza 개발
- 의약품 정보: Zanamivir 흡입 Medline Plus 약물
- 리넨자: 미국 식품의약국(FDA)의 소비자 질의응답
- 레렌자 비오타 홀딩스
- Relenza 웹 사이트 글락소스미스클라인


