시멜라가트란
Ximelagatran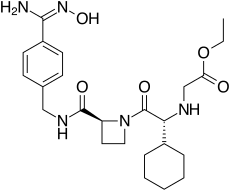 | |
| 임상자료 | |
|---|---|
| 상명 | 엑산타 |
| 임신 범주 |
|
| 경로: 행정 | 구강(테이블) |
| ATC 코드 | |
| 법적현황 | |
| 법적현황 |
|
| 약동학 데이터 | |
| 생체이용가능성 | 20% |
| 신진대사 | 멜라가트란으로 |
| 제거 반감기 | 3~5시간 |
| 배설 | 리날(80%) |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| IUPHAR/BPS | |
| 드러그뱅크 | |
| 켐스파이더 | |
| 유니 | |
| 케그 | |
| 켐벨 | |
| CompTox 대시보드 (EPA) | |
| 화학 및 물리적 데이터 | |
| 공식 | C24H35N5O5 |
| 어금질량 | 473.574 g·migration−1 (전환 후 429 g/mit) |
| 3D 모델(JSmol) | |
| |
| |
| | |
시멜라가트란(Exanta 또는 Exartarta, H 376/95)은 와파린 요법과 관련된 문제 식이요법, 약물 상호작용 및 모니터링 문제를 극복할 와파린의[1] 대체 물질로서 광범위하게 연구되어 온 항응고제다.2006년 제조사 아스트라제네카는 시험 중 간독성(간 손상)이 의심된다는 보고를 받고 판매승인 보류 신청을 철회하고, 의약품 승인 국가(독일, 포르투갈, 스웨덴, 핀란드, 노르웨이, 아이슬란드, 오스트리아, 덴마크, 프랑스, 스위스)에 유통을 중단한다고 발표했다.아르헨티나와 브라질).[2]
작용방법
직접 트롬빈 억제제인 시멜라가트란은 이 클래스의 첫 번째 멤버로 구두로 복용할 수 있었다.[3]그것은 오로지 트롬빈의 작용을 억제함으로써 작용한다.매일 두 번 구강으로 복용하고, 소장에 의해 빠르게 흡수된다.시멜라가트란은 프로드약으로 체내에서 활성제 멜라가트란으로 전환된다.이러한 변환은 수산화 및 탈수증을 통해 간 및 다른 많은 조직에서 일어난다(에틸 및 히드록실 그룹을 수소로 대체).
사용하다
시멜라가트란은 깊은 정맥 혈전증, 이차 정맥 혈전증 예방, 뇌졸중과 같은 심방세동 합병증 등 많은 치료 환경에서 와파린과 아스피린, 헤파린을 대체할 것으로 기대되었다.이러한 적응증에 대한 시멜라가트란의 효능은 비판상 심방세동을 제외하고 잘 입증되었다.[4][5][6]
제조사의 초기 보고에 따르면, 항응고제 성질을 감시하지 않고도 구강으로 복용할 수 있다는 것이 장점이었다.이는 국제표준화비율(INR)과 부분 트롬보플라스틴시간(PTT)의 모니터링을 각각 필요로 하는 와파린과 헤파린과는 차별화했을 것이다.초기에 인식된 단점은 급성 출혈이 발생할 경우 해독제가 없는 반면 와파린은 프로트롬빈 복합 농축액 및/또는 프로타민 황산염에 의해 대항할 수 있다.
부작용
시멜라가트란은 일반적으로 시험 개체군에서 잘 용인되었지만, 적은 비율(5~6%)이 간 효소 수치를 증가시켜 FDA가 2004년 초기 승인 신청을 거절하게 되었다.간독성의 보고에 따라 2006년에 추가 개발이 중단되었다.극한값 모델링을 이용한 임상 2상 연구 데이터의 후속 분석(극한값 이론 참조)에서는 임상 3상 연구에서 관찰된 간 효소 수준 상승이 예측될 수 있었음을 알 수 있었다. 만약 이것이 당시 알려져 있었다면, 향후 화합물 개발에 대한 결정에 영향을 미쳤을 수 있다.[7]
화학적으로는 다르지만 약리학적으로 유사한 물질인 AZD-0837은 비슷한 적응증을 위해 아즈트라제네카에 의해 개발되었다.[2]그것은 ARH0637이라 불리는 자유 및 섬유 결합 트롬빈에 대한 강력하고 경쟁적이며 되돌릴 수 있는 억제제의 약이다.[8]AZD-0837 개발은 중단되었다.확장 릴리즈된 AZD-0837 의약품의 장기적 안정성 한계로 인해 비 Valvular 심방세동 환자의 뇌졸중 예방에 대한 AHEL의 후속 연구는 2010년 2년 만에 조기 마감되었다.와파린에 대한 사망률도 수적으로 높았다.[9][10][11]AF에 대한 2단계 실험에서 평균 혈청 크레아티닌 농도는 치료 중단 후 기준치로 복귀한 AZD-0837로 치료된 환자의 기준치보다 약 10% 증가했다.[12]
참조
- ^ Hirsh J, O'Donnell M, Eikelboom JW (July 2007). "Beyond unfractionated heparin and warfarin: current and future advances". Circulation. 116 (5): 552–560. doi:10.1161/CIRCULATIONAHA.106.685974. PMID 17664384.
- ^ a b "AstraZeneca Decides to Withdraw Exanta" (Press release). AstraZeneca. February 14, 2006. Retrieved 2012-07-16.
- ^ Ho SJ, Brighton TA (2006). "Ximelagatran: direct thrombin inhibitor". Vasc Health Risk Manag. 2 (1): 49–58. doi:10.2147/vhrm.2006.2.1.49. PMC 1993972. PMID 17319469.
- ^ Eriksson, H; Wahlander K; Gustafsson D; Welin LT; Frison L; Schulman S; THRIVE Investigators (January 2003). "A randomized, controlled, dose-guiding study of the oral direct thrombin inhibitor ximelagatran compared with standard therapy for the treatment of acute deep vein thrombosis: THRIVE I". Journal of Thrombosis and Haemostasis. 1 (1): 41–47. doi:10.1046/j.1538-7836.2003.00034.x. PMID 12871538.
- ^ Francis CW, Berkowitz SD, Comp PC, Lieberman JR, Ginsberg JS, Paiement G, Peters GR, Roth AW, McElhattan J, Colwell CW Jr, EXULT A Study Group (October 2003). "Comparison of ximelagatran with warfarin for the prevention of venous thromboembolism after total knee replacement". New England Journal of Medicine. 349 (18): 1703–1712. doi:10.1056/NEJMoa035162. PMID 14585938.
- ^ Schulman, S; Wåhlander K; Lundström T; Clason SB; Eriksson H; THRIVE III investigators (October 2003). "Secondary prevention of venous thromboembolism with the oral direct thrombin inhibitor ximelagatran". New England Journal of Medicine. 349 (18): 1713–1721. doi:10.1056/NEJMoa030104. PMID 14585939.
- ^ Southworth, Harry (30 Jul 2014). "Predicting potential liver toxicity from phase 2 data: a case study with ximelagatran". Statistics in Medicine. 33 (17): 2914–2923. doi:10.1002/sim.6142. PMID 24623062.
- ^ Ahrens, Ingo; Karlheinz Peter; Gregory Y.H. Lip; Christoph Bode (2012). "Development and Clinical Applications of Novel Oral Anticoagulants. Part II. Drugs Under Clinical Investigation". Discovery Medicine. 13 (73): 445–450. PMID 22742650.
- ^ "AZD0837". Astrazenecaclinicaltrials.com. Retrieved 2012-10-16.
- ^ 아스트라제네카 장기요법 비타민-K 길항작용제 AZD0837과 비교한 비타민-K 길항작용제인 AstraZeneca 장기요법은 비발상 심방세동 환자에게 뇌졸중 예방과 뇌졸중 및 전신 색전증 사건에 대한 하나 이상의 위험요인으로 한다.5년 후속 연구 코드 D1250C0004221 2010년 1월 시험 D1250C00042 2013년 11월 10일 웨이백 기계에 보관
- ^ Eikelboom JW, Weitz JI (2010). "Update on Antithrombotic Therapy: New Anticoagulants". Circulation. 121 (13): 1523–32. doi:10.1161/CIRCULATIONAHA.109.853119. PMID 20368532.
- ^ Lip GY, Rasmussen LH, Olsson SB, Jensen EC, Persson AL, Eriksson U, Wåhlander KF (December 2009). "Oral direct thrombin inhibitor AZD0837 for the prevention of stroke and systemic embolism in patients with non-valvular atrial fibrillation: a randomized dose-guiding, safety, and tolerability study of four doses of AZD0837 vs. vitamin K antagonists". Eur. Heart J. 30 (23): 2897–907. doi:10.1093/eurheartj/ehp318. PMC 2785945. PMID 19690349.


