아픽사반
Apixaban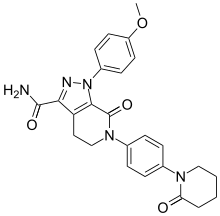 | |
 | |
| 임상자료 | |
|---|---|
| 상호 | 엘리퀴스 외 |
| 기타이름 | BMS-562247-01 |
| AHFS/Drugs.com | 모노그래프 |
| 메드라인 플러스 | a613032 |
| 라이센스 데이터 | |
| 임신 카테고리 |
|
| 경로 행정부. | 입으로 |
| ATC코드 | |
| 법적지위 | |
| 법적지위 | |
| 약동학적 자료 | |
| 생체이용률 | ~50% |
| 단백질결합 | ~87% |
| 신진대사 | CYP3A4, CYP3A5, CYP1A2 등 |
| 제거 반감기 | 9-14시간 |
| 배설 | 담관(75%), 신장(25%) |
| 식별자 | |
| |
| CAS 번호 | |
| 펍켐 CID | |
| IUPHAR/BPS | |
| 드럭뱅크 | |
| 켐스파이더 | |
| 유니아이 | |
| 케그 | |
| 쳄블 | |
| CompTox 대시보드 (EPA) | |
| ECHA 인포카드 | 100.167.332 |
| 화학 및 물리 데이터 | |
| 공식 | C25H25N5O4 |
| 어금니 질량 | 459.506g·mol−1 |
| 3D 모델(JSMO) | |
| |
| |
| (주로) | |
엘리퀴스(Eliquis)라는 브랜드명으로 판매되는 아픽사반(Apixaban)은 직접적인 억제 인자 Xa를 [5][6][7]통해 혈전을 치료하고 예방하며 비판막 심방세동 환자의 뇌졸중을 예방하는 데 사용되는 항응고제입니다.특히 고관절이나 무릎 치환술 후 혈전을 예방하기 위해 사용되며,[5][7] 이전 혈전의 병력이 있는 사람들에게는 사용됩니다.와파린의 대체제로 사용되며 혈액[5] 검사나 식이 [8]제한에 의한 모니터링이 필요하지 않습니다.그것은 [5]입으로 먹습니다.
일반적인 부작용으로는 출혈과 [5][6]메스꺼움이 있습니다.다른 부작용으로는 척추 주변 출혈과 알레르기 [5]반응이 있을 수 있습니다.임신 중이나 [1][6]모유 수유 중에는 사용하지 않는 것이 좋습니다.가벼운 신장 [6]문제가 있는 경우에는 사용이 비교적 안전한 것으로 보입니다.와파린에 비해 다른 [9]약과의 상호작용이 적습니다.직접인자 Xa [5]억제제입니다.
2007년 화이자와 브리스톨마이어스 스퀴브는 [10]항응고제로서 아픽사반의 개발을 시작했습니다.아픽사반은 2011년 5월 유럽연합에서, 2012년 [4][5][11]12월 미국에서 의료용으로 승인되었습니다.그것은 세계보건기구의 필수 [12]의약품 목록에 올라있습니다.2020년에는 1,300만 건 이상의 [13][14]처방을 받아 미국에서 48번째로 많이 처방된 약물이었습니다.미국에서는 아니지만 일반의약품으로 구입할 수 있습니다.[7][15]
의료용
아픽사반은 [3]다음을 가리키는 말입니다.
- 비판막 심방세동 환자의 뇌졸중과 색전증 위험을 낮추기 위해서입니다.
- 심부정맥혈전증(DVT) 예방.DVT는 무릎 또는 고관절 치환술 환자에게 폐색전증(PE)을 유발할 수 있습니다.
- DVT 및 PE 치료.
- 초기 치료 후 DVT와 PE가 재발할 위험을 줄이기 위해서입니다.
EU에서 아픽사반은 고관절 또는 무릎 대체 수술을 받은 성인의 정맥혈전색전증(VTE) 예방, 하나 이상의 위험인자를 가진 비판막 심방세동(NVAF) 성인의 뇌졸중 및 전신색전증 예방, 심부정맥혈전증(DVT) 및 폐질환 치료를 위해 표시됩니다.성인에서 원핵색전증(PE), [4]성인에서 재발하는 DVT와 PE의 예방을 위한 것.
심방세동
아픽사반(Apixaban)은 국립보건임상우수연구소(National Institute for Health and Clinical Excellence)에 의해 비판막 심방세동 환자의 뇌졸중 및 전신색전증 예방을 위해 권장되며, 이전 뇌졸중 또는 일시적 허혈성 발작, 75세 이상, 당뇨병 또는 증상성 [16]심부전 중 하나 이상의 위험 요인 중 하나입니다.
아픽사반과 다른 항응고제(다비가트란, 에독사반 및 리바록사반)는 심방세동 환자의 비출혈성 뇌졸중 예방에 와파린과 동일하게 효과적인 것으로 보이며 두개내 [17][18]출혈 위험 감소와 관련이 있습니다.
아픽사반은 신장 기능이 심각하게 저하된 사람들과 혈액투석을 하는 사람들에게 사용될 수 있지만 이러한 [5]그룹에서는 연구되지 않았습니다.
부작용
출혈
아픽사반은 심각하고 잠재적으로 치명적일 수 있는 출혈의 위험을 증가시킬 수 있습니다.혈액 응고에 영향을 미치는 다른 약물과 동시에 사용하면 이러한 위험이 더욱 커질 수 있습니다.여기에는 기타 항응고제, 헤파린, 아스피린, 항혈소판제, 선택적 세로토닌 재흡수 억제제, 세로토닌 노르에피네프린 재흡수 억제제, 비스테로이드성 소염제(NSAIDs)[3][19][20][21] 등의 약물이 포함됩니다.
Andexan et alfa는 통제되지 않고 생명을 위협하는 출혈 [22][23]사건을 가진 사람들의 아픽사반에 대한 미국 식품의약국(FDA) 승인된 해독제입니다.
척추천자
척추마취나 천자에 이어 항혈전제 치료를 받는 사람들은 장기적 혹은 영구적인 마비를 일으키는 혈종에 걸릴 위험이 높습니다.수술 후 경막외 카테터 또는 경막내 카테터를 사용하거나 [3]지혈에 영향을 미치는 의약품을 동시에 사용함으로써 이러한 위험이 증가할 수 있습니다.
작용기전
아픽사반(Apixaban)은 매우 선택적이고 경구적으로 생물학적으로 이용 가능하며, 자유 및 응고 결합 인자 Xa의 가역적 직접 억제제입니다.인자 Xa는 피브린 응고 [24]형성을 담당하는 응고 캐스케이드의 최종 효소인 프로트롬빈의 트롬빈으로의 전환을 촉매합니다.아픽사반은 혈소판 응집에 직접적인 영향은 없지만 인자 Xa를 억제함으로써 트롬빈에 [3]의해 유도되는 혈전 형성을 간접적으로 감소시킵니다.
역사
아픽사반은 2011년 [4]5월 유럽연합에서 의료용으로 승인되었습니다.
2011년 ARISTOTLE 임상시험 종료 후 브리스톨-마이어스 스퀴브(BMS)와 화이자가 공동으로 미국 식품의약국(FDA)에 아픽사반 승인을 위한 신약신청서(NDA)를 제출하였습니다.아픽사반은 2012년 [11][26]12월 28일 심방세동 환자의 뇌졸중 예방을 위한 승인을 받았습니다.2014년 3월 13일, 최근 무릎 또는 고관절 [27][28]치환술을 받은 사람들의 심부정맥혈전증 및 폐색전증 예방 추가 적응증에 대해 승인되었습니다.2014년 8월 21일 FDA는 반복적인 심부정맥혈전증 및 폐색전증의 [27][29]치료에 대한 추가 적응증에 대해 아픽사반을 승인했습니다.개발되는 동안 이 약물은 BMS-562247-01로 [30]알려져 있었습니다.2019년 말까지 BMS의 제품 매출은 분기별 [31]매출의 30%를 차지했습니다.
사회와 문화
경제학
2019년 12월, 미국 FDA는 마일란과 마이크로 [32][31][7]랩스가 공동으로 생산한 아픽사반의 일반 버전을 승인했습니다.BMS와 화이자는 제네릭이 만들어지는 것을 차단하기 위해 발 빠르게 노력했고, 앞서 25개 [33][34]업체를 상대로 특허 사건을 해결한 끝에 2020년 8월 시그마팜, 선샤인레이크, 유니켐 등을 상대로 특허 침해 소송에서 승소했습니다.2021년 9월 연방순회법원은 [35]판결을 확정했습니다.결과적으로 아픽사반 제네릭은 적어도 2026년까지는 미국에서 구할 수 없을 가능성이 높지만, 가능하면 [15]2031년이 될 것입니다.
2022년 7월, 캐나다 제네릭 의약품 회사인 Apotex Inc.는 아픽사반의 시판을 [36][37]승인 받았습니다.
아픽사반은 인플레이션 감소법에 따라 미국에서 가격 협상을 위해 제안된 10가지 약물 중 하나입니다.브리스톨 마이어스 스퀴브(Bristol Myers Squibb)에 따르면 엘리퀴스의 환자 1인당 월평균 급여는 미화 [38]55달러입니다.
참고문헌
- ^ a b "Apixaban (Eliquis) Use During Pregnancy". Drugs.com. 21 June 2019. Retrieved 13 August 2020.
- ^ "Eliquis 5 mg film-coated tablets - Summary of Product Characteristics (SmPC)". (emc). 3 May 2022. Retrieved 8 October 2022.
- ^ a b c d e "Eliquis- apixaban tablet, film coated Eliquis 30-day starter pack- apixaban kit". DailyMed. 26 November 2019. Retrieved 22 April 2020.
- ^ a b c d 이 출처인 © European Medicine Agency에서 텍스트를 복사했습니다.출처가 확인된 경우에는 복제가 승인됩니다.
- ^ a b c d e f g h i "Apixaban Monograph for Professionals". Drugs.com. American Society of Health-System Pharmacists. Retrieved 27 March 2019.
- ^ a b c d British national formulary: BNF 76 (76 ed.). Pharmaceutical Press. 2018. pp. 124–125. ISBN 9780857113382.
- ^ a b c d "FDA approves first generics of Eliquis". U.S. Food and Drug Administration (FDA). 23 December 2019. Archived from the original on 23 December 2019. Retrieved 23 December 2019.
 이 기사는 공용 도메인에 있는 이 소스의 텍스트를 통합합니다.
이 기사는 공용 도메인에 있는 이 소스의 텍스트를 통합합니다. - ^ Hall H (September–October 2020). "How a Drug Is Born". Skeptical Inquirer. Amherst, New York: Center for Inquiry.
- ^ Kiser K (2017). Oral Anticoagulation Therapy: Cases and Clinical Correlation. Springer. p. 11. ISBN 9783319546438.
- ^ "Bristol-Myers Squibb and Pfizer Announce Worldwide Collaboration to Develop and Commercialize Anticoagulant and Metabolic Compounds". Pfizer (Press release). Archived from the original on 10 September 2015. Retrieved 25 December 2021.
- ^ a b c "Drug Approval Package: Eliquis (apixaban) NDA #202155". U.S. Food and Drug Administration (FDA). 13 February 2013. Retrieved 23 December 2019.
- ^ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. hdl:10665/345533. WHO/MHP/HPS/EML/2021.02.
- ^ "The Top 300 of 2020". ClinCalc. Retrieved 7 October 2022.
- ^ "Apixaban - Drug Usage Statistics". ClinCalc. Retrieved 7 October 2022.
- ^ a b "With Court Win, BMS and Pfizer Stave Off Generic Challengers to Eliquis – For Now". BioSpace. Retrieved 29 November 2021.
- ^ "Apixaban for preventing stroke and systemic embolism in people with nonvalvular atrial fibrillation" (PDF). National Institute for Health and Care Excellence. January 2013. Retrieved 26 February 2016.
- ^ Gómez-Outes A, Terleira-Fernández AI, Calvo-Rojas G, Suárez-Gea ML, Vargas-Castrillón E (2013). "Dabigatran, Rivaroxaban, or Apixaban versus Warfarin in Patients with Nonvalvular Atrial Fibrillation: A Systematic Review and Meta-Analysis of Subgroups". Thrombosis. 2013: 640723. doi:10.1155/2013/640723. PMC 3885278. PMID 24455237.
- ^ Lowenstern A, Al-Khatib SM, Sharan L, Chatterjee R, Allen LaPointe NM, Shah B, et al. (December 2018). "Interventions for Preventing Thromboembolic Events in Patients With Atrial Fibrillation: A Systematic Review". Annals of Internal Medicine. 169 (11): 774–787. doi:10.7326/M18-1523. PMC 6825839. PMID 30383133.
{{cite journal}}: CS1 maint: 재정의된 설정(링크) - ^ "Atrial fibrillation and new oral anticoagulant drugs". U.S. Food and Drug Administration (FDA). 2 December 2015. Retrieved 22 April 2020.
- ^ "Atrial fibrillation, oral anticoagulant drugs, and their reversal agents". U.S. Food and Drug Administration. 2 December 2015. Retrieved 22 April 2020.
- ^ "No change is needed in use of direct oral anticoagulants following EMA-funded study". European Medicines Agency (EMA). 27 March 2020. Retrieved 22 April 2020.
- ^ "Andexxa- andexanet alfa injection, powder, lyophilized, for solution". DailyMed. 8 January 2019. Retrieved 23 December 2019.
- ^ "Andexxa (coagulation factor Xa (recombinant), inactivated-zhzo)". U.S. Food and Drug Administration (FDA). 31 December 2018. Retrieved 22 April 2020.
- ^ Frost C, Wang J, Nepal S, Schuster A, Barrett YC, Mosqueda-Garcia R, et al. (February 2013). "Apixaban, an oral, direct factor Xa inhibitor: single dose safety, pharmacokinetics, pharmacodynamics and food effect in healthy subjects". British Journal of Clinical Pharmacology. 75 (2): 476–487. doi:10.1111/j.1365-2125.2012.04369.x. PMC 3558798. PMID 22759198.
{{cite journal}}: CS1 maint: 재정의된 설정(링크) - ^ Granger CB, Alexander JH, McMurray JJ, Lopes RD, Hylek EM, Hanna M, et al. (September 2011). "Apixaban versus warfarin in patients with atrial fibrillation". The New England Journal of Medicine. 365 (11): 981–992. doi:10.1056/NEJMoa1107039. PMID 21870978. S2CID 43262809.
{{cite journal}}: CS1 maint: 재정의된 설정(링크) - ^ Cada DJ, Levien TL, Baker DE (June 2013). "Apixaban". Hospital Pharmacy. 48 (6): 494–509. doi:10.1310/hpj4806-494. PMC 3839491. PMID 24421512.
- ^ a b "FDA-Approved Drugs: Eliquis (apixaban)". U.S. Food and Drug Administration (FDA). Retrieved 23 December 2019.
- ^ Neale T (14 March 2014). "FDA OKs Apixaban for DVT Prevention". MedPage Today. Retrieved 17 September 2015.
- ^ "U.S. FDA Approves Eliquis (apixaban) for the Treatment of Deep Vein Thrombosis (DVT) and Pulmonary Embolism (PE), and for the Reduction in the Risk of Recurrent DVT and PE Following Initial Therapy" (Press release). Pfizer. 21 August 2014. Retrieved 26 February 2016.
- ^ "Apixaban". PubChem, US National Library of Medicine. 27 August 2022. Retrieved 2 September 2022.
- ^ a b "FIRST: Mylan, Micro Labs get USFDA nod for generic version of blood thinner Eliquis". Business Medical Dialogues. New Delhi, India: Minerva Medical Treatment. 24 December 2019. Retrieved 24 December 2019.
- ^ "2019 First Generic Drugs Approvals". U.S. Food and Drug Administration (FDA). 5 August 2020. Archived from the original on 30 June 2023. Retrieved 30 June 2023.
- ^ "Bristol-Myers Squibb Co. v. Aurobindo Pharma USA Inc". JD Supra. Retrieved 30 November 2021.
- ^ "Bristol Myers, Pfizer fend off a key challenge to their top-selling heart drug". BioPharma Dive. Retrieved 30 November 2021.
- ^ "Federal Circuit Crystallizes BMS' Apixaban District Court Win". The National Law Review. Retrieved 30 November 2021.
- ^ Levy S (1 August 2022). "Apotex offers generic Eliquis in Canada". Drugstore News. Retrieved 2 September 2022.
- ^ "First Generic Alternative to Eliquis Now Available in Canada". Apotex (Press release). 20 July 2022. Retrieved 29 June 2023.
- ^ Kansteiner F (29 August 2023). "Drugs from J&J, Merck, Novartis, BMS and more set for first round of Medicare price negotiations: CMS". Retrieved 31 August 2023.


