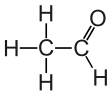
아세트알데히드
Acetaldehyde
| | |||
| | |||
| 이름 | |||
|---|---|---|---|
| 우선 IUPAC 이름 아세트알데히드[3] | |||
| 시스템 IUPAC 이름 에단알[3] | |||
| 기타 이름 | |||
| 식별자 | |||
3D 모델(JSmol) | |||
| 체비 | |||
| 첸블 | |||
| 켐스파이더 | |||
| ECHA 정보 카드 | 100.000.761 | ||
| EC 번호 |
| ||
| 케그 | |||
PubChem CID | |||
| RTECS 번호 |
| ||
| 유니 | |||
CompTox 대시보드 (EPA ) | |||
| |||
| |||
| 특성. | |||
| C2H4O | |||
| 몰 질량 | 44.053 g/120−1 | ||
| 외모 | 무색 가스 또는 액체 | ||
| 냄새 | Ethereal | ||
| 밀도 | 0.784g/cm−3(20°[4]C) 0.7904~0.7928g·cm−3(10°[4]C) | ||
| 녹는점 | -123.37°C(-190.07°F, 149.78K) | ||
| 비등점 | 20.2°C(68.4°F, 293.3K) | ||
| 혼선 | |||
| 용해성 | 에탄올, 에테르, 벤젠, 톨루엔, 자일렌, 테레빈, 아세톤과 혼합 가능 클로로포름에 약간 용해되는 | ||
| 로그 P | -0.34 | ||
| 증기압 | 740mmHg(20°C)[5] | ||
| 산도(pKa) | 13.57 (25 °C, H2O)[6] | ||
자화율(δ) | - 5.5153−6 cm3/g | ||
굴절률(nD) | 1.3316 | ||
| 점성 | 20°C에서 0.21mPa-s(9.5°[7]C에서 0.253mPa-s) | ||
| 구조. | |||
| C에서의1 삼각 평면(sp2) C에서의2 사면체(sp3) | |||
| 2.7 D | |||
| 열화학[8] | |||
열용량 (C) | 89 J·mol−1·K−1 | ||
표준 어금니 엔트로피 (S | 160.2 J·mol−1·K−1 | ||
표준 엔탈피/ 형성 (δHf⦵298) | - 192.2kJ/mol−1 | ||
깁스 자유 에너지 ( (Gf)) | - 127.6 kJ/mol−1 | ||
| 위험 요소 | |||
| 산업안전보건(OHS/OSH): | |||
주요 위험 요소 | 잠재적 직업성 발암[10] 물질 | ||
| GHS 라벨링: | |||
   [9] [9] | |||
| H224, H319, H335, H351[9] | |||
| P210, P261, P281, P305+P351+P338[9] | |||
| NFPA 704(파이어 다이아몬드) | |||
| 플래시 포인트 | -39.00°C, -38.20°F, 234.15K | ||
| 175.00°C, 347.00°F, 448.15K[5] | |||
| 폭발 한계 | 4.0–60% | ||
| 치사량 또는 농도(LD, LC): | |||
LD50(중간선량) | 1930 mg/kg (쥐, 경구) | ||
LC50(중간 농도) | 13,000ppm (랫), 17,000ppm(표준), 20,000ppm (랫)[10] | ||
| NIOSH(미국 건강 노출 제한): | |||
PEL(허용) | 200ppm(360mg/m3)[5] | ||
IDLH(즉시 위험) | 2,000[5][10] 장 / 분 | ||
| 안전 데이터 시트(SDS) | HMDB | ||
| 관련 화합물 | |||
관련 알데히드 | 포름알데히드 프로피온알데히드 | ||
관련 화합물 | 산화 에틸렌 | ||
| 보충 데이터 페이지 | |||
| 아세트알데히드(데이터페이지) | |||
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |||
아세트알데히드(IUPAC 계통명 에탄알데히드)는 화학식3 CHCHO를 가진 유기 화합물이며, 화학자들에 의해 Me = 메틸(Me = methyl)로 약칭되기도 한다.그것은 실온 근처에서 끓는 무색의 액체 또는 기체이다.그것은 가장 중요한 알데하이드 중 하나이며, 자연에서 널리 발생하며 산업계에서 대규모로 생산된다.아세트알데히드는 커피, 빵, [11]익은 과일에 자연적으로 발생하며 식물에서 생산된다.또한 간 효소 알코올 탈수소효소에 의한 에탄올의 부분 산화에 의해 생성되며 알코올 섭취 후 숙취의 원인이 됩니다.노출 경로에는 음료와 연기뿐만 아니라 공기, 물,[12] 육상 또는 지하수가 포함된다.디술피람의 섭취는 아세트알데히드의 대사를 담당하는 효소인 아세트알데히드탈수소효소를 억제하여 체내에 축적시킨다.
국제암연구기구(IARC)는 아세트알데히드를 1그룹 발암물질로 [13]분류했다.아세트알데히드는 "100만분의 1 이상의 발암 위험을 가진 가장 빈번하게 발견되는 공기 독소 중 하나"[14]
역사
아세트알데히드는 스웨덴의 약사/화학자인 칼 빌헬름 셸레(1774)[15]에 의해 처음 관찰되었고, 그 후 프랑스 화학자 앙투안 프랑수아, 푸르크로이와 루이 니콜라 보클랭(1800)[16]과 독일 화학자 요한 볼프강 도베라이너(1821, 1822, 1832,[17] 1832)에 의해 조사되었다.1835년, 리빅은 그것을 "알데히드"[20]라고 이름 붙였고, 나중에 그 이름은 "아세트알데히드"[21]로 바뀌었다.
생산.
2003년의 세계 생산량은 약 100만 톤이었다.1962년 이전에는 에탄올과 아세틸렌이 아세트알데히드의 주요 공급원이었다.그 이후 에틸렌이 주요 [22]공급원료이다.
주요 생산 방법은 웨커 공정에 의한 에틸렌의 산화이며, 이는 균질한 팔라듐/구리 시스템을 사용하여 에틸렌의 산화를 수반합니다.
- 22 CH = CH2 + O2 → 2 CHCHO3
1970년대에 Waker-Hoechst 직접 산화 공정의 세계 용량은 연간 200만 톤을 초과했습니다.
발열 반응에서 에탄올의 부분 산화에 의해 소량을 제조할 수 있다.이 프로세스는 일반적으로 약 500–650°[22]C의 은촉매를 통해 수행됩니다.
- CHHOH32 +1⁄22 O → CHCHO3 + HO2
이 방법은 아세트알데히드를 공업적으로 제조하기 위한 가장 오래된 방법 중 하나이다.
기타 방법
아세틸렌 수화
웨커 공정과 값싼 에틸렌이 나오기 전에는 아세틸렌의 수화 [23]작용으로 아세트알데히드가 생성되었습니다.이 반응은 수은에 의해 촉매된다.II) 소금:
- CH22 + Hg2+ + HO2 → CHCHO3 + Hg
이 메커니즘은 아세트알데히드와 호변이하는 비닐알코올의 중간을 포함합니다.반응은 90~95 °C에서 진행되며 생성된 아세트알데히드는 물과 수은에서 분리되어 25~30 °C로 냉각된다.습식 산화 과정에서 황산철(III)은 수은을 다시 수은으로 산화시키기 위해 사용된다.II) 소금그 결과 발생하는 철(II) 황산염은 질산과 [22]함께 별도의 반응기에서 산화된다.
에탄올 탈수소
전통적으로 아세트알데히드는 에탄올의 부분 탈수소 작용으로 생성되었습니다.
- CHCHOH32 → CHCHO3 + H2
이 흡열 과정에서는 에탄올 증기가 구리 기반 촉매 위로 260–290°C로 통과됩니다.그 과정은 한때 수소 공동 [22]생산물의 가치 때문에 매력적이었지만, 현대에는 경제적으로 가능하지 않다.
메탄올의 하이드로포르밀화
코발트, 니켈 또는 철염과 같은 촉매에 의한 메탄올의 하이드로포름도 아세트알데히드를 생성하지만, 이 과정은 산업적으로 중요하지 않습니다.마찬가지로 아세트알데히드는 약간의 선택성을 [22]가진 합성 가스에서 발생한다.
반응
아세트알데히드의 비닐알코올 호변이성
다른 많은 카르보닐 화합물과 마찬가지로 아세트알데히드는 호변이성으로 에놀(비닐알코올, IUPAC 이름: 에테놀):
- CHCH3=O ch2 CH=CHOH h298,g H = +42.7 kJ/mol
상온에서 평형상수는 6×10이므로−7 아세트알데히드 시료 중 에놀 형태의 상대량은 매우 [24]작다.상온에서 아세트알데히드(CHCH3=O)는 비닐알코올(CH2=CHOH)보다 42.7kJ/mol [25]더 안정적이며, 전체적으로 케토에놀 호변이 느리지만 산에 의해 촉매된다.
광유기성 케토에놀 호변이성은 대기 또는 성층권 조건 하에서 가능하다.비닐 알코올은 대기 [26][27]중 카르본산의 전조로 생각되기 때문에 이러한 광호변이성체는 지구의 대기와 관련이 있습니다.
응축 반응
아세트알데히드는 유기합성에서 [28]흔히 볼 수 있는 친전자성 물질이다.축합반응에서 아세트알데히드는 프로키랄이다.주로 알돌 및 관련 응축 [29]반응에서 "CHCH3+(OH)" 신톤의 공급원으로 사용됩니다.그리냐드 시약과 유기석소 화합물은 MeCHO와 반응하여 히드록시에틸 [30]유도체를 생성한다.보다 극적인 축합 반응 중 하나로, 세 개의 포름알데히드가 MeCHO에 첨가되어 펜타에리트리톨, C(CHOH2)4[31]를 생성한다.
스트레이커 반응에서 아세트알데히드는 시안화물 및 암모니아와 응축되어 가수분해 후 아미노산 알라닌을 [32]얻는다.아세트알데히드는 아민과 응축하여 이미인을 생성한다.예를 들어 시클로헥실아민과 결합하여 N-에틸리덴시클로헥실아민을 생성한다.이러한 이미인은 알돌 [33]응축과 같은 후속 반응을 유도하는 데 사용될 수 있습니다.
그것은 또한 복소환 화합물의 합성에 있어서 구성 요소이다.예를 들어 암모니아 처리 시 5-에틸-2-메틸피리딘("알데히드-콜리딘")[34]으로 변환된다.
고분자 형태
아세트알데히드 3분자가 응축되어 C-O 단결합을 포함한 고리형 삼량체 '파라알데히드'가 형성된다.마찬가지로 아세트알데히드 4분자의 축합은 고리형 분자 금속알데히드를 생성한다.파라알데히드는 황산촉매를 사용하여 좋은 수율로 생산될 수 있습니다.금속알데히드는 수율이 몇 퍼센트이고 냉각을 통해 얻을 수 있으며, 종종 촉매로 HSO가24 아닌 HBr을 사용합니다.산촉매의 존재 하에서 -40 °C에서 폴리아세트알데히드가 [22]생성된다.패럴알데히드는 2개의 입체체와 4개의 금속알데히드가 있다.
독일 화학자 발렌틴 헤르만 바이덴부쉬(1821–1893)는 1848년 아세트알데히드를 산(황산 또는 질산)으로 처리한 후 0°C로 냉각시켜 파라알데히드를 합성했습니다.그는 같은 산의 미량인 파라알데히드를 가열하면 반응이 반대로 진행되어 아세트알데히드를 [35]재생성한다는 것을 알아냈다.
아세탈 유도체

아세트알데히드는 탈수를 선호하는 조건에서 에탄올과 반응하여 안정적인 아세탈을 형성합니다.CHCH(OCHCH23)2라는 제품은3 공식적으로 1,1-디에톡시에탄으로 불리지만 일반적으로 "아세탈"[36]로 불린다.이는 "아세탈"이 이 특정 화합물을 지칭하는 것이 아니라 관능기 RCH(OR')2 또는 RR'C(OR)2와 함께 화합물을 설명하는 데 더 일반적으로 사용되기 때문에 혼동을 일으킬 수 있다. 사실, 1,1-디에톡시에탄은 아세트알데히드의 디에틸 아세트라고도 한다.
비닐포스폰산 전구체
아세트알데히드는 접착제와 이온 전도막을 만드는 데 사용되는 비닐포스폰산의 전구체이다.합성 시퀀스는 [37]삼염화인과의 반응에서 시작됩니다.
- PCl3 + CHCHO3 → CHCH3(O−) PCL3+
- CHCH3(O−) PCL3+ + CHCOH 232 → CHCH3(Cl) PO(OH)2 + CHCOCl3 2
- CHCH3(Cl)PO(OH)2 → CH2=CHPO(OH)2 + HCl
생화학
간에서 알코올탈수소효소는 에탄올을 아세트알데히드로 산화시킨 후 아세트알데히드탈수소효소에 의해 무해한 아세트산으로 산화한다.이 두 산화 반응은 NAD를 [38]NADH로 환원하는 것과+ 결합된다.뇌에서 카탈라아제 효소는 주로 에탄올을 아세트알데히드로 산화시키는 역할을 하며 알코올 탈수소효소는 작은 [38]역할을 한다.박테리아, 식물 및 효모에서 알코올 발효의 마지막 단계는 피루브산이 피루브산 탈탄산화효소에 의해 아세트알데히드와 이산화탄소로 전환되고 이어서 아세트알데히드가 에탄올로 전환됩니다.후자의 반응은 알코올 탈수소효소에 의해 다시 촉매되어 현재는 반대 방향으로 작용한다.
사용하다
전통적으로 아세트알데히드는 아세트산의 전구체로 주로 사용되었다.몬산토 및 카티바 공정에 의해 메탄올에서 아세트산이 보다 효율적으로 생성되기 때문에 이 응용은 감소했습니다.아세트알데히드는 피리딘 유도체, 펜타에리톨, 크로톤알데히드의 중요한 전구체이다.요소와 아세트알데히드가 결합되어 유용한 수지가 됩니다.아세트산 무수물은 아세트알데히드와 반응하여 아세트산비닐의 전구물질인 에틸리덴 디아세테이트를 [22]생성한다.
아세트알데히드의 세계 시장이 감소하고 있다.수요는 가소제 알코올의 생산 변화에 영향을 받았는데, 이는 n-부티랄알데히드가 아세트알데히드에서 생성되는 빈도가 낮기 때문에 프로필렌의 하이드로포름에 의해 생성되기 때문이다.마찬가지로 아세트알데히드에서 생성된 아세트산은 주로 저비용 메탄올 카르보닐화 과정에 [39]의해 만들어진다.수요에 대한 영향은 가격 상승과 시장 침체로 이어졌다.
2003년[22] 아세트알데히드 소비량(10t3)
(* 기타 -글리옥살/글리옥살산, 크로톤알데히드, 젖산, n-부탄올, 2-에틸헥사놀에 포함)
| 제품. | 미국 | 멕시코 | 서유럽 | 일본. | 총 |
|---|---|---|---|---|---|
| 아세트산/무수 아세트산 | - | 11 | 89 | 47 | 147 |
| 아세테이트 에스테르 | 35 | 8 | 54 | 224 | 321 |
| 펜타에리트리톨 | 26 | – | 43 | 11 | 80 |
| 피리딘 및 피리딘 염기 | 73 | – | 10 | * | 83 |
| 과초산 | 23 | – | – | * | 23 |
| 1,3-부틸렌글리콜 | 14 | – | – | * | 14 |
| 다른이들 | 5 | 3 | 10 | 80 | 98 |
| 총 | 176 | 22 | 206 | 362 | 766 |
중국은 2012년 전 세계 소비량의 거의 절반을 차지하는 세계 최대 아세트알데히드 소비국이다.주요 용도는 아세트산의 생산이었다.피리딘과 펜타에리톨과 같은 다른 용도는 아세트산보다 더 빨리 증가할 것으로 예상되지만, 아세트산의 감소를 상쇄할 만큼 부피가 크지 않다.이에 따라 2018년까지 중국의 전체 아세트알데히드 소비량은 연간 1.6%로 소폭 증가할 수 있다.서유럽은 2012년 세계 소비량의 20%를 차지하는 아세트알데히드의 세계 2위 소비국이다.중국과 마찬가지로 서유럽 아세트알데히드 시장도 2012~2018년에는 연 1%로 소폭 증가할 것으로 예상된다.그러나 일본은 부타디엔을 상업적으로 사용하기 때문에 향후 5년 이내에 아세트알데히드의 잠재적 소비국으로 부상할 가능성이 있다.부타디엔의 공급은 일본과 다른 아시아 지역에서 불안정했다.이는 2013년 [40]현재 플랫 마켓에 매우 필요한 부양책을 제공할 것입니다.
안전.
노출 한계
임계값 한계값은 25ppm(STEL/천장값)이고 MAK(최대 작업 공간 집중도)는 50ppm입니다.아세트알데히드 50ppm에서는 코 점막에 자극이나 국소 조직 손상이 관찰되지 않습니다.아세트알데히드는 유기체에 흡수되면 간에서 아세트산으로 빠르게 대사된다.일부만 변경되지 않고 내뱉습니다.정맥주사 후 혈액 내 반감기는 약 90초입니다.[22]
위험들
독성
많은 심각한 급성 중독 사례가 기록되었다.[22]아세트알데히드는 [12][41]인체에서 자연적으로 분해된다.
짜증
아세트알데히드는 피부, 눈, 점막, 목, 호흡기의 자극제이다.이는 1000ppm의 낮은 농도에서 발생합니다.이 화합물에 노출되는 증상에는 메스꺼움, 구토, 두통이 포함됩니다.이러한 증상은 즉시 발생하지 않을 수 있습니다.공기 중 아세트알데히드의 검출 임계값은 0.07~[22]0.25ppm이다.이 농도에서는 아세트알데히드의 과일 냄새가 확연히 난다.결막 자극은 25, 50ppm 농도에 15분간 노출된 후 관찰되었지만, 200ppm 아세트알데히드에 15분간 노출된 후 일시적인 결막염과 호흡기의 자극이 보고되었다.
발암성
아세트알데히드는 사람에게 [42][43]발암성이 있다.1988년 국제암연구기구는 "실험동물에서 [44]아세트알데히드(에탄올의 주요 대사물)의 발암성에 대한 충분한 증거가 있다"고 밝혔다.2009년 10월 국제암연구기구는 알코올 음료에 포함되어 내생적으로 발생하는 아세트알데히드가 I급 인간 [45]발암물질임을 나타내는 아세트알데히드의 분류를 갱신했다.또 아세트알데히드는 DNA에 손상을[46] 주고 [47]단백질과 결합해 근육 발달에 이상을 일으킨다.
DNA 가교
아세트알데히드는 DNA 손상의 한 형태인 DNA 간 교합을 유도한다.이것들은 두 개의 복제 결합 DNA 복구 [48]경로 중 하나를 통해 복구될 수 있다.첫 번째는 FA 경로라고 불리는데, 이는 판코니의 빈혈 환자에게 결함이 있는 유전자 제품을 사용하기 때문이다.이 복구 경로는 돌연변이 빈도를 증가시키고 돌연변이 [48]스펙트럼을 변화시킨다.두 번째 복구 경로는 복제 포크 수렴, 아세트알데히드 가교 파괴, Y족 DNA 중합효소에 의한 트랜스리온 합성 및 상동 [48]재조합을 필요로 한다.
악화 요인
알츠하이머병
아세트알데히드를 아세트산으로 바꾸는 효소에 유전적 결함이 있는 사람들은 알츠하이머병에 걸릴 위험이 더 클 수 있다."이러한 결과는 ALDH2 결핍이 LOAD[말기 알츠하이머병]의 위험인자임을 나타냅니다."[49]
유전적 조건
알코올 탈수소효소를 코드하는 유전자의 유전자 변형을 통해 정상보다 더 많은 아세트알데히드에 노출된 818명을 대상으로 한 연구에서 알코올 탈수소효소를 코드하는 유전자는 상부 소화관과 [50]간암에 걸릴 위험이 더 높은 것으로 나타났다.
디술피람
디술피람(안타부스)은 아세트알데히드탈수소효소를 억제하는데, 아세트산은 아세트산으로 산화시키는 효소이다.아세트알데히드탈수소효소가 아세트산을 형성하기 전에는 에탄올의 대사가 아세트알데히드를 형성하지만, 이 효소가 억제되면 아세트알데히드가 축적된다.디술피람을 복용하면서 에탄올을 섭취하면 에탄올의 숙취 효과가 더욱 빠르고 강렬하게 느껴진다.이와 같이 디술피람은 알코올 중독자들이 술을 마시지 않기를 바라는 것을 억제하는 수단으로 사용되기도 한다.
노출원
실내 공기
아세트알데히드는 작업장, 실내 및 주변 환경에서 잠재적 오염 물질입니다.게다가, 대부분의 인간은 시간의 90% 이상을 실내 환경에서 보내며, 노출과 인간 [51]건강에 대한 위험을 증가시킨다.
프랑스의 한 연구에서 16가구에서 측정된 아세탈데히드의 평균 실내 농도는 외부 아세트알데히드 농도보다 약 7배 높았다.거실의 평균은 18.1±17.5μgm−3, 침실은 18.2±16.9μgm인−3 반면, 실외기 평균 농도는 2.3±2.6μgm였다−3.[citation needed]
벤젠, 포름알데히드, 아세트알데히드, 톨루엔, 자일렌 등 휘발성 유기화합물(VOC)은 건강에 미치는 영향에 대해 우선 오염물질로 간주해야 한다는 결론이 나왔다.리노베이션되거나 완전히 새로 지어진 건물에서는 종종 VOCs 농도 수준이 몇 배 더 높다는 것이 지적되었다.가정에서 아세탈데히드의 주요 공급원은 건축 자재, 라미네이트, PVC 바닥재, 니스를 바른 목재 바닥재, 니스를 바른 코르크/파인 바닥재입니다.플라스틱, 유성 및 수성 페인트, 복합 목재 천장, 파티클 보드, 합판, 처리된 소나무 목재 및 라미네이트 칩 보드 [52]가구에서도 볼 수 있습니다.
야외 공기
아세트알데히드는 다양한 산업에서 널리 사용되고 있으며, 생산, 사용, 운송 및 보관 과정에서 폐수 또는 공기로 방출될 수 있습니다.아세트알데히드의 공급원에는 화석연료, 목재 또는 쓰레기를 태우는 정지 내연기관 및 발전소, 석유 및 가스 추출, 정유소, 시멘트 가마, 목재 및 목공소,[53] 제지 공장에서 발생하는 연료 연소 배출이 포함된다.아세트알데히드는 자동차와 디젤 [54]배기가스에도 존재한다.그 결과 아세트알데히드는 "발암 위험이 백만 [14]분의 1 이상인 가장 빈번하게 발견되는 공기 독성 물질 중 하나"이다.
담배 연기
셀룰로오스를 포함한 천연 담배 다당류는 아세트알데히드를 담배 [55][56]연기의 중요한 성분으로 만드는 주요 전구체인 것으로 나타났다.그것은 설치류 [57][58]중독 연구에서 니코틴과 상승 효과가 있는 것으로 입증되었다.아세트알데히드는 또한 담배연기에 가장 많이 함유된 발암물질이다. 담배를 피우는 동안 침에 녹는다.
대마초 연기
아세트알데히드는 대마초 연기에서 발견되었다.이 연구결과는 아세트알데히드가 실험실 [59]환경에서 DNA 손상을 일으킨다는 것을 증명하는 새로운 화학기술을 사용함으로써 나타났다.
알코올 소비량
많은 미생물들이 에탄올로부터 아세트알데히드를 생산하지만, 그것들은 아세트알데히드를 제거하는 능력이 낮아서 침, 위산, 장 내용물에 아세트알데히드가 축적될 수 있다.발효 식품과 많은 알코올 음료 또한 상당한 양의 아세트알데히드를 포함할 수 있습니다.아세트알데히드는 에탄올, 담배연기, 식이요법의 점막 또는 미생물 산화에서 유래한 것으로,[60] 인간의 상부 소화관에 축적되는 발암물질로 작용한다.유럽위원회 소비자안전과학위원회(SCCS)의 아세트알데히드에 대한 의견(2012)에 따르면 화장품의 특수 위험 한도는 5mg/l이며 아세트알데히드는 구강세척용 제품에 [61]사용해서는 안 된다.
플라스틱
아세트알데히드는 폴리에틸렌 테레프탈레이트(PETe)의 광산화에 의해 2형 노르리쉬 반응을 통해 [62]제조할 수 있다.
이 과정에서 생성되는 아세트알데히드는 약 20-40ppb의 매우 낮은 맛/냄새 역치를 가지며 생수에서 [63]악취의 원인이 될 수 있습니다.일반 소비자가 아세트알데히드를 검출할 수 있는 수준은 여전히 어떤 [64]독성보다 상당히 낮다.
칸디다 과잉 성장
잠재적으로 발암성 구강 질환이 있는 환자의 칸디다 알비칸은 [65]문제를 일으키기에 충분한 양의 아세트알데히드를 생성하는 것으로 나타났다.
「 」를 참조해 주세요.
레퍼런스
- ^ SciFinder Scholar (2009년 11월 4일 액세스)아세트알데히드(75-07-0) 물질 상세.
- ^ 암의 분자병리학 및 진단(P.190)
- ^ a b Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. p. 908. doi:10.1039/9781849733069-00648. ISBN 978-0-85404-182-4.
- ^ a b Stoffdaten Acetaldehydehd bei Celanes Chemicals.1999년 12월 현재 Wayback Machine에서 2008년 5월 17일 아카이브 완료.
- ^ a b c d NIOSH Pocket Guide to Chemical Hazards. "#0001". National Institute for Occupational Safety and Health (NIOSH).
- ^ Haynes, William M., ed. (2016). CRC Handbook of Chemistry and Physics (97th ed.). CRC Press. pp. 5–88. ISBN 9781498754293.
- ^ "Acetaldehyde".
- ^ John Rumble (18 June 2018). CRC Handbook of Chemistry and Physics (99th ed.). CRC Press. pp. 5–3. ISBN 978-1138561632.
- ^ a b c 시그마-알드리치, 아세트알데히드2022-02-15에 취득.
- ^ a b c "Acetaldehyde". NIOSH. 4 December 2014. Retrieved 12 February 2015.
- ^ Uebelacker, Michael; Lachenmeier, Dirk (13 June 2011). "Quantitative Determination of Acetaldehyde in Foods Using Automated Digestion with Simulated Gastric Fluid Followed by Headspace Gas Chromatography". Journal of Automated Methods and Management in Chemistry. 2011: 907317. doi:10.1155/2011/907317. PMC 3124883. PMID 21747735.
- ^ a b "Chemicals in the Environment: Acetaldehyde (CAS NO. 75-07-0)". epa.gov. Office of Pollution Prevention and Toxics, United States Environmental Protection Agency. August 1994. Archived from the original on 17 August 2002. Retrieved 22 January 2011.
- ^ IARC 그룹 1 발암물질 목록
- ^ a b Zhou, Ying; Li, Chaoyang; Huijbregts, Mark A. J.; Mumtaz, M. Moiz (7 October 2015). "Carcinogenic Air Toxics Exposure and Their Cancer-Related Health Impacts in the United States". PLOS ONE. 10 (10): e0140013. Bibcode:2015PLoSO..1040013Z. doi:10.1371/journal.pone.0140013. PMC 4596837. PMID 26444872.
- ^ Schele, C. W. (1774) "Om Brunsten Eller Magnesia nigra och des egenskapskapsakademiens handlingar (갈색석 또는 흑색 마그네슘[즉 망간광석] 및 그 특성에 대하여)", Kungliga Svenska Vetenska vetskapskademienscademienshaneshaneshaneshel (35– 과학 연구소의 취급(스웨덴)109-110페이지에서 쉴은 이산화망간(브룬스텐)과 염산(스피루스 살리스) 또는 황산(스피리투스 비트리오리)으로 역류("소화") 에탄올(Alkohol vini)하면 "에테르 니트리"(질산으로 처리된 에탄올)와 같은 냄새가 난다고 언급했습니다.나중에 조사자들은 쉴이 아세트알데히드를 생산했다는 것을 알았다.
- ^ 주의:
- 프랑스 낭트의 약사 다비트는 일련의 실험을 했고 에탄올의 수소와 황산의 산소가 결합해 물을 만들면서 아세트알데히드가 형성됐다는 결론을 내렸다: 다비트 (1800) "엑스트라 뒤 메무아르 뒤 시트" Dabit sur l'ther" (시민 Dabit의 에테르 회고록 발췌), Annales de Chimie, 34:289-305.
- Fourcroy와 Vauquelin은 아세트알데히드 생산 과정에서 황산이 소비되지 않았다고 밝혔다.Fourcroy and Vauquelin (1800), "Sur l'éther préparé man la maniére du cit." 다빗" (시민 다빗을 위해 준비된 에테르에 대하여), 아날레스 드 치미, 34: 318-332.
- ^ 참조:
- (Döbereiner) (1821) "Neue Aether"(새로운 에테르), 저널 für Chemie und Physik, 32 : 269–270.Döbereiner는 새로운 "에테르"를 "산소 에테르"라고 명명했다.
- (Döbereiner) (1822) "Döbereiner's Devatat zur Darstellung des Sauerstoffaethers"(산소에테르 제조를 위한 Döbereiner의 장치), 저널 für Chemie und Physik, 34:–125.
- Döbereiner, J. W. (1832) "Bildung des Sauerstoff-Aethers durch atmosphérische Oxiation des Alkohols"(알코올의 대기 산화에 의한 옥시에테르 생성), 저널 für Chemie und Physik, 64:466–468.이 논문에서 Döbereiner는 백금 흑색의 존재 하에서 에탄올 증기를 공기에 노출시켜 아세트알데히드를 만들었다.
- ^ Liebig, Justus(1835) "Uber die Producte der Oxydation des Alkohols"(알코올 [에탄올] 산화물에 대하여), Annalen der Chemie, 14:133–167.
- ^ Brock, William H. (1997년) Justus von Liebig: 케미컬 게이트키퍼.영국 케임브리지: 케임브리지 대학 출판부, 83-84페이지.
- ^ Liebig, J. (1835년) "알코올 산화 생성물에 대하여" Annales de Chimie et de L'alcool, 59: 289–327.290페이지부터: "Je le decrirai dans ce mémoire sous le nom d'aldehyde; ce nom est formé de alcool dehrogenatus." (알데히드라는 이름으로 이 회고록에서 설명하겠습니다.이 이름은 알코올 탈수소로부터 만들어졌습니다.)
- ^ 그 이름은 적어도 1868년에 바뀌었다.예를 들어 다음과 같습니다.Eugen F. von Gorup-Besanez, ed., Lehrbuch der Organischen Chemie für den Unterricht auf Universitéten...[대학에서의 수업을 위한 유기화학 교과서...], 제3판 (Braunschweig, 독일:프리드리히 비에베그와 손, 1868), 제2권, 88쪽.
- ^ a b c d e f g h i j k 에커트, 마크 등(2007) Wiley-VCH, Weinheim의 Ulmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim에 있는 "아세트알데히드"doi: 10.1002/14356007.a01_031.pub2
- ^ Dmitry A. Ponomarev; Sergey M. Shevchenko (2007). "Hydration of Acetylene: A 125th Anniversary" (PDF). J. Chem. Educ. 84 (10): 1725. Bibcode:2007JChEd..84.1725P. doi:10.1021/ed084p1725.
- ^ Keeffe, J. R.; Kresge, A. J.; Schepp, N. P. (1990). "Keto-enol equilibrium constants of simple monofunctional aldehydes and ketones in aqueous solution". Journal of the American Chemical Society. 112 (12): 4862–4868. doi:10.1021/ja00168a035.
- ^ Johnson, R.D. III "CCCBDB NIST 표준 참조 데이터베이스"nist.gov
- ^ Heazlewood, B. R.; MacCarone, A. T.; Andrews, D. U.; Osborn, D. L.; Harding, L. B.; Klippenstein, S. J.; Jordan, M. J. T.; Kable, S. H. (2011). "Near-threshold H/D exchange in CD3CHO photodissociation". Nature Chemistry. 3 (6): 443–8. Bibcode:2011NatCh...3..443H. doi:10.1038/nchem.1052. PMID 21602858.
- ^ Andrews, D. U.; Heazlewood, B. R.; MacCarone, A. T.; Conroy, T.; Payne, R. J.; Jordan, M. J. T.; Kable, S. H. (2012). "Photo-Tautomerization of Acetaldehyde to Vinyl Alcohol: A Potential Route to Tropospheric Acids". Science. 337 (6099): 1203–6. Bibcode:2012Sci...337.1203A. doi:10.1126/science.1220712. PMID 22903524. S2CID 42079807.
- ^ J. Wiley & Sons, New York.Doi: 10.1002/047084289X (Ed: L. Paquet), Sowin, J.; Melcher, L. M. (2004) "아세트알데히드" (Ed: L. Paquet)
- ^ Behrens, C.; Paquette, L. A. (1998). "N-Benzyl-2,3-Azetidinedione (2,3-Azetidinedione, 1-(phenylmethyl)-)". Organic Syntheses. 75: 106. doi:10.15227/orgsyn.075.0106.; 를 참조해 주세요.
- ^ Walter, L. A. (1943). "1-(α-Pyridyl)-2-Propanol (2-(β-Hydroxypropyl)pyridine)". Organic Syntheses. 23: 83. doi:10.15227/orgsyn.023.0083.; Collective Volume, vol. 3, p. 757
- ^ Schurink, H. B. J. (1925). "Pentaerythritol". Organic Syntheses. 4: 53. doi:10.15227/orgsyn.004.0053.; Collective Volume, vol. 1, p. 425
- ^ Kendall, E. C.; McKenzie, B. F. (1929). "dl-Alanine". Organic Syntheses. 9: 4. doi:10.15227/orgsyn.009.0004.; Collective Volume, vol. 1, p. 21
- ^ Wittig, G.; Hesse, A. (1970). "Directed Aldol Condensations: β-Phenylcinnamaldehyde (2-Propenal, 3,3-diphenyl-)". Organic Syntheses. 50: 66. doi:10.15227/orgsyn.050.0066.; Collective Volume, vol. 6, p. 901
- ^ Frank, R. L.; Pilgrim, F. J.; Riener, E. F. (1950). "5-Ethyl-2-Methylpyridine (2-Picoline, 5-ethyl-)". Organic Syntheses. 30: 41. doi:10.15227/orgsyn.030.0041.
- ^ Weidenbusch, H. (1848) "Ever einige Producte der Einwirkung von Alkalien und Sauren auf den Aldehyde"(알칼리 및 산이 아세트알데히드와 반응하는 일부 산물에 대하여), Annalen der Chemie, 66: 152-165 참조.
- ^ Adkins, H.; Nissen, B. H. (1923). "Acetal". Organic Syntheses. 3: 1. doi:10.15227/orgsyn.003.0001.; Collective Volume, vol. 1, p. 1
- ^ Lavinia, M.; Gheorghe, I. (2010). "Poly(vinylphosphonic acid) and its derivatives". Progress in Polymer Science. 35 (8): 1078–1092. doi:10.1016/j.progpolymsci.2010.04.001.
- ^ a b Hipolito, L.; Sanchez, M. J.; Polache, A.; Granero, L. (2007). "Brain metabolism of ethanol and alcoholism: An update". Curr. Drug Metab. 8 (7): 716–727. doi:10.2174/138920007782109797. PMID 17979660.
- ^ '아세트알데히드' ihs.com.
- ^ 리서치 앤 마켓즈(주)"아세트알데히드 – 글로벌 비즈니스 전략 보고서"
- ^ Tsukamoto, S; Muto, T; Nagoya, T; Shimamura, M; Saito, M; Tainaka, H (1989). "Determinations of ethanol, acetaldehyde and acetate in blood and urine during alcohol oxidation in man". Alcohol and Alcoholism. 24 (2): 101–8. doi:10.1093/oxfordjournals.alcalc.a044872. PMID 2719768.
- ^ 미국 환경보호청 아세트알데히드 화학요약
- ^ Scientific Committee on Cosmetic Products and Non-Food Products (25 May 2004). "Opinion of the Scientific Committee on Cosmetic Products and Non-Food Products Intended for Consumers Concerning Acetaldehyde" (PDF). p. 11. Retrieved 28 September 2011.
- ^ International Agency for Rescarch on Cancer, World Health Organization. (1988). Alcohol drinking. Lyon: World Health Organization, International Agency for Research on Cancer. ISBN 978-92-832-1244-7. p3
- ^ 국제 암 연구 기관(International Agency for Research on Cancer Monograph Working Group, Special Report: 정책 A 인간 발암물질 검토—Part E: 담배, 아레카 너트, 알코올, 석탄 연기 및 젓갈 생선.Lancet 2009 10, 1033 – 1034.
- ^ Lambert, B; He, S. M. (1988). "DNA and chromosome damage induced by acetaldehyde in human lymphocytes in vitro". Annals of the New York Academy of Sciences. 534 (1): 369–76. Bibcode:1988NYASA.534..369L. doi:10.1111/j.1749-6632.1988.tb30124.x. PMID 3389666. S2CID 22732731.
- ^ Aberle, N. S.; Burd, L; Zhao, B. H.; Ren, J (2004). "Acetaldehyde-Induced Cardiac Contractile Dysfunction May Be Alleviated by Vitamin B1 but Not by Vitamins B6 or B12". Alcohol and Alcoholism. 39 (5): 450–4. doi:10.1093/alcalc/agh085. PMID 15304379.
- ^ a b c Hodskinson MR, Bolner A, Sato K, Kamimae-Lanning AN, Roijers K, Witte M, Mahesh M, Silhan J, Pete M, Williams DM, Kind J, Chin JW, Patel KJ, Kniper.알코올 유래 DNA 가교 링크는 두 가지 다른 메커니즘에 의해 복구됩니다.자연.2020년 3월;579(7800):603-608.doi:10.1038/s41586-020-2059-5.Epub 2020 3월 4일 PMID 32132710, PMCID: PMC7116288.
- ^ Ohta, S; Ohsawa I; Kamino K; Ando F; Shimokata H. (April 2004). "Mitochondrial ALDH2 Deficiency as an Oxidative Stress". Annals of the New York Academy of Sciences. 1011 (1): 36–44. Bibcode:2004NYASA1011...36O. doi:10.1196/annals.1293.004. PMID 15126281. S2CID 28571902.
- ^ Homann, N.; Stickel, F.; König, I. R.; Jacobs, A.; Junghanns, K.; Benesova, M.; Schuppan, D.; Himsel, S.; Zuber-Jerger, I.; Hellerbrand, C.; Ludwig, D.; Caselmann, W. H.; Seitz, H. K. (2006). "Alcohol dehydrogenase 1C*1 allele is a genetic marker for alcohol-associated cancer in heavy drinkers". International Journal of Cancer. 118 (8): 1998–2002. doi:10.1002/ijc.21583. PMID 16287084. S2CID 11716548.
- ^ Spengler, John D.; McCarthy, John F.; Samet, Jonathan M. (2000). Indoor Air Quality Handbook. New York, NY, USA: McGraw-Hill Professional Publishing. p. 761. ISBN 978-0074455494.
- ^ Dafni A. Missia; E. Demetriou; N. Michael; E.I. Tolis; J.G. Bartzis (2010). "Indoor exposure from building materials: A field study". Atmospheric Environment. 44 (35): 4388–4395. Bibcode:2010AtmEn..44.4388M. doi:10.1016/j.atmosenv.2010.07.049.
- ^ Shrestha, Krishna Prasad; Giri, Binod Raj; Adil, Mohammad; Seidel, Lars; Zeuch, Thomas; Farooq, Aamir; Mauss, Fabian (16 September 2021). "Detailed Chemical Kinetic Study of Acetaldehyde Oxidation and Its Interaction with NOx". Energy & Fuels. 35 (18): 14963–14983. doi:10.1021/acs.energyfuels.1c01948. ISSN 0887-0624. S2CID 239683740.
- ^ Clements, A. L.; Jia, Y.; Denbleyker, A.; McDonald-Buller, E.; Fraser, M. P.; Allen, D. T.; Collins, D. R.; Michel, E.; Pudota, J.; Sullivan, D.; Zhu, Y. (2009). "Air pollutant concentrations near three Texas roadways, part II: Chemical characterization and transformation of pollutants". Atmospheric Environment. 43 (30): 4523–4534. Bibcode:2009AtmEn..43.4523C. doi:10.1016/j.atmosenv.2009.06.044.
- ^ Talhout, R; Opperhuizen, A; van Amsterdam, JG (October 2007). "Role of acetaldehyde in tobacco smoke addiction". Eur Neuropsychopharmacol. 17 (10): 627–36. doi:10.1016/j.euroneuro.2007.02.013. PMID 17382522. S2CID 25866206.
- ^ Talhout, Reinskje; Schulz, Thomas; Florek, Ewa; Van Benthem, Jan; Wester, Piet; Opperhuizen, Antoon (2011). "Hazardous Compounds in Tobacco Smoke". International Journal of Environmental Research and Public Health. 8 (12): 613–628. doi:10.3390/ijerph8020613. ISSN 1660-4601. PMC 3084482. PMID 21556207.
- ^ "NIDA – 간행물 – NIDA 노트 – Vol. 20, No. 3" 2009년 8월 25일 Wayback Machine에서 아카이브.drugabuse.gov
- ^ UCI의 연구에 따르면 니코틴의 중독성이 다른 담배 연기 화학물질과 결합하면 증가한다고 한다.캘리포니아 대학교.2004-10-28
- ^ Singh, R (2009). "Evaluation of the DNA Damaging Potential of Cannabis Cigarette Smoke by the Determination of Acetaldehyde Derived N2-Ethyl-2'-deoxyguanosine Adducts". Chem. Res. Toxicol. 22 (6): 1181–1188. doi:10.1021/tx900106y. PMID 19449825.
- ^ Salaspuro, M. (2009). "Acetaldehyde as a common denominator and cumulative carcinogen in digestive tract cancers". Scandinavian Journal of Gastroenterology. 44 (8): 912–925. doi:10.1080/00365520902912563. PMID 19396661. S2CID 23291758.
- ^ 아세트알데히드에 대한 SCCS 소비자 안전 과학 위원회 의견.유럽위원회 2012년 9월 18일
- ^ Day, M.; Wiles, D. M. (January 1972). "Photochemical degradation of poly(ethylene terephthalate). III. Determination of decomposition products and reaction mechanism". Journal of Applied Polymer Science. 16 (1): 203–215. doi:10.1002/app.1972.070160118.
- ^ Nawrocki, J; Dąbrowska, A; Borcz, A (November 2002). "Investigation of carbonyl compounds in bottled waters from Poland". Water Research. 36 (19): 4893–4901. doi:10.1016/S0043-1354(02)00201-4. PMID 12448533.
- ^ "Do Acetaldehyde and Formaldehyde from Pet Bottles Result in Unacceptable Flavor or Aroma in Bottled Water?" (PDF). PET Resin Association. Retrieved 26 February 2015.
- ^ Gainza-Cirauqui, M.L.; Nieminen, M.T.; Novak Frazer, L.; Aguirre-Urizar, J.M.; Moragues, M.D.; Rautemaa, R. (March 2013). "Production of carcinogenic acetaldehyde by Candida albicans from patients with potentially malignant oral mucosal disorders". Journal of Oral Pathology and Medicine. 42 (3): 243–249. doi:10.1111/j.1600-0714.2012.01203.x. PMID 22909057.
외부 링크
- 국제화학안전카드 0009
- NIOSH 화학적 위험에 대한 포켓 가이드
- 샘플링 및 분석 방법
- IARC Monograph: '아세트알데히드'
- Hal Kibbey, 알코올 음주와 알코올 중독에 대한 유전적 영향, 인디애나 대학 연구 및 창작 활동, 제17권 제3호.
- 미국 식품의약국(FDA) 아세트알데히드 정보
- 에틸렌산화법에 의한 아세트알데히드 제조공정 흐름표