VDAC1
VDAC1| VDAC1 | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 식별자 | |||||||||||||||||||||||||
| 별칭 | VDAC1, PROIN, VDAC-1, 전압 종속 음이온 채널 1 | ||||||||||||||||||||||||
| 외부 ID | OMIM: 604492 MGI: 106919 HomoloGene: 107244 GeneCard: VDAC1 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| 직교체 | |||||||||||||||||||||||||
| 종 | 인간 | 마우스 | |||||||||||||||||||||||
| 엔트레스 | |||||||||||||||||||||||||
| 앙상블 | |||||||||||||||||||||||||
| 유니프로트 | |||||||||||||||||||||||||
| RefSeq(mRNA) | |||||||||||||||||||||||||
| RefSeq(단백질) |
| ||||||||||||||||||||||||
| 위치(UCSC) | n/a | Cr 11: 52.36 – 52.39Mb | |||||||||||||||||||||||
| PubMed 검색 | [2] | [3] | |||||||||||||||||||||||
| 위키다타 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
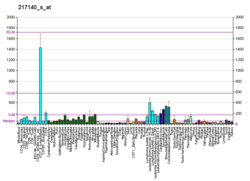
전압 의존성 음이온 선택적 채널 1(VDAC-1)은 베타 배럴 단백질로 인간 내 5번 염색체에 위치한 VDAC1 유전자에 의해 암호화된다.[4][5]외측 미토콘드리아막(OMM)과 외측세포막에서 이온통로를 형성한다.OMM에서는 ATP가 미토콘드리아에서 세포질로 확산되도록 한다.세포막에서는 부피 조절에 관여한다.모든 진핵 세포 내에서 미토콘드리아는 세포 생존에 필요한 다른 대사물들 사이에서 ATP의 합성을 담당한다.따라서 VDAC1은 미토콘드리온과 세포대사와 세포사이의 균형을 중재하는 세포간의 통신을 허용한다.VDAC1은 대사 침투 외에도 헥소키나아제와 같은 단백질의 발판 역할을 하며 차례로 대사를 조절할 수 있다.[6]
이 단백질은 전압에 의존하는 음이온 채널이며 세포 대사, 미토콘드리아 사멸, 정조세포의 조절에 관여하는 다른 VDAC 등소형(VDAC2 및 VDAC3)과 높은 구조적 호몰로학을 공유한다.[7][8][9][10]이 모공의 과도한 발현과 잘못된 조절은 세포의 세포사멸을 초래하여 몸 안의 다양한 질병으로 이어질 수 있다.특히 VDAC1은 주요 칼슘 이온 이송 통로인 만큼 기능장애가 암, 파킨슨병(PD), 알츠하이머병 등에 연관돼 있다.[11][12][13]게다가, 최근의 연구들은 VDAC1 단백질 내의 과잉 표현이 제2형 당뇨병과 연관되어 있다는 것을 보여주었다.룬드대학은 발현보다 VDAC1을 차단하는 효과가 2형 당뇨병의 확산을 막을 수 있다는 연구 결과를 발표했다.[14]
구조
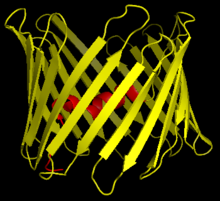
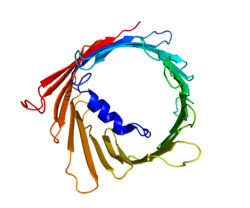
3개의 VDAC 등양식(VDAC1, VDAC2, VDAC3)은 보존성이 높은 DNA 시퀀스와 넓은 β-바렐 구조를 형성하는 3D 구조를 가지고 있으며, 그 안에는 알파 나선형 N단자 세그먼트가 상주하여 모공을 부분적으로 닫는다.[15]VDAC1의 구조는 X선 결정학, 핵자기공명(NMR) 분광학, 또는 이 두 가지를 조합하여 3개의 독립 연구소에 의해 해결되었다.이러한 구조 연구 중 2개는 인간 VDAC1(hDAC1) 구조를 결정하는 데 사용되었고, X선 결정학은 hVDAC1(mVDAC1)과 다른 무린 VDAC1(mVDAC1) 구조를 2개의 잔류물만으로 해결하는 데 사용되었다.[16][17][18]이러한 결정 구조는 알파 나선 및 β-스트랜드 도메인의 존재를 예측한 이전의 원형 이분법 연구와 일치한다.[19]
mVDAC1 구조물의 구조해석 결과, 19암페타 β-가로 구성된 배럴 모양의 채널이 나타났으며, N-terminus와 C-terminus는 모두 미토콘드리온의 막간 공간을 향해 있었다.[20][21]β-strands은 루프를 통해 연결되며, 평행인 β- 1 1과 19를 제외하고 반선호도 패턴으로 배열된다.[18]공극의 높이는 40 ẳ이며, 개구부에서는 27 ẳ, 개구부에서는 20 ẳ, 개방 상태에서 N-단자 α-헬릭스 세그먼트에서는 14 ẳ까지 20 ẳ까지 감소한다.[22]폐쇄된 상태 순응은 아직 고립되고 결정되지 않았다.또한 N-terminus에는 β-시트 8-18의 잔류물과의 소수성 상호작용에 의해 모공 내벽에 고정되는 알파 헬리컬 세그먼트가 있다.[18]이 N단자는 이온의 이동이나 단백질의 부착을 위한 발판 역할을 할 수 있다.그러한 예로는 HK1 바인딩을 위한 도킹 사이트로 보여진다.[6]지적해야 할 상당한 잔류물은 아미노산 체인의 73번째 잔류물에 위치한 글루탐산염이다(E73)이 잔류물은 VDAC1과 VDAC2에서 발견되지만 VDAC3에서는 발견되지 않는다.이 충전된 잔여물의 측면 사슬은 일반적으로 반발력이 발생하는 인지질 빌레이어를 가리킨다.그러나 E73은 VDAC1 기능과 상호작용에 관여하였다.[23]
함수
VDAC1은 미토콘드리아 포린 계열에 속하며 다른 VDAC 등본 형태와 유사한 생물학적 기능을 공유할 것으로 예상된다.[24]세 가지 이소 형태 중 VDAC1은 주요 칼슘 이온 전달 채널이며 가장 많이 기록된다.[12][25]VDAC1은 외부 미토콘드리아 멤브레인(OMM)을 가로질러 ATP와 기타 소규모 대사물을 운반하여 TCA 사이클의 조절을 가능하게 하고, 나아가 활성산소종(ROS) 생산을 가능하게 함으로써 세포대사에 관여한다.[11]효모세포에서는 산화스트레스에 반응하여 ROS가 축적되어 미토콘드리아 기능이 저하되고 '펫라이트' 표현형이 발생한다.그러나 쁘띠 효모세포는 야생형 세포보다 수명이 길며 노화 등 유사한 상황에서 VDAC1에 의한 보호기능을 나타낸다.[6][25]
전압 게이트
VDAC1은 미토콘드리온 내부 및 외부 분자의 전도성을 허용한다.투과성은 전압에 의해 결정되는 VDAC1의 순응 상태에 따라 달라진다.저전압(10mV)에서 모공은 채널이 약하게 음이온 선택적이며 대사물의 더 큰 유속을 허용하는 "개방" 상태에 있다.모공 크기가 크기 때문에 포화 ATP 조건 하에서 대사 게이트는 초당 200만 ATP의 수송량과 생리학적 조건 하에서 10,000 ATP의 수송량을 나타낸다.[26]양극 또는 음극 방향의 높은 전압(>30mV)에서 모공은 "폐쇄" 상태에 있고 신진대사물이 덜 운반될 수 있도록 약하게 양이온 선택적이다.[18]대사물의 유동성은 무시할 수 있는 것으로 볼 수 있다.이러한 상태의 변화는 아직 발견되지 않은 단백질의 순응적인 변화에 의해 매개된다.알파 나선형 N-terminus 세그먼트는 모공 중앙에 위치하기 때문에 대사 게이트에 이상적으로 위치한다.이 연구자들은 알파 나선이 순응 상태를 결정하는데 중요한 기여를 했다고 믿는다.그러나 최근의 연구에서는 N단자가 적절한 전압 동기화를 위해 불필요하다는 것을 보여주었고 따라서 유연한 베타 배럴을 순응적 변화의 메커니즘으로 제시한다.[22]
과점화
아토믹포스 현미경(AFM)은 모공과 자기와의 상호작용을 보여주는 디머와 대형 과점뿐만 아니라 VDAC1 모노머도 존재한다고 밝혔으나 디머는 더 빈번하다.[27]특히 hVDAC1은 모공 투과성을 증가시키는 병렬 조광기로 배열하는 것으로 나타났다.[16]VDAC1에서 73번째 위치에 위치한 글루타민산염도 칼슘이 존재할 때 과점화 작용을 하는 것으로 나타났다.[23]VDAC는 또한 미토콘드리아 투과성 전환 모공(MPTP)의 일부를 형성하기 위해 과점할 수 있으며, 따라서 사이토크롬 C를 방출하여 사멸을 유도한다.VDACs는 또한 Bcl-2 계열 단백질과 키나아제와 같은 친 또는 반독성 단백질과 상호작용을 하는 것으로 관찰되어 왔으며, 따라서 MPTP와는 독립적으로 세포사멸에 기여할 수 있다.[24]
임상적 유의성
전압 의존 음이온 채널은 생리학적 역할은 다르지만 모두 이온과 대사물 수송에서 기능한다.그들의 역할 때문에, 채널의 기능 장애는 다양한 질병으로 이어질 수 있다.VDAC1은 항복제 단백질인 Bcl-2 단백질, 특히 Bcl-xl, 그리고 암 중 과다압박되는 Mcl-1과의 상호작용을 통해 암에 연루되었다.이 두 개의 Bcl-2 단백질은 VDAC1과 상호작용하여 OMM을 통한 칼슘 이온 수송과 궁극적으로, ROS 생산을 조절한다.높은 수준의 ROS가 세포 죽음을 유발하는 반면, 비살상 수준은 암세포의 확산, 이동, 침투를 촉진할 수 있는 신호 전달 경로를 방해한다.[11]더욱이, VDAC1 과다압박은 세포 반응 증가와 항암제 및 치료 효과와 연관되어 있으며, 암 치료의 치료 목표로서 VDAC1을 더욱 뒷받침하고 있다.[11][28]
칼슘 이온 수송에서 VDAC1의 기능은 신경퇴행성 질환과도 연관되어 있다.PD에서 VDAC1은 미토콘드리아 내 칼슘 이온 수치를 증가시켜 미토콘드리아 투과성 증가, 미토콘드리아 막전위차 교란, ROS 생산량 증가, 세포사망, 뉴런 퇴화 등을 초래한다.[12]VDAC1은 아밀로이드 β(Aβ)[13]와 상호작용하여 채널의 전도성을 높이고 결국 셀의 사멸을 초래하는 것으로 나타났다.
상호작용
VDAC1은 모공 내 상호작용을 통해 이온과 대사물의 유동성을 허용할 뿐만 아니라 많은 단백질의 발판 역할을 한다.
이 채널을 통해 이동하는 주요 대사물은 ATP이다.이 분자의 빠른 전송에 사용되는 낮은 친화력 결합 부위는 마르코프 상태 모델링 접근법에 의해 발견되었다.ATP는 채널을 통해 이동하는 본질적으로 순차적으로 모공 내의 여러 기본 잔류물에 결합하는 것으로 나타났다.[29]
VDAC1은 또한 다음과 상호 작용하는 것으로 나타났다.
참고 항목
참조
- ^ a b c GRCm38: 앙상블 릴리스 89: ENSMUSG000020402 - 앙상블, 2017년 5월
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Blachly-Dyson E, Baldini A, Litt M, McCabe ER, Forte M (March 1994). "Human genes encoding the voltage-dependent anion channel (VDAC) of the outer mitochondrial membrane: mapping and identification of two new isoforms". Genomics. 20 (1): 62–7. doi:10.1006/geno.1994.1127. PMID 7517385.
- ^ "Entrez Gene: VDAC1 voltage-dependent anion channel 1".
- ^ a b c d Reina S, Palermo V, Guarnera A, Guarino F, Messina A, Mazzoni C, De Pinto V (July 2010). "Swapping of the N-terminus of VDAC1 with VDAC3 restores full activity of the channel and confers anti-aging features to the cell". FEBS Letters. 584 (13): 2837–44. doi:10.1016/j.febslet.2010.04.066. PMID 20434446. S2CID 22130291.
- ^ Subedi KP, Kim JC, Kang M, Son MJ, Kim YS, Woo SH (February 2011). "Voltage-dependent anion channel 2 modulates resting Ca²+ sparks, but not action potential-induced Ca²+ signaling in cardiac myocytes". Cell Calcium. 49 (2): 136–43. doi:10.1016/j.ceca.2010.12.004. PMID 21241999.
- ^ a b Alvira CM, Umesh A, Husted C, Ying L, Hou Y, Lyu SC, Nowak J, Cornfield DN (November 2012). "Voltage-dependent anion channel-2 interaction with nitric oxide synthase enhances pulmonary artery endothelial cell nitric oxide production". American Journal of Respiratory Cell and Molecular Biology. 47 (5): 669–78. doi:10.1165/rcmb.2011-0436OC. PMC 3547107. PMID 22842492.
- ^ Cheng EH, Sheiko TV, Fisher JK, Craigen WJ, Korsmeyer SJ (July 2003). "VDAC2 inhibits BAK activation and mitochondrial apoptosis". Science. 301 (5632): 513–7. Bibcode:2003Sci...301..513C. doi:10.1126/science.1083995. PMID 12881569. S2CID 37099525.
- ^ Li Z, Wang Y, Xue Y, Li X, Cao H, Zheng SJ (February 2012). "Critical role for voltage-dependent anion channel 2 in infectious bursal disease virus-induced apoptosis in host cells via interaction with VP5". Journal of Virology. 86 (3): 1328–38. doi:10.1128/JVI.06104-11. PMC 3264341. PMID 22114330.
- ^ a b c d e Huang H, Shah K, Bradbury NA, Li C, White C (October 2014). "Mcl-1 promotes lung cancer cell migration by directly interacting with VDAC to increase mitochondrial Ca2+ uptake and reactive oxygen species generation". Cell Death & Disease. 5 (10): e1482. doi:10.1038/cddis.2014.419. PMC 4237246. PMID 25341036.
- ^ a b c Chu Y, Goldman JG, Kelly L, He Y, Waliczek T, Kordower JH (September 2014). "Abnormal alpha-synuclein reduces nigral voltage-dependent anion channel 1 in sporadic and experimental Parkinson's disease". Neurobiology of Disease. 69: 1–14. doi:10.1016/j.nbd.2014.05.003. PMID 24825319. S2CID 22722682.
- ^ a b Smilansky A, Dangoor L, Nakdimon I, Ben-Hail D, Mizrachi D, Shoshan-Barmatz V (December 2015). "The Voltage-dependent Anion Channel 1 Mediates Amyloid β Toxicity and Represents a Potential Target for Alzheimer Disease Therapy". The Journal of Biological Chemistry. 290 (52): 30670–83. doi:10.1074/jbc.M115.691493. PMC 4692199. PMID 26542804.
- ^ Zhang, Enming; Mohammed Al-Amily, Israa; Mohammed, Sarheed; Luan, Cheng; Asplund, Olof; Ahmed, Meftun; Ye, Yingying; Ben-Hail, Danya; Soni, Arvind; Vishnu, Neelanjan; Bompada, Pradeep (2019-01-08). "Preserving Insulin Secretion in Diabetes by Inhibiting VDAC1 Overexpression and Surface Translocation in β Cells". Cell Metabolism. 29 (1): 64–77.e6. doi:10.1016/j.cmet.2018.09.008. ISSN 1550-4131. PMC 6331340. PMID 30293774.
- ^ Amodeo GF, Scorciapino MA, Messina A, De Pinto V, Ceccarelli M (2014). "Charged residues distribution modulates selectivity of the open state of human isoforms of the voltage dependent anion-selective channel". PLOS ONE. 9 (8): e103879. Bibcode:2014PLoSO...9j3879A. doi:10.1371/journal.pone.0103879. PMC 4146382. PMID 25084457.
- ^ a b Bayrhuber M, Meins T, Habeck M, Becker S, Giller K, Villinger S, Vonrhein C, Griesinger C, Zweckstetter M, Zeth K (October 2008). "Structure of the human voltage-dependent anion channel". Proceedings of the National Academy of Sciences of the United States of America. 105 (40): 15370–5. Bibcode:2008PNAS..10515370B. doi:10.1073/pnas.0808115105. PMC 2557026. PMID 18832158.
- ^ Hiller S, Garces RG, Malia TJ, Orekhov VY, Colombini M, Wagner G (August 2008). "Solution structure of the integral human membrane protein VDAC-1 in detergent micelles". Science. 321 (5893): 1206–10. Bibcode:2008Sci...321.1206H. doi:10.1126/science.1161302. PMC 2579273. PMID 18755977.
- ^ a b c d Ujwal R, Cascio D, Colletier JP, Faham S, Zhang J, Toro L, Ping P, Abramson J (November 2008). "The crystal structure of mouse VDAC1 at 2.3 A resolution reveals mechanistic insights into metabolite gating". Proceedings of the National Academy of Sciences of the United States of America. 105 (46): 17742–7. doi:10.1073/pnas.0809634105. PMC 2584669. PMID 18988731.
- ^ Shanmugavadivu B, Apell HJ, Meins T, Zeth K, Kleinschmidt JH (April 2007). "Correct folding of the beta-barrel of the human membrane protein VDAC requires a lipid bilayer". Journal of Molecular Biology. 368 (1): 66–78. doi:10.1016/j.jmb.2007.01.066. PMID 17336328.
- ^ McCommis KS, Baines CP (June 2012). "The role of VDAC in cell death: friend or foe?". Biochimica et Biophysica Acta (BBA) - Biomembranes. 1818 (6): 1444–50. doi:10.1016/j.bbamem.2011.10.025. PMC 3288473. PMID 22062421.
- ^ Tomasello MF, Guarino F, Reina S, Messina A, De Pinto V (December 2013). "The voltage-dependent anion selective channel 1 (VDAC1) topography in the mitochondrial outer membrane as detected in intact cell". PLOS ONE. 8 (12): e81522. Bibcode:2013PLoSO...881522T. doi:10.1371/journal.pone.0081522. PMC 3855671. PMID 24324700.
- ^ a b Teijido O, Ujwal R, Hillerdal CO, Kullman L, Rostovtseva TK, Abramson J (March 2012). "Affixing N-terminal α-helix to the wall of the voltage-dependent anion channel does not prevent its voltage gating". The Journal of Biological Chemistry. 287 (14): 11437–45. doi:10.1074/jbc.M111.314229. PMC 3322836. PMID 22275367.
- ^ a b Keinan N, Pahima H, Ben-Hail D, Shoshan-Barmatz V (July 2013). "The role of calcium in VDAC1 oligomerization and mitochondria-mediated apoptosis". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1833 (7): 1745–54. doi:10.1016/j.bbamcr.2013.03.017. PMID 23542128.
- ^ a b Lee MJ, Kim JY, Suk K, Park JH (May 2004). "Identification of the hypoxia-inducible factor 1 alpha-responsive HGTD-P gene as a mediator in the mitochondrial apoptotic pathway". Molecular and Cellular Biology. 24 (9): 3918–27. doi:10.1128/mcb.24.9.3918-3927.2004. PMC 387743. PMID 15082785.
- ^ a b De Pinto V, Guarino F, Guarnera A, Messina A, Reina S, Tomasello FM, Palermo V, Mazzoni C (2010). "Characterization of human VDAC isoforms: a peculiar function for VDAC3?". Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1797 (6–7): 1268–75. doi:10.1016/j.bbabio.2010.01.031. PMID 20138821.
- ^ Rostovtseva, T.; Colombini, M. (1997). "VDAC channels mediate and gate the flow of ATP: implications for the regulation of mitochondrial function". Biophysical Journal. 72 (5): 1954–1962. Bibcode:1997BpJ....72.1954R. doi:10.1016/s0006-3495(97)78841-6. PMC 1184392. PMID 9129800.
- ^ Hoogenboom BW, Suda K, Engel A, Fotiadis D (July 2007). "The supramolecular assemblies of voltage-dependent anion channels in the native membrane". Journal of Molecular Biology. 370 (2): 246–55. doi:10.1016/j.jmb.2007.04.073. PMID 17524423.
- ^ a b Weisthal S, Keinan N, Ben-Hail D, Arif T, Shoshan-Barmatz V (October 2014). "Ca(2+)-mediated regulation of VDAC1 expression levels is associated with cell death induction". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1843 (10): 2270–81. doi:10.1016/j.bbamcr.2014.03.021. PMID 24704533.
- ^ Choudhary, Om P; Paz, Aviv; Adelman, Joshua L; Colletier, Jacques-Philippe; Abramson, Jeff; Grabe, Michael (2014). "Structure-guided simulations illuminate the mechanism of ATP transport through VDAC1". Nature Structural & Molecular Biology. 21 (7): 626–632. doi:10.1038/nsmb.2841. PMC 4157756. PMID 24908397.
- ^ a b Weng C, Li Y, Xu D, Shi Y, Tang H (March 2005). "Specific cleavage of Mcl-1 by caspase-3 in tumor necrosis factor-related apoptosis-inducing ligand (TRAIL)-induced apoptosis in Jurkat leukemia T cells". The Journal of Biological Chemistry. 280 (11): 10491–500. doi:10.1074/jbc.M412819200. PMID 15637055.
- ^ a b Shi Y, Chen J, Weng C, Chen R, Zheng Y, Chen Q, Tang H (June 2003). "Identification of the protein-protein contact site and interaction mode of human VDAC1 with Bcl-2 family proteins". Biochemical and Biophysical Research Communications. 305 (4): 989–96. doi:10.1016/s0006-291x(03)00871-4. PMID 12767928.
- ^ Shimizu S, Konishi A, Kodama T, Tsujimoto Y (March 2000). "BH4 domain of antiapoptotic Bcl-2 family members closes voltage-dependent anion channel and inhibits apoptotic mitochondrial changes and cell death". Proceedings of the National Academy of Sciences of the United States of America. 97 (7): 3100–5. Bibcode:2000PNAS...97.3100S. doi:10.1073/pnas.97.7.3100. PMC 16199. PMID 10737788.
- ^ Shimizu S, Narita M, Tsujimoto Y (June 1999). "Bcl-2 family proteins regulate the release of apoptogenic cytochrome c by the mitochondrial channel VDAC". Nature. 399 (6735): 483–7. Bibcode:1999Natur.399..483S. doi:10.1038/20959. PMID 10365962. S2CID 4423304.
- ^ Schwarzer C, Barnikol-Watanabe S, Thinnes FP, Hilschmann N (September 2002). "Voltage-dependent anion-selective channel (VDAC) interacts with the dynein light chain Tctex1 and the heat-shock protein PBP74". The International Journal of Biochemistry & Cell Biology. 34 (9): 1059–70. doi:10.1016/s1357-2725(02)00026-2. PMID 12009301.
- ^ Kusano H, Shimizu S, Koya RC, Fujita H, Kamada S, Kuzumaki N, Tsujimoto Y (October 2000). "Human gelsolin prevents apoptosis by inhibiting apoptotic mitochondrial changes via closing VDAC". Oncogene. 19 (42): 4807–14. doi:10.1038/sj.onc.1203868. PMID 11039896.
- ^ Baines CP, Song CX, Zheng YT, Wang GW, Zhang J, Wang OL, Guo Y, Bolli R, Cardwell EM, Ping P (May 2003). "Protein kinase Cepsilon interacts with and inhibits the permeability transition pore in cardiac mitochondria". Circulation Research. 92 (8): 873–80. doi:10.1161/01.RES.0000069215.36389.8D. PMC 3691672. PMID 12663490.
- ^ Sun Y, Vashisht AA, Tchieu J, Wohlschlegel JA, Dreier L (November 2012). "Voltage-dependent anion channels (VDACs) recruit Parkin to defective mitochondria to promote mitochondrial autophagy". The Journal of Biological Chemistry. 287 (48): 40652–60. doi:10.1074/jbc.M112.419721. PMC 3504778. PMID 23060438.
- ^ Noskov SY, Rostovtseva TK, Bezrukov SM (December 2013). "ATP transport through VDAC and the VDAC-tubulin complex probed by equilibrium and nonequilibrium MD simulations". Biochemistry. 52 (51): 9246–56. doi:10.1021/bi4011495. PMC 7259721. PMID 24245503.
추가 읽기
- Verrier F, Mignotte B, Jan G, Brenner C (December 2003). "Study of PTPC composition during apoptosis for identification of viral protein target" (PDF). Annals of the New York Academy of Sciences. 1010 (1): 126–42. Bibcode:2003NYASA1010..126V. doi:10.1196/annals.1299.022. PMID 15033708. S2CID 22660199.
- McEnery MW, Snowman AM, Trifiletti RR, Snyder SH (April 1992). "Isolation of the mitochondrial benzodiazepine receptor: association with the voltage-dependent anion channel and the adenine nucleotide carrier". Proceedings of the National Academy of Sciences of the United States of America. 89 (8): 3170–4. Bibcode:1992PNAS...89.3170M. doi:10.1073/pnas.89.8.3170. PMC 48827. PMID 1373486.
- Dawson SJ, White LA (May 1992). "Treatment of Haemophilus aphrophilus endocarditis with ciprofloxacin". The Journal of Infection. 24 (3): 317–20. doi:10.1016/S0163-4453(05)80037-4. PMID 1602151.
- Jürgens L, Ilsemann P, Kratzin HD, Hesse D, Eckart K, Thinnes FP, Hilschmann N (July 1991). "Studies on human porin. IV. The primary structures of "Porin 31HM" purified from human skeletal muscle membranes and of "Porin 31HL" derived from human B lymphocyte membranes are identical". Biological Chemistry Hoppe-Seyler. 372 (7): 455–63. doi:10.1515/bchm3.1991.372.2.455. PMID 1657034.
- Kayser H, Kratzin HD, Thinnes FP, Götz H, Schmidt WE, Eckart K, Hilschmann N (December 1989). "[Identification of human porins. II. Characterization and primary structure of a 31-lDa porin from human B lymphocytes (Porin 31HL)]". Biological Chemistry Hoppe-Seyler. 370 (12): 1265–78. PMID 2559745.
- Brdiczka D, Kaldis P, Wallimann T (November 1994). "In vitro complex formation between the octamer of mitochondrial creatine kinase and porin". The Journal of Biological Chemistry. 269 (44): 27640–4. doi:10.1016/S0021-9258(18)47033-0. PMID 7525559.
- Yu WH, Wolfgang W, Forte M (June 1995). "Subcellular localization of human voltage-dependent anion channel isoforms". The Journal of Biological Chemistry. 270 (23): 13998–4006. doi:10.1074/jbc.270.23.13998. PMID 7539795.
- Thomas L, Blachly-Dyson E, Colombini M, Forte M (June 1993). "Mapping of residues forming the voltage sensor of the voltage-dependent anion-selective channel". Proceedings of the National Academy of Sciences of the United States of America. 90 (12): 5446–9. Bibcode:1993PNAS...90.5446T. doi:10.1073/pnas.90.12.5446. PMC 46737. PMID 7685903.
- Blachly-Dyson E, Zambronicz EB, Yu WH, Adams V, McCabe ER, Adelman J, Colombini M, Forte M (January 1993). "Cloning and functional expression in yeast of two human isoforms of the outer mitochondrial membrane channel, the voltage-dependent anion channel". The Journal of Biological Chemistry. 268 (3): 1835–41. doi:10.1016/S0021-9258(18)53930-2. PMID 8420959.
- Schleiff E, Shore GC, Goping IS (March 1997). "Human mitochondrial import receptor, Tom20p. Use of glutathione to reveal specific interactions between Tom20-glutathione S-transferase and mitochondrial precursor proteins". FEBS Letters. 404 (2–3): 314–8. doi:10.1016/S0014-5793(97)00145-2. PMID 9119086. S2CID 29177508.
- Reymann S, Haase W, Krick W, Burckhardt G, Thinnes FP (August 1998). "Endosomes: another extra-mitochondrial location of type-1 porin/voltage-dependent anion-selective channels". Pflügers Archiv. 436 (3): 478–80. doi:10.1007/s004240050659. PMID 9644232. S2CID 670898.
- Narita M, Shimizu S, Ito T, Chittenden T, Lutz RJ, Matsuda H, Tsujimoto Y (December 1998). "Bax interacts with the permeability transition pore to induce permeability transition and cytochrome c release in isolated mitochondria". Proceedings of the National Academy of Sciences of the United States of America. 95 (25): 14681–6. Bibcode:1998PNAS...9514681N. doi:10.1073/pnas.95.25.14681. PMC 24509. PMID 9843949.
- Crompton M, Virji S, Ward JM (December 1998). "Cyclophilin-D binds strongly to complexes of the voltage-dependent anion channel and the adenine nucleotide translocase to form the permeability transition pore". European Journal of Biochemistry. 258 (2): 729–35. doi:10.1046/j.1432-1327.1998.2580729.x. PMID 9874241.
- Messina A, Oliva M, Rosato C, Huizing M, Ruitenbeek W, van den Heuvel LP, Forte M, Rocchi M, De Pinto V (February 1999). "Mapping of the human Voltage-Dependent Anion Channel isoforms 1 and 2 reconsidered". Biochemical and Biophysical Research Communications. 255 (3): 707–10. doi:10.1006/bbrc.1998.0136. PMID 10049775.
- Shimizu S, Narita M, Tsujimoto Y (June 1999). "Bcl-2 family proteins regulate the release of apoptogenic cytochrome c by the mitochondrial channel VDAC". Nature. 399 (6735): 483–7. Bibcode:1999Natur.399..483S. doi:10.1038/20959. PMID 10365962. S2CID 4423304.
- Decker WK, Bowles KR, Schatte EC, Towbin JA, Craigen WJ (October 1999). "Revised fine mapping of the human voltage-dependent anion channel loci by radiation hybrid analysis". Mammalian Genome. 10 (10): 1041–2. doi:10.1007/s003359901158. PMID 10501981. S2CID 27663120.
- Jacotot E, Ravagnan L, Loeffler M, Ferri KF, Vieira HL, Zamzami N, Costantini P, Druillennec S, Hoebeke J, Briand JP, Irinopoulou T, Daugas E, Susin SA, Cointe D, Xie ZH, Reed JC, Roques BP, Kroemer G (January 2000). "The HIV-1 viral protein R induces apoptosis via a direct effect on the mitochondrial permeability transition pore". The Journal of Experimental Medicine. 191 (1): 33–46. doi:10.1084/jem.191.1.33. PMC 2195797. PMID 10620603.
- Shimizu S, Tsujimoto Y (January 2000). "Proapoptotic BH3-only Bcl-2 family members induce cytochrome c release, but not mitochondrial membrane potential loss, and do not directly modulate voltage-dependent anion channel activity". Proceedings of the National Academy of Sciences of the United States of America. 97 (2): 577–82. Bibcode:2000PNAS...97..577S. doi:10.1073/pnas.97.2.577. PMC 15372. PMID 10639121.
- Stadtmüller U, Eben-Brunnen J, Schmid A, Hesse D, Klebert S, Kratzin HD, Hesse J, Zimmermann B, Reymann S, Thinnes FP, Benz R, Götz H, Hilschmann N (December 1999). "Mitochondria-derived and extra-mitochondrial human type-1 porin are identical as revealed by amino acid sequencing and electrophysiological characterisation". Biological Chemistry. 380 (12): 1461–6. doi:10.1515/BC.1999.189. PMID 10661876. S2CID 1566781.