수산화 알루미늄
Aluminium hydroxide
 | |
 | |
| 이름 | |
|---|---|
| 우선 IUPAC 이름 수산화 알루미늄 | |
| 시스템 IUPAC 이름 트리히드록시도 알루미늄 | |
| 기타 이름 알루미늄산 수산화 알루미늄 | |
| 식별자 | |
3D 모델(JSmol) | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| 드러그뱅크 | |
| ECHA 정보 카드 | 100.040.433 |
| 케그 | |
PubChem CID | |
| RTECS 번호 |
|
| 유니 | |
CompTox 대시보드 (EPA ) | |
| |
| 속성[1][2] | |
| Al(OH)3 | |
| 몰 질량 | 78.00g/g |
| 외모 | 백색 비정질 분말 |
| 밀도 | 2.42 g/cm3, 솔리드 |
| 녹는점 | 300 °C (572 °F, 573 K) |
| 0.0001 g/100 mL | |
용해도 제품(Ksp) | 3×10−34 |
| 용해성 | 산과 알칼리에 녹는 |
| 산도(pKa) | >7 |
| 등전점 | 7.7 |
| 열화학[3] | |
표준 엔탈피/ 형성 (δHf⦵298) | - 1277 kJ/mol−1 |
| 약리학[4] | |
| A02AB01(WHO) | |
| 위험 요소 | |
| GHS 라벨링: | |
 | |
| H319, H335 | |
| P261, , , , , , , , | |
| NFPA 704(파이어 다이아몬드) | |
| 플래시 포인트 | 불연성 |
| 치사량 또는 농도(LD, LC): | |
LD50(중간선량) | >125mg/kg (랫드, 경구) |
| 안전 데이터 시트(SDS) | 외부 MSDS |
| 관련 화합물 | |
기타 음이온 | 없음. |
관련 화합물 | 산화나트륨, 산화 알루미늄 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
수산화알루미늄, Al(3OH)은 자연에서 광물 깁사이트(hydrargillite라고도 함)와 그 보다 희귀한 세 가지 다형성물인 바이엘라이트, 도일라이트, 노드스트랜다이트로 발견됩니다.수산화알루미늄은 양성입니다. 즉, 염기성 및 산성 특성을 모두 갖습니다.수산화알루미늄, AlO(OH) 및 산화알루미늄 또는 알루미나(AlO)와23 밀접하게 관련되어 있으며, 산화알루미늄 또는 알루미나(AlO)도 양성입니다.이들 화합물은 알루미늄 광석 보크사이트의 주요 성분입니다.
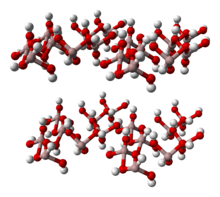
구조.
Al(OH)3은 두 [5][6]층 사이의 8면체 구멍의 3분의 2를 알루미늄 이온이 차지하는 두 층의 하이드록실기로 구성됩니다.4개의 다형이 [7]인식됩니다.모든 층은 8면체 수산화 알루미늄 유닛의 층을 특징으로 하며 층 사이에 수소 결합이 있습니다.다형은 층의 적층 측면에서 다릅니다.모든 형태의 Al(OH)3 결정은 육각형입니다[disputed ].
- 깁사이트는 γ-Al(OH)3 또는 α-Al(OH)3[citation needed]로도 알려져 있다.
- 바이어라이트는 α-Al(OH)3 또는 β-알루미나 삼수화물로도[citation needed] 알려져 있다
- 노드스트랜다이트는 Al(OH)3[8]이라고도 알려져 있다
- 도일라이트
하이드라길라이트는 한때 수산화알루미늄으로 여겨졌던 인산알루미늄이다.그럼에도 불구하고 깁사이트와 하이드라길라이트 모두 동일한 수산화알루미늄의 다형성을 나타내며 깁사이트는 미국에서 가장 일반적으로 사용되고 하이드라길라이트는 유럽에서 더 자주 사용된다.하이드라길라이트는 그리스어로 물(hydra)과 점토(argylles)를 따서 붙여졌다.
특성.
수산화알루미늄은 양성체이다.산에서는 브뢴스테드(Brönsted)로 작용한다.로우리 기지.산을 중화시켜 [9]소금을 생성합니다.
- 3 HCl + Al(OH)3 → AlCl3 + 32 HO
염기에서는 수산화 [9]이온과 결합함으로써 루이스산으로 작용합니다.
- Al(OH)3 + OH− → Al(OH)4−
생산.
상업적으로 사용되는 거의 모든 수산화 알루미늄은 최대 270°C(518°F)의 온도에서 수산화나트륨에 보크사이트를 용해하는 Bayer[10] 공정에 의해 제조됩니다.폐기물 고형물인 보크사이트를 제거하고 남은 알루민산나트륨 용액에서 수산화알루미늄을 침전시킵니다.이 수산화알루미늄은 소성을 통해 산화알루미늄 또는 알루미나로 변환할 수 있습니다.
잔류물 또는 보크사이트 미행물은 대부분 산화철이며 잔류 수산화나트륨으로 인해 부식성이 매우 높습니다.그것은 역사적으로 석호에 저장되었다; 이것은 2010년 헝가리에서 댐 붕괴로 9명이 익사하는 아즈카 알루미나 발전소 사고로 이어졌다.추가로 122명이 화학 화상에 대한 치료를 요청했다.이 진흙은 40평방 킬로미터(15평방 mi)의 땅을 오염시켰고 다뉴브 강에 도달했다.진흙은 중금속 함량이 낮아 무독성으로 간주되었지만 관련 슬러리는 pH가 [11]13이었다.
사용하다
난연성 필러
또한 수산화 알루미늄은 폴리머 용도의 난연성 필러로도 사용됩니다.무색(대부분의 폴리머와 마찬가지로)이며 저렴하고 내화성이 [12]우수하기 때문에 이러한 용도로 선택됩니다.수산화마그네슘과 헌타이트와 하이드로마그네사이트의 혼합물을 [13][14][15][16][17]동일하게 사용한다.약 180°C(356°F)에서 분해되어 상당한 양의 열을 흡수하고 수증기를 방출합니다.내화제로서 기능할 뿐만 아니라, 특히 폴리에스테르, 아크릴, 아세트산에틸렌비닐, 에폭시, 폴리염화비닐(PVC) 및 [18]고무 등 다양한 폴리머에서 매우 효과적입니다.
Al 화합물의 전구체
수산화알루미늄은 소성알루미늄, 황산알루미늄, 염화알루미늄, 염화알루미늄, 제올라이트, 알루민산나트륨, 활성알루미나 및 [6]질산알루미늄 화합물 제조를 위한 공급 원료입니다.
새로 침전된 수산화알루미늄은 겔을 형성하며, 이는 정수 시 응집제로 알루미늄 소금을 사용하는 기초가 됩니다.이 젤은 시간이 지남에 따라 결정화된다.수산화알루미늄 겔은 탈수(예를 들어 에탄올과 같은 수용성 비수성 용제 사용)되어 산에 쉽게 용해되는 비정질 수산화알루미늄 분말을 형성할 수 있습니다.가열하면 활성 알루미늄으로 변환되어 건조제, 가스 정화 흡착제 및 촉매 [12]지지체로 사용됩니다.
제약
일반명 "algeldrate"로 수산화알루미늄은 인간과 동물(주로 고양이와 개)에서 제산제로 사용된다.불용성인 Al(OH)3은 위의 pH를 7 이상으로 증가시키지 않기 때문에 위의 과잉산 분비를 유발하지 않기 때문에 중탄산나트륨과 같은 다른 대안보다 선호된다.브랜드명에는 Alu-Cap, Aludrox, Gaviscon 또는 Pepsamar가 포함됩니다.그것은 위 속의 과도한 산과 반응하여 위 [19][20]내용물의 산도를 감소시켜 궤양, 속쓰림, 소화불량 등의 증상을 완화시킬 수 있다.이러한 제품들은 변비를 일으킬 수 있는데, 왜냐하면 알루미늄 이온이 위장관의 평활근 세포의 수축을 억제하여 연동운동을 늦추고 대변이 [21]대장을 통과하는 데 필요한 시간을 연장시키기 때문이다.이러한 제품 중 일부는 균형잡힌 설사 [22]효과가 있는 수산화마그네슘 또는 탄산마그네슘을 등농도로 함유함으로써 그러한 효과를 최소화하도록 제조되었다.
이 화합물은 또한 신부전을 앓고 있는 사람들과 동물들의 과인산혈증(혈중 인산염, 즉 인의 수치 상승)을 조절하기 위해 사용된다.보통 신장은 혈액에서 과도한 인산염을 걸러내지만 신부전은 인산염을 축적시킬 수 있다.알루미늄 소금은 섭취할 때 장에서 인산염과 결합하고 [23][24]흡수될 수 있는 인의 양을 줄입니다.
침전된 수산화알루미늄은 일부 백신(예: 탄저균 백신)에 보조제로 포함된다.수산화 알루미늄 보조제의 잘 알려진 브랜드 중 하나는 Brenntag Biosector가 [25][full citation needed][dead link]만든 Alhydrogel입니다.단백질을 잘 흡수하기 때문에 보관 시 백신의 단백질이 침전되거나 용기 벽에 달라붙는 것을 막아 백신을 안정시키는 기능도 한다.수산화 알루미늄은 종종 "알룸"이라고 불리기도 하는데, 이는 일반적으로 여러 황산염 [citation needed]중 하나를 위한 용어이다.
수산화알루미늄을 함유한 백신 제제는 면역학적 위험 신호인 요산의 방출을 유도함으로써 면역체계를 자극한다.이것은 수상세포로 분화하는 특정 유형의 단구들을 강하게 끌어당긴다.수상세포는 항원을 포착해 림프절까지 운반해 T세포와 B세포를 [26]자극한다.그것은 좋은 Th2 반응의 유도에 기여하는 것으로 보여 항체에 의해 차단되는 병원균에 대한 면역에 유용하다.그러나 세포(Th1) 면역 반응을 자극하는 능력은 거의 없으며, 많은 [27]병원균으로부터 보호하는 데 중요하며, 항원이 펩타이드 [28]기반일 때는 유용하지 않습니다.
안전.
1960년대와 1970년대에는 알루미늄이 알츠하이머병을 [29][30]포함한 다양한 신경 질환과 관련이 있다고 추측되었다.그 이후 여러 역학 연구에서 환경적 또는 삼킨 알루미늄 및 신경학적 장애에 대한 노출 사이에 아무런 연관성도 발견되지 않았다. 그러나 주입된 알루미늄은 이러한 연구에서 [31][32][33]다루지 않았다.
신경 장애는 걸프전 질병(GWI)에 의해 동기부여된 생쥐를 대상으로 한 실험에서 발견되었다.미군에게 투여된 용량과 동등한 용량으로 주입된 수산화알루미늄은 반응성 성세포의 증가, 운동 뉴런의 아포토시스 증가, 척수와 [34]피질 내 미세아교 증식을 보였다.
레퍼런스
- ^ 용해도 제품의 경우:"Archived copy". Archived from the original on 15 June 2012. Retrieved 17 May 2012.
{{cite web}}: CS1 maint: 제목으로 아카이브된 복사(링크) - ^ 등전점의 경우:
- ^ Zumdahl, Steven S. (2009). Chemical Principles (6th ed.). Houghton Mifflin Company. ISBN 978-0-618-94690-7.
- ^ Black, Ronald A.; Hill, D. Ashley (15 June 2003). "Over-the-Counter Medications in Pregnancy". American Family Physician. 67 (12): 2517–2524. ISSN 0002-838X. PMID 12825840. Retrieved 1 July 2017.
- ^ Wells, A. F. (1975), Structural Inorganic Chemistry (4th ed.), Oxford: Clarendon Press
- ^ a b Evans, K. A. (1993). "Properties and uses of aluminium oxides and aluminium hydroxides". In A. J. Downs (ed.). Chemistry of aluminium, gallium, indium, and thallium (1st ed.). London; New York: Blackie Academic & Professional. ISBN 9780751401035.
- ^ Karamalidis, A. K.; Dzombak D. A. (2010). Surface Complexation Modeling: Gibbsite. John Wiley & Sons. pp. 15–17. ISBN 978-0-470-58768-3.
- ^ a b c Wefers, Karl; Misra, Chanakya (1987). Oxides and hydroxides of aluminum. Alcoa Research Laboratories. p. 2. OCLC 894928306.
- ^ a b Boundless (26 July 2016). "Basic and Amphoteric Hydroxides". Boundless Chemistry. Archived from the original on 22 August 2017. Retrieved 2 July 2017.
- ^ Hind, AR; Bhargava SK; Grocott SC (1999). "The Surface Chemistry of Bayer Process Solids: A Review". Colloids Surf Physiochem Eng Aspects. 146 (1–3): 359–74. doi:10.1016/S0927-7757(98)00798-5.
- ^ "Hungary Battles to Stem Torrent of Toxic Sludge". BBC News Website. 5 October 2010.
- ^ a b Hudson, L. Keith; Misra, Chanakya; Perrotta, Anthony J.; Wefers, Karl; Williams, F. S. (2000). "Aluminum Oxide". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a01_557.
- ^ Hollingbery, LA; Hull TR (2010). "The Fire Retardant Behaviour of Huntite and Hydromagnesite - A Review" (PDF). Polymer Degradation and Stability. 95 (12): 2213–2225. doi:10.1016/j.polymdegradstab.2010.08.019.
- ^ Hollingbery, LA; Hull TR (2010). "The Thermal Decomposition of Huntite and Hydromagnesite - A Review" (PDF). Thermochimica Acta. 509 (1–2): 1–11. doi:10.1016/j.tca.2010.06.012.
- ^ Hollingbery, LA; Hull TR (2012). "The Fire Retardant Effects of Huntite in Natural Mixtures with Hydromagnesite" (PDF). Polymer Degradation and Stability. 97 (4): 504–512. doi:10.1016/j.polymdegradstab.2012.01.024.
- ^ Hollingbery, LA; Hull TR (2012). "The Thermal Decomposition of Natural Mixtures of Huntite and Hydromagnesite" (PDF). Thermochimica Acta. 528: 45–52. doi:10.1016/j.tca.2011.11.002.
- ^ Hull, TR; Witkowski A; Hollingbery LA (2011). "Fire Retardant Action of Mineral Fillers" (PDF). Polymer Degradation and Stability. 96 (8): 1462–1469. doi:10.1016/j.polymdegradstab.2011.05.006.
- ^ Huber Engineered Materials. "Huber Non-Halogen Fire Retardant Additives" (PDF). Retrieved 3 July 2017.
- ^ Galbraith, A; Bullock, S; Manias, E; Hunt, B; Richards, A (1999). Fundamentals of pharmacology: a text for nurses and health professionals. Harlow: Pearson. p. 482.
- ^ Papich, Mark G. (2007). "Aluminum Hydroxide and Aluminum Carbonate". Saunders Handbook of Veterinary Drugs (2nd ed.). St. Louis, Mo: Saunders/Elsevier. pp. 15–16. ISBN 9781416028888.
- ^ Washington, Neena (2 August 1991). Antacids and Anti Reflux Agents. Boca Raton, FL: CRC Press. p. 10. ISBN 978-0-8493-5444-1.
- ^ Bill, Robert L. (1 September 2016). Clinical Pharmacology and Therapeutics for Veterinary Technicians - E-Book. Elsevier Health Sciences. p. 105. ISBN 9780323444026.
- ^ Plumb, Donald C. (2011). "Aluminum Hydroxide". Plumb's Veterinary Drug Handbook (7th ed.). Stockholm, Wisconsin; Ames, Iowa: Wiley. pp. 36–37. ISBN 9780470959640.
- ^ Lifelearn Inc. (1 November 2010). "Aluminum Hydroxide". Know Your Pet. Retrieved 30 June 2017.
- ^ "About Brenntag Biosector - Brenntag". brenntag.com. Retrieved 19 April 2018.
- ^ Kool, M; Soullié T; van Nimwegen M; Willart MA; Muskens F; Jung S; Hoogsteden HC; Hammad H; Lambrecht BN (24 March 2008). "Alum adjuvant boosts adaptive immunity by inducing uric acid and activating inflammatory dendritic cells". J Exp Med. 205 (4): 869–82. doi:10.1084/jem.20071087. PMC 2807488. PMID 18362170.
- ^ Petrovsky N, Aguilar JC (2004). "Vaccine adjuvants: current state and future trends". Immunology & Cell Biology. 82 (5): 488–96. doi:10.1111/j.0818-9641.2004.01272.x. PMID 15479434. S2CID 154670.
- ^ Cranage, MP; Robinson A (2003). Robinson A; Hudson MJ; Cranage MP (eds.). Vaccine Protocols - Volume 87 of Methods in Molecular Medicine Biomed Protocols (2nd ed.). Springer. p. 176. ISBN 978-1-59259-399-6.
- ^ "Alzheimer's Myth's". Alzheimer's Association. Retrieved 29 July 2012.
- ^ Khan, A (1 September 2008). "Aluminium and Alzheimer's disease". Alzheimer's Society. Archived from the original on 11 March 2012. Retrieved 8 March 2012.
- ^ Rondeau V (2002). "A review of epidemiologic studies on aluminum and silica in relation to Alzheimer's disease and associated disorders". Rev Environ Health. 17 (2): 107–21. doi:10.1515/REVEH.2002.17.2.107. PMC 4764671. PMID 12222737.
- ^ Martyn CN, Coggon DN, Inskip H, Lacey RF, Young WF (May 1997). "Aluminum concentrations in drinking water and risk of Alzheimer's disease". Epidemiology. 8 (3): 281–6. doi:10.1097/00001648-199705000-00009. JSTOR 3702254. PMID 9115023. S2CID 32190038.
- ^ Graves AB, Rosner D, Echeverria D, Mortimer JA, Larson EB (September 1998). "Occupational exposures to solvents and aluminium and estimated risk of Alzheimer's disease". Occup Environ Med. 55 (9): 627–33. doi:10.1136/oem.55.9.627. PMC 1757634. PMID 9861186.
- ^ Shaw, Christopher A.; Petrik, Michael S. (November 2009). "Aluminum hydroxide injections lead to motor deficits and motor neuron degeneration". Journal of Inorganic Biochemistry. 103 (11): 1555–1562. doi:10.1016/j.jinorgbio.2009.05.019. ISSN 1873-3344. PMC 2819810. PMID 19740540.





