갑상선
Thyroid| 갑상선 | |
|---|---|
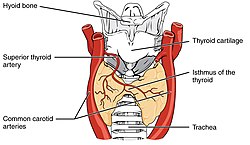 앞에서 본 인간의 갑상선(탄), 그리고 분비선을 공급하는 동맥(빨간색). | |
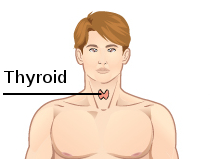 갑상선은 목, 아담의 사과 아래에 위치한다. | |
| 세부 사항 | |
| 발음 | /ˈθaɪrɔɪd/ |
| 전구체 | 갑상선 게실증(두 번째 인두 아치로 내측 확장) |
| 시스템 | 내분비계 |
| 동맥 | 갑상선, 하등 갑상선 동맥 |
| 정맥 | 상, 중, 하 갑상선 정맥 |
| 식별자 | |
| 라틴어 | 티레오아이데아목 |
| 메슈 | D013961 |
| TA98 | A11.3.00.001 |
| TA2 | 3863 |
| FMA | 9603 |
| 해부학적 용어 | |
갑상선, 즉 갑상선은 척추동물의 내분비선이다.인간에서 그것은 목 안에 있고 두 개의 연결된 로브로 구성되어 있다.로브의 3분의 2는 갑상선 이스트머스라고 불리는 얇은 조직 띠로 연결되어 있다.갑상선은 목 앞쪽, 아담의 사과 아래에 위치한다.현미경으로 보면 갑상선의 기능단위는 모낭세포(시세포)가 줄지어 있는 구형 갑상선 모낭이며, 콜로이드를 함유한 루멘을 둘러싸고 있는 간혹 파라폴릭세포가 있다.갑상선은 세 가지 호르몬인 삼디오도티로닌(T)과 티록신(T34)을 분비하고 펩타이드 호르몬인 칼시토닌을 분비한다.갑상선 호르몬은 신진대사율과 단백질 합성에 영향을 미치며, 어린이의 경우 성장과 발육에 영향을 미친다.칼시토닌은 칼슘의 동태현상에 역할을 한다.[1]두 갑상선 호르몬의 분비는 전방 뇌하수체에서 분비되는 갑상선 자극 호르몬(TSH)에 의해 조절된다.TSH는 시상하부에서 생성되는 티로트로핀 방출 호르몬(TRH)에 의해 조절된다.[2]
갑상선은 3-4주 동안 잉태할 때 혀의 밑부분에 있는 인두의 바닥에서 발달한다. 그리고 나서 인두 내장 앞에 내려가고, 궁극적으로 다음 몇 주 동안 목 밑까지 이동한다.이주하는 동안, 갑상선은 좁은 운하인 흉선 관에 의해 혀와 연결된 상태를 유지한다.다섯 번째 주가 끝나면 흉선관(Tyroglossal duct)이 퇴화하며, 이후 2주 동안 분리된 갑상선은 최종 위치로 이동한다.
에우티로이드(Euthyroid)는 신체의 정상적인 갑상선 기능 상태를 설명하는 데 사용되는 용어다.갑상선 질환으로는 갑상선기능저하증, 갑상선염증(갑상선기능저하증), 갑상선확대증(갑상선기능저하증), 갑상선결절, 갑상선암 등이 있다.갑상선 항진증은 갑상선 호르몬이 과도하게 분비되는 것이 특징인데, 가장 흔한 원인은 자가면역 장애 그레이브스병이다.갑상선 기능저하증은 갑상선 호르몬의 분비가 부족한 것이 특징이다. 가장 흔한 원인은 요오드 결핍이다.요오드가 결핍된 지역에서는 요오드 결핍에 따른 갑상선 기능저하증이 어린이들에게 예방 가능한 지적 장애의 주요 원인이다.[3]요오드가 충분한 지역에서 갑상선 기능저하증의 가장 흔한 원인은 하시모토의 갑상선염이다.
갑상선의 존재와 그 여러 가지 질병은 비록 글랜드 자체가 르네상스 시대부터 서술되고 이름만 붙여졌을 뿐이지만 수세기 동안 지적되고 치료되어 왔다.[4]갑상선에 대한 지식, 갑상선의 생화학, 그리고 갑상선의 장애는 19세기 말과 20세기에 걸쳐 발달했다.20세기 중반에 걸쳐 많은 현대적인 치료와 조사 양식이 진화했는데, 여기에는 고트레 치료를 위한 갑상선 제거(시내항절제술) 수술 기법의 정교화, 그레이브스 질환 치료를 위한 방사성 요오드와 티오라실 사용, 갑상선 결절 진단을 위한 미세한 바늘 흡인 등이 포함된다..[4]
구조
특징들
갑상선은 좌우의 두 개의 로브로 구성된 나비 모양의 기관으로, 좁은 조직 띠로 연결되어 '이스트머스'[5]라고 불린다.성인의 무게는 25g으로 각엽의 길이는 약 5cm, 폭은 3cm, 두께는 2cm이며, 이두근은 높이와 폭이 약 1.25cm이다.[5]분비선은 보통 남성보다 여성이 더 크고, 임신 중에는 크기가 커진다.[5][6]
갑상선은 목 앞쪽 가까이에 있으며, 후두와 기관 앞쪽에 기대어 누워 있다.[5]갑상선 연골과 크라이코이드 연골은 아담의 사과 바로 아래, 분비선 바로 위에 놓여 있다.이스트무스는 기관지의 두 번째 고리에서 세 번째 고리로 확장되는데, 가장 윗부분이 갑상선 연골까지 확장되고, 네 번째에서 여섯 번째까지의 기관 고리를 중심으로 가장 아랫부분이 확장된다.[7]적외선근은 분비선 앞에, 선미도마스토이드근은 옆으로 눕는다.[8]갑상선의 외측 날개 뒤에는 두 개의 경동맥이 놓여 있다.기관지, 후두, 하부 인두, 식도 모두 갑상선 뒤에 있다.[6]이 지역에서는 재발성 후두신경과[9] 하갑상선동맥이 인대 옆이나 안쪽으로 통과한다.[10]전형적으로 갑상선엽 뒤쪽에 갑상선 캡슐의 두 층 사이에 양쪽에 각각 두 개의 부갑상선(parathyroid)이 놓여 있다.[5]
갑상선은 얇은 섬유질의 캡슐로 덮여 있는데,[5] 이 캡슐은 내측과 외측층을 가지고 있다.내층은 분비되어 분비되어 갑상선 조직을 미세한 로브로 나누는 셉타를 형성한다.[5]외층은 전근막막과 연속하여, 베리의 인대라고도 알려진 갑상선의 후근막 인대를 형성하기 위해 페시아를 두껍게 하여 크라이코이드와 갑상선 장갑판에[6] 글랜드를 부착한다.[6]이것은 삼킬 때 갑상선이 위아래로 움직이게 한다.[6]
혈액, 림프 및 신경 공급
갑상선은 외부 경동맥의 한 가지인 상급 갑상선동맥과 흉선동맥의 한 가지인 하급 갑상선동맥으로부터 동맥혈이 공급되며, 때로는 해부학적 변형에 의해 갑상선 이미동맥의 혈액이 공급되는데,[5] 이것은 가변적 기원을 가지고 있다.[11]우량 갑상선 동맥은 갑상선을 공급하는 전·후방으로 갈라지고, 하급 갑상선 동맥은 상·하급 분기로 갈라진다.[5]상하의 갑상선동맥과 하의 갑상선동맥은 갑상선엽의 외측부 뒤에 함께 결합한다.[11]정맥혈은 상갑상선과 중간 갑상선 정맥을 통해 배출되는데, 이 정맥은 내부 경정맥으로, 하갑상선 정맥을 통해 배출된다.하급 갑상선 정맥은 정맥의 네트워크에서 유래하여 좌우 대뇌수두 정맥으로 흘러 들어간다.[5]동맥과 정맥 모두 갑상선의 캡슐의 두 층 사이에 플렉서스를 형성한다.[11]
림프 배수는 원장 림프절(isthmus 바로 위에 위치)과 전치 및 근치 림프절을 통과하는 경우가 많다.[5]글랜드는 교감 줄기의 상부, 중하부 경추골절로부터 교감신경을 공급받는다.[5]그샘은 우월한 후두신경과 재발하는 후두신경으로부터 부교감신경을 공급받는다.[5]
변형
갑상선의 크기와 모양, 내장된 부갑상선 위치에는 많은 변형이 있다.[6]
때때로 피라미드 로브라고 불리는 세 번째 로브가 있다.[6]이 로브는 종종 갑상선 이스트무스에서 나오는 효이드 뼈까지 늘어나며 1개에서 몇 개의 분열된 로브일 수 있다.[5]이 로브의 존재는 보고된 연구에서 18.3%에서 44.6%[13]에 이른다.[12]왼쪽에서 더 자주 발생하며 때때로 분리되는 것으로 나타났다.[12]피라미드 로브는 랄루엣의 피라미드로도 알려져 있다.[14]피라미드 로브는 갑상선이 하강하는 동안 주로 낭비되는 흉선관(tyroglossal duct)의 잔해다.[6]작은 부속품 갑상선은 사실 혀의 포아멘 세쿰에서 성인의 갑상선 위치까지 흉선 관을 따라 어디에서나 발생할 수 있다.[5]갑상선엽 뒤쪽에 있는 작은 뿔로, 대개 재발성 후두신경과 하두 갑상선동맥에 가까운 것을 주커칸델의 결핵이라고 한다.[10]
다른 변형으로는 갑상선의 레베레이터 근육, 이스트무스를 효이드 뼈의 몸체에 연결하는 것,[6] 그리고 작은 갑상선 이미아 동맥의 존재 등이 있다.[6]
미세조영술

미시적 수준에서는 갑상선의 세 가지 주요 특징이 있는데, 1664년 제퍼리 웨스터슨이 처음 발견한 것은 사람, 모낭 세포, 파라폴릭 세포다.[15]
- 모낭
갑상선 모낭은 갑상선 기능에서 주 역할을 하는 지름이 0.02~0.9mm인 작은 구형의 세포군이다.[5]이들은 풍부한 혈액 공급과 신경, 임파선 존재를 가진 림으로 구성되어 있으며, 주로 요오드화 당단백질인 티로글로불린이라 불리는 갑상선 호르몬 전구 단백질로 구성된 콜로이드의 핵심을 둘러싸고 있다.[5][16]
- 엽세포
모낭의 핵은 모낭 세포의 단층으로 둘러싸여 있다.갑상선 자극호르몬(TSH)에 자극을 받으면 갑상선 호르몬 T3와 T4를 분비한다.그들은 콜로이드에 함유된 티로글로불린을 운반하고 대사함으로써 이것을 한다.[5]엽상세포는 얼마나 활동적인지에 따라 평면형부터 입체형, 주상형까지 형태가 다양하다.[5][16]
- 파라폴리스 세포
모낭 세포와 구형 모낭 사이의 공간에 흩어져 있는 다른 형태의 갑상선 세포인 파라폴릭 세포도 있다.[5]이 세포들은 석회질(calcitonin)을 분비하기 때문에 C세포라고도 불린다.[17]
개발
배아의 발달에서 임신 3~4주차에 갑상선은 투베르쿨룸 임팔선과 코풀라 언어 사이의 혀 밑바닥 인두 바닥에 상피 증식하는 것으로 나타난다.코풀라는 후에 포아멘 체쿰이 가리키는 지점에서 곧 저선인두의 고지에[18] 의해 덮이게 된다.그리고 나서 갑상선은 흉곽을 통해 편심된 게실처럼 인두 내장 앞으로 내려간다.그 다음 몇 주 동안, 그것은 목의 밑부분까지 이동하며, 효이드 뼈 앞을 통과한다.이주하는 동안, 갑상선은 좁은 운하인 흉선 관에 의해 혀와 연결된 상태를 유지한다.다섯 번째 주가 끝나면 흉선관(Tyroglossal duct)이 퇴화하며, 이후 2주 동안 분리된 갑상선은 최종 위치로 이동한다.[18]
태아 시상하부와 뇌하수체는 티로트로핀 방출 호르몬(TRH)과 갑상선 자극 호르몬(TSH)을 분비하기 시작한다.TSH는 11주에 처음 측정할 수 있다.[19]18-20주까지, 티록신(T4)의 생산은 임상적으로 중요하고 자급자족 수준에 도달한다.[19][20]태아삼디오도로닌(T3)은 30주까지 15ng/dL 미만으로 낮은 상태를 유지하며, 전기에 50ng/dL로 증가한다.[20]태아는 모성 갑상선 기능저하증에서 생길 수 있는 신경발달장애를 경계하기 위해 갑상선 호르몬을 자급자족할 필요가 있다.[21]건강한 신경발달을 위해서는 충분한 요오드의 존재가 필수적이다.[22]
칼시토닌의 생성을 담당하는 C세포라고도 알려진 신경내분비 파라폴릭셀은 전굿 내분비에서 유래한다.갑상선의 이 부분은 처음에는 복측 네 번째 인두 주머니에서 시작하여 최종 위치로 하강하는 동안 원시 갑상선에 합류하는 최후통첩성 갑상선으로 형성된다.[23]
태아발달에 이상이 생기면 선천성 갑상선 기능저하증을 일으킬 수 있는 다양한 형태의 갑상선 이상증세가 나타날 수 있으며, 이를 치료하지 않으면 크레틴증(cretinism)이 발생할 수 있다.[19]
함수
갑상선호르몬
갑상선의 주요 기능은 요오드를 함유한 갑상선 호르몬인 삼오도티로닌(T3)과 티록신(T4)과 펩타이드 호르몬인 칼시토닌의 생성이다.[24]갑상선 호르몬은 요오드와 티로신에서 생성된다.T는3 분자당 3개의 요오드 원자를 포함하고 T는4 분자당 4개의 요오드 원자를 포함하고 있기 때문에 그렇게 이름이 붙여졌다.[25]갑상선 호르몬은 인체에 미치는 영향의 범위가 넓다.여기에는 다음이 포함된다.
- 대사.갑상선 호르몬은 기초대사율을 높이고 거의 모든 신체조직에 영향을 미친다.[26]식욕, 물질의 흡수, 장 운동성은 모두 갑상선 호르몬의 영향을 받는다.[27]그것들은 내장의 흡수, 생성, 세포에 의한 흡수, 포도당의 파괴를 증가시킨다.[28]그것들은 지방의 분해를 자극하고, 자유지방산의 수를 증가시킨다.[28]자유지방산이 증가함에도 불구하고, 갑상선 호르몬은 담즙에서 콜레스테롤의 분비율을 증가시킴으로써 콜레스테롤 수치를 감소시킨다.[28]
- 심혈관.호르몬은 심장 박동의 속도와 강도를 증가시킨다.그들은 호흡, 섭취, 산소 소비율을 증가시키고 미토콘드리아의 활동을 증가시킨다.[27]이러한 요소들을 종합하면 혈류와 체온이 높아진다.[27]
- 발달하다.갑상선 호르몬은 정상적인 발달을 위해 중요하다.[28]그것들은 젊은이들의 성장률을 증가시키며,[29] 발달하는 뇌의 세포는 갑상선 호르몬 T와3 T의4 주요 대상이다.갑상선 호르몬은 태아 발달과 산후 수[28] 년 동안의 뇌 성숙에 특히 중요한 역할을 한다.
- 갑상선 호르몬은 정상적인 성기능, 수면, 사고 패턴을 유지하는 역할도 한다.증가된 수준은 사고 생성 속도는 증가하지만 집중력은 감소하는 것과 관련이 있다.[27]성욕과 정상적인 월경 주기의 유지를 포함한 성기능은 갑상선 호르몬의 영향을 받는다.[27]
분비 후 갑상선 호르몬 중 극히 일부만이 혈액 내에서 자유롭게 이동한다.대부분은 티록신 바인딩 글로불린(약 70%), 트란스히레틴(10%), 알부민(15%)[30]에 묶여 있다.자유롭게 여행하는4 T의 0.033%, T의 0.3%만이 호르몬 활동을 한다.[31]또한 혈액 내 T의3 85%까지 요오드화합물(요오드화합물)에 의한 T로부터의4 전환에 따른 혈액 내 T의 최대 85%가 생성된다.[24]
갑상선호르몬은 세포막을 건너 세포내 핵 갑상선호르몬 수용체 TR-α12, TR-β1, TR-β에2 결합하여 작용하며 호르몬 반응요소 및 전사인자와 결합하여 DNA 전사를 조절한다.[31][32]갑상선 호르몬은 DNA에 대한 이러한 작용 외에도 ATPase 칼슘, 아데닐 사이클라아제, 포도당 전달체 등 효소와의 반응을 통해 세포막이나 세포질 내에서 작용하기도 한다.[19]
호르몬 생성

- Tyroglobulin은 거친 내포성 망막에서 합성되어 분비 경로를 따라 갑상선 모낭의 루멘에 있는 콜로이드로 들어간다.
- 한편, 나트륨-요오드화(Na/I) 심포터는 요오드화−(I)를 세포에 활발하게 펌프하는데, 이는 이전에 대부분 알려지지 않은 메커니즘에 의해 내피질을 건넜다.
- 이 요오드화물은 세포질에서 전달체 펜드린에 의해 모낭 루멘으로 들어간다고 알려져 있다.
- 콜로이드에서는 갑상선 과산화효소라는 효소에 의해 요오드(I−)가 요오드(I0)로 산화된다.
- 요오드(I0)는 반응성이 매우 뛰어나며, 단백질 체인의 티로실 잔류물(총 약 120개의 티로실 잔류물 포함)에서 티로글로불린을 요오드화한다.
- 결합 시 인접한 티로실 잔류물이 서로 짝을 이룬다.
- 복합체 전체가 내분비증에 의해 모낭세포를 재진입한다.
- 다양한 프로테아제들에 의한 프로테롤리시스는 티록신 분자와 트리오도티로닌 분자를 해방시켜주며, 이는 대부분 알려지지 않은 메커니즘에 의해 혈액 속으로 들어온다.
갑상선 호르몬은 티로글로불린으로부터 생성된다.이것은 원래 모낭세포의 거친 내포체성 망막 안에서 생성되어 모낭성 루멘으로 운반되는 모낭성 루멘의 콜로이드 내 단백질이다.티로글로불린은 123단위의 티로신을 함유하고 있는데, 티로신은 모낭 내 요오드와 반응한다.[34]
요오드는 갑상선 호르몬의 생성을 위해 필수적이다.요오드(I0)는 혈액 속에서 요오드화(I−)로 이동하며, 나트륨-요오드화 시모포터에 의해 모낭세포로 흡수된다.이것은 세포막의 이온 채널로, 같은 작용으로 두 개의 나트륨 이온과 한 개의 요오드 이온을 세포로 전달한다.[35]그리고 나서 요오드화물은 세포 안에서 요오드화염소 항정신병인 펜드린의 작용을 통해 루멘으로 이동한다.엽록체 루멘에서 요오드화물은 그 후 요오드로 산화된다.이것은 그것을 더욱 반응하게 만들고,[33] 요오드는 갑상선 과산화효소에 의해 티로글로불린의 활성 타이로신 단위에 부착된다.이것은 갑상선 호르몬인 모노오도티로신(MIT)과 디오도티로신(DIT)의 전구체를 형성한다.[2]
모낭세포가 갑상선 자극 호르몬에 자극을 받으면 모낭세포가 모낭 루멘에서 티로글로불린을 재흡수한다.요오드화 티로진은 분해되어 갑상선 호르몬 T4, T, DIT3, MIT, MIT를 형성하며 역삼오도로닌의 흔적을 형성한다.T와3 T는4 혈액 속으로 방출된다.분비샘에서 분비되는 호르몬은 약 80~90% T4, 약 103~20% T이다.[36][37]말초조직의 디오디나아제 효소는 MIT와 DIT에서 요오드를 제거하고 T와43 RT로3. 변환한다. 이것은 말초조직의 RT3(95%), T3(87%)를 모두 일으키는 주요 공급원이다.[38]
규정
티록신과 삼디오도티로닌의 생산은 주로 전뇌하수체에서 분비되는 갑상선 자극 호르몬(TSH)에 의해 조절된다.차례로 TSH 방출은 시상하부에서 맥동적으로 분비되는 티로트로핀 방출 호르몬(TRH)에 의해 자극을 받는다.[39]갑상선 호르몬은 갑상선 호르몬이 높을 때 TSH 생산을 억제하는 등 흉선 호르몬인 TSH와 TRH에 부정적인 피드백을 제공한다.이러한 부정적인 피드백은 TSH의 수준이 높을 때 발생하여 TRH 생산을 억제한다.[40]
TRH는 열 발생을 촉진하기 위해 저온 노출과 같은 상황에서 증가된 속도로 분비된다.[41]갑상선 호르몬의 존재에 의해 억제될 뿐만 아니라, TSH 생산은 도파민, 소마토스타틴, 글루코코르티코이드에 의해 무뎌진다.[42]
칼시토닌
갑상선은 또한 혈중 칼슘 수치를 조절하는 데 도움을 주는 칼시토닌 호르몬을 생성한다.파라폴리스 세포는 높은 혈중 칼슘에 반응하여 캘시토닌을 생성한다.칼시토닌은 뼈를 분해하는 세포인 골수세포의 활동을 줄임으로써 뼈에서 칼슘의 방출을 감소시킨다.뼈는 골수성형에 의해 끊임없이 재흡수되고 골수성형에 의해 생성되기 때문에 칼시토닌은 칼슘의 뼈로의 이동을 효과적으로 자극한다.캘시토닌의 효과는 부갑상선에서 생성되는 부갑상선호르몬(PST)과는 정반대다.그러나 칼슘대사는 갑상선 제거(시내항절제술) 후에도 임상적으로 정상으로 유지되지만 부갑상선에는 그렇지 않기 때문에 칼시토닌은 PTH보다 훨씬 덜 필수적으로 보인다.[43]
유전자와 단백질 표현
약 2만 개의 단백질 코딩 유전자가 인간의 세포에서 발현된다: 이러한 유전자의 70%는 갑상선 세포에서 발현된다.[44][45]이 중 250개의 유전자는 갑상선에서 더 구체적으로 표현되며, 약 20개의 유전자는 갑상선 특이성이 높다.엽상세포에서, 이러한 유전자에 의해 합성된 단백질은 갑상선 호르몬 합성을 직접 한다. - 시로글로불린, TPO, IYD. 그리고 파라폴릭콜라 c-세포에서, 그들은 캘시토닌 합성을 지시한다.CALCA, CALCB.
임상적 유의성
갑상선 질환의 치료법을 파악하고 감시하는 역할을 일반 전문의와 내과 전문의들이 맡는다.내분비학자와 갑상선학자는 갑상선 전문의다.갑상선 질환의 외과적 관리는 갑상선 외과 의사나 이비인후과 의사가 담당한다.
기능 장애
갑상선항진증
갑상선 호르몬의 과도한 생산을 갑상선 항진증이라고 한다.원인은 Graves병, 독성 다항체 gottre, 독성 다항체, 갑상선 선종, 염증, 그리고 과도한 TSH를 분비하는 뇌하수체 선종이다. 또 다른 원인은 약물 아미오다론에 의해 유발되거나 요오드화 대조영상에 따른 과도한 요오드 가용성이다.[46][47]
갑상선기능항진증은 체중감소, 식욕증진, 불면증, 열에 대한 내성 저하, 떨림, 두근거림, 불안감, 신경과민 등 다양한 비특이성 증상을 유발하는 경우가 많다.어떤 경우에는 흉통, 설사, 탈모, 근육 약화를 일으킬 수 있다.[48]이러한 증상은 베타 차단제와 같은 약물로 일시적으로 관리할 수 있다.[49]
갑상선 항진증의 장기적 관리에는 프로필티오우라실, 카르비마졸, 메티마졸 등 갑상선 기능을 억제하는 약물이 포함될 수 있다.[50]그 대신에 방사성 요오드-131은 갑상선 조직을 파괴하는 데 사용될 수 있다: 방사성 요오드는 갑상선 세포에 의해 선택적으로 흡수되며, 이는 시간이 지남에 따라 그들을 파괴한다.선택된 1차 치료는 개인과 치료 대상 국가에 따라 달라진다.갑상선을 제거하는 수술은 최소 침습적 시술인 경구상 갑상선 절제술로 가끔 시행될 수 있다.[51]그러나 수술은 부갑상선 손상과 성대를 내향적으로 만드는 재발 후두신경 손상 위험을 안고 있다.갑상선 전체를 제거하면 갑상선 기능저하증이 불가피해 갑상선 호르몬 대체제가 필요하다.[52][49]
갑상선기능저하증
갑상선 기능 부진은 갑상선 기능저하증을 초래한다.대표적인 증상으로는 비정상적인 체중 증가, 피로감, 변비, 심한 월경 출혈, 탈모, 냉소불내증, 느린 심박수 등이 있다.[48]요오드결핍은 세계적으로 갑상선기능저하증의 가장 흔한 원인이고,[53] 자가면역질환 하시모토의 갑상선염은 선진국에서 가장 흔한 원인이다.[54]그 밖의 원인으로는 선천성 이상, 일시적인 염증을 일으키는 질환, 갑상선의 외과적 제거나 전파 절제, 약물 아미오다론과 리튬, 아밀로이드증, 사르코이드증 등이 있다.[55]갑상선 기능저하증의 어떤 형태는 근저하증을 유발할 수 있고 심한 경우는 근저하 혼수상태에 빠질 수 있다.[56]
갑상선 기능저하증은 갑상선 호르몬을 대체해 관리한다.이것은 보통 구강 보충제로서 매일 주어지며, 효과가 나타나는데 몇 주가 걸릴 수도 있다.[56]산후 갑상선염, 아급성 갑상선염과 같은 갑상선 기능 저하증의 일부 원인은 일시적인 것일 수 있고 시간이 흐르면서 지나갈 수 있으며 요오드 결핍과 같은 다른 원인도 식이 보충으로 고칠 수 있을 것이다.[57]
질병.
그레이브스병
그레이브스병은 갑상선 항진증의 가장 흔한 원인인 자가면역 장애다.[58]그레이브스병에서는 알 수 없는 이유로 갑상선 자극 호르몬 수용체에 대항하여 자가 항균이 발병한다.이 항체들은 수용체를 활성화하여 괴혈병의 발육과 열불내증, 체중감소, 설사, 두근거림과 같은 갑상선항진증의 증상으로 이어진다.때때로 그러한 항체는 수용체를 차단하지만 활성화하지 못하여 갑상선 기능저하증과 관련된 증상을 초래한다.[58]또 정강이의 앞부분이 부풀어 오를 수 있으므로 그레이브스 안과증이라 불리는 눈의 점진적인 돌출이 발생할 수 있다.[58]그레이브스병은 눈과 정강이 관여되거나 자가 항정신병(Autoantiby)이 분리되는 등 병리학적 특징이 있거나 방사선방사선 흡수 스캔의 결과로 진단할 수 있다.그레이브스병은 프로필티오우라실 등 항시하이드로이드제로 치료해 갑상선 호르몬의 생성을 감소시키지만 재발률이 높다.눈에 관여하지 않는 경우, 글랜드를 수축시키기 위해 방사성 동위원소를 사용하는 것이 고려될 수 있다.후속 갑상선 호르몬 교체를 통한 글랜드의 수술적 제거는 고려될 수 있지만, 이것이 눈이나 피부와 관련된 증상을 조절하지는 못할 것이다.[58]
결절
갑상선 결절은 종종 글랜드에서 발견되는데, 4-7%[59]의 유병률을 보인다.결절의 대다수는 어떠한 증상도 일으키지 않으며 갑상선 호르몬 분비가 정상이며 비암이다.[60]암이 아닌 경우로는 단순 낭종, 콜로이드 결절, 갑상선 아데노마 등이 있다.악성 결절은 결절의 약 5%에서만 발생하는 것으로 다른 부위의 모낭, 유두, 중암, 전이 등이 포함된다. 결절은 여성, 방사선에 노출된 사람, 요오드가 결핍된 사람 등에서 발생할 가능성이 더 높다.[59]
결절이 있을 때 갑상선 기능 검사를 통해 결절이 과잉 갑상선 호르몬을 분비해 갑상선 항진증을 유발하는지 여부를 판단한다.[60]갑상선 기능 검사가 정상일 때는 초음파를 이용해 결절을 조사하는 경우가 많은데, 결절이 유체충전인지 고체질량인지, 외관상으로는 양성암이나 악성암을 암시하는지 등의 정보를 제공한다.[59]그런 다음 바늘 흡인 생검을 수행할 수 있으며, 샘플은 세포의 외관을 관찰하여 정상 세포와 암세포가 닮았는지 여부를 결정한다.[61]
복수의 결절이 존재하는 것을 다항성괴석이라고 하며, 갑상선항진증과 관련이 있다면 독성 다항괴석이라고 한다.[61]
고트레
확대된 갑상선은 gottre라고 불린다.[62]괴사병은 약 5%의 사람들에게 어떤 형태로든 존재하며 [61]요오드결핍, 자가면역질환(그레이브스병, 하시모토 갑상선염 모두), 감염, 염증, 사코이데시스, 아밀로이데시스 등 침투성 질병 등 다량의 원인의 결과물이다.때때로 "단순한 구트레"라고 불리는 상태를 원인을 찾을 수 없다.[63]
어떤 형태의 괴짜는 고통과 관련이 있는 반면, 많은 것들은 어떠한 증상도 일으키지 않는다.확대된 궤도는 갑상선의 정상 위치를 넘어 기도나 식도 주변, 흉골 아래까지 확장될 수 있다.[61]갑상선은 갑상선 기능 항진증 또는 갑상선 기능 항진증과 관련이 있을 수 있으며, 갑상선 기능 항진증은 갑상선의 근본적인 원인과 관련이 있을 수 있다.[61]갑상선 기능 검사는 괴뢰의 원인과 영향을 조사하기 위해 실시될 수 있다.gitre의 근본적인 원인은 치료할 수 있지만, 관련 증상이 없는 많은 giter들은 단순히 모니터링된다.[61]
염증
갑상선의 염증은 갑상선염이라고 하며 갑상선기능항진증이나 갑상선기능항진증의 증상을 일으킬 수 있다.갑상선염에는 초기에 갑상선 기능 항진증이 나타나며, 갑상선 기능 항진증 기간인 하시모토의 갑상선염과 산후 갑상선 기능 항진증이 뒤따르는 경우도 있다.그 밖에 갑상선에 염증을 일으키는 질환이 있으며, 여기에는 아급성 갑상선염, 급성 갑상선염, 무성 갑상선염, 리델의 갑상선염, 외상성 상해 등이 있으며, 여기에는 구개성 갑상선염을 포함한다.[64]
하시모토 갑상선염은 갑상선이 림프구 B세포와 T세포에 의해 침투되는 자가면역질환이다.이것들은 점차적으로 갑상선을 파괴한다.[65]이렇게 해서 하시모토의 갑상선염은 음흉하게 일어났을 수도 있고, 갑상선 호르몬 생성량이 감소하여 갑상선기능저하 증세를 일으킬 때만 눈에 띈다.[65]하시모토는 남성보다 여성에게서 더 흔하고, 60세 이후에는 훨씬 더 흔하며, 유전적 위험 요인을 알고 있다.[65]또한 하시모토 갑상선염을 앓고 있는 개인에게 더 흔하게 나타나는 것은 제1형 당뇨병, 치명적 빈혈증, 애디슨병 비틸리고 등이다.[65]
산후 갑상선염은 출산 후 일부 여성에게서 발생한다.분만 후, 글랜드가 염증을 일으키게 되고 그 상태는 갑상선기능저하증과 보통 정상기능으로의 복귀가 뒤따르는 갑상선기능항진증의 기간을 처음에 나타낸다.[66] 그 질병의 경과는 수개월에 걸쳐 일어나며, 고통 없는 괴짜가 특징지어진다.갑상선 과산화효소에 대한 항체는 검사에서 찾을 수 있다.갑상선 기능저하증 시기에는 갑상선 호르몬 교체가 필요할 수 있지만 대개 치료 없이 염증이 해소된다.[66]
암
갑상선에 영향을 미치는 가장 흔한 신엽은 양성선종이며, 대개 목의 무통질량으로 나타난다.[67]악성 갑상선암은 C세포와 임파선 암 등 갑상선이 구성하는 모든 조직에서 암이 발생할 수 있지만 가장 많이 발생하는 암이다.다른 부위의 암도 갑상선에 거의 머무르지 않는다.[67]머리와 목의 방사선은 갑상선암의 위험요인을 나타내며 암은 남성보다 여성에게 더 흔해 약 2:1의 비율로 발생한다.[67]
대부분의 경우 갑상선암은 목에 통증이 없는 덩어리로 나타난다.갑상선암이 다른 증상과 함께 나타나는 것은 매우 드문 일이지만, 어떤 경우에는 암이 갑상선 항진증을 일으킬 수도 있다.[68]악성 갑상선암은 대부분 유두종이며, 모낭, 중상, 갑상선 림프종이 그 뒤를 잇고 있다.[67][68]갑상선의 두드러기 때문에 암이 결절의 원인으로 질병 진행 초기에 발견되는 경우가 많은데, 이는 미세한 염원을 겪을 수도 있다.갑상선 기능 검사는 결절이 과도한 갑상선 호르몬을 생성하는지 여부를 밝혀내는 데 도움이 될 것이다.방사성 요오드 흡수 테스트는 암과 전이체의 활동과 위치를 밝혀내는 데 도움을 줄 수 있다.[67][69]
갑상선암은 갑상선 전체 또는 일부를 제거하여 치료한다.방사성 요오드-131은 갑상선을 방사선을 제거하기 위해 제공될 수 있다.티록신은 TSH가 재발을 자극할 수 있기 때문에 손실된 호르몬을 대체하고 TSH 생산을 억제하기 위해 투여된다.[69]예후가 매우 좋지 않은 희귀한 과민성 갑상선암을 제외하면 대부분의 갑상선암은 예후가 뛰어나 치료 가능한 것으로까지 볼 수 있다.[70]
선천적
지속적인 혈당관(tyroglossal duct)은 갑상선의 가장 흔한 임상적으로 중요한 선천적 결함이다.지속적인 축농증은 갑상샘의 관형 발달의 잔재물로 남을 수 있다.이 관의 일부분은 소실되어 작은 조각들이 흉선 낭종을 형성하게 할 수 있다.[23]임신 전 신생아는 갑상선이 산후 필요에 맞게 충분히 발달되지 않아 갑상선 기능저하증 위험이 있다.[71]신생아의 갑상선 기능저하증(갑상선 기능저하증)을 감지하기 위해, 노년의 성장과 발육 이상을 예방하기 위해, 많은 나라들이 출생 시에 신생아 검진 프로그램을 실시하고 있다.[72]
갑상선 호르몬 결핍증(당상 갑상선기능저하증)이 있는 유아는 뇌 발달뿐만 아니라 신체 성장과 발육의 문제를 나타낼 수 있는데, 이를 크레틴증이라고 한다.[73][22]선천성 갑상선 기능저하증이 있는 아동은 정상적인 성장과 발달을 촉진하는 부갑상선 기능저하증으로 보충적으로 치료된다.[74]
점액성, 투명한 분비물이 이러한 낭종 내에 모여 직경 2~3cm보다 큰 구형 질량 또는 방추형 팽창 중 하나를 형성할 수 있다.이것들은 기관 앞 목의 중간선에 있다.목에서 높게 발생하는 덕트와 낭종의 세그먼트는 층화된 편평상피에 의해 줄지어 있는데, 이는 포아멘 체쿰 부위에서 혀의 후부를 덮고 있는 것과 본질적으로 동일하다.아랫목에서 갑상선에 더 가까운 곳에서 발생하는 질환은 갑상선 아세나 상피와 유사한 상피에 의해 정렬된다.특징적으로 안감 상피 옆에는 강렬한 림프구 침투가 있다.중첩된 감염은 이러한 병변을 종기 충치로 전환시킬 수 있으며, 드물게 암을 유발한다.[citation needed]
또 다른 장애는 갑상선 이상 부속 갑상선의 다양한 발현으로 이어질 수 있는 갑상선 이상이다.[5]이것들은 무증상일 수 있다.
요오드
내륙과 산악 지역에서 가장 흔한 요오드 결핍은 만연할 경우 고트레에 걸리기 쉽다. 고트레라고 알려져 있다.[73]요오드가 부족한 임산부는 갑상선 호르몬이 부족한 유아를 출산할 수 있다.[73][22]요오드화 소금을 식단에[22] 첨가하는 것은 대부분의 선진국에서 풍토적인 크레티니즘을 없앴고 120여 개국이 소금 요오드화를 의무화했다.[76][77][78]
갑상선은 요오드를 농축하기 때문에 핵분열로 생성된 요오드의 다양한 방사성 동위원소도 농축한다.그러한 물질이 환경으로 대량으로 방출되는 경우, 이론적으로 갑상선에 의한 방사성 요오드 동위원소 흡수는 요오드화 칼륨 알약의 형태로 섭취된 비방사성 요오드가 많은 잉여로 흡수 메커니즘을 포화시켜 차단될 수 있다.체르노빌 참사의 한 가지 결과는 사고 후 몇 년 동안 어린이들의 갑상선 암이 증가했다는 것이다.[79]
과도한 요오드 섭취는 흔치 않으며 보통 갑상선 기능에 영향을 주지 않는다.때로는 갑상선 기능 항진증을 유발할 수도 있지만, 때로는 갑상선 기능 항진증을 유발하여 갑상선 기능 항진증을 유발할 수도 있다.[80]
평가하기
갑상선은 갑상선과 주변 목의 부기 또는 팽창 여부를 관찰하여 검사한다.[81]그리고 나서 그것은 주로 뒤에서 느껴지고, 사람은 종종 시험관의 손가락에 대고 분비선을 더 잘 느끼기 위해 삼키도록 요청 받는다.[81]갑상선과 크라이코이드 포장마차에 부착되어 있기 때문에 글랜드가 삼킬 때 위아래로 움직인다.[6]건강한 사람에게는 아직 보이지 않는 분비샘이 부드러운 덩어리로 눈에 띈다.갑상선 검사에는 비정상적인 질량 탐색과 전반적인 갑상선 크기 평가가 포함된다.[82]갑상선의 성격, 붓기, 결절, 그리고 그 일관성을 모두 느낄 수 있을 것이다.만약 괴짜가 있다면, 검사자는 또한 가슴 윗부분을 두드려 연장 여부를 확인하는 것을 고려하는 것을 목 아래로 느낄 수 있다.추가적인 검사에는 팔을 들어올리는 것(펨버튼의 기호), 과일에 대한 청진기로 글랜드의 소리를 듣는 것, 반사작용의 시험, 머리와 목의 림프절의 팰프팅 등이 포함될 수 있다.
갑상선 검사에는 또한 그레이브스 병에서 눈이 튀어나오거나 종아리가 부풀어 오르는 등 체중 증가나 감소와 같은 전신 징후를 찾기 위해 그 사람을 전체적으로 관찰하는 것도 포함될 것이다.[83][81]
테스트
갑상선 기능 검사에는 갑상선 호르몬 측정은 물론 갑상선 자극 호르몬(TSH) 측정 등 혈액 검사 전지가 포함된다.[84]그들은 갑상선 기능 항진증(높은 T3와 T4), 갑상선 기능 항진증(낮은 T3, T4), 또는 부임상 갑상선 기능 항진증(TSH가 낮은 정상 T3와 T4)을 드러낼 수 있다.[84]
TSH 수치는 갑상선 기능 장애의 가장 민감한 지표로 여겨진다.[84]그러나 갑상선 기능저하증의 원인이 불충분한 티로트로핀 방출 호르몬(TRH) 분비물과 관련이 있다고 생각되는 경우, 이 경우 낮거나 잘못된 정상일 수 있다.이 경우 TRH가 주어지고 TSH 수준이 30분 및 60분 후에 측정되는 TRH 자극 시험을 실시할 수 있다.[84]
T3와 T4는 직접 측정할 수 있다.그러나 두 갑상선호르몬이 다른 분자와 결합한 상태로 이동하며 생물학적으로 활성하는 것이 '자유' 성분인 만큼 T3와 T4 수치를 자유롭게 측정할 수 있다.[84]갑상선기능저하증에서 T3 수준은 정상일 수 있기 때문에 T4가 선호된다.[84]결합되지 않은 갑상선 호르몬에 대한 결합 비율은 갑상선 호르몬 결합비(THBR)로 알려져 있다.[85]갑상선 호르몬인 트리오글로불린과 스로틀빈 결합 글로불린의 주요 매개체를 직접 측정하는 것도 가능하다.[86]티로글로불린은 건강한 갑상선에서도 측정할 수 있게 되며 염증과 함께 증가하게 되며, 갑상선 제거나 절제술의 성공 여부를 측정하는 데도 사용될 수 있다.만약 성공한다면, thyroglobulin은 감지할 수 없어야 한다.[85]마지막으로 갑상선의 성분, 특히 항 TPO와 항티로글로불린에 대한 항체를 측정할 수 있다.이것들은 정상적인 개인에게 있을 수 있지만 자가면역 관련 질병에는 매우 민감하다.[85]
이미징
갑상선의 초음파는 구조물이 고체인지 유체로 채워져 있는지 여부를 밝혀내는 데 사용되어 결절과 궤간, 낭종과의 구별에 도움을 줄 수 있다.그것은 또한 악성 병변과 양성 병변을 구별하는 데 도움이 될 수 있다.[87]
추가 영상이 필요한 경우 방사선방사선 요오드-123 또는 테크네튬-99 흡수 스캔이 발생할 수 있다.이를 통해 병변의 크기와 형태를 결정하고, 결절이나 괴물이 신진대사적으로 활발히 활동하는지 여부를 밝혀낼 수 있으며, 갑상선 질환이나 갑상선 외부의 암 퇴적물 부위를 밝히고 감시할 수 있다.[88]
갑상선 조직 샘플의 미세한 바늘 흡인력은 초음파에서 보이는 병변을 평가하기 위해 채취할 수 있으며, 이는 조직병리학과 세포학으로 보내진다.[89]
갑상선의 컴퓨터단층촬영은 갑상선암 평가에 중요한 역할을 한다.[90]CT스캔은 갑상선 이상을 우연히 발견하는 경우가 많아 사실상 첫 조사 방식이 된다.[90]
역사
갑상선은 1600년대에 해부학자 토마스 와튼이 고대 그리스 방패나 사이오스에 그것의 모양을 비유하면서 현대적인 이름을 얻었다.그러나, 선체의 존재, 그리고 그와 관련된 질병의 존재는 그 훨씬 전에 알려져 있었다.
고대
갑상선의 유무와 질병은 수천 년 동안 지적되고 치료되어 왔다.[4]기원전 1600년에 탄 스펀지와 해초(요오드가 들어 있는 것)가 중국 내에서 사용되었는데, 이는 세계 각지에서 발전된 관행이다.[4][91]아유르베딕 의학에서는 기원전 1400년경에 쓰여진 서슈루타 삼히타가 갑상선기능항진증, 갑상선기능항진증, 갑상선기능항진증, 갑상선기능항진증 등을 기술하였다.[91]기원전 5세기의 아리스토텔레스와 크세노폰은 독성 고트레의 확산 사례를 묘사하고 있다.[91]기원전 4세기 히포크라테스와 플라톤은 침샘으로서의 기능을 제안하면서 글랜드 자체에 대한 최초의 묘사를 몇 가지 제공했다.[91]기원전 1세기 장로 플린은 알프스 산맥의 고트레 전염병을 언급하고 불에 탄 해초를 이용한 치료를 제안했는데,[4] 2세기 갈렌은 고트레 치료를 위해 탄 스펀지를 언급하기도 했다.[4]ca. 200-250이라고 쓰여진 중국의 약리학 전문 Sennong Ben Cao Jing도 gotre를 가리킨다.[4][91]
과학시대
1500년에 다산술 레오나르도 다빈치는 갑상선의 첫 삽화를 제공했다.[4]1543년 해부학자 안드레아스 베살리우스가 최초로 해부학적 설명과 선에 대한 삽화를 들려주었다.[4]1656년에 갑상선은 해부학자 토마스 와튼에 의해 현대적인 이름을 받았다.[4]이 글랜드의 모양은 고대 그리스에서 흔히 사용되는 방패와 닮아 방패를 뜻하는 갑상선이라는 이름이 붙여졌다.[4]갑상선이라는[92] 영어 이름은 와튼 - 글랜드울라 티레오이데아가 사용하는 의학 라틴어에서 유래되었다.[93]글레둘라는 라틴어로 'gland'를 의미하며,[94] 티레오이데아는 고대 그리스어 wordυρεεδδδδ to to to to to to to로 거슬러 올라갈 수 있는데, 이는 '방패 모양/방패 모양'[95]이라는 뜻이다.
1811년 프랑스의 화학자 베르나르 쿠르투아가 요오드를 발견하였고,[91] 1896년 유겐 바우만은 이를 갑상선의 중심 성분으로 기록하였다.그는 천 마리의 양의 갑상선을 끓여서 이렇게 했고, 갑상선 호르몬의 조합인 침전물 이름을 '오도티슈린'이라고 지었다.[91]1907년 데이비드 마린은 갑상선 기능에 요오드가 필요하다는 것을 증명했다.[91][4]
그레이브스의 병은 1834년 로버트 제임스 그레이브스에 의해 묘사되었다.신진대사에 있어서 갑상선의 역할은 1895년 아돌프 마그누스 레비에 의해 증명되었다.[96]티록신은 1914년에 처음 격리되어 1927년에 합성되었고, 1952년에 트리오도티록신(triodoothyroxine)이 합성되었다.[91][97]T4에서 T3로의 전환은 1970년에 발견되었다.[4]TSH를 발견하는 과정은 20세기 초반에서 중반에 걸쳐 이루어졌다.[98]TRH는 폴란드 내분비학자인 앤드류 샬리에 의해 1970년에 발견되어 1977년 노벨 의학상에 부분적으로 기여했다.[4][99]
19세기에 많은 저자들이 크레틴증과 뜸을 모두 묘사했고 갑상선과의 관계를 묘사했다.[91]찰스 마요는 1910년에 갑상선 항진증이라는 용어를 만들었다.[4]하시모토 하카루는 1912년에 하시모토의 갑상선염의 사례를 기록하였고, 1956년에 이 병의 항체가 증명되었다.[91]갑상선에 대한 지식과 갑상선의 상태에 대한 지식은 19세기 후반과 20세기 후반에 걸쳐 발전했으며 방사능 요오드, 티오라실, 미세한 바늘 흡인 등 20세기 중반에 걸쳐 많은 현대적인 치료법과 조사 방법이 진화했다.[4]
수술
6세기 CE의[91] 에이티우스나 990년 CE의 페르시아인 알리 이븐 압바스 알 마구시 중 어느 한 쪽이 괴레 치료제로 최초의 기록적인 갑상선 절제술을 시행했다.[4][100]수술은 위험했고, 프러시아 의사 테오도르 빌로스, 스위스 의사 및 생리학자 테오도르 코허, 미국 의사 찰스 메이요, 미국 외과의사 윌리엄 할스테드, 조지 크릴을 포함한 다수의 저자들로부터 설명이 나왔을 때까지 일반적으로 성공적이지 못했다.이러한 묘사는 현대 갑상선 수술의 기초를 제공했다.[101]테오도르 코허는 1909년 "갑상선의 생리학, 병리학, 수술에 관한 연구"로 노벨 생리의학상을 수상했다.[102]
다른동물

갑상선은 모든 척추동물에서 발견된다.물고기에서는 보통 아가미 아래에 위치하며 항상 뚜렷한 로브로 나뉘지는 않는다.그러나 일부 텔레오스트에서는 신장, 비장, 심장 또는 눈과 관련된 갑상선 조직의 조각이 신체의 다른 곳에서 발견된다.[103]
사두엽에서 갑상선은 항상 목 부위 어딘가에서 발견된다.대부분의 테트라포드 종에서, 두 쌍의 갑상샘이 있다. 즉, 오른쪽과 왼쪽 로브는 서로 연결되지 않는다.하지만 대부분의 포유동물에는 갑상선 한 개만 있을 뿐이고, 인간에게서 발견되는 모양은 다른 많은 종들에게 흔하다.[103]
애벌레 등잔에서 갑상선은 외분비샘으로 발원하여 호르몬을 내장으로 분비하며 애벌레의 여과기기와 관련이 있다.성충등에서는 분비선이 내장과 분리되어 내분비가 되지만 이 발달의 길은 갑상선의 진화적 기원을 반영할 수도 있다.예를 들어 척추동물의 가장 가까운 살아 있는 친족인 튜네틱과 암피오시(랜슬렛)는 애벌레 등잔류(내시경)와 매우 유사한 구조를 가지고 있으며, 이것은 티록신은 아니지만 요오드 함유 화합물을 분비하기도 한다.[103]
Tyroxine은 신진대사 조절에 매우 중요하며 척추동물 쇄골 전체에 걸쳐 성장한다.요오드와 T4는 다른 포식동물에서 볼 수 있듯이, 식물을 먹는 올챙이에서 육식을 하는 육지개구리로의 변화를 촉발시킨다.네오틴 양서류 도롱뇽에서도 비슷한 현상이 일어나는데, 요오드를 도입하지 않으면 육지식 성인으로 변신하지 않고 수생 악솔로틀의 애벌레 형태로 살고 번식한다.양서류 중에서는 프로필티오우라실(PTU)과 같은 갑상선 차단제를 투여하면 올챙이가 개구리로 변하는 것을 막을 수 있다. 반대로 티록신을 투여하면 변태를 유발할 수 있다.양서류 변태에서 티록신과 요오드는 올챙이의 아가미, 꼬리, 지느러미의 세포에도 잘 연구된 실험 모델을 발휘한다.요오드는 요오드올리피드를 통해 육지 동물 종의 진화를 선호해 왔으며 인간의 뇌 진화에 결정적인 역할을 했을 가능성이 높다.[104][105]
참고 항목
참조
- ^ 가이튼 & 홀 2011, 페이지 907.
- ^ a b Boron WF, Boulpaep EL (2012). Medical Physiology (2nd ed.). Philadelphia: Saunders. p. 1052. ISBN 978-1-4377-1753-2.
- ^ 해리슨의 2011년, 2913페이지, 2918페이지.
- ^ a b c d e f g h i j k l m n o p q "Thyroid History Timeline – American Thyroid Association". www.thyroid.org. Retrieved 13 November 2016.
- ^ a b c d e f g h i j k l m n o p q r s t u Gray's Anatomy 2008, 페이지 462–4.
- ^ a b c d e f g h i j k 엘시어의 2007년판 342페이지.
- ^ 엘시어의 2007년판 342-3페이지.
- ^ Ellis H, Standring S, Gray HD (2005). Gray's anatomy: the anatomical basis of clinical practice. St. Louis, Mo: Elsevier Churchill Livingstone. pp. 538–539. ISBN 978-0-443-07168-3.
- ^ Netter FH (2014). Atlas of Human Anatomy Including Student Consult Interactive Ancillaries and Guides (6th ed.). Philadelphia, Penn.: W B Saunders Co. p. 27. ISBN 978-1-4557-0418-7.
- ^ a b Page C, Cuvelier P, Biet A, Boute P, Laude M, Strunski V (July 2009). "Thyroid tubercle of Zuckerkandl: anatomical and surgical experience from 79 thyroidectomies". The Journal of Laryngology and Otology. 123 (7): 768–71. doi:10.1017/s0022215108004003. PMID 19000342. S2CID 22063700.
- ^ a b c 엘시어의 2007년판 343페이지.
- ^ a b Cicekcibasi AE, Salbacak A, Seker M, Ziylan T, Tuncer I, Buyukmumcu M (April 2007). "Developmental variations and clinical importance of the fetal thyroid gland. A morphometric study". Saudi Medical Journal. 28 (4): 524–8. PMID 17457471.
- ^ Kim DW, Jung SL, Baek JH, Kim J, Ryu JH, Na DG, et al. (January 2013). "The prevalence and features of thyroid pyramidal lobe, accessory thyroid, and ectopic thyroid as assessed by computed tomography: a multicenter study". Thyroid. 23 (1): 84–91. doi:10.1089/thy.2012.0253. PMID 23031220.
- ^ Dorland WA (2012). Anderson DM (ed.). Dorland'sIllustrated Medical Dictionary (32nd ed.). Elsevier Saunders. pp. 999 redirect to 1562. ISBN 978-1-4160-6257-8.
- ^ Fawcett D, Jensh R (2002). Bloom & Fawcett's Concise Histology. New York: Arnold Publishers. pp. 257–258. ISBN 978-0-340-80677-7.
- ^ a b Wheater PR, Young B (2006). Wheater's functional histology : a text and colour atlas (5th ed.). Oxford: Churchill Livingstone. pp. 333–335. ISBN 978-0-443-06850-8.
- ^ Hazard JB (July 1977). "The C cells (parafollicular cells) of the thyroid gland and medullary thyroid carcinoma. A review". The American Journal of Pathology. 88 (1): 213–50. PMC 2032150. PMID 18012.
- ^ a b Larsen WJ (2001). Human embryology (3. ed.). Philadelphia, Pa.: Churchill Livingstone. pp. 372–374. ISBN 978-0-443-06583-5.
- ^ a b c d 그린스펀의 2011년, 페이지 179.
- ^ a b Eugster EA, Pescovitz OH (2004). Pediatric endocrinology: mechanisms, manifestations and management. Hagerstwon, MD: Lippincott Williams & Wilkins. p. 493 (Table 33–3). ISBN 978-0-7817-4059-3.
- ^ Zoeller RT (April 2003). "Transplacental thyroxine and fetal brain development". The Journal of Clinical Investigation. 111 (7): 954–7. doi:10.1172/JCI18236. PMC 152596. PMID 12671044.
- ^ a b c d "Iodine supplementation in pregnant and lactating women". World Health Organization. Archived from the original on January 4, 2014. Retrieved 2016-11-13.
- ^ a b Langman J, Sadler TW, Sadler-Redmond SL, Tosney K, Byrne J, Imseis H (2015). Langman's Medical Embryology (13th ed.). pp. 285–6, 293. ISBN 978-1-4511-9164-6.
- ^ a b 데이비드슨의 2010년 736페이지.
- ^ 가이튼 & 홀 2011, 페이지 909.
- ^ 가이튼 & 홀 2011, 페이지 934.
- ^ a b c d e 가이튼 & 홀 2011, 페이지 937.
- ^ a b c d e 가이튼 & 홀 2011, 페이지 936.
- ^ 가이튼 & 홀 2011, 935-6페이지.
- ^ 그린스펀의 2011년, 페이지 169.
- ^ a b Bowen R (2000). "Thyroid Hormone Receptors". Colorado State University. Archived from the original on 27 September 2011. Retrieved 22 February 2015.
- ^ 그린스펀의 2011년, 페이지 178.
- ^ a b Boron WF, Boulpaep E (2003). "Chapter 48: "synthesis of thyroid hormones"". Medical Physiology: A Cellular And Molecular Approaoch. Elsevier/Saunders. p. 1300. ISBN 978-1-4160-2328-9.
- ^ a b Bianco AC, Salvatore D, Gereben B, Berry MJ, Larsen PR (February 2002). "Biochemistry, cellular and molecular biology, and physiological roles of the iodothyronine selenodeiodinases". Endocrine Reviews. 23 (1): 38–89. doi:10.1210/er.23.1.38. PMID 11844744.
- ^ Melmed S, Polonsky KS, Larsen PR, Kronenberg HM (2011). Williams Textbook of Endocrinology (12th ed.). Saunders. p. 331. ISBN 978-1-4377-0324-5.
- ^ 갑상선의 작동 방식: 섬세한 피드백 메커니즘.2009-05-21 업데이트.
- ^ 내분비학의 갑상선: Stephen Nussey와 Saffron Whitehead(2001)의 통합 접근법 BIOS Scientific Publishers Ltd.ISBN 1-85996-252-1
- ^ Ganong's review of medical physiology Edition 25.
- ^ 그린스펀의 2011년, 페이지 174.
- ^ 그린스펀의 2011년, 페이지 177.
- ^ 가이튼 & 홀 2011, 페이지 896.
- ^ 해리슨의 2011년, 2215페이지.
- ^ 가이튼 & 홀 2011, 페이지 988–9.
- ^ "The human proteome in thyroid gland – The Human Protein Atlas". www.proteinatlas.org. Retrieved 2017-09-25.
- ^ Uhlén M, Fagerberg L, Hallström BM, Lindskog C, Oksvold P, Mardinoglu A, et al. (January 2015). "Proteomics. Tissue-based map of the human proteome". Science. 347 (6220): 1260419. doi:10.1126/science.1260419. PMID 25613900. S2CID 802377.
- ^ 데이빗슨의 2010년 738페이지.
- ^ Rusandu A, Sjøvold BH, Hofstad E, Reidunsdatter RJ (June 2020). "Iodinated contrast media and their effect on thyroid function - Routines and practices among diagnostic imaging departments in Norway". Journal of Medical Radiation Sciences. 67 (2): 111–118. doi:10.1002/jmrs.390. PMC 7276191. PMID 32232955.
- ^ a b 데이비드슨의 2010년, 페이지 740.
- ^ a b 데이비드슨의 2010년 739페이지.
- ^ 데이비드슨의 2010년 745페이지.
- ^ Cury AN, Meira VT, Monte O, Marone M, Scalissi NM, Kochi C, et al. (March 2013). "Clinical experience with radioactive iodine in the treatment of childhood and adolescent Graves' disease". Endocrine Connections. 2 (1): 32–7. doi:10.1530/EC-12-0049. PMC 3680965. PMID 23781316.
- ^ 갑상선 문제 e메디컬 건강.2010-02-07년 검색됨
- ^ "Iodine Deficiency & Nutrition". www.thyroidfoundation.org.au. Australian Thyroid Foundation. Archived from the original on 13 January 2017. Retrieved 11 January 2017.
- ^ So M, MacIsaac R, Grossmann M. "Hypothyroidism – Investigation and management". www.racgp.org.au. The Royal Australian College of General Practitioners. Retrieved 11 January 2017.
- ^ 데이빗슨의 2010년, 741페이지.
- ^ a b 데이비드슨의 2010년, 743페이지.
- ^ 데이빗슨 2010년 741-3페이지
- ^ a b c d Smith TJ, Hegedüs L (October 2016). "Graves' Disease" (PDF). The New England Journal of Medicine. 375 (16): 1552–1565. doi:10.1056/nejmra1510030. PMID 27797318.
- ^ a b c Dean DS, Gharib H (December 2008). "Epidemiology of thyroid nodules". Best Practice & Research. Clinical Endocrinology & Metabolism. 22 (6): 901–11. doi:10.1016/j.beem.2008.09.019. PMID 19041821.
- ^ a b Welker MJ, Orlov D (February 2003). "Thyroid nodules". American Family Physician. 67 (3): 559–66. PMID 12588078. Retrieved 6 September 2016.
- ^ a b c d e f g 데이비드슨의 2010년, 페이지 744.
- ^ "goitre – definition of goitre in English". Oxford Dictionaries English. Retrieved 18 September 2016.
- ^ 데이비드슨의 2010년 750페이지.
- ^ 해리슨의 2011년, 2237페이지.
- ^ a b c d 해리슨의 2011페이지 2230.
- ^ a b 해리슨의 2011년, 2238페이지.
- ^ a b c d e 해리슨의 2011년, 2242페이지.
- ^ a b 데이비드슨의 2010년, 페이지 751.
- ^ a b 데이비드슨의 2010년, 페이지 752.
- ^ 해리슨의 2011년, 2242,2246페이지.
- ^ Berbel P, Navarro D, Ausó E, Varea E, Rodríguez AE, Ballesta JJ, et al. (June 2010). "Role of late maternal thyroid hormones in cerebral cortex development: an experimental model for human prematurity". Cerebral Cortex. 20 (6): 1462–75. doi:10.1093/cercor/bhp212. PMC 2871377. PMID 19812240.
- ^ Büyükgebiz A (15 November 2012). "Newborn screening for congenital hypothyroidism". Journal of Clinical Research in Pediatric Endocrinology. 5 Suppl 1 (4): 8–12. doi:10.4274/Jcrpe.845. PMC 3608007. PMID 23154158.
- ^ a b c 그린스펀의 2011년, 페이지 164.
- ^ Rose SR, Brown RS, Foley T, Kaplowitz PB, Kaye CI, Sundararajan S, Varma SK (June 2006). "Update of newborn screening and therapy for congenital hypothyroidism". Pediatrics. 117 (6): 2290–303. doi:10.1542/peds.2006-0915. PMID 16740880.
- ^ 갑상선 건강 및 질병 연도의 갑상선: 1917년 로버트 맥캐리슨
- ^ Harris RE (2015-05-07). Global Epidemiology of Cancer. Jones & Bartlett Publishers. p. 268. ISBN 978-1-284-03445-5.
- ^ Leung AM, Braverman LE, Pearce EN (November 2012). "History of U.S. iodine fortification and supplementation". Nutrients. 4 (11): 1740–6. doi:10.3390/nu4111740. PMC 3509517. PMID 23201844.
- ^ "Map: Count of Nutrients In Fortification Standards". Global Fortification Data Exchange. Retrieved 23 December 2019.
- ^ "Chernobyl children show DNA changes". BBC News. 2001-05-08. Retrieved 2010-05-25.
- ^ "Iodine - Disorders of Nutrition". MSD Manual Consumer Version. Archived from the original on 18 December 2019. Retrieved 18 December 2019.
- ^ a b c Talley N (2014). Clinical Examination. Churchill Livingstone. pp. Chapter 28. "The endocrine system". pp 355–362. ISBN 978-0-7295-4198-5.
- ^ Fehrenbach; Herring (2012). Illustrated Anatomy of the Head and Neck. Elsevier. p. 158. ISBN 978-1-4377-2419-6.
- ^ 해리슨의 2011년, 2228페이지.
- ^ a b c d e f 그린스펀의 2011년, 페이지 184.
- ^ a b c 해리슨의 2011년, 2229페이지.
- ^ 그린스펀 2011 페이지 186.
- ^ 그린스펀의 2011년, 페이지 189.
- ^ 그린스펀의 2011년, 페이지 188-9.
- ^ 그린스펀의 2011년 페이지 190.
- ^ a b Bin Saeedan M, Aljohani IM, Khushaim AO, Bukhari SQ, Elnaas ST (August 2016). "Thyroid computed tomography imaging: pictorial review of variable pathologies". Insights into Imaging. 7 (4): 601–17. doi:10.1007/s13244-016-0506-5. PMC 4956631. PMID 27271508. Creative Commons Attribution 4.0 International License
- ^ a b c d e f g h i j k l Niazi AK, Kalra S, Irfan A, Islam A (July 2011). "Thyroidology over the ages". Indian Journal of Endocrinology and Metabolism. 15 (Suppl 2): S121-6. doi:10.4103/2230-8210.83347. PMC 3169859. PMID 21966648.
- ^ Anderson DM (2000). Dorland's Illustrated Medical Dictionary (29th ed.). Philadelphia/London/Toronto/Montreal/Sydney/Tokyo: W.B. Saunders Company.
- ^ His W (1895). Die anatomische Nomenclatur. Nomina Anatomica. Der von der Anatomischen Gesellschaft auf ihrer IX. Versammlung in Basel angenommenen Namen [The anatomical nomenclature. Nominal Anatomica. Anatomical Society on its IX. Assembly adopted in Basel] (in German). Leipzig: Verlag Veit & Comp.
- ^ Lewis CT, Short C (1879). A Latin dictionary. founded on Andrews' edition of Freund's Latin dictionary. Oxford: Clarendon Press.
- ^ Liddell HG, Scott R (1940). A Greek-English Lexicon. revised and augmented throughout by Sir Henry Stuart Jones. with the assistance of. Roderick McKenzie. Oxford: Clarendon Press.
- ^ Freake HC, Oppenheimer JH (1995). "Thermogenesis and thyroid function". Annual Review of Nutrition. 15 (1): 263–91. doi:10.1146/annurev.nu.15.070195.001403. PMID 8527221.
- ^ Hamdy, Roland. "The thyroid glands: a brief historical perspective". www.medscape.com. Retrieved 2016-11-13.
- ^ Magner J (June 2014). "Historical note: many steps led to the 'discovery' of thyroid-stimulating hormone". European Thyroid Journal. 3 (2): 95–100. doi:10.1159/000360534. PMC 4109514. PMID 25114872.
- ^ "The Nobel Prize in Physiology or Medicine 1977". www.nobelprize.org. Retrieved 14 January 2017.
- ^ Slidescenter.com. "Hormones.gr". www.hormones.gr. Retrieved 2016-11-13.
- ^ Werner SC, Ingbar SH, Braverman LE, Utiger RD (2005). Werner & Ingbar's the Thyroid: A Fundamental and Clinical Text. Lippincott Williams & Wilkins. p. 387. ISBN 978-0-7817-5047-9.
- ^ "The Nobel Prize in Physiology or Medicine 1909". Nobel Foundation. Retrieved 2007-07-28.
- ^ a b c Romer AS, Parsons TS (1977). The Vertebrate Body. Philadelphia, PA: Holt-Saunders International. pp. 555–556. ISBN 978-0-03-910284-5.
- ^ Venturi S (2011). "Evolutionary Significance of Iodine". Current Chemical Biology. 5 (3): 155–162. doi:10.2174/187231311796765012. ISSN 1872-3136.
- ^ Venturi S (2014). "Iodine, PUFAs and Iodolipids in Health and Disease: An Evolutionary Perspective". Human Evolution. 29 (1–3): 185–205. ISSN 0393-9375.
책들
- Greer MA, ed. (1990). The Thyroid Gland. Comprehensive Endocrinology Revised Series. N.Y.: Raven Press. ISBN 0-88167-668-3.
- Shoback D (2011). Gardner DG (ed.). Greenspan's basic & clinical endocrinology (9th ed.). New York: McGraw-Hill Medical. ISBN 978-0-07-162243-1.
- Hall JE, Guyton AC (2011). Guyton and Hall textbook of medical physiology (12th ed.). Philadelphia, Pa.: Saunders/Elsevier. ISBN 978-1-4160-4574-8.
- Longo D, Fauci A, Kasper D, Hauser S, Jameson J, Loscalzo J (August 11, 2011). Harrison's Principles of Internal Medicine (18 ed.). McGraw-Hill Professional. ISBN 978-0-07-174889-6.
- Colledge NR, Walker BR, Ralston SH, eds. (2010). Davidson's principles and practice of medicine. Illustrated by Robert Britton (21st ed.). Edinburgh: Churchill Livingstone/Elsevier. ISBN 978-0-7020-3085-7.
- Ort V, Bogart BI (2007). Elsevier's integrated anatomy and embryology. Philadelphia, Pa.: Elsevier Saunders. ISBN 978-1-4160-3165-9.
- Standring S, Borley NR, et al., eds. (2008). Gray's anatomy : the anatomical basis of clinical practice (40th ed.). London: Churchill Livingstone. ISBN 978-0-8089-2371-8.
외부 링크
| 위키미디어 커먼즈에는 갑상선과 관련된 미디어가 있다. |








