금속단백질
Metalloprotein금속단백질은 금속이온 [1][2]보조인자를 포함하는 단백질의 총칭이다.모든 단백질의 많은 부분이 이 범주에 속합니다.예를 들어, 최소 1000개의 인간 단백질(약 20,000개 중)은 아연 결합[3] 단백질 도메인을 포함하지만, 최대 3000개의 인간 아연 금속단백질이 [4]있을 수 있다.
풍부
모든 단백질의 약 절반이 [5]금속을 포함하고 있는 것으로 추정된다.또 다른 추정에 따르면, 모든 단백질의 약 1/4에서 1/3이 금속이 [6]그 기능을 수행하도록 요구된다고 한다.따라서, 금속단백질은 단백질, 효소, 신호전달단백질의 저장과 운반,[7] 또는 전염병과 같은 많은 다른 기능을 가지고 있다.금속 결합 단백질의 풍부함은 단백질이 사용하는 아미노산에 고유한 것일 수 있는데, 진화력이 없는 인공 단백질도 금속을 [8]쉽게 결합시킬 수 있기 때문이다.
인체에 있는 대부분의 금속은 단백질에 결합되어 있다.예를 들어, 인체에서 상대적으로 높은 철분 농도는 대부분 헤모글로빈의 철분 때문이다.
| 간 | 신장 | 폐 | 하트 | 뇌 | 근육 | |
|---|---|---|---|---|---|---|
| Mn(망간어) | 138 | 79 | 29 | 27 | 22 | 4 ~ 40 미만 |
| Fe(철) | 16,769 | 7,168 | 24,967 | 5530 | 4100 | 3,500 |
| Co(코발트) | 2 ~ 13 미만 | 2 미만 | 2 ~ 8 미만 | --- | 2 미만 | 150 (?) |
| 니켈(니켈) | 5 미만 | 5 ~ 12 미만 | 5 미만 | 5 미만 | 5 미만 | 15 미만 |
| Cu(구리) | 882 | 379 | 220 | 350 | 401 | 85-305 |
| Zn(아연) | 5,543 | 5,018 | 1,470 | 2,772 | 915 | 4,688 |
배위 화학 원리
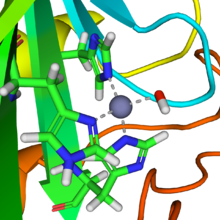
금속이온은 보통 단백질의 아미노산 잔기에 속하는 질소, 산소 또는 유황 중심으로 배위되어 있다.이러한 기증자 그룹은 종종 아미노산 잔류물의 곁사슬에 의해 제공됩니다.특히 중요한 것은 히스티딘 잔기의 이미다졸 치환기, 시스테인 잔기의 티올 치환기 및 아스파르트산이 제공하는 카르본산기이다.금속단백질의 다양성을 고려할 때, 사실상 모든 아미노산 잔류물은 금속의 중심을 결합하는 것으로 나타났다.펩타이드 골격은 또한 기증자 그룹을 제공하는데, 여기에는 탈양성자 아미드 및 아미드 카르보닐 산소 센터가 포함됩니다.천연 및 인공 단백질의 납(II) 결합이 [10]검토되었다.
아미노산 잔기에 의해 제공되는 공여체 그룹 외에도 많은 유기 보조 인자가 배위자로 기능한다.아마도 가장 유명한 것은 헴 단백질에 통합된 사환산4 N 매크로사이클릭 리간드이다.황화나 산화물과 같은 무기 배위자들도 흔하다.
저장 및 운반 금속단백질
이들은 약간 더 강한 산과 알칼리 처리를 통해 얻은 단백질 가수분해의 2단계 산물이다.
산소 운반체
헤모글로빈은 인간의 주요 산소 운반체이며 철분이 함유된 4개의 소단위(sub-units)를 가지고 있다.II) 이온은 히스티딘 잔기의 평면 매크로사이클 리간드 프로포르피린 IX(PIX)와 이미다졸 질소 원자에 의해 배위된다.여섯 번째 배위부위는 물 분자 또는 다이옥시겐 분자를 포함한다.반면 근육 세포에서 발견되는 단백질 미오글로빈은 그러한 단위가 하나밖에 없다.활성 부위는 소수성 포켓에 위치합니다.이것이 없으면 철분도 중요합니다.II)는 철(II)로 불가역적으로 산화된다.HbO2 형성의 평형 상수는 폐나 근육의 산소 분압에 따라 산소가 흡수되거나 방출되는 것이다.헤모글로빈에서 네 개의 서브유닛은 헤모글로빈에서 [11]미오글로빈으로 산소를 쉽게 전달할 수 있는 협동성 효과를 보여줍니다.
헤모글로빈과 미오글로빈 모두에서 산소화된 종에 철(II)이 함유되어 있다고 잘못 기재되는 경우가 있습니다.이 종들의 반자성적인 성질은 철분 때문이다.II) 원자가 저회전 상태에 있다.옥시헤모글로빈에서 철 원자는 포르피린 고리 평면에 위치하지만, 상사성 디옥시헤모글로빈에서 철 원자는 고리 [11]평면 위에 있습니다.스핀 상태의 이러한 변화는 옥시 헤모글로빈 부분에서의 높은 결정장 분할과 더 작은2+ 이온 반지름으로 인한 협동 효과입니다.
헤메리스린은 또 다른 철분 함유 산소 운반체이다.산소 결합 부위는 2핵 철의 중심이다.철 원자는 글루탐산염과 아스파르트산염의 카르복실산 측쇄와 5개의 히스티딘 잔기를 통해 단백질과 배위된다.헤메리스린에 의한 O의2 흡수는 결합된 과산화물(OOH)−을 생성하기 위해 환원된 2핵 중심부의 2전자 산화를 동반한다.산소 흡수 및 방출 메커니즘이 [12][13]상세하게 설명되었습니다.
헤모시아닌은 대부분의 연체동물과 투구게와 같은 일부 절지동물의 혈액에 산소를 운반합니다.그것들은 산소 운반에 사용되는 생물학적 인기 면에서 헤모글로빈 다음으로 많다.산소화 시 활성 부위의 두 개의 구리(I) 원자는 구리로 산화됩니다.II) 및 상기 다이옥시젠 분자를 과산화물 [14][15]O로2−
2 환원한다.
클로로크루오린(큰 운반체 에리트로크루오린)은 많은 환형동물, 특히 특정 해양 폴리케트의 혈장에 존재하는 산소 결합 헴단백질이다.
시토크롬
산화 및 환원 반응은 유기 화학에서 흔하지 않습니다. 산화 또는 환원제로 작용할 수 있는 유기 분자가 적기 때문입니다.반면 철(II)은 쉽게 철(II)로 산화된다.이 기능은 전자 전달 벡터로 기능하는 시토크롬에 사용됩니다.금속 이온의 존재는 금속 효소가 아미노산에서 [16]발견되는 제한된 일련의 기능성 기에 의해 쉽게 수행될 수 없는 산화 환원 반응과 같은 기능을 수행할 수 있도록 합니다.대부분의 시토크롬의 철 원자는 헴 그룹에 포함되어 있다.그 사이토크롬의 차이는 다른 측쇄에 있다.예를 들어 시토크롬a는 보철기, 시토크롬b는 보철기를 가진다.이러한 차이는 다양한 시토크롬이 미토콘드리아 전자전달망에 [17]관여하도록 서로 다른2+ Fe3+/Fe 산화환원 전위를 초래한다.
시토크롬 P450 효소는 산화반응인 C-H 결합에 산소 [18][19]원자를 삽입하는 기능을 한다.

루브레독신
루브레독신은 황화세균과 고세균에서 발견되는 전자담체다.활성 부위에는 거의 정다면체를 형성하는 4개의 시스테인 잔류물의 황 원자에 의해 조정된 철 이온이 포함되어 있습니다.루브레독신은 단일 전자 전달 과정을 수행합니다.철 원자의 산화 상태는 +2와 +3 상태 사이에서 변화합니다.두 산화 상태 모두에서 금속은 높은 스핀으로 구조 변화를 최소화하는 데 도움이 됩니다.
플라스토시아닌
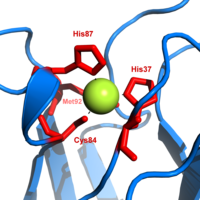
플라스토시아닌은 전자전달 반응에 관여하는 청동단백질 중 하나이다.구리 결합 부위는 일그러진 삼각 피라미드로 [20]묘사됩니다.피라미드 베이스의 삼각면은 분리된 히스티딘에서 나온 두 개의 질소 원자(N12, N)와 시스테인에서 나온 황(S1)으로 구성되어 있다.축방향 메티오닌으로부터의 황(S2)이 정점을 형성한다.구리와 유황 배위자 사이의 결합 길이에서 왜곡이 발생합니다.Cu-S1 접점은 Cu-S2(282 pm)보다 짧다(207 pm).길쭉한2 Cu-S 결합은 Cu(II) 형태를 불안정하게 하고 단백질의 산화환원 전위를 증가시킨다.파란색(597 nm 피크 흡수)은 S(p†)에서 Cu(dx2−y2)로의 전하 전달이 발생하는 [21]Cu-S1 결합에 기인합니다.
환원된 플라스토시아닌 형태에서 His-87은 pKa 4.4로 양성자화된다.양성자화는 그것이 배위자로 작용하는 것을 막고 구리 부위의 형상이 삼각 평면이 된다.
금속 이온 저장 및 전송
철
철은 철(III)로서 페리틴에 저장된다.결속 부위의 정확한 성질은 아직 밝혀지지 않았다.철은 FeO(OH)와 같은 가수분해 생성물로 존재하는 것으로 보인다.철은 트랜스페린에 의해 운반되며, 그 결합 부위는 아스파라긴산과 히스티딘의 [22]2개의 티로신이다.인체에는 철분 [citation needed]배설 메커니즘이 없다.이것은 예를 들어 β-thalassemia와 같이 수혈로 치료된 환자에게 철분 과부하 문제를 야기할 수 있다.철분은 실제로 소변으로[23] 배출되고 [25]대변으로 배출되는 담즙에[24] 농축된다.
구리
세룰로플라스민은 혈액에서 구리를 운반하는 주요 단백질이다.세룰로플라스민은 Fe(II)가 Fe(III)로 산화될 수 있는 산화효소 활성을 나타내므로 Fe(II) 상태에서만 철분을 운반할 수 있는 트랜스페린과 관련하여 혈장 내 수송을 돕는다.
칼슘
골폰틴은 뼈와 치아의 세포외 매트릭스에서 광물질화에 관여한다.
금속효소
금속효소는 모두 하나의 공통점을 가지고 있는데, 그것은 금속이온이 하나의 불안정한 배위 부위와 단백질에 결합되어 있다는 것이다.모든 효소와 마찬가지로 활성 부위의 모양이 중요합니다.금속 이온은 보통 기질에 맞는 모양의 포켓에 위치합니다.금속 이온은 유기 화학에서 달성하기 어려운 반응을 촉매합니다.
탄산무수분해효소
- CO22 + HO † HCO23
이 반응은 촉매가 없을 때는 매우 느리지만 수산화 이온이 있을 때는 매우 빠릅니다.
- CO2− + OH † HCO−
3
이와 유사한 반응은 탄산무수분해효소에 의해 거의 즉각적으로 나타난다.탄소 무수분해효소의 활성 부위의 구조는 많은 결정 구조에서 잘 알려져 있습니다.그것은 3개의 히스티딘 단위에서 3개의 이미다졸 질소 원자에 의해 조정된 아연 이온으로 구성되어 있다.네 번째 배위 부위는 물 분자가 차지하고 있다.아연 이온의 배위 구는 대략 사면체이다.양전하 아연 이온은 배위수 분자를 분극시켜 이산화탄소에 음전하 수산화물 부분에 의한 친핵성 공격을 빠르게 진행한다.촉매 사이클은 중탄산 이온과 수소[2] 이온을 평형으로 생성합니다.
- HCO23 † HCO−
3 + H+
비타민B의존성효소12
코발트가 함유된12 비타민 B는 두 분자 사이의 메틸기3(-CH) 전달을 촉매하는데, 이것은 유기 반응에 에너지적으로 비용이 많이 드는 과정인 C-C 결합의 분해를 포함한다.금속 이온은 과도 Co-CH3 [27]결합을 형성하여 공정의 활성화 에너지를 낮춥니다.코엔자임의 구조는 도로시 호지킨과 동료들에 의해 결정되었고, 그녀는 이 [28]공로로 노벨 화학상을 받았다.그것은 코발트로 이루어져 있다.II) 코린 고리의 4개의 질소 원자와 이미다졸기로부터의 5번째 질소 원자에 배위된 이온.정지 상태에서는 [29]아데노신의 5' 탄소 원자와 Co-C 시그마 결합이 있다.이것은 자연적으로 발생하는 유기 금속 화합물로, 메티오닌 합성효소에 의해 수행되는 반응과 같은 트랜스-메틸화 반응에서 그 기능을 설명한다.
질소화효소(질소고정)
대기 중 질소의 고정은 질소 원자 사이의 매우 안정적인 삼중 결합을 깨는 것을 수반하기 때문에 매우 에너지 집약적인 과정입니다.효소 질소화효소는 그 과정을 촉매할 수 있는 몇 안 되는 효소 중 하나이다.그 효소는 Rhizobium 박테리아에서 발생한다.활성 부위의 몰리브덴 원자, 질소를 감소시키는 데 필요한 전자를 운반하는 데 관여하는 철-황 클러스터, 마그네슘 ATP의 형태로 풍부한 에너지원의 세 가지 성분이 있습니다.이 마지막은 박테리아와 숙주 식물(종종 콩과) 사이의 상호주의적 공생에 의해 제공됩니다.반응은 다음과 같이 상징적으로 표시될 수 있다.
여기서i P는 무기인산염을 나타낸다.활성 부위의 정확한 구조는 파악하기가 어려웠다.그것은 디니트로겐 분자와 결합할 수 있고 아마도 환원 과정을 [30]시작할 수 있는 MoFeS78 클러스터를 포함하는 것으로 보인다.전자는 연관된 "P" 클러스터에 의해 운반되며, 이 클러스터에는 유황 [31]브릿지에 의해 결합된 두 개의 입방체 FeS44 클러스터가 포함되어 있습니다.
슈퍼옥시드디스무타아제
슈퍼옥시드 이온, O는−
2 분자 산소 감소에 의해 생물학적 시스템에서 생성됩니다.쌍이 없는 전자를 가지고 있기 때문에 유리기로 작용합니다.강력한 산화제입니다.이러한 특성은 슈퍼옥시드 이온을 매우 독성으로 만들고 식세포에 의해 침입 미생물을 죽이기 위해 유리하게 전개된다.그렇지 않으면 세포에 불필요한 손상을 입히기 전에 슈퍼옥시드 이온을 파괴해야 합니다.슈퍼옥사이드 디스뮤타아제 효소는 이 기능을 [32]매우 효율적으로 수행합니다.
산소 원자의 공식 산화 상태는 다음과 같습니다.1h2 중성 pH에서의 용액에서 과산화물 이온은 산소 분자 및 과산화수소와 불균형이 된다.
- 2−
2 O + 2+ H → O2 + HO22
생물학에서는 이런 종류의 반응을 절단 반응이라고 부른다.이것은 산화 및 초산화물 이온의 환원을 모두 포함한다.슈퍼옥사이드 디스뮤타아제(SOD) 그룹은 확산 제한 속도에 [33]근접할 때까지 반응 속도를 증가시킨다.이러한 효소의 작용의 열쇠는 산화제 또는 환원제 역할을 할 수 있는 다양한 산화 상태의 금속 이온입니다.
- 산화:M(n+1)+ + O−
2 → Mn+ + O2 - 삭감:Mn+ + O−
2 + 2 H+ → M(n+1)+ + HO22.
인간 SOD에서 활성 금속은 구리이며, Cu(II) 또는 Cu(I)로서 4개의 히스티딘 잔기에 의해 사면체적으로 배위되어 있다.또한 이 효소는 안정화를 위한 아연 이온을 포함하고 있으며 슈퍼옥사이드 디스뮤타아제(CCS)를 위한 구리 샤페론에 의해 활성화된다.다른 동질효소는 철, 망간 또는 니켈을 포함할 수 있다.Ni-SOD는 이 원소의 특이한 산화 상태인 니켈(III)을 포함하고 있어 특히 흥미롭다.활성 부위 니켈 기하학은 티올레이트(Cys2 및 Cys6) 및 골격 질소(His1 및 Cys2) 배위자를 가진 정사각형 평면 Ni(II)에서 축 방향1 His 측쇄 [34]배위자를 추가한 정사각형 피라미드 Ni(III)로 순환합니다.
클로로필 함유 단백질
엽록소는 광합성에 중요한 역할을 한다.그것은 염소 고리에 둘러싸인 마그네슘을 함유하고 있다.그러나 마그네슘 이온은 광합성 기능에 직접 관여하지 않으며 활성 손실이 거의 없는 다른 2가 이온으로 대체될 수 있다.오히려 광자는 클로로린 고리에 흡수되며, 그 전자구조는 이 목적에 잘 적응된다.
처음에 광자의 흡수는 전자를 Q밴드의 싱글t 상태로 들뜨게 한다.들뜬 상태는 싱글렛 상태에서 병렬 스핀을 가진 두 개의 전자가 있는 트리플렛 상태로 시스템 간 교차합니다.이 종은 사실상 활성산소이고 매우 반응적이며 전자가 엽록소의 엽록소에 인접한 수용체에 전달되도록 합니다.이 과정에서 엽록소가 산화된다.나중에 광합성 주기에서, 엽록소는 다시 환원된다.이러한 감소는 궁극적으로 물로부터 전자를 끌어당겨 최종 산화 산물로 산소 분자를 생산합니다.
수소화효소
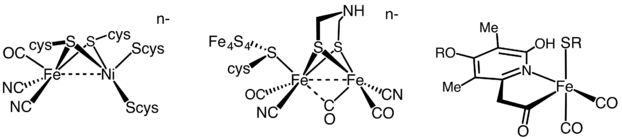
수소화효소는 활성 부위 금속 함량에 따라 철-철 수소화효소, 니켈-철 수소화효소 및 철 수소화효소의 [35]세 가지 다른 유형으로 분류됩니다.모든 수소화효소는 가역2 H 흡수를 촉매하지만, [FeFe] 및 [NiFe] 수소화효소는 진정한 산화 환원 촉매인 반면, H 산화 및+ H 환원을 촉진합니다2.
- H2 2 2+ H + 2 e−
[Fe] 수소화효소는 H의2 가역적 이종 분해 분열을 촉매한다.
- H2 † H+ + H−
리보자임 및 디옥시리보자임
1980년대 초 토마스 체흐와 시드니 알트먼에 의해 리보자임이 발견된 이후 리보자임은 금속효소의 [36]다른 종류로 나타났다.많은 리보자임은 화학적 촉매 작용을 위해 활성 부위에 금속 이온을 필요로 하기 때문에 금속 효소라고 불립니다.또한 금속 이온은 리보자임의 구조적 안정화에 필수적이다.I족 인트론은 촉매 [37]작용에 참여하는 세 개의 금속을 가진 가장 많이 연구된 리보자임이다.다른 알려진 리보자임에는 그룹 II 인트론, RNase P 및 여러 작은 바이러스 리보자임(해머헤드, 헤어핀, HDV 및 VS)과 리보솜의 큰 서브유닛이 포함된다.최근, 4개의 새로운 종류의 리보자임이 발견되었는데, 이들은 모두 스스로 분리되는 [38]리보자임이다.
DNAzymes 또는 촉매 DNA라고도 불리는 디옥시리보자임은 인공 촉매 DNA 분자로, 1994년에 처음 생산되었고 그 이후로 급속히 관심을 끌었다.거의 모든 DNAzymes는 기능하기 위해 금속 이온을 필요로 하기 때문에 금속 효소로 분류된다.리보자임은 대부분 RNA 기질의 분열을 촉매하지만, RNA/DNA 분열, RNA/DNA 결속, 아미노산 인산화와 탈인산화, 탄소-탄소 결합 [40]형성을 포함한 다양한 반응을 촉매할 수 있다.그러나 RNA 분해 반응을 촉매하는 DNA는 가장 광범위하게 연구되고 있다. 1997년에 발견된 10-23 DNA는 치료제로 임상 [41]응용이 가능한 촉매 DNA 중 하나이다.GR-5 DNAzyme(납 특이적),[42] CA1-3 DNAzyme(구리 특이적), 39E DNAzme(우라닐 특이적)[43] 및 NaA43 DNAzyme(나트륨 특이적)를 포함한 여러 금속 특이적 DNAzyme(나트륨 특이적)[44]이 보고되었다.
신호전달금속단백질
칼모듈린
칼모듈린은 신호 전달 단백질의 한 예이다.이것은 4개의 EF-핸드 모티브를 포함하는 작은 단백질로, 각각은 Ca2+ 이온과 결합할 수 있습니다.
EF-핸드 루프에서 칼슘 이온은 오각형 쌍추체 형태로 배위되어 있다.결합에 관여하는 6개의 글루탐산 및 아스파라긴산 잔기는 폴리펩타이드 사슬의 위치 1, 3, 5, 7, 9에 있다.위치 12에는 글루탐산염 또는 아스파르트산염 배위자가 존재하며, 2개의 산소 원자를 제공한다.루프의 아홉 번째 잔기는 반드시 백본의 구조 요건에 의해 글리신이다.칼슘 이온의 배위구에는 카르복실산소 원자만 들어 있고 질소 원자는 들어 있지 않습니다.이것은 칼슘 이온의 단단한 성질과 일치합니다.
단백질은 유연한 "힌지" 영역으로 분리된 두 개의 거의 대칭적인 도메인을 가지고 있습니다.칼슘의 결합은 단백질의 구조 변화를 일으킨다.칼모듈린은 초기 [45][46]자극에 대한 확산성 제2메신저로서 작용함으로써 세포내 시그널링 시스템에 관여한다.
트로포닌
심장근육과 골격근육 모두에서 근력생성은 주로 세포내 칼슘농도의 변화에 의해 제어된다.일반적으로 칼슘이 올라가면 근육이 수축하고 칼슘이 떨어지면 근육이 이완된다.트로포닌은 액틴, 트로포미오신과 함께 칼슘이 결합해 근력을 발생시키는 단백질 복합체이다.
전사 계수
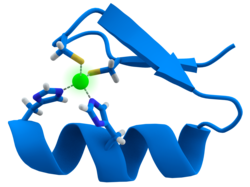
많은 전사 인자는 아연 핑거로 알려진 구조를 포함하고 있는데, 이것은 단백질 영역이 아연 이온 주위로 접히는 구조 모듈입니다.아연은 이 단백질들이 결합하는 DNA와 직접적으로 접촉하지 않는다.대신, 보조 인자는 단단히 접힌 단백질 [47]사슬의 안정성을 위해 필수적이다.이들 단백질에서 아연 이온은 보통 시스테인과 히스티딘 측쇄 쌍에 의해 배위된다.
기타 금속효소
일산화탄소 탈수소효소에는 두 가지 유형이 있습니다. 하나는 철과 몰리브덴을 포함하고 다른 하나는 철과 니켈을 포함합니다.촉매 전략의 유사점과 차이점을 [48]검토했습니다.
Pb2+(납)는 예를 들어 칼모듈린 또는 Zn(아연2+)과 같이 Ca(칼슘)를2+ 대체할 수 있다[49].
관련된 금속에 따라 다음 표에 다른 금속효소가 제시되어 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ Banci L (2013). Sigel A, Sigel H, Sigel RK (eds.). Metallomics and the Cell. Metal Ions in Life Sciences. Vol. 12. Springer. pp. 1–13. doi:10.1007/978-94-007-5561-1_1. ISBN 978-94-007-5561-1. PMID 23595668.
- ^ a b Shriver DF, Atkins PW (1999). "Charper 19, Bioinorganic chemistry". Inorganic chemistry (3rd ed.). Oxford University Press. ISBN 978-0-19-850330-9.
- ^ 2018년 1월 12일 Uniprot의 인간 참조 프로테옴에 접속
- ^ Andreini C, Banci L, Bertini I, Rosato A (November 2006). "Zinc through the three domains of life". Journal of Proteome Research. 5 (11): 3173–8. doi:10.1021/pr0603699. PMID 17081069.
- ^ Thomson AJ, Gray HB (1998). "Bioinorganic chemistry" (PDF). Current Opinion in Chemical Biology. 2 (2): 155–158. doi:10.1016/S1367-5931(98)80056-2. PMID 9667942.
- ^ Waldron KJ, Robinson NJ (January 2009). "How do bacterial cells ensure that metalloproteins get the correct metal?". Nature Reviews. Microbiology. 7 (1): 25–35. doi:10.1038/nrmicro2057. PMID 19079350. S2CID 7253420.
- ^ Carver PL (2013). "Chapter 1. Metal Ions and Infectious Diseases. An Overview from the Clinic". In Sigel A, Sigel H, Sigel RK (eds.). Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences. Vol. 13. Springer. pp. 1–28. doi:10.1007/978-94-007-7500-8_1. ISBN 978-94-007-7499-5. PMID 24470087.
- ^ Wang, MS; Hoegler, KH; Hecht, M (2019). "Unevolved De Novo Proteins Have Innate Tendencies to Bind Transition Metals". Life. 9 (8): 8. doi:10.3390/life9010008. PMC 6463171. PMID 30634485.
- ^ Maret W (February 2010). "Metalloproteomics, metalloproteomes, and the annotation of metalloproteins". Metallomics. 2 (2): 117–25. doi:10.1039/b915804a. PMID 21069142.
- ^ Cangelosi V, Ruckthong L, Pecoraro VL (2017). "Chapter 10. Lead(II) Binding in Natural and Artificial Proteins". In Astrid S, Helmut S, Sigel RK (eds.). Lead: Its Effects on Environment and Health. Metal Ions in Life Sciences. Vol. 17. de Gruyter. pp. 271–318. doi:10.1515/9783110434330-010. ISBN 9783110434330. PMC 5771651. PMID 28731303.
- ^ a b Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8. 그림 25.7, 페이지 1100은 디옥시헤모글로빈의 구조를 나타낸다.
- ^ Stenkamp, R. E. (1994). "Dioxygen and hemerythrin". Chem. Rev. 94 (3): 715–726. doi:10.1021/cr00027a008.
- ^ Wirstam M, Lippard SJ, Friesner RA (April 2003). "Reversible dioxygen binding to hemerythrin". Journal of the American Chemical Society. 125 (13): 3980–7. doi:10.1021/ja017692r. PMID 12656634.
- ^ Karlin K, Cruse RW, Gultneh Y, Farooq A, Hayes JC, Zubieta J (1987). "Dioxygen–copper reactivity. Reversible binding of O2 and CO to a phenoxo-bridged dicopper(I) complex". J. Am. Chem. Soc. 109 (9): 2668–2679. doi:10.1021/ja00243a019.
- ^ Kitajima N, Fujisawa K, Fujimoto C, Morooka Y, Hashimoto S, Kitagawa T, Toriumi K, Tatsumi K, Nakamura A (1992). "A new model for dioxygen binding in hemocyanin. Synthesis, characterization, and molecular structure of the μ-η2:η2-peroxo dinuclear copper(II) complexes, [Cu(Hb(3,5-R2pz)3)]2(O2) (R = isopropyl and Ph)". J. Am. Chem. Soc. 114 (4): 1277–1291. doi:10.1021/ja00030a025.
- ^ Messerschmidt A, Huber R, Wieghardt K, Poulos T (2001). Handbook of Metalloproteins. Wiley. ISBN 978-0-471-62743-2.
- ^ Moore GR, Pettigrew GW (1990). Cytochrome c: Structural and Physicochemical Aspects. Berlin: Springer.
- ^ Sigel A, Sigel H, Sigel RK, eds. (2007). The Ubiquitous Roles of Cytochrome 450 Proteins. Metal Ions in Life Sciences. Vol. 3. Wiley. ISBN 978-0-470-01672-5.
- ^ Ortiz de Montellano P (2005). Cytochrome P450 Structure, Mechanism, and Biochemistry (3rd ed.). Springer. ISBN 978-0-306-48324-0.
- ^ Colman PM, Freeman HC, Guss JM, Murata M, Norris VA, Ramshaw JA, Venkatappa MP (1978). "X-Ray Crystal-Structure Analysis of Plastocyanin at 2.7 Å Resolution". Nature. 272 (5651): 319–324. Bibcode:1978Natur.272..319C. doi:10.1038/272319a0. S2CID 4226644.
- ^ Solomon EI, Gewirth AA, Cohen SL (1986). Spectroscopic Studies of Active Sites. Blue Copper and Electronic Structural Analogs. ACS Symposium Series. Vol. 307. pp. 236–266. doi:10.1021/bk-1986-0307.ch016. ISBN 978-0-8412-0971-8.
- ^ Anderson BF, Baker HM, Dodson EJ, Norris GE, Rumball SV, Waters JM, Baker EN (April 1987). "Structure of human lactoferrin at 3.2-A resolution". Proceedings of the National Academy of Sciences of the United States of America. 84 (7): 1769–73. doi:10.1073/pnas.84.7.1769. PMC 304522. PMID 3470756.
- ^ Rodríguez E, Díaz C (December 1995). "Iron, copper and zinc levels in urine: relationship to various individual factors". Journal of Trace Elements in Medicine and Biology. 9 (4): 200–9. doi:10.1016/S0946-672X(11)80025-8. PMID 8808191.
- ^ Schümann K, Schäfer SG, Forth W (1986). "Iron absorption and biliary excretion of transferrin in rats". Research in Experimental Medicine. Zeitschrift für die Gesamte Experimentelle Medizin Einschliesslich Experimenteller Chirurgie. 186 (3): 215–9. doi:10.1007/BF01852047. PMID 3738220. S2CID 7925719.
- ^ "Biliary excretion of waste products". Archived from the original on 2017-03-26. Retrieved 2017-03-24.
- ^ Lindskog S (1997). "Structure and mechanism of carbonic anhydrase". Pharmacology & Therapeutics. 74 (1): 1–20. doi:10.1016/S0163-7258(96)00198-2. PMID 9336012.
- ^ Sigel A, Sigel H, Sigel RK, eds. (2008). Metal–carbon bonds in enzymes and cofactors. Metal Ions in Life Sciences. Vol. 6. Wiley. ISBN 978-1-84755-915-9.
- ^ "The Nobel Prize in Chemistry 1964". Nobelprize.org. Retrieved 2008-10-06.
- ^ Hodgkin, D. C. (1965). "The Structure of the Corrin Nucleus from X-ray Analysis". Proc. Roy. Soc. A. 288 (1414): 294–305. Bibcode:1965RSPSA.288..294H. doi:10.1098/rspa.1965.0219. S2CID 95235740.
- ^ Orme-Johnson, W. H. (1993). Steifel, E. I.; Coucouvannis, D.; Newton, D. C. (eds.). Molybdenum enzymes, cofactors and model systems. Advances in chemystry, Symposium series no. 535. Washington, DC: American Chemical Society. pp. 257. ISBN 9780841227088.
- ^ Chan MK, Kim J, Rees DC (May 1993). "The nitrogenase FeMo-cofactor and P-cluster pair: 2.2 A resolution structures". Science. 260 (5109): 792–4. doi:10.1126/science.8484118. PMID 8484118.
- ^ Packer, L., ed. (2002). Superoxide Dismutase: 349 (Methods in Enzymology). Academic Press. ISBN 978-0-12-182252-1.
- ^ Heinrich P, Löffler G, Petrides PE (2006). Biochemie und Pathobiochemie (in German). Berlin: Springer. p. 123. ISBN 978-3-540-32680-9.
- ^ Barondeau DP, Kassmann CJ, Bruns CK, Tainer JA, Getzoff ED (June 2004). "Nickel superoxide dismutase structure and mechanism". Biochemistry. 43 (25): 8038–47. doi:10.1021/bi0496081. PMID 15209499.
- ^ Parkin, Alison (2014). "Chapter 5. Understanding and Harnessing Hydrogenases, Biological Dihydrogen Catalysts". In Kroneck, Peter M. H.; Sosa Torres, Martha E. (eds.). The Metal-Driven Biogeochemistry of Gaseous Compounds in the Environment. Metal Ions in Life Sciences. Vol. 14. Springer. pp. 99–124. doi:10.1007/978-94-017-9269-1_5. ISBN 978-94-017-9268-4. PMID 25416392.
- ^ Pyle AM (August 1993). "Ribozymes: a distinct class of metalloenzymes". Science. 261 (5122): 709–14. Bibcode:1993Sci...261..709P. doi:10.1126/science.7688142. PMID 7688142.
- ^ Shan S, Yoshida A, Sun S, Piccirilli JA, Herschlag D (October 1999). "Three metal ions at the active site of the Tetrahymena group I ribozyme". Proceedings of the National Academy of Sciences of the United States of America. 96 (22): 12299–304. Bibcode:1999PNAS...9612299S. doi:10.1073/pnas.96.22.12299. PMC 22911. PMID 10535916.
- ^ Weinberg Z, Kim PB, Chen TH, Li S, Harris KA, Lünse CE, Breaker RR (August 2015). "New classes of self-cleaving ribozymes revealed by comparative genomics analysis". Nature Chemical Biology. 11 (8): 606–10. doi:10.1038/nchembio.1846. PMC 4509812. PMID 26167874.
- ^ Breaker RR, Joyce GF (December 1994). "A DNA enzyme that cleaves RNA". Chemistry & Biology. 1 (4): 223–9. doi:10.1016/1074-5521(94)90014-0. PMID 9383394.
- ^ Silverman SK (May 2015). "Pursuing DNA catalysts for protein modification". Accounts of Chemical Research. 48 (5): 1369–79. doi:10.1021/acs.accounts.5b00090. PMC 4439366. PMID 25939889.
- ^ Santoro SW, Joyce GF (April 1997). "A general purpose RNA-cleaving DNA enzyme". Proceedings of the National Academy of Sciences of the United States of America. 94 (9): 4262–6. Bibcode:1997PNAS...94.4262S. doi:10.1073/pnas.94.9.4262. PMC 20710. PMID 9113977.
- ^ Breaker RR, Joyce GF (December 1994). "A DNA enzyme that cleaves RNA". Chemistry & Biology. 1 (4): 223–9. doi:10.1016/1074-5521(94)90014-0. PMID 9383394.
- ^ Liu J, Brown AK, Meng X, Cropek DM, Istok JD, Watson DB, Lu Y (February 2007). "A catalytic beacon sensor for uranium with parts-per-trillion sensitivity and millionfold selectivity". Proceedings of the National Academy of Sciences of the United States of America. 104 (7): 2056–61. Bibcode:2007PNAS..104.2056L. doi:10.1073/pnas.0607875104. PMC 1892917. PMID 17284609.
- ^ Torabi SF, Wu P, McGhee CE, Chen L, Hwang K, Zheng N, Cheng J, Lu Y (May 2015). "In vitro selection of a sodium-specific DNAzyme and its application in intracellular sensing". Proceedings of the National Academy of Sciences of the United States of America. 112 (19): 5903–8. Bibcode:2015PNAS..112.5903T. doi:10.1073/pnas.1420361112. PMC 4434688. PMID 25918425.
- ^ Stevens FC (August 1983). "Calmodulin: an introduction". Canadian Journal of Biochemistry and Cell Biology. 61 (8): 906–10. doi:10.1139/o83-115. PMID 6313166.
- ^ Chin D, Means AR (August 2000). "Calmodulin: a prototypical calcium sensor". Trends in Cell Biology. 10 (8): 322–8. doi:10.1016/S0962-8924(00)01800-6. PMID 10884684.
- ^ Berg JM (1990). "Zinc finger domains: hypotheses and current knowledge". Annual Review of Biophysics and Biophysical Chemistry. 19 (1): 405–21. doi:10.1146/annurev.bb.19.060190.002201. PMID 2114117.
- ^ Jeoung J, Fesseler J, Goetzl S, Dobbek H (2014). "Chapter 3. Carbon Monoxide. Toxic Gas and Fuel for Anaerobes and Aerobes: Carbon Monoxide Dehydrogenases". In Kroneck PM, Sosa Torres ME (eds.). The Metal-Driven Biogeochemistry of Gaseous Compounds in the Environment. Metal Ions in Life Sciences. Vol. 14. Springer. pp. 37–69. doi:10.1007/978-94-017-9269-1_3. ISBN 978-94-017-9268-4. PMID 25416390.
- ^ Aoki K, Murayama K, Hu N (2017). "Chapter 7. Solid State Structures of Lead Complexes with Relevance for Biological Systems". In Astrid S, Helmut S, Sigel RK (eds.). Lead: Its Effects on Environment and Health. Metal Ions in Life Sciences. Vol. 17. de Gruyter. pp. 123–200. doi:10.1515/9783110434330-007. ISBN 9783110434330. PMID 28731300.
- ^ Romani, Andrea M. P. (2013). "Chapter 4. Magnesium Homeostasis in Mammalian Cells". In Banci, Lucia (ed.). Metallomics and the Cell. Metal Ions in Life Sciences. Vol. 12. Springer. pp. 69–118. doi:10.1007/978-94-007-5561-1_4. ISBN 978-94-007-5561-1. ISSN 1868-0402. PMID 23595671.
- ^ Roth J, Ponzoni S, Aschner M (2013). "Chapter 6. Manganese Homeostasis and Transport". In Banci L (ed.). Metallomics and the Cell. Metal Ions in Life Sciences. Vol. 12. Springer. pp. 169–201. doi:10.1007/978-94-007-5561-1_6. ISBN 978-94-007-5561-1. ISSN 1868-0402. PMC 6542352. PMID 23595673.
- ^ Dlouhy AC, Outten CE (2013). "Chapter 8. The Iron Metallome in Eukaryotic Organisms". In Banci L (ed.). Metallomics and the Cell. Metal Ions in Life Sciences. Vol. 12. Springer. pp. 241–78. doi:10.1007/978-94-007-5561-1_8. ISBN 978-94-007-5561-1. ISSN 1868-0402. PMC 3924584. PMID 23595675.
- ^ Cracan V, Banerjee R (2013). "Chapter 10 Cobalt and Corrinoid Transport and Biochemistry". In Banci L (ed.). Metallomics and the Cell. Metal Ions in Life Sciences. Vol. 12. Springer. doi:10.1007/978-94-007-5561-10_10 (inactive 31 July 2022). ISBN 978-94-007-5561-1. ISSN 1868-0402.
{{cite book}}: CS1 유지 : 2022년 7월 현재 DOI 비활성화 (링크) - ^ Sigel A, Sigel H, Sigel RK, eds. (2008). Nickel and Its Surprising Impact in Nature. Metal Ions in Life Sciences. Vol. 2. Wiley. ISBN 978-0-470-01671-8.
- ^ Sydor AM, Zambie DB (2013). "Chapter 11. Nickel Metallomics: General Themes Guiding Nickel Homeostasis". In Banci L (ed.). Metallomics and the Cell. Metal Ions in Life Sciences. Vol. 12. Springer. doi:10.1007/978-94-007-5561-10_11 (inactive 31 July 2022). ISBN 978-94-007-5561-1. ISSN 1868-0402.
{{cite book}}: CS1 유지 : 2022년 7월 현재 DOI 비활성화 (링크) - ^ Vest KE, Hashemi HF, Cobine PA (2013). "Chapter 13. The Copper Metallome in Eukaryotic Cells". In Banci L (ed.). Metallomics and the Cell. Metal Ions in Life Sciences. Vol. 12. Springer. doi:10.1007/978-94-007-5561-10_12 (inactive 31 July 2022). ISBN 978-94-007-5561-1. ISSN 1868-0402.
{{cite book}}: CS1 유지 : 2022년 7월 현재 DOI 비활성화 (링크) - ^ Maret W (2013). "Chapter 14 Zinc and the Zinc Proteome". In Banci L (ed.). Metallomics and the Cell. Metal Ions in Life Sciences. Vol. 12. Springer. doi:10.1007/978-94-007-5561-10_14 (inactive 31 July 2022). ISBN 978-94-007-5561-1. ISSN 1868-0402.
{{cite book}}: CS1 유지 : 2022년 7월 현재 DOI 비활성화 (링크) - ^ Peackock AF, Pecoraro V (2013). "Chapter 10. Natural and artificial proteins containing cadmium". In Sigel A, Sigel H, Sigel RK (eds.). Cadmium: From Toxicology to Essentiality. Metal Ions in Life Sciences. Vol. 11. Springer. pp. 303–337. doi:10.1007/978-94-007-5179-8_10. ISBN 978-94-007-5178-1. PMID 23430777.
- ^ Freisinger EF, Vasac M (2013). "Chapter 11. Cadmium in Metallothioneins". In Sigel A, Sigel H, Sigel RK (eds.). Cadmium: From Toxicology to Essentiality. Metal Ions in Life Sciences. Vol. 11. Springer. pp. 339–372. doi:10.1007/978-94-007-5179-8_11. ISBN 978-94-007-5178-1. PMID 23430778.
- ^ Mendel, Ralf R. (2013). "Chapter 15. Metabolism of Molybdenum". In Banci, Lucia (ed.). Metallomics and the Cell. Metal Ions in Life Sciences. Vol. 12. Springer. doi:10.1007/978-94-007-5561-10_15 (inactive 31 July 2022). ISBN 978-94-007-5561-1. ISSN 1868-0402.
{{cite book}}: CS1 유지 : 2022년 7월 현재 DOI 비활성화 (링크) - ^ ten Brink, Felix (2014). "Chapter 2. Living on acetylene. A Primordial Energy Source". In Kroneck, Peter M. H.; Sosa Torres, Martha E. (eds.). The Metal-Driven Biogeochemistry of Gaseous Compounds in the Environment. Metal Ions in Life Sciences. Vol. 14. Springer. pp. 15–35. doi:10.1007/978-94-017-9269-1_2. ISBN 978-94-017-9268-4. PMID 25416389.
외부 링크
- 미국 국립 의학 도서관 의학 주제 표제(MeSH)의 금속단백질
- 캐서린 드레넌의 세미나: 금속단백질 스냅샷