맨틀세포림프종
Mantle cell lymphoma| 맨틀세포림프종 | |
|---|---|
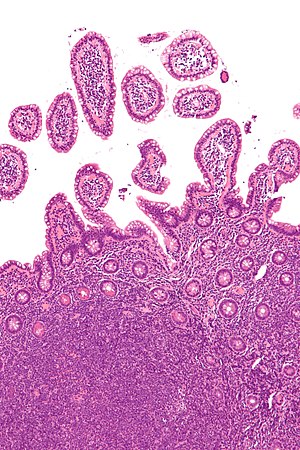 | |
| 회장 말기 생검에서 맨틀 세포 림프종(이미지 하단)을 보여주는 현미경 사진.H&E 염색. | |
| 전문 | 혈액학 및 종양학 |
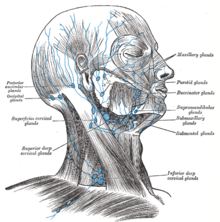
맨틀 세포 림프종(MCL)은 NHL 사례의 약 6%를 구성하는 비호지킨 [1][2]림프종(NHL)의 일종이다.현재 미국에서는 맨틀 세포 림프종 환자가[when?] 약 15,000명에 불과하다.그것은 림프절의 맨틀 존에서 이름을 따왔다.
MCL은 B세포 림프종의 하위 유형으로, 정상적인 생식기 중심 모낭을 둘러싸고 있는 맨틀 존 내의 CD5 양성 항원-네이티브 전생 중심 B세포에 기인한다.MCL 세포는 일반적으로 DNA의 t(11:14)[3] 염색체 전위 때문에 사이클린 D1을 과잉 발현한다.구체적으로는 t(11;14)(q13;q32)[4][5]에 전위치가 있다.
징후 및 증상
진단 시 환자는 일반적으로 60대이며 의사에게 진행성 질환을 보여 줍니다.절반 정도가 발열, 식은땀, 원인 모를 체중 감소(체중의 10% 이상)와 같은 B 증상을 보인다.림프절(예를 들어 목, 겨드랑이 또는 사타구니에 있는 '엉덩이')이나 비장의 종대가 나타난다.골수, 간, 위장관은 비교적 [6]초기에 발병한다.맨틀 세포 림프종은 드물게 모기에 물린 것에 대한 심각한 알레르기 반응과 관련이 있는 것으로 보고되었다.이러한 반응은 통증 및 괴사를 수반할 수 있는 크게 확대된 물린 부위에서 전신 증상(예: 발열, 부은 림프절, 복통 및 설사) 또는 극히 드문 경우 생명을 위협하는 과민증에 이르기까지 광범위한 알레르기 반응을 포함한다.이러한 사례들 중 몇 가지에서, MBA가 초기 발달 맨틀 세포 [7][8]림프종의 징후일 수 있다는 MCL의 진단 전에 모기 물림 알레르기(MBA) 반응이 일어났다.
병인 발생
MCL은 대부분의 암과 마찬가지로 체세포에서 (상속되지 않은) 유전자 돌연변이의 조합 획득에서 발생한다.이것은 악성 B림프구의 복제 확장을 이끈다.유전적 변화를 일으키는 인자는 일반적으로 식별할 수 없으며 림프종 발생에 대한 특별한 위험 요소가 없는 사람에게서 주로 발생한다.후천성 유전 질환이기 때문에 MCL은 전염되지도 [citation needed]않고 유전되지도 않는다.
MCL의 명확한 특징은 악성세포의 비정상적인 증식에 기여하는 세포주기 유전자인 사이클린 D1의 돌연변이와 과잉발현이다.MCL 세포는 또한 약물에 의해 유도되는 아포토시스에 내성이 있을 수 있으며, 화학요법이나 방사선 치료로 치료하기 어렵게 만든다.MCL의 영향을 받는 세포는 두 가지 주요 세포학적 변이(일반적 또는 수포성)와 함께 결절 또는 확산 패턴으로 증식한다.전형적인 경우는 불규칙한 핵을 가진 작고 중간 크기의 세포이다.블라스틱(일명 블라스토이드) 변종은 미세하게 분산된 크로마틴을 가진 중간에서 큰 크기의 세포를 가지고 있으며,[9] 성질이 더 공격적이다.종양세포는 림프절과 비장을 포함한 림프계에 축적되어 쓸모없는 세포는 결국 시스템을 기능장애로 만든다.MCL은 또한 골수의 정상 세포를 대체할 수 있는데, 이것은 정상적인 혈구 [citation needed]생성을 손상시킨다.
진단.
진단에는 일반적으로 수술로 제거된 림프절 부분의 얼룩진 슬라이드가 필요합니다.세포유전학 및 형광인사이트하이브리제이션(FISH)을 포함한 다른 방법들도 일반적으로 사용된다.중합효소 연쇄반응(PCR)과 CER3 클론형 프라이머는 추가 방법이지만 [medical citation needed]덜 자주 사용됩니다.
면역표현형 프로파일은 CD5+(경우 [10]약 80%), CD10-/+로 구성되며, 보통 CD5+와 CD10-.[11] CD20+, CD23-/+(희귀한 경우이지만)입니다.일반적으로 사이클린 D1이 발현된다.SOX11 마커를 검출함으로써 사이클린 D1-음성 맨틀세포 림프종을 진단할 수 있다.맨틀 세포 림프종에 대한 연구는 많은 게으른 림프종과 특정한 공격적인 림프종에 대한 작업과 유사하다.
맨틀 세포 림프종은 골수와 위장관에 자주 관여하는 전신 질환이다.또한 혈액에 존재하는 것으로 특징지어지는 흔하지 않은 백혈병 단계도 있다.이 때문에 말초혈액과 골수 모두 악성세포의 존재 여부를 평가한다.흉부, 복부 및 골반 CT 스캔을 정기적으로 수행합니다.[medical citation needed]
맨틀 세포 림프종은 대장 림프종 용종증을 나타낼 수 있고 대장 내시경 검사는 일반적인 평가의 일부로 간주됩니다.상부 내시경 검사와 목 CT 스캔은 일부 경우에 도움이 될 수 있습니다.일부 쇄골 변형 환자에서는 요추 천자가 척수액의 [medical citation needed]관여를 평가하기 위해 시행된다.
치료법
MCL에 대한 입증된 치료 표준이 없으며, 어떻게 [12]최적으로 치료해야 하는지에 대한 전문가들 간의 합의가 이루어지지 않았습니다.많은 요법들이 이용 가능하고 종종 좋은 반응률을 얻지만, 환자들은 거의 항상 화학요법 후에 질병이 진행됩니다.각 재발은 일반적으로 치료가 더 어렵고 재발은 일반적으로 더 빠릅니다.재발을 치료하는 요법을 이용할 수 있으며, 새로운 접근법이 시험 중이다.앞서 언급한 요인들 때문에 많은 MCL 환자들이 최신 [medical citation needed]치료를 받기 위해 임상시험에 등록한다.
일반적으로 사용되는 치료법에는 화학요법, 면역요법, 방사선 면역요법, 생물학적 약제 등 4가지 종류가 있다.치료 단계는 일반적으로 전방, 진단에 따른 통합, 전방 대응 후(완화를 연장하기 위한) 및 재발이다.재발은 보통 여러 [medical citation needed]번 발생합니다.
화학 요법
항암화학요법은 최전방 치료법으로 널리 사용되고 있으며 부작용으로 재발하지 않는 경우가 많다.대체 화학요법은 때때로 처음 재발했을 때 사용된다.최전방 치료에서는 리턱시맙을 사용한 CHIP이 가장 일반적인 화학요법이며 링거에 의해 외래환자로 종종 투여된다.더 큰 부작용을 동반하는 강력한 화학요법은 HyperCVAD이며, 종종 병원에서 리턱시맵과 함께 제공되며 일반적으로 더 적합한 환자(65세 이상 환자도 있음)에게 주어진다.HyperCVAD는 인기를 얻고 있으며, 특히 리턱시맵에서 유망한 결과를 보이고 있습니다.일부 노인 환자(65세 이상)에게 사용할 수 있지만, 기본 Beta-2-MG 혈액 검사가 정상일 때만 효과가 있는 것으로 보입니다.CHOP 요법보다 완전완화(CR)와 무진행 생존(PFS)이 우수하다.덜 강도 높은 옵션은 리턱시맙을 [13]사용한 벤다무스틴입니다.
두 번째 라인은 보통 리턱시맙과 함께 시클로포스파미드 및/또는 미톡산트론과 결합된 플루다라빈을 포함할 수 있다.클래드리빈과 클로파라빈은 MCL에서 조사되고 있는 다른 두 가지 약물이다. 오래된 약물을 사용하는 비교적 새로운 방법은 PEP-C이다. PEP-C는 비교적 적은 양의 프레디손, 에토포시드, 프로카르바진, 그리고 경구 복용한 시클로포스파미드를 포함한다.존 레너드 박사에 따르면, PEP-C는 항혈관신생 [14][15]특성을 가지고 있을 수 있으며, 이는 그와 그의 동료들이 진행 중인 약물 [16]실험을 통해 시험하고 있는 것이라고 한다.
또 다른 접근법은 질병의 모든 증거를 파괴하기 위해 때로는 전신 조사(TBI)와 결합된 매우 높은 용량의 화학 요법을 사용하는 것이다.이것의 단점은 환자의 전체 면역체계가 파괴되는 것이며, 자가 줄기세포 이식 또는 일치하는 기증자의 면역체계가식(동종 줄기세포 이식)을 사용하여 새로운 면역체계가식(혈액 줄기세포 이식)을 통해 구조를 필요로 한다.2007년 12월 미국 혈액학(재가)회의의 크리스티안 Geisler, 북유럽 Lymphoma Group[17]의 회장에서 수여식은 재판 결과에 의하면 맨틀 세포 림프종은 잠재적으로 집중 chemo-immunotherapy가 줄기 세포 이식에 일 때톤의 첫번째 프레젠테이션에 치료로 치료할 수 있다고 주장했다그질병.[18][19]
이러한 결과는 유럽 맨틀 세포 림프종 네트워크의 대규모 시험에서 확인된 것으로 보이며, 이는 모노클로널 항체와 고용량 ARA-C(시타라빈)를 포함한 유도 요법이 약 65년까지 MCL 환자의 새로운 관리 [20][21]표준이 되어야 한다는 것을 나타낸다.
2013년 4월에 발표된 연구에 따르면 이전에 치료되지 않은 무진장 림프종, 벤다무스틴, 리턱시맙을 가진 환자는 무진행 생존이 증가하고 독성 효과가 [22]적기 때문에 R-CHOP에 대한 바람직한 1차 치료 접근법으로 간주될 수 있다.
면역 요법
면역 기반 치료는 리투산(Rituxan, 유럽 및 호주에서는 Mabthera)이라는 상표명으로 판매되는 리투시맙 모노클로널 항체의 사용에 의해 지배된다.리턱시맵은 MCL에 대해 단일 약제로서 좋은 활성을 가질 수 있지만, 일반적으로 화학요법과 함께 투여되어 반응 기간을 연장한다.방사성 면역 요법으로 알려진 방사성 분자와 결합된 모노클로널 항체에 대한 새로운 변이가 있다[when?].여기에는 Zevalin과 Bexar가 포함됩니다.리턱시맵은 또한 소수의 환자들에게 탈리도마이드와 함께 사용되어 어느 정도 [23]효과가 있었다.이러한 항체 기반의 '수동적' 면역 치료와는 대조적으로, '능동적' 면역 치료 분야는 환자의 면역 체계를 활성화시켜 종양 세포를 구체적으로 제거하려고 시도한다.능동 면역 요법의 예로는 암 백신, 입양 세포 이식, 백신 접종과 자가 줄기세포 이식을 결합한 면역 이식 등이 있다.현재 치료의 기준이[when?] 되는 활성 면역 요법은 없지만, 수많은 임상 실험이 [24][25][26]진행 중입니다.
표적 치료
두 브루 턴로는 티로신 인산화 효소 억제제,는 11월 2013년에는ibrutinib(상표명 Imbruvica, Pharmacyclics LLC)과 10월 2017년에,acalabrutinib(상표명 Calquence, AstraZeneca 제약 회사 LP)미국에서 MCL.[27] 다른 목표 요원들을 치료하는 것을 받은 단백질 분해 효소 복합체 억제제 bortezomib,mTOR 억제제 등(BTKi). 그런Temsirolimus 및 P110 inhibitor 억제제 GS-1101.[citation needed]
2019년 11월 미국에서 자누브루티닙(Brukinsa)이 최소 1건의 사전 [28]치료를 받은 맨틀 세포 림프종 성인의 치료 대상으로 승인되었다.
유전자 치료
Brexucabtagene autoleucel(Tecartus)은 2020년 7월 미국에서 의료용으로 승인되었으며, 재발 또는 난치성 맨틀 세포 림프종이 [29][30][31]있는 성인의 치료에 대한 징후가 있다.2020년 [32]12월 유럽연합에서 의료용으로 승인되었다.
렉수카브타겐 오토류셀의 각 복용량은 림프종 [29]퇴치를 돕기 위해 수용자 자신의 면역 체계를 사용하여 만들어진 맞춤형 치료법이다.백혈구의 일종인 수용자의 T세포는 림프종 [29]세포의 표적화와 사멸을 용이하게 하는 새로운 유전자를 포함하도록 수집되고 유전적으로 변형된다.이 수정된 T세포는 [29]수신자에게 다시 주입됩니다.
예후
최근[when?] 맨틀 세포 림프종(MCL)의 임상적 진보로 표준 치료 알고리즘이 변형되었다.전방 리턱시맙 결합 치료, 젊은 환자의 고용량 시타라빈 기반 유도, 그리고 최근에는 [when?]재발 설정의 브루톤 티로신 키나제(BTK) 억제제가 모두 임상 시험에서 생존 우위를 보였다(Wang 등, 2013년, Eskelund 등, 2016년; Rule 등, 2016년).지난[when?] 15년 동안 이러한 관행은 점차 임상 실무에 포함되었고 실제 데이터는 그에 상응하는 환자 생존율 개선을 관찰했다(Abrahamson 등, 2014; Leux 등, 2014).[33]
MCL의 전체 5년 생존율은 일반적으로 50%([34]어드밴스트 스테이지 MCL)~70%([35]제한 스테이지 MCL)입니다.
MCL을 가진 사람의 예후는 문제가 있고 진행성 질환이 있는 환자들로 인해 지표가 잘 작동하지 않는다.악성 B세포는 림프계를 통해 자유롭게 이동할 수 있고, 따라서 대부분의 환자는 진단 시 III 또는 IV 단계에 있기 때문에 스테이징이 사용되지만 매우 유익하지는 않다.예후는 MCL에서의 단계에 의해 크게 영향을 받지 않으며 전이의 개념은 실제로 [medical citation needed]적용되지 않는다.
맨틀 세포 림프종 국제 예후 지수(MIPI)는 독일/유럽에서 일련의 임상 시험에서 치료된 455명의 진행 단계 MCL 환자의 데이터 세트에서 도출되었다.평가 대상 인구 중 약 18%가 첫 완화에서 고용량 치료와 줄기세포 이식을 받았다.MIPI는 환자를 저위험군(중간 32개월 후속 조치 및 5년 OS 비율 60%)과 중간위험군(중간 생존 51개월) 및 고위험군(중간 생존 29개월)으로 분류할 수 있다.모델에 포함된 4가지 독립적인 예후인자 외에도 세포증식지수(Ki-67)는 추가적인 예후 관련성이 있는 것으로 나타났다.Ki67을 사용할 수 있는 경우 생물학적 MIPI를 [36]계산할 수 있습니다.
MCL은 경계를 넘어 뇌로 들어갈 수 있는 몇 안 되는 NHL 중 하나이지만,[medical citation needed] 그 경우에 치료될 수 있습니다.
연구된 많은 예후 지표들이 있다.예후에서 [medical citation needed]그들의 중요성이나 유용성에 대한 보편적인 동의는 없다.
Ki-67은 세포가 얼마나 빨리 성숙하는지를 나타내는 지표로 약 10%에서 90%의 범위에서 발현된다.비율이 낮을수록 성숙 속도가 느려지고 질병이 나태해진다.캣젠버거 외혈액 2006;107:3407은 다양한 Ki-67 지수를 가진 환자의 하위 집합에 대한 생존 대 시간을 그래프로 나타낸다.그는 61-90% Ki-67의 경우 약 1년, 5-20% Ki-67 지수의 경우 거의 4년의 중간 생존 시간을 보여준다.
MCL 세포 유형은 주관적인 방법으로 예후에 도움을 줄 수 있다.쇄설은 더 큰 세포 유형입니다.확산은 노드를 통해 확산됩니다.결절세포는 결절을 통해 퍼지는 수집된 세포의 작은 그룹입니다.확산과 결절의 행동은 비슷하다.블라스틱은 더 빨리 자라고 장기간의 완화를 얻기가 더 어렵다.어떤 사람들은 시간이 오래 걸리면 비탄성 MCL이 탄성으로 변한다고 생각합니다.대부분의 포도상구균 환자의 생존 기간은 짧지만, 일부 데이터에 따르면 포도상구균 MCL 환자의 25%가 5년까지 생존한다.이는 확산형보다 길고 결절형(약 7년)[medical citation needed]만큼 길다.
베타-2 마이크로글로불린은 주로 이식 환자에게 사용되는 MCL의 또 다른 위험 요소이다.값이 3 미만일 경우 자동 SCT의 경우 전체 생존율이 95%에서 6년으로 산출되며, 이 경우 3개를 초과하면 자동 SCT의 전체 생존율이 44로 가장 높습니다(Khouri 03).이것은 아직 완전히 [medical citation needed]검증되지[when?] 않았다.
NHL 환자에게서 높은 수준의 락틴산탈수소효소(LDH)를 검사하는 것은 어떠한 이유로든 신체 조직이 분해될 때 LDH가 방출되기 때문에 유용하다.NHL을 진단하는 유일한 수단으로 사용될 수는 없지만, 다른 방법으로 진단된 사람들의 종양 부담을 추적하기 위한 대용품이다.정상 범위는 약 100 ~[medical citation needed]190입니다
역학
비호지킨 림프종 사례의 6%는 맨틀 세포 [2]림프종이다.2015년 현재[update], 영향을 받는 남성과 여성의 비율은 약 4:[2]1이다.
참고 항목
레퍼런스
- ^ "Mantle Cell Lymphoma Facts" (PDF). lls.org. Retrieved 10 April 2018.
- ^ a b c Skarbnik AP, Goy AH (January 2015). "Mantle cell lymphoma: state of the art". Clin Adv Hematol Oncol. 13 (1): 44–55. PMID 25679973.
- ^ "t(11;14)(q13;q32) IGH/CCND1". atlasgeneticsoncology.org. Retrieved 10 April 2018.
- ^ Li JY, Gaillard F, Moreau A, et al. (May 1999). "Detection of translocation t(11;14)(q13;q32) in mantle cell lymphoma by fluorescence in situ hybridization". Am. J. Pathol. 154 (5): 1449–52. doi:10.1016/S0002-9440(10)65399-0. PMC 1866594. PMID 10329598.
- ^ Barouk-Simonet E, Andrieux J, Copin MC, et al. (2002). "TPA stimulation culture for improved detection of t(11;14)(q13;q32) in mantle cell lymphoma". Ann. Genet. 45 (3): 165–8. doi:10.1016/S0003-3995(02)01122-X. PMID 12381451.
- ^ Leukemia&Lymphoma Society (2014). "Mantle Cell Lymphoma Facts" (PDF). www.LLS.org.
- ^ Tatsuno K, Fujiyama T, Matsuoka H, Shimauchi T, Ito T, Tokura Y (June 2016). "Clinical categories of exaggerated skin reactions to mosquito bites and their pathophysiology". Journal of Dermatological Science. 82 (3): 145–52. doi:10.1016/j.jdermsci.2016.04.010. PMID 27177994.
- ^ Kyriakidis I, Vasileiou E, Karastrati S, Tragiannidis A, Gompakis N, Hatzistilianou M (December 2016). "Primary EBV infection and hypersensitivity to mosquito bites: a case report". Virologica Sinica. 31 (6): 517–520. doi:10.1007/s12250-016-3868-4. PMC 8193400. PMID 27900557. S2CID 7996104.
- ^ Goy, Andre. "Mantle Cell Lymphoma: An Update for Clinicians". Medscape. Retrieved 18 October 2007.
- ^ 스탠포드 의과대학: '망토세포 림프종, 감별진단' [1]
- ^ Barekman CL, Aguilera NS, Abbondanzo SL (July 2001). "Low-grade B-cell lymphoma with coexpression of both CD5 and CD10. A report of 3 cases". Arch. Pathol. Lab. Med. 125 (7): 951–3. doi:10.5858/2001-125-0951-LGBCLW. PMID 11419985.
- ^ Rajabi B, Sweetenham JW (2015). "Mantle cell lymphoma: observation to transplantation". Ther Adv Hematol. 6 (1): 37–48. doi:10.1177/2040620714561579. PMC 4298490. PMID 25642314.
- ^ "Archived copy" (PDF). Archived from the original (PDF) on 23 June 2017. Retrieved 18 March 2015.
{{cite web}}: CS1 maint: 제목으로 아카이브된 복사(링크) - ^ http://www.asco.org/ASCO/Abstracts+&+Virtual+Meeting/Abstracts?&vmview=abst_detail_view&confID=23&abstractID=104642[인용필수]
- ^ "Archived copy". Archived from the original on 17 April 2008. Retrieved 24 February 2008.
{{cite web}}: CS1 maint: 제목으로 아카이브된 복사(링크)[인용필수] - ^ "Phase II Trial of Anti-Angiogenic Therapy with RT-PEPC in Patients with Relapsed Mantle Cell Lymphoma". 26 June 2018.
{{cite journal}}:Cite 저널 요구 사항journal=(도움말) - ^ "Archived copy". Archived from the original on 16 April 2008. Retrieved 15 February 2008.
{{cite web}}: CS1 maint: 제목으로 아카이브된 복사(링크) - ^ "Mantle Cell Lymphoma is Curable with Intensive Immunochemotherapy". DocGuide.
- ^ [2][인용필수]
- ^ Ye H, Desai A, Huang S, et al. (July 2018). "Paramount therapy for young and fit patients with mantle cell lymphoma: strategies for front-line therapy". J. Exp. Clin. Cancer Res. 37 (1): 150. doi:10.1186/s13046-018-0800-9. PMC 6044039. PMID 30005678.
- ^ Ye H, Desai A, Zeng D, et al. (November 2018). "Frontline Treatment for Older Patients with Mantle Cell Lymphoma". Oncologist. 23 (11): 1337–1348. doi:10.1634/theoncologist.2017-0470. PMC 6291324. PMID 29895632.
- ^ Rummel MJ, Niederle N, Maschmeyer G, et al. (April 2013). "Bendamustine plus rituximab versus CHOP plus rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: an open-label, multicentre, randomised, phase 3 non-inferiority trial". Lancet. 381 (9873): 1203–10. doi:10.1016/S0140-6736(12)61763-2. PMID 23433739. S2CID 27886488.
- ^ Kaufmann H, Raderer M, Wöhrer S, et al. (October 2004). "Antitumor activity of rituximab plus thalidomide in patients with relapsed/refractory mantle cell lymphoma". Blood. 104 (8): 2269–71. doi:10.1182/blood-2004-03-1091. PMID 15166030. S2CID 24548471.
- ^ "Chemotherapy Plus Vaccination to Treat Mantle Cell Lymphoma – NCT00101101". ClinicalTrials.gov. Retrieved 28 February 2016.
- ^ "Chemotherapy Plus Vaccination to Treat Mantle Cell Lymphoma – NCT00005780". ClinicalTrials.gov. Retrieved 28 February 2016.
- ^ "Chemotherapy Plus Vaccination to Treat Mantle Cell Lymphoma – NCT00490529". ClinicalTrials.gov. Retrieved 28 February 2016.
- ^ "FDA approves Imbruvica for rare blood cancers". U.S. Food and Drug Administration (FDA) (Press release). 13 November 2013. "FDA approves Calquence, on October 31, 2017, the Food and Drug Administration granted accelerated approval to acalabrutinib, (AstraZeneca Pharmaceuticals Inc. under license of Acerta Pharma BV) with an indication for the treatment of adults with mantle cell lymphoma (MCL) who have received at least one prior round of therapy" (Press release). Archived from the original on 16 February 2017. Retrieved 15 November 2019.
- ^ "FDA approves therapy to treat patients with relapsed and refractory mantle cell lymphoma supported by clinical trial results showing high response rate of tumor shrinkage". U.S. Food and Drug Administration (FDA) (Press release). 14 November 2019. Retrieved 15 November 2019.
 이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다..
이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다.. - ^ a b c d "FDA Approves First Cell-Based Gene Therapy For Adult Patients with Relapsed or Refractory MCL". U.S. Food and Drug Administration (FDA). 24 July 2020. Retrieved 24 July 2020.
 이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다..
이 문서에는 퍼블릭 도메인에 있는 이 소스로부터의 텍스트가 포함되어 있습니다.. - ^ "Tecartus". U.S. Food and Drug Administration (FDA). 24 July 2020. STN: BL 125703. Retrieved 24 July 2020.
- ^ "U.S. FDA Approves Kite's Tecartus, the First and Only CAR T Treatment for Relapsed or Refractory Mantle Cell Lymphoma" (Press release). Kite Pharma. 24 July 2020. Retrieved 24 July 2020 – via Business Wire.
- ^ "Tecartus EPAR". European Medicines Agency (EMA). Retrieved 25 January 2021.
- ^ 영국 혈액학 저널 2018년 11월 20일
- ^ 최신 값:Herrmann A, Hoster E, Zwingers T, et al. (February 2009). "Improvement of overall survival in advanced stage mantle cell lymphoma". J. Clin. Oncol. 27 (4): 511–8. doi:10.1200/JCO.2008.16.8435. PMID 19075279.
- ^ Leitch HA, Gascoyne RD, Chhanabhai M, Voss NJ, Klasa R, Connors JM (October 2003). "Limited-stage mantle-cell lymphoma". Ann. Oncol. 14 (10): 1555–61. doi:10.1093/annonc/mdg414. PMID 14504058.
- ^ Hoster E, Dreyling M, Klapper W, et al. (January 2008). "A new prognostic index (MIPI) for patients with advanced-stage mantle cell lymphoma". Blood. 111 (2): 558–65. doi:10.1182/blood-2007-06-095331. PMID 17962512.
추가 정보
- Cohen JB, Zain JM, Kahl BS (2017). "Current Approaches to Mantle Cell Lymphoma: Diagnosis, Prognosis, and Therapies". Am Soc Clin Oncol Educ Book. 37 (37): 512–25. doi:10.1200/EDBK_175448. PMID 28561694.
- Dreyling M, Ferrero S, Hermine O (November 2014). "How to manage mantle cell lymphoma". Leukemia. 28 (11): 2117–30. doi:10.1038/leu.2014.171. PMID 24854989. S2CID 22105743.
- Schieber M, Gordon LI, Karmali R (2018). "Current overview and treatment of mantle cell lymphoma". F1000Res. 7: 1136. doi:10.12688/f1000research.14122.1. PMC 6069726. PMID 30109020.