니오비움
Niobium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 니오비움 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 발음 | /naɪˈoʊbiəm/ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 외관 | 산화되면 푸르스름하고 금속성이 희끗희끗한 회색. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 표준 원자량Ar, std(Nb) | 92.90637(1)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 주기율표의 니오비움 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자번호 (Z) | 41 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 그룹 | 5그룹 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 기간 | 5주기 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 블록 | d-블록 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전자 구성 | [Kr] 4d4 5s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 셸당 전자 | 2, 8, 18, 12, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 물리적 성질 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 위상 STP서 | 실체가 있는 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 녹는점 | 2750K(2477°C, 4491°F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 비등점 | 5017K(4744°C, 8571°F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 밀도 (근처 ) | 8.57 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 융해열 | 30kJ/몰 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 기화열 | 689.9 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 어금니열용량 | 24.60 J/(몰·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
증기압
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자성 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 산화 상태 | -3, -1, 0, +1, +2, +3, +4, +5(약산성 산화물) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전기성 | 폴링 척도: 1.6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 이온화 에너지 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자 반지름 | 경험적: 오후 146시 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 공동 반지름 | 164±6시 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 니오비움의 스펙트럼 라인 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 기타 속성 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 자연발생 | 원시적인 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 결정구조 | 신체 중심 입방체(BCc) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 음속 얇은 막대기 | 3480m/초(20°C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 열팽창 | 7.3 µm/(m³K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 열전도도 | 53.7 W/(m³K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전기저항도 | 152 NΩ⋅m(0°C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 자기순서 | 파라자성의 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 영의 계량 | 105 GPA | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전단 계수 | 38개 GPA | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 벌크 계량 | 170 GPA | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 포아송 비율 | 0.40 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 모스 경도 | 6.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 비커즈 경도 | MPa 870–1320 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 브리넬 경도 | MPa 735–2450 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS 번호 | 7440-03-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 역사 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 이름 지정 | 그리스 신화에 나오는 니오베에 이어 탄탈루스의 딸(탄탈룸) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 디스커버리 | 찰스 해쳇(1801) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 제1격리듬 | 크리스티안 빌헬름 블롬스트란트(1864) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 에 의해 구별되는 요소로 인식됨 | 하인리히 로즈 (1844년) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 니오비움의 주 동위 원소 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
니오비움(Niobium, columbium)이라고도 하며, 기호 Nb(구 Cb)와 원자 번호 41을 가진 화학 원소다.니오비움은 옅은 회색, 결정체, 연성 전이 금속이다.퓨어 니오비움은 순수 티타늄과 비슷한 모스 경도 등급을 갖고 있으며 [2]철과 연성도 비슷하다.니오비움은 지구 대기에서 매우 천천히 산화되기 때문에, 니켈에 대한 저자극성 대안으로 보석류에 응용된다.니오비움은 종종 광물과 컬럼바이트에서 발견되는데, 따라서 예전 이름인 "콜럼비움"에서 유래되었다.그 이름은 그리스 신화, 특히 니오베에서 유래되었는데, 그는 탄탈룸의 이름인 탄탈루스의 딸이었다.그 이름은 물리적 성질과 화학적 성질에 있는 두 원소의 큰 유사성을 반영하고 있어 구별이 어렵다.[3]
영국의 화학자 찰스 해쳇은 1801년 탄탈룸과 유사한 새로운 원소를 보고하고 콜럼비아라고 명명했다.1809년 영국의 화학자 윌리엄 하이드 울라스톤은 탄탈룸과 콜럼바륨이 동일하다고 잘못 결론지었다.독일의 화학자 하인리히 로즈는 1846년 탄탈룸 광석이 두 번째 원소를 포함하고 있다고 결정했는데, 이 원소를 니오비움이라고 명명했다.1864년과 1865년에 일련의 과학적 발견으로 니오비움과 컬럼비움이 같은 원소(탄탈룸과 구별되는 것)임을 명확히 하였고, 한 세기 동안 두 명칭을 서로 교환하여 사용하였다.니오비움은 1949년 원소의 이름으로 공식 채택되었지만, 콜럼비아라는 이름은 현재 미국에서 야금용으로 사용되고 있다.
니오비움이 상업적으로 처음 사용된 것은 20세기 초였다.브라질은 니오비움과 페로니오비움의 선두 생산국으로, 니오비움의 60%~70% 철분이 함유된 합금이다.니오비움은 가스관 등 특수강에서 가장 큰 부분인 합금에 주로 사용된다.이러한 합금은 최대 0.1%를 함유하고 있지만, 니오비움이 적은 비율이 강철의 강도를 높여준다.니오비움이 함유된 슈퍼 알로이의 온도 안정성은 제트 엔진과 로켓 엔진에서 사용하기 위해 중요하다.
니오비움은 다양한 초전도 물질에 사용된다.티타늄과 주석도 함유된 초전도 합금은 MRI 스캐너의 초전도 자석에 널리 사용된다.니오비움의 다른 응용 분야로는 용접, 핵 산업, 전자, 광학, 숫자 및 보석 등이 있다.마지막 두 응용에서 양극화에 의해 생성되는 낮은 독성과 발광은 매우 원하는 특성이다.니오비움은 기술적으로 중요한 요소로 간주된다.
역사


니오비움은 1801년 영국의 화학자 찰스 해쳇에 의해 확인되었다.[4][5][6]그는 1734년 미국 코네티컷에서 존 윈드롭 F.R.S(존 윈드롭 더 젊은이의 손자)에 의해 영국으로 보내진 광물 샘플에서 새로운 원소를 발견했고, 이 광물 콜럼바이트와 새로운 원소의 이름을 미국의 시적 이름인 컬럼비아의 이름을 따서 지었다.[7][8][9]해쳇이 발견한 콜럼비움은 아마도 새로운 원소와 탄탈룸의 혼합물이었을 것이다.[7]
이어 컬럼비아(니오비움)와 밀접하게 연관된 탄탈룸의 차이를 두고 상당한 혼란이[10] 있었다.1809년 영국의 화학자 윌리엄 하이드 울라스턴은 밀도 5.918 g/cm의3 콜럼바이트와 8 g/cm3 이상의 탄탈륨에서 파생된 산화물과 밀도 8 g/cm 이상의 탄탈륨을 비교하여 두 산화물 모두 밀도의 차이가 크지만 동일하다고 결론지어서 탄탈룸이라는 이름을 유지했다.[10]이러한 결론은 1846년 독일의 화학자 하인리히 로즈가 탄탈라이트 샘플에 두 가지 다른 원소가 있다고 주장하여 탄탈루스의 아이들의 이름을 따서 니오비움(니오베에서)과 펠로피움(펠롭스에서)이라고 명명함으로써 논란이 되었다.[11][12]이러한 혼란은 탄탈룸과 니오비움 사이에 관찰된 최소한의 차이에서 비롯되었다.주장된 새로운 원소 펠로피움, 일메늄, 디아늄은[13] 사실 니오비움 또는 니오비움과 탄탈륨의 혼합물과 동일했다.[14]
탄탈룸과 니오비움의 차이는 1864년 루이 J뿐만 아니라 크리스티안 빌헬름 블롬스트란드와[14] 앙리 에티엔 사인테 클레어 데빌에 의해 뚜렷이 입증되었다. 1865년[14][15] 일부 화합물의 공식을 결정하고 마침내 1866년 스위스의 화학자 장 샤를 갈리사르 드 마리낙에[16] 의해 이 모든 것이 두 가지 원소만 있다는 것을 증명했다.일메니움 관련 기사는 1871년까지 계속 나왔다.[17]
드 마리낙은 1864년 이 금속을 가장 먼저 준비했는데, 이때 그는 염화 니오비움을 수소 대기에서 가열하여 줄였다.[18]드 마리낙은 1866년까지 탄탈륨이 없는 니오비움을 더 큰 규모로 생산할 수 있었지만, 최초의 상업적 응용인 백열등 필라멘트에 니오비움이 사용된 것은 20세기 초가 되어서였다.[15]이 용도는 니오비움을 녹는점이 높은 텅스텐으로 대체함으로써 빠르게 구식이 되었다.그 니오비움이 강철의 강도를 향상시키는 것은 1920년대에 처음 발견되었으며, 이 용도는 여전히 그 주요 용도로 남아 있다.[15]1961년 미국의 물리학자 유진 쿤즐러와 벨 연구소의 동료들은 니오비움-틴이 강한 전류와 자기장이 있는 곳에서 초전도성을 계속 보인다는 것을 발견했는데,[19] 이는 유용한 고출력 자석과 전력 기계에 필요한 높은 전류와 장을 지원하는 최초의 재료가 되었다.이 발견은 20년이 지난 후에 긴 멀티 스트랜드 케이블의 생산을 가능하게 하여 회전 기계, 입자 가속기 및 입자 감지기를 위한 크고 강력한 전자석을 만들었다.[20][21]
요소 이름 지정
Columbium(기호 "Cb")[22]은 해쳇이 1801년 금속을 발견했을 때 원래 부여한 이름이다.[5]그 이름은 광석의 유형 표본이 미국(콜럼비아)에서 왔다는 것을 반영했다.[23]이 명칭은 1953년부터[24] 미국 화학 협회가 콜럼비움을 타이틀 날짜에 두고 발행한 마지막 논문인 미국 저널에서 계속 사용되었고, 유럽에서 니오비움이 사용되었다.이러한 혼란을 종식시키기 위해 1949년 암스테르담에서 열린 제15차 화학 연합 회의에서 원소 41에 니오비움이라는 이름이 선택되었다.[25]1년 뒤 국제순수응용화학연합(IUPAC)은 콜럼비아라는 명칭이 연대기적으로 우선시됐음에도 불구하고 100년 간의 논란 끝에 이 명칭을 공식 채택했다.[25]이것은 일종의 절충안이었다; IUPAC는 북미의 사용량에 대한 존중으로 울프램 대신 텅스텐을,[25] 유럽인의 사용량에 대한 존중으로 콜롬비아 대신 니오비움을 받아들였다.많은 미국 화학 사회와 정부 기관들이 일반적으로 공식 IUPAC 이름을 사용하는 반면, 일부 금속 학자들과 금속 학회는 여전히 원래의 미국 이름인 "columbium"[26][27][28][29]을 사용한다.
특성.
물리적인
니오비움은 주기율표(표 참조)의 5그룹에 속하는 윤기, 회색, 연성, 파라자성 금속으로, 5그룹에 대한 가장 바깥쪽 쉘 비정형에서 전자적 구성을 가지고 있다.(이는 루테늄(44), 로듐(45), 팔라듐(46) 근처에서 관찰할 수 있다.
| Z | 요소 | 전자/껍질 번호 |
|---|---|---|
| 23 | 바나듐 | 2, 8, 11, 2 |
| 41 | 니오븀 | 2, 8, 18, 12, 1 |
| 73 | 탄탈룸 | 2, 8, 18, 32, 11, 2 |
| 105 | 더브니움 | 2, 8, 18, 32, 32, 11, 2 |
절대영점부터 녹는점까지 체내 중심의 입방결정 구조를 가지고 있다고 생각되지만, 3개의 결정도축을 따라 열팽창에 대한 고해상도 측정 결과 입방구조와 일관성이 없는 음이소트로피가 나타난다.[30]따라서 이 분야에 대한 추가 연구와 발견이 기대된다.
니오비움은 극저온에서 초전도체가 된다.대기압에서는 9.2K로 원소 초전도체의 임계온도가 가장 높다.[31]니오비움은 어떤 원소보다도 자기 침투 깊이가 가장 크다.[31]또 바나듐, 테크네튬과 함께 3원소 타입 II 초전도체 중 하나이다.초전도성 성질은 니오비움 금속의 순도에 크게 의존한다.[32]
매우 순수할 때는 비교적 부드럽고 연성이지만 불순물이 있으면 단단해진다.[33]
이 금속은 열 중성자에 대한 포획 단면이 낮기 때문에 중성자 투명 구조를 원하는 원자력 산업에서 사용된다.[34][35]
케미컬
이 금속은 장시간 실온에서 공기에 노출되면 푸르스름한 색조를 띤다.[36]원소 형태(2,468 °C)의 높은 용해점에도 불구하고 다른 내화금속보다 밀도가 낮다.게다가, 그것은 내식성이 있고 초전도성을 보이며, 유전 산화층을 형성한다.
니오비움은 주기율표인 지르코늄의 전임자보다 약간 덜 전기성이 있고 더 콤팩트한 반면, 란타니드 수축의 결과로 더 무거운 탄탈룸 원자와 사실상 크기가 동일하다.[33]그 결과 니오비움의 화학적 성질은 주기율표에서 니오비움 바로 아래에 나타나는 탄탈륨과 매우 유사하다.[15]비록 그것의 내식성이 탄탈룸만큼 뛰어나지는 않지만, 낮은 가격과 높은 가용성은 화학 공장의 바트 라이닝과 같은 덜 까다로운 용도에 니오비움을 매력적으로 만든다.[33]
동위 원소
지구 지각의 니오비움은 Nb라는 하나의 안정된 동위원소로 구성되어 있다.[37] 2003년까지 적어도 32개의 방사성 동위원소가 합성되었는데, 원자 질량은 81에서 113에 이른다.이 중 가장 안정된 것은 3470만 년의 반감기를 가진 nb이다.가장 안정적이지 않은 것 중 하나는 Nb로 추정 반감기가 30밀리초이다.안정적 Nb보다 가벼운 동위원소는 β+ 붕괴에 의해 붕괴하는 경향이 있고, 무거운 동위원소는 일부 예외로− β 붕괴에 의해 붕괴되는 경향이 있다.81Nb, Nb 및 Nb에는 경미한 β+ 지연 양성자 방출 붕괴 경로가 있고, 전자 포획 및 양전자 방출에 의한 Nb 소멸, β+ 및 β− 붕괴에 의한 Nb 소멸이 있다.[37]
84개에서 104개까지의 원자 질량 범위에서 최소한 25개의 핵 이소머가 설명되었다.이 범위 내에 있는 Nb, Nb, Nb만 등가선을 가지고 있지 않다.니오비움의 이소머 중 가장 안정된 것은 반감기가 16.13년인 nb이다.안정성이 가장 낮은 이소체는 103ns의 반감기를 가진 Nb이다.Nb를 제외한 니오비움의 이소머는 모두 이소메릭 전환이나 베타 붕괴에 의해 붕괴되며, 단전자 포획 분기가 있는 Nb를 제외한다.[37]
발생
니오비움은 20ppm으로 지구 표면에서 34번째로 흔한 원소로 추정된다.[38]어떤 사람들은 지구의 풍요가 훨씬 더 크고, 원소의 높은 밀도가 그것을 지구의 중심부에 집중시켰다고 생각한다.[27]자유 원소는 자연에서 발견되지 않지만, 니오비움은 미네랄의 다른 원소와 결합하여 발생한다.[33]니오비움을 함유한 미네랄도 탄탈룸을 함유하고 있는 경우가 많다.예를 들면 columbite(columbite)가 있다. (Fe,Mn)(Nb,Ta)2O6) 및 콜럼바이트-탄탈라이트(또는 콜탄, (Fe,Mn)(Ta,Nb)2O6).[39]콜럼바이트-탄탈라이트 광물(가장 흔한 종은 컬럼바이트-(Fe)와 탄탈라이트-(Fe)이며 여기서 "-(Fe)"는 망간과[40][41][42][43] 같은 다른 원소보다 철의 우세함을 알려주는 레빈슨 접미사)로 주로 페그마타이트 침입과 알칼리성 침입암에서 부속 광물로 발견된다.칼슘, 우라늄, 토륨, 희토류 원소의 니오베이트가 덜 흔하다.Examples of such niobates are pyrochlore ((Na,Ca)2Nb2O6(OH,F)) (now a group name, with a relatively common example being, e.g., fluorcalciopyrochlore[42][43][44][45][46]) and euxenite (correctly named euxenite-(Y)[42][43][47]) ((Y,Ca,Ce,U,Th)(Nb,Ta,Ti)2O6).이 많은 양의 니오비움 퇴적물은 탄산염(탄산염-실리케이트성 암석)과 화로클로르 성분으로 연관되어 발견되었다.[48]
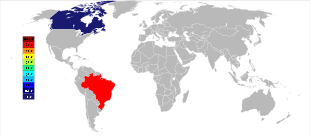
브라질 2개, 캐나다 1개 등 현재 채굴된 3개의 가장 큰 화로클로르 매장량은 1950년대에 발견되었으며, 여전히 니오비움 광물 농축액의 주요 생산국이다.[15]가장 큰 예금은 CBM(Companyhia Brasileira de Metalurgia e Minerazang)이 소유한 브라질 미나스 제라이스 주의 카르보나타이트 침입 내에서 주최되며, 다른 활성 브라질 예금은 고이아스 주의 카탈랑 근처에 위치하고 있으며, 중국 몰리브덴이 소유하기도 한다.[49]이 두 기뢰를 합치면 세계 공급량의 약 88%가 생산된다.[50]브라질은 또한 아마조나스 주의 상 가브리엘 다 카셰이라 근방에 크지만 아직 밝혀지지 않은 예금을 가지고 있으며, 특히 로라이마 주의 몇몇 소규모 예금을 보유하고 있다.[50][51]
세 번째로 큰 니오비움의 생산국은 캐나다 퀘벡주 치쿠티미 인근 생호노레에 있는 카보나타이트가 주최하는 니오벡 광산이며, 마그리스 자원이 소유하고 있다.[52]전 세계 공급량의 7%~10%를 생산한다.[49][50]
생산
다른 광물과의 분리 후에 탄탈룸 TaO와25 니오비움 NBO의25 혼합 산화물들을 얻는다.처리의 첫 번째 단계는 산화물과 불산물의 반응이다.[39]
- Ta2O5 + 14 HF → 2 H2[TaF7] + 5 H2O
- Nb2O5 + 10 HF → 2 H2[NbOF5] + 3 H2O
드 마리낙이 개발한 제1차 산업규모 분리는 복합 니오비움과 탄탈룸 플루오르화물, 이포칼륨 옥시펜타플루오로노바이트 단수화물(K2[NbOF5]····의 서로 다른 용해도를 이용한다.HO2) 및 헵타플루오르탄탈산칼륨(K27[TaF])을 물에 담근다.새로운 공정은 사이클로헥사논과 같은 유기 용제에 의해 수용액에서 불소를 액체로 추출하는 것을 사용한다.[39]복합 니오비움과 탄탈룸 플루오르화물은 물과 함께 유기용매로부터 분리하여 추출하고 불화칼륨을 첨가하여 불화칼륨 복합체를 생성하거나, 오산화 암모니아로 침전한다.[53]
- H2[NbOF5] + 2 KF → K2[NbOF5]↓ + 2 HF
그 다음:
- 2 H2[NbOF5] + 10 NHOH4 → NbOH25 + 10 NHF4 + 7 HO2
금속 니오비움의 감소에는 몇 가지 방법이 사용된다.K2[NbOF5]와 염화 나트륨의 용융 혼합물의 전기분해는 한 가지이고, 다른 하나는 나트륨과 함께 불소를 감소시키는 것이다.이 방법으로 비교적 높은 순도의 니오비움을 얻을 수 있다.대규모 생산에서 NbO는25 수소나 탄소로 감소한다.[53]알루미늄 발열 반응에서 산화철과 산화 니오비움의 혼합물은 알루미늄과 반응한다.
- 3 Nb2O5 + Fe2O3 + 12 Al → 6 Nb + 2 Fe + 6 Al2O3
질산나트륨과 같은 소량의 산화제가 첨가되어 반응을 강화시킨다.그 결과는 철강 생산에 사용되는 철과 니오비움의 합금인 산화알루미늄과 페로니오비움이다.[54][55]페로니오비움은 60~70%의 니오비움을 함유하고 있다.[49]산화철 없이 알루미늄의 열처리 공정이 니오비움을 생산하는데 사용된다.초전도 합금의 등급에 도달하기 위해서는 추가적인 정화가 필요하다.진공 상태에서 녹는 전자빔은 니오비움의 양대 유통업체가 사용하는 방법이다.[56][57]
2013년[update] 현재 브라질의 CBMM은 전 세계 니오비움 생산량의 85%를 점유하고 있다.[58]미국 지질조사국은 2005년 38,700톤에서 2006년 44,500톤으로 생산량이 증가한 것으로 추정하고 있다.[59][60]전 세계의 자원은 440만 톤으로 추정된다.[60]1995년부터 2005년까지 10년 동안 생산량은 1995년 17,800톤에서 시작해 두 배 이상 증가했다.[61]2009~2011년 생산량은 연 6만3000톤으로 안정적이었고,[62] 2012년에는 연 5만톤으로 소폭 감소했다.[63]
| 나라 | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | 2019 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 160 | 230 | 290 | 230 | 200 | 200 | 200 | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | |
| 30,000 | 22,000 | 26,000 | 29,000 | 29,900 | 35,000 | 40,000 | 57,300 | 58,000 | 58,000 | 58,000 | 58,000 | 63,000 | 53,100 | 53,000 | 58,000 | 57,000 | 60,700 | 59,000 | 88,900 | |
| 2,290 | 3,200 | 3,410 | 3,280 | 3,400 | 3,310 | 4,167 | 3,020 | 4,380 | 4,330 | 4,420 | 4,630 | 5,000 | 5,260 | 5,000 | 5,750 | 6,100 | 6,980 | 7,700 | 6,800 | |
| ? | 50 | 50 | 13 | 52 | 25 | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | |
| ? | ? | 5 | 34 | 130 | 34 | 29 | ? | ? | 4 | 10 | 29 | 30 | 20 | ? | ? | ? | ? | ? | ||
| 35 | 30 | 30 | 190 | 170 | 40 | 35 | ? | ? | ? | ? | ? | ? | ? | ? | 29 | 104 | 122 | 181 | 150 | |
| 28 | 120 | 76 | 22 | 63 | 63 | 80 | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | |
| 월드 | 32,600 | 25,600 | 29,900 | 32,800 | 34,000 | 38,700 | 44,500 | 60,400 | 62,900 | 62,900 | 62,900 | 63,000 | 50,100 | 59,400 | 59,000 | 64,300 | 63,900 | 69,100 | 68,200 | 97,000 |
적은 액수는 말라위의 칸니카 예금(칸니카 광산)에서 발견된다.
화합물
많은 면에서 니오비움은 탄탈룸과 지르코늄과 비슷하다.그것은 고온에서 대부분의 비금속과 반응한다; 상온에서는 불소, 150 °C에서는 염소, 200 °C에서는 수소를, 그리고 400 °C에서는 질소와 반응하며, 종종 중간 및 비스토리치계 제품이다.[33]그 금속은 200 °C에서 공기로 산화되기 시작한다.[53]그것은 알칼리 용융에 의한 부식과 아쿠아 리지아, 염산, 황산, 질산, 인산 등의 산물에 의한 부식을 억제한다.[33]니오비움은 불산과 불산/니트산 혼합물의 공격을 받는다.
니오비움은 +5에서 -1까지의 모든 공식 산화 상태를 나타내지만, 가장 흔한 화합물은 +5 상태에서 니오비움을 가진다.[33]특징적으로 산화 상태의 화합물은 5+ 이하의 표시 Nb-Nb 결합을 나타낸다.수용액에서 니오비움은 +5 산화 상태만 나타낸다.또한 쉽게 가수분해되기 쉬우며 수성 Nb산화물의 침전 때문에 염산, 황산, 질산, 인산 등의 희석 용액에 거의 용해되지 않는다.[56]nb(V)도 용해성 폴리오소니오베이트 종의 형성으로 인해 알칼리성 매체에 약간 용해된다.[67][68]
산화물, 니오바이트, 황화물
니오비움은 산화 상태 +5(NbO25),[69] +4(NbO2), +3(NbO
2
3),[53] 희소 산화 상태 +2(NbO)에서 산화물을 형성한다.[70]가장 흔한 것은 거의 모든 니오비움 화합물과 합금의 전조인 오산화질소다.[53][71]니오바이트는 기본적인 수산화물 용액에 오산화물을 녹이거나 알칼리 금속 산화물에 녹여 생성된다.리튬 니오베이트(LiNbO3)와 란타넘 니오베이트(LaNbO4)가 대표적이다.리튬 니오베이트는 삼각으로 왜곡된 페로브스카이트와 같은 구조인 반면 란타넘 니오베이트는 외로운 NbO3−
4 이온을 함유하고 있다.[53]층층이 쌓인 황화 니오비움(NbS2)도 알려져 있다.[33]
재료는 350℃ 이상에서 에산화 니오비움의 열분해로 생산되는 산화 니오비움(V) 화학증기 증착 또는 원자층 증착 공정의 박막으로 코팅할 수 있다.[72][73]
할리데스
니오비움은 +5와 +4의 산화 상태뿐만 아니라 다양한 부분치하 화합물에서도 할로겐화물을 형성한다.[53][56]펜타할리드(NBX
5)는 팔면체 Nb 센터를 특징으로 한다.니오비움 펜타플루오리드(NbF5)는 녹는점이 79.0℃인 흰색 고형분이고, 니오비움 펜타클로라이드(NbCl5)는 녹는점이 203.4℃인 노란색(왼쪽 이미지 참조)이다.둘 다 NBOCl과3 같은 산화물과 옥시할라이드를 주기 위해 가수 분해된다.펜타클로라이드는 니오보세 디클로로이드(CH
5
5)
2NbCl과
2 같은 유기측정 화합물을 생성하는 데 사용되는 다용도 시약이다.[74]테트라할리드(NBX
4)는 Nb-Nb 결합을 가진 어두운 색상의 폴리머로, 예를 들어 흑색하이오성 니오비움 테트라플루오리드(NbF4)와 갈색 니오비움 테트라클로라이드(NbCl4) 등이 있다.
니오비움의 음이온 할로겐화합물은 부분적으로 펜타할라이드의 루이스 산도 때문에 잘 알려져 있다.가장 중요한 것은 광석에서 Nb와 Ta를 분리하는 중간인 2−[NbF7]이다.[39]이 헵타플루오라이드는 탄탈룸 화합물보다 옥소펜타플루오라이드를 더 쉽게 형성하는 경향이 있다.다른 할로겐화 복합체로는 팔면체[NbCl6]−가 있다.
- NbCl210 + 2Cl− → 2 [NbCl6]−
원자 번호가 낮은 다른 금속과 마찬가지로, 다양한 감소 할로겐화 군집 이온이 알려져 있는데, 대표적인 예는 [NbCl618]4−[75]이다.
질화물 및 탄화물
니오비움의 다른 이항 화합물로는 저온에서 초전도체가 되어 적외선 검출기에 사용되는 니오비움 질화수소(NbN)가 있다.[76]주 나이오비움 카바이드(Niobium carbide)는 NbC로, 절삭 공구 비트에 상업적으로 사용되는 매우 단단하고 내화성이 강한 세라믹 소재다.
적용들
2006년 채굴된 니오비움 44,500톤 중 90%가 고급 구조용 강재에 사용된 것으로 추정된다.두 번째로 큰 애플리케이션은 슈퍼앨로이즈다.[77]니오비움 합금 초전도체와 전자부품이 세계 생산에서 차지하는 비중은 매우 적다.[77]
철강생산
니오비움은 강철에 효과적인 마이크로 알로이징 원소로, 그 안에서 니오비움 카바이드와 니오비움 질화물을 형성한다.[27]이 화합물들은 곡물 정제, 재분배 및 강수 경화를 지연시킨다.이러한 효과는 강인성, 강도, 조형성 및 용접성을 증가시킨다.[27]마이크로앨로이드 스테인리스강 내에서는 니오비움 함량이 작지만([78]0.1% 미만) 현대 자동차에서 구조적으로 널리 사용되는 고강도 저알로이강에 중요한 추가가 된다.[27]Niobium은 때로 고도로 마모에 강한 기계 구성품과 칼에 상당히 높은 양으로 사용되며, 도가니 CPM S110V 스테인리스강에서는 최대 3%까지 사용된다.[79]
이와 같은 니오비움 합금은 파이프라인 건설에 종종 사용된다.[80][81]
슈퍼앨로이스
니오비움의 양은 니켈, 코발트 및 철 기반 슈퍼앨로이에서 제트 엔진 구성품, 가스 터빈, 로켓 서브 어셈블리, 터보 충전기 시스템, 내열성 및 연소 장비와 같은 용도에 [78]6.5%나 되는 비율로 사용된다.니오비움은 초알로이의 곡물 구조 내에서 경화 γ' 단계를 촉진한다.[82]
슈퍼할로이(Superalloy)의 한 예로 약 50% 니켈, 18.6% 크롬, 18.5% 철, 5% 니오비움, 3.1% 몰리브덴, 0.9% 티타늄, 0.4% 알루미늄으로 구성된 Iconfel 718이 있다.[83][84]예를 들어, 이러한 슈퍼 알로이는 제미니 프로그램을 위한 고급 공기 프레임 시스템에 사용되었다.아폴로 서비스 모듈의 노즐에는 또 다른 니오비움 합금이 사용되었다.니오비움은 400 °C 이상의 온도에서 산화되기 때문에 이러한 용도에 대해서는 합금이 부서지는 것을 방지하기 위한 보호 코팅이 필요하다.[85]
니오븀 기반 합금
C-103 합금은 1960년대 초 와창 주식회사와 보잉사가 공동으로 개발하였다.듀폰, 유니온 카바이드, 제너럴 일렉트릭, 그리고 몇몇 다른 회사들은 주로 냉전과 우주 경쟁에 의해 주도된 nb 기반 합금을 동시에 개발하고 있었다.니오븀 89%, 하프늄 10%, 티타늄 1%로 구성되며, 아폴로 달 모듈 메인 엔진 등 액체 로켓 추진기 노즐에 사용된다.[85]

스페이스X가 팰컨9 로켓의 상단을 위해 개발한 멀린 진공 엔진 시리즈의 노즐은 니오비움 합금으로 만들어졌다.[86]
산소와 함께 니오비움의 반응성은 진공이나 불활성 대기에서 작용해야 하므로 생산 비용과 난이도가 크게 증가한다.당시 새로운 공정인 진공 아크 리멜팅(VAR)과 전자 빔 용해(EBM)는 니오비움과 기타 반응성 금속의 개발을 가능하게 했다.C-103을 산출한 프로젝트는 1959년 "C 시리즈"(아마도 컬럼비아에서 온 것 같다)에 256개나 되는 실험용 니오비움 합금으로 시작되었는데, 이 합금은 단추처럼 녹여 시트로 압착할 수 있었다.Wah Chang은 핵 등급의 지르코늄 합금에서 정제된 하프늄 재고를 가지고 있었는데, 그것은 상업적으로 사용하기를 원했다.C 시리즈 합금의 103번째 실험 구성인 Nb-10Hf-1Ti는 조형성과 고온 성질의 조합이 가장 우수했다.Wah Chang은 EBM과 VAR을 사용하여 1961년에 C-103의 처음 500파운드 열을 시트마다 조작했다.의도된 용도에는 터빈 엔진과 액체 금속 열 교환기가 포함되었다.그 시대의 경쟁사인 니오비움 합금은 팬스틸 메탈릭사의 FS85(Nb-10W-28Ta-1Zr) Cb129Y(Nb-10W-10Hf-0)를 포함했다.Wah Chang과 Boeing의 2Y, Union Carbide의 Cb752(Nb-10W-2.5Zr), Superficer Tube Co.[85]의 Nb1Zr.
초전도 자석
니오비움-게르마늄(NbGe
3), 니오비움-틴(NbSn
3)은 물론 니오비움-티타늄 합금이 초전도 자석을 위한 제2종 초전도체 와이어로 사용된다.[87][88]이 초전도 자석은 입자 가속기뿐만 아니라 자기 공명 영상과 핵 자기 공명 기구에 사용된다.[89]예를 들어 대형 하드론 충돌기는 초전도 가닥 600t을 사용하며, 국제열핵실험로에서는 NbSn3 가닥 600t, NbTi 가닥 250t을 추정해 사용한다.[90]1992년 한 해에만 10억 달러 이상의 임상 자기 공명 영상 시스템이 니오븀-티타늄 와이어로 건설되었다.[20]
기타 초전도체
프리전자 레이저 FLASH(TESLA 선형가속기 프로젝트 취소 결과)와 XFEL에 사용되는 초전도 무선 주파수(SRF) 캐비티는 순수 니오비움으로 만들어진다.[91]페르밀랍의 한 크라이오모듈 팀은 순수 니오비움으로 만든 1.3GHz 9셀 SRF 캐비티를 개발하기 위해 플래시 프로젝트와 동일한 SRF 기술을 사용했다.캐비티는 국제 선형 충돌기의 30km(19mi) 선형 입자 가속기에 사용될 것이다.[92]SLAC 국립가속기 연구소의 LCLS-II와 페르밀랍의 PIP-II에도 동일한 기술이 사용될 것이다.[93]
초전도 니오비움 질화수소 볼로미터의 높은 감도는 그들을 THZ 주파수 대역에서 전자기 방사선에 이상적인 검출기로 만든다.이러한 검출기는 서브밀리미터 망원경, 남극 망원경, 수신기 실험실 망원경, 에이펙스에서 시험되었으며, 현재 허셜 우주 관측소에 탑재된 HIFI 기구에서 사용되고 있다.[94]
기타 용도
전기 세라믹스
페로 전기인 리튬 니오베이트는 휴대전화와 광학 변조기, 표면 음향파 소자 제조 등에 광범위하게 사용된다.그것은 탄탈산리튬이나 타이탄산바륨과 같은 ABO3 구조 철전체에 속한다.[95]탄탈룸 콘덴서 대안으로 니오비움 콘덴서가 있지만 탄탈룸 콘덴서가 여전히 우세하다.[96]더 높은 굴절률을 얻기 위해 유리에 니오비움을 첨가해 더 얇고 가벼운 교정안경을 만들 수 있다.
저자극성 용법: 의약품 및 보석류
Niobium과 일부 Niobium 합금은 생리학적으로 불활성적이고 저칼로르겐성이다.이 때문에 니오비움은 페이스메이커와 같은 보철물과 임플란트 장치에 사용된다.[97]수산화나트륨으로 처리된 니오비움은 오서 통합을 돕는 다공성 층을 형성한다.[98]
티타늄, 탄탈룸, 알루미늄과 마찬가지로 니오비움을 가열하고 양극화("반응성 금속 양극화")하여 저농축 특성이 매우 바람직한 보석류용 무지개빛 색상을 다양하게 연출할 수 있다.[99][100][101]
숫자론
니오비움은 종종 은이나 금과 함께 기념주화에 귀중한 금속으로 사용된다.예를 들어, 오스트리아는 2003년부터 일련의 은 니오비움 유로 동전들을 생산했다; 이 동전들의 색깔은 얇은 양극 산화층에 의한 빛의 회절에 의해 만들어진다.[102]2012년에는 동전 중앙에 파란색, 녹색, 갈색, 보라색, 보라색, 보라색 또는 노란색 등 다양한 색상을 보여주는 10개의 동전을 구입할 수 있다.두 가지 다른 예로는 2004년 오스트리아 €25 150년 세메링 알파인 철도 기념 [103]코인과 2006년 오스트리아 €25 유럽 위성항법 기념 코인이 있다.[104]오스트리아의 민트는 라트비아를 위해 2004년부터 비슷한 종류의 동전을 생산했고,[105] 2007년에 한 동전을 생산했다.[106]2011년 캐나다 왕립 조폐국은 니오비움이 선택적으로 산화된 5달러짜리 스털링 실버와 니오비움 동전인 헌터의 달(Hunter's Moon[107])을 생산하기 시작해 두 동전이 정확히 일치하지 않는 독특한 마무리를 만들었다.

기타
고압 나트륨 증기등의 아크 튜브 씰은 니오비움으로 만들어지며, 때로는 지르코늄의 1%를 합금하기도 한다. 니오비움은 열팽창 계수가 매우 유사하여, 인시 함유된 뜨거운 액체 나트륨과 나트륨 증기의 화학적 공격이나 감소를 억제하는 반투명 물질인 소결 알루미나 아크 튜브 세라믹과 일치한다.작동 램프를 제거한다.[108][109][110]
니오비움은 일부 안정화된 등급의[111] 스테인리스강을 위한 아크용접봉과 일부 물탱크의 음극방호 시스템을 위한 양극에 사용되며, 이 양극은 보통 백금으로 도금된다.[112][113]
니오비움은 프로판의 선택적 산화에 의한 아크릴산 생산을 위한 고성능 이기종 촉매의 중요한 성분이다.[114][115][116][117]
니오비움은 파커 솔라 프로브의 태양 코로나 입자 수용기 모듈의 고전압 와이어를 만드는 데 사용된다.[118]
주의사항
| 위험 | |
|---|---|
| NFPA 704(화재 다이아몬드) | |
니오비움은 알려진 생물학적 역할이 없다.니오비움 분진은 눈과 피부에 자극을 주며 잠재적인 화재 위험성이 있는 반면, 더 큰 규모의 원소 니오비움은 생리학적으로 불활성(따라서 저자극성)이며 무해하다.보석류에서 자주 사용되며 일부 의료용 임플란트에서는 사용 테스트를 거쳤다.[119][120]
니오븀 함유 화합물은 대부분의 사람들이 거의 접하지 못하지만 독성이 있는 것도 있다.수용성인 두 가지 화학물질인 니오바이트와 염화 니오비움에 대한 장단기 피폭은 쥐를 대상으로 실험됐다.니오비움 펜타클로라이드 또는 니오바이트를 한 번 주사하여 치료한 쥐는 10~100mg/kg 사이의 치사량(LD50)을 나타낸다.[121][122][123]경구 투여의 경우 독성이 더 낮다; 쥐를 대상으로 한 연구에서는 940mg/kg의 7일 후 LD가50 나왔다.[121]
참조
- ^ "Standard Atomic Weights: Niobium". CIAAW. 2017.
- ^ G.V. Samsonov, ed. (1968). "Mechanical Properties of the Elements". Handbook of the physicochemical properties of the elements. New York, USA: IFI-Plenum. pp. 387–446. doi:10.1007/978-1-4684-6066-7_7. ISBN 978-1-4684-6066-7. Archived from the original on 2 April 2015.
- ^ 크냅, 브라이언(2002년).프랑슘과 폴로늄으로.대서양 유럽 출판사, 페이지 40.ISBN 0717256774.
- ^ Hatchett, Charles (1802). "An analysis of a mineral substance from North America, containing a metal hitherto unknown". Philosophical Transactions of the Royal Society of London. 92: 49–66. doi:10.1098/rspl.1800.0045. JSTOR 107114.
- ^ a b Hatchett, Charles (1802), "Outline of the Properties and Habitudes of the Metallic Substance, lately discovered by Charles Hatchett, Esq. and by him denominated Columbium", Journal of Natural Philosophy, Chemistry, and the Arts, I (January): 32–34.
- ^ Hatchett, Charles (1802). "Eigenschaften und chemisches Verhalten des von Charles Hatchett entdeckten neuen Metalls, Columbium" [Properties and chemical behavior of the new metal, columbium, (that was) discovered by Charles Hatchett]. Annalen der Physik (in German). 11 (5): 120–122. Bibcode:1802AnP....11..120H. doi:10.1002/andp.18020110507.
- ^ a b Noyes, William Albert (1918). A Textbook of Chemistry. H. Holt & Co. p. 523.
- ^ Percival, James (January 1853). "Middletown Silver and Lead Mines". Journal of Silver and Lead Mining Operations. 1: 186. Retrieved 24 April 2013.
- ^ Griffith, William P.; Morris, Peter J. T. (2003). "Charles Hatchett FRS (1765–1847), Chemist and Discoverer of Niobium". Notes and Records of the Royal Society of London. 57 (3): 299–316. doi:10.1098/rsnr.2003.0216. JSTOR 3557720. S2CID 144857368.
- ^ a b Wollaston, William Hyde (1809). "On the Identity of Columbium and Tantalum". Philosophical Transactions of the Royal Society. 99: 246–252. doi:10.1098/rstl.1809.0017. JSTOR 107264. S2CID 110567235.
- ^ Rose, Heinrich (1844). "Ueber die Zusammensetzung der Tantalite und ein im Tantalite von Baiern enthaltenes neues Metall". Annalen der Physik (in German). 139 (10): 317–341. Bibcode:1844AnP...139..317R. doi:10.1002/andp.18441391006.
- ^ Rose, Heinrich (1847). "Ueber die Säure im Columbit von Nordamérika". Annalen der Physik (in German). 146 (4): 572–577. Bibcode:1847AnP...146..572R. doi:10.1002/andp.18471460410.
- ^ Kobell, V. (1860). "Ueber eine eigenthümliche Säure, Diansäure, in der Gruppe der Tantal- und Niob- verbindungen". Journal für Praktische Chemie. 79 (1): 291–303. doi:10.1002/prac.18600790145.
- ^ a b c Marignac, Blomstrand; Deville, H.; Troost, L.; Hermann, R. (1866). "Tantalsäure, Niobsäure, (Ilmensäure) und Titansäure". Fresenius' Journal of Analytical Chemistry. 5 (1): 384–389. doi:10.1007/BF01302537. S2CID 97246260.
- ^ a b c d e Gupta, C. K.; Suri, A. K. (1994). Extractive Metallurgy of Niobium. CRC Press. pp. 1–16. ISBN 978-0-8493-6071-8.
- ^ Marignac, M. C. (1866). "Recherches sur les combinaisons du niobium". Annales de chimie et de physique (in French). 4 (8): 7–75.
- ^ Hermann, R. (1871). "Fortgesetzte Untersuchungen über die Verbindungen von Ilmenium und Niobium, sowie über die Zusammensetzung der Niobmineralien (Further research about the compounds of ilmenium and niobium, as well as the composition of niobium minerals)". Journal für Praktische Chemie (in German). 3 (1): 373–427. doi:10.1002/prac.18710030137.
- ^ "Niobium". Universidade de Coimbra. Archived from the original on 10 December 2007. Retrieved 5 September 2008.
- ^ 게발레 외 연구진(1993)은 150킬로암페어 전류와 8.8 테슬라의 자기장에서 임계점을 부여한다.
- ^ a b Geballe, Theodore H. (October 1993). "Superconductivity: From Physics to Technology". Physics Today. 46 (10): 52–56. Bibcode:1993PhT....46j..52G. doi:10.1063/1.881384.
- ^ Matthias, B. T.; Geballe, T. H.; Geller, S.; Corenzwit, E. (1954). "Superconductivity of Nb3Sn". Physical Review. 95 (6): 1435. Bibcode:1954PhRv...95.1435M. doi:10.1103/PhysRev.95.1435.
- ^ Kòrösy, F. (1939). "Reaction of Tantalum, Columbium and Vanadium with Iodine". Journal of the American Chemical Society. 61 (4): 838–843. doi:10.1021/ja01873a018.
- ^ Nicholson, William, ed. (1809), The British Encyclopedia: Or, Dictionary of Arts and Sciences, Comprising an Accurate and Popular View of the Present Improved State of Human Knowledge, vol. 2, Longman, Hurst, Rees, and Orme, p. 284.
- ^ Ikenberry, L.; Martin, J. L.; Boyer, W. J. (1953). "Photometric Determination of Columbium, Tungsten, and Tantalum in Stainless Steels". Analytical Chemistry. 25 (9): 1340–1344. doi:10.1021/ac60081a011.
- ^ a b c Rayner-Canham, Geoff; Zheng, Zheng (2008). "Naming elements after scientists: an account of a controversy". Foundations of Chemistry. 10 (1): 13–18. doi:10.1007/s10698-007-9042-1. S2CID 96082444.
- ^ Clarke, F. W. (1914). "Columbium Versus Niobium". Science. 39 (995): 139–140. Bibcode:1914Sci....39..139C. doi:10.1126/science.39.995.139. JSTOR 1640945. PMID 17780662.
- ^ a b c d e Patel, Zh.; Khul'ka K. (2001). "Niobium for Steelmaking". Metallurgist. 45 (11–12): 477–480. doi:10.1023/A:1014897029026. S2CID 137569464.
- ^ Norman N., Greenwood (2003). "Vanadium to dubnium: from confusion through clarity to complexity". Catalysis Today. 78 (1–4): 5–11. doi:10.1016/S0920-5861(02)00318-8.
- ^ "ASTM A572 / A572M-18, Standard Specification for High-Strength Low-Alloy Columbium-Vanadium Structural Steel". ASTM International, West Conshohocken. 2018. Retrieved 12 February 2020.
- ^ Bollinger, R. K.; White, B. D.; Neumeier, J. J.; Sandim, H. R. Z.; Suzuki, Y.; dos Santos, C. A. M.; Avci, R.; Migliori, A.; Betts, J. B. (2011). "Observation of a Martensitic Structural Distortion in V, Nb, and Ta". Physical Review Letters. 107 (7): 075503. Bibcode:2011PhRvL.107g5503B. doi:10.1103/PhysRevLett.107.075503. PMID 21902404.
- ^ a b Peiniger, M.; Piel, H. (1985). "A Superconducting Nb3Sn Coated Multicell Accelerating Cavity". IEEE Transactions on Nuclear Science. 32 (5): 3610–3612. Bibcode:1985ITNS...32.3610P. doi:10.1109/TNS.1985.4334443. S2CID 23988671.
- ^ Salles Moura, Hernane R.; Louremjo de Moura, Louremjo (2007). "Melting And Purification of Niobium". AIP Conference Proceedings. 927 (927): 165–178. Bibcode:2007AIPC..927..165M. doi:10.1063/1.2770689.
- ^ a b c d e f g h Nowak, Izabela; Ziolek, Maria (1999). "Niobium Compounds: Preparation, Characterization, and Application in Heterogeneous Catalysis". Chemical Reviews. 99 (12): 3603–3624. doi:10.1021/cr9800208. PMID 11849031.
- ^ Jahnke, L. P.; Frank, R. G.; Redden, T. K. (1960). "Columbium Alloys Today". Metal Progr. 77 (6): 69–74. OSTI 4183692.
- ^ Nikulina, A. V. (2003). "Zirconium-Niobium Alloys for Core Elements of Pressurized Water Reactors". Metal Science and Heat Treatment. 45 (7–8): 287–292. Bibcode:2003MSHT...45..287N. doi:10.1023/A:1027388503837. S2CID 134841512.
- ^ Lide, David R. (2004). "The Elements". CRC Handbook of Chemistry and Physics (85th ed.). CRC Press. pp. 4–21. ISBN 978-0-8493-0485-9.
- ^ a b c Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "The NUBASE evaluation of nuclear and decay properties", Nuclear Physics A, 729: 3–128, Bibcode:2003NuPhA.729....3A, doi:10.1016/j.nuclphysa.2003.11.001
- ^ Emsley, John (2001). "Niobium". Nature's Building Blocks: An A-Z Guide to the Elements. Oxford, England: Oxford University Press. pp. 283–286. ISBN 978-0-19-850340-8.
- ^ a b c d Soisson, Donald J.; McLafferty, J. J.; Pierret, James A. (1961). "Staff-Industry Collaborative Report: Tantalum and Niobium". Industrial and Engineering Chemistry. 53 (11): 861–868. doi:10.1021/ie50623a016.
- ^ "Columbite-(Fe): Mineral information, data and localities". www.mindat.org.
- ^ "Tantalite-(Fe): Mineral information, data and localities". www.mindat.org.
- ^ a b c Burke, Ernst A.J. (2008). "The use of suffixes in mineral names" (PDF). Elements. 4 (2): 96. Retrieved 7 December 2019.
- ^ a b c "CNMNC". nrmima.nrm.se. Archived from the original on 10 August 2019. Retrieved 6 October 2018.
- ^ "Pyrochlore Group: Mineral information, data and localities". www.mindat.org.
- ^ "Fluorcalciopyrochlore: Mineral information, data and localities". www.mindat.org.
- ^ http://rruff.info/uploads/AM62_403.pdf[bare URL PDF]
- ^ "Euxenite-(Y): Mineral information, data and localities". www.mindat.org.
- ^ Lumpkin, Gregory R.; Ewing, Rodney C. (1995). "Geochemical alteration of pyrochlore group minerals: Pyrochlore subgroup" (PDF). American Mineralogist. 80 (7–8): 732–743. Bibcode:1995AmMin..80..732L. doi:10.2138/am-1995-7-810.
- ^ a b c Kouptsidis, J.; Peters, F.; Proch, D.; Singer, W. "Niob für TESLA" (PDF) (in German). Deutsches Elektronen-Synchrotron DESY. Archived from the original (PDF) on 17 December 2008. Retrieved 2 September 2008.
- ^ a b c Alvarenga, Darlan (9 April 2013). "'Monopólio' brasileiro do nióbio gera cobiça mundial, controvérsia e mitos" [Brazilian niobium 'monopoly' brings about the world's greed, controversy, and myths]. G1 (in Portuguese). São Paulo. Retrieved 23 May 2016.
- ^ Siqueira-Gay, Juliana; Sánchez, Luis E. (2020). "Keep the Amazon niobium in the ground". Environmental Science & Policy. 111: 1–6. doi:10.1016/j.envsci.2020.05.012. ISSN 1462-9011. S2CID 219469278.
- ^ "Magris Resources, officially owner of Niobec" (Press release). Niobec. 23 January 2015. Retrieved 23 May 2016.
- ^ a b c d e f g Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). "Niob". Lehrbuch der Anorganischen Chemie (in German) (91–100 ed.). Walter de Gruyter. pp. 1075–1079. ISBN 978-3-11-007511-3.
- ^ Tither, Geoffrey (2001). Minerals, Metals and Materials Society (ed.). Progress in Niobium Markets and Technology 1981–2001 (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). ISBN 978-0-9712068-0-9. Archived from the original (PDF) on 17 December 2008.
- ^ Dufresne, Claude; Goyette, Ghislain (2001). Minerals, Metals and Materials Society (ed.). The Production of Ferroniobium at the Niobec mine 1981–2001 (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). ISBN 978-0-9712068-0-9. Archived from the original (PDF) on 17 December 2008.
- ^ a b c Agulyansky, Anatoly (2004). The Chemistry of Tantalum and Niobium Fluoride Compounds. Elsevier. pp. 1–11. ISBN 978-0-444-51604-6.
- ^ Choudhury, Alok; Hengsberger, Eckart (1992). "Electron Beam Melting and Refining of Metals and Alloys". The Iron and Steel Institute of Japan International. 32 (5): 673–681. doi:10.2355/isijinternational.32.673.
- ^ Lucchesi, Cristane; Cuadros, Alex (April 2013), "Mineral Wealth", Bloomberg Markets (paper), p. 14
- ^ Papp, John F. "Niobium (Columbium)" (PDF). USGS 2006 Commodity Summary. Retrieved 20 November 2008.
- ^ a b Papp, John F. "Niobium (Columbium)" (PDF). USGS 2007 Commodity Summary. Retrieved 20 November 2008.
- ^ Papp, John F. "Niobium (Columbium)" (PDF). USGS 1997 Commodity Summary. Retrieved 20 November 2008.
- ^ Niobium (Colombium) 미국 지질조사국, 광물 상품 요약, 2011년 1월
- ^ 니오비움(콜롬비움) 미국 지질조사국, 광물품 요약서, 2016년 1월
- ^ Cunningham, Larry D. (5 April 2012). "USGS Minerals Information: Niobium (Columbium) and Tantalum". Minerals.usgs.gov. Retrieved 17 August 2012.
- ^ "Niobium (Columbium) and Tantalum Statistics and Information U.S. Geological Survey".
- ^ "Nigeria: Production volume of niobium".
- ^ Deblonde, Gauthier J. -P.; Chagnes, Alexandre; Bélair, Sarah; Cote, Gérard (1 July 2015). "Solubility of niobium(V) and tantalum(V) under mild alkaline conditions". Hydrometallurgy. 156: 99–106. doi:10.1016/j.hydromet.2015.05.015. ISSN 0304-386X.
- ^ Nyman, May (2 August 2011). "Polyoxoniobate chemistry in the 21st century". Dalton Transactions. 40 (32): 8049–8058. doi:10.1039/C1DT10435G. ISSN 1477-9234. PMID 21670824.
- ^ Pubchem. "Niobium oxide Nb2O5 – PubChem". pubchem.ncbi.nlm.nih.gov. Retrieved 29 June 2016.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ Cardarelli, Francois (2008). Materials Handbook. Springer London. ISBN 978-1-84628-668-1.
- ^ Rahtu, Antti (2002). Atomic Layer Deposition of High Permittivity Oxides: Film Growth and In Situ Studies (Thesis). University of Helsinki. hdl:10138/21065. ISBN 952-10-0646-3.
- ^ Maruyama, Toshiro (1994). "Electrochromic Properties of Niobium Oxide Thin Films Prepared by Chemical Vapor Deposition". Journal of the Electrochemical Society. 141 (10): 2868–2871. Bibcode:1994JElS..141.2868M. doi:10.1149/1.2059247.
- ^ Lucas, C. R.; Labinger, J. A.; Schwartz, J. (1990). Robert J. Angelici (ed.). Dichlorobis(η5-Cyclopentadienyl)Niobium(IV). Inorganic Syntheses. Vol. 28. New York. pp. 267–270. doi:10.1002/9780470132593.ch68. ISBN 978-0-471-52619-3.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ Verevkin, A.; Pearlman, A.; Slstrokysz, W.; Zhang, J.; et al. (2004). "Ultrafast superconducting single-photon detectors for near-infrared-wavelength quantum communications". Journal of Modern Optics. 51 (12): 1447–1458. doi:10.1080/09500340410001670866.
- ^ a b Papp, John F. "Niobium (Columbium ) and Tantalum" (PDF). USGS 2006 Minerals Yearbook. Retrieved 3 September 2008.
- ^ a b Heisterkamp, Friedrich; Carneiro, Tadeu (2001). Minerals, Metals and Materials Society (ed.). Niobium: Future Possibilities – Technology and the Market Place (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). ISBN 978-0-9712068-0-9. Archived from the original (PDF) on 17 December 2008.
- ^ "Datasheet CPM S110V" (PDF). Crucible Industries LLC. Retrieved 20 November 2017.
- ^ Eggert, Peter; Priem, Joachim; Wettig, Eberhard (1982). "Niobium: a steel additive with a future". Economic Bulletin. 19 (9): 8–11. doi:10.1007/BF02227064. S2CID 153775645.
- ^ Hillenbrand, Hans-Georg; Gräf, Michael; Kalwa, Christoph (2 May 2001). "Development and Production of High Strength Pipeline Steels" (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). Archived from the original (PDF) on 5 June 2015.
- ^ Donachie, Matthew J. (2002). Superalloys: A Technical Guide. ASM International. pp. 29–30. ISBN 978-0-87170-749-9.
- ^ Bhadeshia, H. k. d. h. "Nickel Based Superalloys". University of Cambridge. Archived from the original on 25 August 2006. Retrieved 4 September 2008.
- ^ Pottlacher, G.; Hosaeus, H.; Wilthan, B.; Kaschnitz, E.; Seifter, A. (2002). "Thermophysikalische Eigenschaften von festem und flüssigem Inconel 718". Thermochimica Acta (in German). 382 (1––2): 55–267. doi:10.1016/S0040-6031(01)00751-1.
- ^ a b c Hebda, John (2 May 2001). "Niobium alloys and high Temperature Applications" (PDF). Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). Archived from the original (PDF) on 17 December 2008.
- ^ Dinardi, Aaron; Capozzoli, Peter; Shotwell, Gwynne (2008). Low-cost Launch Opportunities Provided by the Falcon Family of Launch Vehicles (PDF). Fourth Asian Space Conference. Taipei. Archived from the original (PDF) on 15 March 2012.
- ^ Lindenhovius, J.L.H.; Hornsveld, E. M.; Den Ouden, A.; Wessel, W. A. J.; et al. (2000). "Powder-in-tube (PIT) Nb/sub 3/Sn conductors for high-field magnets". IEEE Transactions on Applied Superconductivity. 10 (1): 975–978. Bibcode:2000ITAS...10..975L. doi:10.1109/77.828394. S2CID 26260700.
- ^ Nave, Carl R. "Superconducting Magnets". Georgia State University, Department of Physics and Astronomy. Retrieved 25 November 2008.
- ^ Glowacki, B. A.; Yan, X. -Y.; Fray, D.; Chen, G.; Majoros, M.; Shi, Y. (2002). "Niobium based intermetallics as a source of high-current/high magnetic field superconductors". Physica C: Superconductivity. 372–376 (3): 1315–1320. arXiv:cond-mat/0109088. Bibcode:2002PhyC..372.1315G. doi:10.1016/S0921-4534(02)01018-3. S2CID 118990555.
- ^ Grunblatt, G.; Mocaer, P.; Verwaerde Ch.; Kohler, C. (2005). "A success story: LHC cable production at ALSTOM-MSA". Fusion Engineering and Design (Proceedings of the 23rd Symposium of Fusion Technology). 75–79 (2): 3516. Bibcode:2005ITAS...15.3516M. doi:10.1016/j.fusengdes.2005.06.216. S2CID 41810761.
- ^ Lilje, L.; Kako, E.; Kostin, D.; Matheisen, A.; et al. (2004). "Achievement of 35 MV/m in the superconducting nine-cell cavities for TESLA". Nuclear Instruments and Methods in Physics Research Section A: Accelerators, Spectrometers, Detectors and Associated Equipment. 524 (1–3): 1–12. arXiv:physics/0401141. Bibcode:2004NIMPA.524....1L. doi:10.1016/j.nima.2004.01.045. S2CID 2141809.
- ^ The International Linear Collider Technical Design Report 2013. International Linear Collider. 2013. Retrieved 15 August 2015.
- ^ "ILC-type cryomodule makes the grade". CERN Courier. IOP Publishing. 27 November 2014. Retrieved 15 August 2015.
- ^ Cherednichenko, Sergey; Drakinskiy, Vladimir; Berg, Therese; Khosropanah, Pourya; et al. (2008). "A Hot-electron bolometer terahertz mixers for the Herschel Space Observatory". Review of Scientific Instruments. 79 (3): 0345011–03451010. Bibcode:2008RScI...79c4501C. doi:10.1063/1.2890099. PMID 18377032.
- ^ Volk, Tatyana; Wohlecke, Manfred (2008). Lithium Niobate: Defects, Photorefraction and Ferroelectric Switching. Springer. pp. 1–9. ISBN 978-3-540-70765-3.
- ^ Pozdeev, Y. (1991). "Reliability comparison of tantalum and niobium solid electrolytic capacitors". Quality and Reliability Engineering International. 14 (2): 79–82. doi:10.1002/(SICI)1099-1638(199803/04)14:2<79::AID-QRE163>3.0.CO;2-Y.
- ^ Mallela, Venkateswara Sarma; Ilankumaran, V.; Srinivasa Rao, N. (1 January 2004). "Trends in Cardiac Pacemaker Batteries". Indian Pacing Electrophysiol J. 4 (4): 201–212. PMC 1502062. PMID 16943934.
- ^ Godley, Reut; Starosvetsky, David; Gotman, Irena (2004). "Bonelike apatite formation on niobium metal treated in aqueous NaOH". Journal of Materials Science: Materials in Medicine. 15 (10): 1073–1077. doi:10.1023/B:JMSM.0000046388.07961.81. PMID 15516867. S2CID 44988090.
- ^ Biason Gomes, M. A.; Onofre, S.; Juanto, S.; Bulhões, L. O. de S. (1991). "Anodization of niobium in sulphuric acid media". Journal of Applied Electrochemistry. 21 (11): 1023–1026. doi:10.1007/BF01077589. S2CID 95285286.
- ^ Chiou, Y. L. (1971). "A note on the thicknesses of anodized niobium oxide films". Thin Solid Films. 8 (4): R37–R39. Bibcode:1971TSF.....8R..37C. doi:10.1016/0040-6090(71)90027-7.
- ^ Azevedo, C. R. F.; Spera, G.; Silva, A. P. (2002). "Characterization of metallic piercings that caused adverse reactions during use". Journal of Failure Analysis and Prevention. 2 (4): 47–53. doi:10.1361/152981502770351860.
- ^ Grill, Robert; Gnadenberge, Alfred (2006). "Niobium as mint metal: Production–properties–processing". International Journal of Refractory Metals and Hard Materials. 24 (4): 275–282. doi:10.1016/j.ijrmhm.2005.10.008.
- ^ "25 Euro – 150 Years Semmering Alpine Railway (2004)". Austrian Mint. Archived from the original on 21 July 2011. Retrieved 4 November 2008.
- ^ "150 Jahre Semmeringbahn" (in German). Austrian Mint. Archived from the original on 20 July 2011. Retrieved 4 September 2008.
- ^ "Neraža – mēs nevarējām atrast meklēto lapu!" (in Latvian). Bank of Latvia. Archived from the original on 9 January 2008. Retrieved 19 September 2008.
- ^ "Neraža – mēs nevarējām atrast meklēto lapu!" (in Latvian). Bank of Latvia. Archived from the original on 22 May 2009. Retrieved 19 September 2008.
- ^ "$5 Sterling Silver and Niobium Coin – Hunter's Moon (2011)". Royal Canadian Mint. Retrieved 1 February 2012.
- ^ Henderson, Stanley Thomas; Marsden, Alfred Michael; Hewitt, Harry (1972). Lamps and Lighting. Edward Arnold Press. pp. 244–245. ISBN 978-0-7131-3267-0.
- ^ Eichelbrönner, G. (1998). "Refractory metals: crucial components for light sources". International Journal of Refractory Metals and Hard Materials. 16 (1): 5–11. doi:10.1016/S0263-4368(98)00009-2.
- ^ Michaluk, Christopher A.; Huber, Louis E.; Ford, Robert B. (2001). Minerals, Metals and Materials Society (ed.). Niobium and Niobium 1% Zirconium for High Pressure Sodium (HPS) Discharge Lamps. Niobium Science & Technology: Proceedings of the International Symposium Niobium 2001 (Orlando, Florida, USA). ISBN 978-0-9712068-0-9.
- ^ 미국 특허 5254836, 오카다, 유우지; 고바야시, 도시히코; 사사베, 히로시; 아오키, 요시미쓰; 니시자와, 마코토; 엔도, 슌지, "페라이트 스테인리스 용접봉으로 아크 용접하는 방법"이 1993년 10월 19일 발행되었다.
- ^ Moavenzadeh, Fred (14 March 1990). Concise Encyclopedia of Building and Construction Materials. MIT Press. pp. 157–. ISBN 978-0-262-13248-0. Retrieved 18 February 2012.
- ^ Cardarelli, François (9 January 2008). Materials handbook: a concise desktop reference. Springer. pp. 352–. ISBN 978-1-84628-668-1. Retrieved 18 February 2012.
- ^ Hävecker, Michael; Wrabetz, Sabine; Kröhnert, Jutta; Csepei, Lenard-Istvan; Naumann d'Alnoncourt, Raoul; Kolen'Ko, Yury V; Girgsdies, Frank; Schlögl, Robert; Trunschke, Annette (2012). "Surface chemistry of phase-pure M1 MoVTeNb oxide during operation in selective oxidation of propane to acrylic acid" (PDF). Journal of Catalysis. 285: 48–60. doi:10.1016/j.jcat.2011.09.012. hdl:11858/00-001M-0000-0012-1BEB-F.
- ^ Amakawa, Kazuhiko; Kolen'Ko, Yury V; Villa, Alberto; Schuster, Manfred E/; Csepei, Lénárd-István; Weinberg, Gisela; Wrabetz, Sabine; Naumann d'Alnoncourt, Raoul; Girgsdies, Frank; Prati, Laura; Schlögl, Robert; Trunschke, Annette (2013). "Multifunctionality of Crystalline MoV(TeNb) M1 Oxide Catalysts in Selective Oxidation of Propane and Benzyl Alcohol". ACS Catalysis. 3 (6): 1103. doi:10.1021/cs400010q. hdl:11858/00-001M-0000-000E-FA39-1.
- ^ Csepei, Lénárd-István (2011). Kinetic studies of propane oxidation on Mo and V based mixed oxide catalysts. Technische Universität Berlin. pp. 157–166. doi:10.14279/depositonce-2972.
- ^ Naumann d'Alnoncourt, Raoul; Csepei, Lénárd-István; Hävecker, Michael; Girgsdies, Frank; Schuster, Manfred E; Schlögl, Robert; Trunschke, Annette (2014). "The reaction network in propane oxidation over phase-pure MoVTeNb M1 oxide catalysts" (PDF). Journal of Catalysis. 311: 369–385. doi:10.1016/j.jcat.2013.12.008. hdl:11858/00-001M-0000-0014-F434-5.
- ^ Dr. Tony Case (24 August 2018). Scientist Interview: Dr. Tony Case (Parker Solar Probe). Archived from the original on 7 November 2021. Retrieved 24 August 2018.
- ^ Vilaplana, J.; Romaguera, C.; Grimalt, F.; Cornellana, F. (1990). "New trends in the use of metals in jewellery". Contact Dermatitis. 25 (3): 145–148. doi:10.1111/j.1600-0536.1991.tb01819.x. PMID 1782765. S2CID 30201028.
- ^ Vilaplana, J.; Romaguera, C. (1998). "New developments in jewellery and dental materials". Contact Dermatitis. 39 (2): 55–57. doi:10.1111/j.1600-0536.1998.tb05832.x. PMID 9746182. S2CID 34271011.
- ^ a b Haley, Thomas J.; Komesu, N.; Raymond, K. (1962). "Pharmacology and toxicology of niobium chloride". Toxicology and Applied Pharmacology. 4 (3): 385–392. doi:10.1016/0041-008X(62)90048-0. PMID 13903824.
- ^ Downs, William L.; Scott, James K.; Yuile, Charles L.; Caruso, Frank S.; et al. (1965). "The Toxicity of Niobium Salts". American Industrial Hygiene Association Journal. 26 (4): 337–346. doi:10.1080/00028896509342740. PMID 5854670.
- ^ Schroeder, Henry A.; Mitchener, Marian; Nason, Alexis P. (1970). "Zirconium, Niobium, Antimony, Vanadium and Lead in Rats: Life term studies" (PDF). Journal of Nutrition. 100 (1): 59–68. doi:10.1093/jn/100.1.59. PMID 5412131. S2CID 4444415. Archived from the original (PDF) on 19 February 2020.
외부 링크
| 위키미디어 커먼즈에는 니오비움과 관련된 미디어가 있다. |
| 무료 사전인 위키트리노에서 니오비움을 찾아봐라. |
- 로스 알라모스 국립 연구소 – 니오비움
- 탄탈룸니오비움국제학습센터
- 입자 가속기용 니오비움(ILC. 2005)
- . Encyclopædia Britannica (11th ed.). 1911.
- Gilman, D. C.; Peck, H. T.; Colby, F. M., eds. (1905). . New International Encyclopedia (1st ed.). New York: Dodd, Mead.
- 주기율표 비디오에서 니오비움(Niobium at the Periody Table of Videos (University of Nottingham)