표준 원자량
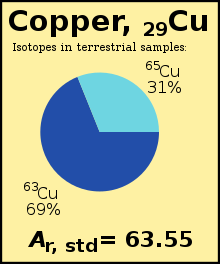
Standard atomic weight화학 원소의 표준 원자량(원소 "E"의 경우 기호r A°(E))는 지구상 각 동위원소의 풍부함으로 가중된 해당 원소의 모든 동위원소 상대 동위원소 질량의 가중 산술 평균이다.예를 들어, 동위원소 Cu(Ar = 62.929)는 지구상 구리의 69%를 구성하고 나머지는 Cu(Ar = 64.927)이다.
상대 동위원소 질량은 무차원 양이기 때문에 이 가중 평균도 무차원이다.원자질량상수라고도 하는 달톤을 곱하면 질량의 측정값(치수 M)으로 변환할 수 있습니다.
과학자들이 사용한 원자량 개념의 다양한 변형(Ar, 상대 원자량이라고도 함) 중에서 표준 원자량(Ar°)은가장 일반적이고 실용적입니다.각 화학 원소의 표준 원자량은 원소의 자연적이고 안정적인 지상 선원을 기반으로 국제순수응용화학연합(IUPAC)의 동위원소 풍부성 및 원자량 위원회(CIAW)에 의해 결정되고 발표된다.이 정의는 지구의 많은 대표적인 원천에서 추출한 샘플의 사용을 명시하고, 그 값을 의약품 및 과학 연구 등 실제 물질에 대한 "원자량"으로 널리 사용할 수 있도록 한다.원소의 비표준 원자량은 특정 고고학 현장의 특정 뼈에 있는 탄소의 원자량과 같은 소스 및 샘플에 고유하다.표준 원자량은 화학자가 지구로부터 많은 무작위 샘플로부터 얻을 것으로 예상할 수 있는 원자량의 범위까지 그러한 값의 평균을 낸다.이 범위는 일부 표준 원자량 값에 대해 주어진 구간 표기법의 근거이다.
알려진 118개의 화학 원소 중 80개는 안정적인 동위원소를 가지고 있고 84개는 이러한 지구 환경 값을 가지고 있다.일반적으로 이러한 값은 예를 들어 헬륨r: A°(그는) = 4.002602(2)이다."(2)"는 4.002602±0.000002로 표시된 마지막 자릿수의 불확실성을 나타냅니다.IUPAC는 5개의 유효 수치로 반올림된 요약 값도 발표한다.헬륨의r, abridged 경우 A°(그는) = 4.0026.
13개 원소의 경우 표본 발생원이 다른 붕괴 이력을 가지고 있기 때문에 표본은 이 값을 기준으로 분산된다.예를 들어 퇴적암의 탈륨(Tl)은 화성암이나 화산가스와는 동위원소 구성이 다르다.이들 원소의 경우 표준 원자량은 A°로r 표기된다.Tl) = [132.38, 204.39]이러한 간격을 두고 IUPAC는 요구가 적은 상황에 대해서도 통상적인 값을 공개합니다.탈륨의 경우r, conventional A°(Tl) = 204.38.
정의.
표준 원자량은 상대 원자량의 특별한 값이다.이는 지구 지각과 대기의 국지적 환경에서 상대 원자 질량의 "권장 값"으로 정의되며, IUPAC 원자 중량 및 동위원소 풍부성 위원회(CIAW)[2]가 결정한다.일반적으로 다른 선원의 값은 선원의 다른 방사능 이력으로 인해 자연 변동의 영향을 받는다.따라서 표준 원자량은 표본 또는 선원의 범위에서 예상되는 원자량 범위이다.선원을 지상 원점으로만 제한함으로써 CIAAW가 결정한 값은 편차가 적고, 실제로 세계 물질에서 발견되어 사용되는 상대 원자 질량(원자량)에 대한 보다 정확한 값이다.
CIAAW가 공표한 값은 대량 계산에 사용되며 때로는 법적으로 요구되기도 한다.값은 불확실성이 있거나(괄호 안에 표시), 또는 기대 간격입니다(위 그림의 예 참조).이 불확실성은 측정의 불확실성보다는 원소에 [3]대한 동위원소 분포의 자연적 변동을 반영한다(품질 계측기를 사용하면 훨씬 작다).
비록 표준 원자량 수치로 지구상의 변동 범위를 다루려는 시도가 있지만, 표준 원자량 [2]범위로부터 특이치인 원자량을 가진 원소를 포함하는 광물 샘플의 경우들이 있다.
합성 원소의 경우 형성된 동위원소는 합성 방법에 따라 달라지기 때문에 자연 동위원소 풍부성의 개념은 의미가 없다.따라서 합성 원소의 경우 가장 안정적인 동위원소(즉, 반감기가 가장 긴 동위원소)의 총 핵자 수는 표준[dubious ] 원자량 대신 괄호 안에 표시된다.
화학에서 "원자량"이라는 용어가 사용될 때, 일반적으로 암시되는 것은 더 구체적인 표준 원자량이다.그것은 주기율표에 사용되는 표준 원자량이고 일반적인 지상 화학에서 많은 표준 참고 문헌이다.
리튬은 [citation needed][dubious ]하천과 같은 자연 발생원에서 얻은 샘플에서도 표준 원자량의 불확실성에 영향을 미칠 정도로 인간 동위원소 분리 활동에 의해 동위원소의 자연적 풍부성이 교란된 독특한 경우이다.
지상 정의
표준 원자량 값을 부여할 때 "기존 지상 선원"을 지정해야 하는 이유의 예는 아르곤 원소이다.태양계 내 위치들 사이에서 아르곤의 원자량은 동위원소 조성의 극단적인 차이로 인해 10%까지 변화한다.아르곤의 주요 공급원이 암석 내 K의 붕괴인 경우 Ar이 주요 동위원소이다.그러한 장소에는 수성과 화성, 그리고 달 타이탄이 포함된다.지구상에서는 3개의 동위원소 Ar: Ar: Ar의 비율이 약 5:1:1600으로 지상 아르곤의 원자량은 39.948(1)이다.
그러나 우주의 나머지 지역에서는 그렇지 않다.별의 핵합성에 의해 직접 생성된 아르곤은 알파 과정 핵종 Ar에 의해 지배된다.이에 대응하여 태양 아르곤은 (태양풍 [4]측정 결과) 84.6%의 Ar을 함유하고 있으며, 3개의 동위원소 Ar : Ar : Ar : Ar의 외행성 대기 중 비율은 8400 : 1600 [5]: 1이다.따라서 태양과 우주의 대부분에 있는 아르곤의 원자량은 약 36.[6]3에 불과할 것이다.
지구의 불확실성의 원인
유명하게도, 공개된 원자량 값은 불확실성을 수반한다.이러한 불확실성(및 관련: 정밀도)은 "지상적이고 안정적인" 선원이라는 정의에서 비롯된다.불확실성의 체계적인 원인은 다음과 같습니다.
- 측정 한계.항상 그렇듯이 물리적 측정은 결코 유한하지 않습니다.항상 더 자세한 내용을 찾아서 읽을 수 있습니다.이는 발견된 모든 순수 동위원소에 적용된다.예를 들어, 오늘날 주요 천연 불소 동위원소(불소-19)의 질량은 소수점 11자리 숫자 18.998403163(6)의 정확도로 측정할 수 있다.그러나 더 정확한 측정 시스템을 사용할 수 있게 되어 더 많은 소수를 생산할 수 있습니다.
- 동위원소의 불완전한 혼합물.채취하여 측정한 표본에서 이들 동위원소의 혼합(상대적 풍부성)은 다를 수 있다.예를 들어 구리.일반적으로 두 개의 동위원소가 발견된 구리 중 각각 69.15%와 30.85%를 차지하지만, 측정되는 자연 샘플은 불완전한 '끈끈이'를 가지고 있을 수 있기 때문에 비율이 다릅니다.물론 더 많은 시료를 측정함으로써 정밀도가 향상되지만, 불확실성의 원인이 남아 있다(예: 납 시료가 너무 많이 달라서 4개의 수치 207.2보다 더 정밀하게 나타낼 수 없다).
- 다른 역사를 가진 지구상의 원천들.원천은 '해양수' 또는 '화산암'과 같이 조사되는 더 넓은 영역이다('샘플'이 아니라 조사되는 단일 물질 더미).일부 원소는 소스별로 다른 동위원소 혼합을 가지고 있는 것으로 보입니다.예를 들어 화성암에 있는 탈륨은 더 가벼운 동위원소를 가지고 있는 반면 퇴적암에 있는 탈륨은 더 무거운 동위원소를 가지고 있다.지구 평균은 없다.다음r 요소는 간격 표기를 나타냅니다.A°)를 나타냅니다.Tl) = [132.38, 204.39]실제적인 이유로 단순화된 '재래식' 숫자도 발표된다(Tl: 204.38).
이 세 가지 불확실성은 누적됩니다.공개된 값은 이 모든 것의 결과입니다.
상대 원자질량 측정
현대의 상대 원자 질량(특정 원소 표본에 특정한 용어)은 (각 핵종에 대해) 원자 질량의 측정값과 표본의 동위원소 성분으로부터 계산된다.거의 모든 비방사성 핵종에 대해 고정밀 원자 질량을 사용할[7][8] 수 있지만, 동위원소 구성은 고정밀로 측정하기 어렵고 [9][10]표본 간의 변동도 더 쉽다.이러한 이유로, 22개의 단핵 원소의 상대적인 원자 질량은 특히 높은 정확도로 알려져 있다(이러한 원소의 단일 자연 발생 핵종에 대한 동위원소 질량과 동일).
| 동위원소 | 원자[8] 질량 | 풍성[9] | |
|---|---|---|---|
| 표준. | 범위 | ||
| 28시 | 27.976 926 532 46(194) | 92.2297(7)% | 92.21–92.25% |
| 29시 | 28.976 494 700(22) | 4.6832(5)% | 4.67–4.69% |
| 30시 | 29.973 770 171(32) | 3.0872(5)% | 3.08–3.10% |
이 계산은 상대 원자 질량이 도량형에서 특히 중요한 실리콘에 대해 예시된다.실리콘은 자연에서 세 가지 동위원소인 Si, Si, Si의 혼합물로 존재한다.이들 핵종의 원자 질량은 Si의 경우 140억분의 1의 정밀도로 알려져 있고, 다른 핵종의 경우 10억분의 1의 정밀도로 알려져 있다.그러나 동위원소에 대한 자연 풍요도 범위는 표준 풍요도가 약 ±0.001%에 불과할 정도로 한정된다(표 참조).계산은
- Ar(Si) = (27.97693 × 0.922297) + (28.97649 × 0.046832) + (29.97377 × 0.030872) = 28.0854
특히 표본 분포가 반드시 대칭인 것은 아니기 때문에 불확실성의 추정은 [11]복잡하다. IUPAC 표준 상대 원자 질량은 추정 대칭 불확실성과 [12]함께 인용되며 실리콘 값은 28.0855(3)이다.이 값의 상대 표준 불확도는 1×10–5 또는 10ppm이다.이러한 자연적 변동을 더욱 반영하기 위해 2010년 IUPAC는 10개 원소의 상대적 원자 질량을 고정수가 [13]아닌 구간으로 나열하기로 결정했다.
명명 논란
"[14]원자량"이라는 이름의 사용은 과학자들 사이에서 많은 논란을 불러 일으켰다.그 이름에 대한 거부자들은 보통 "상대적인 원자 질량"이라는 용어를 선호한다.기본적인 반대는 원자량이 무게가 아니라는 것이다. 즉, 뉴턴이나 파운드와 같은 힘의 단위로 측정되는 중력장의 물체에 가해지는 힘이다.
이에 대해, "원자량"이라는 용어의 지지자들은 (다른 [14]주장들 중에서) 다음과 같이 지적한다.
- 이름은 [15]1808년 처음 개념화된 이후 동일한 수량에 대해 지속적으로 사용되어 왔다.
- 대부분의 시간 동안 원자량은 계량(즉, 중량분석)에 의해 실제로 측정되었으며, 물리량의 이름은 단순히 결정 방법이 변경되었다고 해서 변경되어서는 안 된다.
- '원자질량'이라는 용어는 특정 핵종(또는 동위원소)의 질량을 위해 남겨야 하며, '원자질량'은 표본의 모든 원자에 걸친 원자질량의 가중평균에 사용해야 한다.
- 다음과 같은 역사적 이유로 유지되는 물리적 수량의 잘못된 이름을 갖는 것은 드문 일이 아니다.
원자량은 개별 원자의 성질에 해당되지 않기 때문에 종종 진정한 "원자"가 아니라고 덧붙일 수 있다.이런 의미에서 사용되는 "상대 원자질량"에 대해서도 같은 주장이 제기될 수 있다.
공개된 값
이 섹션은 업데이트해야 합니다.그 이유는 {{CIAW2021}} 데이터 및 값 표기법을 사용하는 것입니다.(2022년 7월) |
IUPAC는 표준 [16][17]원자량이라고 불리는 안정 요소별로 하나의 공식 값을 공개합니다.모든 업데이트는 2년에 한 번(불균일한 연도에) 발행됩니다.2015년에는 이터튬의 원자량이 [16]업데이트되었다.2017년에는 아르곤이 단일 번호에서 간격 [18][19]값으로 변경되는 등 14개의 원자 무게가 변경되었다.
공개된 값은 네온: 20.1797(6)과 같이 불확실성을 가질 수 있고 붕소: [10.806, 10.821]과 같이 간격이 될 수 있습니다.
IUPAC는 이들 84개의 값 옆에 요약된 값(1개 번호당 최대 5자리)과 12개의 인터벌 값의 경우 일반 값(단일 번호 값)도 퍼블리시합니다.
기호r A는 예를 들어 특정 샘플의 상대적인 원자 질량입니다.구체적으로 말하면, 표준 원자량은 A°(E)로r 표기할 수 있다. 여기서 (E)는 원소 기호이다.
요약 원자량
또한 CIAAW에 의해 발표된 요약 원자량은 5자리 숫자로 감소된 표준 원자량에서 도출되었다(유효한 숫자 5개).이름에는 '둥근'이 없습니다.
간격 테두리는 첫 번째(최저) 테두리에 대해서는 아래쪽으로 반올림되고 위쪽(최고) 테두리에 대해서는 위쪽으로 반올림됩니다.이렇게 하면 더 정확한 원래 간격이 완전히 [20]커버됩니다.
예:
- 칼슘:Ar°(Ca) = 40.078(4) → Ar, abridged°(Ca) = 40.078
- 헬륨: Ar°(He) = 4.002602 (2) → Ar, abridged°(그) = 4.0026
- 수소: Ar°(H) = [1.00784, 1.00811] → Ar, abridged°(H) = [1.0078, 1.0082]
표준 원자량
수소, 리튬, 붕소, 탄소, 질소, 산소, 마그네슘, 실리콘, 황, 염소, 아르곤, 브롬, 탈륨, 납 등 14가지 화학 원소는 단일 수치가 아닌 간격으로 정의되는 표준 원자량을 가지고 있습니다.예를 들어, 수소는 Ar°(H) = [1.00 784, 1.00811]이 표기법은 지구의 다양한 원천들이 실질적으로 다른 동위원소 구성을 가지고 있으며, 두 숫자에 불확실성이 포함되어 있음을 나타낸다.이러한 원소의 경우, '지구 평균' 구성은 존재하지 않으며, '오른쪽' 값은 중간값이 아니다(수소의 경우 1.007975이며, (±0.000135)의 불확실성으로 구간만 커버한다).단, 보다 정밀도가 낮은 값이 허용 가능한 상황의 경우, CIAAW는 예를 들어 무역에 사용할 수 있는 단일 번호의 재래식 원자량을 발표했다.수소의 경우r, conventional A°(H) = 1.008이다.[21]
형식적으로 짧은 원자량
요약값과 13 간격값의 종래값을 이용하여 모든 안정요소에 대해 짧은 IUPAC 정의값(5자리+불확도)을 얻을 수 있다.많은 상황에서 그리고 주기율표에서 이것은 충분히 [22]상세하게 설명될 수 있습니다.
| 요소(E) | Ar°(E) | 값 유형 | Ar°(E), 요약 또는 재래식 | 질량수 [가장 안정적인 동위원소] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수소 | 1H | [1.00784, 1.00811] | 간격 | 1.0080±0.0002 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 질소 | 7N | [14.00643, 14.00728] | 간격 | 14.007±0.001 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 불소 | 9에프 | 18.998403162±0.0000005 | 값 ± 불확실성 | 18.998±0.001 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 칼슘 | 20Ca | 40.078±0.004 | 값 ± 불확실성 | 40.078±0.004 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 테크네튬 | 43Tc | (없음) | 최안정 동위원소 | [97] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
원자량 목록
| Z | 기호. | 이름. | Ar, 표준 | 요약된 | 해가 바뀌었다 | ||
|---|---|---|---|---|---|---|---|
| 1 | H | 수소 | [1.00784, 1.00811] | 1.0080±0.0002 | 2009 | ||
| 2 | 그 | 헬륨 | 4.002602±0.000002 | 4.0026±0.0001 | 1983 | ||
| 3 | 리 | 리튬 | [6.938, 6.997] | 6.94±0.06 | 2009 | ||
| 4 | 있다 | 베릴륨 | 9.0121831±0.0000005 | 9.0122±0.0001 | 2013 | ||
| 5 | B | 붕소 | [10.806, 10.821] | 10.81±0.02 | 2009 | ||
| 6 | C | 카본 | [12.0096, 12.0116] | 12.011±0.002 | 2009 | ||
| 7 | N | 질소 | [14.00643, 14.00728] | 14.007±0.001 | 2009 | ||
| 8 | O | 산소 | [15.99903, 15.99977] | 15.999±0.001 | 2009 | ||
| 9 | F | 불소 | 18.998403162±0.0000005 | 18.998±0.001 | 2021 | ||
| 10 | 네 | 네온 | 20.1797±0.0006 | 20.180±0.001 | 1985 | ||
| 11 | 나 | 나트륨 | 22.9876928±0.00000002 | 22.990±0.001 | 2005 | ||
| 12 | Mg | 마그네슘 | [24.304, 24.307] | 24.305±0.002 | 2011 | ||
| 13 | 알 | 알루미늄 | 26.9815384±0.0000003 | 26.982±0.001 | 2017 | ||
| 14 | 시 | 실리콘 | [28.084, 28.086] | 28.085±0.001 | 2009 | ||
| 15 | P | 인 | 30.973761998±0.0000005 | 30.974±0.001 | 2013 | ||
| 16 | S | 유황 | [32.059, 32.076] | 32.06±0.02 | 2009 | ||
| 17 | 클론 | 염소 | [35.446, 35.457] | 35.45±0.01 | 2009 | ||
| 18 | 아르 | 아르곤 | [39.792, 39.963] | 39.95±0.16 | 2017 | ||
| 19 | K | 칼륨 | 39.0983±0.0001 | 39.098±0.001 | 1979 | ||
| 20 | Ca | 칼슘 | 40.078±0.004 | 40.078±0.004 | 1983 | ||
| 21 | 스케이 | 스칸듐 | 44.955907±0.000004 | 44.956±0.001 | 2021 | ||
| 22 | 티 | 티타늄 | 47.867±0.001 | 47.867±0.001 | 1993 | ||
| 23 | V | 바나듐 | 50.9415±0.0001 | 50.942±0.001 | 1977 | ||
| 24 | Cr | 크롬 | 51.9961±0.0006 | 51.996±0.001 | 1983 | ||
| 25 | Mn | 망간 | 54.938043±0.000002 | 54.938±0.001 | 2017 | ||
| 26 | Fe | 철 | 55.845±0.002 | 55.845±0.002 | 1993 | ||
| 27 | 회사 | 코발트 | 58.933194±0.000003 | 58.933±0.001 | 2017 | ||
| 28 | 니 | 니켈 | 58.6934±0.0004 | 58.693±0.001 | 2007 | ||
| 29 | CU | 구리 | 63.546±0.003 | 63.546±0.003 | 1969 | ||
| 30 | Zn | 아연 | 65.38±0.02 | 65.38±0.02 | 2007 | ||
| 31 | 가 | 갈륨 | 69.723±0.001 | 69.723±0.001 | 1987 | ||
| 32 | ge | 게르마늄 | 72.630±0.008 | 72.630±0.008 | 2009 | ||
| 33 | ~하듯이 | 비소 | 74.921595±0.000006 | 74.922±0.001 | 2013 | ||
| 34 | 세 | 셀렌 | 78.971±0.008 | 78.971±0.008 | 2013 | ||
| 35 | 브르 | 브롬화 | [79.901, 79.907] | 79.904±0.003 | 2011 | ||
| 36 | Kr | 크립톤 | 83.798±0.002 | 83.798±0.002 | 2001 | ||
| 37 | Rb | 루비듐 | 85.4678±0.0003 | 85.468±0.001 | 1969 | ||
| 38 | 시르 | 스트론튬 | 87.62±0.01 | 87.62±0.01 | 1969 | ||
| 39 | Y | 이트륨 | 88.905838±0.000002 | 88.906±0.001 | 2021 | ||
| 40 | Zr | 지르코늄 | 91.224±0.002 | 91.224±0.002 | 1983 | ||
| 41 | Nb | 니오브 | 92.90637±0.00001 | 92.906±0.001 | 2017 | ||
| 42 | 모 | 몰리브덴 | 95.95±0.01 | 95.95±0.01 | 2013 | ||
| 43 | Tc | 테크네튬 | - | ||||
| 44 | 루 | 루테늄 | 101.07±0.02 | 101.07±0.02 | 1983 | ||
| 45 | Rh | 로듐 | 102.90549±0.00002 | 102.91±0.01 | 2017 | ||
| 46 | PD | 팔라듐 | 106.42±0.01 | 106.42±0.01 | 1979 | ||
| 47 | 아그 | 실버 | 107.8682±0.0002 | 107.87±0.01 | 1985 | ||
| 48 | CD | 카드뮴 | 112.414±0.004 | 112.41±0.01 | 2013 | ||
| 49 | 인 | 인듐 | 114.818±0.001 | 114.82±0.01 | 2011 | ||
| 50 | 스니 | 주석 | 118.710±0.007 | 118.71±0.01 | 1983 | ||
| 51 | Sb | 안티몬 | 121.760±0.001 | 121.76±0.01 | 1993 | ||
| 52 | 테 | 텔루루 | 127.60±0.03 | 127.60±0.03 | 1969 | ||
| 53 | I | 요오드 | 126.90447±0.00003 | 126.90±0.01 | 1985 | ||
| 54 | Xe | 크세논 | 131.293±0.006 | 131.29±0.01 | 1999 | ||
| 55 | Cs | 세슘 | 132.90545196±0.00000006 | 132.91±0.01 | 2013 | ||
| 56 | 바 | 바륨 | 137.327±0.007 | 137.33±0.01 | 1985 | ||
| 57 | 라 | 랜턴 | 138.90547±0.00007 | 138.91±0.01 | 2005 | ||
| 58 | Ce | 세륨 | 140.140±0.001 | 140.12±0.01 | 1995 | ||
| 59 | PR | 플라시오뮴 | 140.90766±0.00001 | 140.91±0.01 | 2017 | ||
| 60 | Nd | 네오디뮴 | 144.242±0.003 | 144.24±0.01 | 2005 | ||
| 61 | Pm | 프로메튬 | |||||
| 62 | SM | 사마리움 | 150.36±0.02 | 150.36±0.02 | 2005 | ||
| 63 | 에우 | 유로피움 | 151.964±0.001 | 151.96±0.01 | 1995 | ||
| 64 | Gd | 가돌리늄 | 157.25±0.03 | 157.25±0.03 | 1969 | ||
| 65 | Tb | 터비움 | 158.925354±0.000007 | 158.93±0.01 | 2021 | ||
| 66 | Dy | 디스프로슘 | 162.500±0.001 | 162.50±0.01 | 2001 | ||
| 67 | 호 | 홀뮴 | 164.930329±0.000005 | 164.93±0.01 | 2021 | ||
| 68 | 음.정말 | 엘비움 | 167.259±0.003 | 167.26±0.01 | 1999 | ||
| 69 | Tm | 탈륨 | 168.934219±0.000005 | 168.93±0.01 | 2021 | ||
| 70 | YB | 이터비움 | 173.045±0.010 | 173.05±0.02 | 2015 | ||
| 71 | 루 | 루테튬 | 174.9668±0.0001 | 174.97±0.01 | 2007 | ||
| 72 | HF | 하프늄 | 178.486±0.006 | 178.49±0.01 | 2019 | ||
| 73 | 타 | 탄탈 | 180.94788±0.00002 | 180.95±0.01 | 2005 | ||
| 74 | W | 텅스텐 | 183.84±0.01 | 183.84±0.01 | 1991 | ||
| 75 | 레 | 레늄 | 186.207±0.001 | 186.21±0.01 | 1973 | ||
| 76 | OS | 오스뮴 | 190.23±0.03 | 190.23±0.03 | 1991 | ||
| 77 | Ir | 이리듐 | 192.217±0.002 | 192.22±0.01 | 2017 | ||
| 78 | Pt | 백금 | 195.084±0.009 | 195.08±0.02 | 2005 | ||
| 79 | 오 | 골드 | 196.966570±0.000004 | 196.97±0.01 | 2017 | ||
| 80 | Hg | 수성. | 200.592±0.003 | 200.59±0.01 | 2011 | ||
| 81 | Tl | 탈륨 | [132.382, 204.385] | 204.38±0.01 | 2009 | ||
| 82 | PB | 이끌다 | [132.14, 207.94] | 207.2±1.1 | 2020 | ||
| 83 | 비 | 비스무트 | 208.98040±0.00001 | 208.98±0.01 | 2005 | ||
| 84 | 포 | 폴로늄 | - | ||||
| 85 | 앳 | 아스타틴 | - | ||||
| 86 | Rn | 라돈 | - | ||||
| 87 | 프루 | 프랑슘 | - | ||||
| 88 | 라 | 라듐 | - | ||||
| 89 | AC | 악티늄 | - | ||||
| 90 | Th(Th) | 토륨 | 232.0377±0.0004 | 232.04±0.01 | 2013 | ||
| 91 | 빠 | 프로탁티늄 | 231.03588±0.00001 | 231.04±0.01 | 2017 | ||
| 92 | U | 우라늄 | 238.02891±0.00003 | 238.03±0.01 | 1999 | ||
| 93 | Np | 넵투늄 | - | ||||
| 94 | 푸 | 플루토늄 | - | ||||
| 95 | 암 | 아메리슘 | - | ||||
| 96 | Cm | 퀴륨 | - | ||||
| 97 | Bk | 버켈륨 | - | ||||
| 98 | Cf | 칼리포늄 | - | ||||
| 99 | Es | 아인스타이늄 | - | ||||
| 100 | Fm | 페르미움 | - | ||||
| 101 | Md | 멘델레비움 | - | ||||
| 102 | 아니요. | 노벨륨 | - | ||||
| 103 | Lr | 로렌슘 | - | ||||
| 104 | Rf | 러더포디움 | - | ||||
| 105 | 데이터베이스 | 더브늄 | - | ||||
| 106 | Sg | 시보르기움 | - | ||||
| 107 | Bh | 보륨 | - | ||||
| 108 | Hs | 핫시움 | - | ||||
| 109 | 산 | 마이트네륨 | - | ||||
| 110 | Ds | 단스타튬 | - | ||||
| 111 | Rg | 엑스레이 | - | ||||
| 112 | Cn | 코페르니슘 | - | ||||
| 113 | Nh | 니혼륨 | - | ||||
| 114 | 플 | 플레로비움 | - | ||||
| 115 | 맥 | 모스코비움 | - | ||||
| 116 | Lv | 간모륨 | - | ||||
| 117 | Ts | 테네신 | - | ||||
| 118 | 오그 | 오가네손 | - | ||||
- ^ (이 목록: 됨)CIAAW는 원자량(정밀도와 파생값 포함)의 변경을 공표할 수 있다.1947년 이후, 이 업데이트는 명목상 홀수 년도에 이루어지며, 실제 발행일은 다소 늦어질 수 있습니다.
- 2009년 (간격 표기법 도입; Ge):
- "Atomic weights of the elements 2009 (IUPAC Technical Report)". Pure Appl. Chem. 83 (2): 359–396. 12 December 2010. doi:10.1351/PAC-REP-10-09-14.
- 2011년(Br, Mg 간격):
- "Atomic weights of the elements 2011 (IUPAC Technical Report)". Pure Appl. Chem. 85 (5): 1047–1078. 29 April 2013. doi:10.1351/PAC-REP-13-03-02.
- 2013년(목록에 있는 모든 요소):
- Meija, Juris; et al. (2016). "Atomic weights of the elements 2013 (IUPAC Technical Report)". Pure and Applied Chemistry. 88 (3): 265–91. doi:10.1515/pac-2015-0305.
- 2015년(나트륨 변경):
- "Standard Atomic Weight of Ytterbium Revised". Chemistry International. 37 (5–6): 26. October 2015. doi:10.1515/ci-2015-0512. eISSN 0193-6484. ISSN 0193-6484.
- 2017년(14개 값 변경):
- "Standard atomic weights of 14 chemical elements revised". CIAAW. 2018-06-05.
- 2019년(하프늄 값 변경):Meija, Juris; et al. (2019-12-09). "Standard atomic weight of hafnium revised". CIAAW. Retrieved 2020-02-25.
- 2020*(납값 변경):Zhu, Xiang-Kun; Benefield, Jacqueline; Coplen, Tyler B.; Gao, Zhaofu; Holden, Norman E. (1 October 2020). "Variation of lead isotopic composition and atomic weight in terrestrial materials (IUPAC Technical Report)". doi:10.1515/pac-2018-0916.
- * "2020년"은 변화 발표에 일관성이 없는 해이다: CIAAW는 홀수 연도만 공개한다고 주장한다.
- 2021년(목록된 모든 요소); (4개의 값이 변경됨; 새로운 기호 도입; "기존"을 "요약" 열에 병합; 불확실성 표기법 변경("±" 사용))
- Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. (2022-05-04). "Standard atomic weights of the elements 2021 (IUPAC Technical Report)". Pure and Applied Chemistry. doi:10.1515/pac-2019-0603. ISSN 1365-3075.
- 불확실성 처리
[ ] 범위의 값을 포함하여 값의 불확실성 표기 및 처리에 대해:
- Possolo, Antonio; van der Veen, Adriaan M.H.; Meija, Juris; et al. (4 Jan 2018). "Interpreting and propagating the uncertainty of the standard atomic weights (IUPAC Technical Report)". doi:10.1515/pac-2016-0402. Retrieved 20 Oct 2020.
- {{CIAW2021}: 표기법(값이 아닌 해석)을 123.45(2)에서123.45±0.02로 변경
오래된 참조- {{NUBASE 1997}}: Audi
- {{NUBASE 2003}}: Audi (2008년 enwiki "Isotopes of <Element>" 빅테이블에 사용)
- {{NUBASE 2012}}
- {{CIAW2003}}: De Laeter
- {{CIAW 2005}} : Wieser
- {{CRC85}}({CRC85장=11}) &mdsh; 홀든
- "Universal Nuclide Chart". nucleonica. -- 접속이 끊기거나 잘못됨
주기율표에서
「 」를 참조해 주세요.
- 국제순수응용화학연합(IUPAC)
- 동위원소 함유량 및 원자량 위원회(CIAW)
레퍼런스
- ^ a b c Meija, Juris; et al. (2016). "Atomic weights of the elements 2013 (IUPAC Technical Report)". Pure and Applied Chemistry. 88 (3): 265–91. doi:10.1515/pac-2015-0305.
- ^ a b "IUPAC Goldbook". Compendium of Chemical Terminology. doi:10.1351/goldbook.S05907. Retrieved 12 July 2019.
standard atomic weights: Recommended values of relative atomic masses of the elements revised biennially by the IUPAC Commission on Atomic Weights and Isotopic Abundances and applicable to elements in any normal sample with a high level of confidence. A normal sample is any reasonably possible source of the element or its compounds in commerce for industry and science and has not been subject to significant modification of isotopic composition within a geologically brief period.
- ^ Wieser, M. E (2006). "Atomic weights of the elements 2005 (IUPAC Technical Report)" (PDF). Pure and Applied Chemistry. 78 (11): 2051–2066. doi:10.1351/pac200678112051. S2CID 94552853.
- ^ Lodders, K. (2008). "The solar argon abundance". Astrophysical Journal. 674 (1): 607–611. arXiv:0710.4523. Bibcode:2008ApJ...674..607L. doi:10.1086/524725. S2CID 59150678.
- ^ Cameron, A. G. W. (1973). "Elemental and isotopic abundances of the volatile elements in the outer planets". Space Science Reviews. 14 (3–4): 392–400. Bibcode:1973SSRv...14..392C. doi:10.1007/BF00214750. S2CID 119861943.
- ^ 이는 원자량과 WP의 정의에 따라 위의 그림에서 확인할 수 있다.계산
- ^ "Atomic Weights and Isotopic Compositions for All Elements". National Institute of Standards and Technology.
- ^ a b Wapstra, A.H.; Audi, G.; Thibault, C. (2003), The AME2003 Atomic Mass Evaluation (Online ed.), National Nuclear Data Center. 기준:
- Wapstra, A.H.; Audi, G.; Thibault, C. (2003), "The AME2003 atomic mass evaluation (I)", Nuclear Physics A, 729: 129–336, Bibcode:2003NuPhA.729..129W, doi:10.1016/j.nuclphysa.2003.11.002
- Audi, G.; Wapstra, A.H.; Thibault, C. (2003), "The AME2003 atomic mass evaluation (II)", Nuclear Physics A, 729: 337–676, Bibcode:2003NuPhA.729..337A, doi:10.1016/j.nuclphysa.2003.11.003
- ^ a b Rosman, K. J. R.; Taylor, P. D. P. (1998), "Isotopic Compositions of the Elements 1997" (PDF), Pure and Applied Chemistry, 70 (1): 217–35, doi:10.1351/pac199870010217
- ^ Coplen, T. B.; et al. (2002), "Isotopic Abundance Variations of Selected Elements" (PDF), Pure and Applied Chemistry, 74 (10): 1987–2017, doi:10.1351/pac200274101987
- ^ Meija, Juris; Mester, Zoltán (2008). "Uncertainty propagation of atomic weight measurement results". Metrologia. 45 (1): 53–62. Bibcode:2008Metro..45...53M. doi:10.1088/0026-1394/45/1/008.
- ^ Holden, Norman E. (2004). "Atomic Weights and the International Committee—A Historical Review". Chemistry International. 26 (1): 4–7.
- ^ "IUPAC – International Union of Pure and Applied Chemistry: Atomic Weights of Ten Chemical Elements About to Change". Archived from the original on 2020-07-28. Retrieved 2019-07-12.
- ^ a b de Bièvre, Paul; Peiser, H. Steffen (1992). "'Atomic Weight' — The Name, Its History, Definition, and Units" (PDF). Pure and Applied Chemistry. 64 (10): 1535–43. doi:10.1351/pac199264101535.
- ^ Dalton, John (1808). A New System of Chemical Philosophy. Manchester.
- ^ a b "Standard Atomic Weights 2015". Commission on Isotopic Abundances and Atomic Weights. 12 October 2015. Retrieved 18 February 2017.
- ^ Meija 2016, 표 1. 오류:: 2016
- ^ "Standard atomic weights of 14 chemical elements revised". CIAAW. 2018-06-05. Retrieved 2019-02-02.
- ^ "Standard Atomic Weights of 14 Chemical Elements Revised". Chemistry International. 40 (4): 23–24. 2018. doi:10.1515/ci-2018-0409. ISSN 0193-6484.
- ^ Meija 2016, 표 2. 오류:: 2016
- ^ Meija 2016, 표 3. 오류:: 2016
- ^ Meija 2016, 표 2 및 3. 없음: 도움말
- ^ a b Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. (2022-05-04). "Standard atomic weights of the elements 2021 (IUPAC Technical Report)". Pure and Applied Chemistry. doi:10.1515/pac-2019-0603. ISSN 1365-3075.