인간 베타헤르페스바이러스 5
Human betaherpesvirus 5| 인간사이토메갈로바이러스 | |
|---|---|
| 전문 | 전염병 |
| 원인들 | 인간 베타헤르페스바이러스 5 |
| 인간 베타헤르페스바이러스 5 | |
|---|---|
 | |
| 폐폐렴구균의 CMV 감염 | |
| 바이러스 분류 | |
| (랭킹되지 않음): | 바이러스 |
| 영역: | 두피오드나비리아속 |
| 킹덤: | 흥공비래 |
| 망울: | 페플로비리코타 |
| 클래스: | 에르비비리케테스속 |
| 순서: | 헤르페스비르목 |
| 패밀리: | 헤르페스비루스과 |
| 속: | 키토메갈로바이러스 |
| 종: | 인간 베타헤르페스바이러스 5 |
| 동의어[1] | |
| |
인간 베타헤르페스바이러스 5는 인간사이토메갈로바이러스(HCMV)라고도 불리는데,[2] 사이토메갈로바이러스 속에서는 헤르페스비루스(Herpesvirus) 또는 헤르페스비루스(Herpesvirus)로 알려진 바이러스 계열의 일종이다.흔히 CMV라고도 한다.[3] Herpesvirae 내에서는 HCMV가 베타헤르페스비리네 아과에 속하는데, 다른 포유류로부터 온 세포질갈로비루스를 포함하기도 한다.[4]CMV는 이중 가닥의 DNA 바이러스다.[5]
비록 그것들은 몸 전체에서 발견될 수 있지만, HCMV 감염은 침샘과 자주 관련된다.[4]HCMV 감염은 일반적으로 건강한 사람들에게서 눈에 띄지 않지만, HIV 감염자, 장기 이식 수혜자 또는 신생아와 같은 면역억제자들에게는 생명을 위협할 수 있다.[3]선천적 세포질갈로바이러스 감염은 중대한 질병과 심지어 죽음으로 이어질 수 있다.감염 후 HCMV는 평생 동안 몸 안에 잠재되어 있으며 언제든지 다시 활성화될 수 있다.결국, 그것은 점막암과 전립선암과[7] 유방암과 같은 다른 악성[6] 종양을 일으킬 수 있다.[8]
HCMV는 모든 지리적 위치와 모든 사회경제적 그룹에서 발견되며 선진국의 성인의 60~70%, 개발도상국의 성인의 거의 100%에 감염된다.[9]HCMV는 모든 대상 바이러스 중에서 선천적, 적응적 숙주 면역의 변화(탈진)에 가장 헌신적인 유전자를 갖고 있으며 항원적 T세포 감시와 면역 기능장애의 평생적 부담을 나타낸다.[10]일반적으로 그것은 일반 인구의 항체 존재에 의해 표시된다.[3]세로프레발란스는 연령에 따라 달라진다. 6세 이상 인구의 58.9%가 CMV에 감염되어 있는 반면, 80세 이상 인구의 90.8%가 HCMV에 양성 반응을 보인다. HCMV는 또한 성장 중인 태아에게 가장 자주 전염되는 바이러스다.[11][12]HCMV 감염은 개발도상국과 사회경제적 지위가 낮은 지역사회에서 더욱 광범위하게 발생하며, 산업화된 국가에서 선천성 결함의 가장 중요한 바이러스적 원인을 나타낸다.선천성 HCMV는 소아 청각장애, 학습장애, 지적장애의 대표적인 감염원인이다.[13]CMV는 또한 "나중에 면역 파라미터에 큰 영향을 미치고 질병률 증가와 궁극적인 사망률에 기여할 수 있을 것"[14]이라고 말했다.
징후 및 증상
인간 베타페스바이러스 5 감염은 전형적인 삼중의 증상인 발열, 늦은 오후나 이른 저녁에 정점을 찍는 것, 대개 발출성 인두염, 대칭성 아데모병증을 가지고 있다.[citation needed]
바이러스학
전송
사람에서 사람으로 HCMV가 전달되는 방식은 알 수 없지만 침, 소변, 혈액, 눈물 등 체액을 통해 발생하는 것으로 추정된다.[15]사이토메갈로바이러스는 키스나 성교를 통해 가장 흔하게 전염된다.감염된 어머니에서 태어나지 않은 아이로 옮겨질 수도 있다.[4]감염은 타액, 소변 또는 다른 체액에 있는 바이러스를 분비하는 사람과 밀접하고 친밀한 접촉을 필요로 한다.CMV는 성적으로나 모유를 통해 전염될 수 있으며 이식된 장기나 수혈을 통해서도 발생한다.[16]HCMV는 전염성이 높지 않지만 가정 내, 어린이집 유아 사이에 확산되는 것으로 나타났다.[3]
복제
HCMV는 감염된 내피 세포[17] 내에서 느린 속도로 복제하여 세포 배양에 약 5일이 걸린다.[18]다른 헤르페스바이러스와 마찬가지로 HCMV는 일시적으로 조절되는 방식으로 유전자를 표현한다.[19][20]즉시 초기 유전자(감염 후 0~4시간)가 전사 규제에 관여하고, 바이러스성 DNA 복제와 추가 전사 규제에 관여하는 초기 유전자(감염 후 4~48시간)가 그 뒤를 잇는다.[19]후기 유전자는 바이러스 퇴출까지의 감염의 나머지 기간 동안 발현되며 전형적으로 구조 단백질에 대해 코딩한다.HCMV가 자체 기능 DNA 중합효소를 위해 암호화하는 동안, 바이러스는 숙주 RNA 중합효소를 모든 유전자의 전사에 사용한다.[21]
바이러스 이중 가닥 DNA 게놈의 합성은 전문 바이러스 복제 구획 내의 숙주 세포핵에서 발생한다.[22]
HCMV 변종 AD169에 의해 인코딩된 유전자의 거의 75%는 삭제될 수 있고 여전히 전염성 바이러스의 생산을 초래한다.[23]이는 이 바이러스가 숙주 면역체계를 피하는 데 초점을 맞추고 있다는 것을 시사한다.[citation needed]
위험에 처한 인구
CMV 감염은 생리 기간과 면역 확약된 사람들에게 가장 중요하다.
임신 및 선천성 감염
HCMV는 선천성 이상을 일으키는 수직으로 전염되는 감염의 하나이다. (기타로는 독소포체증, 풍진, 헤르페스 심플렉스 등이 있다.)선천성 HCMV 감염은 산모가 임신 중 1차 감염을 겪을 때 발생한다.[citation needed]
1,000명당 살아있는 출생아 중 최대 5명이 감염된다.5%는 여러 가지 핸디캡이 발생하며 풍진과 비슷한 비특이성 징후를 가진 세포질포착성 질환이 발생한다.또 다른 5%는 나중에 뇌 석회화를 일으킨다. (IQ 수치가 급격히 떨어지고 감각 청각장애와 정신지체장애를 유발한다.)[citation needed]
그러나, 임신 전으로 태어나 출생 후 HCMV에 감염된 유아는 만년에 인지장애와 운동장애를 경험할 수 있다.[24]
면역촉진 성인
면역체계가 손상된 사람들(예: 이식을 받았거나 크게 화상을 입은 사람들)의 CMV 감염 또는 재활성화는 질병을 유발하고 사망 위험을 증가시킨다.[25][26]
CMV 재활성화는 심각한 대장염을 가진 사람들에게서 흔히 볼 수 있다.[27]
그 사람들에게 인식된 특정 질병의 실체는
- CMV 간염으로 간 기능저하를 유발할 수 있음
- 시토메갈로바이러스 망막염(망막의 부위는 안과 내시경에서 "파이의 외관"으로 특징지어짐)
- 시토메갈로바이러스성대장염(대장의 소견)
- CMV 폐염
- CMV 식도염[28]
- 다면증, 횡격근염, 아급성 뇌염
CMV에 감염된 기증자로부터 장기이식을 받은 CMV 감염자가 있는 사람은 발간시클로비르(이상적으로) 또는 간시클로비르로 예방적 치료를 받아야 하며, 상승하는 CMV 티트르를 감지하기 위한 정기적인 세리학적 모니터링이 필요하다. 만약 생명을 위협하는 감염의 조기 확립을 예방할 수 있다.[citation needed]
면역항암성인
CMV 감염은 성인 면역항암군에서 여전히 임상적으로 중요할 수 있다.[29]
- CMV 단핵증(일부 소스는 엡스타인-바르 바이러스에 한해 "단핵증"을 보존한다).그러나 CMV와 관련된 단핵증후군은 일반적으로 자궁 림프절 확대와 비장염의 징후가 부족하다.[30][15]
- CMV는 기예인-바레 증후군,[31] 제1형 당뇨병, [32]제2형 당뇨병과도 관련이 있다.[33]
잠복성 CMV 감염이 건강한 사람들에게 부정적인 영향을 미치는가에 대한 문제는 논의되어 왔다; 2016년 현재 대답은 명확하지 않았지만, 잠복성 CMV가 일부 심혈관 질환과 암의 위험을 증가시킬 수 있는지에 대한 논의에 초점이 맞춰져 있었다.[25]
병생성
출생 후 HCMV에 감염된 대부분의 건강한 사람은 증상이 없다.[3]감염성 단핵증이나 선열과 유사한 증후군이 발병하고,[34] 열이 오래 지속되며, 가벼운 간염도 발병한다.목이 아픈 것은 흔히 있는 일이다.감염 후, 바이러스는 그 사람의 남은 일생 동안 몸 안의 림프구에 잠복해 있다.공공연한 질병은 약물, 감염, 노후에 의해 면역력이 억제되지 않는 한 거의 발생하지 않는다.초기 HCMV 감염은 종종 무증상으로 나타나며, 바이러스가 검출 가능한 손상이나 임상 질환을[citation needed] 일으키지 않고 단핵 세포에 상주하는 장기간의 불순물 감염이 뒤따른다.
감염성 CMV는 감염된 사람의 체액에서 배출될 수 있으며, 소변, 침, 혈액, 눈물, 정액, 모유에서 발견될 수 있다.바이러스의 유출은 감지할 수 있는 징후나 증상 없이 간헐적으로 발생할 수 있다.
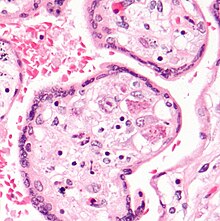
CMV 감염은 비핵산 포함 기관의 검출에 의해 현미경으로 증명될 수 있다.H&E 얼룩에서는, 포착체가 진한 분홍색을 얼룩지게 하고, "부엉이의 눈" 포착체라고 불린다.[35]
HCMV 감염은 특정 고위험군에 중요하다.[36]주요 감염 위험 영역에는 산전 또는 산후 유아와 장기이식수여자, 백혈병 환자, 인체면역결핍바이러스(HIV) 감염자 등 면역촉진 개인이 포함된다.HIV 감염자의 경우 HCMV는 에이즈 정의 감염자로 간주돼 T세포 수치가 낮은 수준으로 떨어졌음을 보여준다.
라이언리 복제 바이러스는 사이토스켈레톤을 교란시켜, 바이러스 이름의 근원인 대규모 세포 확대를 일으킨다.
2009년에 발표된 한 연구는 CMV에 의한 감염을 생쥐의 고혈압과 연관시키고 있으며, 인간 내 혈관 내피에 대한 CMV 감염의 결과가 아테롬성 동맥경화의 주요 원인이라고 제시하고 있다.[37]연구원들은 또한 이 세포들이 CMV에 감염되었을 때 고혈압에 기여하는 것으로 알려진 단백질인 레닌을 만들어냈다는 것을 발견했다.
인간 CMV는 세포 노화를 유발하여 만성 염증을 유발할 수 있다.[38]인간 CMV는 또한 나이와 관련된 T세포 기능장애와 연결되어 면역억제에 기여한다.[38]COVID-19 증상 심각도는 정확한 메커니즘이 설명되지는 않았지만 CMV와 연관되어 있다.[39]
CMV는 NK 세포 반응의 면역 회피에 관여하는 단백질 UL16을 암호화한다.NK세포 활성수용체 NKG2D의 리간드 ULBP1, ULBP2, MICB에 결합해 표면표현을 방지한다.이 리간드는 바이러스 감염과 같은 세포 스트레스 때 일반적으로 상향 조절되며, 상향 조절을 방지함으로써 CMV는 NK 세포로[40] 인해 숙주 세포가 죽는 것을 막을 수 있다.
면역 체계의 상당 부분은 면역 체계의 자원을 고갈시키는 CMV를 지속적으로 제어하는 데 관여한다.[41][42]감염병으로 인한 사망률은 나이가 들수록 빨라지고,[43] CMV 감염은 백신 접종 효과 감소와 관련이 있다.[44]CMV 항체 수치가 가장 높은 사람은 항체가 거의 없거나 없는 사람에 비해 모든 원인에 의한 사망 위험이 훨씬 높다.[45][46]
진단
대부분의 CMV 감염은 진단되지 않은 상태로 진행되는데, 바이러스는 대개 증상이 거의 없고 증상 없이 간헐적으로 재활성화하는 경향이 있기 때문이다.CMV에 감염된 사람들은 바이러스에 대한 항체를 개발하는데, 바이러스는 그 개인의 평생 동안 몸에 지속된다.CMV에 대한 이러한 항체를 검출하는 여러 실험실 테스트는 감염이 발생했는지 여부를 판단하기 위해 개발되었으며 상업용 실험실에서 광범위하게 이용할 수 있다.또 소변, 목 면봉, 기관지 변기, 조직 샘플 등에서 얻은 시료를 통해 바이러스를 배양해 활성 감염을 검출할 수 있다.CMV에 대한 질적 및 정량적 중합효소 연쇄반응(PCR) 테스트도 이용할 수 있어, 의사는 CMV에 감염된 사람의 바이러스 부하를 감시할 수 있다.
CMV pp65 항원혈증 검사는 말초혈액 백혈구 내 세포질갈로바이러스의 pp65 단백질을 식별하기 위해 간접 면역울루오렌스 기법을 활용하는 면역울루오렌스 기반 검사다.[47]CMV pp65 검사는 증상 CMV 질환이 발생하기 약 5일 전에 항원혈증 결과를 얻기 때문에 면역억제요법을 받고 신장이식수술을 받은 사람들의 CMV 감염과 항바이러스 치료에 대한 반응 감시에 널리 사용된다.이 검사의 장점은 몇 시간 안에 결과를 신속하게 제공할 수 있다는 것과 pp65 항원 결정이 의사가 항바이러스 치료를 시작하기 위한 유용한 기준을 나타낸다는 것이다.pp65 검사의 주요 단점은 시험 배치당 제한된 수의 검체만 처리할 수 있다는 것이다.
CMV는 감염성 단핵증 증세가 있으나 단핵증, 엡스타인-바르 바이러스에 대한 음성 검사 결과가 있거나 간염의 징후가 있으나 A, B, C형 간염에 대한 음성 검사 결과가 있는 경우 의심해야 한다.
최상의 진단 결과를 위해 CMV 항체에 대한 실험실 검사는 쌍체 혈청 샘플을 사용하여 수행해야 한다.CMV 의심 시 혈액 샘플 1개를 채취하고 2주 이내에 다른 1개를 채취해야 한다.바이러스 배양균은 그 사람이 증상이 있을 때 언제든지 행해질 수 있다.CMV에 대한 항체에 대한 실험실 테스트를 수행하여 여성이 CMV에 이미 감염되었는지 여부를 판단할 수 있다.그러나 모든 임산부의 일상적인 테스트는 비용이 많이 들고 따라서 테스트의 필요성을 사례별로 평가해야 한다.
세롤로그 검사
효소연계 면역항체검사(또는 ELISA)는 CMV에 대한 항체 측정에 가장 흔히 이용 가능한 세롤로그 검사다.이 결과는 유아에게 급성 감염, 사전 감염 또는 수동적으로 획득한 모성 항체가 있는지 여부를 판단하는 데 사용될 수 있다.다른 시험에는 다양한 형광 분석, 간접 혈당응고(PCR), 라텍스 응고 등이 포함된다.[citation needed]
CMV 특이 IgM에 대한 ELISA 기법을 사용할 수 있지만 혈청 검체를 검사하기 전에 류마티스 인자 또는 IgG 항체의 대부분을 제거하는 조치를 취하지 않는 한 거짓 양성 결과를 제공할 수 있다.CMV 특이 IgM은 재활성화된 CMV 감염에서 낮은 수준으로 생성될 수 있기 때문에, CMV 특이 IgM이 항상 1차 감염을 나타내는 것은 아니다.폐와 같은 표적기관에서 회복된 바이러스만이 현재의 질병이 후천성 CMV 감염에 의해 발생한다는 명백한 증거를 제공한다.세롤로그 검사에서 IgG의 양수 또는 고수 치수를 검출하는 경우, 이 결과는 활성 CMV 감염이 있음을 의미하는 것으로 자동으로 해석되어서는 안 된다.쌍체 혈청 검체의 항체 검사에서 IgG 항체가 4배 상승하고 IgM 항체가 유의 수준(IgG 값의 최소 30%에 해당)이거나 소변이나 목구멍 검체에서 바이러스가 배양된 경우 활성 CMV 감염이 존재하는 것으로 간주된다.[citation needed]
헌혈자와의 관련성
위에서 논의된 위험은 일반적으로 낮지만, CMV 검사는 미국, 영국 및 많은 다른 국가에서 비지도출혈(특정 인원에 대해 명시되지 않은 기부금)에 대한 표준 심사의 일부분이다.그리고 나서 CMV 음성 기부는 영아나 면역 확약을 받은 사람들에게 수혈할 수 있도록 배정된다.일부 헌혈센터에서는 특별한 요구로 인해 CMV 음성인 헌혈자 명단을 유지하고 있다.[48]
골수 기증자와 관련성
동종 조혈모세포 이식 시 일반적으로 기증자와 기증자의 세로스타투스를 일치시키는 것이 좋다.만약 수혜자가 세르노네제인 경우, 세르노포시적 기증자는 노보감염의 위험을 수반한다.반대로, 세로포시적 수혜자는 세로포시적 기증자로부터 이식을 받으면 바이러스 재활성화의 위험에 처하게 되며, 그 과정에서 선천적인 방어력을 상실하게 된다.일반적으로 바이러스 재활성화가 유의미한 병증의 원인이 되는 CMV 세로포시적 수혜자의 위험성이 가장 높다.이러한 이유로, CMV 세롤로그 검사는 골수 기증자와 수혜자 모두에게 일상적이다.[49][50]
예방
예방접종
2009년에 발표된 CMV-백신을 대상으로 한 2단계 연구는 50%의 효능을 보였다. 즉, 제공된 보호는 제한적이었으며, 백신 접종에도 불구하고 다수의 환자가 CMV 감염에 걸렸다.한 사례에서 선천성 CMV도 마주쳤다.[51]
2013년 아스텔라스파마는 CMV 디옥시리보핵산 DNA 시토메갈로바이러스 백신 ASP0113으로 조혈모세포 이식을 받은 개인들을 대상으로 연구를 시작했다.[52]
2015년 아스텔라스파마는 사이토메갈로바이러스 백신 ASP0113으로 건강한 자원봉사자들을 대상으로 1단계 임상시험을 시작했다.[53]
시토메갈로바이러스 백신 후보로는 CMV-MVA 트리플렉스 백신과 CMVpp65-A*0201 펩타이드 백신 등이 있다.두 백신 후보지 모두 희망시립의료원이 후원한다.2016년 현재 개발은 임상 2상 시험 단계에 있다.[54][55]
위생
질병관리본부는 특히 기저귀를 갈은 후 손을 자주 씻을 것을 권장한다.[56][57]어린이에게 먹이를 주거나, 아이의 코나 입을 닦거나, 어린이 장난감을 취급한 후에는 손세탁도 권장된다.[58]
치료
CMV(CMV-IGIV)용으로 농축된 하이퍼임문 글로불린은 시토메갈로바이러스에 대한 표준화된 수의 항체를 포함하는 면역글로불린 G(IgG)이다.신장, 폐, 간, 췌장, 심장 이식과 관련된 시토메갈로바이러스 질환의 예방에 사용될 수 있다.단독으로 또는 항바이러스제와 조합하여 다음과 같이 나타났다.
- 고위험 이식 수혜자의 CMV 관련 질병 및 사망 위험 감소
- 측정 가능한 장기 생존 이익 제공
- 치료와 관련된 부작용과 부작용을 최소화한다.[59]
간키클로비르(사이토베네) 치료는 시력 관련 질환이나 생명을 위협하는 질환을 가진 우울한 면역력을 가진 사람들에게 사용된다.발간시클로비르(Valganciclovir, Valcyte)는 항바이러스제로도 효과적이며 경구적으로 투여되는 약으로, 체내에서 간시클로비르로 전환되는 프로약이지만 후자보다 경구적으로 훨씬 잘 흡수된다.약물에 내성이 있는 바이러스의 출현으로 치료 효과가 자주 손상된다.UL97 단백질 키나아제와 바이러스성 DNA 중합효소의 다양한 아미노산 변화가 약물 내성을 유발하는 것으로 보고되었다.Foscarnet 또는 cidofovir는 Ganciclovir에 내성이 있는 CMV를 가진 사람들에게만 주어지는데, Foscarnet은 신독성이 현저하여 Ca 또는 PO가2+43− 증가하거나 감소하고 Mg 수치가2+ 감소하기 때문이다.[citation needed]
레테모비르는 유럽 의약청과[60] FDA로부터[61] HCMV 감염의 치료와 예방에 대한 승인을 받았다.
약물 저항성
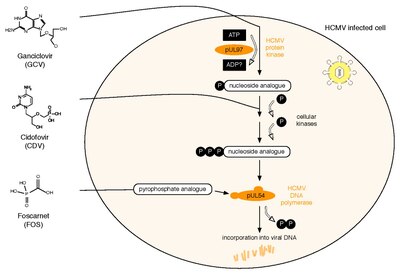
현재 허가된 세 가지 항HCMV 약물은 모두 바이러스 DNA 중합효소 pUL54를 대상으로 한다.간키클로비르(GCV)는 뉴클레오사이드 아날로그 역할을 한다.그것의 항바이러스 활성은 HCMV 단백질 키나아제인 pUL97에 의한 인산화를 필요로 한다.[62]두 번째 약인 시도포비르(Cidofovir, CDV)는 뉴클레오티드 아날로그로, 이미 인광화 되어 있어 활성화가 되어 있다.마지막으로 Foscarnet(FOS)은 행동 방식이 다르다.pUL54의 피로인산염 결합 부지를 차단하여 중합효소 기능을 직접 억제한다(참고: 조사 약물 레테모비르는 바이러스 종말제를 수반하는 메커니즘을 통해 작용한다).[63]두 개의 HCMV 단백질은 이 세 가지 약인 pUL97과 pUL54에 대한 항바이러스 저항성에 관여한다.pUL97의 특정한 돌연변이는 이 바이러스성 단백질 키나제의 인산화 활성을 감소시킬 수 있다.따라서 보다 적은 수의 단일 인산염(monophospholated) GCV를 합성하여 [64]GCV에 대한 항바이러스 저항을 유발할 수 있다. 모든 GCV 저항의 약 90%는 UL97의 그러한 돌연변이에 의해 발생한다.[65]pUL54의 돌연변이는 항바이러스제 내성을 유발하는 다른 영향을 미칠 수 있다. A그것들은 항바이러스 화합물에 대한 친화력 저하를 초래할 수 있다.이 저항 메커니즘은 GCV, CDV 및 FOS와 관련이 있으며 다중 약품 저항을 초래할 수 있다.[66]B. pUL54의 일부 돌연변이는 중합효소의 엑소누클리스 활성을 증가시킬 수 있다.이것은 통합된 GCV와 CDV의 인식을 향상시킨다.결과적으로, 이러한 dNTP 유사점은 더 효율적으로 배제된다.HCMV 약물 내성을 위한 주요 위험 요인은 바이러스 복제를 통제하기 위한 호스트 면역 시스템의 잔류 용량과 바이러스 복제의 전체 양과 기간이다.[67]HCMV 항바이러스제 내성은 표현형 또는 유전자형 약물 내성 검사를 통해 검출할 수 있다.표현형 저항성 테스트는 세포 배양에서 바이러스를 배양하고 EC50 값을 결정하기 위해 다른 항바이러스제 농도를 사용하여 그 민감성을 테스트하는 것이다.대조적으로 유전자형 저항성 시험은 시퀀싱에 의해 UL97과 UL54에서 저항 관련 돌연변이를 검출하는 것을 의미한다.유전자형 저항성 검사는 속도가 빠르지만 새로 발견된 돌연변이 각각에 대한 이전의 표현형 특성화가 필요하기 때문에 선택의 방법이 되고 있다.이는 사람의 HCMV 시퀀스를 모든 공개된 UL97 및 UL54 돌연변이와 해당 항바이러스제 민감성 표현형태를 포함하는 데이터베이스에 연결하는 웹 기반 검색 도구를 통해 수행될 수 있다.[68]
역학
미국에서 CMV 감염은 연령에 따라 6세[26] 감염자의 약 60%에서 75~80세 인구의 약 85~90%로 증가한다.[69]
참조
- ^ Davison, Andrew (27 January 2016). "Rename species in the family Herpesviridae to incorporate a subfamily designation" (PDF). International Committee on Taxonomy of Viruses (ICTV). Retrieved 13 March 2019.
- ^ taxonomy. "Taxonomy browser (Human betaherpesvirus 5)". www.ncbi.nlm.nih.gov. Retrieved 25 July 2020.
- ^ a b c d e Ryan KJ, Ray CG, eds. (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. pp. 556, 566–9. ISBN 978-0-8385-8529-0.
- ^ a b c Koichi Yamanishi; Arvin, Ann M.; Gabriella Campadelli-Fiume; Edward Mocarski; Moore, Patrick; Roizman, Bernard; Whitley, Richard (2007). Human herpesviruses: biology, therapy, and immunoprophylaxis. Cambridge, UK: Cambridge University Press. ISBN 978-0-521-82714-0.
- ^ Zanella M, Cordey S, Kaiser L (2020). "Beyond Cytomegalovirus and Epstein-Barr Virus: a Review of Viruses Composing the Blood Virome of Solid Organ Transplant and Hematopoietic Stem Cell Transplant Recipients". Clinical Microbiology Reviews. 33 (4): e00027-20. doi:10.1128/CMR.00027-20. PMC 7462738. PMID 32847820.
- ^ Melnick M, Sedghizadeh PP, Allen CM, Jaskoll T (10 November 2011). "Human cytomegalovirus and mucoepidermoid carcinoma of salivary glands: cell-specific localization of active viral and oncogenic signaling proteins is confirmatory of a causal relationship". Experimental and Molecular Pathology. 92 (1): 118–25. doi:10.1016/j.yexmp.2011.10.011. PMID 22101257.
- ^ Geder L, Sanford EJ, Rohner TJ, Rapp F (1977). "Cytomegalovirus and cancer of the prostate: in vitro transformation of human cells". Cancer Treat Rep. 61 (2): 139–46. PMID 68820.
- ^ Kumar, Amit; Tripathy, Manoj Kumar; Pasquereau, Sébastien; Al Moussawi, Fatima; Abbas, Wasim; Coquard, Laurie; Khan, Kashif Aziz; Russo, Laetitia; Algros, Marie-Paule; Valmary-Degano, Séverine; Adotevi, Olivier (April 2018). "The Human Cytomegalovirus Strain DB Activates Oncogenic Pathways in Mammary Epithelial Cells". EBioMedicine. 30: 167–183. doi:10.1016/j.ebiom.2018.03.015. ISSN 2352-3964. PMC 5952350. PMID 29628341.
- ^ T. Fülöp; A. Larbi & G. Pawelec (September 2013). "Human T cell aging and the impact of persistent viral infections". Frontiers in Immunology. 4: 271. doi:10.3389/fimmu.2013.00271. PMC 3772506. PMID 24062739. article: 271.
- ^ S. Varani & M. P. Landini (2011). "Cytomegalovirus-induced immunopathology and its clinical consequences". Herpesviridae. 2 (6): 6. doi:10.1186/2042-4280-2-6. PMC 3082217. PMID 21473750.
- ^ Staras SA, Dollard SC, Radford KW, Flanders WD, Pass RF, Cannon MJ (November 2006). "Seroprevalence of cytomegalovirus infection in the United States, 1988–1994". Clin. Infect. Dis. 43 (9): 1143–51. doi:10.1086/508173. PMID 17029132.
- ^ Britt, William J. (1 August 2017). "Congenital Human Cytomegalovirus Infection and the Enigma of Maternal Immunity". Journal of Virology. 91 (15): e02392–16. doi:10.1128/JVI.02392-16. ISSN 0022-538X. PMC 5512250. PMID 28490582.
- ^ Elizabeth G. Damato; Caitlin W. Winnen (2006). "Cytomegalovirus infection: perinatal implications". J Obstet Gynecol Neonatal Nurs. 31 (1): 86–92. doi:10.1111/j.1552-6909.2002.tb00026.x. PMID 11843023.
- ^ Caruso C, et al. (2009). "Mechanisms of immunosenescence". Immun Ageing. 6: 10. doi:10.1186/1742-4933-6-10. PMC 2723084. PMID 19624841.
- ^ a b 라르센, 로라성병 출처. 건강 참조 시리즈 디트로이트:2009년 주식회사 옴니그래픽스온라인.
- ^ Taylor GH (February 2003). "Cytomegalovirus". Am Fam Physician. 67 (3): 519–24. PMID 12588074.
- ^ Kahl, M.; Siegel-Axel, D.; Stenglein, S. (1 August 2000). "Efficient Lytic Infection of Human Arterial Endothelial Cells by Human Cytomegalovirus Strains". Journal of Virology. 74 (16): 7628–7635. doi:10.1128/jvi.74.16.7628-7635.2000. ISSN 0022-538X. PMC 112284. PMID 10906217.
- ^ Emery, Vincent C.; Cope, Alethea V.; Bowen, E. Frances; Gor, Dehila; Griffiths, Paul D. (19 July 1999). "The Dynamics of Human Cytomegalovirus Replication in Vivo". The Journal of Experimental Medicine. 190 (2): 177–182. doi:10.1084/jem.190.2.177. ISSN 0022-1007. PMC 2195570. PMID 10432281.
- ^ a b Wathen, M. W.; Stinski, M. F. (1 February 1982). "Temporal patterns of human cytomegalovirus transcription: mapping the viral RNAs synthesized at immediate early, early, and late times after infection". Journal of Virology. 41 (2): 462–477. doi:10.1128/JVI.41.2.462-477.1982. ISSN 0022-538X. PMC 256775. PMID 6281461.
- ^ Stern-Ginossar, Noam; Weisburd, Ben; Michalski, Annette; Le, Vu Thuy Khanh; Hein, Marco Y.; Huang, Sheng-Xiong; Ma, Ming; Shen, Ben; Qian, Shu-Bing (23 November 2012). "Decoding Human Cytomegalovirus". Science. 338 (6110): 1088–1093. Bibcode:2012Sci...338.1088S. doi:10.1126/science.1227919. ISSN 0036-8075. PMC 3817102. PMID 23180859.
- ^ Snaar, S. P.; Vincent, M.; Dirks, R. W. (1 February 1999). "RNA polymerase II localizes at sites of human cytomegalovirus immediate-early RNA synthesis and processing". Journal of Histochemistry and Cytochemistry. 47 (2): 245–254. doi:10.1177/002215549904700213. ISSN 0022-1554. PMID 9889260.
- ^ Penfold, M. E.; Mocarski, E. S. (8 December 1997). "Formation of cytomegalovirus DNA replication compartments defined by localization of viral proteins and DNA synthesis". Virology. 239 (1): 46–61. doi:10.1006/viro.1997.8848. ISSN 0042-6822. PMID 9426445.
- ^ Dunn, Walter; Chou, Cassie; Li, Hong; Hai, Rong; Patterson, David; Stolc, Viktor; Zhu, Hua; Liu, Fenyong (25 November 2003). "Functional profiling of a human cytomegalovirus genome". Proceedings of the National Academy of Sciences. 100 (24): 14223–14228. Bibcode:2003PNAS..10014223D. doi:10.1073/pnas.2334032100. ISSN 0027-8424. PMC 283573. PMID 14623981.
- ^ Brecht, Katharina F.; Goelz, Rangmar; Bevot, Andrea; Krägeloh-Mann, Ingeborg; Wilke, Marko; Lidzba, Karen (1 April 2015). "Postnatal Human Cytomegalovirus Infection in Preterm Infants Has Long-Term Neuropsychological Sequelae". The Journal of Pediatrics. 166 (4): 834–839.e1. doi:10.1016/j.jpeds.2014.11.002. ISSN 0022-3476. PMID 25466679.
- ^ a b Cook CH (2007). "Cytomegalovirus reactivation in "immunocompetent" patients: a call for scientific prophylaxis". The Journal of Infectious Diseases. 196 (9): 1273–1275. doi:10.1086/522433. PMID 17922387.
- ^ Sager K, Alam S, Bond A, Chinnappan L, Probert CS (2015). "Review article: cytomegalovirus and inflammatory bowel disease". Alimentary Pharmacology & Therapeutics. 41 (8): 725–733. doi:10.1111/apt.13124. PMID 25684400. S2CID 5969716.
- ^ Meinhard Classen; Guido N. J. Tytgat; M.D. PhD; Charles J. Lightdale (2010). Gastroenterological Endoscopy. Thieme. pp. 490–. ISBN 978-3-13-125852-6. Retrieved 26 June 2010.
- ^ Rafailidis, PI; Mourtzoukou, EG; Varbobitis, IC; Falagas, ME (27 March 2008). "Severe cytomegalovirus infection in apparently immunocompetent patients: a systematic review". Virology Journal. 5: 47. doi:10.1186/1743-422X-5-47. PMC 2289809. PMID 18371229.
- ^ Klemola E, Von Essen R, Henle G, Henle W (June 1970). "Infectious-mononucleosis-like disease with negative heterophil agglutination test. Clinical features in relation to Epstein–Barr virus and cytomegalovirus antibodies". J. Infect. Dis. 121 (6): 608–14. doi:10.1093/infdis/121.6.608. PMID 4316146.
- ^ Lunn, M.; Hughes, R. (1 April 2011). "The Relationship between Cytomegalovirus Infection and Guillain-Barre Syndrome". Clinical Infectious Diseases. 52 (7): 845–847. doi:10.1093/cid/cir082. ISSN 1058-4838. PMID 21427391.
- ^ Pak, Chiny; McArthur, Robertg; Eun, Hyone-Myong; Yoon, Ji-Won (1988). "Association of Cytomegalovirus Infection with Autoimmune Type 1 Diabetes". The Lancet. 332 (8601): 1–4. doi:10.1016/S0140-6736(88)92941-8. PMID 2898620. S2CID 42852009.
- ^ Lohr, J.M; Oldstone, M.B.A (1990). "Detection of cytomegalovirus nucleic acid sequences in pancreas in type 2 diabetes". The Lancet. 336 (8716): 644–648. doi:10.1016/0140-6736(90)92145-8. PMID 1975850. S2CID 9783330.
- ^ Bottieau E, Clerinx J, Van den Enden E, et al. (2006). "Infectious mononucleosis-like syndromes in febrile travelers returning from the tropics". Journal of Travel Medicine. 13 (4): 191–7. doi:10.1111/j.1708-8305.2006.00049.x. PMID 16884400.
- ^ Mattes FM, McLaughlin JE, Emery VC, Clark DA, Griffiths PD (August 2000). "Histopathological detection of owl's eye inclusions is still specific for cytomegalovirus in the era of human herpesviruses 6 and 7". J. Clin. Pathol. 53 (8): 612–4. doi:10.1136/jcp.53.8.612. PMC 1762915. PMID 11002765.
- ^ Bennekov T, Spector D, Langhoff E (March 2004). "Induction of immunity against human cytomegalovirus". Mt. Sinai J. Med. 71 (2): 86–93. PMID 15029400.
- ^ Cheng J, Ke Q, Jin Z, et al. (May 2009). Früh K (ed.). "Cytomegalovirus infection causes an increase of arterial blood pressure". PLOS Pathog. 5 (5): e1000427. doi:10.1371/journal.ppat.1000427. PMC 2673691. PMID 19436702.
- ^ a b Wei W, Ji S (2018). "Cellular senescence: Molecular mechanisms and pathogenicity". Journal of Cellular Physiology. 233 (12): 9121–9135. doi:10.1002/jcp.26956. PMID 30078211.
- ^ Bartleson JM, Radenkovic D, Verdin E (2021). "SARS-CoV-2, COVID-19 and the Ageing Immune System". Nature Aging. 1 (9): 769–782. doi:10.1038/s43587-021-00114-7. PMC 8570568. PMID 34746804.
- ^ Welte, Stefan A.; Sinzger, Christian; Lutz, Stefan Z.; Singh-Jasuja, Harpreet; Sampaio, Kerstin Laib; Eknigk, Ute; Rammensee, Hans-Georg; Steinle, Alexander (2003). "Selective intracellular retention of virally induced NKG2D ligands by the human cytomegalovirus UL16 glycoprotein". European Journal of Immunology. 33 (1): 194–203. doi:10.1002/immu.200390022. PMID 12594848. S2CID 20718868.
- ^ Hadrup SR, Strindhall J, Køllgaard T, Seremet T, Johansson B, Pawelec G, thor Straten P, Wikby A (2006). "Longitudinal studies of clonally expanded CD8 T cells reveal a repertoire shrinkage predicting mortality and an increased number of dysfunctional cytomegalovirus-specific T cells in the very elderly". Journal of Immunology. 176 (4): 2645–2653. doi:10.4049/jimmunol.176.4.2645. PMID 16456027.
- ^ Derhovanessian E, Maier AB, Hähnel K, Beck R, de Craen AJ, Slagboom EP, Westendorp RG, Pawelec G (2011). "Infection with cytomegalovirus but not herpes simplex virus induces the accumulation of late-differentiated CD4+ and CD8+ T-cells in humans" (PDF). Journal of General Virology. 92 (Pt 12): 2746–2756. doi:10.1099/vir.0.036004-0. PMID 21813708.
- ^ Pawelec G, Koch S, Franceschi C, Wikby A (2006). "Human immunosenescence: does it have an infectious component?". Annals of the New York Academy of Sciences. 1067 (1): 56–65. Bibcode:2006NYASA1067...56P. doi:10.1196/annals.1354.009. PMID 16803971. S2CID 45806175.
- ^ Derhovanessian E, Theeten H, Hähnel K, Van Damme P, Cools N, Pawelec G (2013). "Cytomegalovirus-associated accumulation of late-differentiated CD4 T-cells correlates with poor humoral response to influenza vaccination" (PDF). Vaccine. 31 (4): 685–690. doi:10.1016/j.vaccine.2012.11.041. PMID 23196209. S2CID 10483363. Archived from the original (PDF) on 19 April 2018.
- ^ Roberts ET, Haan MN, Dowd JB, Aiello AE (2010). "Cytomegalovirus antibody levels, inflammation, and mortality among elderly Latinos over 9 years of follow-up" (PDF). American Journal of Epidemiology. 172 (4): 363–371. doi:10.1093/aje/kwq177. PMC 2950794. PMID 20660122. S2CID 14983626. Archived from the original (PDF) on 19 April 2018.
- ^ Simanek AM, Dowd JB, Pawelec G, Melzer D, Dutta A, Aiello AE (2011). "Seropositivity to cytomegalovirus, inflammation, all-cause and cardiovascular disease-related mortality in the United States". PLOS One. 6 (2): e16103. Bibcode:2011PLoSO...616103S. doi:10.1371/journal.pone.0016103. PMC 3040745. PMID 21379581.
- ^ Ross, S.A.; Novak, Z.; Pati, S.; Boppana, S.B. (October 2011). "Diagnosis of Cytomegalovirus Infections". Infectious Disorders Drug Targets. 11 (5): 466–474. doi:10.2174/187152611797636703. ISSN 1871-5265. PMC 3730495. PMID 21827433.
- ^ "United Blood Services FAQs". Archived from the original on 19 May 2007. Retrieved 23 May 2007.
- ^ Ljungman, Per (15 August 2014). "Donor cytomegalovirus status influences the outcome of allogeneic stem cell transplant: a study by the European group for blood and marrow transplantation". Clin Infect Dis. 59 (4): 473–81. doi:10.1093/cid/ciu364. PMID 24850801. Retrieved 3 September 2020.
- ^ Ljungman, Per; Hakki, Morgan; Boeckh, Michael (February 2011). "Cytomegalovirus in Hematopoietic Stem Cell Transplant Recipients". Hematology/Oncology Clinics of North America. 25 (1): 151–169. doi:10.1016/j.hoc.2010.11.011. PMC 3340426. PMID 21236396.
- ^ Pass RF, Zhang C, Evans A, et al. (March 2009). "Vaccine prevention of maternal cytomegalovirus infection". N. Engl. J. Med. 360 (12): 1191–9. doi:10.1056/NEJMoa0804749. PMC 2753425. PMID 19297572.
- ^ "A Study to Evaluate a Therapeutic Vaccine, ASP0113, in Cytomegalovirus (CMV)-Seropositive Recipients Undergoing Allogeneic, Hematopoietic Cell Transplant (HCT) (HELIOS)". ClinicalTrials.gov. 12 June 2013. Retrieved 26 October 2015.
- ^ "An Evaluation of a Cytomegalovirus (CMV) Vaccine (ASP0113) in CMV-Seropositive and CMV-Seronegative Healthy Subjects and CMV-Seronegative Dialysis Patients". ClinicalTrials.gov. 8 July 2015. Retrieved 22 October 2015.
- ^ "Multi-antigen CMV-MVA Triplex Vaccine in Reducing CMV Complications in Patients Previously Infected With CMV and Undergoing Donor Hematopoietic Cell Transplant". ClinicalTrials.gov. 21 July 2015. Retrieved 23 January 2016.
- ^ "Vaccine Therapy in Reducing the Frequency of Cytomegalovirus Events in Patients With Hematologic Malignancies Undergoing Donor Stem Cell Transplant". ClinicalTrials.gov. 12 March 2015. Retrieved 23 January 2016.
- ^ "When & How to Wash Your Hands Handwashing". CDC. 7 March 2016. Archived from the original on 13 September 2017. Retrieved 16 October 2017.
- ^ "CMV Overview Cytomegalovirus and Congenital CMV Infection". CDC. 17 June 2016. Archived from the original on 16 October 2017. Retrieved 16 October 2017.
- ^ "CMV Transmission". National CMV Foundation. Archived from the original on 16 October 2017. Retrieved 16 October 2017.
- ^ 2012년 4월 26일 웨이백 머신 CSL Behring AG에 보관된 Cytogue 처방 정보
- ^ "Previmys EPAR summary for the public" (PDF). European Medicines Agency. Archived (PDF) from the original on 27 June 2018. Retrieved 27 June 2018.
- ^ "Approval Package for Letermovir" (PDF). FDA. Archived (PDF) from the original on 27 June 2018. Retrieved 27 June 2018.
- ^ Sullivan V, Talarico CL, Stanat SCC, Davis M, Coen DM, Biron KK (1992). "A protein kinase homologue controls phosphorylation of ganciclovir in human cytomegalovirus-infected cells". Nature. 358 (6382): 162–164. Bibcode:1992Natur.358..162S. doi:10.1038/358162a0. PMID 1319560. S2CID 4309307.
- ^ Chrisp P, Clissold SP (1991). "Foscarnet. A review of its antiviral activity, pharmacokinetic properties and therapeutic use in immunocompromised patients with cytomegalovirus retinitis". Drugs. 41 (1): 104–129. doi:10.2165/00003495-199141010-00009. PMID 1706982.
- ^ Biron KK, Fyfe JA, Stanat SC, Leslie LK, Sorrell JB, Lambe CU, Coen DM (1986). "A human cytomegalovirus mutant resistant to the nucleoside analog 9-([2-hydroxy-1-(hydroxymethyl)ethoxy]methyl)guanine (BW B759U) induces reduced levels of BW B759U triphosphate". Proc. Natl. Acad. Sci. U.S.A. 83 (22): 8769–8773. Bibcode:1986PNAS...83.8769B. doi:10.1073/pnas.83.22.8769. PMC 387013. PMID 3022304.
- ^ Chou S (1999). "Antiviral drug resistance in human cytomegalovirus". Transpl. Infect. Dis. 1 (2): 105–114. doi:10.1034/j.1399-3062.1999.010204.x. PMID 11428978. S2CID 23668301.
- ^ C. Gilbert & G. Boivin (2005). "Human cytomegalovirus resistance to antiviral drugs". Antimicrob. Agents Chemother. 49 (3): 873–883. doi:10.1128/AAC.49.3.873-883.2005. PMC 549271. PMID 15728878.
- ^ Drew WL (2000). "Ganciclovir resistance: a matter of time and titre". Lancet. 356 (9230): 609–610. doi:10.1016/S0140-6736(00)02597-6. PMID 10968428. S2CID 46533224.
- ^ Chevillotte M, von Einem J, Meier BM, Lin FM, Kestler HA, Mertens T (2010). "A new tool linking human cytomegalovirus drug resistance mutations to resistance phenotypes". Antiviral Research. 85 (2): 318–27. doi:10.1016/j.antiviral.2009.10.004. PMID 19853628.
- ^ Pawelec G, McElhaney JE, Aiello AE, Derhovanessian E (2012). "The impact of CMV infection on survival in older humans" (PDF). Current Opinion in Immunology. 24 (4): 507–511. doi:10.1016/j.coi.2012.04.002. PMID 22541724. S2CID 623760. Archived from the original (PDF) on 19 April 2018.
외부 링크
| 위키미디어 커먼즈에는 휴먼 사이토메갈로바이러스와 관련된 미디어가 있다. |
| 위키피아는 인간 베타헤르페스 바이러스 5와 관련된 정보를 가지고 있다. |
- 컬리의 인간 베타페스바이러스 5
- 시토메갈로바이러스(CMV) 미국 질병관리예방센터(CDC). 2009년 5월 22일
- HCMV 약물 내성 돌연변이 도구
- "Human herpesvirus 5". NCBI Taxonomy Browser. 10359.