소아마비 백신
Polio vaccine | |
| 백신 설명 | |
|---|---|
| 대상 | 소아마비 |
| 백신 종류 | IPV: 비활성화 OPV: 감쇠 |
| 임상 데이터 | |
| 상호 | Ipol, Poliovax, 기타 |
| AHFS/Drugs.com | 모노그래프 |
| Medline Plus | a601177 |
| 라이선스 데이터 | |
| 임신 카테고리 |
|
| 루트 행정부. | IPV: 비경구 OPV: 구강 |
| ATC 코드 | |
| 법적 상태 | |
| 법적 상태 |
|
| 식별자 | |
| CAS 번호 | |
| 드러그뱅크 | |
| 켐스파이더 |
|
| | |
소아마비 백신은 소아마비 예방을 위해 사용되는 백신이다.[2]두 가지 유형이 사용됩니다: 주입에 의해 제공되는 비활성 폴리오 바이러스와 구강에서 제공되는 약화된 폴리오 바이러스.[2]세계보건기구(WHO)[2]는 모든 어린이들이 소아마비 예방접종을 완전히 받을 것을 권고하고 있다.이 두 가지 백신은 [3][4]전 세계에서 소아마비를 제거했고 1988년 약 35만 건에서 2018년 [5][6]33건으로 매년 보고되는 환자 수를 줄였다.
불활성화 소아마비 백신은 매우 [2]안전하다.주사 [2]부위가 약간 붉어지거나 아플 수 있습니다.경구 소아마비 백신은 [2]백신과 관련된 마비성 소아마비 백신을 100만 회 투여할 때마다 약 3건의 사례를 일으킨다.이것은 소아마비 [7]감염으로 마비된 백만 명당 5천 명의 환자들과 비교된다.두 종류의 백신은 일반적으로 임신 중이나 HIV/AIDS에 걸렸지만 [2]그 외에는 건강한 사람들에게 투여해도 안전합니다.그러나 소아마비 바이러스의 일종인 순환성 백신유래 폴리오바이러스(cVDPV)의 출현은 백신을 안전하게 만들어 CVDPV2의 [8]발병을 막기 위한 새로운 경구 소아마비 백신 타입 2(nOPV2)의 개발로 이어졌다.
소아마비 백신의 첫 번째 성공적인 시연은 1950년 힐러리 코프로스키가 사람들이 마신 [9]살아있는 약독화 바이러스를 가지고 있었다.이 백신은 미국에서는 사용이 허가되지 않았지만 다른 [9]곳에서는 성공적으로 사용되었습니다.조나스 솔크에 의해 개발된 불활성화(죽인) 소아마비 백신의 성공은 1955년에 발표되었다.[2][10]또 다른 감쇠형 경구 소아마비 백신은 Albert Sabin에 의해 개발되어 [2][11]1961년에 상업적으로 사용되었다.
소아마비 백신은 세계보건기구의 필수 [12]의약품 목록에 있다.
의료 용도
그 바이러스의 백신 접종으로 간의 전염의 Interruption 세계 소아마비 eradication,[13]에 정상적인 면역 기능을 가진 개인에 poliovirus하기도 어떤 장기적인 캐리어 태감 존재하는데, 소아마비 바이러스 nature,[14]이 바이러스의 ti의 장기간 원자 환경에서 생존에 없nonprimate 저장 장치하는 게 중요하다.나 appea리모트여야 합니다.백신에는 두 가지 종류가 있다: 불활성화 소아마비 백신과 경구 소아마비 백신.
비활성화
IPV(주입)를 사용하면 90% 이상의 개인이 2회 불활성화 소아마비 백신(IPV) 투여 후 세 가지 혈청형 모두에 대한 보호 항체를 개발하고 최소 99%는 3회 투여 후 소아마비 바이러스에 면역된다.IPV에 의해 유도되는 면역의 지속 시간은 확실치 않지만, 완전한 연속이 [15]수 년 동안 보호를 제공하는 것으로 생각된다.1990년대 많은 선진국에서 경구백신을 대체한 것은 주로 경구백신의 [16][17]백신 유래 소아마비 위험이 작았기 때문이다.
감쇠
경구 소아마비 백신은 무균 주사기의 필요성을 없애고 대량 예방 접종 캠페인에 더 적합했기 때문에 IPV보다 투여하기 쉬웠다.OPV는 또한 체액 면역과 세포 매개 [18]면역 모두를 제공하기 때문에 소크 백신보다 더 오래 지속되는 면역력을 제공했습니다.
OPV 1회 복용량은 [19]약 50%의 수용자에서 세 가지 폴리오바이러스 혈청형에 대한 면역성을 생성한다.생감쇠성 OPV 3회 복용량은 수용자의 95% 이상에서 세 가지 폴리오바이러스 유형에 대한 보호 항체를 생성한다.OPV는 야생 폴리오바이러스의 주요 침입 장소인 장에서 우수한 면역력을 만들어, 바이러스가 [20]풍토적인 지역의 야생 바이러스 감염을 예방하는 데 도움을 준다.백신에 사용된 살아있는 바이러스는 대변에서 거의 배출되지 않으며 지역 사회 내의 다른 사람들에게도 거의 전파되지 않는다.또한 살아있는 바이러스는 운송과 저장에 대한 엄격한 요구사항이 있으며, 일부 고온지역이나 원격지역에서는 문제가 됩니다.다른 생바이러스 백신과 마찬가지로 OPV에 의해 시작된 면역은 아마도 [15]평생 지속될 것이다.
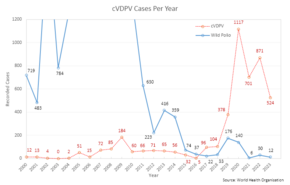
3가 OPV(야생 1, 2, 3에 대한)는 전 세계적으로 소아마비 감염을 거의 근절하기 위해 사용되어 왔다.[21]세계 소아마비 퇴치 이니셔티브가 주도하는 155개국은 2016년 [22]4월 17일부터 5월 1일까지 2가(야생 유형 1과 3에 대한)를 사용하도록 전환했다.2가의 OPV는 타입 1과 타입 3에 대해 더 효과적이지만 타입 [23]2에는 적용되지 않습니다.2017년 현재 미국은 3가 버전 사용을 계속 권장하고 있지만 완전히 비활성화된 [21]버전의 사용을 권장하고 있다.다른 요인들 중에서도 2형 변종에 대한 2가 백신으로의 전환과 관련 면역 결핍은 순환 백신 유래 폴리오바이러스 2형(cVDPV2)의 발생으로 이어져 2016년 2건에서 2020년 [24]1037건으로 증가했다.이에 따라 신종 경구 소아마비 백신 타입 2(nOPV2)는 감염성 [8]소아마비로 돌아갈 위험이 적은 타입 2에 대한 보다 안전한 형태의 예방접종을 제공하기 위해 개발됐다.
스케쥴
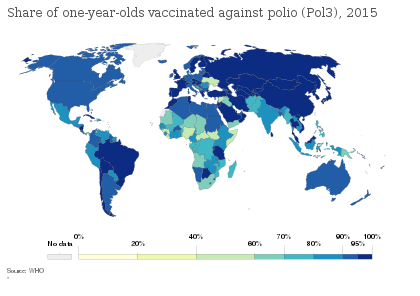
WHO는 풍토성 소아마비가 있거나 수입 사례의 위험이 높은 국가에서 출생 시 OPV 백신을 권장하고, 그 후 생후 6주부터 최소 4주 간격으로 3회 OPV 선량과 최소 1회 이상의 IPV 선량을 권장한다.예방접종 범위가 90% 이상이고 수입 위험이 낮은 국가에서 WHO는 생후 2개월부터 시작하는 하나 또는 두 개의 IPV 선량을 권장하고, 피폭 위험에 따라 선량을 4-8주 간격으로 분리한다.WHO는 적용 범위가 가장 높고 수입 및 전염 위험이 가장 낮은 국가에서 생후 [2]2개월 전에 첫 번째 선량을 투여한 경우 6개월 이상의 간격 후에 추가 선량을 투여하는 3가지 IPV 주입의 1차 시리즈를 권장한다.
부작용
불활성화 소아마비 백신은 매우 안전하다.주사 부위가 약간 붉어지거나 아플 수 있습니다.경구 소아마비 백신은 백신과 관련된 마비성 소아마비 백신을 약 3회 복용할 때 발생한다.그것들은 일반적으로 임신한 사람이나 HIV/AIDS에 걸린 사람, 그러나 그 [2]외에는 건강한 사람에게 주어도 안전합니다.
백신 알레르기 반응
불활성화 소아마비 백신은 미량의 항생제, 스트렙토마이신, 폴리믹신 B, 네오마이신을 함유하고 있기 때문에 몇몇 사람들에게 알레르기 반응을 일으킬 수 있다.이 약에 알레르기 반응을 보이는 사람에게 투여해서는 안 된다.보통 주사를 맞은 후 몇 분에서 몇 시간 안에 나타나는 알레르기 반응의 징후와 증상에는 호흡곤란, 약함, 소음 또는 쌕쌕거림, 심박수 변동, 피부 발진, [26]현기증이 포함된다.
백신에 의한 소아마비
OPV의 잠재적인 부작용은 신경학적 감염과 [27]마비를 일으키는 형태로 재결합하는 것으로 알려진 능력이다.이 병원체가 치명적인 형태로 유전적으로 역전되는 것은 상당한 시간이 걸리며(최소 12개월), 최초 예방접종을 받은 사람에게 영향을 미치지 않는다.백신에서 파생된 약독화 바이러스는 보통 백신 접종을 받은 사람들로부터 제한된 기간 동안 배설된다.따라서 위생상태가 불량하고 예방접종범위가 낮은 지역에서는 백신에서 유래한 바이러스가 자연히 치명적인 형태로 전환되어 환경 내에서 확산되면 미접종자가 [28]감염될 수 있다.백신유래 폴리오바이러스(VDPV)에 의한 마비를 포함한 임상질환은 야생 폴리오바이러스에 [29]의한 질병과 구별할 수 없다.순환하는 백신 유래 폴리오바이러스(cVDPV)[30]에 의해 야기되는 백신 관련 마비성 폴리오바이러스(VAPP)의 발병이 보고되었으며, 아마도 OPV 자체가 관련된 [31][32]발병주로부터 보호되기 때문에 OPV에 의한 커버리지가 낮은 영역에서 발생하는 경향이 있다.야생 소아마비 환자가 사상 최저치를 기록하면서 2017년은 야생 폴리오 바이러스보다 더 많은 cVDPV 환자가 기록된 첫 해로,[33] 이러한 추세는 계속될 것으로 예상된다.
이에 맞서기 위해 WHO는 2016년 3가 소아마비 백신에서 2가 소아마비 [34]백신으로 바꾸기로 결정했다.이 백신은 [35]1999년에 근절되었기 때문에 더 이상 2형 소아마비 바이러스를 포함하지 않는다.
오염 우려
1960년 폴리오바이러스 백신 제조에 사용된 붉은털원숭이 신장세포는 1960년에도 발견된 원숭이를 감염시키는 자연발생 바이러스인 시미안바이러스-40(SV40)[36]에 감염된 것으로 확인됐다.1961년 SV40은 [37]설치류에게 종양을 일으키는 것으로 밝혀졌다.보다 최근에, 그 바이러스는 뇌와 뼈 종양, 흉막과 복막 중피종,[38][39] 그리고 비호지킨 림프종과 같은 인간의 특정 형태의 암에서 발견되었다.그러나 SV40은 이러한 [40]암을 유발하는 것으로 결정되지 않았다.
SV40은 1955년에서 [36]1963년 사이에 사용되었던 주입된 형태의 IPV 재고가 있는 것으로 밝혀졌다.OPV [36]양식에는 없습니다.백신의 일부가 SV40에 오염된 1955년부터 1963년 사이에 9800만 명 이상의 미국인이 소아마비 백신을 1회 이상 접종했으며, 약 1000만-3000만 명의 미국인이 SV40에 [36]오염된 백신을 접종했을 것으로 추정된다.이후 1980년까지 구소련권 국가들이 생산해 구소련, 중국, 일본 및 여러 아프리카 국가에서 사용하던 백신이 오염됐을 가능성이 있다는 분석이 나왔고, 이는 수억 명이 [41]더 SV40에 노출되었을 수 있다는 것을 의미한다.
1998년 국립암연구소는 연구소의 SEER 데이터베이스에서 암 환자 정보를 사용하여 대규모 연구를 수행했다.연구에서 발표된 연구 결과는 SV40이 [42]포함된 백신을 접종한 사람에게서 암 발병률이 증가하지 않았음을 보여주었다.스웨덴의 또 다른 대규모 연구는 1957년까지 잠재적으로 오염된 소아마비 백신을 접종한 70만 명의 암 발생률을 조사했다. 이번 연구에서는 SV40이 포함된 소아마비 백신을 접종한 사람과 그렇지 [43]않은 사람 간에 암 발생률이 증가하지 않았음을 다시 밝혔다.그러나 SV40이 사람에게 암을 유발하는지에 대한 의문은 여전히 논란이 되고 있으며,[40] 논란을 해결하기 위해서는 인체 조직에서 SV40을 검출하기 위한 개선된 분석 개발이 필요할 것이다.
경구 소아마비 백신을 개발하기 위한 경쟁 동안, 몇 가지 대규모 인체 실험이 수행되었다.1958년까지 국립보건원은 사빈 균주를 사용하여 생산된 OPV가 가장 [44]안전하다고 결정했다.그러나 1957년에서 1960년 사이에 힐러리 코프로스키는 전 세계에서 그의 백신을 계속 투여했다.아프리카에서는 벨기에 영토(현 콩고 민주 공화국, 르완다, 부룬디)[45][46]에서 약 100만 명의 사람들에게 백신을 투여했다.이러한 인간 실험의 결과는 [47]논란이 되어 왔으며, 1990년대에 이 백신이 침팬지에서 인간으로 시미안 면역 결핍 바이러스를 전염시키는 데 필요한 조건을 만들어 HIV/AIDS를 유발했다는 근거 없는 주장이 제기되었다.그러나 이 가설들은 결정적으로 [45]반박되었다.2004년까지 아프리카의 소아마비 환자는 대륙 서부의 일부 고립된 지역으로 감소했으며, 다른 지역에서는 산발적으로 발생했다.백신 접종 캠페인에 대한 최근 현지 반대는 적절한 [48][49]정보 부족으로 인해 진화했으며, 종종 백신이 [50]불임성을 유발할 수 있다는 우려와 관련이 있다.이 질병은 나이지리아와 몇몇 다른 아프리카 국가들에서 필요한 정보 없이 다시 발생했는데, 역학학자들은 이 질병이 그들의 아이들이 소아마비 [51]백신을 맞도록 허락하기 위해 특정 지역 주민들에 의해 거부되었기 때문이라고 믿고 있다.
제조하다
비활성화
소크 백신인 IPV는 원숭이 신장 조직 배양(Vero 세포주)의 한 종류에서 자란 야생 독성 참조 변종인 Mahoney(타입 1 폴리오바이러스), MEF-1(타입 2 폴리오바이러스), Saukett(타입 3 폴리오바이러스)을 기반으로 하며, 이들은 포르말린에 [52]의해 활성화되지 않습니다.주사된 소크 백신은 혈류에 IgG 매개 면역력을 부여해 소아마비 감염이 바이러스혈증으로 진행되는 것을 막고 운동 신경세포를 보호함으로써 구근성 소아마비와 폴리오 증후군의 위험을 없앤다.
미국에서는 파상풍, 디프테리아 및 무세포성 백일해 백신(DTaP)과 B형 간염 [19]백신 소아용량과 함께 백신을 투여한다.영국에서 IPV는 파상풍, 디프테리아, 백일해, 헤모필루스 인플루엔자 [53]b형 백신과 결합된다.
감쇠

OPV는 바이러스가 인간 이외의 세포를 통해 아생리학적 온도로 전달되어 바이러스 [54]게놈에서 자발적인 돌연변이를 만들어 내는 약화된 백신이다.경구 소아마비 백신은 여러 그룹에 의해 개발되었으며, 그 중 하나는 Albert Sabin에 의해 주도되었다.힐러리 코프로스키와 H.R. 콕스가 이끄는 다른 그룹은 자체 감쇠 백신 변종을 개발했다.1958년 국립보건원은 살아있는 소아마비 백신에 대한 특별 위원회를 만들었다.다양한 백신은 원숭이에게서 낮은 신경병리 발생률을 유지하면서 소아마비에 대한 면역성을 유도하는 능력에 대해 신중하게 평가되었다.미하일 추마코프와 그의 동료들에 의해 1950년대 후반에서 1960년대 초반에 소련에서 수행된 대규모 임상 실험은 [55][56]백신의 안전성과 높은 효과를 입증했다.이러한 결과를 바탕으로 Sabin 균주가 전 세계 [44]유통용으로 선택되었습니다.57개의 뉴클레오티드 치환에 의해 감쇠된 사빈1의 변종(마호니 혈청형)과 구별되며, 2개의 뉴클레오티드 치환에 의해 사빈2의 변종이 감쇠되며, 10개의 치환이 사빈3의 [52]변종을 감쇠시킨다.세 가지 사빈 백신 모두에 공통적인 1차 감쇠 인자는 바이러스의 내부 리보솜 진입 [57]부위에 위치한 돌연변이로, 이는 줄기세포 구조를 변화시키고 폴리오바이러스가 숙주 [58]세포 내에서 RNA 템플릿을 번역하는 능력을 감소시킨다.사빈백신의 약화된 폴리오바이러스는 감염과 복제의 주요 부위인 내장에서 매우 효율적으로 복제되지만 신경계 조직 내에서 효율적으로 복제될 수 없다.1961년 타입 1과 타입 2의 경구 폴리오바이러스 백신(MOPV)이 허가되었고 1962년 타입 3 MOPV가 허가되었다.1963년, 3가 OPV(TOPV)가 허가되었고, 미국과 세계 대부분의 다른 국가에서 선택 백신이 되었고, 주로 비활성화된 소아마비 [59]백신을 대체했다.두 번째 대량 예방 접종 물결은 소아마비 환자 수를 더욱 극적으로 감소시켰다.1962년에서 1965년 사이에 약 1억 명의 미국인이 (당시 인구의 56%가) 사빈 백신을 맞았습니다.그 결과 소크백신 [60]도입 이후 상당히 감소된 수치에서도 소아마비 환자 수가 상당히 감소하였다.
OPV는 보통 10~20회분의 백신이 담긴 병에 담겨 제공된다.경구 소아마비 백신 1회 복용량(보통 2방울)에는 사빈 1(PV1에 유효), 사빈 2주 감염량 100,000개, 사빈 3주 감염량 60만개가 포함된다.이 백신에는 약간의 항생제인 네오마이신과 스트렙토마이신이 들어있지만 [61]방부제는 들어있지 않다.
역사
일반적인 의미에서, 예방접종은 면역체계를 '면역원'으로 프라이밍함으로써 효과가 있다.감염제를 사용하여 면역반응을 자극하는 것을 면역이라고 한다.소아마비에 대한 면역의 발달은 야생 폴리오바이러스의 사람 대 사람 전염을 효율적으로 차단함으로써 개인 백신 접종자와 더 넓은 [13]지역사회를 보호한다.
두 가지 소아마비 백신의 개발은 최초의 현대적 대량 접종으로 이어졌다.미국에서 야생 바이러스의 풍토병으로 인한 마비성 소아마비성 근막염의 마지막 사례는 1979년에 발생했으며, 중서부 몇몇 [19]주에서 아미쉬족 사이에서 발병했다.
1930년대
1930년대에는 폴리오바이러스가 어떻게 전염되는지, 어떻게 예방할 수 있는지에 대해 알려진 것이 거의 없기 때문에, 폴리오바이러스는 특히 무서운 것으로 인식되었다.또한 이 바이러스는 비교적 낮은 사망률과 [62]질병률에도 불구하고 주로 부유한 어린이에게 영향을 미치는 것으로 알려져 백신 개발의 주요 표적이 되었다.그럼에도 불구하고, 이 분야의 연구자 커뮤니티는 지금까지 백신 개발에 대한 비공식적인 모라토리엄을 대부분 관찰해 왔다. 왜냐하면 백신 개발은[63][64] 너무 높은 위험을 보이는 것으로 인식되었기 때문이다.
이것은 1930년대 초에 미국 단체들이 이 도전에 나서면서 바뀌었다.모리스 브로디는 뉴욕시의 공중 보건 연구실에서 팀을 이끌었고 존 콜머 박사는 필라델피아 피부 의학 연구소와 협력했다.이 두 연구자 사이의 경쟁은 의학 연구에 대한 감독 부족과 결합되어 이러한 초기 백신 개발 [65][66][62]벤처의 방법론과 결과에 반영되는 인종과 같은 사고방식을 갖게 되었다.
콜머 생백신
콜머는 1932년에 백신 개발 프로젝트를 시작했고 궁극적으로 감쇠 또는 살아있는 바이러스 백신을 생산하는 데 초점을 맞췄다.광견병과 황열 백신의 성공에 영감을 받아, 그는 소아마비 바이러스를 [65]변성시키기 위해 비슷한 과정을 사용하기를 희망했다.소아마비 백신을 감쇠시키기 위해 그는 반복적으로 원숭이를 [67]통해 바이러스를 전파했다.콜머는 나중에 "머리카락날 정도로 아마추어적인 목욕통 [68]진과 동등한 치료제"라고 묘사되는 생산 방법을 사용하여 감염된 원숭이들의 척수를 갈아서 소금 용액에 담갔다.그리고 나서 그는 용액을 메쉬로 여과하여 리시놀라트로 처리한 후 제품을 14일[65] 동안 냉장 보관하여 궁극적으로 "검증 가능한 마녀 양조"[69]라고 명명될 것을 만들었습니다.
당시의 규범에 따라,[64] 콜머는 1934년 자가 실험을 진행하기 전에 42마리의 원숭이로 비교적 작은 동물 실험을 완료했다.그는 자신과 두 자녀, 그리고 [64]조수에게 백신을 시험했다.그는 그의 백신이 안전하다고 선언하기 전에 단지 23명의 아이들에게만 더 백신을 투여했고,[64] 더 큰 효과의 시험을 위해 의사와 보건 부서에 백신을 보냈습니다.1935년 4월, 그는 백신을 100명의 아이들에게 아무런 부작용 [70]없이 실험했다고 보고할 수 있었다.콜머의 첫 공식 결과는 1935년 11월에야 발표되었는데, 콜머는 약화된 [70]백신을 접종한 446명의 어린이와 어른의 결과를 발표했다.그는 또한 피부과학연구소와 신시내티의 머렐사가 함께 미국과 캐나다 [70]전역에 약 700명의 의사에게 12,000회분의 백신을 배포했다고 보고했다.콜머는 이 실험적인 백신 접종 프로그램에 대한 모니터링에 대해 설명하지 않았고, 이 의사들에게 백신을 투여하는 방법이나 부작용을 [70]보고하는 방법에 대한 지침을 제공하지도 않았다.콜머는 이후 대부분의 출판물을 백신 접종 후 [70][71]마비성 소아마비 환자 10명 이상의 원인이 무엇이라고 생각되는지를 설명하는 데 할애했다.이 사건들 중 [70]6건은 치명적이었다.콜머는 통제 그룹이 없었지만 더 많은 어린이들이 병에 [71]걸렸을 것이라고 주장했다.
브로디 불활성화 백신
콜머의 프로젝트와 거의 동시에 모리스 브로디는 뉴욕시 보건부의 면역학자인 윌리엄 H. 파크 박 박사와 함께 폴리오바이러스를 연구했다.대통령 생일 무도회 위원회의 보조금 지원으로 브로디는 불활성화되거나 "살해된 바이러스" 백신의 개발을 추진할 수 있었다.브로디의 과정은 또한 전염성 원숭이의 척수를 갈고 그 척수를 다양한 [72]살균제로 치료함으로써 시작되었고, 궁극적으로 포름알데히드가 가장 효과적이라는 것을 발견했다.1934년 6월 1일, 브로디는 불활성 소아마비 바이러스에 [73][74]걸린 세 마리의 원숭이에게 면역력을 성공적으로 유도했다는 그의 첫 번째 학술 논문을 출판할 수 있었다.26마리의 원숭이에 대한 지속적인 연구를 통해 브로디는 살아있는 바이러스 백신을 투여하면 체액 면역이 생기는 반면 죽은 바이러스 백신을 투여하면 조직 [70]면역이 생기는 경향이 있다고 결론지었다.
곧이어 콜머와 비슷한 프로토콜을 따라 브로디는 뉴욕 보건부 연구소에서 자신과 [64]동료들을 대상으로 자가 실험을 진행했습니다.대중들은 성공적인 백신이 [74]출시되기를 바랐기 때문에 브로디의 진전은 대중 언론에 의해 열렬히 보도되었다.이러한 보고는 초기 안전 시험을 [64]받은 뉴욕시 정신병원에 있는 12명의 아이들에 대해서는 언급하지 않았다.어떤 실험 대상도 부작용을 겪지 않자, 동시대에 의해 [75]"발밑에서 풀이 자라게 놔두지 않는 사람"이라고 묘사된 박 박사는 백신이 [67]안전하다고 선언했다.심각한 소아마비가 캘리포니아 컨 카운티를 강타했을 때, 그곳은 매우 짧은 시간에 새로운 백신을 위한 첫 번째 시험 장소가 되었습니다.1934년 11월부터 1935년 5월 사이에 Kern County에서 1,500회 이상의 백신이 투여되었다.초기 결과는 매우 유망했지만, 인력 부족과 열악한 프로토콜 설계로 인해 Brodie는 1935년 [74][70]8월 캘리포니아 결과를 발표했을 때 비판의 대상이 되었습니다.민간 의사를 통해 브로디는 또한 백신을 접종한 9,000명의 어린이와 백신을 접종하지 않은 4,500명의 연령 및 위치 일치 대조군을 포함한 광범위한 현장 연구를 수행했다.이번에도 결과는 유망했다.백신을 접종한 사람들 중 극소수만이 소아마비에 걸렸다.대부분은 백신 접종 전에 피폭되었고,[70] 연구 중인 전체 일련의 백신 접종을 받은 사람은 아무도 없었다.또한 노스캐롤라이나 롤리의 소아마비 유행은 미국 공중 보건국이 생일 무도회 [67][70]자금으로 브로디 백신을 고도로 구조적으로 시험할 수 있는 기회를 제공했다.
학술적 리셉션
그들의 연구가 진행되는 동안, 더 많은 세균학자들이 새로운 폴리오바이러스 [63]백신의 안전성과 효능에 대한 우려를 제기하기 시작했다.이 시기에는 의학 연구에 대한 감시가 거의 없었고, 연구 참가자들에 대한 윤리적 처우는 주로 동료 [65]학자들의 도덕적 압력에 의존했다.브로디의 불활성화 백신은 죽은 바이러스 백신이 효과가 없다고 느끼는 많은 사람들로부터 정밀 조사를 받았다.연구자들이 그가 동물 실험을 통해 만들어 낸 조직 면역력을 복제할 수 있었던 반면, 지배적인 지혜는 체액 면역력이 효과적인 [70]백신을 위해 필수적이라는 것이었다.콜머는 학술지에 [72]실린 살처분된 바이러스의 접근법에 대해 직접적으로 의문을 제기했다.그러나 콜머의 연구는 그의 살아있는 바이러스 백신 접종 후 마비된 어린이들이 늘어나고, 특히 많은 [76]경우 발이 아닌 팔에서 마비가 시작된다는 보고에 대해 훨씬 더 많은 우려를 불러일으켰다.콜머와 브로디 둘 [63]다 1935년 10월 밀워키에서 열린 미국 공중보건협회 연차총회에서 연구를 발표하기 위해 소집되었다.추가로, 닥터.Thomas M. Rivers는 백신 개발 [63]노력에 대한 저명한 비평가로서 제시된 각각의 논문을 논의하도록 요청받았다.이에 따라 APHA는 다음 [63]달 남부지부 연차총회에서 소아마비 관련 심포지엄을 개최하기로 했다.이 회의에서 미국 공중 보건국의 제임스 리크 박사는 콜머 백신이 여러 명의 사망자를 냈다는 임상 증거를 즉시 제시하고 콜머를 [63]살인자라고 비난한 것이 바로 이 회의에서였다.리버스가 그의 구술사에서 회상했듯이, "모든 지옥이 무너졌고, 모두가 동시에 말하려고 하는 것처럼 보였다...Jimmy Leake는 과학 회의에서 [63]제가 들어본 것 중 가장 강한 언어를 사용했습니다."모든 측면에서 공격을 받은 브로디는 일어서서 "리버스 박사에 따르면 내 백신은 좋지 않은 것 같다. 리크 박사에 따르면 콜머 박사의 백신은 위험하다."[63]라고 말했다고 한다. 콜머는 간단히 대답했다. "여러분, 이번에는 제가 바닥을 열고 [63]삼켰으면 좋겠어요."결국 콜머의 생백신은 확실히 위험한 것으로 나타났고 밀워키 [76][71][70]회담 전에 이미 1935년 9월에 철회되었다.심포지엄의 합의는 브로디 백신의 효능에 대해 대체로 회의적이었지만, 그 안전성에 대해서는 의문의 여지가 없었고, 그 권고는 훨씬 더 큰 규모의 통제된 실험에 [76]대한 것이었다.그러나 백신을 접종한 후 세 아이가 마비성 소아마비에 걸렸을 때 조지아주 웜스프링스 재단(이 프로젝트의 주요 후원자 역할을 함) 이사들은 1935년 [76]12월 백신을 철회할 것을 요구했다.그 철회 이후, 이전에 관측되었던 인간 소아마비 백신 개발의 모라토리엄이 재개되었고 거의 20년 동안 [70][71]다른 시도는 없을 것이다.
브로디는 폴리오바이러스 백신을 추구하는 데 있어 가장 큰 진전을 이뤘지만, [74]덜 알려진 연구원이라는 그의 지위 때문에 가장 중요한 경력상의 영향을 받았다.현대의 연구자들은 브로디가 효과적인 소아마비 백신을 개발했을지 모르지만, 이 [70]돌파구를 이해하고 이용하기에는 당시의 기초 과학과 기술이 부족했다는 것을 인식하고 있다.포르말린 불활성화 바이러스를 사용한 브로디의 연구는 나중에 소크 백신의 기초가 될 것이지만,[70] 그는 이 성공을 보기 위해 살지는 못할 것이다.브로디는 심포지엄이 [70]발표된 지 3개월 만에 자리에서 해고되었다.그는 다른 실험실 자리를 구할 수 있었지만, 불과 3년 후 [70][74]36세의 나이로 심장마비로 사망했다.반면 노년기에 노쇠한 것으로 여겨졌던 박 전 대표는 1939년 [67]사망하기 전 명예롭게[63] 퇴임할 수 있었다.이미 정평이 나 있고 존경받는 연구원인 콜머는 템플 대학교 [70]의과 교수로 돌아왔다.콜머는 1957년 [67][63][71][77]은퇴할 때까지 여러 개의 상을 받았고 수많은 논문, 기사, 교과서를 출판하는 등 매우 생산적인 경력을 가지고 있었습니다.
1948
1948년 보스턴 아동병원의 존 엔더스 연구팀이 실험실의 인체 조직에서 [78]폴리오바이러스를 배양하는 데 성공하면서 돌파구가 열렸다.이 그룹은 최근 세포 배양에서 유행성 이하선염을 성공적으로 키웠다.1948년 3월, 토마스 H. 웰러는 배아 폐조직에서 수두 바이러스를 배양하려고 시도하고 있었다.그는 사용하지 않는 튜브가 몇 개 있다는 것을 알았을 때 계획된 수의 튜브를 접종했다.폴리오바이러스에 감염된 쥐의 뇌 샘플을 채취해 남은 시험관에 넣었다.수두 배양은 성장하지 못했지만 소아마비 배양은 성공적이었다.이 개발은 백신 연구를 크게 촉진시켰고 궁극적으로 소아마비에 대한 백신 개발을 가능하게 했다.엔더스와 그의 동료인 토마스 H. 웰러와 프레드릭 C. 로빈스는 1954년 노벨 [79]생리의학상을 받은 공로를 인정받았다.소아마비 백신 개발로 이끈 다른 중요한 발전들은 세 가지 폴리오바이러스 혈청형(폴리오바이러스 유형 1 – PV1, 또는 마호니; PV2, 랜싱; PV3, 레온)의 식별, 마비 전에 바이러스가 혈액에 존재해야 한다는 발견, 그리고 감마 형태로 항체를 투여한다는 입증이었다.로불린은 마비성 [63][52][80]소아마비로부터 보호해준다.
1950–1955
1950년대 초, 미국의 소아마비 발병률은 연간 25,000건 이상이었다; 1952년과 1953년에 미국은 각각 58,000건과 35,000건의 소아마비 발병률을 경험했는데, 이는 일반적인 연간 약 20,000건에서 증가된 수치이며, 그 해에 3,200건과 1,400건의 [81]사망자가 발생했다.이 미국 소아마비 전염병 속에서 수백만 달러가 H. R. 콕스의 지시로 뉴욕의 레더리 연구소를 포함한 상업적 관심사에 의해 소아마비 백신을 발견하고 판매하는데 투자되었다.또한 1950년 [9][46]폴란드 태생의 바이러스학자이자 면역학자인 필라델피아 위스타 연구소의 힐러리 코프로스키가 처음으로 소아마비 백신을 성공적으로 테스트했다.그러나 그의 백신은 경구 투여된 살아있는 약독화 바이러스여서 조나스 솔크의 소아마비 백신(죽은 바이러스 주사 백신)이 시장에 출시된 지 5년이 지나야 사용할 수 있게 됐다.코프로스키의 약화된 백신은 스위스 알비노 생쥐의 뇌를 연속적으로 통과시켜 조제되었다.7번째 통로로, 백신 변종은 더 이상 신경 조직을 감염시키거나 마비를 일으키지 않았다.쥐에게 1-3회 더 투여한 후, 그 백신은 사람이 [44][82]사용하기에 안전한 것으로 간주되었다.1950년 2월 27일 뉴욕에 위치한 신체적, 정신적 장애인을 위한 기관인 레치워스 빌리지에 사는 8세 소년에게 코프로스키의 살아있는 약독 백신이 처음으로 시험되었다.아이가 부작용이 없자 코프로우스키는 실험을 확대해 19명의 [44][83]다른 아이들을 포함시켰다.
조나스 솔크
최초의 효과적인 소아마비 백신은 1952년 Jonas Salk와 피츠버그 대학의 Julius Youngner, Byron Bennett, L. James Lewis, 그리고 Lorraine Friedman을 포함한 팀에 의해 개발되었으며, 몇 년간의 후속 테스트가 필요했다.1953년 3월 26일, 소크는 CBS 라디오에서 성인과 어린이의 소규모 그룹에 대한 성공적인 테스트를 보고했다. 이틀 후, 결과는 [71]JAMA에 발표되었다.Lion N. Farrell은 토론토에서 그녀가 [84][85]이끄는 팀에 의해 백신을 대량 생산할 수 있는 중요한 실험실 기술을 발명했다.1954년 2월 23일부터 백신은 아스널 초등학교와 펜실베니아 [86]피츠버그의 왓슨 어린이집에서 테스트되었다.
소크의 백신은 그 당시 역사상 가장 큰 의학 실험이었던 토마스 프란시스가 주도한 프란시스 필드 트라이얼이라고 불리는 실험에 사용되었다.이 테스트는 버지니아 [87][88]맥클린에 있는 프랭클린 셔먼 초등학교의 약 4,000명의 어린이들로 시작되었고, 결국 메인주에서 [89]캘리포니아에 이르는 44개 주에서 180만 명의 어린이들이 참여하였다.연구의 결론으로, 약 44만 명이 백신을 1회 이상 주사 받았고, 약 21만 명의 어린이들이 무해한 배지로 구성된 위약을 받았고, 120만 명의 어린이들이 예방접종을 받지 않고 대조군으로 활동했으며,[44] 그 후 소아마비에 걸렸는지 관찰할 수 있었다.
현장 재판 결과는 1955년 4월 12일(프랭클린 D 대통령 서거 10주년)에 발표되었다. 루즈벨트는 마비성 질환이 소아마비에 의한 것으로 일반적으로 생각되었다.소크 백신은 PV1(폴리오바이러스 유형 1)에 대해 60~70%, PV2와 PV3에 대해 90%, 구근성 [90]소아마비 발생에 대해 94%의 효과가 있었다.소크의 백신이 1955년에 허가된 직후, 어린이 백신 접종 캠페인이 시작되었다.미국에서는, March of Dimes에 의해 추진된 집단 예방 접종 캠페인에 따라, 연간 소아마비 환자 수가 1953년 35,[91]000명에서 1957년 5,600명으로 감소했다.1961년까지 미국에서는 [92]161건만이 기록되었다.
1955년 4월 Francis Field Trial 결과가 발표되기 일주일 전 파리 파스퇴르 연구소의 Pierre Lépine도 효과적인 소아마비 [93][94]백신을 발표했다.
안전 사고
1955년 4월, 미국에서 집단 소아마비 예방접종이 시작된 직후, 의무총장은 커터 제약회사로부터 소크 소아마비 백신 접종을 받은 후 약 1주일 후에 마비성 소아마비에 걸린 환자에 대한 보고를 받기 시작했다.커터 백신은 미국 [95]서부와 중서부의 20만 명의 어린이에게 백신을 접종하는 데 사용되었다.이후 조사 결과 커터 백신이 4만 건의 소아마비를 유발해 [95]10명이 사망한 것으로 나타났다.이에 대해 의무총장은 커터 연구소가 만든 모든 소아마비 백신을 시장에서 철수시켰지만 250건의 마비성 질환이 발생하기 전에는 그렇지 않았다.와이스 소아마비 백신은 또한 여러 명의 아이들을 마비시키고 사망케 한 것으로 보고되었다.곧 커터와 와이스가 만든 많은 수의 소크 소아마비 백신이 제대로 활성화되지 않아 살아있는 폴리오바이러스가 백신을 10만 회 이상 투여할 수 있다는 것이 밝혀졌다.1955년 5월, 국립 보건 및 공중 보건 서비스 연구소는 모든 소아마비 백신 로트를 테스트 및 검토하고 공중 보건 서비스에 어떤 로트를 공개해야 하는지 조언하기 위해 폴리 근염 백신 기술 위원회를 설립했습니다.이러한 사건들은 소아마비 백신에 대한 대중의 신뢰를 떨어뜨렸고, 백신 [96]접종률의 하락으로 이어졌다.
1961
Salk가 백신을 테스트하는 동시에 Albert Sabin과 Hilary Koprowski 둘 다 살아있는 바이러스를 이용한 백신을 개발하는 작업을 계속했다.1955년 11월 스톡홀름에서 소아마비 백신을 논의하기 위한 회의에서 사빈은 80명의 지원자를 대상으로 얻은 결과를 발표했고, 코프로우스키는 150명을 [44]대상으로 한 실험 결과를 상세히 기록한 논문을 읽었다.사빈과 코프로스키 모두 결국 백신 개발에 성공했다.미국에서 Salk 백신에 대한 헌신 때문에 Sabin과 Koprowski는 둘 다 미국 밖에서, Sabin은[54] [97]멕시코와 소련, Koprowski는 [46]콩고와 폴란드에서 실험을 했다.1957년, Sabin은 세 종류의 폴리오바이러스의 [97]모든 감쇠된 변종을 포함하는 3가 백신을 개발했다.1959년, 소련의 천만 명의 어린이들이 사빈 경구 백신을 맞았습니다.이 공로로 사빈은 소련에서 가장 높은 민간 [98]명예로 묘사되는 국민우호훈장을 받았다.살아있는 바이러스를 이용한 사빈의 경구 백신은 [2]1961년에 상용화 되었다.
사빈의 경구백신이 널리 보급되자 1955년 한 회사가 부적절하게 준비한 소크백신이 여러 명의 어린이를 사망시키거나 [71]마비시키는 사건이 일어나면서 여론에 퇴색된 소크백신을 대체했다.
1987
1987년 11월 미국에서 강화된 효능의 IPV가 허가되었고,[19] 현재 미국에서 선택된 백신이다.소아마비 백신의 첫 번째 접종은 생후 1개월에서 2개월 사이에, 두 번째 접종은 [19]생후 4개월에 투여된다.세 번째 투여 시기는 백신 제제에 따라 다르지만,[53] 생후 6개월에서 18개월 사이에 투여해야 한다.4세부터 6세까지의 나이에 부스터 [20]예방접종을 실시하여 입학 전 또는 입학 전 총 4회 접종을 실시합니다.일부 국가에서는 [53]청소년기에 다섯 번째 예방접종을 한다.선진국에서 성인(18세 이상)의 정기적인 예방접종은 필요하지도 않고 권장하지도 않는다. 왜냐하면 대부분의 성인들은 이미 면역이 되어 있고 그들의 [19]모국에서 야생 폴리오바이러스에 노출될 위험이 매우 작기 때문이다.2002년,[101][100] IPV를 포함한 5가 결합 백신(Pediarix라 [99][100]불린다)이 미국에서 사용이 승인되었다.
1988
세계보건기구(WHO)와 [102]유니세프, 로터리재단이 주도하는 소아마비 근절을 위한 세계적 노력은 1988년 시작돼 알버트 사빈과 미하일 추마코프(사빈 추마코프 백신)[103]가 개발한 경구 소아마비 백신에 크게 의존해 왔다.
1990년 이후
소아마비는 [104]1994년까지 아메리카에서 제거되었다.이 병은 [105][106]2000년 중국과 호주를 포함한 36개 서태평양 국가에서 공식적으로 제거되었다.유럽은 2002년에 [107]소아마비가 없는 것으로 선언되었다.2011년 1월 이후 인도에서는 발병 사례가 보고되지 않았기 때문에 2012년 2월 소아마비 종말국가 목록에서 제외되었다.2014년 3월 인도는 소아마비가 없는 나라로 [108][109][110]선언되었다.
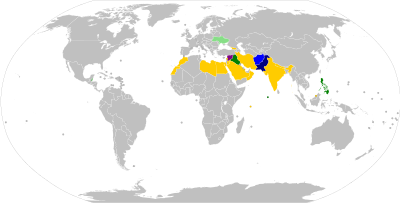
폴리오바이러스 전염은 세계 대부분에서 중단되었지만, 야생 폴리오바이러스의 전염은 계속되며 이전에 소아마비가 없었던 지역으로 야생 폴리오바이러스의 수입에 대한 지속적인 위험을 야기한다.폴리오바이러스의 수입이 발생하면, 특히 예방접종 범위가 낮고 위생상태가 좋지 않은 지역에서 소아마비염이 발병할 수 있다.그 결과, 높은 수준의 예방접종이 [104]유지되어야 한다.2013년 11월, WHO는 시리아에서 소아마비가 발생했다고 발표했습니다.이에 대해 아르메니아 정부는 15세 미만의 시리아 아르메니아인들에게 소아마비 [111]백신을 접종할 것을 요청하는 공문을 냈다.2014년 현재 소아마비 바이러스는 주로 아프리카, 아시아, 중동 등 10개국으로 확산됐으며 파키스탄, 시리아, 카메룬은 해외여행자에게 [112]예방접종을 권고하고 있다.
소아마비 백신 접종 프로그램은 파키스탄, 아프가니스탄, 나이지리아에서 일부 사람들에 의해 거부되어 왔다. 이 세 나라는 2017년 현재 소아마비 환자가 남아 있다.거의 모든 무슬림 종교 및 정치 지도자들은 [113]백신을 지지했지만, 한 소수파는 백신이 [51]무슬림의 살균을 위해 비밀리에 사용되고 있다고 믿고 있다.CIA가 오사마 빈 라덴을 찾기 위해 2011년 가짜 백신 접종 프로그램을 마련한 것도 [114]불신의 한 원인이다.2015년, WHO는 탈레반이 통제하고 [115]있는 지역에 백신을 배포하도록 장려하기 위한 협상을 발표했다.그러나 파키스탄 탈레반은 지지하지 않았다.2016년 9월 11일 파키스탄 탈레반과 연관된 신원 미상의 무장괴한 2명, 자마트울아흐라가 파키스탄에서 소아마비 백신을 투여하던 의사 자칼라 칸을 총으로 쐈다.자마트-울-아흐라르의 지도자는 총격의 책임이 있다고 주장했고 이 단체는 이런 유형의 공격을 계속할 것이라고 말했다.백신 접종에 대한 그러한 저항과 회의주의는 결과적으로 나머지 두 [114]풍토 국가 내에서 소아마비 근절 과정을 늦췄다.
출장 요건
특정 국가에 입국하거나 출국하려는 여행객은 일반적으로 국경을 통과하기 최소 12개월에서 최소 4주 전에 소아마비 예방접종을 받아야 하며 국경 검색에서 [116]: 25–27 예방접종 기록/증명서를 제시할 수 있어야 한다.대부분의 요건은 이른바 '폴리오 엔데믹', '폴리오 영향', '폴리오 수출', '폴리오 전염' 또는 '고위험'[117] 국가를 오가는 여행에만 적용된다.2020년 8월 현재, 아프가니스탄과 파키스탄은 세계에서 유일하게 소아마비가 [118]근절되지 않은 국가이다.일부 국가는 '핵심 위험 국가'를 오가는 등 추가적인 예방적 소아마비 예방 접종 여행 요건을 가지고 있으며, 2020년 12월 현재 중국, 인도네시아, 모잠비크, 미얀마 및 파푸아 [117][119]뉴기니를 포함하고 있다.
| 해외여행을[117] 위한 소아마비 예방접종 요건 | |
|---|---|
| 나라 | 세부 사항 |
| 소아마비 종말기 국가(파키스탄) 여행자는 도착 시 소아마비 예방접종(출발 4~12개월 전 접종)의 Carte Jaune 증명이 필요합니다.거주자와 4주 이상 아프가니스탄에 체류하는 모든 여행객은 아프가니스탄을 [117][120]출발할 때 소아마비 예방접종(출발 4주에서 12개월 사이 접종)의 증명이 필요합니다. | |
| 아프가니스탄과 파키스탄에서 온 여행객은 도착 시 OPV 또는 IPV 백신 접종(출발 4주에서 12개월 사이)의 Carte Jaune 증명이 필요합니다.소아마비 환자가 확인된 국가를 여행하는 벨리즈 주민들도 예방접종 [121]증명이 필요하다. | |
| 소아마비 수출국에서 온 여행객은 [122]도착 시 OPV 또는 IPV 백신(출발 4주에서 12개월 사이 접종)의 Carte Jaune 증명이 필요합니다. | |
| 아프가니스탄, 앙골라, 베냉, 카메룬, 중앙아프리카공화국, 중국, 콩고-킨샤사, 에티오피아, 가나, 인도네시아, 케냐, 모잠비크, 미얀마, 니제르, 나이지리아, 파키스탄, 파푸아뉴기니, 필리핀, 소말리아에서 온 여행객은 OPV 또는 IPV 접종 증명서(Carte Jaune)가 필요하다.l.[123] | |
| 위험 국가의 여행자는 도착 시 OPV 또는 IPV 백신(출발 4주에서 12개월 사이 접종)의 Carte Jaune 증명이 필요하다.증거가 없는 여행자는 도착 [124]시 OPV 예방 접종을 받을 수 있습니다. | |
| 아프가니스탄, 콩고-킨샤사, 에티오피아, 케냐, 나이지리아, 파키스탄, 소말리아 및 시리아에서 온 여행객은 도착 [125]시 OPV 또는 IPV 백신(출발 4~12개월 전 접종)의 Carte Jaune 증명이 필요합니다. | |
| 아프가니스탄, 파키스탄 및 나이지리아 여행자는 도착 후 OPV 또는 IPV 백신 접종(출발 4~12개월 전)에 대한 Carte Jaune 증명이 필요합니다.증거가 없는 여행자는 [126]도착 즉시 예방 접종을 받을 수 있습니다. | |
| 아프가니스탄과 파키스탄에서 온 15세 이상 여행자는 도착 후 OPV 또는 IPV 백신(출국 4주에서 12개월 사이)의 Carte Jaune 증명이 필요하다. 15세 미만 어린이는 여행 전에 소아마비 백신을 3회 접종받아야 한다.증거가 없는 여행자는 도착 즉시 예방 접종을 받을 수 있습니다.이라크를 떠나 아프가니스탄과 파키스탄으로 가는 여행자들은 또한 [127]출발할 때 예방접종 증명서를 제출해야 한다. | |
| 아프가니스탄과 파키스탄에서 온 여행객은 도착 [128]시 OPV 또는 IPV 백신 접종(출발 4주에서 12개월 사이)의 Carte Jaune 증명이 필요합니다. | |
| 소아마비 감염 국가를 오가는 여행자는 도착 [129]후 OPV 또는 IPV 백신(출발 4~12개월 전 접종)의 Carte Jaune 증명이 필요하다. | |
| 아프가니스탄과 파키스탄에서 온 여행객은 도착 [130]시 OPV 또는 IPV 백신 접종(출발 4주에서 12개월 사이)의 Carte Jaune 증명이 필요합니다. | |
| 소아마비 수출국 및 Hajj와 Umrah 순례자들은 도착 [131]후 OPV 또는 IPV 백신(출발 4주에서 12개월 사이 접종)의 Carte Jaune 증명이 필요합니다. | |
| 소아마비 감염 국가의 여행자는 도착 [132]시 OPV 또는 IPV 백신(출발 4주에서 12개월 사이 접종)의 Carte Jaune 증명이 필요하다. | |
| 아프가니스탄, 케냐, 나이지리아, 파키스탄 및 파푸아 뉴기니에서 온 여행객은 도착 [133]시 OPV 또는 IPV 백신(출발 4~12개월 전 접종)의 Carte Jaune 증명이 필요합니다. | |
| 소아마비 수출국에서 온 여행객은 [134]도착 시 OPV 또는 IPV 백신(출발 4주에서 12개월 사이 접종)의 Carte Jaune 증명이 필요합니다. | |
| 파키스탄에 4주 이상 체류하려는 모든 국가의 여행객은 도착 시 OPV 예방 접종의 Carte Jaune 증명이 필요합니다.거주자와 파키스탄에 4주 이상 체류하는 모든 여행객은 파키스탄에서 [117][135]출발할 때 OPV 예방 접종 증명이 필요합니다. | |
| 고위험 국가에서 또는 고위험 국가로 이동하는 여행자는 각각 [117]도착 시 또는 출발 전에 소아마비 예방접종의 Carte Jaune 증명이 필요하다.계속되는 현지 VDPV2 감염으로 인해, 정부는 다른 모든 여행자들에게 상황에 [136]따라 소아마비 백신이나 추가 복용을 고려할 것을 권고하고 있다. | |
| 소아마비 수출국(카타르에 의해 아프가니스탄, 나이지리아, 파키스탄 및 필리핀으로 식별됨)의 여행자는 [137]도착 시 OPV 또는 IPV 백신(출발 4주에서 12개월 사이 접종)의 Carte Jaune 증명이 필요하다. | |
| WHO(아프가니스탄과 파키스탄)가 식별한 소아마비 빈혈 국가의 여행자는 도착 [117][138]후 OPV 또는 IPV 백신(출발 4주에서 12개월 사이 접종)의 Carte Jaune 증명이 필요하다. | |
| 활성 전염(야생 또는 백신에서 파생된 폴리오바이러스 포함) 및 위험 국가 및 아프가니스탄, 콩고-킨샤사, 모잠비크, 미얀마, 니제르, 나이지리아, 파키스탄, 파푸아 뉴기니, 소말리아, 시리아, 예멘에서 온 모든 여행자는 OPV 또는 IPV 접종(접종)의 증명 Carte Jaune가 필요하다.도착 즉시 출발)예방접종 상태에 관계없이 아프가니스탄, 미얀마, 나이지리아, 파키스탄, 파푸아 뉴기니, 소말리아, 시리아, 예멘에서 온 모든 여행객은 [139]도착 시 경구 소아마비 백신 접종을 받게 됩니다. | |
| 소아마비 발병 국가의 여행자는 도착 [140]시 OPV 또는 IPV 백신(출발 4주에서 12개월 사이 접종)의 Carte Jaune 증명이 필요합니다. | |
| 카메룬, 적도 기니, 파키스탄에서 온 여행객은 도착 후 OPV 또는 IPV 백신 접종(출발 4주에서 12개월 사이)의 Carte Jaune 증명이 필요합니다.시리아를 출국하는 모든 시리아 주민들도 예방접종 [141]증명이 필요하다. | |
| 야생 또는 순환 백신에서 유래한 폴리오바이러스가 전염된 주를 떠나는 장기 방문자는 적어도 1회 용량 이상의 2가 OPV 또는 IPV(출발 4주에서 12개월 사이에 접종)와 함께 Carte Jaune 예방접종 증거를 제시해야 한다.긴급한 국제 여행을 해야 하는 사람들은 [117]출발 전에 소아마비 백신을 1회 접종해야 한다.우크라이나 자체에서도 폴리오바이러스가 전염될 위험이 있으며, 우크라이나 여행자는 [142]입국 전에 소아마비 예방접종을 최신 상태로 받을 것을 권장합니다. | |
사회와 문화
비용.
세계백신 및 면역 동맹은 [143]2015년에 10회 복용 약병에서 용량당 불과 0.75유로(약 0.86달러)에 불활성화 백신을 개발도상국에 공급한다.
오해
파키스탄에서는 소아마비 백신에 하람 성분이 들어 있어 남성 아동의 발기부전과 불임을 유발할 수 있다는 오해가 제기돼 일부 부모들이 백신을 접종하지 않고 있다.이 믿음은 카이버 파크툰크화 지방과 FATA 지역에서 가장 흔하다.소아마비 예방접종팀에 대한 공격도 발생해 파키스탄과 [144][145]전 세계적으로 소아마비를 근절하려는 국제적인 노력이 저해되고 있다.
대중문화
1964년 팝송 "A Spoonful of Sugar (약물을 내려갈 수 있게 도와준다)"는 각설탕에 투여된 경구용 백신을 말합니다.
레퍼런스
- ^ 임신 및 모유 수유 중 사용
- ^ a b c d e f g h i j k l World Health Organization (March 2016). "Polio vaccines: WHO position paper". Weekly Epidemiological Record. 91 (12): 145–68. hdl:10665/254399. PMID 27039410. Archived from the original on 10 April 2016.
- ^ Aylward RB (2006). "Eradicating polio: today's challenges and tomorrow's legacy". Annals of Tropical Medicine and Parasitology. 100 (5–6): 401–413. doi:10.1179/136485906X97354. PMID 16899145. S2CID 25327986.
- ^ Schonberger LB, Kaplan J, Kim-Farley R, Moore M, Eddins DL, Hatch M (1984). "Control of paralytic poliomyelitis in the United States". Reviews of Infectious Diseases. 6 Suppl 2: S424–S426. doi:10.1093/clinids/6.Supplement_2.S424. PMID 6740085.
- ^ "Global Wild Poliovirus 2014–2019" (PDF). Retrieved 3 February 2019.
- ^ "Does polio still exist? Is it curable?". World Health Organization (WHO). Retrieved 21 May 2018.
- ^ "Poliomyelitis". World Health Organization (WHO). Archived from the original on 18 April 2017. Retrieved 25 April 2017.
- ^ a b "GPEI-nOPV2". Retrieved 1 August 2021.
- ^ a b c Fox M (20 April 2013). "Hilary Koprowski, Who Developed First Live-Virus Polio Vaccine, Dies at 96". The New York Times.
- ^ Bazin H (2011). Vaccination: A History. John Libbey Eurotext. p. 395. ISBN 978-2742007752. Archived from the original on 8 September 2017.
- ^ Smith DR, Leggat PA (2005). "Pioneering figures in medicine: Albert Bruce Sabin – inventor of the oral polio vaccine". The Kurume Medical Journal. 52 (3): 111–116. doi:10.2739/kurumemedj.52.111. PMID 16422178.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ a b Fine PE, Carneiro IA (November 1999). "Transmissibility and persistence of oral polio vaccine viruses: implications for the global poliomyelitis eradication initiative". American Journal of Epidemiology. 150 (10): 1001–1021. doi:10.1093/oxfordjournals.aje.a009924. PMID 10568615.
- ^ Koike S, Taya C, Kurata T, Abe S, Ise I, Yonekawa H, Nomoto A (February 1991). "Transgenic mice susceptible to poliovirus". Proc. Natl. Acad. Sci. U.S.A. 88 (3): 951–955. Bibcode:1991PNAS...88..951K. doi:10.1073/pnas.88.3.951. PMC 50932. PMID 1846972.
- ^ a b Robertson S. Module 6: Poliomyelitis (PDF). The Immunological Basis for Immunization Series. World Health Organization (WHO). WHO/EPI/GEN/93.16. Archived from the original (PDF) on 19 October 2019. Retrieved 18 October 2019.
- ^ Canada, Public Health Agency of (18 July 2007). "Poliomyelitis vaccine: Canadian Immunization Guide". www.canada.ca. Retrieved 1 August 2021.
- ^ "Polio Vaccination: What Everyone Should Know CDC". www.cdc.gov. 25 March 2021. Retrieved 1 August 2021.
- ^ Wahid R, Cannon MJ, Chow M (May 2005). "Virus-Specific CD4+ and CD8+ Cytotoxic T-Cell Responses and Long-Term T-Cell Memory in Individuals Vaccinated against Polio". Journal of Virology. 79 (10): 5988–5995. doi:10.1128/JVI.79.10.5988-5995.2005. PMC 1091702. PMID 15857985.
- ^ a b c d e f Atkinson W, Hamborsky J, McIntyre L, Wolfe S, eds. (2008). Epidemiology and Prevention of Vaccine-Preventable Diseases (The Pink Book) (PDF) (10th ed. (2nd printing) ed.). Washington, D.C.: Public Health Foundation. Archived from the original (PDF) on 24 September 2008. Retrieved 29 November 2008.
- ^ a b "Poliomyelitis prevention: recommendations for use of inactivated poliovirus vaccine and live oral poliovirus vaccine. American Academy of Pediatrics Committee on Infectious Diseases". Pediatrics. 99 (2): 300–305. February 1997. doi:10.1542/peds.99.2.300. PMID 9024465.
- ^ a b Marin M, Patel M, Oberste S, Pallansch MA (January 2017). "Guidance for Assessment of Poliovirus Vaccination Status and Vaccination of Children Who Have Received Poliovirus Vaccine Outside the United States". MMWR. Morbidity and Mortality Weekly Report. 66 (1): 23–25. doi:10.15585/mmwr.mm6601a6. PMC 5687270. PMID 28081056.
- ^ Al Idrus A (13 April 2016). "Worldwide switch to bivalent oral polio vaccine to kick off on Sunday". fiercepharma.com. Archived from the original on 15 April 2016. Retrieved 1 May 2016.
- ^ Ramirez Gonzalez A, Farrell M, Menning L, Garon J, Everts H, Hampton LM, Dolan SB, Shendale S, Wanyoike S, Veira CL, Châtellier GM, Kurji F, Rubin J, Boualam L, Chang Blanc D, Patel M (July 2017). "Implementing the Synchronized Global Switch from Trivalent to Bivalent Oral Polio Vaccines-Lessons Learned From the Global Perspective". The Journal of Infectious Diseases. 216 (suppl 1): S183–S192. doi:10.1093/infdis/jiw626. PMC 5854099. PMID 28838179.
- ^ "GPEI Strategy for the Response to cVDPV2 2020-2021" (PDF). Polio Global Eradication Initiative. Retrieved 1 August 2021.
- ^ "Share of one-year-olds vaccinated against polio (Pol3)". Our World in Data. Retrieved 4 March 2020.
- ^ "Common and Rare Side Effects for poliovirus vaccine injection". www.webmd.com. Retrieved 24 August 2021.
- ^ Shimizu H, Thorley B, Paladin FJ, Brussen KA, Stambos V, Yuen L, Utama A, Tano Y, Arita M, Yoshida H, Yoneyama T, Benegas A, Roesel S, Pallansch M, Kew O, Miyamura T (December 2004). "Circulation of type 1 vaccine-derived poliovirus in the Philippines in 2001". Journal of Virology. 78 (24): 13512–13521. doi:10.1128/JVI.78.24.13512-13521.2004. PMC 533948. PMID 15564462.
- ^ "What is vaccine-derived polio?". World Health Organization (WHO). World Health Organization (WHO). April 2017.
- ^ Cono J, Alexander LN (2002). "Chapter 10: Poliomyelitis" (PDF). Vaccine-Preventable Disease Surveillance Manual (3rd ed.). Archived from the original (PDF) on 22 October 2011.
- ^ "What is vaccine-derived polio?". World Health Organization (WHO). October 2014. Archived from the original on 7 September 2015. Retrieved 6 September 2015.
- ^ Kew O, Morris-Glasgow V, Landaverde M, Burns C, Shaw J, Garib Z, et al. (April 2002). "Outbreak of poliomyelitis in Hispaniola associated with circulating type 1 vaccine-derived poliovirus". Science. 296 (5566): 356–359. Bibcode:2002Sci...296..356K. doi:10.1126/science.1068284. PMID 11896235. S2CID 38725709.
- ^ Yang CF, Naguib T, Yang SJ, Nasr E, Jorba J, Ahmed N, Campagnoli R, van der Avoort H, Shimizu H, Yoneyama T, Miyamura T, Pallansch M, Kew O (August 2003). "Circulation of endemic type 2 vaccine-derived poliovirus in Egypt from 1983 to 1993". Journal of Virology. 77 (15): 8366–8377. doi:10.1128/JVI.77.15.8366-8377.2003. PMC 165252. PMID 12857906.
- ^ Kunasekaran M. "Eradication of polio – Is Syria being left behind?". UNSW School of Public Health and Community Medicine. Retrieved 6 October 2018.
- ^ "Replacing trivalent OPV with bivalent OPV". World Health Organization (WHO). Archived from the original on 11 March 2015. Retrieved 30 May 2019.
- ^ "Poliomyelitis". World Health Organization (WHO). 22 July 2019. Retrieved 18 October 2019.
- ^ a b c d "Simian Virus 40 (SV40), Polio Vaccine, and Cancer". Vaccine Safety. Centers for Disease Control. 22 April 2004. Archived from the original on 22 May 2013. Retrieved 22 May 2013.
- ^ Eddy BE, Borman GS, Berkeley WH, Young RD (May 1961). "Tumors induced in hamsters by injection of rhesus monkey kidney cell extracts". Proceedings of the Society for Experimental Biology and Medicine. 107: 191–197. doi:10.3181/00379727-107-26576. PMID 13725644. S2CID 31275908.
- ^ Carbone M (December 1999). "Simian virus 40 and human tumors: It is time to study mechanisms". Journal of Cellular Biochemistry. 76 (2): 189–193. doi:10.1002/(SICI)1097-4644(20000201)76:2<189::AID-JCB3>3.0.CO;2-J. PMID 10618636. S2CID 795975.
- ^ Vilchez RA, Kozinetz CA, Arrington AS, Madden CR, Butel JS (June 2003). "Simian virus 40 in human cancers". The American Journal of Medicine. 114 (8): 675–684. doi:10.1016/S0002-9343(03)00087-1. PMID 12798456.
- ^ a b Engels EA (April 2005). "Cancer risk associated with receipt of vaccines contaminated with simian virus 40: epidemiologic research". Expert Review of Vaccines. 4 (2): 197–206. doi:10.1586/14760584.4.2.197. PMID 15889993. S2CID 5861910.
- ^ Bookchin D (7 July 2004). "Vaccine scandal revives cancer fear". New Scientist. Archived from the original on 20 July 2004. Retrieved 29 November 2008.
- ^ Strickler HD, Rosenberg PS, Devesa SS, Hertel J, Fraumeni JF, Goedert JJ (January 1998). "Contamination of poliovirus vaccines with simian virus 40 (1955–1963) and subsequent cancer rates". JAMA. 279 (4): 292–295. doi:10.1001/jama.279.4.292. PMID 9450713.
- ^ Olin P, Giesecke J (1998). "Potential exposure to SV40 in polio vaccines used in Sweden during 1957: no impact on cancer incidence rates 1960 to 1993". Developments in Biological Standardization. 94: 227–233. PMID 9776244.
- ^ a b c d e f "Competition to develop an oral vaccine". Conquering Polio. Sanofi Pasteur SA. 2 February 2007. Archived from the original on 7 October 2007.
- ^ a b Plotkin SA (April 2001). "CHAT oral polio vaccine was not the source of human immunodeficiency virus type 1 group M for humans". Clinical Infectious Diseases. 32 (7): 1068–1084. doi:10.1086/319612. PMID 11264036.
- ^ a b c Koprowski H (July 1960). "Historical aspects of the development of live virus vaccine in poliomyelitis". British Medical Journal. 2 (5192): 85–91. doi:10.1136/bmj.2.5192.85. PMC 2096806. PMID 14410975.
- ^ Collins, Huntly (6 November 2000). "The Gulp Heard Round the World". The Philadelphia Inquirer. p. D-1. Archived from the original on 5 April 2004. Retrieved 29 November 2008.
- ^ "Nigeria Muslims oppose polio vaccination". BBC News Online. 27 June 2002. Archived from the original on 29 November 2008. Retrieved 29 November 2008.
- ^ Dugger CW, McNeil DG (20 March 2006). "Rumor, Fear and Fatigue Hinder Final Push to End Polio". The New York Times. Archived from the original on 10 December 2008. Retrieved 29 November 2008.
- ^ "Anti-polio vaccine Malians jailed". BBC News Online. 12 May 2005. Archived from the original on 10 January 2006. Retrieved 29 November 2008.
- ^ a b Jegede AS (March 2007). "What led to the Nigerian boycott of the polio vaccination campaign?". PLOS Medicine. 4 (3): e73. doi:10.1371/journal.pmed.0040073. PMC 1831725. PMID 17388657.
- ^ a b c Kew OM, Sutter RW, de Gourville EM, Dowdle WR, Pallansch MA (2005). "Vaccine-derived polioviruses and the endgame strategy for global polio eradication". Annual Review of Microbiology. 59: 587–635. doi:10.1146/annurev.micro.58.030603.123625. PMID 16153180.
- ^ a b c Joint Committee on Vaccination and Immunisation (2006). "26: Poliomyelitis" (PDF). In Salisbury D, Ramsay M, Noakes K (eds.). Immunisation Against Infectious Disease. Edinburgh: Stationery Office. pp. 313–329. ISBN 978-0-11-322528-6. Archived from the original (PDF) on 15 June 2007.
- ^ a b Sabin AB, Ramos-Alvarez M, Alvarez-Amezquita J, Pelon W, Michaels RH, Spigland I, Koch MA, Barnes JM, Rhim JS (August 1960). "Live, orally given poliovirus vaccine. Effects of rapid mass immunization on population under conditions of massive enteric infection with other viruses". JAMA. 173 (14): 1521–1526. doi:10.1001/jama.1960.03020320001001. PMID 14440553.
- ^ Sabin AB (1987). "Role of my cooperation with Soviet scientists in the elimination of polio: possible lessons for relations between the U.S.A. and the USSR". Perspectives in Biology and Medicine. 31 (1): 57–64. doi:10.1353/pbm.1987.0023. PMID 3696960. S2CID 45655185.
- ^ Benison S (1982). "International medical cooperation: Dr. Albert Sabin, live poliovirus vaccine and the Soviets". Bulletin of the History of Medicine. 56 (4): 460–483. PMID 6760938.
- ^ Ochs K, Zeller A, Saleh L, Bassili G, Song Y, Sonntag A, Niepmann M (January 2003). "Impaired binding of standard initiation factors mediates poliovirus translation attenuation". Journal of Virology. 77 (1): 115–122. doi:10.1128/JVI.77.1.115-122.2003. PMC 140626. PMID 12477816.
- ^ Gromeier M, Bossert B, Arita M, Nomoto A, Wimmer E (February 1999). "Dual stem loops within the poliovirus internal ribosomal entry site control neurovirulence". Journal of Virology. 73 (2): 958–964. doi:10.1128/JVI.73.2.958-964.1999. PMC 103915. PMID 9882296.
- ^ Pearce JM (November 2004). "Salk and Sabin: poliomyelitis immunisation". Journal of Neurology, Neurosurgery, and Psychiatry. 75 (11): 1552. doi:10.1136/jnnp.2003.028530. PMC 1738787. PMID 15489385.
- ^ Smallman-Raynor M (2006). Poliomyelitis: A World Geography: Emergence to Eradication. Oxford University Press (US). ISBN 978-0-19-924474-4.[페이지 필요]
- ^ Poliomyelitis Eradication: Field Guide. Washington: Pan American Health Organization. 2006. ISBN 978-92-75-11607-4.[페이지 필요]
- ^ a b Löwy, Ilana (1 April 2006). "Book Review". Medical History. 50 (2): 253–254. doi:10.1017/S0025727300009790. ISSN 0025-7273. PMC 1472109.
- ^ a b c d e f g h i j k l Rivers, T. (1967). Tom Rivers: reflections on a life in medicine and science : an oral history memoir. MIT Press. hdl:2027/heb.05734. ISBN 978-0262020268.
- ^ a b c d e f Halpern, Sydney A. (2006). Lesser harms: The morality of risk in medical research. Chicago, Ill: University of Chicago Press. OCLC 877210630.
- ^ a b c d Hovern, Dayna (2018). The Trials and Triumphs of the American Polio Vaccine (Thesis). Cooper Medical School of Rowan University.
- ^ "Vaccine Testing and Vulnerable Human Subjects History of Vaccines". www.historyofvaccines.org. Retrieved 18 July 2021.
- ^ a b c d e Gould, Tony (1997). A Summer Plague: Polio and Its Survivors. New Haven: Yale University Press. ISBN 978-0300072761. OCLC 38243151.
- ^ Wilson, John Rowan (1963). Margin of Safety: The Story of Poliomyelitis Vaccine. Garden City, NY: Collins. OCLC 630735949.
- ^ 폴, J.R.(1971년).소아마비의 역사뉴헤이븐: 예일대학교 출판부.[ISBN missing][page needed]
- ^ a b c d e f g h i j k l m n o p q r Berk, Lawrence B. (1989). "Polio Vaccine Trials of 1935". Transactions & Studies of the College of Physicians of Philadelphia. 5. 11 (4): 321–336. PMID 2692236.
- ^ a b c d e f g Offit PA (2007). The Cutter Incident: How America's First Polio Vaccine Led to the Growing Vaccine Crisis. Yale University Press. p. 38. ISBN 978-0-300-12605-1.
- ^ a b Broadie, Maurice; Park, William (5 October 1935). "Active immunization against poliomyelitis". Journal of the American Medical Association. 105 (14): 1089–1093. doi:10.1001/jama.1935.02760400005002. S2CID 1640997.
- ^ Brodie, Maurice (1935). "Active immunization in monkeys against poliomyelitis with germicidally inactivated virus". The Journal of Immunology. 28 (1): 1–18.
- ^ a b c d e Johnston, Keith (22 February 2021). "The tragic story of a Canadian vaccine trailblazer". Macleans.ca. Retrieved 18 July 2021.
- ^ Oshinsky, David M. (2005). Polio: An American Story. Oxford University Press. p. 57. ISBN 978-0-19-515294-4.
- ^ a b c d Leake, James P. (February 1936). "Discussion of Poliomyelitis Papers Delivered at the Symposium on Poliomyelitis before the Fourth Annual Meeting of the Southern Branch, American Public Health Association in St. Louis, Mo., November 19, 1935". American Journal of Public Health. 26 (2): 143–48. doi:10.2105/AJPH.26.2.181. PMC 1562619. PMID 18014373.
- ^ "John A. Kolmer, M.D." Retrieved 28 November 2017.
- ^ Enders JF, Weller TH, Robbins FC (January 1949). "Cultivation of the Lansing Strain of Poliomyelitis Virus in Cultures of Various Human Embryonic Tissues". Science. 109 (2822): 85–87. Bibcode:1949Sci...109...85E. doi:10.1126/science.109.2822.85. PMID 17794160.
- ^ "The Nobel Prize in Physiology or Medicine 1954". The Nobel Foundation. Archived from the original on 19 December 2008. Retrieved 29 November 2008.
- ^ Hammon WM, Coriell LL, Wehrle PF, Stokes J (April 1953). "Evaluation of Red Cross gamma globulin as a prophylactic agent for poliomyelitis. IV. Final report of results based on clinical diagnoses". Journal of the American Medical Association. 151 (15): 1272–1285. PMID 13034471.
- ^ Ochmann S, Roser M (9 November 2017). "Polio – Polio Cases (OWID based on US Public Health Service (1910–1951) and US Center for Disease Control (1960–2010))". Our World in Data. Retrieved 26 March 2018.
- ^ "Public Health Weekly Reports for October 10, 1947". Public Health Reports. 62 (41): 1467–1498. October 1947. PMC 1995293. PMID 19316151.
- ^ Koprowski H (15 October 2010). "Interview with Hilary Koprowski, sourced at History of Vaccines website". College of Physicians of Philadelphia. Archived from the original on 15 May 2016. Retrieved 15 October 2010.
- ^ "science.ca : Leone N. Farrell". www.science.ca. Retrieved 1 August 2021.
- ^ Elliott, Carol K. (March 2011). "Leone Norwood Farrell, PhD". polioplace. Post-polio Health International. Retrieved 10 August 2019.
- ^ Shors T (2008). Understanding viruses. Jones & Bartlett Learning. pp. 294–. ISBN 978-0-7637-2932-5. Archived from the original on 21 July 2014. Retrieved 22 February 2011.
- ^ Conis E (2016). "Political Ills". Distillations. 2 (2): 34–37. Retrieved 27 March 2018.
- ^ Oshinsky D (Winter 2010). "Miracle Workers". American Heritage.
- ^ "Polio Victory Remembered as March of Dimes Marks 50th Anniversary of Salk Vaccine Field Trials". News Desk. 26 April 2004. Archived from the original on 27 September 2015. Retrieved 14 November 2014.
- ^ Smith JS (1990). Patenting the Sun: Polio and the Salk Vaccine. William Morrow & Co. ISBN 978-0-688-09494-2.
- ^ Sorem A, Sass EJ, Gottfried G (1996). Polio's legacy: an oral history. Washington, D.C: University Press of America. ISBN 978-0-7618-0144-3.
- ^ Hinman AR (June 1984). "Landmark perspective: Mass vaccination against polio". JAMA. 251 (22): 2994–2996. doi:10.1001/jama.1984.03340460072029. PMID 6371280.
- ^ 파스퇴르 연구소는 피에르 레핀 교수가 개발한 항골수염 백신이 곧 대량으로 생산될 것이라고 밝혔다.(타임스, 런던, 1955년 4월 4일).
- ^ Pasteur, Archives. "Pierre Lépine (1901–1989) – Notice biographique". webext.pasteur.fr. Archived from the original on 28 November 2016. Retrieved 28 November 2016.
- ^ a b 피츠패트릭, 마이클(2006년 3월)."리뷰:커터 사건: 미국 최초의 소아마비 백신이 어떻게 백신 위기를 초래했는가." JR Soc Med. 99(3) 페이지 156. MCID: PMC1383764.2020년 10월 31일 회수.
- ^ Juskewitch JE, Tapia CJ, Windebank AJ (August 2010). "Lessons from the Salk polio vaccine: methods for and risks of rapid translation". Clinical and Translational Science (Review). 3 (4): 182–185. doi:10.1111/j.1752-8062.2010.00205.x. PMC 2928990. PMID 20718820.
- ^ a b "Two Vaccines: Sabin and Salk". Smithsonian National Museum of American History. 27 September 2021.
- ^ "Sabin receives highest Soviet civilian honor". U.P.I. archives. 20 November 1986.
- ^ 디프테리아 및 파상풍 독성물질과 무세포성 백일해 흡착제, B형 간염(재생제) 및 불활성화 폴리오바이러스 백신 조합
- ^ a b "Pediarix". U.S. Food and Drug Administration (FDA). 6 November 2019. Retrieved 8 July 2020.
- ^ "FDA Statistical Review and Evaluation" (PDF). U.S. Food and Drug Administration (FDA).
- ^ Mansoor H (23 October 2015). "Can India's social mobilisation strategy work in Pakistan?". The Express Tribune. Archived from the original on 24 October 2015. Retrieved 24 October 2015.
- ^ Mastny L (25 January 1999). "Eradicating Polio: A Model for International Cooperation". Worldwatch Institute. Archived from the original on 3 December 2006. Retrieved 29 November 2008.
- ^ a b Centers for Disease Control and Prevention (CDC) (October 1994). "Certification of poliomyelitis eradication – the Americas, 1994". MMWR. Morbidity and Mortality Weekly Report. Centers for Disease Control and Prevention. 43 (39): 720–722. PMID 7522302. Archived from the original on 21 May 2017.
- ^ Yamazaki, S.; Toraya, H. (2001). "General News. Major Milestone reached in Global Polio Eradication: Western Pacific Region is certified Polio-Free". Health Educ Res. 16 (1): 109–114. Bibcode:2001PDiff..16..110Y. doi:10.1093/her/16.1.109.
- ^ D' Souza RM, Kennett M, Watson C (2002). "Australia declared polio free". Communicable Diseases Intelligence Quarterly Report. 26 (2): 253–260. PMID 12206379.
- ^ "Europe achieves historic milestone as Region is declared polio-free" (Press release). World Health Organization (WHO). 21 June 2002. Archived from the original on 16 September 2008. Retrieved 23 August 2008.
- ^ Ray K (26 February 2012). "India wins battle against dreaded polio". Deccan Herald.
- ^ "India polio-free for a year: 'First time in history we're able to put up such a map'". The Telegraph. 26 February 2012. Archived from the original on 27 February 2012. Retrieved 26 February 2012.
- ^ "India three years polio-free". World Health Organization (WHO). Archived from the original on 1 March 2017. Retrieved 19 February 2017.
- ^ Barron L (4 November 2013). "Armenian Health Ministry: Syrian Armenian children need polio vaccine". CISTran Finance. Archived from the original on 19 December 2013. Retrieved 18 December 2013.
- ^ De Vivo DC, Ryan MM, Jones HR, Darras BT (2014). Neuromuscular Disorders of Infancy, Childhood, and Adolescence: A Clinician's Approach. Elsevier Science. p. 161. ISBN 978-0-12-417127-5. Archived from the original on 23 April 2017.
- ^ Charles Kurzman. The Missing Martyrs. Oxford University Press. p. 130.
Resistance to polio vaccination is a fringe position. Almost every Muslim scholar and political leader has endorsed the vaccine, and all but a few Muslim-majority countries have wiped out the disease entirely.
- ^ a b "Pakistan polio official killed in Peshawar: police". The Daily Star: Lebanon. 11 September 2016. Archived from the original on 11 September 2016. Retrieved 11 September 2016.
- ^ Najafizada E (15 December 2015). "Taliban Join Global Effort to Kill Off Polio in 2016". Bloomberg.com. Archived from the original on 28 February 2017.
- ^ "International Travel and Health. Chapter 6 – Vaccine-preventable diseases and vaccines (2019 update)" (PDF). World Health Organization. United Nations. 2020. Retrieved 2 December 2020.
- ^ a b c d e f g h "Countries with risk of yellow fever transmission and countries requiring yellow fever vaccination (July 2019)". World Health Organization. United Nations. 4 July 2019. Retrieved 2 December 2020.
- ^ Scherbel-Ball, Naomi (25 August 2020). "Africa declared free of polio". BBC News. Archived from the original on 26 August 2020. Retrieved 25 August 2020.
- ^ "Key At-Risk Countries". Global Polio Eradication Initiative. World Health Organization. Retrieved 2 December 2020.
- ^ "Afghanistan Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 1 October 2020. Retrieved 2 December 2020.
- ^ "Belize Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Brunei Darussalam Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Egypt Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Georgia Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "India Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Iran Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Iraq Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Jordan Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Lebanon Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Libya Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Maldives Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Morocco Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Nepal Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Oman Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Pakistan Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Philippines Recommended Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Qatar Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Saint Kitts & Nevis Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Saudi Arabia Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Seychelles Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Syria Required Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Ukraine Recommended Vaccinations: Polio". iamat.org. International Association for Medical Assistance to Travellers (IAMAT). 23 October 2020. Retrieved 2 December 2020.
- ^ "Availability and price of inactivated polio vaccine". The Global Polio Eradication Initiative. Archived from the original on 11 April 2015.
- ^ "Impotence fears hit polio drive". BBC News Online. 25 January 2007. Archived from the original on 9 October 2015. Retrieved 15 December 2015.
- ^ Junaidi I (14 January 2015). "Lab tests show polio vaccine is not 'Haram'". dawn.com. Archived from the original on 22 December 2015. Retrieved 15 December 2015.
추가 정보
- Ramsay M, ed. (2013). "Polio: the green book, chapter 26". Immunisation against infectious disease. London: Public Health England.
- Wallace G, Alexander J (2015). "Chapter 18: Poliomyelitis". In Hamborsky J, Kroger A, Wolfe S (eds.). Epidemiology and Prevention of Vaccine-Preventable Diseases (13th ed.). Washington D.C.: U.S. Centers for Disease Control and Prevention (CDC). ISBN 978-0990449119.
- Routh JA, Oberste MS, Patel M (2018). "Chapter 12: Poliomyelitis". In Roush SW, Baldy LM, Hall MH (eds.). Manual for the surveillance of vaccine-preventable diseases. Atlanta, Georgia: U.S. Centers for Disease Control and Prevention (CDC).
외부 링크
- "Polio Vaccine Information Statement". Centers for Disease Control and Prevention (CDC). 10 August 2021.
- 백신의 역사 웹사이트 – 필라델피아 의사대학의 프로젝트인 백신의 소아마비 역사
- PBS.org – '사람과 발견: Salk는 소아마비 백신 1952를 생산한다', 공영방송서비스(PBS)
- "IPOL – Poliovirus Vaccine Inactivated (Monkey Kidney Cell)". U.S. Food and Drug Administration (FDA). 11 December 2019. STN: 103930.
- 미국 국립의학도서관(MeSH)의 폴리오바이러스 백신