식도암
Esophageal cancer| 식도암 | |
|---|---|
| 기타이름 | 식도암 |
 | |
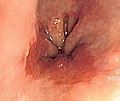
| 식도선암 내시경 영상 | |
| 전문 | 소화기학 일반외과 종양학의 |
| 증상 | 삼킴곤란, 체중감소, 쉰 목소리, 쇄골주위 림프절확대,[1] 구토혈, 대변내 피 |
| 종류들 | 식도 편평상피세포암, 식도선암[2] |
| 위험요소 | 흡연 담배, 술, 아주 뜨거운 음료, 씹는 베텔넛, 비만, 산 역류[3][4] |
| 진단방법 | 조직생검[5] |
| 치료 | 수술, 화학요법, 방사선[5] 치료 |
| 예후 | 5년 생존율 ~15%[1][6] |
| 빈도수. | 2015년 기준[7] 746,000명이 영향을 받았습니다. |
| 데스 | 509,000 (2018)[8] |
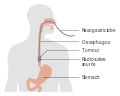
식도암은 식도, 즉 목과 [2]위 사이를 흐르는 음식관에서 발생하는 암입니다.증상은 종종 삼키기 힘들고 체중 [1]감소를 포함합니다.다른 증상으로는 삼킬 때의 통증, 목이 쉰 목소리, 쇄골 주변의 림프절 확장, 마른 기침, 기침이나 구토 등이 있을 [1]수 있습니다.
이 질병의 두 가지 주요 하위 유형은 개발도상국에서 더 흔한 식도 편평세포암(종종 ESCC로 [9]약칭됨)과 선진국에서 [2]더 흔한 식도선암(EAC)입니다.덜 일반적인 유형도 많이 [2]발생합니다.편평상피암은 [10]식도를 따라 늘어선 상피세포에서 발생합니다.선암은 식도의 3분의 1 아래에 있는 선세포에서 발생하며, 종종 이미 장세포형([2][11]바렛식도라고 알려진 상태)으로 변형됩니다.편평세포형의 원인에는 담배, 술, 아주 뜨거운 음료, 형편없는 식단, 그리고 씹는 베텔넛 [3][4]등이 포함됩니다.선암종의 가장 흔한 원인은 흡연 담배, 비만, 산 [3]역류입니다.
이 질환은 내시경(섬유광학 카메라)[5]을 이용한 조직 검사로 진단됩니다.예방에는 금연과 건강한 [1][2]식단이 포함됩니다.치료는 암의 병기와 위치, 그리고 그 사람의 일반적인 상태와 개인의 [5]선호도에 따라 결정됩니다.작은 국소 편평상피암은 [5]치료의 희망으로 수술만으로 치료될 수 있습니다.대부분의 다른 경우에는 방사선 치료를 포함하거나 포함하지 않는 화학요법이 [5]수술과 함께 사용됩니다.더 큰 종양은 화학요법과 방사선 [2]치료로 성장이 느려질 수 있습니다.광범위한 질병이 있거나 환자가 수술을 받을 만큼 건강하지 못한 경우에는 완화의료를 [5]권장하는 경우가 많습니다.
2018년 기준으로 식도암은 한 해 동안 572,000건의 신규 환자가 발생하여 전 세계에서 8번째로 흔한 암입니다.이로 인해 1990년의 [8][12]345,000명에서 그 해 약 509,000명의 사망자가 발생한 사망자 수는 1990년의 345,000명에서 증가했습니다.비율은 국가마다 천차만별인데, 전체 사례의 절반 정도가 [2]중국에서 발생하고 있습니다.여성보다 남성에서 [2]약 3배 더 흔합니다.결과는 질병의 범위 및 기타 의학적 상태와 관련이 있지만 진단이 [2][13]늦는 경우가 많기 때문에 일반적으로 상당히 좋지 않은 경향이 있습니다.5년 생존율은 약 13%에서 18%[1][6]입니다.
징후 및 증상
두드러진 증상은 대개 암이 식도관 둘레의 60% 이상 침윤할 때까지 나타나지 않으며, 이때 종양은 이미 진행 [14]단계에 있습니다.증상의 시작은 대개 [15]종양의 물리적 존재로 인해 관이 좁아짐으로써 발생합니다.
첫 번째 증상이자 가장 흔한 증상은 대개 삼키기가 어렵다는 것인데, 처음에는 고체 음식을, 나중에는 더 부드러운 음식과 [1]액체를 경험하는 경우가 많습니다.삼킬 때의 통증은 처음에는 [1]덜 흔합니다.체중 감소는 종종 편평세포암의 경우 초기 징후이지만, 보통 선암의 [16]경우는 아닙니다.식욕 감소와 영양실조로 인한 궁극적인 체중 감소는 [17]일반적입니다.가슴뼈 뒤쪽이나 배 주변의 통증은 흔히 속쓰림처럼 느껴집니다.어떤 종류의 음식이든 삼키면 통증이 심해져 악화되는 경우가 종종 있습니다.또 다른 징후는 종양이 재발된 후두 신경에 영향을 미치는 결과인 비정상적으로 허스키하고, 쉰 듯한 기침일 수 있습니다.
종양의 존재는 삼킬 때 식도의 정상적인 수축을 방해할 수 있습니다.이것은 메스꺼움과 구토, 음식물 역류, [14]기침으로 이어질 수 있습니다.식도와 기관(윈드파이프)[13] 사이에 발생할 수 있는 비정상적인 연결(피스트)을 통해 음식물이 기도로 유입돼[14] 흡인성 폐렴의 위험도 증가합니다.이 심각한 합병증의 초기 증상은 술을 마시거나 [18]먹을 때 기침을 하는 것일 수도 있습니다.종양 표면이 약하고 출혈이 있어 피를 토할 수 있습니다.진행성 질환에서는 국소 구조의 압박이 발생하여 상기도 폐쇄, 상대정맥 증후군 등의 문제가 발생합니다.고칼슘혈증(혈중 칼슘 과다)이 [14]발생할 수 있습니다.
암이 다른 곳으로 전이된 경우 전이성 질환과 관련된 증상이 나타날 수 있습니다.흔한 확산 부위는 근처 림프절, 간, 폐, [14]뼈 등입니다.간 전이는 황달과 복부 종창을 유발할 수 있습니다.폐 전이는 다른 증상 중에서도 폐 주변의 과도한 유체로 인한 호흡 장애(흉막 유출) 및 호흡 곤란(흔히 호흡 장애와 관련된 감정)을 유발할 수 있습니다.
원인들
두 가지 주요 유형(즉, 편평세포암과 선암)은 별개의 위험 [16]요소를 가지고 있습니다.편평세포암은 흡연이나 [19]알코올과 같은 생활습관 요인과 관련이 있습니다.선암종은 장기적인 산 [19]역류의 영향과 관련이 있습니다.담배는 두 [16]종류 모두의 위험요소입니다.두 가지 유형 모두 60세 [20]이상의 사람들에게서 더 흔합니다.
편평세포암
식도 편평세포암의 두 가지 주요 위험 요인은 담배([2]흡연 또는 씹기)와 알코올입니다.담배와 술의 결합은 강력한 시너지 [21]효과를 냅니다.일부 자료에 따르면 전체 사례의 약 절반이 담배 때문이고 약 3분의 1이 술 때문이라고 합니다. 반면 남성의 경우 4분의 3 이상이 흡연과 [2]과음이 복합적으로 원인이라고 합니다.알코올과 관련된 위험은 알코올의 알데히드 대사산물 및 특정 관련 [16]효소의 돌연변이와 관련이 있는 것으로 보입니다.그러한 대사 변이는 [2]아시아에서 비교적 흔합니다.
다른 관련 위험 요소로는 매우 뜨거운 음료(65°C 또는 149°[22][23]F 이상)의 규칙적인 섭취와 가성 [2]물질의 섭취가 있습니다.니트로사민(담배 연기와 특정 식품에서 모두 발견되는 화학적 화합물)에 대한 높은 수준의 식이 노출도 관련 위험 [16]요소인 것으로 보입니다.부정적인 식생활 패턴은 가공 및 바비큐 고기, 절인 야채 등을 통해 니트로사민에 노출되고 신선한 음식의 [2]섭취가 적은 것으로 보입니다.다른 관련 요인으로는 영양 결핍, 낮은 사회 경제적 상태, 그리고 불량한 구강 [16]위생 등이 있습니다.베텔 너트를 씹는 것은 [4]아시아에서 중요한 위험 요소입니다.
신체적 외상은 [24]위험을 증가시킬 수 있습니다.이것은 아주 뜨거운 [3]음료를 마시는 것을 포함할 수 있습니다.
선암
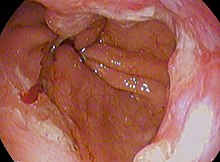
이런 [25]종류의 식도암은 남성에게 7배에서 10배 정도 더 많이 발생하는 남성 우세 현상이 특히 강합니다.이러한 불균형은 산 역류 및 [25]비만을 포함한 알려진 다른 위험 요소의 특성 및 상호 작용과 관련이 있을 수 있습니다.
위식도역류질환
위식도 역류 질환(위식도 역류 질환 또는 GERD라고도 알려진 매우 일반적인 질환)의 장기 미란 효과는 이러한 유형의 [26]암과 밀접하게 관련되어 있습니다.장기간의 GERD는 편평한 [26]내벽의 침식에 반응하여 식도의 하부에 세포 유형의 변화를 유도할 수 있습니다.바렛식도라고 알려진 이 현상은 남성보다 여성에서 약 20년 늦게 나타나는 것으로 보이는데, 아마도 호르몬 [26]요인 때문일 것입니다.기계적인 수준에서 식도에는 정상적인 편평 상피로서 담즙과 산에 더 내성이 있고 온유성 형질전환뿐만 아니라 장 분화가 일어나기 쉬운 작은 HOXA13 발현 구획이 있습니다.GERD에 이어 이 HOXA13 발현 구획은 정상적인 편평 구획을 능가하여 식도의 장측면과 [27]식도암 발생 경향의 증가로 이어집니다.증상이 있는 GERD나 담즙 역류가 바렛식도를 더 가능하게 하고, 이는 결국 선암으로 [16]이어질 수 있는 추가적인 변화의 위험을 증가시킵니다.디옥시콜산 및 케노데옥시콜산을 포함하는 비결합 담즙산을 포함하는 담즙 환류는 산화 스트레스 및 DNA[28] 손상을 유도하여 식도 선암 발생에 기여하는 것으로 보입니다.바렛식도가 있는 곳에서 선암이 발생할 위험성은 명확하지 않으며 과거에는 [2]과대평가되었을 수도 있습니다.
비만이나 과체중은 [29]둘 다 위험 증가와 관련이 있는 것으로 보입니다.비만과의 연관성은 어떤 유형의 비만과 관련된 암 중에서도 가장 강한 것으로 보이지만, 이것에 대한 이유는 아직 [30]명확하지 않습니다.복부 비만은 GERD와 바렛식도 [30]뿐만 아니라 이러한 종류의 암과의 밀접한 연관성을 고려할 때 특히 관련성이 있는 것으로 보입니다.이런 유형의 비만은 [30]남성들의 특징입니다.생리학적으로, 그것은 GERD를 자극하고 다른 만성 염증 [26]효과도 가지고 있습니다.
헬리코박터 파일로리 감염(세계 인구의 절반 이상이 영향을 받았다고 생각되는 흔한 일)은 식도 선암의 위험 요소가 아니며 실제로는 보호적인 것으로 보입니다.GERD의 원인이자 위암의 위험 요인임에도 불구하고, 이 감염은 50%[31][32]에 달하는 식도 선암의 위험 감소와 관련이 있는 것으로 보입니다.보호 효과에 대한 생물학적 설명은 [32]다소 불분명합니다.한 가지 설명은 H. pylori의 일부 균주가 위산을 감소시켜 [33]GERD에 의한 손상을 감소시킨다는 것입니다.최근 수십 년간 서구 인구에서 H. pylori 감염률이 감소하는 것은 가구의 과밀화 감소와 관련이 있으며 식도 선암의 [31]동시 증가의 한 요인이 될 수 있습니다.
EAC는 여성에게 훨씬 덜 흔할 뿐만 아니라 인생 후반에 평균 20년 정도 발전하기 때문에 여성 호르몬 또한 보호 효과를 가질 수 있습니다.비록 많은 생식 요인들에 대한 연구들이 명확한 그림을 만들어내지는 못했지만, 모유 [31]수유 기간이 길어지면서 산모의 위험은 감소하는 것으로 보입니다.
담배 흡연은 위험을 증가시키지만 식도선암의 경우 편평세포암에 비해 효과가 미미하며 알코올이 [31]원인으로 입증되지 않았습니다.
관련조건
- 두경부암은 현장 암화(즉, 장기적인 [34][35]발암성 노출에 대한 지역적 반응)로 인해 식도 편평세포암종을 포함한 지역의 두 번째 1차 종양과 관련이 있습니다.
- 흉부의 다른 상태에 대한 방사선 치료의 과거력은 식도선암의 [16]위험인자입니다.
- 가성 물질을 실수로 또는 [2]고의로 삼킴으로써 식도에 부식성 손상을 입히는 것은 편평상피암의 위험 요소입니다.
- 식도암을 동반한 타일로시스는 17번 염색체에 존재하는 RHBDF2 유전자의 돌연변이와 관련이 있는 상염색체 우성 유전을 가진 희귀한 가족 질환입니다. 손바닥과 발바닥의 피부가 두꺼워지고 평생에 걸쳐 편평세포암에 [2][36]걸릴 위험이 높습니다.
- 무찰라증(즉, 삼킨 후 식도에 비자발적 반사가 없는 것)은 갇힌 음식과 [37]음료의 정체로 인해 적어도 남성에서 식도암의 주요 유형 모두에 위험 요소로 보입니다.
- 플럼머-빈슨 증후군(식도줄이 생기는 희귀질환)도 [2]위험요인입니다.
- 인유두종 바이러스(HPV)와 식도 편평세포암 [38]사이에 인과관계가 있을 가능성을 시사하는 몇 가지 증거가 있습니다.그 관계는 불분명합니다.[39]HPV의 가능한 관련성은 [41]중국을 포함한 일부 아시아 국가와 같이 이러한 형태의 [40]질병의 발병률이 특히 높은 곳에서 더 클 수 있습니다.
- 셀리악병과 식도암 사이에는 연관성이 있습니다.셀리악병을 치료하지 않은 사람들은 더 높은 위험을 가지고 있지만, 이러한 위험은 진단 후 시간이 지남에 따라 감소하는데, 아마도 셀리악병을 가진 사람들의 악성 종양 발생에 대한 보호 역할을 하는 것으로 보이는 글루텐이 없는 식단의 채택 때문일 것입니다.그러나 글루텐이 없는 식단의 진단과 시작이 늦어지는 것은 악성화의 위험을 증가시키는 것으로 보입니다.게다가, 어떤 경우에 셀리악병의 발견은 초기 증상이 셀리악병에서 [42]나타날 수 있는 것과 비슷한 암의 발생 때문입니다.
진단.

임상평가
바륨 제비 또는 바륨 식사에서 폐색성 종양이 의심될 수 있지만 내시경을 이용한 검사로 진단하는 것이 가장 좋습니다.이것은 빛과 카메라가 있는 유연한 튜브를 식도 아래로 통과시키고 벽을 검사하는 것을 포함하며, 식도 위내시경 검사라고 불립니다.의심스러운 병변을 촬영한 생체검사는 악성 징후가 있는지 조직학적으로 검사됩니다.
암의 확산 정도를 평가하기 위해서는 추가적인 검사가 필요합니다(아래 ③ 단계 참조).흉부, 복부 및 골반의 컴퓨터 단층 촬영(CT)은 암이 인접한 조직 또는 멀리 떨어진 기관(특히 간 및 림프절)으로 전이되었는지 여부를 평가할 수 있습니다.CT 스캔의 민감도는 일반적으로 [43][44]1cm보다 큰 종괴(예: 림프절 또는 관련 기관의 확장)를 감지하는 기능에 의해 제한됩니다.양전자 방출 단층 촬영은 질병의 정도를 추정하는 데도 사용되며 CT 단독 [45]촬영보다 더 정밀한 것으로 간주됩니다.새로운 모달리티로서 PET/MR은 PET/CT와 비교하여 공정한 실현 가능성과 양호한 상관 관계로 수술 전 단계에서 유망한 결과를 보여주었습니다.환자에 [46]대한 방사선량을 낮춤으로써 조직 분화를 강화할 수 있습니다.식도 내시경 초음파는 종양의 침범 정도와 지역 림프절로의 확산 가능성에 대한 병기 정보를 제공할 수 있습니다.
종양의 위치는 일반적으로 치아와의 거리로 측정됩니다.식도(길이 25cm 또는 10cm)는 위치를 결정하기 위해 일반적으로 세 부분으로 나뉩니다.선암은 위 근처에서, 편평상피세포암은 목 근처에서 발생하는 경향이 있지만 식도 어디에서나 발생할 수 있습니다.
-
식도 중심부 점막하 종양의 내시경 및 방사상 내시경 초음파 영상
-
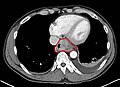
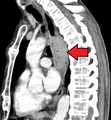
식도 종양을 보여주는 조영 CT 촬영(관상 보기)
-
식도암
종류들
식도암은 일반적으로 식도의 상피 또는 표면 라이닝으로 인해 발생하는 암종입니다.대부분의 식도암은 외관상 두경부암과 유사하고 담배 및 알코올 소비와 관련이 있는 식도 편평세포암(ESCC)과 종종 GERD 및 바렛식도의 역사와 관련이 있는 식도선암(EAC)의 두 가지 등급 중 하나에 해당합니다.경험의 법칙은 위쪽의 2/3에 있는 암은 ESCC이고 아래쪽의 1/3 EAC에 있는 암일 가능성이 높다는 것입니다.
희귀한 조직학적 유형의 식도암은 다양한 변이의 편평세포암, 그리고 다른 [47][48]것들 중에서 레이오미오스육종, 악성 흑색종, 횡문근육종 그리고 림프종과 같은 상피가 아닌 종양을 포함합니다.
스테이징
stageing은 TNM stageing system을 기반으로 하며, 종양 침범량(T), 림프절 침범량(N), 원격 전이량([16]M)을 분류합니다.현재 선호되는 분류는 식도와 식도 위 접합부의 [16]암에 대한 2010년 AJCC 병기 시스템입니다.또한 이 시스템은 임상 의사결정을 안내하기 위해 세포 유형(ESCC, EAC 등), 등급(분화 정도 – 암세포의 생물학적 공격성을 나타내는 지표), 종양 위치(상, 중간, 하부 또는 접합부[49])[50]에 대한 정보를 통합합니다.
-
식도암의 T1, T2, T3기
-
T4기 식도암
-
림프절까지 전이된 식도암
예방
예방은 담배를 끊거나 [2]씹는 것을 포함합니다.아시아의 오락 중독 극복은 식도 [4]편평세포암 예방을 위한 또 하나의 유망한 전략입니다.정상 [51]체중을 유지함으로써 위험을 줄일 수도 있습니다.2022년 우산 리뷰에 따르면 칼슘 섭취는 위험을 낮추는 [52]것과 관련이 있을 수 있습니다.
국립암연구소에 따르면, "십자가나무(배추, 브로콜리/브로콜리니, 콜리플라워, 브뤼셀 새싹)와 녹황색 채소와 과일이 많이 함유된 식단은 식도암 [53]위험 감소와 관련이 있습니다."식이섬유는 특히 식도 [54]선암에 대한 보호작용으로 생각됩니다.비타민 보충제가 [1]위험을 바꾼다는 증거는 없습니다.
상영
바렛식도(식도 하부에 늘어선 세포의 변화)를 가진 사람들은 훨씬 더 높은 [55]위험에 처해 있으며,[56] 암의 초기 징후에 대해 정기적인 내시경 검사를 받을 수도 있습니다.증상이 없는 사람의 선암 검진의 효과가 [2]불분명하기 때문에 미국에서는 [1]권장하지 않습니다.편평암 비율이 높은 세계의 일부 지역에는 검진 [2]프로그램이 있습니다.
관리



치료는 관련된 [57][58]다양한 전문 분야를 다루는 다학제 팀에 의해 가장 잘 관리됩니다.충분한 영양 공급이 보장되어야 하며, 적절한 치과 관리가 필수적입니다.치료 결정에 영향을 미치는 요소는 암의 병기와 세포 유형(EAC, ESCC 및 기타 유형), 그리고 그 사람의 일반적인 상태 및 [16]존재하는 다른 질병을 포함합니다.
일반적으로, 치료 의도를 가진 치료는 원격 전이 없이 국소적인 질병으로 제한됩니다: 그러한 경우 수술을 포함하는 결합된 접근법이 고려될 수 있습니다.광범위하거나 전이되거나 재발하는 질병은 완화적으로 관리됩니다: 이 경우 화학요법은 생존 기간을 연장하는 데 사용될 수 있고 방사선 치료나 스텐트 시술과 같은 치료는 증상을 완화하고 [16]삼키기 쉽도록 사용될 수 있습니다.
수술.
만약 암이 아직 초기 단계에 있는 상태에서 진단되었다면, 치료 의도를 가지고 수술적 치료가 가능할 것입니다.식도의 점막이나 안감만을 포함하는 일부 작은 종양은 내시경 점막 절제술(EMR)[59][60]을 통해 제거될 수 있습니다.그렇지 않으면 초기 병변의 치료적 수술은 식도의 전부 또는 일부를 제거(식도절제술)하는 것을 수반할 수 있지만, 이 수술은 사망 위험이 상대적으로 높거나 수술 후 어려움을 수반하는 어려운 수술입니다.수술의 이점은 EAC보다 초기 ESCC에서 덜 명확합니다.여러 가지 수술 방법이 있으며, 특정한 상황에 가장 적합한 선택은 여전히 연구와 [57][61][62]논의의 대상입니다.종양의 특성과 위치뿐만 아니라 환자의 상태, 수술팀이 가장 많이 경험하는 수술의 종류 등이 다른 요인으로 꼽힙니다.
치료 [63]후 삶의 질은 수술을 고려할 때 중요한 요소입니다.수술 결과는 시술이 [61]빈번하게 이루어지는 큰 중심부에서 더 나을 수 있습니다.암이 신체의 다른 부분으로 전이된 경우, 식도 절제술은 요즘 정상적으로 [61][64]시행되지 않습니다.
식도 절제술은 식도의 한 부분을 제거하는 것입니다. 남은 식도의 길이가 짧아지면 소화관의 다른 일부 부분이 흉강을 통해 끌어올려져 개재됩니다.이것은 대개 위나 대장의 일부입니다.위를 단축된 식도에 다시 연결하는 것을 식도 [61]위문합술이라고 합니다.
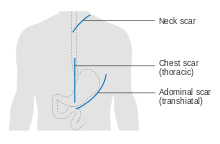
식도 절제술은 여러 가지 방법으로 시행할 수 있습니다.수술 방법의 선택은 종양의 특성과 위치, 그리고 외과의사의 선호도에 따라 달라집니다.다양한 상황에서 최상의 결과를 제공하는 임상 시험의 명확한 증거가 [61]부족합니다.진입 지점에 대한 첫 번째 결정은 경흉부 시술과 경흉부 시술 사이에 있습니다.최근의 횡사적 접근법은 가슴을 열 필요를 피합니다. 대신 외과의사는 하복부의 절개와 목의 다른 절개를 통해 몸으로 들어갑니다.식도의 아래 부분은 주변 조직으로부터 해방되고 필요에 따라 절단됩니다.그리고 나서 위는 식도 구멍(식도가 횡격막을 통과하는 구멍)을 통해 밀려 [61]목 부분에 있는 식도의 남은 상부에 결합됩니다.
전통적인 경흉부 접근법은 가슴을 통해 몸으로 들어가며, 다양한 변형이 있습니다.흉부 복부 접근법은 복부와 흉부 공동을 개방하고, 2단계 아이버 루이스(Lewis-Tanner라고도 함) 접근법은 초기 개복술과 위관의 구성을 포함하며, 종양을 절제하고 식도 위문합을 만들기 위해 오른쪽 개복술이 뒤따릅니다.3단계 맥키언 접근법은 목에 3번째 절개를 추가하여 경추 문합을 완성합니다.최근 일부 외과의사들의 접근법은 확장 식도 절제술이라 불리는 것을 사용하는데, 림프절을 포함한 더 많은 주변 조직이 [61]일괄적으로 제거됩니다.
환자가 전혀 삼킬 수 없는 경우 식도를 열어두기 위해 식도 스텐트를 삽입할 수 있습니다. 스텐트는 누공 폐쇄에도 도움이 될 수 있습니다.종양 치료가 진행되는 동안 수유를 계속하기 위해서는 비위관이 필요할 수 있으며, 일부 환자들은 위루술(위에 직접 접근할 수 있는 피부의 수유 구멍)이 필요합니다.후자의 두 가지는 환자가 음식이나 침을 기도로 흡입하는 경향이 있고, 흡입성 폐렴에 걸리기 쉬운 경우에 특히 중요합니다.
화학요법 및 방사선 치료
화학요법은 종양의 종류에 따라 다르지만, 3주마다 연속적으로 또는 3주마다 플루오로우라실(5-FU)과 함께 시스플라틴 기반(또는 카보플라틴 또는 옥살리플라틴)이 되는 경향이 있습니다.더 최근의 연구들에서, 에피루비신의 첨가는 진행성 절제 불가능한 [65][medical citation needed]암에서 다른 유사한 요법들보다 더 뛰어났습니다[clarification needed].수술 후(즉, 재발 위험을 줄이기 위해), 수술 전(neoadjuvant) 또는 수술이 불가능한 경우 화학요법을 시행할 수 있습니다. 이 경우 시스플라틴과 5-FU가 사용됩니다.진행 중인 실험은 화학 요법의 다양한 조합을 비교합니다. 예를 들어, II/III REAL-2 단계는 에피루비신과 시스플라틴 또는 옥살리플라틴, 플루오로우라실 또는 카페시타빈을 포함하는 4가지 요법을 비교합니다.
방사선 치료는 화학요법이나 수술 전, 도중 또는 수술 후에 시행되며, 때로는 증상을 조절하기 위해 스스로 시행되기도 합니다.국소 질환을 앓고 있지만 수술을 금지하는 환자의 경우, "방사선 방사선 치료"를 치료 목적으로 사용할 수 있습니다.
기타접근방법
내시경 치료의 형태는 0기 및 I기 질환에 사용되어 왔습니다: 내시경 점막 절제술(EMR)[66] 및 고주파 절제술, 광역학 치료, Nd-YAG 레이저 또는 아르곤 플라즈마 응고를 사용하는 점막 절제술입니다.
레이저 치료는 치료 부위에만 영향을 미치면서 종양 세포를 파괴하기 위해 고강도의 빛을 사용하는 것입니다.이것은 일반적으로 수술로 암을 제거할 수 없는 경우에 행해집니다.막힘을 완화하면 통증과 삼키기 어려움을 도울 수 있습니다.레이저 치료의 한 종류인 광역학 치료는 암세포에 흡수되는 약물을 사용하는 것을 포함합니다. 특별한 빛에 노출되면 약물이 활성화되어 암세포를 파괴합니다.
-
식도암 내부방사선치료
후속 조치
치료 요법이 완료된 후 환자를 면밀하게 추적합니다.종종, 다른 치료법들이 증상을 개선하고 영양을 최대화하기 위해 사용됩니다.
예후
일반적으로 식도암의 예후는 상당히 좋지 않은데, 대부분의 환자들이 진행성 질환을 가지고 있기 때문입니다.첫 증상(삼키기 곤란 등)이 나타날 때는 이미 병이 진행된 상태입니다.미국의 전체 5년 생존율(5YSR)은 약 15%로 대부분의 사람들이 진단 [67]첫 해 안에 사망합니다.영국과 웨일즈(2007년 동안 진단받은 환자)의 최근 생존 데이터는 10명 중 1명만이 식도암에서 적어도 10년 [68]이상 생존한다는 것을 보여줍니다.
개별화된 예후는 주로 단계에 따라 달라집니다.전적으로 식도 점막에만 국한된 암을 가진 사람들은 약 80%의 5YSR을 갖지만, 점막하 침범은 이를 50% 이하로 감소시킵니다.근막(식도의 근육층)으로의 확장은 20% 5YSR을 시사하며 식도에 인접한 구조로의 확장은 7% 5YSR을 예측합니다. 원격 전이가 있는 환자(치료 수술 후보자가 아닌)는 3%[69] 5YSR 미만입니다.
역학

식도암은 전 [2]세계적으로 8번째로 많이 진단되는 암이며, 예후가 좋지 않기 때문에 암과 [55]관련된 사망의 6번째로 흔한 원인입니다.2012년에는 약 40만 명의 사망자를 발생시켰으며, 이는 전체 암 사망자의 약 5%를 차지합니다(신규 환자는 약 456,000명으로 전체 [2]암의 약 3%를 차지합니다).
ESCC(식도 편평세포암)는 전 세계 식도암의 모든 사례의 60-70%를 차지하는 반면, EAC(식도선암)는 20-30%를 더 차지합니다(멜라노마, 레이오모사르코마, 카르키노이드 및 림프종은 덜 일반적인 [70]유형임).식도암의 두 가지 주요 유형의 발병률은 서로 다른 지리적 [71]영역에 따라 크게 다릅니다.일반적으로 ESCC는 개발도상국에서 더 흔하고 EAC는 [2]선진국에서 더 흔합니다.
2012년 ESCC의 전 세계 발병률은 10만 년당 5.2건으로 남성이 우세했습니다(남성은 10만 명당 7.7건 대 [72]여성은 2.8건).연구 [72]대상 국가의 90%에서 일반적인 유형이었습니다.ESCC는 중국 북부, 러시아 남부, 이란 북동부, 아프가니스탄 북부, [70]터키 동부를 지나는 이른바 '아시아 식도암 벨트'에서 특히 빈번합니다.2012년 전 세계 ESCC 사례의 약 80%가 중부 및 동남아시아에서 발생했으며, 전체 사례의 절반 이상(53%)이 [72]중국에서 발생했습니다.추정 국가별 발병률이 가장 높은 나라는 (아시아의) 몽골과 투르크메니스탄 그리고 (아프리카의) 말라위, 케냐,[72] 우간다였습니다.식도암 문제는 사하라 이남 아프리카 동부와 남부에서 오래전부터 인식되어 왔는데, 이 지역에서는 ESCC가 우세한 [73]것으로 보입니다.
서구 국가에서 EAC는 최근 수십 년간 발병률이 증가한 후 질병의 지배적인 형태가 되었습니다(대부분 [5][31]안정적으로 유지된 ESCC의 발병률과는 대조적입니다).2012년 전 세계 EAC 발병률은 10만 명당 0.7명으로 남성이 우세했습니다. (남성은 10만 명당 1.1명 대 여성은 0.3명)특히 발병률이 높은 지역은 북유럽과 서유럽, 북아메리카와 오세아니아입니다.기록된 비율이 가장 높은 나라는 영국, 네덜란드, 아일랜드, 아이슬란드,[72] 뉴질랜드였습니다.
미국
미국에서 식도암은 남성의 암 사망률 7위(전체의 [74]4%)를 차지하고 있습니다.국립 암 연구소는 2013년에 약 18,000명의 새로운 환자가 발생하고 식도암으로 인해 15,000명 이상이 사망한 것으로 추정했습니다(미국 암 협회는 2014년 동안 약 18,170명의 새로운 식도암 환자가 진단되어 15,450명이 [71][74]사망한 것으로 추정했습니다).
편평상피세포암종은 심한 흡연이나 알코올 복용의 과거력이 있는 아프리카계 미국인 남성들 사이에서 더 흔합니다.1970년대까지만 해도 편평세포암은 미국 식도암의 대부분을 차지했습니다.최근 수십 년간 미국에서는 (바렛식도와 관련된) 식도 선암 발병률이 꾸준히 증가하여 이제 편평세포암을 넘어섰습니다.편평세포암과는 대조적으로 식도선암은 아프리카계 미국인보다 백인 미국인 남성(60세 이상)에게 더 흔합니다.다수의 보고에 따르면 지난 20년간 특히 히스패닉계가 아닌 백인 남성에서 식도선암 발생이 증가했습니다.1973년부터 2002년까지 뉴멕시코주에서 식도선암 연령 조정 발병률이 증가했습니다.이러한 증가는 비히스패닉계 백인들과 히스패닉계 백인들에게서 발견되었고 비히스패닉계 [75]백인들에게서 우세하게 되었습니다.아프리카계 미국인들의 식도암 발병률과 사망률은 인과관계가 있는 사람들의 사망률보다 계속 높습니다.하지만, 1980년대 초부터 미국 흑인들 사이에서 식도암의 발병률과 사망률은 상당히 감소한 반면 백인들 사이에서는 계속 [76]증가하고 있습니다.1975년과 2004년 사이에 선암종의 발병률은 미국 백인 남성에서 460% 이상 증가했고 미국 백인 여성에서 335%[71] 증가했습니다.
영국
최근 수십 [16]년간 영국에서 식도선암 발병률이 크게 증가했습니다.전체적으로 식도암은 영국에서 13번째로 흔한 암(2011년 약 8,300명이 진단)이며, 6번째로 흔한 암 사망 원인(2012년 [77]약 7,700명이 사망)입니다.
사회와 문화
주목할 만한 사례
배우 험프리 보가트는 1957년 57세의 나이로 식도암으로 세상을 떠났습니다.
밴드 리더이자 작곡가인 듀크 엘링턴과 협력한 미국의 재즈 작곡가, 피아니스트, 작사가, 편곡가 빌리 스트레이혼은 1967년 51세의 나이로 식도암으로 세상을 떠났습니다.
배우 존 해빙은 2002년 60세의 나이로 식도암으로 세상을 떠났습니다.
작가이자 저널리스트인 크리스토퍼 히친스는 2011년 62세의 [78]나이로 식도암으로 사망했습니다.
2015년 10월, 모리세이는 그가 병에 걸렸다고 말했고, 그가 병에 [79]걸렸다는 것을 처음 들었을 때의 경험을 설명합니다.
아바타 성우 이와마츠 마코: 이로 장군 역의 라스트 에어벤더와 아쿠 역의 사무라이 잭은 2006년 72세의 나이로 식도암으로 사망했습니다.
변호사이자 사업가인 로버트 카다시안은 2003년 59세의 나이로 식도암으로 사망했습니다.
가수이자 리얼리티 TV 스타인 트레이시 브랙스턴은 2022년 50세의 나이로 식도암으로 세상을 떠났습니다.
연구방향
아스피린이나 관련 NSAID를 [80]사용하는 사람들에게서 식도 편평세포암의 위험이 감소될 수 있지만 무작위 대조군 실험이 없는 현재의 증거는 [2][31]결론에 이르지 못합니다.
식도선암의 유전체학은 Cancer genome sequencing - Wikipedia를 이용하여 연구되고 있습니다.식도선암은 종양 미세 [82]환경 내에서 이질성을 갖는 복잡한 종양 유전체를 특징으로 합니다.
참고 항목
참고문헌
- ^ a b c d e f g h i j Ferri FF, ed. (2012). "Tumors". Ferri's clinical advisor 2013. Philadelphia, PA: Mosby (Elsevier). pp. 389–391. ISBN 978-0323083737. Archived from the original on 2015-09-19.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z Montgomery EA, Basman FT, Brennan P, Malekzadeh R (2014). "Oesophageal Cancer". In Stewart BW, Wild CP (eds.). World Cancer Report 2014. World Health Organization. pp. 528–543. ISBN 978-9283204299.
- ^ a b c d Zhang HZ, Jin GF, Shen HB (June 2012). "Epidemiologic differences in esophageal cancer between Asian and Western populations". Chinese Journal of Cancer. 31 (6): 281–286. doi:10.5732/cjc.011.10390. PMC 3777490. PMID 22507220.
- ^ a b c d Akhtar S (February 2013). "Areca nut chewing and esophageal squamous-cell carcinoma risk in Asians: a meta-analysis of case-control studies". Cancer Causes & Control. 24 (2): 257–265. doi:10.1007/s10552-012-0113-9. PMID 23224324. S2CID 14356684.
- ^ a b c d e f g h Stahl M, Mariette C, Haustermans K, Cervantes A, Arnold D (October 2013). "Oesophageal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up". Annals of Oncology. 24 (Suppl 6): vi51–vi56. doi:10.1093/annonc/mdt342. PMID 24078662.
- ^ a b "SEER Stat Fact Sheets: Esophageal Cancer". National Cancer Institute. Archived from the original on 6 July 2014. Retrieved 18 June 2014.
- ^ Vos T, Allen C, Arora M, Barber RM, Bhutta ZA, Brown A, et al. (GBD 2015 Disease and Injury Incidence and Prevalence Collaborators) (October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
- ^ a b "Esophageal Cancer Factsheet" (PDF). Global Cancer Observatory. Retrieved 8 November 2019.
- ^ 심지어 영국 영어 철자를 사용하는 사람들에 의해서도 "오식도"
- ^ Kelsen D (2007). Gastrointestinal oncology: principles and practices (2nd ed.). Philadelphia, Pa.: Lippincott Williams & Wilkins. p. 4. ISBN 9780781776172. Archived from the original on 2015-09-25.
- ^ Schottenfeld D, Fraumeni J, eds. (2006). Cancer epidemiology and prevention (3rd ed.). Oxford: Oxford University Press. p. 697. ISBN 9780199747979. Archived from the original on 2015-10-31.
- ^ Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, et al. (December 2012). "Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859): 2095–2128. doi:10.1016/S0140-6736(12)61728-0. hdl:10536/DRO/DU:30050819. PMID 23245604. S2CID 1541253.
- ^ a b Enzinger PC, Mayer RJ (December 2003). "Esophageal cancer" (PDF). The New England Journal of Medicine. 349 (23): 2241–2252. doi:10.1056/NEJMra035010. PMID 14657432. Archived from the original (PDF) on 2014-07-14.
- ^ a b c d e Mayer RJ (2008). "Gastrointestinal Tract Cancer". In Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson JL, Loscalzo J (eds.). Harrison's principles of internal medicine. Vol. 1 (18th ed.). New York: McGraw-Hill Medical Publishing Division. pp. 764–5. ISBN 978-0071748896.
- ^ Cheifetz AS, Brown A, Curry M, Moss AC (2011). Oxford American Handbook of Gastroenterology and Hepatology. Oxford University Press. p. 106. ISBN 978-0-19-983012-1.
- ^ a b c d e f g h i j k l m Pennathur A, Gibson MK, Jobe BA, Luketich JD (February 2013). "Oesophageal carcinoma". Lancet. 381 (9864): 400–412. doi:10.1016/S0140-6736(12)60643-6. PMID 23374478. S2CID 13550805.
- ^ Yamada T (2011). Textbook of Gastroenterology. John Wiley & Sons. pp. 1590–1. ISBN 978-1-4443-5941-1. Archived from the original on 2015-09-20.
- ^ Gerdes H, Ferguson MK (2002). "Palliation of Esophageal Cancer". In Posner MC, Vokes EE, Weichselbaum RR (eds.). Cancer of the Upper Gastrointestinal Tract. PMPH-USA. p. 184. ISBN 978-1-55009-101-4. Archived from the original on 2015-10-30.
- ^ a b Lao-Sirieix P, Caldas C, Fitzgerald RC (June 2010). "Genetic predisposition to gastro-oesophageal cancer". Current Opinion in Genetics & Development. 20 (3): 210–217. doi:10.1016/j.gde.2010.03.002. PMID 20347291.
- ^ Tobias JS, Hochhauser D (2013). Cancer and its management (6th ed.). John Wiley & Sons. p. 254. ISBN 978-1-11871-325-9.
- ^ Prabhu A, Obi KO, Rubenstein JH (June 2014). "The synergistic effects of alcohol and tobacco consumption on the risk of esophageal squamous cell carcinoma: a meta-analysis". The American Journal of Gastroenterology. 109 (6): 822–827. doi:10.1038/ajg.2014.71. PMID 24751582. S2CID 205103765.
- ^ Loomis D, Guyton KZ, Grosse Y, Lauby-Secretan B, El Ghissassi F, Bouvard V, et al. (International Agency for Research on Cancer Monograph Working) (July 2016). "Carcinogenicity of drinking coffee, mate, and very hot beverages" (PDF). The Lancet. Oncology. 17 (7): 877–878. doi:10.1016/s1470-2045(16)30239-x. PMID 27318851. Archived from the original (PDF) on 2016-10-05. Retrieved 2016-10-03.
- ^ "Q&A on Monographs Volume 116: Coffee, maté, and very hot beverages" (PDF). www.iarc.fr. IARC / WHO. Archived (PDF) from the original on 5 July 2016. Retrieved 3 October 2016.
- ^ Jobe BA, Thomas CR, Hunter JG, eds. (2009). Esophageal cancer principles and practice. New York: Demos Medical. p. 93. ISBN 9781935281177. Archived from the original on 2017-09-10.
- ^ a b Rutegård M, Lagergren P, Nordenstedt H, Lagergren J (July 2011). "Oesophageal adenocarcinoma: the new epidemic in men?". Maturitas. 69 (3): 244–248. doi:10.1016/j.maturitas.2011.04.003. PMID 21602001.
- ^ a b c d de Jonge PJ, van Blankenstein M, Grady WM, Kuipers EJ (January 2014). "Barrett's oesophagus: epidemiology, cancer risk and implications for management". Gut. 63 (1): 191–202. doi:10.1136/gutjnl-2013-305490. hdl:1765/67455. PMC 6597262. PMID 24092861.
- ^ Janmaat VT, Nesteruk K, Spaander MC, Verhaar AP, Yu B, Silva RA, et al. (June 2021). "HOXA13 in etiology and oncogenic potential of Barrett's esophagus". Nature Communications. 12 (1): 3354. Bibcode:2021NatCo..12.3354J. doi:10.1038/s41467-021-23641-8. PMC 8184780. PMID 34099670.
- ^ Režen T, Rozman D, Kovács T, Kovács P, Sipos A, Bai P, Mikó E (April 2022). "The role of bile acids in carcinogenesis". Cellular and Molecular Life Sciences. 79 (5): 243. doi:10.1007/s00018-022-04278-2. PMC 9013344. PMID 35429253.
- ^ Turati F, Tramacere I, La Vecchia C, Negri E (March 2013). "A meta-analysis of body mass index and esophageal and gastric cardia adenocarcinoma". Annals of Oncology. 24 (3): 609–617. doi:10.1093/annonc/mds244. PMID 22898040.
- ^ a b c Lagergren J (June 2011). "Influence of obesity on the risk of esophageal disorders". Nature Reviews. Gastroenterology & Hepatology. 8 (6): 340–347. doi:10.1038/nrgastro.2011.73. PMID 21643038. S2CID 31598439.
- ^ a b c d e f Lagergren J, Lagergren P (2013). "Recent developments in esophageal adenocarcinoma". CA. 63 (4): 232–248. doi:10.3322/caac.21185. PMID 23818335.
- ^ a b Falk GW (July 2009). "Risk factors for esophageal cancer development" (PDF). Surgical Oncology Clinics of North America. 18 (3): 469–485. doi:10.1016/j.soc.2009.03.005. PMID 19500737. Archived (PDF) from the original on 2014-08-12.
- ^ Harris RE (2013). "Epidemiology of Esophageal Cancer". Epidemiology of Chronic Disease: Global Perspectives. Burlington, MA: Jones & Bartlett Publishers. pp. 157–161. ISBN 978-0-7637-8047-0. Archived from the original on 2015-09-25.
- ^ Priante AV, Castilho EC, Kowalski LP (April 2011). "Second primary tumors in patients with head and neck cancer". Current Oncology Reports. 13 (2): 132–137. doi:10.1007/s11912-010-0147-7. PMID 21234721. S2CID 207335139.
- ^ Scherübl H, Steinberg J, Schwertner C, Mir-Salim P, Stölzel U, de Villiers EM (June 2008). "[Coincidental squamous cell cancers of the esophagus, head, and neck: risk and screening]" [Coincidental squamous cell cancers of the esophagus, head, and neck: risk and screening]. Hno (in German). 56 (6): 603–608. doi:10.1007/s00106-007-1616-7. PMID 17928979. S2CID 9504791.
- ^ "Tylosis with esophageal cancer". rarediseases.info.nih.gov. Genetic and Rare Diseases Information Center (GARD) – NIH. 18 January 2013. Archived from the original on 19 August 2014. Retrieved 16 August 2014.
- ^ Nyrén O, Adami HO (2008). "Esophageal Cancer". In Adami HO, Hunter DJ, Trichopoulos D (eds.). Textbook of Cancer Epidemiology. Vol. 1. Oxford University Press. p. 224. ISBN 978-0-19-531117-4. Archived from the original on 2015-10-25.
- ^ Liyanage SS, Rahman B, Ridda I, Newall AT, Tabrizi SN, Garland SM, et al. (2013). "The aetiological role of human papillomavirus in oesophageal squamous cell carcinoma: a meta-analysis". PLOS ONE. 8 (7): e69238. Bibcode:2013PLoSO...869238L. doi:10.1371/journal.pone.0069238. PMC 3722293. PMID 23894436.
- ^ Sitas F, Egger S, Urban MI, Taylor PR, Abnet CC, Boffetta P, et al. (January 2012). "InterSCOPE study: Associations between esophageal squamous cell carcinoma and human papillomavirus serological markers". Journal of the National Cancer Institute. 104 (2): 147–158. doi:10.1093/jnci/djr499. PMC 3260131. PMID 22228147.
- ^ Syrjänen K (January 2013). "Geographic origin is a significant determinant of human papillomavirus prevalence in oesophageal squamous cell carcinoma: systematic review and meta-analysis". Scandinavian Journal of Infectious Diseases. 45 (1): 1–18. doi:10.3109/00365548.2012.702281. PMID 22830571. S2CID 22862509.
- ^ Hardefeldt HA, Cox MR, Eslick GD (June 2014). "Association between human papillomavirus (HPV) and oesophageal squamous cell carcinoma: a meta-analysis". Epidemiology and Infection. 142 (6): 1119–1137. doi:10.1017/S0950268814000016. PMC 9151180. PMID 24721187. S2CID 21457534.
- ^ Han Y, Chen W, Li P, Ye J (September 2015). "Association Between Coeliac Disease and Risk of Any Malignancy and Gastrointestinal Malignancy: A Meta-Analysis". Medicine. 94 (38): e1612. doi:10.1097/MD.0000000000001612. PMC 4635766. PMID 26402826.
- ^ Sultan R, Haider Z, Chawla TU (January 2016). "Diagnostic accuracy of CT scan in staging resectable esophageal cancer". JPMA. The Journal of the Pakistan Medical Association. 66 (1): 90–92. PMID 26712189.
- ^ Kim TJ, Kim HY, Lee KW, Kim MS (2009). "Multimodality assessment of esophageal cancer: preoperative staging and monitoring of response to therapy". Radiographics. 29 (2): 403–421. doi:10.1148/rg.292085106. PMID 19325056.
- ^ Bruzzi JF, Munden RF, Truong MT, Marom EM, Sabloff BS, Gladish GW, et al. (November 2007). "PET/CT of esophageal cancer: its role in clinical management". Radiographics. 27 (6): 1635–1652. doi:10.1148/rg.276065742. PMID 18025508.
- ^ Linder G, Korsavidou-Hult N, Bjerner T, Ahlström H, Hedberg J (September 2019). "18F-FDG-PET/MRI in preoperative staging of oesophageal and gastroesophageal junctional cancer". Clinical Radiology. 74 (9): 718–725. doi:10.1016/j.crad.2019.05.016. PMID 31221468. S2CID 80059143.
- ^ Shields TW, LoCicero JW, Reed CE, Feins RH (2009). General Thoracic Surgery. Lippincott Williams & Wilkins. pp. 2047–. ISBN 978-0-7817-7982-1. Archived from the original on 2015-10-25.
- ^ Halperin EC, Perez CA, Brady LW (2008). Perez and Brady's Principles and Practice of Radiation Oncology. Lippincott Williams & Wilkins. pp. 1137–. ISBN 978-0-7817-6369-1. Archived from the original on 2015-10-19.
- ^ 식도와 위의 접합부에서 발생하는 암은 종종 ICD-10에서와 같이 위암으로 분류됩니다.참조:
- ^ Rice TW, Blackstone EH, Rusch VW (March 2010). "A cancer staging primer: esophagus and esophagogastric junction". The Journal of Thoracic and Cardiovascular Surgery. 139 (3): 527–529. doi:10.1016/j.jtcvs.2009.11.002. PMID 20176201.
- ^ Lauby-Secretan B, Scoccianti C, Loomis D, Grosse Y, Bianchini F, Straif K (August 2016). "Body Fatness and Cancer--Viewpoint of the IARC Working Group". The New England Journal of Medicine. 375 (8): 794–798. doi:10.1056/NEJMsr1606602. PMC 6754861. PMID 27557308.
- ^ Qin X, Jia G, Zhou X, Yang Z (December 2022). "Diet and Esophageal Cancer Risk: An Umbrella Review of Systematic Reviews and Meta-Analyses of Observational Studies". Advances in Nutrition. 13 (6): 2207–2216. doi:10.1093/advances/nmac087. PMC 9776643. PMID 36041184.
- ^ Chainani-Wu N (2002). "Diet and oral, pharyngeal, and esophageal cancer". Nutrition and Cancer. 44 (2): 104–126. doi:10.1207/S15327914NC4402_01. PMID 12734057. S2CID 1546319. Archived from the original on 2008-04-30.
- ^ Coleman HG, Murray LJ, Hicks B, Bhat SK, Kubo A, Corley DA, et al. (July 2013). "Dietary fiber and the risk of precancerous lesions and cancer of the esophagus: a systematic review and meta-analysis". Nutrition Reviews. 71 (7): 474–482. doi:10.1111/nure.12032. PMID 23815145.
- ^ a b Zhang Y (September 2013). "Epidemiology of esophageal cancer". World Journal of Gastroenterology. 19 (34): 5598–5606. doi:10.3748/wjg.v19.i34.5598. PMC 3769895. PMID 24039351.
- ^ Dunbar KB, Spechler SJ (July 2014). "Controversies in Barrett esophagus". Mayo Clinic Proceedings. 89 (7): 973–984. doi:10.1016/j.mayocp.2014.01.022. PMID 24867396.
- ^ a b Tobias JS, Hochhauser D (2010). Cancer and its Management (6th ed.). John Wiley & Sons. p. 257. ISBN 978-1118713259.
- ^ Berry 2014, 페이지 S292
- ^ Fernández-Esparrach G, Calderón A, de la Peña J, Díaz Tasende JB, Esteban JM, Gimeno-García AZ, et al. (April 2014). "Endoscopic submucosal dissection". Endoscopy. 46 (4): 361–370. doi:10.1055/s-0034-1364921. PMID 24671864.
- ^ Sun F, Yuan P, Chen T, Hu J (May 2014). "Efficacy and complication of endoscopic submucosal dissection for superficial esophageal carcinoma: a systematic review and meta-analysis". Journal of Cardiothoracic Surgery. 9: 78. doi:10.1186/1749-8090-9-78. PMC 4052291. PMID 24885614.
- ^ a b c d e f g Mendenhall WM, Werning JW, Pfister DG (2011). "Ch Chapter 72: Treatment of head and neck cancer". In DeVita Jr VT, Lawrence TS, Rosenberg SA (eds.). DeVita, Hellman, and Rosenberg's Cancer: Cancer: Principles & Practice of Oncology (9th ed.). Philadelphia, Pa: Lippincott Williams & Wilkins. pp. 729–780. ISBN 978-1-4511-0545-2. 온라인 에디션, 2014년 업데이트 포함
- ^ Berry MF (May 2014). "Esophageal cancer: staging system and guidelines for staging and treatment". Journal of Thoracic Disease. 6 (Suppl 3): S289–S297. doi:10.3978/j.issn.2072-1439.2014.03.11. PMC 4037413. PMID 24876933.
- ^ Parameswaran R, McNair A, Avery KN, Berrisford RG, Wajed SA, Sprangers MA, Blazeby JM (September 2008). "The role of health-related quality of life outcomes in clinical decision making in surgery for esophageal cancer: a systematic review". Annals of Surgical Oncology. 15 (9): 2372–2379. doi:10.1245/s10434-008-0042-8. PMID 18626719. S2CID 19933001.
- ^ Berry 2014, 페이지 S293
- ^ Ross P, Nicolson M, Cunningham D, Valle J, Seymour M, Harper P, et al. (April 2002). "Prospective randomized trial comparing mitomycin, cisplatin, and protracted venous-infusion fluorouracil (PVI 5-FU) With epirubicin, cisplatin, and PVI 5-FU in advanced esophagogastric cancer". Journal of Clinical Oncology. 20 (8): 1996–2004. doi:10.1200/JCO.2002.08.105. PMID 11956258.
- ^ Wang KK, Prasad G, Tian J (September 2010). "Endoscopic mucosal resection and endoscopic submucosal dissection in esophageal and gastric cancers". Current Opinion in Gastroenterology. 26 (5): 453–458. doi:10.1097/MOG.0b013e32833e4712. PMC 3215503. PMID 20703112.
- ^ Polednak AP (May 2003). "Trends in survival for both histologic types of esophageal cancer in US surveillance, epidemiology and end results areas". International Journal of Cancer. 105 (1): 98–100. doi:10.1002/ijc.11029. PMID 12672037. S2CID 6539230.
- ^ "Oesophageal cancer survival statistics". Cancer Research UK. 2015-05-15. Archived from the original on 2014-10-08.
- ^ "Esophageal Cancer Treatment How We Treat Esophageal Cancer KAIZEN Hospital". www.kaizenhospital.com. Retrieved 2021-01-17.
- ^ a b Conteduca V, Sansonno D, Ingravallo G, Marangi S, Russi S, Lauletta G, Dammacco F (August 2012). "Barrett's esophagus and esophageal cancer: an overview". International Journal of Oncology. 41 (2): 414–424. doi:10.3892/ijo.2012.1481. PMID 22615011. Archived from the original on 2013-05-17.
- ^ a b c Napier KJ, Scheerer M, Misra S (May 2014). "Esophageal cancer: A Review of epidemiology, pathogenesis, staging workup and treatment modalities". World Journal of Gastrointestinal Oncology. 6 (5): 112–120. doi:10.4251/wjgo.v6.i5.112. PMC 4021327. PMID 24834141.
- ^ a b c d e Arnold M, Soerjomataram I, Ferlay J, Forman D (March 2015). "Global incidence of oesophageal cancer by histological subtype in 2012". Gut. 64 (3): 381–387. doi:10.1136/gutjnl-2014-308124. PMID 25320104.
- ^ Kachala R (September 2010). "Systematic review: epidemiology of oesophageal cancer in Sub-Saharan Africa". Malawi Medical Journal. 22 (3): 65–70. doi:10.4314/mmj.v22i3.62190. PMC 3345777. PMID 21977849.
- ^ a b "Cancer Facts and Figures 2014" (PDF). American Cancer Society. Archived (PDF) from the original on 29 April 2014. Retrieved 28 April 2014.
- ^ Vega KJ, Jamal MM, Wiggins CL (June 2010). "Changing pattern of esophageal cancer incidence in New Mexico: a 30-year evaluation". Digestive Diseases and Sciences. 55 (6): 1622–1626. doi:10.1007/s10620-009-0918-x. PMC 2882567. PMID 19688596.
- ^ "Incidence and Mortality Rate Trends" (PDF). A Snapshot of Esophageal Cancer. National Cancer Institute. September 2006. Archived from the original (PDF) on 2007-03-16. Retrieved 2007-03-21.
- ^ "Oesophageal cancer statistics". Cancer Research UK. 2015-05-14. Archived from the original on 6 October 2014. Retrieved 3 October 2014.
- ^ "Christopher Hitchens' widow on his death: "God never came up"". www.cbsnews.com. 7 September 2012. Archived from the original on 30 October 2015. Retrieved 11 November 2015.
- ^ "Morrissey Talks Trump, Cancer Diagnosis, TSA Groping With Larry King". Rolling Stone. 2015-08-19. Archived from the original on 9 December 2015. Retrieved 11 November 2015.
- ^ Sun L, Yu S (November 2011). "Meta-analysis: non-steroidal anti-inflammatory drug use and the risk of esophageal squamous cell carcinoma". Diseases of the Esophagus. 24 (8): 544–549. doi:10.1111/j.1442-2050.2011.01198.x. PMID 21539676.
- ^ Frankell AM, Jammula S, Li X, Contino G, Killcoyne S, Abbas S, et al. (March 2019). "The landscape of selection in 551 esophageal adenocarcinomas defines genomic biomarkers for the clinic". Nature Genetics. 51 (3): 506–516. doi:10.1038/s41588-018-0331-5. PMC 6420087. PMID 30718927.
- ^ a b M Naeini M, Newell F, Aoude LG, Bonazzi VF, Patel K, Lampe G, et al. (May 2023). "Multi-omic features of oesophageal adenocarcinoma in patients treated with preoperative neoadjuvant therapy". Nature Communications. 14 (1): 3155. Bibcode:2023NatCo..14.3155M. doi:10.1038/s41467-023-38891-x. PMC 10232490. PMID 37258531.