아테로마
Atheroma| 아테로마 | |
|---|---|
| 기타 이름 | 아테로마타(아테로마타), 아테로마(아테로마타), 아테로마(아테로마타), 플라그 |
 | |
| 경동맥내막절제술 검체의 아테롬성 경화성 플라크.이것은 공통의 내경동맥과 외경동맥으로의 분열을 보여준다. | |
| 전문 | 심장학 |
| 합병증 | 혈전증, 색전증, 아테롬성 동맥경화증 |
| 원인들 | 고지혈증, 고트리글리세리드혈증, 고콜레스테롤혈증 |
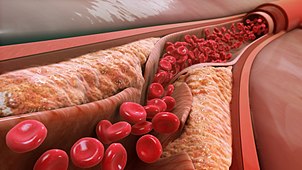
아테로마 또는 아테로마 플라그는 [1][2]동맥벽의 내층에 비정상적이고 가역적인 물질이 축적되는 것입니다.
이 물질은 대부분 지질, 칼슘 및 다양한 양의 섬유 결합 조직을 포함하는 대식세포 [3][4]또는 파편으로 구성됩니다.축적된 물질은 동맥 벽에 붓기를 형성하고 동맥의 내강으로 침입하여 좁아지고 혈류를 제한합니다.아테로마는 동맥경화의 [citation needed]아형인 아테롬성 동맥경화의 병리학적 기반이다.
징후 및 증상
대부분의 사람들에게 첫 번째 증상은 심장 동맥 내의 아테롬 진행에서 비롯되며, 가장 일반적으로 심장마비와 그에 따른 쇠약함을 초래한다.심장 동맥은 (a) 작기 때문에 (약 5mm에서 현미경까지), (b) 가슴 깊숙이 숨겨져 있고 (c) 움직임을 멈추지 않기 때문에 추적하기가 어렵다.또한, 대량 적용된 모든 임상 전략은 (a) 최소 비용과 (b) 시술의 전반적인 안전성 모두에 초점을 맞춘다.따라서, 심폐종을 검출하고 치료에 대한 반응을 추적하기 위한 기존 진단 전략은 매우 제한적이었다.가장 일반적으로 의존하는 방법인 환자 증상과 심장 스트레스 테스트는 동맥이 증가하는 아테로마에 [5]반응하여 수축하는 것이 아니라 확장하기 때문에 아테로마 질환이 매우 진행되기 전까지는 문제의 어떤 증상도 감지하지 못합니다.플라크 파열로 혈류 하류를 방해하는 파편과 응괴가 생성되며, 때로는 국소적으로(혈관 조영술에서 볼 수 있음) 혈류를 감소/정지시킵니다.그러나 이러한 사건들은 갑작스럽게 발생하며 스트레스 테스트나 혈관 [citation needed]조영술에 의해 미리 드러나지 않는다.
메커니즘
건강한 심외 관상동맥은 튜니카 인티마, 미디어,[6][7] 외막의 세 층으로 구성되어 있습니다.아테롬 및 동맥벽의 변화는 일반적으로 내강 직경의 변화 없이 추가 벽 두께를 보상할 수 있을 정도로 작은 동맥류(확대)를 초래합니다.그러나 일반적으로 플라그 위의 내강 내 취약한 플라그와 응괴의 파열로 인해 혈관의 협착(협착)이 일부 영역에서 발생한다.동맥이 너무 많이 확장되어 동맥의 총팽창이 일어난다.세 가지 결과 모두 동일한 [citation needed]개체 내에서 서로 다른 위치에서 관찰되는 경우가 많습니다.
협착 및 폐쇄
시간이 지남에 따라, 아테로마타는 보통 크기와 두께가 진행되며, 동맥의 주변 근육 중심 영역(미디어)이 확장되도록 유도하는데, 이를 리모델링이라고 하며, 일반적으로 동맥 개구부(루멘)의 구경이 동맥벽 횡단부의 50퍼센트 이상이 될 때까지 변하지 않도록 그 크기를 보상하기에 충분하다.nal 영역은 아테로마 [5]조직으로 구성됩니다.
근벽의 확대가 결국 아테로마 부피의 확대를 따라가지 못하거나 플라그 위에 응괴가 형성되어 조직되면 동맥의 내강은 혈류에서 아테로마를 분리하는 조직 위의 반복적인 파열, 응고 및 섬유화의 결과로 좁아진다.이러한 협소함은 수십 년을 산 후에 더 흔해지고, 30대에서 40대가 [citation needed]된 후에 점점 더 흔해진다.
내피(혈관 내부의 세포 단분자층)와 피복 조직인 섬유모자(fiberal cap)는 내강 내 혈액에서 아테로마를 분리합니다.내피와 섬유 캡의 파열(취약 플라크 참조)이 발생하면 플라크의 파편 소나기(5마이크로미터보다 큰 데브리가 모세혈관을 통과하기에는 너무 크다)와 혈소판 및 응고 반응(파열 부위와 파편 모두에 대한 부상/복구 반응)이 일부 부분 내에서 시작된다.둘째, 결국 내강이 좁아지거나 닫히기도 한다.결국 하류 조직 손상은 하류 미세혈관의 폐쇄 또는 폐색 및/또는 파열 시 내강 폐쇄에 의해 발생하며, 둘 다 하류 조직으로의 혈류 손실을 초래한다.이것은 심근경색, 뇌졸중 또는 기타 관련 심혈관 질환의 [citation needed]주요 메커니즘이다.
파열 부위의 응괴는 일반적으로 시간이 지남에 따라 부피가 줄어드는 반면, 일부 응괴는 섬유 조직으로 조직되어 동맥 내강이 좁아질 수 있습니다. 혈관 조영 검사에서 종종 볼 수 있는 협착은 충분히 심하면 혈관 조영 검사에서 볼 수 있습니다.혈관조영법은 일반적으로 200마이크로미터보다 큰 큰 내강만을 나타낼 수 있기 때문에 심혈관 이벤트 후 혈관조영술은 일반적으로 무슨 [citation needed]일이 일어났는지 밝히지 않습니다.
동맥 확장
만약 근육벽의 확대가 시간이 지남에 따라 과다하게 되면 동맥의 대폭적인 확대가 일어나는데, 보통 수십 년 이상 삽니다.이것은 그다지 흔하지 않은 결과입니다.동맥류 확장(혈관 팽만) 내의 아테롬은 또한 파열되어 아테롬과 하류의 응고 잔해를 씻어낼 수 있다.동맥의 확대가 통상 직경의 2~3배까지 계속되면, 벽이 충분히 약해져 맥박의 스트레스만으로 벽의 온전성이 상실되어 갑작스런 출혈(출혈), 주요 증상 및 쇠약함(종종 빠른 사망)이 발생할 수 있습니다.동맥류 형성의 주요 자극은 근육층의 구조적 지지대의 압력 위축이다.주요 구조 단백질은 콜라겐과 엘라스틴이다.이로 인해 [citation needed]대동맥의 복부 영역에서 흔히 볼 수 있듯이 두께가 얇아지고 벽 풍선이 크게 확대됩니다.
조직학
축적은 항상 내피 라이닝과 [citation needed]동맥 벽의 평활근 중간층 사이의 튜니카 내막에 있습니다.
총 외모를 바탕으로 한 초기 단계는 전통적으로 병리학자에 의해 지방줄이라고 불리지만, 지방세포가 아니라 산화 저밀도 리포단백질(LDL)[citation needed]을 흡수하는 백혈구, 특히 대식세포의 축적으로 구성되어 있다.
그들이 다량의 세포질 막을 축적한 후, 그것들은 거품 세포라고 불립니다.거품 세포가 죽으면, 그 내용물이 방출되어 더 많은 대식세포를 끌어당기고 각 아테롬성 동맥경화 [citation needed]플라크의 안쪽 표면에서 중앙 부근에 세포외 지질핵을 형성합니다.
반대로 플라크의 바깥쪽, 오래된 부분은 시간이 [citation needed]지남에 따라 더 석회화되고, 신진대사가 덜 활발해지고, 신체적으로 더 단단해진다.
정맥은 우회수술에서처럼 동맥으로 기능하기 위해 외과적으로 움직이지 않는 한 동맥과 [8]같은 혈류역학적 압력을 받지 않기 때문에 아테로마타가 생기지 않는다.
진단.

동맥벽은 아테롬이 [5]있는 부위에서 확대되기 때문에 사망 전 아테롬을 발견하거나 부검하는 것은 기껏해야 오래 전부터 문제가 있었다.대부분의 방법은 동맥의 개구부에 초점을 맞췄습니다. 이러한 방법들은 매우 관련성이 [citation needed]높지만 동맥 내강 내의 아테로마를 완전히 놓칩니다.
역사적으로 동맥벽 고정, 염색 및 얇은 단면은 사후 및 부검 후 아테로마의 발견과 묘사에 있어 황금 기준이었다.특별한 얼룩과 검사를 통해 미세 석회화를[9] 검출할 수 있으며, 일반적으로 지방 줄무늬가 형성되고 1~2년 이내에 동맥 매체의 평활근 세포 내에서 검출됩니다.
아테롬성 동맥경화증을 검출하기 위한 중재적 방법, 특히 취약한 플라크(비폐쇄성 또는 부드러운 플라크)는 [citation needed]오늘날 연구와 임상 실무에서 널리 사용되고 있다.
경동맥 인티마 미디어 두께 스캔(CIMT는 B 모드 초음파 검사로 측정할 수 있음) 측정은 미국 심장 협회에 의해 아테롬성 동맥 경화증을 식별하는 가장 유용한 방법으로 추천되었으며 현재는 [citation needed]검출의 황금 표준이 될 수 있습니다.
혈관 내 초음파는 현재 살아있는 개인 내에서 더 진행된 아테롬을 감지하고 측정하는 가장 민감한 방법이지만 비용과 신체 [10][11]침윤성으로 인해 응용이 제한적이었다.
최첨단 고해상도 나선형 또는 고속 EBT를 이용한 CT 스캔은 플라크에 존재하는 석회화를 검출하는 가장 효과적인 방법입니다.그러나 CT 스캐너의 소프트웨어가 다른 주변 조직과 구별되는 130 Hounsfield 단위까지 충분히 큰 영역을 형성하려면 상대적으로 큰 석회화 영역이 있을 정도로 아테로마가 진행되어야 합니다.전형적으로, 그러한 부위는 심장의 동맥 내에서 아테로마가 발병하기 시작한 지 약 2~3년 후에 발생하기 시작한다.작고 얼룩덜룩한 플라크의 존재는 사실 급성 [12]심근경색으로 진행되는 데 더 위험할 수 있다.
동맥 초음파, 특히 경동맥의 동맥벽 두께 측정을 통해 질병의 진행을 부분적으로 추적하는 방법을 제공합니다.2006년 현재, 일반적으로 내막-중간 두께에 대해 IMT라고 불리는 두께는 임상적으로 측정되지 않았지만, 1990년대 중반 이후 일부 연구자들에 의해 동맥 벽의 변화를 추적하기 위해 사용되어 왔다.전통적으로 임상 경동맥 초음파는 매우 진행된 질환의 결과인 혈강 제한, 협착 정도를 추정했을 뿐이다.국립보건연구소는 아테롬성 경화성 [citation needed]플라크에 관한 혈관내 초음파 기술을 연구하기 위해 의학 연구원인 케네스 오리엘이 이끄는 5년간 5백만 달러 규모의 연구를 실시했다.보다 진보적인 임상의들은 개별 [citation needed]환자 내에서 질병 진행 또는 안정성을 정량화하고 추적하는 방법으로 IMT 측정을 사용하기 시작했다.
1960년대부터 혈관조영술은 아테롬을 평가하는 전통적인 방법이었습니다.그러나 혈관조영술은 동맥 내강 내의 혈액과 혼합된 염료의 움직임 또는 정지 이미지일 뿐이며 절대 아테로마를 나타내지 않습니다. 동맥벽 내의 아테로마를 포함한 동맥벽은 보이지 않습니다.이 규칙에 대한 제한적인 예외는 벽 내에서 광범위한 석회화와 함께 매우 진행된 아테로마의 경우, 특히 동맥 내강이 끝부분에서 시각화될 때 대부분의 노년층에서 방사선 강도의 후광과 같은 고리를 볼 수 있다는 것이다.시네플로로(cine-floro)에서 심장 전문의와 방사선 전문의는 일반적으로 혈관 [citation needed]조영 중 조영제를 주입하기 전에 이러한 석회화 그림자를 찾아 동맥을 인식합니다.
병변의 분류
- 타입 I: 분리형[6][13] 대식세포
- 타입 II: 복수의 폼 셀층[6][13]
- 타입 III: 전열종, 중간병변[6][13]
- 타입 IV: 아테로마[6][13]
- 타입 V: 섬유열종[6][13]
- 타입 VI: 균열, 궤양, 출혈, 혈전성[6][13] 병변
- 타입 VII: 석회병변[6][13]
- 타입 VII: 섬유화 병변[6][13]
치료
많은 접근법이 아테로마의 [citation needed]진행을 줄이거나[14] 되돌리는 방법으로 추진되어[by whom?] 왔다.
- 생과일, 채소, 견과류, 콩, 딸기 및 [14][15]곡물의 식단 섭취
- 생선, 생선 유래 보충제, 아마씨유, 보라지유 및 기타 비동물성 기름과 같은 오메가3 지방산이 함유된 식품 소비
- 복부 지방 감소
- 유산소 [14]운동
- 콜레스테롤 합성 억제제(스타틴으로 알려져 있음)[14]
- 낮은 정상 혈당치(당화 헤모글로빈, HbA1c라고도 함)
- 미량 영양소(산소, 칼륨 및 마그네슘) 섭취
- 혈압 수준을 정상 또는 건강한 상태로 유지할 것.
- 아스피린 보충제
- 올리고당 2-히드록시프로필-β-시클로덱스트린은 콜레스테롤을 가용화하여 플라크에서[16][better source needed] 제거할 수 있다
연구의 역사
선진국에서는 공중 보건, 감염 관리, 수명 연장으로 인해 아테로마 과정이 사회의 중요한 문제이자 부담이 되고 있다.아테로마타는 1960년대 초반(환자 연령에 맞게 조정됨) 이후 점진적인 개선 추세에도 불구하고 장애와 사망의 주요 기초가 되고 있다.따라서 문제를 더 잘 이해하고, 치료하고, 예방하기 위한 노력이 계속 [citation needed]진화하고 있습니다.
2004년 미국 자료에 따르면 남성의 약 65%와 여성의 47%에서 심혈관 질환의 첫 증상은 심근경색(심근경색) 또는 돌연사(증상 시작 [citation needed]후 1시간 이내 사망)이다.
50% 미만의 내강 협착 위치에서 상당한 비율의 동맥 흐름 중단 이벤트가 발생합니다.전통적으로 혈류 제한에 대해 가장 일반적으로 수행되는 비침습적 검사 방법인 심장 스트레스 검사는 일반적으로 75% 이상의 내강 협착만 감지하지만, 일부 의사들은 때때로 [citation needed]50%만 탐지할 수 있는 핵 스트레스 방법을 옹호한다.
기존의 아테로마의 합병증인 취약한 플라크(비폐쇄성 또는 연성 플라크)의 갑작스러운 성격은 1950년대부터 중환자실의 개발과 복잡한 의료 및 외과적 개입으로 이어졌다.협착을 시각화하거나 간접적으로 감지하기 위해 혈관조영술 및 이후 심장응력 검사가 시작되었습니다.다음으로 정맥, 때로는 동맥, 협착장 주변의 연관을 이식하는 우회수술, 그리고 최근에는 협착장을 [citation needed]더 벌리기 위해 스텐트를 포함한 혈관성형술이 나왔습니다.
그러나 협심증의 증상을 줄이고 혈류를 감소시키는 데 성공함으로써 이러한 의학적 진보에도 불구하고, 무혈종 파열 사건은 여전히 주요 문제로 남아 있으며 오늘날 어디서든 가능한 가장 빠르고, 거대하고, 숙련된 의료 및 외과적 개입에도 불구하고 여전히 갑작스러운 장애와 사망을 야기한다.일부 임상시험에 따르면 바이패스 수술과 혈관성형술 시술은 기껏해야 전반적인 생존을 개선하는 데 최소한의 영향을 끼쳤다.일반적으로 바이패스 수술의 사망률은 1~4%, 혈관성형술의 사망률은 [citation needed]1~1.5%이다.
또한, 이러한 혈관 개입은 종종 질병의 결과로 이미 부분적으로 장애가 있는 증상을 보인 후에만 행해진다.혈관성형술과 우회술이 미래의 심장마비를 [citation needed]예방하지 못한다는 것 또한 분명하다.
제2차 세계대전 이전으로 거슬러 올라가는 오래된 아테로마를 이해하는 방법은 부검 데이터에 의존했다.부검 데이터는 수십 [5]년에 걸쳐 느린 무증상 진행과 함께 늦은 소아기에 지방줄의 시작을 오랫동안 보여 왔다.
아테롬을 볼 수 있는 한 가지 방법은 매우 침습적이고 비용이 많이 드는 IVUS 초음파 기술입니다; 그것은 우리에게 내장의 정확한 부피와 동맥 길이의 약 25 mm (1 in)의 중앙 미디어 층을 제공합니다.안타깝게도 동맥의 구조적 강도에 대한 정보는 없습니다.혈관조영술은 아테로마를 시각화하는 것이 아니라 혈관 내 혈류만 보이게 한다.물리적으로 침습적이지 않거나 개별 테스트당 비용이 적게 드는 대체 방법들이 사용되었고 컴퓨터 단층 촬영(CT; 더 빠른 속도를 감안할 때 전자선 단층 촬영 형태에 의해 주도됨)과 자기 공명 영상(MRI)을 사용하는 방법들과 같이 계속해서 개발되고 있다.1990년대 초반부터 가장 유망한 것은 EBT로, 대부분의 사람들이 임상적으로 인정받은 증상과 쇠약함을 갖기 전에 아테로마 내의 석회화를 감지했다.(콜레스테롤을 낮추기 위한) 스타틴 치료는 CT 스캔을 통해 확인된 석회화 속도를 늦추지 않습니다.MRI 관상동맥 혈관벽 이미징은 현재 연구 연구에 국한되어 있지만,[17] 무증상 고위험 개인에서 혈관벽 비후를 검출할 수 있는 능력을 입증했다.MRI 기반 기법은 비침습적이고 이온화 방사선이 없는 기법으로서 질병의 진행 및 퇴행을 모니터링하는 데 미래에 사용될 수 있다.대부분의 시각화 기법은 연구에 사용되며, 대부분의 환자에게 널리 이용되지 않으며, 상당한 기술적 한계가 있으며, 널리 받아들여지지 않았으며, 일반적으로 의료 보험 [citation needed]사업자의 적용을 받지 않는다.
인간 임상 시험에서 치료의 보다 효과적인 초점은 아테로마의 성장 과정을 [15]늦추고, 멈추고, 심지어 부분적으로 되돌리는 것이라는 것이 점점 더 분명해지고 있다.심혈관 질환이 없는 환자의 심근경색 및 뇌졸중 위험과 직접적인 상관관계를 뒷받침하는 ARIC(Athero sclerosis in community) 연구 및 심혈관 건강 연구(CHS)를 포함한 몇 가지 선행 역학 연구가 있다.ARIC 연구는 1987년부터 1989년까지 미국의 4개 지역에서 5세에서 65세 사이의 15,792명을 대상으로 실시되었다.본 연구에서는 경동맥 B 모드 초음파 검사를 통해 기준 CIMT를 측정하고 4 - 7년 간격으로 측정을 반복했다.CIMT의 증가는 CAD의 위험 증가와 관련이 있습니다.CHS는 1988년에 시작되었으며, CIMT와 심근경색 및 뇌졸중 위험의 관계를 65세 이하의 4,476명을 대상으로 조사하였다.약 6년간의 추적 조사 끝에 CIMT 측정은 심혈관 사건과 [citation needed]관련이 있었다.
아시아 아프리카/중동 및 중남미(PARC-AALA)의 Paroi Artérielle et Risque Cardivasculaire는 또 다른 중요한 대규모 연구로 아시아, 아프리카, 중동, 중남미 79개국의 센터가 참여했으며, CIMT의 다양한 인종 및 골격에 따른 분포도 조사했다.혈관계 점수가 조사되었습니다.다선형 회귀 분석 결과, 증가된 프레이밍햄 심혈관 점수가 [citation needed]CIMT 및 지리적 차이와 무관한 경동맥 플라크와 관련이 있는 것으로 밝혀졌다.
Cahn 등은 6-11개월 동안 경동맥 초음파 검사를 통해 관상동맥 질환 환자 152명을 추적 관찰했으며 이 기간 동안 22개의 혈관 이벤트(심근경색, 일시적인 허혈성 공격, 뇌졸중, 관상혈관 형성)를 기록했다.그들은 이 비간섭적 방법에 의해 측정된 경동맥 아테롬성 동맥 경화증이 관상동맥 [citation needed]환자에게서 예후적 의미를 갖는다는 결론을 내렸다.
로테르담 연구에서, Bots 등은 평균 4.6년 동안 7,983명 > 55세 환자를 추적했고, 이 기간 동안 194건의 심근경색을 보고했다.CIMT는 심근경색 그룹에서 다른 그룹에 비해 유의하게 높았다.Demircan 등은 급성 관상동맥증후군 환자의 CIMT가 안정적인 협심증 [citation needed]환자에 비해 유의미하게 증가했음을 발견했다.
다른 연구에서는 최대 CIMT 값 0.956mm가 혈관조영 CAD를 예측하기 위해 85.7%의 민감도와 85.1%의 특이성을 갖는 것으로 보고되었다.연구 그룹은 안정적인 협심증 증세를 보이는 심장내과 외래 환자들로 구성되었다.연구는 CIMT가 비중대 관상동맥 병변 환자보다 유의한 CAD 환자에서 더 높은 것으로 나타났다.회귀 분석 결과 평균 인티마 미디어 복합체가 1.0 이상 두꺼워지는 것은 환자의 유의한 CAD를 예측할 수 있었다.CIMT는 관상동맥 혈관의 수와 함께 점차적으로 유의한 증가를 보였다.문헌에 따르면 CAD가 존재하는 경우 CIMT가 상당히 높은 것으로 나타났습니다.또한, CIMT는 관련된 혈관의 수가 증가함에 따라 증가했으며 좌심장 주요 관상동맥 관련 환자에서 가장 높은 CIMT 값이 확인되었다.그러나 인간 임상시험은 임상 및 의학적 증거를 제공하는 데 느렸다. 부분적으로는 아테로마타의 무증상적 특성 때문에 연구하기가 특히 어려웠기 때문이다.경동맥내 미디어 두께 스캔(CIMT는 B모드 초음파 검사로 측정 가능), 단백질 부식성을 감소시키고 목 경동맥 플라크 부피와 두께를 감소시키는 B-비타민, 호모시스테인, 뇌졸중을 사용하여 말기 [citation needed]질환에서도 유망한 결과를 얻을 수 있습니다.
또한, 아테로마의 발생을 촉진하는 요인을 이해하는 것은 복잡한데, 그 중 리포단백질, 보다 중요한 리포단백질 아급 분석, 혈당 수치 및 고혈압과 같은 일부만 가장 잘 알려져 연구된다.보다 최근에는 아테로마 진행에 관여하는 염증 대식세포 유발 과정을 촉진하거나 억제하는 복잡한 면역체계 패턴의 일부는 아테롬성 [citation needed]동맥경화의 동물 모델에서 서서히 더 잘 설명되고 있다.
「 」를 참조해 주세요.
레퍼런스
- ^ Lusis, Aldons J. (September 2000). "Atherosclerosis". Nature. 407 (6801): 233–241. doi:10.1038/35025203. PMC 2826222. PMID 11001066.
- ^ Francis, Andrew A; Pierce, Grant N (2011). "An integrated approach for the mechanisms responsible for atherosclerotic plaque regression". Experimental & Clinical Cardiology. 16 (3): 77–86. ISSN 1205-6626. PMC 3209544. PMID 22065938.
- ^ Hotamisligil, Gökhan S (April 2010). "Endoplasmic reticulum stress and atherosclerosis". Nature Medicine. 16 (4): 396–399. doi:10.1038/nm0410-396. PMC 2897068. PMID 20376052.
- ^ Oh, Jisu; Riek, Amy E.; Weng, Sherry; Petty, Marvin; Kim, David; Colonna, Marco; Cella, Marina; Bernal-Mizrachi, Carlos (6 April 2012). "Endoplasmic Reticulum Stress Controls M2 Macrophage Differentiation and Foam Cell Formation". Journal of Biological Chemistry. 287 (15): 11629–11641. doi:10.1074/jbc.M111.338673. PMC 3320912. PMID 22356914.
- ^ a b c d e Glagov, Seymour; Weisenberg, Elliot; Zarins, Christopher K.; Stankunavicius, Regina; Kolettis, George J. (28 May 1987). "Compensatory Enlargement of Human Atherosclerotic Coronary Arteries". New England Journal of Medicine. 316 (22): 1371–1375. doi:10.1056/NEJM198705283162204. PMID 3574413.
- ^ a b c d e f g h i eMedicine의 관상동맥 아테롬성 동맥 경화증
- ^ Waller, Bruce F.; Orr, Charles M.; Slack, John D.; Pinkerton, Cass A.; Van Tassel, James; Peters, Thomas (June 1992). "Anatomy, histology, and pathology of coronary arteries: A review relevant to new interventional and imaging techniques-Part I". Clinical Cardiology. 15 (6): 451–457. doi:10.1002/clc.4960150613. PMID 1617826. S2CID 12034096.
- ^ Zhang, Hongqi; Sun, Aijun; Shen, Yanguo; Jia, Jianguo; Wang, Shijun; Wang, Keqiang; Ge, Junbo (November 2004). "Artery interposed to vein did not develop atherosclerosis and underwent atrophic remodeling in cholesterol-fed rabbits". Atherosclerosis. 177 (1): 37–41. doi:10.1016/j.atherosclerosis.2004.06.019. PMID 15488863.
- ^ Roijers, Ruben B.; Debernardi, Nicola; Cleutjens, Jack P.M.; Schurgers, Leon J.; Mutsaers, Peter H.A.; van der Vusse, Ger J. (June 2011). "Microcalcifications in Early Intimal Lesions of Atherosclerotic Human Coronary Arteries". The American Journal of Pathology. 178 (6): 2879–2887. doi:10.1016/j.ajpath.2011.02.004. PMC 3124018. PMID 21531376.
- ^ Mintz, Gary S.; Nissen, Steven E. (April 2001). "American College of Cardiology Clinical Expert Consensus Document on Standards for Acquisition, Measurement and Reporting of Intravascular Ultrasound Studies (IVUS)". Journal of the American College of Cardiology. 37 (5): 1485. doi:10.1016/S0735-1097(01)01175-5. ISSN 0735-1097. PMID 11300468.
- ^ Tuzcu, E. Murat; Berkalp, Berktan; de Franco, Anthony C.; Ellis, Stephen G.; Goormastic, Marlene; Whitlow, Patrick L.; Franco, Irving; Raymond, Russell E.; Nissen, Steven E. (March 1996). "The Dilemma of Diagnosing Coronary Calcification: Angiography Versus Intravascular Ultrasound". Journal of the American College of Cardiology. 27 (4): 832–838. doi:10.1016/0735-1097(95)00537-4. ISSN 0735-1097. PMID 8613611.
- ^ Ehara, Shoichi; Kobayashi, Yoshiki; Yoshiyama, Minoru; Shimada, Kenei; Shimada, Yoshihisa; Fukuda, Daiju; Nakamura, Yasuhiro; Yamashita, Hajime; Yamagishi, Hiroyuki; Takeuchi, Kazuhide; Naruko, Takahiko; Haze, Kazuo; Becker, Anton E.; Yoshikawa, Junichi; Ueda, Makiko (30 November 2004). "Spotty Calcification Typifies the Culprit Plaque in Patients With Acute Myocardial Infarction: An Intravascular Ultrasound Study". Circulation. 110 (22): 3424–3429. doi:10.1161/01.CIR.0000148131.41425.E9. PMID 15557374. S2CID 11917149.
- ^ a b c d e f g h Stary, Herbert C. (2003). Atlas of atherosclerosis: progression and regression. Parthenon Pub. p. 16. ISBN 978-1-84214-153-3.
- ^ a b c d "Ask the doctor: Reversing atherosclerosis?". Harvard Health. November 2016.
- ^ a b Bodai, Balazs I.; Nakata, Therese E.; Wong, William T.; Clark, Dawn R.; Lawenda, Steven; Tsou, Christine; Liu, Raymond; Shiue, Linda; Cooper, Neil; Rehbein, Michael; Ha, Benjamin P.; McKeirnan, Anne; Misquitta, Rajiv; Vij, Pankaj; Klonecke, Andrew; Mejia, Carmelo S.; Dionysian, Emil; Hashmi, Sean; Greger, Michael; Stoll, Scott; Campbell, Thomas M. (2018). "Lifestyle Medicine: A Brief Review of Its Dramatic Impact on Health and Survival". The Permanente Journal. 22: 17–025. doi:10.7812/TPP/17-025. PMC 5638636. PMID 29035175.
- ^ Zimmer, Sebastian; Grebe, Alena; Bakke, Siril S.; Bode, Niklas; Halvorsen, Bente; Ulas, Thomas; Skjelland, Mona; De Nardo, Dominic; Labzin, Larisa I.; Kerksiek, Anja; Hempel, Chris; Heneka, Michael T.; Hawxhurst, Victoria; Fitzgerald, Michael L.; Trebicka, Jonel; Björkhem, Ingemar; Gustafsson, Jan-Åke; Westerterp, Marit; Tall, Alan R.; Wright, Samuel D.; Espevik, Terje; Schultze, Joachim L.; Nickenig, Georg; Lütjohann, Dieter; Latz, Eicke (6 April 2016). "Cyclodextrin promotes atherosclerosis regression via macrophage reprogramming". Science Translational Medicine. 8 (333): 333ra50. doi:10.1126/scitranslmed.aad6100. PMC 4878149. PMID 27053774.
- ^ Kim, W. Yong; Stuber, Matthias; Börnert, Peter; Kissinger, Kraig V.; Manning, Warren J.; Botnar, René M. (16 July 2002). "Three-Dimensional Black-Blood Cardiac Magnetic Resonance Coronary Vessel Wall Imaging Detects Positive Arterial Remodeling in Patients With Nonsignificant Coronary Artery Disease". Circulation. 106 (3): 296–299. doi:10.1161/01.cir.0000025629.85631.1e. PMID 12119242. S2CID 2294253.
추가 정보
- Ornish, D.; Brown, S.E.; Billings, J.H.; Scherwitz, L.W.; Armstrong, W.T.; Ports, T.A.; McLanahan, S.M.; Kirkeeide, R.L.; Gould, K.L.; Brand, R.J. (July 1990). "Can lifestyle changes reverse coronary heart disease?". The Lancet. 336 (8708): 129–133. doi:10.1016/0140-6736(90)91656-u. PMID 1973470. S2CID 4513736.
- Gould, K. Lance; Ornish, D; Scherwitz, L; Brown, S; Edens, RP; Hess, MJ; Mullani, N; Bolomey, L; Dobbs, F; Armstrong, WT (20 September 1995). "Changes in Myocardial Perfusion Abnormalities by Positron Emission Tomography After Long-term, Intense Risk Factor Modification". JAMA. 274 (11): 894–901. doi:10.1001/jama.1995.03530110056036. PMID 7674504.
- Ornish, Dean; Scherwitz, LW; Billings, JH; Brown, SE; Gould, KL; Merritt, TA; Sparler, S; Armstrong, WT; Ports, TA; Kirkeeide, RL; Hogeboom, C; Brand, RJ (16 December 1998). "Intensive Lifestyle Changes for Reversal of Coronary Heart Disease". JAMA. 280 (23): 2001–7. doi:10.1001/jama.280.23.2001. PMID 9863851. S2CID 21508600.
- Ornish, Dean (November 1998). "Avoiding revascularization with lifestyle changes: the multicenter lifestyle demonstration project". The American Journal of Cardiology. 82 (10): 72–76. doi:10.1016/s0002-9149(98)00744-9. PMID 9860380.
- Dod, Harvinder S.; Bhardwaj, Ravindra; Sajja, Venu; Weidner, Gerdi; Hobbs, Gerald R.; Konat, Gregory W.; Manivannan, Shanthi; Gharib, Wissam; Warden, Bradford E.; Nanda, Navin C.; Beto, Robert J.; Ornish, Dean; Jain, Abnash C. (February 2010). "Effect of Intensive Lifestyle Changes on Endothelial Function and on Inflammatory Markers of Atherosclerosis". The American Journal of Cardiology. 105 (3): 362–367. doi:10.1016/j.amjcard.2009.09.038. PMID 20102949.
- Silberman, Anna; Banthia, Rajni; Estay, Ivette S.; Kemp, Colleen; Studley, Joli; Hareras, Dennis; Ornish, Dean (March 2010). "The Effectiveness and Efficacy of an Intensive Cardiac Rehabilitation Program in 24 Sites". American Journal of Health Promotion. 24 (4): 260–266. doi:10.4278/ajhp.24.4.arb. PMID 20232608. S2CID 25915559.
- Glagov, Seymour; Weisenberg, Elliot; Zarins, Christopher K.; Stankunavicius, Regina; Kolettis, George J. (28 May 1987). "Compensatory Enlargement of Human Atherosclerotic Coronary Arteries". New England Journal of Medicine. 316 (22): 1371–1375. doi:10.1056/NEJM198705283162204. PMID 3574413.