포스폰산염
Phosphonate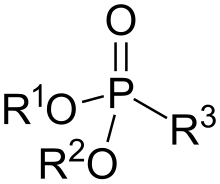
포스포네이트 또는 포스폰산은 C-PO(OH)2 또는 C-PO(OR)2 기(여기서 R = 알킬, 아릴)를 포함하는 유기인 화합물이다.일반적으로 소금으로 취급되는 포스폰산은 일반적으로 유기 용매에는 잘 녹지 않지만 물과 일반 알코올에는 녹는 비휘발성 고체입니다.상업적으로 중요한 많은 화합물은 글리포세이트와 널리 사용되는 식물 성장 조절제인 에테폰을 포함한 포스포네이트이다.비스포네이트는 골다공증 [1]치료에 인기 있는 약이다.
생물학 및 의약화학에서 포스폰산기는 항바이러스성 뉴클레오티드 유사체인 Tenofovir와 같이 항HIV 치료의 주춧돌 중 하나인 인산염의 안정적인 생체 이성질체로 사용된다.그리고 포스폰산 유도체가 "핵의학을 위한 리간드를 약속한다"는 징후가 있다."[2]
기본 속성
포스포네이트는 사면체 인의 중심을 특징으로 한다.그것들은 구조적으로 인산과 [3]밀접하게 관련되어 있다(그리고 종종 그것으로부터 준비된다).
포스폰산염은 디프로톤산인 포스폰산의 탈양성자의 결과물이다.
- RPO(OH)2 + NaOH → HO2 + RPO(OH)(ONA)(포스폰산나트륨)
- RPO(OH)(ONA) + NaOH → HO2 + RPO(ONA)2 (포스폰산나트륨)
포스폰산 에스테르는 포스폰산과 알코올이 응축된 결과입니다.
합성
포스폰산과 그 소금을 제조하기 위한 몇 가지 방법이 있다.
포스폰산
대부분의 과정은 반응성 P-H [1][3]결합을 이용하여 인산(일명 포스폰산, HPO33)으로 시작합니다.
포스폰산은 만니히 조건 하에서 알킬화되어 복합체로 유용한 아미노메틸화 포스폰산염이 생성될 수 있다.한 가지 예는 니트릴로트리스(메틸렌포스폰산)의 공업용 제제이다.
- NH3 + 3 HPO33 + 32 CHO → N(CHPOH232)3 + 3 HO2
포스폰산은 또한 카르복실화 포스폰산을 생성하기 위해 아크릴산 유도체와 함께 알킬화될 수 있다.이 반응은 Michael 추가의 변형입니다.
- CH2=CHCOR2 + 3 HPO33 → (HO)2P(O)CHCOR222
히라오 결합디알킬인산염(포스폰산의 디에스테르로도 볼 수 있음)2은 팔라듐 촉매 결합반응을 할로겐화 아릴과 하여 포스폰산염을 형성한다.
미카엘리스-아르부조프 반응
포스폰 에스터는 미카엘리스-아르부조프 반응을 이용하여 제조된다.예를 들어 요오드화메틸은 트리메틸포스파이트의 포스폰산에스테르디메틸포스폰산으로의 전환을 촉매한다.
- P(OME)3 → MePO(OME)2
이러한 에스테르들은 산(Me = 메틸)으로 가수 분해될 수 있다.
- MePO(OME)2 + HO2 → MePO(OH)2 + 2 Me오호
미카엘리스-베커 반응에서는 먼저 포스폰산수소 디에스테르를 탈양성자화하고 음이온을 알킬화한다.
삼염화인으로부터
비닐포스폰산은 PCl과3 아세트알데히드의 반응으로 제조할 수 있다.
- PCl3 + CHCHO3 → CHCH3(O−) PCL+
3
이 부가물은 아세트산과 반응합니다.
- CHCH3(O−) PCL+
3 + CHCOH 232 → CHCH3(Cl) PO(OH)2 + CHCOCl3 2
이 염화물은 표적을 얻기 위해 탈염소화 과정을 거친다.
- CHCH3(Cl)PO(OH)2 → CH2=CHPO(OH)2 + HCl
Kinnear-Perren 반응에서 알킬포스포닐 이염화물 및 에스터는 삼염화알루미늄의 존재 하에서 삼염화인 알킬화에 의해 생성된다.알킬트리클로로포스포늄염은 다음과 같은 [1]중간체이다.
- PCl3 + RCl + AlCl3 → RPCl+
3 + AlCl−
4
그런+
3 다음 RPCl 생성물을 물로 분해하여 알킬포스폰 이염화물 RP(=O)Cl를2 생성할 수 있다.
반응
가수 분해
포스포네이트 에스터는 일반적으로 산성 및 염기성 조건 모두에서 가수분해되기 쉽습니다.P-C 결합의 분할은 더 어렵지만 공격적인 조건 하에서 이루어질 수 있습니다.
- O=PC(OR)2 + 22 HO → O=PC(OH)2 + 2 ROH
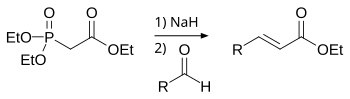
호너-워즈워스-에몬스 반응
Horner-Wadsworth-Emons 반응에서 디알킬포스폰산염은 탈양성자화되어 안정화 카르바니온을 생성하고, 이들 카르바니온은 알데히드와 반응하여 E-알케인을 생성하며 디알킬인산을 [4]제거한다.
구조 서브클래스
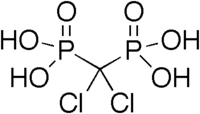
비스포네이트
2개의 쌍둥이자리 포스폰산기를 포함하는 화합물은 비스포네이트로 알려져 있다.그것들은 1897년 폰 바이어와 호프만에 의해 처음 합성되었고, 지금은 골다공증과 유사한 질병을 치료하는데 사용되는 중요한 종류의 약물의 기초를 형성하고 있다.예를 들어 HEDP(에티드론산 또는 디드로넬)는 인산 및 아세트산 [1]무수물로 제조됩니다.
- 233 HPO + (CHCO3)2 O → CHC3(OH)(POH32)2 + CHCOH32
티오포스폰산염
티오포스폰산염기는 황에 산소원자를 치환함으로써 포스포네이트와 관련된 관능기이다.그것들은 많은 살충제와 신경제의 반응성 성분이다.치환된 티오포스폰산염은 O기 또는 S기를 통해 티오네 및 티올을 각각 형성하는 2개의 주요 구조 이성질체 결합을 가질 수 있다.이는 티오카르복실산 및 유기인산염과 같은 관련 기능군과 공유되는 특성이다.
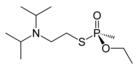
포스포나미다테스
포스포나미데이트는 질소 대신 산소 원자를 치환함으로써 포스포나이트와 관련이 있다.이들은 드물게 볼 수 있는 기능성 그룹이며, 신경작용제인 Tabun이 그 예입니다.
자연발생
포스포네이트는 생물학적 [citation needed]세포에서 인산염 섭취의 세 가지 원천 중 하나이다.다른 두 가지는 무기인산과 유기인산염이다.
자연적으로 발생하는 포스폰산 2-아미노에틸포스폰산은 1959년 식물과 많은 동물에서 처음 확인되었으며, 세포막에 국소화되었습니다.포스포네이트는 원핵생물부터 유박테리아, 버섯, 연체동물, 곤충 등에 이르기까지 다양한 유기체 사이에서 꽤 흔하다.그것들은 뉴먼과 테이트(1980)에 의해 자연 토양에서 처음 보고되었다.천연 포스폰산염의 생물학적 역할은 아직 잘 알려져 있지 않다.비스포네이트 또는 폴리포스폰산염은 자연적으로 발생하는 것으로 밝혀진 바 없다.
항생제 성질을 가진 다수의 천연물 포스폰산 물질이 확인되었다.[5]Phosphonate 자연 제품이 항생제 FDA에 의해non-complicated 요로 감염증의 치료뿐만 아니라 Fosmidomycin(억제제 isoprenyl 합성 효소), acti의 알려지지 않은 모드의 당분 해 효소 enolase,[6]과 물질의 SF-2312(억제제 같은 몇가지 pre-clinically 조사 물질이 승인된 fosfomycin을 포함한다.에예를 들어 alahopcin.포스포네이트는 세포 투과성이 매우 강하지만, 많은 박테리아 종이 포스포네이트 항생제에 의해 납치될 수 있는 글리세롤-3-인산과 포도당-6-인산 수입자를 나타내기 때문에 천연 제품 포스포네이트 항생제는 많은 유기체에 대해 효과적이다.포스포마이신 내성 박테리아 균주는 종종 이러한 운반체를 비활성화하는 돌연변이를 가지고 있다; 하지만, 그러한 돌연변이는 그들이 부과하는 적합성 비용 때문에 항생제가 없으면 유지되지 않는다.
사용하다
1998년 포스폰산염 소비량은 전 세계적으로 5만6천톤으로 미국 4만톤, 유럽 1만5천톤, 일본 800톤 미만이었다.포스폰산염의 수요는 매년 3%씩 꾸준히 증가하고 있다.
금속 킬란트
1949년 게롤트 슈바르첸바흐의 연구 이후 포스폰산은 효과적인 킬레이트제로 알려져 있다.-NH-C-PO2(OH)2를 얻기 위해 분자에 아민기를 도입하면 포스포네이트의 금속 결합 능력이 증가한다.이러한 화합물의 예로는 NTMP, EDTMP 및 DTPMP가 있다.이들 포스포네이트는 EDTA와 같은 잘 알려진 아미노폴리카르본산염과 구조적으로 유사하다.금속 복합체의 안정성은 포스폰산 그룹의 수가 증가함에 따라 증가한다.포스포네이트는 수용성이 매우 높은 반면 포스포네이트는 극소수이다.
포스포네이트는 효과적인 킬레이트제이다.즉, 2가 및 3가 금속 이온에 단단히 결합되어 물의 연화에 유용합니다.이렇게 하면 불용성 침전물(스케일)의 형성을 방지할 수 있다.이러한 리간드의 결합은 또한 금속 이온의 촉매 특성을 억제합니다.그들은 가혹한 조건에서도 안정적입니다.이러한 이유로, 포스포네이트의 중요한 산업적 용도는 냉각수, 담수화 시스템, 그리고 스케일 형성을 억제하기 위한 유전에서이다.포스포네이트는 또한 항칼슘제로 역삼투 시스템에서 정기적으로 사용된다.냉각수 시스템의 포스포네이트는 철과 강철의 부식을 제어하는 역할도 합니다.펄프 및 제지 및 섬유 산업에서 과산화물을 비활성화할 수 있는 킬레이트 금속을 사용하여 "과산화물 표백제" 역할을 합니다.세제에서는 킬레이트제, 스케일 억제제 및 표백 안정제의 조합으로 사용됩니다.포스포네이트는 또한 뼈 형성 및 칼슘 대사와 관련된 질환을 치료하기 위해 의학적으로 점점 더 많이 사용되고 있다.또한 골암 치료에서 방사성핵종의 운반체 역할을 한다(사마륨-153-에틸렌디아민테트라메틸렌포스폰산 참조).
콘크리트 혼화재
포스포네이트는 콘크리트 [7][8]리타더로도 사용된다.시멘트 세팅 시간을 지연시켜 콘크리트를 타설하거나 시멘트 수화열을 장시간 분산시켜 고온과 균열 발생을 방지합니다.또한 양호한 분산 특성을 가지고 있기 때문에 가능한 새로운 종류의 슈퍼 가소성제로 조사되고 있습니다.그러나 현재 포스폰산염은 슈퍼 가소성제로 시판되고 있지 않다.슈퍼 가소성제는 콘크리트의 유동성과 가공성을 높이거나 물 대 시멘트의 비(w/c)를 낮추도록 설계된 콘크리트 혼합제이다.콘크리트 내 수분 함량을 줄임으로써 다공성을 감소시켜 기계적 특성(압축 및 인장 강도)과 콘크리트의 내구성(물, 가스 및 용질 수송 특성 [9]감소)이 개선된다.
약
의학에서는 인산염과 디포스포네이트를 기질로 하는 효소의 억제제로 포스폰산염과 비스포네이트가 일반적으로 사용된다.가장 주목할 만한 것은 이러한 효소들은 콜레스테롤 생합성 [10]중간체를 생성하는 효소들을 포함한다.
테노포비르, 시도포비르, 아데포비르 등의 포스포네이트 뉴클레오티드 유사체는 중요한 항바이러스제이며, 다양한 약물 치료 형태로 HIV, B형 간염 등의 치료에 사용된다.
틈새 용도
유기규산염과 함께, 포스포네이트는 곰팡이 같은 진핵생물 피토프토라 라모룸에 의해 야기되는 "갑작스러운 참나무 죽음"을 치료하는데도 사용된다.
독물학
물에 사는 유기체에 대한 포스포네이트의 독성은 낮다.물고기의 48시간50 LC 값에 대해 보고된 값은 0.1~1.1mM이다.또한 생선의 생물 농도 계수도 매우 낮습니다.
생분해
자연에서 박테리아는 [11]포스폰산염의 분해에 주요한 역할을 한다.환경에 천연 포스폰산염이 존재하기 때문에 박테리아는 포스폰산염을 영양소원으로 대사하는 능력을 발전시켰다.몇몇 박테리아들은 성장을 위한 인 공급원으로 포스포네이트를 사용한다.아미노포스폰산염은 또한 일부 박테리아에 의해 유일한 질소원으로 사용될 수 있다.산업에서 사용되는 폴리포스폰산염은 크기가 훨씬 크고 음전하가 높으며 금속과 복합되어 있기 때문에 2-아미노에틸포스폰산 같은 천연 포스폰산염과는 크게 다릅니다.HEDP와 NTMP를 사용한 도시 하수 처리장의 슬러지에 대한 생분해 테스트에서는 열화 징후가 나타나지 않았다.표준 생분해 테스트에서 HEDP, NTMP, EDTMP 및 DTPMP에 대한 조사에서도 생분해는 발견되지 않았습니다.그러나 일부 시험에서는 높은 슬러지 대 포스폰산비율로 인해 DOC 손실이 관찰된 용액에서 시험물질의 제거가 관찰되었다.이 인자는 생분해보다는 흡착에 기인했다.그러나 P 제한 조건에서 아미노폴리포스폰산염과 HEDP를 분해할 수 있는 박테리아 균주는 토양, 호수, 폐수, 활성 슬러지 및 퇴비에서 분리되었다.
수처리 중 포스포네이트의 생분해는 관찰되지 않지만 Fe(III)-복합체의 광분해는 빠르다.또한 아미노폴리포스폰산염은 Mn(II)의 존재 하에서 빠르게 산화되어 폐수에서 검출된 산소와 안정된 분해물을 형성한다.환경에서의 포스폰산염에 대한 정보 부족은 자연수의 미량 농도에서 포스폰산염 측정의 분석 문제와 관련이 있다.포스포네이트는 주로 천연수에서 Ca와 Mg-복합체로 존재하기 때문에 금속의 사양이나 [12]수송에 영향을 주지 않는다.포스포네이트는 일부 표면과 강하게 상호작용하며, 이는 기술적 및 자연적 시스템에서 상당한 제거를 초래합니다.
포스포네이트 화합물
- 테노포비르 알라페나미드:HIV 치료에 중요한 뉴클레오티드 유사 테노포비르의 프로 약물.
- AMPA : 아미노메틸포스폰산, 글리포세이트 분해물
- 비닐포스폰산: 단량체
- 디메틸메틸포스폰산염(DMMP), 가장 단순한 포스폰산염 다이에스테르 중 하나
- 에티드론산(HEDP): 1-히드록시에틸리덴-1,1-디포스폰산, 세제, 수처리, 화장품 및 의약품에 사용
- ATP : 아미노트리스(메틸렌포스폰산), 킬레이트제
- EDTMP: 에틸렌디아민테트라(메틸렌포스폰산), 킬레이트제
- TDTMP : 테트라메틸렌디아민테트라(메틸렌포스폰산), 킬레이트제
- HDTMP : 헥사메틸렌디아민테트라(메틸렌포스폰산), 킬레이트제
- DTPMP : 디에틸렌트리아민펜타(메틸렌포스폰산), 킬레이트제
- PBTC : 포스포노부탄메트릭카르본산
- PMIDA: N-(포스포노메틸)이미노디아세트산
- CEPA: 2-카르복시에틸포스폰산
- HPAA: 2-히드록시포스포노카르본산
- AMP: 아미노트리스(메틸렌포스폰산)
- BPMG: N, N-비스(포스포노메틸)글리신
- 글리포세이트: 일반적인 농업용 제초제
- 포스카넷: 헤르페스 치료용
- 퍼진포텔: 뇌졸중 치료용
- SF2312: 천연물 엔올라아제 포스폰산 항생제 억제제
- Selfotel: 뇌졸중을 위한 버려진 실험약
「 」를 참조해 주세요.
레퍼런스
- ^ a b c d Wiley-VCH, Wiley-VCH, 2008.doi:10.1002/14356007.19_45pub.2, Weinheim, Weferling, N.; Wefmann, T. "인 화합물, 유기물"에 게재되어 있습니다.
- ^ Pazderová, Lucia; David, Tomáš; Hlinová, Veronika; Plutnar, Jan; Kotek, Jan; Lubal, Přemysl; Kubíček, Vojtěch; Hermann, Petr (2020-06-15). "Cross-Bridged Cyclam with Phosphonate and Phosphinate Pendant Arms: Chelators for Copper Radioisotopes with Fast Complexation". Inorganic Chemistry. 59 (12): 8432–8443. doi:10.1021/acs.inorgchem.0c00856. ISSN 0020-1669. PMID 32437603. S2CID 218834212.
- ^ a b Philippe Savignac과 Bogdan Iorga의 Modern Forsponate Chemistry, CRC Press, Boca Raton, FL, 2003.ISBN 0-8493-1099-7
- ^ Boutagy, John; Thomas, Richard (February 1974). "Olefin synthesis with organic phosphonate carbanions". Chemical Reviews. 74 (1): 87–99. doi:10.1021/cr60287a005.
- ^ Ju KS, Doroghazi JR, Metcalf WW (2014). "Genomics-enabled discovery of phosphonate natural products and their biosynthetic pathways". J. Ind. Microbiol. Biotechnol. 41 (2): 345–356. doi:10.1007/s10295-013-1375-2. PMC 3946943. PMID 24271089.
- ^ Leonard PG, Satani N, Maxwell D, Lin YH, Hammoudi N, Peng Z, Pisaneschi F, Link TM, Lee GR, Sun D, Prasad BA, Di Francesco ME, Czako B, Asara JM, Wang YA, Bornmann W, DePinho RA, Muller FL (December 2016). "SF2312 is a natural phosphonate inhibitor of enolase". Nature Chemical Biology. 12 (12): 1053–1058. doi:10.1038/nchembio.2195. PMC 5110371. PMID 27723749.
- ^ Ramachandran, V. S.; Lowery, M. S.; Wise, T.; Polomark, G. M. (1993). "The role of phosphonates in the hydration of Portland cement". Materials and Structures. 26 (7): 425–432. doi:10.1007/BF02472943. ISSN 0025-5432. S2CID 97857221.
- ^ Collier, Nicholas C.; Milestone, Neil B.; Travis, Karl P.; Gibb, Fergus.G.F. (2016). "The effect of organic retarders on grout thickening and setting during deep borehole disposal of high-level radioactive waste". Progress in Nuclear Energy. 90: 19–26. doi:10.1016/j.pnucene.2016.02.021. ISSN 0149-1970.
- ^ Flatt, R.; Schober, I. (2012). "Superplasticizers and the rheology of concrete". Understanding the Rheology of Concrete. pp. 144–208. doi:10.1533/9780857095282.2.144. ISBN 9780857090287.
- ^ Wiemer, AJ; Hohl, RJ; Wiemer, DF (June 2009). "The intermediate enzymes of isoprenoid metabolism as anticancer targets". Anti-Cancer Agents in Medicinal Chemistry. 9 (5): 526–42. doi:10.2174/187152009788451860. PMID 19519294.
- ^ Huang J, Su Z, Xu Y (November 2005). "The evolution of microbial phosphonate degradative pathways". Journal of Molecular Evolution. 61 (5): 682–90. Bibcode:2005JMolE..61..682H. doi:10.1007/s00239-004-0349-4. PMID 16245012. S2CID 13414302.
- ^ Nowack Bernd (2003). "Environmental chemistry of phosphonates". Water Research. 37 (11): 2533–2546. doi:10.1016/S0043-1354(03)00079-4. PMID 12753831.
추가 정보
- Newman R.H., Tate K.R. (1980). "Soil characterized by 31P nuclear magnetic resonance". Communications in Soil Science and Plant Analysis. 11: 835–842. doi:10.1080/00103628009367083.
- Abhimanyu S. Paraskar & Arumugam Sudalai (2006). "A novel Cu(OTf)2 mediated three component high yield synthesis of α-aminophosphonates" (PDF). Arkivoc (1838EP): 183–9.[영구 데드링크]
- Singh R, Nolan SP (November 2005). "Synthesis of phosphorus esters by transesterification mediated by N-heterocyclic carbenes (NHCs)". Chemical Communications (43): 5456–8. doi:10.1039/b509783e. PMID 16261245.