신장 이식
Kidney transplantation| 신장 이식 | |
|---|---|
 | |
| 기타 이름 | 신장 이식 |
| 전문 | 종양학, 이식학 |
| ICD-10-PCS | OTY |
| ICD-9-CM | 55.6 |
| 메슈 | D016030 |
| OPS-301 코드 | 5-555 |
| 메드라인플러스 | 003005 |
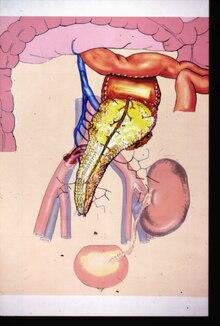
신장 이식 또는 신장 이식은 말기 신장질환(ESRD) 환자에게 신장을 이식하는 것으로, 신장 이식은 일반적으로 기증 장기의 근원에 따라 사망-기증자(기존 사체) 또는 생활-기증자 이식으로 분류된다. 생활-기증자 신장 이식은 기증자와 수령자 사이에 생물학적 관계가 존재하느냐에 따라 유전적으로 관련된(생계 관련) 이식 또는 비관련(생계 관련 없음) 이식 수술로 더욱 특징지어진다.
신장 이식을 받기 전에 ESRD를 받은 사람은 이식을 받을 수 있을 정도로 건강한지 확인하기 위해 철저한 건강 진단을 받아야 한다. 만약 그들이 좋은 후보자로 여겨진다면, 그들은 죽은 기증자로부터 신장을 받기 위해 대기자 명단에 올려질 수 있다.[1] 일단 그들이 대기자 명단에 오르면, 그들은 새로운 신장을 매우 빨리 받을 수 있고, 또는 그들은 많은 시간을 기다려야 할지도 모른다; 미국의 경우, 평균 대기 시간은 3년에서 5년이다.[2] 이식수술 중 신장은 대개 아랫배(아래쪽)에 놓이게 되는데, 사람의 두 토종 신장은 의학적인 사유가 없는 한 보통 꺼내지 않는다.[1]
신장 이식을 받은 ESRD 환자는 일반적으로 투석 중인 ESRD 환자보다 수명이 길며 삶의 질이 더 좋을 수 있다.[1] 그러나 신장이식 수혜자는 신체가 신장을 거부하는 것을 막기 위해 평생 면역억제제(면역계 억제 치료제)를 복용해야 한다.[1] 이러한 장기적 면역억제는 그들을 감염과 암에 걸릴 위험이 더 높다.[3] 신장 이식 거부반응은 세포 거부반응 또는 항체 매개 거부반응으로 분류할 수 있다. 항체 매개 거부반응은 이식 후 발생 기간에 따라 과급성, 급성 또는 만성성으로 분류할 수 있다. 거부반응이 의심되면 신장 조직검사를 받아야 한다.[3] 혈청 크레아티닌과 다른 실험실을 측정하여 정기적으로 신장의 기능을 감시하는 것이 중요하다; 이것은 적어도 3개월마다 한 번씩 그 사람의 남은 생애 동안 이루어져야 한다.[3]
2018년에는 전세계적으로 약 9만5,479개의 신장 이식이 수행되었고, 이 중 36%가 살아있는 기증자로부터 왔다.[4] 최초의 성공적인 신장 이식은 1954년 조셉 머레이에 의해 수행되었다; 머레이는 장기 이식에 대한 그의 업적으로 1990년에 노벨 생리의학상을 받았다.[5]
역사
신장 이식 가능성에 대해 가장 먼저 언급한 것 중 하나는 1907년 시카고 대학의 "병리학의 경과"에 관한 논문을 읽은 미국의 의학 연구자 사이먼 플렉스너에 의한 것으로, 그는 다음과 같은 것을 포함하여, 건강한 장기를 수술에 의해 대체하는 것이 그 당시 미래에도 가능할 것이라고 선언했다.g동맥, 위, 신장, 심장.[6]
1933년 우크라이나의 케르손 출신의 외과의사 유리 보로니는 기증자의 6시간 전에 제거된 신장을 사용하여 허벅지에 다시 이식되는 최초의 인간 신장 이식을 시도했다. 그는 신장과 피부 사이의 연관성을 이용하여 신장 기능을 측정했다. 접종 대상자의 혈액군과 양립할 수 없어 이틀 뒤 첫 환자가 숨졌다.[7]
1950년 6월 17일에야 일리노이주 에버그린 파크의 리틀 컴퍼니 메리 병원의 리처드 롤러[8] 박사에 의해 다낭성 신장질환을 앓고 있는 44세의 여성 루스 터커에게 성공적인 이식수술을 시행하게 되었다. 기증된 신장은 그 당시에는 면역억제 요법이 없었기 때문에 10개월 후에 거부당했지만, 즉 효과적인 방제제의 개발은 몇 년이 지난 후였다. 그 사이에 터커의 남은 신장이 회복될 수 있는 시간을 주었고 그녀는 5년을 더 살았다.[9]
비록 신장이 3주 후에 실패했지만, 살아있는 환자들 사이의 신장 이식은 1952년에 장 햄버거에 의해 파리의 네커 병원에서 시행되었다.[10] 이런 종류의 최초의 진정으로 성공적인 이식수술은 1954년 보스턴에서 일어났다. 1954년 12월 23일 브리검 병원에서 수행된 보스턴 이식은 조셉 머레이, J. 하트웰 해리슨, 존 P. 메릴과 다른 사람들. 그 절차는 일란성 쌍둥이 로날드와 리처드 헤릭 사이에서 이루어졌는데, 이것은 면역 반응의 문제를 줄였다. 이것과 이후의 작업을 위해, 머레이 박사는 1990년에 노벨 의학상을 받았다. 이식받은 리처드 헤릭은 이식 8년 만에 사망했다.[11]
1955년 찰스 롭, 윌리엄 제임스 '짐' 뎀스터(런던 세인트 메리스와 해머스미스)가 영국에서 처음으로 사망한 기증자 이식을 실시했으나 성공하지 못했다.[citation needed] 1959년 7월, '프레드' 피터 래퍼(레즈)가 영국에서 처음으로 성공적인(8개월) 기증자 이식을 수행했다. 1년 후인 1960년에 영국에서 최초로 성공적인 살아있는 신장 이식이 일어났는데, 이때 마이클 우드러프가 에든버러에서 일란성 쌍둥이 사이에서 한 쌍을 수행했다.[12]
1994년 11월 오만 술탄 카부스 대학병원이 세계 최연소 시체성 신장 이식을 성공적으로 수행했다. 이 작업은 33주의 갓난아기에서 22년간 생존한 17개월의 수양생까지(그에게 이식된 장기 커플 덕택)[13] 이뤄졌다.
1964년에 도입된 급성 거부반응을 예방하고 치료하기 위한 약물의 일상적 사용 전까지는 사망한 기증자의 이식이 수행되지 않았다. 신장은 이식하기 가장 쉬운 장기였다. 조직 타이핑은 간단했다. 장기는 비교적 쉽게 제거하고 이식할 수 있었다. 살아있는 기증자는 어려움 없이 사용할 수 있었다. 그리고 실패의 경우, 1940년대부터 신장 투석을 받을 수 있었다.
유전적으로 비식별적인 환자들 사이의 장기 이식의 주요 장벽은 이식된 신장을 '비자체'로 취급하고 즉시 또는 만성적으로 거부하게 되는 수령자의 면역체계에 있었다. 따라서 면역체계를 억제하는 약을 먹는 것이 필수적이었다. 그러나 개인의 면역체계를 억제하면 약의 부작용 외에도 감염과 암(특히 피부암과 림프종)의 위험이 더 크다.
대부분의 면역억제적 요법의 기본은 코르티코스테로이드인 프레드니솔론이다. 프레드니솔론은 면역체계를 억제하지만 장기간 복용하면 포도당 과민증과 당뇨, 체중증가, 골다공증, 근육 약화, 고철혈성혈소판증, 백내장 형성 등 부작용이 속출한다. 프레드니솔론만 해도 이식된 신장의 거부반응을 막기에는 보통 불충분하다. 따라서 다른 비스테로이드 면역억제제가 필요하며, 이는 프레드니솔론(prednisolone)의 저선량도 허용한다. 여기에는 아자티오프린과 미코페놀레이트, 시클로스포린과 타크로리무스가 포함된다.
적응증
신장 이식의 징후는 주된 원인과 관계없이 말기 신장병(ESRD)이다. 이는 15ml/min/1.73m2 미만의 글루머 여과율로 정의된다. ESRD로 이어지는 일반적인 질병은 재생근육 질환, 감염, 당뇨병, 만성 글루머신염과 루푸스와 같은 자가면역 질환을 포함한다. 유전적 원인으로는 다낭성 신장 질환, 선천적인 신진대사 오류 등이 있다. 가장 흔한 '원인'은 특발성(즉, 알 수 없음)이다.
당뇨병은 신장 이식의 가장 흔한 원인으로 미국에서 약 25%를 차지한다. 신장 이식 대상자의 대다수는 이식 당시 투석(복막 투석 또는 혈액 투석)을 받고 있다. 다만, 생활공여자가 있는 만성신장질환자는 투석이 필요하기 전에 사전 이식을 받을 수 있다. 만약 환자가 충분히 일찍 사망한 기증자의 이식 대기자 명단에 올려진다면, 이것은 또한 사전투석도 일어날 수 있다.
규제 및 요구 사항
간 질환과 일부 암은 물론 심장과 폐결핍도 포함된다. 동시에 담배를 피우는 것과 병적인 비만도 수술 합병증의 위험을 높이는 지표 중 하나이다.
신장 이식 요건은 프로그램마다, 국가마다 다르다. 많은 프로그램은 나이에 제한을 두고(예: 대기자 명단에 들어가려면 특정 연령 이하가 되어야 함) 건강(신장 질환으로 인한 것)을 요구한다. 중대한 심혈관질환, 불치병 말기 감염병, 암 등은 이식 제외 기준이 되는 경우가 많다. 또 후보자들은 일반적으로 이식의 생존에 필수적인 약물에 대한 준수 여부를 판단하기 위해 검사를 받는다. 정신질환자 및/또는 중요한 약물 남용 문제를 겪고 있는 사람은 제외될 수 있다.
HIV는 한때 이식에 대한 완전한 금기로 여겨졌다. 면역체계가 고갈된 누군가를 면역억제하면 질병이 진행된다는 두려움이 있었다. 그러나 일부 연구에서는 면역억제제와 항레트로비럴이 시너지 효과를 발휘해 HIV 바이러스 부하/CD4 세포수치를 모두 돕고 적극적인 거부반응을 예방할 수 있을 것으로 보고 있다.
신장의 원천
거부반응을 막기 위한 약물치료가 매우 효과적이기 때문에, 기증자들은 그들의 수혜자들과 비슷할 필요가 없다. 기증된 신장은 대부분 고인이 된 기증자들로부터 나온 것이지만, 미국에서 살아있는 기증자들의 이용은 증가하고 있다. 2006년에는 기증된 신장의 47%가 살아있는 기증자의 것이었다.[14] 이것은 나라마다 다르다: 예를 들어, 스페인에서 2006년에 이식된 신장의 3%만이 살아있는 기증자로부터 왔다.[15] 스페인에서 모든 시민들은 그들이 생전에 명시적으로 탈퇴하지 않는 한, 사망할 경우 장기 기증 가능성이 있는 사람들이다.[16]
생활 기부자
미국, 영국, 이스라엘의 기부금 3건 중 약 1건이 현재 살아있는 기부금에서 나온 것이다.[17][18][19] 잠재적 기증자는 의료 및 심리학적 근거로 세심하게 평가된다. 이것은 기증자가 수술에 적합하고 기증자나 기증자에게 좋지 않은 결과를 초래할 수 있는 과도한 위험이나 가능성을 초래하는 질병이 없음을 보장한다. 심리학적 평가는 기증자가 정보에 근거한 동의를 제공하고 강제되지 않는지 확인하는 것이다. 장기 결제가 불법인 나라에서는, 당국은 기부가 금융 거래에서 비롯된 것이 아니라는 것을 확실히 하기 위해 노력할 수도 있다.
기증자가 받는 사람과 갖는 관계는 수년간 발전해 왔다. 1950년대에 최초의 성공적인 살아있는 기증자 이식은 일란성 쌍둥이 사이의 것이었다. 1960~1970년대에는 살아있는 기증자가 유전적으로 수혜자와 관련이 있었다. 그러나 1980~1990년대에는 기증자 풀이 감정적으로 관련된 개인(스위스, 친구)으로 더욱 확대되었다. 이제 기증자 관계의 탄력성은 지인과 심지어 낯선 사람까지 포함하도록 늘어났다. 2009년 미국의 이식수혜자 크리스 스트러스가 트위터에서 자신과 연결된 기증자로부터 신장을 받았는데, 이는 전적으로 소셜네트워크를 통해 마련된 최초의 이식인 것으로 추정된다.[20][21]
교환과 체인은 살아있는 기증자 풀을 확장하기 위한 새로운 접근법이다. 2012년 2월, 살아있는 기증자 풀을 확장하기 위한 이러한 새로운 접근방식은 미국 신장 등록소에 의해 조직된 60명의 참가자가 참여하는 세계에서 가장 큰 체인을 형성했다.[22] 2014년에 70명의 참가자가 참여한 교환으로 가장 큰 체인 기록을 다시 깼다.[23] 이타적인 기증자의 수용은 이식의 사슬을 형성할 수 있게 되었다. 신장 사슬은 이타적인 기증자가 기꺼이 기증하지만 양립할 수 없는 기증자를 가진 환자에게 신장을 기증할 때 시작된다. 이 양립할 수 없는 기증자는 '앞으로 미루고' 그리고 또한 양립할 수 없는 기증자를 가진 다른 기증자에게 관대함을 전한다. 톨레도 대학의 Michael Rees는 오픈 엔드 체인 개념을 개발했다.[24] 이것은 존스 홉킨스 대학에서 개발된 개념의 변형이었다.[25] 2008년 7월 30일, 이타적 기증자 신장이 상업 항공사를 통해 코넬에서 UCLA로 운송되어 연쇄 이식을 촉발시켰다.[26] 살아있는 기증자의 신장, 컴퓨터 매칭 소프트웨어 알고리즘, 이식 센터 간의 협력으로 긴 호흡 체인이 형성될 수 있게 되었다.[27]
2004년에 FDA는 Cedars-Sinai High Dose IVG 치료를 승인했다. 이 치료법은 살아있는 기증자가 동일한 혈액형(ABO 호환) 또는 심지어 조직 일치일 필요성을 줄여준다.[28][29] 그 치료는 매우 감각적인 환자들에게 기증된 신장을 거부하는 받는 사람의 면역 체계의 발생률을 감소시켰다.[29]
신중하게 선별된 신장 기증자에서는 생존과 말기 신장병의 위험이 일반 인구와 유사한 것으로 보인다.[30] 그러나, 일부 최근의 연구는 비록 절대적인 위험은 여전히 매우 작지만 만성 신장 질환의 평생 위험성이 신장 기증자에게서 몇 배 더 높다는 것을 시사한다.[31]
뉴잉글랜드 의학저널(New England Journal of Medicine of Medicine)의 2017년 기사는 만성 신장질환의 장기적 위험을 줄이기 위해 이식용 신장을 기증한 사람을 포함해 신장 1개만 가진 사람은 고단백 식단을 피하고 단백질 섭취를 1kg당 1g 미만으로 제한해야 한다고 제안했다.[32] 신장을 기증한 여성은 유사한 기준 건강 지표를 가진 일치된 런던 사람보다 임신성 고혈압과 혈압증 위험이 더 높다.[33]
수술 절차
전통적으로 기증자 시술은 4~7인치(10~18cm)의 단일 절개를 거쳤으나 복강경 수술로 라이브 기증이 늘고 있다. 이것은 고통을 줄이고 기증자의 회복을 가속화한다. 수술 시간과 합병증은 외과의사가 150건의 수술을 한 후 현저하게 감소했다. 살아있는 기증자 신장 이식 수술은 사망한 기증자보다 장기 성공률이 더 높다.[34] 복강경 수술 이용이 늘어난 이후 살아있는 기증자가 늘었다. 고통과 흉터 감소와 더 빠른 회복으로 이어지는 어떠한 진전도 기증자 수를 증가시킬 수 있는 잠재력을 가지고 있다. 2009년 1월 뉴저지주 리빙스턴에 위치한 생 바르나바스 메디컬 센터에서 2인치 절개를 통해 첫 번째 전지형 신장 이식이 실시되었다. 이후 6개월 동안 같은 팀이 로봇 보조 이식을 8번 더 수행했다.[35]
2009년 존스홉킨스 메디컬 센터에서 건강한 신장이 기증자의 질을 통해 제거되었다. 질 기부는 회복 속도를 높이고 흉터를 줄이도록 약속한다.[36] 첫 번째 기증자는 그녀가 이전에 자궁 절제술을 받았던 것처럼 선택되었다.[37] 내시경을 오리피스를 통해 삽입한 뒤 내시경을 내부 절개를 통해 외부 흉터가 없도록 천연 오리피스 반투명 내시경 수술을 이용해 추출했다. 배꼽에 하나의 진입점만 있으면 되는 단일 좌현 복강경 검사가 최근 진척된 것도 보다 빈번한 사용 가능성을 가진 또 다른 진척이다.
장기매매
개발도상국에서 어떤 사람들은 그들의 장기를 불법으로 판다. 그런 사람들은 종종 심각한[38] 가난에 빠지거나 판매원들에게 이용당한다. 이러한 신장을 이용하기 위해 여행하는 사람들은 종종 '이식 관광객'으로 알려져 있다. 이러한 관행은 의료인류학자들이 설립한 단체인 오르간 시계(Organ Watch)를 비롯한 다양한 인권단체들이 반대하고 있는데, 이는 불법 국제기관 판매 반지를 노출하는 데 큰 역할을 했다. 이런 환자들은 감염관리 부실과 낮은 의료 및 수술 기준 때문에 합병증을 증가시켰을 수 있다. 한 외과의사는 이러한 관광을 막기 위해 영국에서 장기 무역이 합법화될 수 있다고 말했지만, 국립 신장 연구 기금에서는 이것이 기증자의 적자에 대한 해답으로 보지 않는다.[39]
불법 암시장에서 기증자들은 수술 후 충분한 치료를 받지 못할 수도 있고,[40] 신장 가격은 16만 달러가 넘을 수도 있으며,[41] 중간 상인들은 그 돈의 대부분을 가져가고, 수술은 기증자와 수취인 모두에게 더 위험하며, 구매자는 종종 간염이나 HIV에 걸리기도 한다.[42] 이란의 합법적인 시장에서 신장의 가격은 2천 달러에서 4천 달러다.[42][43]
게리 베커와 훌리오 엘리아스의 '라이브와 시체 장기 기증을 위한 시장에 인센티브를 도입한다'[44]는 기사는 자유시장이 장기 이식의 희소성 문제를 해결하는 데 도움이 될 수 있다고 했다. 그들의 경제 모델링은 인간의 신장(15,000달러)과 인간의 간(32,000달러)의 가격표를 추정할 수 있었다.
조지타운 대학의 제이슨 브레넌과 피터 자우르스키도 장기 시장에 대한 도덕적 반대가 시장에 내재된 것이 아니라 활동 그 자체라고 주장해 왔다.[45]
장기 기증자에 대한 금전적 보상은 호주와 싱가포르에서 호주와 싱가포르에서 합법화되었다.[46][47][48]
기부자
고인의 기증자
사망한 기증자는 두 그룹으로 나눌 수 있다.
- 뇌사(BD) 기증자
- DCD(Cardiac Death) 기증
뇌사(또는 '심장박동') 기증자는 죽은 것으로 간주되지만 기증자의 심장은 계속 펌프질을 하고 순환을 유지한다. 이는 장기들이 여전히 관류(공급된 혈액)되고 있는 동안 외과의사들이 수술을 시작하는 것을 가능하게 한다. 수술하는 동안 대동맥은 식인되고 그 후 기증자의 혈액은 UW(Viaspan), HTK 또는 Perfadex와 같은 얼음냉이 저장 용액으로 대체된다. 어떤 장기를 이식하느냐에 따라 둘 이상의 용액을 동시에 사용할 수도 있다. 용액의 온도 때문에, 그리고 빠른 냉각을 위해 많은 양의 차가운 NaCl-solution이 장기에 쏟아지기 때문에, 심장은 펌핑을 멈출 것이다.
'심장사후 기증' 기증자는 뇌사자 기준을 충족하지 못하지만 회복 가능성이 희박하기 때문에 생계형 의지와 가족을 통해 지원을 철회하도록 선출한 환자들이다. 이 절차에서는 치료가 중단된다(기계 환기가 차단된다). 사망선고가 내려진 후 환자는 장기가 회복되는 수술실로 급히 옮겨진다. 저장 용액은 장기를 통해 플러싱된다. 혈액이 더 이상 순환되지 않기 때문에 헤파린 등 다량의 응고제로 응고를 막아야 한다. 몇 가지 윤리적, 절차적 지침을 준수해야 한다. 가장 중요한 것은 장기 회복 팀이 사망이 선언될 때까지 환자의 치료에 어떤 식으로든 참여해서는 안 된다는 것이다.
기부자 증가
많은 정부들이 기부자의 수를 늘리기 위해 기본적으로 옵트인 시스템인 법률을 통과시켰다.
2015년 12월부터 웨일스 정부가 통과시킨 2013년 인간 이식법(Wales)으로 영국에서 처음으로 장기 기증 옵트아웃 등록이 가능해졌다. 이 법안은 '기증 동의서'로, 모든 시민들이 이 등록부를 선택하지 않는 한 기부자가 되는 것에 반대하지 않는 것으로 간주된다.[49]
호환성.
일반적으로 기증자와 수령자는 ABO 혈액군이어야 하며 교차 일치(인간 백혈구 항원 - HLA)가 적합해야 한다. 만약 잠재적 생존 기증자가 그들의 기증자와 양립할 수 없다면, 기증자는 양립할 수 있는 신장과 교환될 수 있다. "키드니 쌍체 기증" 또는 "체크"로도 알려진 신장 교환이 최근 인기를 얻고 있다.[citation needed]
양립불가능 이식 시 거부반응 위험을 줄이기 위한 노력의 일환으로 정맥내 면역글로불린(IVIG)을 활용한 ABO-비호환성 및 담수화 프로토콜이 개발되었으며, 이를 통해 수혜자가 기증자에게 가질 수 있는 ABO 및 HLA 항체를 감소시킬 수 있다. 2004년에 FDA는 Cedars-Sinai High Dose IVG 치료를 승인했다. 이 치료법은 살아있는 기증자가 동일한 혈액형(ABO 호환) 또는 심지어 조직 일치일 필요성을 줄여준다.[50][29] 그 치료는 매우 감각적인 환자들에게 기증된 신장을 거부하는 받는 사람의 면역 체계의 발생률을 감소시켰다.[29]
1980년대에는 면역억제력 증가와 플라스마페러시스를 이용한 ABO 호환이식에 대한 실험 프로토콜이 개발되었다. 1990년대까지 이러한 기술들이 개선되었고 일본의 장기적 결과에 대한 중요한 연구가 발표되었다.[51] 현재, 전 세계의 많은 프로그램들이 일상적으로 ABO 호환이 불가능한 이식을 수행하고 있다.[52]
기증자 HLA 항원에 대한 감작성 수준은 잠재적 수령자에 대한 패널 반응 항체 검사를 수행하여 결정된다. 미국에서는 모든 기증자 신장 이식의 17%까지 HLA 불일치가 없다. 그러나 HLA 매칭은 이식 결과에 대한 비교적 작은 예측 변수다. 사실, 살아 있는 비관련 기부자들은 이제 거의 생활(유전자적으로) 관련 기부자들만큼 흔하다.[citation needed]
절차
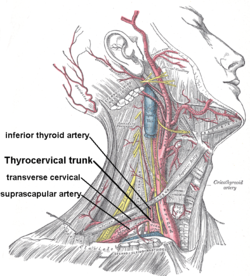
대부분의 경우 거의 기능하지 않는 기존 신장은 제거가 외과적 병증의 비율을 증가시키는 것으로 나타났기 때문에 제거되지 않는다. 따라서 신장은 대개 원래 신장과 다른 위치에 놓이게 된다. 종종 이것은 장골에 있기 때문에 종종 다른 혈액 공급을 사용해야 한다.
- 이전에 기증자의 복부 대동맥에서 분기되었던 신장의 신장동맥은 종종 수령자의 외부 장골동맥과 연결된다.
- 이전에 기증자의 하대정맥으로 배출되었던 신장의 신정맥은 종종 수령자의 외대정맥과 연결된다.
공여 요인은 수혈자 방광과 함께 문합되어 있다. 어떤 경우에는 보다 나은 배수 및 치유가 가능하다는 가정 하에 요관 스텐트가 문합 시간에 배치된다. 그러나, 개타노 치안치오는 변형된 리치-그르고르 기법을 사용하여 더 이상 요관 스텐트를 필요로 하지 않는 기법을 개발하여 스텐트와 관련된 많은 합병증을 피했다.[53]
이식수술을 받을 때 받는 사람의 골반 어느 쪽을 사용할지 외과 교과서에 이견이 있다. 캠벨의 비뇨기과(2002)는 향후 수술이 필요한 경우 신장 골반과 요관이 전방에 있도록 하기 위해 기증자 신장을 수령자의 대측면(즉, 수령자의 우측에 왼쪽 신장을 이식할 것)에 배치할 것을 권고한다. 기증자의 신장을 위한 수령자의 골반에 충분한 공간이 있는지 의심스러운 경우, 교과서는 오른쪽이 재건을 위한 동맥과 정맥의 선택의 폭이 넓기 때문에 오른쪽을 사용할 것을 권고하고 있다.
글렌의 비뇨기과 수술(2004)은 모든 상황에서 신장을 대측면에 놓는 것을 추천한다. 명시적으로 제시된 이유는 없지만, 그 근거가 캠벨의 근거와 유사하다고 가정할 수 있다. 즉, 미래의 수술 교정이 필요할 경우 신장 골반과 요관이 가장 앞쪽에 있음을 확실히 하기 위함이다.
스미스의 비뇨기과(2004)는 받는 사람의 골반 어느 한쪽이 허용될 수 있다고 기술하고 있지만, 올바른 혈관은 서로에 대해 '더 수평적'이므로 문합에서 사용하기 쉽다고 말한다. '더 수평적'이라는 단어가 무엇을 의미하는지 분명하지 않다.
신장-판두 이식
때때로 신장은 췌장과 함께 이식된다. 미네소타 대학의 외과의사 리차드 릴헤이와 윌리엄 켈리는 1966년 세계 최초로 동시 췌장-키드니 이식에 성공했다.[54] 이는 당뇨병이 췌장 베타세포의 파괴로 인한 것으로 당뇨병이 신장 기능 저하(당뇨병 네프로패스)를 일으킨 1형 당뇨병 환자에게서 행해진다. 이것은 거의 항상 죽은 기증자의 이식이다. 살아 있는 기증자(부분적) 췌장 이식은 몇 차례밖에 이뤄지지 않았다. 당뇨병과 신부전을 앓고 있는 개인의 경우, 살아있는 기증자의 조기 이식(가능한 경우)의 이점은 사망한 기증자로부터 신장과 췌장을 결합할 수 있을 때까지 지속적인 투석의 위험보다 훨씬 더 높다.[citation needed] 환자는 살아있는 신장에 이어 나중에 기증자 췌장(PAK 또는 췌장 후 키드니) 또는 기증자로부터 결합된 신장-패트리버(SKP, 동시 신장-패트리버)를 받을 수 있다.
췌장에서 나오는 섬세포만 이식하는 것은 아직 실험 단계에 있지만, 장래성이 있다. 이것은 죽은 기증자 췌장을 가져다가 분해하고 인슐린을 만드는 섬세포들을 추출하는 것을 포함한다. 그리고 나서 세포들은 카테터를 통해 수신자에게 주입되고 그들은 일반적으로 간에서 머무른다. 거부반응을 피하기 위해서는 여전히 면역억제제를 복용해야 하지만 수술은 필요 없다. 대부분의 사람들은 그런 주사를 두세 번 맞아야 하는데, 많은 사람들이 완전히 인슐린이 없는 것은 아니다.
사후작업
이식수술은 약 3시간이 걸린다.[55] 기증된 신장은 하복부에 위치하게 되며 기증자의 신장은 받는 사람의 몸에서 동맥과 정맥과 연결된 혈관에 위치하게 된다. 이것이 완성되면 다시 신장을 통해 피가 흐르게 될 것이다. 마지막 단계는 기증자 신장에서 방광으로 요인을 연결하는 것이다. 대부분의 경우 신장은 곧 오줌을 생산하기 시작할 것이다.
그 품질에 따라, 새 신장은 보통 즉시 기능을 시작한다. 살아있는 기증자의 신장은 보통 정상 작동 수준에 도달하는데 3-5일이 필요한 반면 시체 기증은 그 간격을 7-15일로 늘린다. 입원 기간은 보통 4-10일이다. 합병증이 발생할 경우 신장이 소변을 만들 수 있도록 돕기 위해 추가 약물(이뇨제)을 투여할 수 있다.
면역억제제는 면역체계가 기증된 신장을 거부하지 못하도록 억제하는데 사용된다. 이 약들은 받는 사람의 남은 평생 동안 복용해야 한다. 오늘날 가장 흔한 약물요법은 타크로리무스, 마이코페놀레이트, 프레드니솔론의 혼합물이다. 일부 수혜자는 대신 시클로스포린, 시로리무스 또는 아자티오프린 등을 복용할 수 있다. 이식 후 코르티코스테로이드를 피하거나 회수할 경우 이식된 신장의 조기 거부 위험이 높아진다.[56] 1980년대에 처음 발견되었을 때 획기적인 면역억제제로 여겨졌던 시클로스포린은 아이러니하게도 신독성을 유발하고 새로 이식된 신장에 이아트로겐 손상을 줄 수 있다. 비슷한 약인 타크로리무스도 신독성을 유발한다. 두 가지 모두의 혈중 수치는 면밀히 관찰되어야 하며, 받는 사람이 신장 기능이나 단백뇨가 감소하는 것처럼 보이면, 이것이 거부반응인지, 시클로스포린인지, 타크로리무스 도취 때문인지 결정하기 위해 신장 이식 조직검사가 필요할 수 있다.
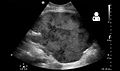
이미징
수술 후 신장은 주기적으로 초음파를 통해 이식 거부반응에 수반되는 영상 및 생리학적 변화를 평가한다. 또한 영상촬영을 통해 아나스토모이식동맥, 정맥, 요인과 같은 지지 구조물을 평가하여 외관상 안정성이 확보된다.
정량적 초음파 평가에서 주요 소노그래픽 척도는 저항성 지수(RI)의 다점 평가로 주 신장 동맥과 정맥에서 시작하여 아큐레이트 혈관에서 끝난다. 다음과 같이 계산한다.
- RI = (피크 수축 속도 – 끝 수축 속도 )/피크 수축 속도
정상 값은 ≈ 0.60이며, 0.70은 정상의 상한이다.[59][60]
이식 후 방사성 동위원소 재생법은 혈관 및 비뇨기학적 합병증의 진단에 사용할 수 있다.[61] 또한 이식 지연 기능의 평가에는 초기 이식 후 재생성 재생술이 사용된다.[62][63]
다이어트
신장 이식 대상자는 자몽, 석류, 녹차 제품 섭취를 자제한다. 이러한 식품들은 특히 타크로리무스, 사이클로스포린, 시로리무스 등 이식 약물과 상호작용을 하는 것으로 알려져 있다. 이러한 약물의 혈중 수치가 증가하여 잠재적으로 과다복용으로 이어질 수 있다.[64]
급성 거부반응은 처음 60일 동안 이식 후 10~25%의 사람들에게 발생한다.[citation needed] 거부반응은 반드시 장기의 손실을 의미하지는 않지만 추가 치료와 약물 조정이 필요할 수 있다.[65]
합병증
이식 후 문제점에는 다음이 포함될 수 있다.
- 출혈, 감염, 혈관 혈전증, 비뇨기 합병증[66] 등 수술 후 합병증
- 이식 거부(고급성, 급성 또는 만성)[66]
- 거부반응 위험을 줄이는 면역억제제로 인한 감염 및 패혈증
- 이식 후 림프구 수축 장애(면역 억제제로 인한 림프종의 일종) 이는 약 2%의 환자에게서 발생하며, 특히 이식[66] 후 처음 2년 동안 발생한다.
- 피부 종양[68]
- 칼슘과 인산염을 포함한 전해질의 불균형으로 뼈에 문제가 생길 수 있음
- 단백뇨[58]
- 고혈압
- 신장 기능 부전의 원래 원인의 재발
- 그 밖에 위·식도의 위장염과 궤양, 치클로스포린을 동반한 히르수티즘(남성형 분포에서의 과도한 모발 성장), 타크로리무스를 동반한 탈모, 비만, 여드름, 당뇨병성 제2형, 고콜로테롤혈증, 골다공증 등의 부작용도 있다.
이식 전 환자의 나이와 건강 상태는 합병증의 위험에 영향을 미친다. 이식센터마다 합병증 관리 성공률이 달라 센터마다 합병증 발생률이 다르다.
죽은 기증자의 신장의 평균 수명은 10년이고, 살아있는 기증자의 신장은 15년이다. 이식이 실패할 경우 환자는 2차 이식을 선택할 수도 있고, 중간 시간 동안 투석으로 돌아가야 할 수도 있다. 소수의 (보통 나이가 많은) 환자들은 투석으로 돌아가지 않고 보조적인 치료(투석이나 이식 불가)로 치료를 받는 것을 선택한다.
신장 이식을 받은 사람에게 사용되는 면역억제제로 인한 감염은 점막 부위(41%), 요로(17%), 호흡기(14%)[69]에서 가장 많이 발생한다. 가장 흔한 감염성 물질은 세균(46%), 바이러스(41%), 곰팡이(13%), 원생동물(1%)[69] 등이다. 바이러스성 질환 중 가장 많이 발생하는 요인은 사람사이토메갈로바이러스(31.5%), 대상포진(23.4%), 대상포진(23.4%)[69] 등이다. BK 바이러스는 이제 이식 위험 인자로 점점 더 인식되고 있다.[70] 감염은 신장 이식을 받은 사람의 약 3분의 1이 사망 원인이며, 폐렴은 감염으로 인한 환자 사망의 50%를 차지한다.[69]
초음파상[71] 신장 이식 후 수술 후 출혈
예후
신장 이식은 생명을 연장하는 과정이다.[72] 일반적인 환자는 신장 이식을 통해 투석을 계속하는 경우보다 10년에서 15년 더 오래 살 것이다.[73] 장수의 증가는 젊은 환자의 경우 더 크지만 75세 수급자(데이터가 있는 가장 오래된 집단)조차 평균 4년 더 많은 수명을 얻게 된다. 사람들은 일반적으로 전통적인 투석을 계속하는 경우보다 더 많은 에너지, 덜 제한적인 식단, 그리고 신장 이식에 따른 합병증을 덜 가지고 있다.[citation needed]
일부 연구에서는 이식 전 투석 기간이 길어질수록 신장이 오래 지속되는 시간이 줄어든다는 연구 결과가 나온 것으로 보인다. 왜 이런 일이 발생하는지는 분명하지 않지만, 이식 프로그램에 대한 신속한 소개가 필요하다는 것을 강조한다. 신장 이식은 환자가 투석을 시작하기 전에 먼저 시행하는 것이 이상적이다. 이식 후 신장이 시간이 흐르면서 고장나는 이유는 최근 몇 년 사이 해명된 바 있다. 원래 신장질환의 재발과는 별개로 거부반응(주로 항체 매개 거부반응)과 진행성 흉터(다발성 흉터)도 결정적인 역할을 한다.[74] 신장이식의 실패를 피하기 위해서는 엄격한 약물 고수에 의한 거부반응을 피하는 것이 가장 중요하다.[citation needed]
적어도 4명의 프로 선수들이 이식 받은 후 그들의 스포츠에 복귀했다. 뉴질랜드 럭비 유니온 선수 조나 로무, 독일-크로아티아 축구 선수 이반 클라스니치, NBA 농구선수 숀 엘리엇과 알론조 모우팅.[citation needed]
살아있는 신장 기증자의 경우, 예측 연구는 일반 인구보다 건강한 사람들 중에서 신장 기증자를 선택하는 선택 편향에 잠재적으로 교란되지만, 해당 건강한 대조군과 일치할 경우 신장 기증자의 전체 장기 사망률에는 차이가 없는 것으로 보인다.[75]
통계
| 나라 | 연도 | 시체 기증자 | 생활공여자 | 총이식 |
|---|---|---|---|---|
| 호주.[76][77] | 2020 | 704 | 182 | 886 |
| 캐나다[78] | 2020 | 1,063 | 396 | 1,459 |
| 프랑스.[79] | 2003 | 1,991 | 136 | 2,127 |
| 이탈리아[79] | 2003 | 1,489 | 135 | 1,624 |
| 일본.[80] | 2010 | 208 | 1276 | 1,484 |
| 스페인[79] | 2003 | 1,991 | 60 | 2,051 |
| 영국[79] | 2020년 4월 ~ 2021년 3월 | 1,836 | 422 | 2,258 |
| 미국[81] | 2020 | 17,583 | 5,234 | 22,817 |
국적 외에도 인종, 성별, 소득에 따라 이식률이 다르다. 장기 투석을 시작하는 환자들을 대상으로 한 연구에 따르면 신장 이식에 대한 사회-기록적 장벽은 환자가 이식 대상에 오르기도 전에 관련이 있는 것으로 나타났다.[82] 예를 들어, 사회-기록 그룹마다 서로 다른 관심을 나타내고 다른 비율로 이식 전 작업을 완료한다. 공정한 이식 정책을 만들기 위한 이전의 노력은 현재 이식 대기자 명단에 있는 환자들에 초점을 맞추었다.
미국의 보건 시스템에서는
이식수혜자는 이식된 신장이 기능하는 한 면역억제제제를 복용해야 한다. 일상적인 면역억제제는 타크로리무스, 마이코페놀레이트, 프레드니솔론이다. 이 약들은 한 달에 1,500달러가 든다. 1999년 미국 의회는 환자가 그렇지 않으면 의료보험에 가입할 수 없는 한 의료보험료를 3년 이상 지불할 수 없도록 제한하는 법안을 통과시켰다. 이식 프로그램은 의료보험 가입이 만료된 후 환자가 약값을 지불할 합리적인 계획이 없는 한 환자를 이식할 수 없다. 그러나, 환자들은 재정적인 이유만으로 거절당하지는 않는다. 말기 신장병 환자의 절반은 메디케어 보장만 받고 있다. 이 조항은 2020년 12월에 폐지되었고, 2023년 1월 1일부터 폐지될 것이다. 메디케어(Medicare)에 가입했거나 시술 당시 메디케어(Medicare)에 지원했던 사람은 이식 후 약물을 평생 보장받을 수 있게 된다.[83]
미국의 장기 이식을 감독하는 장기 공유를 위한 연합 네트워크는 이식 후보자들이 '복수 상장'으로 알려진 관행인 두 개 이상의 이식 센터에 등록할 수 있도록 허용하고 있다.[84] 이러한 관행은 특히 보스턴과 같은 수요가 많은 지역에 거주하는 환자들을 위해 장기이식 대기 시간의 극적인 지리적 차이를 완화시키는 데 효과가 있는 것으로 나타났다.[85][86] 다중 리스트 작성의 관행도 의료진들에 의해 승인되었다.[87][88]
주목할 만한 수신자
참고 항목: 카테고리:신장이식수여자와 장기이식수여부
- 캐나다 패션 평론가 스티븐 코조카루(1970년생)가 ???에 이식을 했다.?와 2005년
- 영국 축구선수[89][90][91] 앤디 콜(1971년생)이 2017년 4월 이식
- 미국 가수 나탈리 콜(1950~2015년)이 2009년 이식(생존 6년)
- 미국 배우 게리 콜먼(1968~2010)이 1차 이식 <5세, 14세 때 2차 이식>(1981년경)[92]
- 영국 여배우 루시 데이비스(1973년생) 1997년 이식
- 미국 축구선수 케니 이즐리(1959년 출생) 1990년 이식수술
- 미국 배우 아론 아이젠버그(1969~2019)가 1986년과 2015년 이식(생존 23년, 4년)
- 데이비드 에어스(1977년생) 캐나다 하키선수 2004년 이식
- 미국 농구선수 숀 엘리엇(1968년생) 1999년 이식
- 셀레나 고메즈(1992년생) 미국 가수 겸 작곡가 겸 배우 2017년 이식
- 미국 포커플레이어 제니퍼 하먼(64년생)이 ???에 이식??와 2004년
- 영국인 예술가 켄 하워드(1932년생)가 2000년 이식
- 미국 여배우 사라 하이랜드(1990년생)가 2012년 이식수술
- 크로아티아 축구선수 이반 클라스니치(1980년 출생) 2007년 이식
- 호주 음악가 겸 배우 지미 리틀(1937–2012), 2004년 이식(생존: 8년)
- 조나 로무(1975~2015), 뉴질랜드 럭비선수 2004년 이식(생존 11년)
- 미국 코미디언 겸 배우 조지 로페즈(1961년생)가 2005년 이식 수술을 받았다.
- 미국 코미디언 겸 배우 트레이시 모건(1968년생)이 2010년 이식수술
- 미국 농구선수 알론조 모우딩(1970년 출생) 2003년 이식
- 호주 사업가 케리 패커(1937~2005) 2000년 이식(생존 5년)
- 1972년 호주 축구선수 겸 활동가인 찰스 퍼킨스(1936~2000년)가 이식(생존: 28년)
- 2002년 미국 음악가 빌리 프레스턴(1946~2006)이식(생존 4년)
- 미국 극작가 닐 사이먼(1927~2018)이 2004년 이식(생존 14년)
- 미국 축구선수 론 스프링스(1956~2011), 2007년 이식(생존: 4년)[citation needed]
- 일본 프로레슬러인 '점보' 츠루타 도모미(1951~2000년)가 2000년 이식(생존 1개월)
- 엘리엇 F. 미국 변호사 케이(Kaye) 미국 소비자제품안전위원회 위원장, 2022년[93] 이식
참고 항목
- 인공신장
- 구르가온 신장 스캔들
- 예수 그리스도인 – 호주 종교 단체로, 많은 구성원들이 낯선 사람에게 신장을 기증했다.
- 간 이식
참고 문헌 목록
- Brook, Nicholas R.; Nicholson, Michael L. (2003). "Kidney transplantation from non heart-beating donors". Surgeon. 1 (6): 311–322. doi:10.1016/S1479-666X(03)80065-3. PMID 15570790.
- Danovitch, Gabriel M.; Delmonico, Francis L. (2008). "The prohibition of kidney sales and organ markets should remain". Current Opinion in Organ Transplantation. 13 (4): 386–394. doi:10.1097/MOT.0b013e3283097476. PMID 18685334.
- El-Agroudy, Amgad E.; El-Husseini, Amr A.; El-Sayed, Moharam; Ghoneim, Mohamed A. (2003). "Preventing Bone Loss in Renal Transplant Recipients with Vitamin D". Journal of the American Society of Nephrology. 14 (11): 2975–2979. doi:10.1097/01.ASN.0000093255.56474.B4. PMID 14569109.
- El-Agroudy, Amgad E.; Sabry, Alaa A.; Wafa, Ehab W.; Neamatalla, Ahmed H.; Ismail, Amani M.; Mohsen, Tarek; Khalil, Abd Allah; Shokeir, Ahmed A.; Ghoneim, Mohamed A. (2007). "Long-term follow-up of living kidney donors: a longitudinal study". BJU International. 100 (6): 1351–1355. doi:10.1111/j.1464-410X.2007.07054.x. ISSN 1464-4096. PMID 17941927. S2CID 32904086.[데드링크]
- Grens, Kerry (9 April 2012). "Living kidney donations favor some patient groups: study". Reuters.
- Gore John L, et al. (2012). "The Socioeconomic Status of Donors and Recipients of Living Unrelated Renal Transplants in the United States". The Journal of Urology. 187 (5): 1760–1765. doi:10.1016/j.juro.2011.12.112. PMID 22425125.
메모들
- ^ a b c d "20 Common Kidney Transplant Questions and Answers". National Kidney Foundation. 26 January 2017. Archived from the original on 21 March 2021. Retrieved 23 March 2021.
- ^ "The Kidney Transplant Waitlist – What You Need to Know". National Kidney Foundation. 10 February 2017. Retrieved 26 March 2021.
- ^ a b c Voora S, Adey DB (June 2019). "Management of Kidney Transplant Recipients by General Nephrologists: Core Curriculum 2019". American Journal of Kidney Diseases. 73 (6): 866–879. doi:10.1053/j.ajkd.2019.01.031. PMID 30981567.
- ^ "International Report on Organ Donation And Transplantation Activities: Executive Summary 2018" (PDF). Global Observatory on Donation and Transplantation. ONT/WHO. October 2020. Archived (PDF) from the original on 21 March 2021. Retrieved 24 March 2021.
- ^ Shrestha B, Haylor J, Raftery A (March 2015). "Historical Perspectives in Kidney Transplantation: An Updated Review". Progress in Transplantation. 25 (1): 64–69. doi:10.7182/pit2015789. PMID 25758803. S2CID 26032497.
- ^ 인간의 심장을 이식하는 5월(.PDF), 뉴욕 타임즈, 1908년 1월 2일
- ^ Matevossian E, Kern H, Hüser N, Doll D, Snopok Y, Nährig J, Altomonte J, Sinicina I, Friess H, Thorban S (Dec 2009). "Surgeon Yurii Voronoy (1895–1961) – a pioneer in the history of clinical transplantation: in Memoriam at the 75th Anniversary of the First Human Kidney Transplantation". Transplant International. 22 (12): 1132–1139. doi:10.1111/j.1432-2277.2009.00986.x. PMID 19874569. S2CID 12087935.
- ^ Stressmarq.com; 인디아토데이.intoday.in; Healthcentral.com (2018년 2월 12일 발표)
- ^ David Petechuk (2006). Organ transplantation. Greenwood Publishing Group. p. 11. ISBN 978-0-313-33542-6.
- ^ Legendre, Ch; Kreis, H. (November 2010). "A Tribute to Jean Hamburger's Contribution to Organ Transplantation". American Journal of Transplantation. 10 (11): 2392–2395. doi:10.1111/j.1600-6143.2010.03295.x. PMID 20977631. S2CID 24674177.
- ^ "Transplant Pioneers Recall Medical Milestone". NPR. 20 December 2004. Retrieved 20 December 2010.
- ^ Hakim, Nadey (2010). Living Related Transplantation. World Scientific. p. 39. ISBN 978-1-84816-497-0.
- ^ Daar, Abdallah S.; Al Lawati, Nabil Mohsin (December 1, 2016). "The World's Youngest Cadaveric Kidney Transplant: Medical, Surgical and Ethical Issues". Transplant Direct. 2 (12 (Article number: e117)): e117. doi:10.1097/TXD.0000000000000631. ISSN 2373-8731. OCLC 8892768132. PMC 5142357. PMID 27990482.
- ^ 장기조달 및 이식 네트워크, 2007
- ^ Nacional de Transplantes (ONT), 2007
- ^ "How Spain became the world leader in organ transplants". The Local. 15 September 2017.
- ^ "How to become an organ donor". The Sentinel. 24 February 2009. Retrieved 19 December 2010.
- ^ 하이빔 주디 시겔 "간과 폐 기증 승인" 새로운 규제는 수십 명에게 희망을 줄 것이다." '예루살렘 포스트', 1995년 5월 9일(가입 필요)
- ^ "국가 데이터 보고서". 장기 조달 및 이식 네트워크(OPTN). 동적. 2013년 10월 22일 회수 (조회 인터페이스에 대한 링크; 카테고리 = 이식, 장기 = 신장 선택, '기부자 유형별 이식' 보고서 링크 선택)
- ^ Kiser, Kim (August 2010). "More than Friends and Followers: Facebook, Twitter, and other forms of social media are connecting organ recipients with donors". Minnesota Medicine. Retrieved 17 October 2014.
- ^ "To Share or Not to Share on Social Media". The Ricki Lake Show. Season 1. Episode 19. 4 October 2014. Event occurs at 29:40. 20th Television. Archived from the original on 2013-08-03. Retrieved 17 October 2014.
- ^ Sack, Kevin (18 February 2012). "60 Lives, 30 Kidneys, All Linked". New York Times.
- ^ Pitts, Byron (15 April 2015). "Changing Lives Through Donating Kidneys to Strangers". ABC News Nightline.
- ^ Rees M. A.; Kopke J. E.; Pelletier R. P.; Segev D. L.; Rutter M. E.; Fabrega A. J.; et al. (2009). "A nonsimultaneous, extended, altruistic-donor chain". The New England Journal of Medicine. 360 (11): 1096–1101. doi:10.1056/NEJMoa0803645. PMID 19279341.
- ^ Montgomery R. A.; Gentry S. E.; Marks W. H.; Warren D. S.; Hiller J.; Houp J.; et al. (2006). "Domino paired kidney donation: a strategy to make best use of live non-directed donation". Lancet. 368 (9533): 419–421. CiteSeerX 10.1.1.576.6386. doi:10.1016/S0140-6736(06)69115-0. PMID 16876670. S2CID 2035816.
- ^ Butt F. K.; Gritsch H. A.; Schulam P.; Danovitch G. M.; Wilkinson A.; Del Pizzo J.; et al. (2009). "Asynchronous, Out-of-Sequence, Transcontinental Chain Kidney Transplantation: A Novel Concept". American Journal of Transplantation. 9 (9): 2180–2185. doi:10.1111/j.1600-6143.2009.02730.x. PMID 19563335. S2CID 26186779.
- ^ Sack, Kevin. (19 February 2012). "60 Lives, 30 Kidneys, All Linked". The New York Times. Retrieved 22 October 2013.
- ^ "Kidney and Pancreas Transplant Center – ABO Incompatibility". Cedars-Sinai Medical Center. Retrieved 12 October 2009.
- ^ a b c d Jordan SC, Tyan D, Stablein D, et al. (December 2004). "Evaluation of intravenous immunoglobulin as an agent to lower allosensitization and improve transplantation in highly sensitized adult patients with end-stage renal disease: report of the NIH IG02 trial". J Am Soc Nephrol. 15 (12): 3256–62. doi:10.1097/01.ASN.0000145878.92906.9F. PMID 15579530.
- ^ Ibrahim, H. N.; Foley, R; Tan, L; Rogers, T; Bailey, RF; Guo, H; Gross, CR; Matas, AJ (2009). "Long-Term Consequences of Kidney Donation". N Engl J Med. 360 (5): 459–46. doi:10.1056/NEJMoa0804883. PMC 3559132. PMID 19179315.
- ^ Muzaale AD, Massie AB, Wang MC, Montgomery RA, McBride MA, Wainright JL, Segev DL (12 February 2014). "Risk of end-stage renal disease following live kidney donation". JAMA. 311 (6): 579–86. doi:10.1001/jama.2013.285141. PMC 4411956. PMID 24519297.
- ^ Kalantar-Zadeh K, Fouque D (2 November 2017). "Nutritional management of chronic kidney disease". N. Engl. J. Med. 377 (18): 1765–1776. doi:10.1056/NEJMra1700312. PMID 29091561. S2CID 27499763.
- ^ Garg, Amit X.; Nevis, Immaculate F.; McArthur, Eric; Sontrop, Jessica M.; Koval, John J.; Lam, Ngan N.; Hildebrand, Ainslie M.; Reese, Peter P.; Storsley, Leroy; Gill, John S.; Segev, Dorry L.; Habbous, Steven; Bugeja, Ann; Knoll, Greg A.; Dipchand, Christine; Monroy-Cuadros, Mauricio; Lentine, Krista L. (2014). "Gestational Hypertension and Preeclampsia in Living Kidney Donors". New England Journal of Medicine. 372 (2): 124–133. doi:10.1056/NEJMoa1408932. ISSN 0028-4793. PMC 4362716. PMID 25397608.
- ^ "Kidney Transplant". National Health Service. 29 March 2010. Retrieved 19 November 2011.
- ^ 새로운 로봇 기술 신장 이식 용이 2009년 8월 4일 웨이백 머신, CBS 뉴스, 2009년 6월 22일 – 2009년 7월 8일에 액세스
- ^ "Donor kidney removed via vagina". BBC News. 3 February 2009. Retrieved 12 October 2009.
- ^ "Surgeons remove healthy kidney through donor's vagina - CNN.com". cnn.com. 3 February 2009. Retrieved 12 October 2009.
- ^ Rohter, Larry (23 May 2004). "The Organ Trade – A Global Black Market – Tracking the Sale of a Kidney On a Path of Poverty and Hope". New York Times. Retrieved 19 December 2010.
- ^ "Call to legalise live organ trade". 19 May 2003 – via news.bbc.co.uk.
- ^ 미트 마켓, 월스트리트 저널, 2010년 1월 8일.
- ^ Martinez, Edecio (27 July 2009). "Black Market Kidneys, $160,000 a Pop". CBS News. Archived from the original on 4 November 2012. Retrieved 12 June 2011.
- ^ a b "Psst, wanna buy a kidney?". Organ transplants. The Economist Newspaper Limited 2011. 16 November 2006. Retrieved 12 June 2011.
- ^ Schall, John A. (May 2008). "A New Outlook on Compensated Kidney Donations". RENALIFE. American Association of Kidney Patients. Archived from the original on 27 September 2011. Retrieved 14 June 2011.
- ^ Gary S. Becker; Julio Jorge Elías. "Introducing Incentives in the Market for Live and Cadaveric Organ Donations" (PDF). New York Times. Retrieved 24 December 2013.
- ^ Comments; Tweet; Like; Submit; Plus (2 November 2015). "If You May Do It for Free, You May Do It for Money". Cato Unbound.
- ^ Plibersek, Tanya (7 April 2013). "Supporting Paid Leave for Living Organ Donors". Retrieved 18 August 2021.
- ^ Bland, B (2008). "Singapore legalises compensation payments to kidney donors". BMJ. 337: a2456. doi:10.1136/bmj.a2456. PMID 18996933. S2CID 38062784.
- ^ "Singapore: Human Organ Transplant Act Amended". Library of Congress. 15 April 2009. Retrieved 19 August 2021.
{{cite web}}: CS1 maint : url-status (링크) - ^ "Organ donation law in Wales". NHS Wales. Retrieved 31 January 2021.
- ^ "Kidney and Pancreas Transplant Center – ABO Incompatibility". Cedars-Sinai Medical Center. Retrieved 12 October 2009.
- ^ "Archived copy" (PDF). Archived from the original (PDF) on 29 May 2008. Retrieved 4 May 2008.
{{cite web}}: CS1 maint: 타이틀로 보관된 사본(링크) - ^ "Overcoming Antibody Barriers to Kidney Transplant". discoverysedge.mayo.edu. Archived from the original on 28 August 2009. Retrieved 20 July 2009.
- ^ Gołębiewska, Justyna; Ciancio, Gaetano; Farag, Ahmed; Gonzalez, Javier; Vincenzi, Paolo; Gaynor, Jeffrey J. (2021). "Results of a previously unreported extravesical ureteroneocystostomy technique without ureteral stenting in 500 consecutive kidney transplant recipients". PLOS ONE. 16 (1): e0244248. Bibcode:2021PLoSO..1644248C. doi:10.1371/journal.pone.0244248. ISSN 1932-6203. PMC 7799771. PMID 33428659.
- ^ David E. R. Sutherland; Rainer W. G. Gruessner; David L. Dunn; Arthur J. Matas; Abhinav Humar; Raja Kandaswamy; S. Michael Mauer; William R. Kennedy; Frederick C. Goetz; R. Paul Robertson; Angelika C. Gruessner; John S. Najarian (April 2001). "Lessons Learned From More Than 1,000 Pancreas Transplants at a Single Institution". Ann. Surg. 233 (4): 463–501. doi:10.1097/00000658-200104000-00003. PMC 1421277. PMID 11303130.
- ^ "Kidney transplant: MedlinePlus Medical Encyclopedia". National Institutes of Health. 22 June 2009. Retrieved 19 December 2010.
- ^ Haller, Maria C.; Royuela, Ana; Nagler, Evi V.; Pascual, Julio; Webster, Angela C. (22 August 2016). "Steroid avoidance or withdrawal for kidney transplant recipients". The Cochrane Database of Systematic Reviews (8): CD005632. doi:10.1002/14651858.CD005632.pub3. hdl:1854/LU-8083451. ISSN 1469-493X. PMID 27546100.
- ^ Nankivell, B (2011). "Diagnosis and prevention of chronic kidney allograft loss". Lancet. 378 (9800): 1428–37. doi:10.1016/s0140-6736(11)60699-5. PMID 22000139. S2CID 33946493.
- ^ a b Naesens (2015). "Proteinuria as a Noninvasive Marker for Renal Allograft Histology and Failure: An Observational Cohort Study". J Am Soc Nephrol. 27 (1): 281–92. doi:10.1681/ASN.2015010062. PMC 4696583. PMID 26152270.
- ^ Krumme, B; Hollenbeck, M (March 2007). "Doppler sonography in renal artery stenosis—does the Resistive Index predict the success of intervention?". Nephrology, Dialysis, Transplantation. 22 (3): 692–6. doi:10.1093/ndt/gfl686. PMID 17192278.
- ^ van de Kuit A, Benjamens S, Sotomayor CG, Rijkse E, Berger SP, Moers C, Bakker SJ, Minnee RC, Yakar D, Pol RA (2020). "Postoperative Ultrasound in Kidney Transplant Recipients: Association Between Intrarenal Resistance Index and Cardiovascular Events". Transplant Direct. 6 (8): e581. doi:10.1097/TXD.0000000000001034. PMC 7581034. PMID 33134505.
- ^ Benjamens S, Berger SP, Glaudemans AW, Sanders JS, Pol RA, Slart RH (2018). "Renal scintigraphy for post-transplant monitoring after kidney transplantation". Transplantation Reviews. 32 (2): 102–109. doi:10.1016/j.trre.2017.12.002. PMID 29395726.
- ^ Benjamens S, Pol RA, de Geus-Oei LF, de Vries AP, Glaudemans AW, Berger SP, Slart RH (2018). "Can transplant renal scintigraphy predict the duration of delayed graft function? A dual center retrospective study". PLOS ONE. 13 (3): e0193791. Bibcode:2018PLoSO..1393791B. doi:10.1371/journal.pone.0193791. PMC 5862448. PMID 29561854.
- ^ Benjamens S, Pol RA, Berger SP, Glaudemans AW, Dibbets-Schneider P, Slart RH, de Geus-Oei LF (2020). "Limited clinical value of two consecutive post-transplant renal scintigraphy procedures". European Radiology. 30 (1): 452–460. doi:10.1007/s00330-019-06334-1. PMC 6890596. PMID 31338652.
- ^ "Transplant Medication Questions". Piedmont Hospital. 13 May 2011. Archived from the original on 17 September 2011. Retrieved 5 June 2011.
- ^ "Kidney transplant". www.webmd.com. Retrieved 20 July 2009.
- ^ a b c Kim, Nancy; Juarez, Roxanna; Levy, Angela D. (October 2018). "Imaging non-vascular complications of renal transplantation". Abdominal Radiology. 43 (10): 2555–2563. doi:10.1007/s00261-018-1566-4. ISSN 2366-004X. PMID 29550956. S2CID 3969029.
- ^ Syu S-H, Lin Y-W, Lin K-H, L-M, 시아오 C-H, Wen Y-C. 패혈증이 있는 신장 이식 환자의 합병증 및 이식 부전의 위험 요인. Bosn J of Basic Med Sci. 2019년 8월.20;19(3):304-11. PMID: 30242808 PMCID: PMC6716102 DOI: 10.17305/bjbms.2018.3874
- ^ Roche CD, Dobson JS, Williams SK, Quante M, Chow J (2014). "Malignant and Noninvasive Skin Tumours in Renal Transplant Recipients". Dermatology Research and Practice. 409058: 409058. doi:10.1155/2014/409058. PMC 4180396. PMID 25302063.
- ^ a b c d 신장 이식 > e메디컬의 신장 이식 합병증. 작성자: Mert Erogul, MD; 편집장: 에릭 슈라가, MD 업데이트: 2008년 12월 5일
- ^ Chong S, Antoni M, Macdonald A, Reeves M, Harber M, Magee CN (July 2019). "BK virus: Current understanding of pathogenicity and clinical disease in transplantation" (PDF). Reviews in Medical Virology. 29 (4): e2044. doi:10.1002/rmv.2044. PMID 30958614. S2CID 102348985.
- ^ a b c d "UOTW #32 - Ultrasound of the Week". Ultrasound of the Week. 8 January 2015. Retrieved 27 May 2017.
- ^ McDonald SP, Russ GR (2002). "Survival of recipients of cadaveric kidney transplants compared with those receiving dialysis treatment in Australia and New Zealand, 1991–2001". Nephrol. Dial. Transplant. 17 (12): 2212–9. doi:10.1093/ndt/17.12.2212. PMID 12454235.
- ^ Wolfe RA, Ashby VB, Milford EL, et al. (1999). "Comparison of Mortality in All Patients on Dialysis, Patients on Dialysis Awaiting Transplantation, and Recipients of a First Cadaveric Transplant". NEJM. 341 (23): 1725–1730. doi:10.1056/nejm199912023412303. PMID 10580071. S2CID 1758680.
- ^ Naesens, M (2014). "The Histology of Kidney Transplant Failure: A Long-Term Follow-Up Study". Transplantation. 98 (4): 427–435. doi:10.1097/TP.0000000000000183. PMID 25243513. S2CID 20703626.
- ^ Morgan, Benjamin R.; Ibrahim, Hassan N. (2019). "Long-term outcomes of kidney donors". Arab Journal of Urology. 9 (2): 79–84. doi:10.1016/j.aju.2011.06.006. ISSN 2090-598X. PMC 4150560. PMID 26579273.
- ^ "2020 deceased organ donation and transplantation". DonateLife. 22 February 2021. Retrieved 19 August 2021.
{{cite web}}: CS1 maint : url-status (링크) - ^ "2020 living organ donation and transplantation". DonateLife. 22 February 2021. Retrieved 19 August 2021.
{{cite web}}: CS1 maint : url-status (링크) - ^ "e-Statistics on organ transplants, waiting lists and donors CIHI". www.cihi.ca. Retrieved 2021-08-19.
- ^ a b c d "Transplant activity report". NHS Organ Donation. Retrieved 2021-08-19.
- ^ "Kidney Transplantation Factbook 2011" (PDF).
- ^ "National Data Reports". The Organ Procurement and Transplant Network (OPTN). Retrieved 19 August 2021.
{{cite web}}: CS1 maint: url-status (링크) (쿼리 인터페이스에 대한 링크; Category = Transplant, Organ = Knodium 선택, 'Transplant by donor type' report 링크 선택) - ^ Alexander, G. C.; Sehgal, A. R. (1998). "Barriers to Cadaveric Renal Transplantation Among Blacks, Women, and the Poor". Journal of the American Medical Association. 280 (13): 1148–1152. doi:10.1001/jama.280.13.1148. PMID 9777814.
- ^ "Expanded Medicare Coverage of Immunosuppressive Drugs for Kidney Transplant Recipients". National Kidney Foundation. 2021-02-05. Retrieved 2021-05-27.
- ^ "Questions & Answers for Transplant Candidates about Multiple Listing and Waiting Time Transfer" (PDF). United Network for Organ Sharing. Archived from the original (PDF) on 8 July 2014. Retrieved 6 March 2015.
- ^ Sommer Gentry (2013). "Addressing Geographic Disparities in Organ Availability" (PDF). Scientific Registry of Transplant Recipients (SRTR). Archived from the original (PDF) on September 4, 2014. Retrieved March 6, 2015.
- ^ Leamanczyk, Lauren (29 November 2014). "I-Team: Professor Helps Organ Transplant Patients On Multiple Waiting Lists". WBZ-TV. Retrieved 30 November 2014.
- ^ Ubel, P. A. (2014). "Transplantation Traffic — Geography as Destiny for Transplant Candidates". New England Journal of Medicine. 371 (26): 2450–2452. doi:10.1056/NEJMp1407639. PMID 25539104.
- ^ Neidich, E.; Neidich, A. B.; Axelrod, D. A.; Roberts, J. P. (2013). "Consumerist Responses to Scarcity of Organs for Transplant". Virtual Mentor. 15 (11): 966–972. doi:10.1001/virtualmentor.2013.15.11.pfor2-1311. PMID 24257089.
- ^ "Former Man United striker Andy Cole undergoes kidney transplant: Club ambassador has a condition called Focal Segmental Glomerulosclerosis". The Irish Times. 7 April 2017. Retrieved 7 April 2017.
- ^ "Andrew Cole: Former Manchester United and England star has kidney op". BBC News. 7 April 2017. Retrieved 7 April 2017.
- ^ Jepson, Anthony (3 September 2017). "Manchester United great Andy Cole thanks two former teammates as he battles to regain full health". Manchester Evening News. Retrieved 6 November 2017.
- ^ "Coleman battled lifelong health woes: transplants, kidney problems - CNN.com". www.cnn.com. Retrieved 27 June 2019.
- ^ Dvorak, Petula (January 10, 2022). "He thought getting a new kidney in the pandemic would be impossible. His son's coach stepped up". The Washington Post. Washington, D.C. Archived from the original on 2022-01-11.