투석(화학)
Dialysis (chemistry)화학에서 투석은 투석 [1]튜브와 같은 반투과성 막을 통한 확산 속도의 차이로 용액 중의 분자를 분리하는 과정이다.
투석은 의료용 투석과 동일한 원리로 작동하는 일반적인 실험실 기술입니다.생명과학 연구의 맥락에서, 투석의 가장 일반적인 적용은 단백질, DNA 또는 [2]다당류와 같은 더 큰 고분자에서 소금, 환원제 또는 염료와 같은 원하지 않는 작은 분자를 제거하는 것입니다.투석은 완충 교환 및 약물 결합 연구에도 일반적으로 사용됩니다.
투석의 개념은 1861년 스코틀랜드의 화학자 토마스 [3]그레이엄에 의해 도입되었다.그는 수용액에서 수크로스(작은 분자)와 아라비아 고무 용질(큰 분자)을 분리하기 위해 이 기술을 사용했다.그는 확산성 용질 결정체와 막 콜로이드를 [4]통과하지 않는 것을 결정체라고 불렀다.
이 개념에서 투석은 용존 이온 또는 반투과성 막을 통해 작은 크기의 분자에서 부유 콜로이드 입자가 자발적으로 분리되는 과정으로 정의할 수 있다.가장 일반적인 투석막은 셀룰로오스, 변형 셀룰로오스 또는 합성 폴리머(셀룰로오스 아세트산 또는 니트로셀룰로오스)[5]로 만들어진다.
어원학
투석은 그리스어로 through를 뜻하는 ιά, and and and와 느슨하게 하다를 뜻하는 ε the the the the the the the the the the the에서 유래한다.[3]
원칙
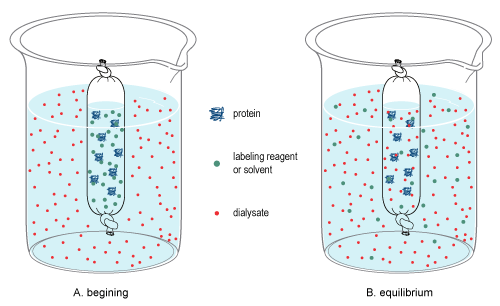
투석은 크기 [6][7]분류에 따라 분자를 구분하여 시료 내 분자의 매트릭스를 변화시키는 과정이다.그것은 확산에 의존하는데, 이것은 용액 내 분자의 무작위적인 열 이동(브라운 운동)으로, 평형에 도달할 때까지 더 높은 농도의 영역에서 낮은 농도로 분자의 순 이동을 이끈다.막의 세공 크기로 인해 시료 내의 큰 분자는 막을 통과할 수 없기 때문에 시료실로부터의 확산이 제한된다.반면, 작은 분자는 막 전체에 자유롭게 확산되어 전체 용액 부피에서 평형을 얻으며, 따라서 시료 및 투석액에서 이러한 분자의 전체적인 농도를 변화시킵니다(오른쪽 투석 그림 참조).
투석을 가능하게 하는 또 다른 원리다.삼투시, 유체는 고농도 영역에서 평형이 될 때까지 반투과성 막을 통해 저농도로 이동한다.투석 시 여분의 유체는 시료와 투석액 사이의 유체 레벨이 같아질 때까지 막을 통해 시료에서 투석액으로 이동합니다.
마지막으로, 외여과란 정수력 또는 삼투압력에 의해 발생하는 압력 구배를 따라 물과 용해된 용질이 대류하는 것을 말한다.투석 시,[6][7] 한외 여과는 시료에서 노폐물 분자와 여분의 액체를 제거합니다.
예를 들어 투석은 셀룰로오스 봉투에 포함된 시료를 투석액에 담글 때 발생한다.투석 중 작은 분자만이 셀룰로오스 막을 통과할 수 있고 큰 입자만 남기 때문에 시료와 투석액 사이의 평형이 달성됩니다.
일단 평형에 도달하면, 분자의 최종 농도는 관련된 용액의 부피에 따라 달라지며, 평형화된 투석액을 새로운 투석액으로 대체(또는 교환)하면(아래 절차 참조), 확산은 샘플의 작은 분자의 농도를 더욱 감소시킬 것이다.
투석은 작은 분자가 양쪽 방향으로 막 위를 자유롭게 이동하기 때문에 시료에서 작은 분자를 도입하거나 제거하는 데 사용될 수 있습니다.투석은 염분을 제거하기 위해 사용될 수도 있다.이를 통해 투석은 다양한 용도에 유용한 기술이 됩니다.투석에 사용되는 반투과성 막의 이력, 특성 및 제조에 대한 자세한 내용은 투석 튜브를 참조하십시오.
종류들
확산 투석
확산 투석은 분리를 일으키는 원동력이 농도 구배인 자발적 분리 과정이다.엔트로피가 증가하고 깁스 자유 에너지가 감소하여 열역학적으로 유리합니다.확산 투석은 분리할 화합물에 따라 음이온 교환막(AEM) 또는 양이온 교환막(CEM)을 사용한다.AEM은 음이온의 통과를 허용하면서도 전기적 중립성을 유지하고 있기 때문에 양이온의 통과를 방해합니다.양이온 [8]교환막에서는 반대의 현상이 발생합니다.
전기 투석
전기투석은 이온교환막과 전위를 원동력으로 사용하는 분리 과정입니다.주로 수용액에서 이온을 제거하는 데 사용됩니다.일반적으로 사용되는 전기 투석 공정은 도난 투석, 역전기 투석, 전기 투석 세 가지가 있습니다.이러한 프로세스에 대해서는,[9] 이하에 대해 설명합니다.
도난 투석
Donnan 투석은 CEM 또는 AEM 막으로 분리된 두 수용액 간에 이온을 교환하는 분리 공정이다.산도가 다른 두 용액을 분리하는 양이온 교환막의 경우 양성자(H+)가 그 막을 통과하여 산도가 낮은 쪽으로 이동한다.이는 산도가 낮은 쪽에 존재하는 양이온의 플럭스를 산도가 높은 쪽으로 유도하는 전위를 유도합니다.분리된 양이온의 농도 [10]차이와 같은 크기의 H 농도의 변화가+ 있을 때 프로세스가 종료된다.
역전기 투석
역전기투석은 염도가 다른 두 물줄기의 혼합으로 전기를 얻는 막에 기반한 기술이다.일반적으로 음이온 교환막(AEM)과 양이온 교환막(CEM)을 사용합니다.AEM은 음이온의 통과를 허용하고 양이온 및 CEM의 통과를 방해하기 위해 사용됩니다.고염도 물 속의 양이온과 음이온은 저염도 물로 이동하며 양이온은 CEM을 통과하고 음이온은 AEM을 통과합니다.이 현상은 [11]전기로 바뀔 수 있다.
전기 투석
전기투석은 전기투석과 전기분해를 결합한 3개의 구획을 이용한 전기막 프로세스입니다.일반적으로 AEM, CEM 및 전기 분해를 사용하여 용액에서 산을 회수하는 데 사용됩니다.3개의 구획은 이온 교환막인 2개의 장벽으로 분리되어 있습니다.가운데 칸에는 처리수가 있습니다.측면에 있는 컴파트먼트에는 깨끗한 물이 들어 있습니다.음이온은 AEM을 통과하고 양이온은 CEM을 통과합니다.이 전기는 음이온 쪽에 H, 양이온− 쪽에 OH를 만들어 각각의+ [9]이온과 반응합니다.
절차.
장비.
투석을 통해 용액 중의 분자를 분리하는 것은 비교적 간단한 과정이다.샘플 버퍼와 투석액 버퍼를 제외하고 일반적으로 필요한 것은 다음과 같습니다.
일반 프로토콜
단백질 검체에 대한 일반적인 투석 절차는 다음과 같습니다.
- 지시사항에 따라 막 준비
- 샘플을 투석 튜브, 카세트 또는 장치에 장착합니다.
- 시료를 투석 완충기의 외부 챔버에 넣습니다(완충기를 부드럽게 저으면서).
- 2시간 동안 투석(실온 또는 4°C)
- 투석 완충제를 교체하고 2시간 동안 투석합니다.
- 투석 완충액 및 투석액을 2시간 또는 밤새 교환합니다.
시료와 투석액의 총 부피는 막 양쪽에 있는 작은 분자의 최종 평형 농도를 결정합니다.적절한 양의 투석액과 여러 개의 완충액을 교환함으로써 시료 내의 작은 오염물질의 농도를 허용치 또는 무시할 수 있는 수준으로 낮출 수 있다.예를 들어 시료 1 mL를 투석액 200 mL에 대하여 투석하면 평형상태가 되면 불필요한 투석물질의 농도가 200배 감소한다.각각 200mL의 버퍼를 두 번 더 변경하면 샘플의 오염물질 수준이6 8 x 10(200 x 200 x 200)만큼 감소합니다.
변수 및 프로토콜 최적화
검체의 투석술은 비교적 간단하지만, 다음과 같은 변수로 인해 모든 용도에 대한 범용 투석 시술이 제공될 수는 없습니다.
- 샘플 볼륨
- 분리되는 분자의 크기
- 사용된 막
- 확산 거리에 영향을 미치는 막의 형상
또한 투석 끝점은 다소 주관적이고 용도에 따라 다르다.따라서 일반적인 절차에서는 최적화가 필요할 수 있습니다.
투석막 및 MWCO
투석막은 분자량 컷오프(MWCO) 한계에 따라 제작 및 특성화됩니다.1-1,000,000kDa 범위의 MWCO를 가진 막이 시판되고 있지만, MWCO가 10kDa에 가까운 막이 가장 일반적으로 사용됩니다.막의 MWCO는 투석막 생산 시 생성되는 모공의 수와 평균 크기에 따른 결과입니다.MWCO는 일반적으로 연장 투석 중 막을 통해 효과적으로 확산되지 않는 표준 분자의 최소 평균 분자량을 말한다.따라서 10K MWCO의 투석막은 일반적으로 최소 분자량이 [12][13]10kDa인 단백질의 90% 이상을 유지한다.
막의 MWCO는 명확하게 정의된 값이 아니라는 점에 유의해야 합니다.막의 MWCO 한계 부근에 질량이 있는 분자는 MWCO보다 훨씬 작은 분자보다 더 느리게 막 전체에 확산됩니다.분자가 막을 통해 빠르게 확산되기 위해서는 일반적으로 막의 MWCO 정격보다 최소 20~50배 작아야 한다.따라서 20K 정격 투석막에서 투석을 사용하여 30kDa 단백질을 10kDa 단백질에서 분리하는 것은 실용적이지 않습니다.
실험실용 투석막은 일반적으로 재생된 셀룰로오스 또는 셀룰로오스 에스테르 필름으로 만들어집니다.셀룰로오스 막 및 [14]제조에 대한 검토는 참조를 참조하십시오.
검사실 투석 형식
투석은 일반적으로 투석 튜브의 클립 백 또는 다양한 형식의 투석기에서 수행됩니다.사용되는 투석 설정의 선택은 검체의 크기와 사용자의 선호도에 따라 크게 달라집니다.투석 튜브는 실험실에서 투석에 사용되는 가장 오래되고 일반적으로 가장 저렴한 형식입니다.튜브는 한쪽 끝을 클립으로 절단하고 밀봉한 다음 다른 한쪽 끝을 클립으로 채우고 밀봉합니다.튜빙은 유연성을 제공하지만 취급, 씰링 및 샘플 회수에 대한 우려가 커졌습니다.투석 튜브는 일반적으로 롤 또는 주름 망원경으로 습식 또는 건조 상태로 공급됩니다.
여러 공급업체에서 다양한 투석 장치(또는 투석기)를 구입할 수 있습니다.투석기는 특정 검체 체적 범위에 맞게 설계되었으며, 튜브를 통한 투석 실험의 향상된 사용 편의성 및 성능을 제공합니다.가장 일반적인 사전 포맷 다이얼라이저는 Slide-A-Lyzer, Float-A-Lyzer 및 Pur-A-Lyzer/D-Tube/GeBAflex Dialyzers 제품군입니다.
적용들
투석은 다양한 용도로 사용됩니다.사용되는 투석의 종류에 따라 두 가지 범주로 나눌 수 있습니다.
확산 투석
확산 투석의 몇 가지 용도는 다음과 같습니다.
- 강한 가성소다 수용액은 확산 투석을 통해 헤미셀룰로오스를 정제할 수 있다.이것은 거의 사용되지 않는 비스코스 프로세스에만 해당됩니다.이 과정의 첫 번째 단계는 거의 순수한 셀룰로오스(면 린터 또는 용해 펄프)를 수산화나트륨(원인성 소다)의 강한 용액(17~20% w/w)으로 처리하는 것입니다.이 공정의 한 가지 효과는 반미셀룰로스(저MW 폴리머)를 용해시키는 것이다.경우에 따라서는 가능한 한 많은 헤미셀룰로오스를 프로세스에서 제거하는 것이 바람직하며,[15][16][17] 이는 투석을 사용하여 수행할 수 있다.
- 산은 음이온 교환막을 사용하여 수용액에서 회수할 수 있습니다.그 과정은 산업 폐수의 대체 처리이다.혼합산(HF+ HNO3), HSO24+ CuSO4 및 HSO24+ ZnSO에서의4 Zn2+ 및2+ Cu의 회수 및 농도, 다이아몬드 제조 [4]공정에서 생성되는 Fe 및 Ni 이온을 포함한 폐황산 용액으로부터의 HSO24 회수 등에 사용된다.
- 알칼리 폐기물은 에너지 비용이 낮아 확산 투석을 통해 회수할 수 있다.NaOH 베이스는 일본 [8]Astom Corporation이 개발한 기술을 적용한 알루미늄 식각 용액에서 회수할 수 있습니다.
- 맥주의 탈알코올화는 확산 투석의 또 다른 응용 분야이다.이 기술에 농도 구배를 적용하면 알코올과 기타 소분자 화합물이 고농도에서 저농도인 물로 막을 통과합니다.이 용도는 낮은 작동 조건과 [18]알코올을 0.5%까지 제거할 수 있는 가능성에 사용됩니다.
전기 투석
전기 투석의 몇 가지 용도는 아래에 설명되어 있습니다.
- 유장의 담수화술은 식품 산업에서 이런 종류의 투석술에 가장 많이 사용되는 분야이다.케이크, 빵, 아이스크림, 이유식과 같은 다양한 음식을 생산하기 위해서는 칼슘, 인, 그리고 다른 무기 염분을 함유한 생치즈 유장을 제거하는 것이 필요하다.유청 탈염의 한계는 거의 90%[19]이다.
- 포도, 오렌지, 사과, 레몬 등의 과일 주스의 제산 작용은 전기 투석이 적용되는 과정이다.음이온 교환막은 주스로부터 구연산 이온을 추출해 수산화 [19]이온으로 치환하는 것을 암시하는 이 기술에 이용된다.
- 간장의 탈염은 전기 투석을 통해 할 수 있다.양조 간장의 염분 함량은 약 16~18%로 상당히 높다.전기투석은 간장에 존재하는 염분의 양을 줄이기 위해 사용된다.요즘 [19]사회에서는 염분이 적은 식단이 매우 보편화되어 있다.
- 전기투석은 아미노산을 산성, 염기성, 중성 그룹으로 분리할 수 있게 해준다.구체적으로는 전기투석을 하는 알팔파 잎에서 세포질 잎 단백질을 추출한다.단백질이 변성되면 용액은 (K 이온의+) 탈염되고 H [19]이온으로 산성화될+ 수 있습니다.
장점과 단점
투석은 장점과 단점을 모두 가지고 있다.이전 섹션의 구조에 따라 사용된 투석 유형에 따라 장단점을 논의합니다.확산 투석과 전기 투석의 장점과 단점은 다음과 같습니다.
확산 투석
확산 투석의 주요 장점은 장치의 에너지 소비량이 낮다는 것입니다.이 막 기술은 정상 압력 하에서 작동하며 상태 변화는 없습니다.이것에 의해, 필요한 에너지가 큰폭으로 삭감되어 운용 코스트를 삭감할 수 있다.또한 설치 비용이 저렴하고 조작이 용이하며 프로세스의 안정성과 신뢰성이 우수합니다.확산 투석이 환경을 [8]오염시키지 않는 것도 장점이다.
확산 투석기는 처리능력이 낮고 처리효율이 낮은 것이 단점이다.확산 [8]투석보다 더 나은 효율성을 달성할 수 있는 전기 투석 및 역삼투석 같은 다른 방법이 있습니다.
전기 투석
전기 투석의 주된 장점은 높은 회복력, 특히 물 회복력이다.또 다른 장점은 고압이 가해지지 않는다는 점인데, 이는 반칙 효과가 크지 않기 때문에 이에 대항하기 위해 화학물질이 필요하지 않다는 것을 의미합니다.또한 오염층이 콤팩트하지 않아 회수율이 높고 막수명이 길다.70,000ppm 이상의 농도에 대한 처리로 농도 한계를 제거하는 것도 중요합니다.마지막으로, 비상변화로 인해 작동에 필요한 에너지가 낮습니다.실제로 MED(Mechanical Vapor Compression) 공정 및 MVC([20]Mechanical Vapor Compression) 공정에서 필요한 것보다 낮다.
전기 투석의 주요 단점은 전류 밀도 한계이며, 프로세스는 허용되는 최대값보다 낮은 전류 밀도로 작동해야 합니다.사실 일정한 전압이 인가되면 이온의 막 내 확산은 물의 해리로 이어지지 않으며, 이는 작동의 효율성을 떨어뜨릴 수 있습니다.고려해야 할 또 다른 측면은 작동에 낮은 에너지가 필요하지만 염분 공급 농도가 높을수록 필요한 에너지가 더 높아진다는 것입니다.마지막으로 일부 제품의 경우 전기투석이 미생물 및 유기오염물질을 제거하지 못하기 때문에 후처리가 필요하다.[20]
「 」를 참조해 주세요.
레퍼런스
- ^ Reed, R (2007). Practical Skills in Biomolecular Sciences (3rd ed.). Essex: Pearson Education Limited. p. 379. ISBN 978-0-13-239115-3.
- ^ Berg, JM (2007). Biochemistry (6th ed.). New York: W.H. Freeman and Company. p. 69. ISBN 978-0-7167-8724-2.
- ^ a b Chisholm, Hugh, ed. (1911). . Encyclopædia Britannica. Vol. 8 (11th ed.). Cambridge University Press. p. 157.
- ^ a b Stancheva, K.A. (2008). "Applications of dialysis". Oxidation Communications 31. 4: 758–775.
- ^ Ninfa, A.J.; Ballou, D. P.; Benore, M. (2009). Fundamental Laboratory Approaches for Biochemistry and Biotechnology. p. 45. ISBN 978-0-470-08766-4.
- ^ a b "What is dialysis?".
- ^ a b "What is dialysis and how does dialysis work?".
- ^ a b c d Luo, J.; Wu, C.; Xu, T.; Wu, Y. (2011). "Diffusion dialysis-concept, principle and applications". Journal of Membrane Science. 366 (1–2): 1–16. doi:10.1016/j.memsci.2010.10.028.
- ^ a b Luis, P. (2018). Fundamental Modeling of Membrane Systems: Membrane and Process Performance. Elsevier. pp. 275–292. ISBN 978-0-12-813483-2.
- ^ Scott, K. (1995). Handbook of Industrial Membranes. Kidlington: Elsevier Advanced Technology. pp. 704-706. ISBN 978-1-85617-233-2.
- ^ Mei, Y.; Tang, C.Y. (2018). "Recent developments and future perspectives of reverse electrodialysis technology: A review". Desalination. 425: 156–174. doi:10.1016/j.desal.2017.10.021.
- ^ "Separation characteristics of dialysis membranes". Retrieved 13 November 2013.
- ^ "Fundamentals of membrane dialysis". Retrieved 13 November 2013.
- ^ Klemm, Dieter; Heublein, Brigitte; Fink, Hans-Peter; Bohn, Andreas (2005). "Cellulose: Fascinating Biopolymer and Sustainable Raw Material". Angewandte Chemie International Edition. 44 (22): 3358–3393. doi:10.1002/anie.200460587. PMID 15861454.
- ^ Lovett, Louis E. (1938). "The Application of Osmosis to the Recovery of Caustic Soda Solutions Containing Hemicellulose in the Rayon Industry". Trans. Electrochem. Soc. 73 (1): 163–172. doi:10.1149/1.3493960.
- ^ Marshall, R. D.; Storrow, J. Anderson (1 December 1951). "Dialysis of Caustic Soda Solutions". Ind. Eng. Chem. 43 (12): 2934–2942. doi:10.1021/ie50504a074.
- ^ Lee, Eric K.; Koros, W. J. (2003). "Membranes, Synthetic, Applications: Industrial Dialysis". ScienceDirect. From Encyclopedia of Physical Science and Technology (3rd edition). Retrieved 29 September 2020.
- ^ Jackowski, M.; Trusek, A. (2018). "Non-alcoholic beer production - an overview". Polish Journal of Chemical Technology. 20 (4): 32–38. doi:10.2478/pjct-2018-0051. S2CID 104447271.
- ^ a b c d Scott, K.; Hughes, R. (1996). Industrial Membrane Separation Technology. Springer-Science+Business Media, B.V. pp. 222–225. ISBN 978-94-010-4274-1.
- ^ a b Charisiadis, C. "Electrodialysis/ED Reversal" (PDF).