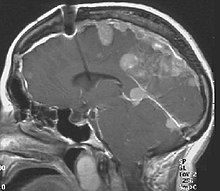
신경섬유화증 타입 II
Neurofibromatosis type II| 신경섬유화증 타입 II | |
|---|---|
| 기타 이름 | 다중 상속된 슈완노마, 메닌기오마, 에피네마(MISME 증후군) |
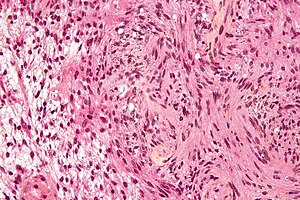 | |
| 신경섬유종 2형에서 보이는 종양인 슈완노마 마이크로그래프 입니다.HPS 얼룩. | |
| 전문 | 의학유전학, 신경학 |
신경섬유종증 타입 II(MISSNEE 증후군이라고도 함)는 유전될 수 있거나 자연적으로 발생할 수 있는 유전적 질환으로 뇌, 척수, 말초신경의 양성 종양을 유발한다.NF2와 자주 관련되는 종양의 종류에는 전정맥류 슈완노마, 메닌기오마, 에피디모마 등이 있다.이 질환의 주요 징후는 두개골 신경 8세의 신경 피복에 있는 양쪽 양성 뇌종양의 발달로, 내이에서 뇌로 감각 정보를 전달하는 '감청-전정신경'이다.게다가, 다른 양성 뇌와 척추 종양이 발생한다.증상은 종양의 존재, 국소화 및 성장에 따라 달라지는데, 여기에는 여러 개의 두개골이 관여할 수 있다.[1]이러한 상태를 가진 많은 사람들도 시력 문제를 경험한다.신경섬유화증 타입 II(Neurofibromatosis type II, NF2 또는 NF II)는 'Merlin' 유전자의 돌연변이에 의해 발생하는데,[2] 이는 세포의 형태와 움직임에 영향을 미치는 것으로 보인다.주된 치료법은 종양의 신경외과적 제거와 눈병변의 수술적 치료로 이루어진다.역사적으로 근본적인 장애는 유전적 돌연변이에 의한 세포 기능 때문에 어떠한 치료도 받지 못했다.
분류
NF2는 자가 지배적인 전송 모드를 가진 유전적 장애다.[3]
NF2에는 두 가지 형태가 있다.[4]
- 위시아트-페노타입 형태는 20세 이하 연령대의 뇌·척수 병변과 종양의 급속한 진행으로 특징지어진다.
- NF2가 있는 사람들은 20세 이후에 느린 진행으로 단일 중심 종양에 걸리는 사람들은 Feiling-Gardner 표현형을 가지고 있는 것으로 생각된다.
원인
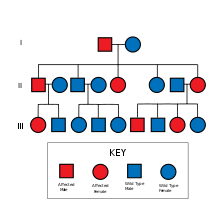
NF2는 22번 염색체의 22Q12.2에 위치한 NF2 유전자의 돌연변이에 의해 발생하며, 돌연변이의 유형은 다양하며 단백질-트랜코팅 변경(오류 삭제/삽입 및 난센스 돌연변이), 스플라이스 사이트 돌연변이, 오식 돌연변이 등을 포함한다.멀린 단백질의 NH2 말단 영역에서의 삭제 역시 초기 종양 발생과 NF2 환자들의 좋지 않은 예후와 관련이 있다.[5]단백질을 잘라내는 돌연변이는 더 심각한 표현형과 관련이 있다.[6]알려진 광범위한 임상 스펙트럼이 있지만, 검사를 받은 모든 사람들은 22번 염색체에서 같은 유전자의 일부 돌연변이를 가지고 있는 것으로 밝혀졌다.통계를 통해 2분의 1은 유전되고, 2분의 1은 새로운 데 노보 돌연변이의 결과라는 의심을 받고 있다.[citation needed]
병생성
NF2는 일반적으로 22번 염색체 q11-13.1에 위치한 멀린 또는 슈완노민이라는 제품을 발생시키는 유전자의 결함으로 인해 발생한다.멀린은 액틴 시토스켈레톤 조절기 역할을 하는 구조 단백질로 처음 발견되었다.나중에 멀린의 종양 억제 역할이 설명되었다.Merlin은 수용체 tyrosine kinase 신호 전달, p21 활성화 키나제 신호 전달, Ras 신호 전달, MEK-ERK 캐스케이드, MST-YAP 캐스케이드와 같은 다중 증식 신호 전달 캐스케이드를 조절한다.[7]정상 세포에서 활성(탈인산화) 멀린의 농도는 세포 접착과 같은 과정에 의해 제어된다(세포 분열을 억제할 필요성을 나타낼 수 있음).Merlin은 세포 운동성과 종양 침입에 중요한 Rac1을 억제하는 것으로 나타났다.[8]또한, 멀린의 사이클린 D와의 상호작용도 설명되었다.[9]멀린의 결핍은 주로 신경섬유화증 타입 II의 종양 특성을 유발하기에 충분한 세포 접점 붕괴 때문에 접촉 매개 종양 억제 부족으로 세포 사이클을 통해 즉각 진행되지 않는 결과를 초래할 수 있는 것으로 알려져 있다.최근 연구는 세포골격계 및 세포질 기능 외에도 멀린도 핵으로 반투명하며 E3 유비퀴틴 리가제 CRL4(DCAF1)를 억제하여 증식을 억제한다는 것을 보여주었다.[10]마지막으로, 대부분의 최근의 연구는 멀린이 에너지 대사 조절에 중요한 역할을 한다는 것을 보여주었다.[11][12]NF2의 돌연변이는 멀린을 합성하지 못하거나 정상적인 종양 억제 효과가 없는 결함 있는 펩타이드의 생산을 초래하는 것으로 추정된다.슈완노민펩타이드에는 595개의 아미노산이 있다.슈완노민을 다른 단백질과 비교한 결과 세포막과 세포막을 연결하는 단백질과 유사성이 나타난다.슈완노민겐의 돌연변이는 접촉 억제 상실과 함께 영향을 받는 세포의 움직임과 형태를 변화시키는 것으로 생각된다.후두근은 중추신경계의 상피와 같은 조직인 후두근에서 발생하는 종양이다.[13]NF2와 에펜디모마가 있는 사람에서는 멀린의 종양 억제 기능이 저하될 수 있다.멀린 단백질이 암호화된 22q 염색체에서 발생하는 기능 돌연변이는 종양세포의 생성, 즉 새로운 종양세포를 촉진시킬 수 있다.[5]멀린 단백질의 NH2단말 영역에서의 삭제 역시 초기 종양 발생과 영향을 받은 사람들의 좋지 않은 예후와 관련이 있다.[5]
병리학
NF2의 이른바 음향신경종은 사실 신경전정맥종, 즉 전정맥류의 슈완노마다.어쿠스틱 뉴로마의 오노머는 여전히 자주 사용된다.전정맥류 슈완노마스는 내부 청각 미투스의 내부 입구에서 천천히 자란다.그것들은 뇌에서 1 cm 떨어진 포루스의 음향 영역 내에 있는 중앙과 말초 몰린(Obersteiner-Redlich-Zone) 사이의 영역에 있는 신경 전정맥 상부의 신경 피복으로부터 얻는다.[citation needed]
유전자형-문자형 상관 관계
NF2를 가진 많은 사람들이 관련 돌연변이의 정확한 결정과 질병의 종류와 진행을 비교하기 위해 고안된 연구에 포함되었다.유전자형과 표현형의 이러한 비교의 목적은 특정한 돌연변이가 각각의 증상 조합을 유발하는지 여부를 결정하는 것이다.이것은 질병 진행의 예측과 어린 나이에 시작되는 치료 계획에 매우 유용할 것이다.이러한 연구의 결과는 다음과 같다.
- 대부분의 경우 NF2 유전자의 돌연변이는 펩타이드를 단축시킨다.
- 돌연변이 핫스팟은 없다.
- 일시적인 돌연변이나 말도 안 되는 돌연변이를 가진 사람들은 예후가 좋지 않다.
- 오감 변이를 가진 사람들은 더 나은 예후를 가지고 있다.
- 스플라이스-수용체 영역에 돌연변이가 있는 경우, 판단하기에 좋은 상관관계가 없다.
- 점 돌연변이는 사소한 영향만 미칠 수 있다.
- 정확히 동일한 돌연변이가 명백하게 다른 결과와 연관되어 있는 경우를[citation needed] 발표한다.
이러한 결과는 다른 요인(환경, 기타 돌연변이)이 임상 결과를 결정할 것임을 시사한다.
증상
증상은 어느 연령대에나 발생할 수 있으며, 전형적으로 청소년기와 초기 성인기에 발생할 수 있으며, 어린이에게는 거의 볼 수 없으며, 중증도는 종양의 위치에 따라 달라진다.증상에는 다음이 포함되지만 이에 국한되지는 않는다.
- 이명
- 잔액손실/문제
- 녹내장
- 발작
- 청력손실
- 시력손상
- 무감각 또는 팔다리의 약함
진단
NF2는 유전적으로 전염되는 조건이다.진단은 성인 초기(20~30년)에 가장 많이 나타나지만 조기 진단할 수 있다.NF2는 양쪽 전정맥 슈완노마, 또는 일방적으로 청력 손실이 발생할 수 있는 음향신경종 때문에 진단할 수 있다.[14]환자가 이 진단 기준을 충족하지 못하면 반드시 NF2의 가족력이 있어야 하며, 일방적인 전정전증 슈완노마 및 기타 관련 종양(뇌막종양, 두개신경 슈완노마, 척추측두종양, 척추측두종양, 척추측두종양, 피하종양, 피부 플라크)을 가지고 있어야 한다.이는 NF2 진단을 받은 전체 환자의 절반 이상이 이 질환에 대한 가족력이 없는 것으로 알려졌다.[14]아직 임상 분류에 포함되지는 않았지만 손발에 허약, 저림, 통증을 유발하는 말초신경장애나 말초신경의 손상도 NF2의 진단으로 이어질 수 있다.어린이의 경우 NF2는 유사한 증상을 보일 수 있지만 일반적으로 "시력 장애(카타르, 하마르토마스), 피부 종양, 모노뉴로패시(구두, 드롭풋), 증상성 척수종양 또는 비수상내종양"을 유발한다.[14]
태내
양쪽 전정체 슈완노마는 NF2의 진단이다.[15]
산후
Ferner 외 [16]연구진은 NF2에 대한 세 가지 진단 기준을 제시한다.
- NF2 + 일방적 VS 또는 두 가지 중 하나인 뇌전정맥전증(VS) 또는 가족력: 뇌전수종, 교모종, 신경섬유종, 슈완노마, 후부갑상선망상완종(VS) 또는 가족력
- 일방적인 VS + 뇌막하수종, 교모종, 신경피브롬종, 슈완노마, 후하악막하반경막외피종 2개 포함
- 두 개 이상의 뇌막종과 일방적인 VS 또는 두 개의 교모종, 슈완노마, 백내장.
또 다른 진단 기준 세트는 다음과 같다.
- 영상시술을 통한 쌍방향 음향신경종 검출
- NF2 및 신경섬유종, 메닌기오마, 교모종 또는 슈완노마 발생과 1도 상대적 관계
- NF2와 청소년 후두막하백내장의 발생과 관련된 1도.
그 기준은 시간이 지남에 따라 달라졌다.[17]NF2 기준의 마지막 개정은 2017년 엠제이 스미스가 했다.여기에는 NF2 대신 LZTR1 돌연변이(슈완노마토증)를 고려하고, 70세 이후에 발생하는 양쪽 전정 슈완노마(chwannomas)는 제외했다.[18]
치료
수술
음향신경종 제거에는 몇 가지 다른 수술 기법이 있다.[19]접근방법의 선택은 종양의 크기, 청각 능력 및 개인의 일반적인 임상 조건에 따라 결정된다.
- 리터러그로이드 접근법은 청력을 유지할 수 있는 기회를 제공한다.
- 반투명 접근법은 그 쪽에서는 청력을 희생시키겠지만 대개 안면신경을 살려준다.수술 후 뇌척수액 누수는 더 흔하다.
- 중간 fossa 접근법은 작은 종양에 선호되며 청력과 전정 기능의 유지 가능성이 가장 높다.
- 미국 밖에서 한동안 덜 침습적인 내시경 기술이 행해져 왔다.회복 시간이 더 빠른 것으로 보고되었다.그러나, 이 기술은 미국의 외과의사들 사이에서 아직 주류가 아니다.
더 큰 종양은 수술팀의 경험에 따라 반투명 접근법이나 반역자적 접근법으로 치료할 수 있다.종양이 크면 어떤 접근으로도 청력 보존 가능성은 적다.이미 청력이 좋지 않을 때, 작은 종양에도 반투명 접근법을 사용할 수 있다.청력이 좋은 NF2 환자의 작고 편중된 종양은 중간 fossa 접근법을 가져야 한다.종양의 위치가 좀 더 내적인 경우, 회고록 접근법이 더 나을 수 있다.
청각관 감압은 전정맥 슈완노마가 너무 커져 달팽이관 신경에 손상을 주지 않고 제거할 수 없을 때 사용 가능한 청력을 연장할 수 있는 또 다른 수술 기법이다.IAC(내부 청각관) 감압에서는 종양을 제거하려는 시도 없이 IAC의 뼈 지붕을 노출시키기 위해 중간 fossa 접근법을 사용한다.음향신경에 걸쳐 있는 뼈는 제거되어 종양이 중앙 두개골 포사까지 위쪽으로 확장될 수 있다.이렇게 하면 달팽이관신경에 가해지는 압력이 완화되어 직접 압박이나 신경으로의 혈관 공급 방해로 인한 청력 손실의 위험이 더 줄어들게 된다.
라디오 수술은 두개골 베이스나 다른 두개내 수술에 대한 보수적인 대안이다.순응적 방사선 수술 기법으로 치료용 방사선은 종양에 초점을 맞추고 주변 정상 조직에 대한 노출을 줄였다.비록 라디오 수술은 종양을 완전히 파괴할 수 없지만, 종종 종양의 성장을 막거나 크기를 줄일 수 있다.방사선은 기존 수술에 비해 즉각적인 손상은 덜하지만, 조사조직에 후속 악성변화의 위험이 더 높으며, 산발적인 (NF2) 병변보다 NF2에서 더 위험하다.
약물
환자 연구에서 베바시주맙은 일부 환자의 종양 증가율 감소와 청력 개선 효과를 가져왔으나 현재 NF2 환자에 대해 종양 부담 감소를 위한 처방약은 없다.[20][21]
청력손실
NF2를 가진 사람들의 청력 손실은 거의 항상 언어 능력을 습득한 후에 발생하기 때문에, NF2를 가진 사람들은 항상 청각 장애 문화에 잘 통합되지 않고 청각 보조 기술에 의존할 가능성이 더 높다.[citation needed]이런 장치 중 하나가 달팽이관 이식인데, 자연 청력이 완전히 소실돼도 때로는 높은 수준의 청각 기능을 회복할 수 있다.그러나 전형적인 NF2 슈완노마에 의한 달팽이관 신경의 파괴량은 종종 그러한 임플란트의 사용을 금지한다.이 경우 청각 뇌관 삽입물(ABI)은 어느 정도 청력을 회복할 수 있으며, 입술 판독을 통해 보충된다.
원인
NF2에 의한 청력 손실은 점진적이며 달팽이관 신경의 손상이 청력 손실을 유발하는 음향 신경증이라고도 알려진 양쪽 달팽이관 슈완노마(schwannomas)의 존재에서 비롯된다.[22]또한 청력 손실은 전정신경과 청각신경에 자라는 양성종양에서 발생하여 내이(內이)로 이어질 수 있다.
유형/도
일반적으로, NF2로 진단된 환자들은 보통 양쪽에 있는 경미하거나 중간 정도의 청력 손실로 나타나며, 심해질 수 있다.[23]환자들은 보청기 사용으로 이득을 볼 수 있지만, 많은 경우, 그들의 청력 손실은 결국 이것이 효과적인 치료로 간주되는 수준을 넘어설 것이다.[24]
치료
NF2를 가진 개개인의 청력 손실은 일반적으로 점진적이고, 결국 심오하며, 감각적이기 때문에, 청력 손실에 대한 최선의 치료 방법은 달팽이관 삽입물과 청각 뇌관 이식(ABIs)이며, 또한 입술 읽기, 큐딩 스피치 또는 수화로 청력을 보충하는 것이다.
달팽이관 삽입물
달팽이관 임플란트는 달팽이관 신경을 자극하기 위해 외과적으로 이식하는 전자 장치다.[25]달팽이관 이식수술은 달팽이관 신경(8번째 신경)과 달팽이가 여전히 기능할 때에만 효과가 있을 것이다.네프 외 연구진이 개방형 음성 인식 테스트와 폐쇄형 음성 인식 테스트를 실시한 연구에서는 달팽이관 삽입물을 NF2 환자와 함께 사용하면 청각 능력이 크게 향상된다는 것을 발견했다.[26]일상 언어의 문장 인식 테스트에서는 환자 6명 중 5명이 90%~100% 범위 내에서, 소음 환경에서의 청력 테스트에서는 환자 6명 중 4명이 83~96%[26] 범위 내에서 점수를 받았다.게다가, 모든 테스트는 립 레딩 없이 수행되었다.
청각 뇌관 삽입물(ABI)
청각 브레인스팀 임플란트(Brainsteam Implant) 또는 ABI는 코클레아 또는 코클레오페스텔라 신경의 어떤 부분이 그러한 부위의 손상이나 해부학적 이상으로 인해 기능하지 않을 때 사용된다.[27]이 절차는 전기 신호를 달팽이관 핵에 직접 보내는 장치를 이식하여 소리가 말초 청각계를 우회하여 뇌간으로 바로 들어갈 수 있도록 하는 것이다.
유병률
그 질환의 발병률은 약 6만분의 1이다.[28]
예후
NF2는 생명 제한 조건이다.내이에서 뇌로 균형과 음향 자극을 전달하는 신경의 비암성 종양을 수반하는 희귀한 유전적 질환이다.예후는 조기 발병, 메닌기오마와 슈완노마 수가 많고 돌연변이가 감소하는 등의 영향을 받는다.[29]
조기 진단이 경영 개선을 보장하는 최선의 방법이다.비록, 조기 진단을 받더라도, 몇몇 환자들은 여전히 매우 젊게 죽는다.
Meningiomas와 Schwannomas는 NF2 환자들의 약 절반에서 발생한다.뇌막내종양(meningiomas)은 두개골내종양과 두개골내종양이다.슈완노마(Schwannomas)는 종종 내부 청각 관을 중심으로 하는 종양이다.메닌기오마균이 있는 NF2 환자는 사망 위험이 높아 치료가 매우 어려울 수 있다.슈완노마를 발달시킨 개인은 청력 상실과 청각장애가 자주 발생한다.[29]이 개인들은 또한 일방적인 청력 손실을 받은 후에 이명이 생길 수도 있다.개인이 처음 겪을 수 있는 증상은 어지럼증이나 불균형이다.
돌연변이를 잘라내면 더 작고 비기능적인 단백질 제품이 나온다.연구에 따르면, 잘못된 돌연변이와 큰 삭제는 둘 다 주로 가벼운 표현형을 유발할 수 있다.표현형은 이중 부위의 돌연변이를 가진 환자에게서 더 가변적이며, 9-15년 전의 돌연변이를 가진 환자들에게는 더 가벼운 질병이다.[29]오감 돌연변이가 있는 환자들은 허튼소리나 액자 변이보다 생존율이 더 높다.
참조
- ^ Rissardo JP, Caprara AL (2018-11-08). "Neurofibromatosis two presenting with bilateral sixth and seventh nerve palsies". Neurology and Clinical Neuroscience. 7 (1): 47–47. doi:10.1111/ncn3.12239. ISSN 2049-4173.
- ^ Striedinger K, VandenBerg SR, Baia GS, McDermott MW, Gutmann DH, Lal A (November 2008). "The neurofibromatosis 2 tumor suppressor gene product, merlin, regulates human meningioma cell growth by signaling through YAP". Neoplasia. 10 (11): 1204–1212. doi:10.1593/neo.08642. PMC 2570596. PMID 18953429.
- ^ Asthagiri AR, Parry DM, Butman JA, Kim HJ, Tsilou ET, Zhuang Z, Lonser RR (June 2009). "Neurofibromatosis type 2". Lancet. 373 (9679): 1974–1986. doi:10.1016/S0140-6736(09)60259-2. PMC 4748851.
- ^ Walter J, Kuhn SA, Brodhun M, Reichart R, Kalff R (June 2009). "Pulmonary meningioma and neurinoma associated with multiple CNS tumours in a patient with neurofibromatosis type 2". Clinical Neurology and Neurosurgery. 111 (5): 454–459. doi:10.1016/j.clineuro.2008.11.018. PMID 19249154. S2CID 22696343.
- ^ a b c Stamenkovic I, Yu Q (September 2010). "Merlin, a "magic" linker between extracellular cues and intracellular signaling pathways that regulate cell motility, proliferation, and survival". Current Protein & Peptide Science. 11 (6): 471–484. doi:10.2174/138920310791824011. PMC 2946555. PMID 20491622.
- ^ Cooper J, Giancotti FG (August 2014). "Molecular insights into NF2/Merlin tumor suppressor function". FEBS Letters. 588 (16): 2743–2752. doi:10.1016/j.febslet.2014.04.001. PMC 4111995. PMID 24726726.
- ^ Okada T, You L, Giancotti FG (May 2007). "Shedding light on Merlin's wizardry". Trends in Cell Biology. 17 (5): 222–229. doi:10.1016/j.tcb.2007.03.006. PMID 17442573.
- ^ Sherman LS, Gutmann DH (November 2001). "Merlin: hanging tumor suppression on the Rac". Trends in Cell Biology. 11 (11): 442–444. doi:10.1016/S0962-8924(01)02128-6. PMID 11684412.
- ^ Xiao GH, Gallagher R, Shetler J, Skele K, Altomare DA, Pestell RG, et al. (March 2005). "The NF2 tumor suppressor gene product, merlin, inhibits cell proliferation and cell cycle progression by repressing cyclin D1 expression". Molecular and Cellular Biology. 25 (6): 2384–2394. doi:10.1128/MCB.25.6.2384-2394.2005. PMC 1061616. PMID 15743831.
- ^ Cooper J, Li W, You L, Schiavon G, Pepe-Caprio A, Zhou L, et al. (August 2011). "Merlin/NF2 functions upstream of the nuclear E3 ubiquitin ligase CRL4DCAF1 to suppress oncogenic gene expression". Science Signaling. 4 (188): pt6. doi:10.1126/scisignal.2002314. PMID 21878678. S2CID 9582719.
- ^ Stepanova DS, Braun L, Chernoff J (May 2018). "A new concept in NF2 pharmacotherapy: targeting fatty acid synthesis". Oncoscience. 5 (5–6): 126–127. doi:10.18632/oncoscience.417. PMC 6049319. PMID 30035161.
- ^ Stepanova DS, Semenova G, Kuo YM, Andrews AJ, Ammoun S, Hanemann CO, Chernoff J (September 2017). "An Essential Role for the Tumor-Suppressor Merlin in Regulating Fatty Acid Synthesis". Cancer Research. 77 (18): 5026–5038. doi:10.1158/0008-5472.CAN-16-2834. PMC 5600854. PMID 28729415.
- ^ "Ependymoma". The Lecturio Medical Concept Library. Retrieved 19 July 2021.
- ^ a b c Asthagiri AR, Parry DM, Butman JA, Kim HJ, Tsilou ET, Zhuang Z, Lonser RR (June 2009). "Neurofibromatosis type 2". Lancet. 373 (9679): 1974–1986. doi:10.1016/S0140-6736(09)60259-2. PMC 4748851. PMID 19476995.
- ^ Christopher Gillberg (16 October 2003). Clinical Child Neuropsychiatry. Cambridge University Press. pp. 231–. ISBN 978-0-521-54335-4. Retrieved 20 December 2010.
- ^ 페너, 로잘리 E, 수잔 M.Huson, and D.가레스 R.에반스, 임상실험에서 신경섬유종이야스프링거, 2011년
- ^ "Neurofibromatosis Type 2: eMedicine Radiology". 2016-09-26. Retrieved 2010-12-20.
{{cite journal}}:Cite 저널은 필요로 한다.journal=(도움말) - ^ Jean Régis; Pierre-Hugues Roche (2008). Modern Management of Acoustic Neuroma. Karger Publishers. pp. 191–. ISBN 978-3-8055-8370-1. Retrieved 20 December 2010.
- ^ "Neurofibromatosis Information Page". National Institute of Neurological Disorders and Stroke. Retrieved June 16, 2019.
- ^ Morris KA, Golding JF, Axon PR, Afridi S, Blesing C, Ferner RE, et al. (December 2016). "Bevacizumab in neurofibromatosis type 2 (NF2) related vestibular schwannomas: a nationally coordinated approach to delivery and prospective evaluation". Neuro-Oncology Practice. 3 (4): 281–289. doi:10.1093/nop/npv065. PMC 5909937. PMID 29692918.
- ^ 인용필요
- ^ Emmanouil B, Houston R, May A, Ramsden JD, Hanemann CO, Halliday D, et al. (April 2019). "Progression of hearing loss in neurofibromatosis type 2 according to genetic severity". The Laryngoscope. 129 (4): 974–980. doi:10.1002/lary.27586. PMID 30456886.
- ^ Lee JM, Chang JW, Choi JY, Chang WS, Moon IS (July 2016). "Hearing Restoration in Neurofibromatosis Type II Patients". Yonsei Medical Journal. 57 (4): 817–823. doi:10.3349/ymj.2016.57.4.817. PMC 4951455. PMID 27189272.
- ^ "Cochlear Implant Surgery". www.hopkinsmedicine.org. Retrieved 2021-11-29.
- ^ a b Neff BA, Wiet RM, Lasak JM, Cohen NL, Pillsbury HC, Ramsden RT, Welling DB (June 2007). "Cochlear implantation in the neurofibromatosis type 2 patient: long-term follow-up". The Laryngoscope. 117 (6): 1069–1072. doi:10.1097/MLG.0b013e31804b1ae7. PMID 17545869.
- ^ Wong K, Kozin ED, Kanumuri VV, Vachicouras N, Miller J, Lacour S, et al. (2019). "Auditory Brainstem Implants: Recent Progress and Future Perspectives". Frontiers in Neuroscience. 13: 10. doi:10.3389/fnins.2019.00010. PMC 6361749. PMID 30760974.
- ^ Evans DG (June 2009). "Neurofibromatosis type 2 (NF2): a clinical and molecular review". Orphanet Journal of Rare Diseases. 4: 16. doi:10.1186/1750-1172-4-16. PMC 2708144. PMID 19545378.
- ^ a b c "Neurofibromatosis type 2 (NF2): A clinical and molecular review". Orphanet Journal of Rare Diseases. doi:10.1186/1750-1172-4-16. Retrieved 2021-11-29.
추가 읽기
- Evans, D. Gareth (1993). "Neurofibromatosis 2". GeneReviews. University of Washington, Seattle. Retrieved 30 May 2017.