대체 주기율표
Alternative periodic tables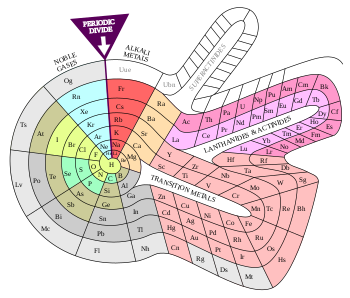
| 다음 시리즈의 일부 |
| 주기율표 |
|---|
대체 주기율표는 주기율 체계에서 전통적인 묘사와는 조직에서 다른 화학 원소들의 표이다.[1][2]
화학 원소들 간의 모든 상관관계가 표준 주기율표에 의해 효과적으로 포착되지 않기 때문에 종종 교훈적인 이유로 천 개 이상의 화학적 이유가 고안되었다.
주요 대체 구조물
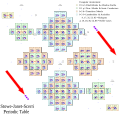
왼쪽 단계 주기율표(Janet, 1928년)
찰스 자넷의 왼쪽 단계 주기율표는[3] 전통적인 주기율 체계 묘사에 가장 널리 사용되는 대안이다. 이상화된 궤도 충전(용기 대신)에 따라 원소를 구성한다.[4] 예를 들어, Sc to Zn 원소는 궤도 점유[Ar] 4s2 3d를x 의미하는 3d 블록으로 표시된다.(Cr과 Cu는 기체 위상의 예외사항이지만 이상화된 구성은 지상 상태에서 너무 멀리 떨어져 있지 않으며, 에너지 차이는 화학 환경에 의해 제어될 만큼 작다.)
| f1 | f2 | f3 | f4 | f5 | f6 | f7 | f8 | f9 | f10 | f11 | f12 | f13 | f14 | d1 | d2 | d3 | d4 | d5 | d6 | d7 | d8 | d9 | d10 | p1 | p2 | p3 | p4 | p5 | p6 | s1 | s2 | |
| 1s | H | 그 | ||||||||||||||||||||||||||||||
| 2s | 리 | 있다 | ||||||||||||||||||||||||||||||
| 2p 3s | B | C | N | O | F | 네 | 나 | MG | ||||||||||||||||||||||||
| 3p 4s | 알 | SI | P | S | CL | 아르 | K | CA | ||||||||||||||||||||||||
| 3d 4p 5s | sc | 티 | V | CR | Mn | Fe | Co. | 니 | CU | Zn | 가 | Ge | 로서 | SE | BR | 크르 | Rb | SR | ||||||||||||||
| 4d 5펜스 6s | Y | Zr | Nb | 모 | TC | 루 | RH | 피디 | AG | cd | 인 | Sn | SB | Te | I | 세 | Cs | BA | ||||||||||||||
| 4f 5d 6p 7s | 라 | CE | PR | ND | PM | sm | Eu | Gd | TB | DY | 호 | 음.정말 | TM | Yb | 루 | Hf | 타 | W | 레 | Os | Ir | PT | Au | Hg | Tl | PB | 비 | 포 | 에서 | Rn | FR | 라 |
| 5f 6d 7p 8s | Ac | TH | 파 | U | Np | PU | 암 | CM | Bk | cf | 에스 | FM | md | 아니요. | Lr | RF | db | sg | BH | HS | MT | Ds | RG | 씨엔 | NH | 플 | 맥 | LV | TS | Og | 119 | 120 |
| f-블록 | d-블록 | p-block | s-블록 | |||||||||||||||||||||||||||||
일반적인 레이아웃과 비교하여 왼쪽 단계 표에는 다음과 같은 변경 사항이 있다.
- 헬륨은 그룹 2 (그룹 18이 아닌)에 위치한다.
- 연장 8의 요소 119와 120을 포함한 그룹 1과 그룹 2(s-block)는 테이블 우측으로 이동한다.
- s-블록은 한 행 위쪽으로 이동하며, s-블록이 아닌 모든 요소는 현재 표준 표보다 한 행 낮다. 예를 들어, 표준 테이블의 네 번째 행은 대부분 이 테이블의 다섯 번째 행이다.
그 결과, 그 순서는 여전히 원자 번호(Z), 1–120으로 일관된다.
2차원 나선형(Benfey, 1964)
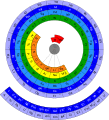
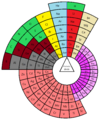
테오도르 벤페이의 주기율표에서 원소들은 수소로부터 시작하여 두 개의 반도, 전이 금속, 란타니드와 액티나이드를 중심으로 2차원 나선형을 형성한다. 초액티나이드 섬이 이미 자리 잡고 있다.[5] 벤페이 테이블은 극소수의 테이블이 나타내는 몇 가지 독특한 측면을 가지고 있다. 이것의 한 예는 수소가 나선형 안에 가지고 있는 배치다. 대부분의 테이블에서 수소는 "이상한 원아웃"처럼 보인다. 그 이유는 수소는 알칼리 금속과 같은 발란스 전자 구성을 가지고 있지만 할로겐의 성질을 가지고 있기 때문이다. 벤페이 테이블은 수소 박스를 알칼리 금속과 할로겐 둘 다로 확장함으로써 이 난관을 극복한다.
입체, 꽃다운 (폴 기구에르, 1966)
Paul Giguere의 3-D 주기율표는 앞면과 뒷면에 원소가 적혀 있는 4개의 연결된 광고판으로 구성되어 있다. 첫 번째 광고판은 전면에는 그룹 1 원소가, 후면에는 그룹 2 원소가 각각 배치되어 있으며 수소와 헬륨이 모두 생략되어 있다. 90° 각도로 두 번째 광고판은 13~18개의 그룹을 앞뒤로 담고 있다. 각각 90° 각도를 만드는 두 개의 광고판은 다른 요소들을 포함하고 있다.[6][7]
3차원 물리학자 (Timothy Stowe, 1986)
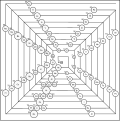
티모시 스토우의 물리학자 주기율표는 주 양자수, 궤도 양자수, 궤도자기 양자수를 나타내는 세 개의 축이 3차원이다.[8][9] 헬륨은 다시 그룹 2 원소다.
요소 반복(Ronald L. 리치, 2005)
로널드 L. 리치는 원소가 적절할 때 두 번 이상 나타나는 주기율표를 제안했다.[10] 그는 수소가 비금속이기 때문에 그룹 17 원소와 그룹 1 원소와 성질을 공유하지만 전환 금속과 화학적 결합의 유사성과 유사한 전기성을 기반으로 한 탄소 그룹과도 성질을 공유한다는 점에 주목한다. 이러한 주기율표 탄소 및 실리콘의 증가는 티타늄 및 지르코늄과 같은 그룹에 나타나기도 한다.
ADOMAH (Valery Tsimmerman, 2006)

ADOMAH 테이블은 왼쪽 단계 테이블을 적응시킨 것이다.[12] 표의 엄밀하게 수직으로 된 각 열은 주 양자수 n의 값이 같다. 예를 들어, n = 3 for Fe. 원소의 각 블록은 2차 양자수 l의 값이 동일하다. 예를 들어, l = 2 for Fe. 모든 선행 요소와 함께 각 요소 엔트리는 해당 원소의 전자 구성에 해당한다(118개의 알려진 요소 중 20개의 예외 포함). 예를 들어, Fe의 전자 구성은 1s인1 H에서 시작하여 원자 번호 순서로 계산함으로써 결정된다. 이것은 1s2 2s2 2p6 3s2 3p6 4s2 3d6 또는 짧은 형태로 [Ar] 4s2 3d의6 구성을 제공한다.
아도마 테이블의 네 블록은 일정한 간격을 두고 일반 사면체 내부에 맞도록 다시 배열할 수 있다. 후자는 차례로 큐브에 맞는다.[13]
고전적 레이아웃의 변형
멘델레예프의 원래 주기율표에서 원소들은 기본적으로 발란스(기둥의 집단)와 거기에 있는 반복(기둥의 주기)에 의해 배열되어 왔다. 수년 동안 그리고 원자 구조에 대한 발견으로, 이 스키마는 조정되고 확장되었지만, 원칙으로서 바뀌지는 않았다.
가장 오래된 주기율표는 드미트리 멘델레예프의 짧은 형식표(컬럼스 I–VIII)로 2차 화학적 친족관계를 보여준다. 예를 들어 알칼리 금속과 코인지 금속(코퍼, 은, 금)은 두 그룹 모두 용맹성이 1인 경향이 있기 때문에 같은 열에 있다. 뢴트게늄까지 모든 원소와 원소명을 포함하는 이 현대 러시아어 짧은 양식표에서 보듯이, 이 형식은 여전히 많은 사람들에 의해 사용된다.
H. G. 데밍은 1923년(와일리) 처음으로 미국에 등장한 교과서 '일반 화학'에 이른바 긴 주기율표(18열)를 사용했으며, 처음 두 개의 주요 그룹과 마지막 다섯 개의 주요 그룹을 표기법 'A'로, 중간 인수 그룹 'B'로 표기했다.
B 집단의 특징적인 산소가 A 집단의 산소와 일치하도록 숫자를 선택했다. 철, 코발트, 니켈 그룹은 A, B로 지정되지 않았다. 고귀한 가스 그룹은 원래 주기율표 왼쪽에 붙어 있었다(데밍에 의해). 그 그룹은 나중에 오른쪽으로 바뀌었고 보통 그룹 VIIIA로 라벨이 붙여졌다.
주기율표 연장
Glenn T가 제안한 확장된 주기율표에서. 1969년, 아직 알려지지 않은 원소들이 원자 번호 168까지 포함되어 있다. 정규 기간 7 이상의 이론적 기간이 추가된다.
슈퍼아톰의 연구분야에서 원자의 군집은 다른 원소의 단일 원자의 성질을 가지고 있다. 이러한 클러스터 화합물들이 점유할 두 번째 층을 가진 주기율표를 확장할 것을 제안한다. 이 다층 테이블에 가장 최근에 추가된 것은 다층 게르마늄 원자처럼 작용하는 알루미늄 클러스터 이온 알이다−
7.[14]
2020년 10월 과학자들은 멘델레예프 번호를 제시하고 화학적 공간을 구성하는 비해적 방법을 보고했다.[15][16][17]
갤러리
참조
- ^ E. R. Scerri. 주기율표, 그것의 이야기 그리고 그것의 중요성. 2006년 뉴욕 옥스퍼드 대학 출판부 ISBN0195345673.
- ^ 헨리 벤트 주기적인 법칙을 위한 신선한 에너지의 화학에 대한 새로운 아이디어들 AuthorHouse, 2006, ISBN 978-1-4259-4862-7.
- ^ "Left Step Periodic Table". 1928. Retrieved 2014-02-15.
- ^ Stewart, Philip J. (2009). "Charles Janet: Unrecognized genius of the periodic system". Foundations of Chemistry. 12: 5–15. doi:10.1007/s10698-008-9062-5. S2CID 171000209.
- ^ 벤페이의 테이블은 글렌 시보그의 기사에 "플루토늄: 1964년 6월 화학 "오너리 요소" 37 (6), 12–17 페이지 14.
- ^ Mazurs, E. G. (1974). Graphical Representations of the Periodic System During One Hundred Years. Alabama: University of Alabama Press. p. 111. ISBN 978-0-8173-3200-6.
- ^ 인터넷(여기 포함)에서 널리 구할 수 있는 기구에르의 주기율표를 애니메이션으로 묘사한 것은 수소와 헬륨을 포함하지 않기 때문에 잘못된 것이다. 기구에르는 리튬 위 수소와 베릴륨 위 헬륨을 포함했다. Giguer P. A.(1966년)를 참조하십시오. "주기적인 시스템을 위한 '새로운 모습'" 캐나다의 화학 제18권 (12) : 36–39 (37 페이지 참조)
- ^ Stowe, Timothy. "Physicist's Periodic Table 1989". jeries.rihani.com. Retrieved 24 September 2019.
A physicist's chart of the chemical elements
- ^ Bradley, David (20 July 2011). "At Last, A Definitive Periodic Table?". ChemViews. ChemistryViews.org. doi:10.1002/chemv.201000107. Retrieved 24 September 2019.
- ^ Rich, Ronald L. (2005). "Are Some Elements More Equal Than Others?". J. Chem. Educ. 82 (12): 1761. Bibcode:2005JChEd..82.1761R. doi:10.1021/ed082p1761.
- ^ Clancy, Christina; et al. (2010). Chemistry 11. Canada: McGraw-Hill Ryerson. p. 28. ISBN 978-007091575-6.
- ^ Leach, M. R. "ADOMAH Periodic Table by Valery Tsimmerman". Internet Database of Periodic Tables. Retrieved July 29, 2019.; Stewart, P. J. (2010). "Charles Janet: unrecognized genius of the periodic system". Foundations of Chemistry. 12 (1): 5–15. doi:10.1007/s10698-008-9062-5. S2CID 171000209.
- ^ 스튜어트, P.(2018년).화학에서 "아마추어들은, 프로:.주기율 table" 사례Scerri, E, 라스 레스트레포, G.(eds.)에서.멘델레 예프 Oganesson까지:Multidisciplinary적 관점에서 주기율 표상에서.뉴욕:옥스포드 대학 출판부.를 대신하여 서명함. 66–79(76–77).아이 에스비엔 978-0-190-66853-2., 리치, M.R."ADOMAH 주기율 표 유리 큐브".인터넷 데이터베이스 주기율 표의.Retrieved 8월 1일 2019년.
- ^ Amato, Ivan (November 21, 2006). "Beyond The Periodic Table Metal clusters mimic chemical properties of atoms". Chemical & Engineering News.
- ^ Norman, Nick (November 26, 2020). "Periodic table: scientists propose new way of ordering the elements". The Conversation. Retrieved November 28, 2020.
- ^ Ball, Philip (November 18, 2020). "New ordering of elements could help find materials with promising properties". Chemistry World. Retrieved November 28, 2020.
- ^ Allahyan, Zahed; Oganov, Artem R. (October 20, 2020). "Nonempirical Definition of the Mendeleev Numbers: Organizing the Chemical Space". The Journal of Physical Chemistry. 124 (43): 23867–23878. arXiv:2007.00091. doi:10.1021/acs.jpcc.0c07857. Retrieved November 28, 2020.
추가 읽기
- 당시 알려진 표에 대한 1974년 검토는 이 주제에 대한 확정적인 작품으로 간주된다:[1] 100년 동안의 주기적 시스템의 그래픽 표현. 앨라배마 대학 출판부, 1974년 ISBN 0-8173-3200-6
- 히외를랜드, 버거(2011년). 주기율표와 분류철학. 지식 조직, 38(1), 9-21.
외부 링크
- 미시간 주립 대학교 동문회 지식네트워크가 관리하는 사이트 다양한 방식으로 주기율표 표현
- 로버트 해리슨의 현대 나선 주기율표
- 자넷의 왼발 주기율표
- 메이트네리움이 하시움이 가져야 할 위치를 차지함에 따라 제리스 리하니가 제시한 물리학자 주기율표에 대한 수정.
- 대체 주기율표에 관한 유선 기사
- 주기율표 선택
- 아마존닷컴은 주기율표를 나선형으로 배열한다.
- Rotaperiod.com 새로운 주기율표.
- Z-스파이럴의 티셔츠 위상 참고.
- 원소의 새로운 주기율표는 정사각형 3각형의 주기적 배열로 되어 있다.
- 전자 구성 기반 주기율표
- 주기율표 데이터베이스
- 원소의 주기적 프랙탈
- 전자 그룹화를 더 잘 설명하기 위해 사용되는 성질에 의해 다시 그룹화하는 A 원소의 Bob Doyle 주기적 표
- 에릭 스크리의 웹사이트 주기율표에 관한 것
- 지구과학자 주기율표
- ^ Kauffman, George B. (1975). "Graphic representations of the periodic system during one hundred years (Mazurs, Edward G.)". Journal of Chemical Education. 52 (9): A436. doi:10.1021/ed052pA436.1.