불소 구조
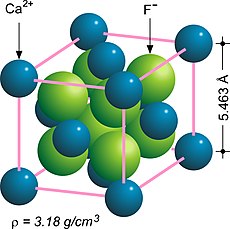
Fluorite structure고체 화학에서 불소 구조는 MX라는2 공식을 가진 화합물에 대한 일반적인 모티브를 말한다.[1][2]X 이온은 8개의 사면체 중간 부위를 차지하고 M 이온은 얼굴 중심 입방체(FCC) 구조의 정규 부위를 차지하고 있다.많은 화합물, 특히 일반 미네랄 플루오르산염(CaF2)은 이 구조를 채택한다.
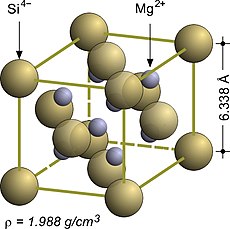
X가 원소 Si, Ge, Sn 또는 Pb 중 하나가 될 수 있는 MgX와2 같은 마그네슘 화합물은 음이온과 양이온의 위치가 불소(대구조물)에 비해 역전되기 때문에 부동액 구조를 가지고 있다고 하며, 음이온은 FCC 정규 사이트를 점유하는 반면 양이온은 사면체 간 사이트를 점유한다.마그네슘실산염2 MgSi는 격자 매개변수 6.338 å을 가지며, 마그네슘 양이온이 사면체 중간 부지를 점유하고 있으며, 각각의 사면체 음이온은 8개의 마그네슘 양이온에 둘러싸여 있고, 각 마그네슘 양이온은 4개의 사면체 방식으로 4개의 사면체 음이온에 둘러싸여 있다.[3]
| 재료 | 격자 상수(å) | 결정구조 |
|---|---|---|
| BAF2 | 6.196 | 플루오르산염(Fluorite |
| β-PbF2 | 5.94 | 플루오르산염(Fluorite |
| 푸오2 | 5.399 | 플루오르산염(Fluorite |
| SRF2 | 5.7996 | 플루오르산염(Fluorite |
| UO2 | 5.47065 | 플루오르산염(Fluorite |
| CAF2 | 5.463 | 플루오르산염(Fluorite |
| 제로2 | 5.14 | 플루오르산염(Fluorite |
| K2O | 6.449 | 부동액(FCC) |
| K2S | 7.406 | 부동액(FCC) |
| 리오2 | 4.61 | 부동액(FCC) |
| Na2O | 5.55 | 부동액(FCC) |
| 나스2 | 6.54 | 부동액(FCC) |
| RBO2 | 6.74 | 부동액(FCC) |
| Mg2Si | 6.338 | 부동액(FCC) |
불소 칼슘 예제
결정학은 결정 물질의 구조를 조사하는 강력한 도구다.구조-재산 관계를 형성하기 위해서는 재료의 결정 구조를 이해하는 것이 중요하다.이러한 관계는 결정 물질의 행동을 예측하는 데 도움을 줄 수 있을 뿐만 아니라 그 성질을 조절하는 능력을 도입할 수 있다.불소화칼슘은 불소 구조를 가진 결정체의 전형적인 예다.결정학적 정보는 X선 회절을 통해 수집될 수 있으며 결정 구조 내에서 전자 밀도의 위치에 대한 정보를 제공한다.Olex2와 같은 현대 소프트웨어를 사용하면 결정학적 출력 파일에서 결정 구조를 해결할 수 있다.[4]
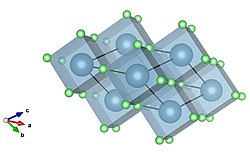
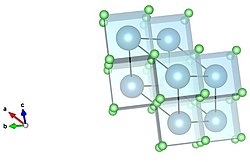
불소화칼슘 결정구조의 전경
불소화 칼슘에서는 칼슘 양이온을 사면 부위를 차지하고 있는 불소 음이온에 둘러싸여 있는데, 8:4의 조정 번호로 불소부터 칼슘까지의 조정 번호로 되어 있다.이 배급량은 불소 대 칼슘의 비율이 2:1인 화합물의 스토이치측정법과 일치한다.이 관계는 칼슘 양이온을 둘러싸고 있는 입방체 배열로 시각화할 수 있다.
확장 불소 구조
셀까지를 넘어서 불소의 확장 결정 구조는 얼굴 중심 입방체(fcc) 패킹 리큐어(cubic close packed 또는 ccp라고도 한다)에서 패킹을 계속한다.[5]이 구형 패킹의 패턴은 ABC 패턴을 따르며, 각각의 연속된 구 층이 격자의 인접한 구멍 위에 자리를 잡는다.이와는 대조적으로 육각형 클로즈패킹(hcp)은 ABAB 패턴으로 연속적으로 레이어드된다.이 두 종류의 포장재는 가장 촘촘하게 포장된 형태의 구형 포장이다.[6]
참고 항목
참조
- ^ Holleman, Arnold Frederik; Wiberg, Egon (2001), Wiberg, Nils (ed.), Inorganic Chemistry, translated by Eagleson, Mary; Brewer, William, San Diego/Berlin: Academic Press/De Gruyter, ISBN 0-12-352651-5
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ a b c d Rizescu, Costel; Rizescu, Mihaela (2018). Structure of Crystalline Solids, Imperfections and Defects in Crystals (First ed.). Parker, TX: Shutter Waves. ISBN 978-1-947641-17-4. Retrieved 29 January 2020.
- ^ "OlexSys". OlexSys.
- ^ Shriver; et al. (January 2014). Inorganic Chemistry (Sixth ed.). Oxford University Press. ISBN 978-1-4292-9906-0.
- ^ Redwing, Ronald. "Face Centered Cubic Structure (FCC)". The Pennsylvania State University.