바인딩 선택성
Binding selectivity결합선택성은 착체를 형성하는 기판에 대한 리간드의 결합에 관해 정의된다.결합 선택성은 리간드가 어떻게 [1]다른 수용체보다 한 수용체에 더 우선적으로 결합할 수 있는지를 기술한다.선택도계수는 기판과의 복합체 중 다른 배위자의 한쪽 배위자에 의한 변위반응의 평형상수이다.결합 선택성은 생화학[2] 및 화학적 분리 과정에서 매우 중요하다.
선택 계수
선택성의 개념은 하나의 화학물질 A가 다른 두 가지 화학물질 B와 C를 결합하는 정도를 정량화하기 위해 사용된다.가장 간단한 경우는 형성된 복합체가 1:1 화학량계를 갖는 경우이다.그러면, 두 상호작용은 평형 상수AB K와AC [note 1]K로 특징지을 수 있다.
[X]는 물질 X(A, B, C, …)의 농도를 나타낸다.선택성 계수는 두 평형 상수의 비율로 정의된다.
이 선택성 계수는 사실 변위 반응에 대한 평형 상수이다.
동일한 정의가 다른 화학측정학 AB와pq ACpq 복합체에 적용된다는 것을 쉽게 알 수 있다.선택성 계수가 클수록 리간드 C는 기질 A와 형성된 착화체로부터 리간드 B를 더 많이 치환한다.또 다른 해석은 선택성 계수가 클수록 B를 AB에서 이동시키는 데 필요한 C의 농도가 낮다는 것입니다.선택성 계수는 두 평형상수 K와ABAC K를 측정하여 실험적으로 구한다.
적용들
생화학
생화학에서 기질은 수용체로 알려져 있다.수용체는 하나 이상의 특정 종류의 신호 전달 분자가 결합할 수 있는 세포막 또는 세포질 중 하나에 내장된 단백질 분자입니다.배위자는 펩타이드 또는 신경전달물질, 호르몬, 의약품 또는 독소와 같은 다른 작은 분자일 수 있다.수용체의 특이성은 공간 기하학 및 수소 결합 또는 반데르발스 [3]힘과 같은 비공유 상호작용을 통해 리간드에 결합하는 방식에 의해 결정됩니다.
수용체를 분리할 수 있는 경우에는 수용체, 작용제를 자극하거나 길항제인 수용체를 차단하는 합성약을 개발할 수 있다.위궤양 약물인 시메티딘은 수용체를 포함하는 분리 조직에 대한 최대의 특이성을 위해 분자를 화학적으로 엔지니어링하여 H 길항제로서2 개발되었습니다.정량적 구조-활성 관계(QSAR)의 추가 사용은 라니티딘과 같은 다른 약물의 개발로 이어졌다.
약물을 언급할 때 "선택성"은 절대적이지 않고 상대적이라는 점에 유의해야 한다.예를 들어, 더 높은 용량에서 특정 약물 분자는 "선택적"이라고 하는 수용체보다 다른 수용체에 결합할 수도 있다.
킬레이트 요법
킬레이트 요법은 킬레이트 배위자가[note 2] 선택적으로 몸에서 금속을 제거하기 위해 사용되는 의료 치료의 한 형태이다.금속이 납2+, Pb, 수은과 같이 2가 이온으로 존재할 경우 처리 과정에서 필수 [4]금속이 제거되지 않기 위해 칼슘, Ca2+ 및 마그네슘 Mg에2+ 대한 Hg2+ 선택성이 필수적입니다.
선택성은 다양한 요인에 의해 결정됩니다.수혈을 받은 β-thalesemia 개체에서 발생할 수 있는 철 과부하의 경우, 표적 금속 이온은 +3 산화 상태이므로 2가 이온보다 더 강한 복합체를 형성한다.또한 질소 기증자 리간드보다 산소 기증자 리간드와 더 강한 복합체를 형성합니다. 디페록사민은 악티노박터 스트렙토미세스 필로수스에 의해 생성되어 킬레이트 치료제로 초기에 사용되었습니다.디페록사민의 알려진 구조를 출발점으로 [5][6]하여 디페로프론 및 디페라시록스와 같은 합성 시데로포어가 개발되었습니다.킬레이트화는 두 개의 산소 원자와 함께 일어난다.
윌슨병은 구리 대사의 결함으로 인해 신체의 여러 기관에 구리 금속이 축적되는 것이다.이 경우 타깃 이온은 2가 Cu이다2+.이 이온은 아흐랜드, 채트, 데이비스 [7]제도에서 경계선으로 분류된다.이는 공여 원자가 N, O 또는 F인 리간드와 공여 원자가 P, S 또는 Cl인 리간드와 거의 동일하게 강한 복합체를 형성한다는 것을 의미한다.질소와 황 공여 원자를 포함하는 페니실라민은 이러한 유형의 배위자가 칼슘과 마그네슘 이온보다 구리 이온에 더 강하게 결합하기 위해 사용됩니다.
납과 수은과 같은 중금속에 의한 중독 처리는 더 문제가 있는데, 사용된 리간드는 칼슘에 비해 높은 특이성을 가지고 있지 않기 때문이다.예를 들어 중금속과 함께 뼈에서 칼슘의 제거를 줄이기 위해 EDTA를 칼슘염으로 투여할 수 있다.아연, 카드뮴 및 칼슘에 대한 납의 선택성을 결정하는 요소들이 [8]검토되었다.
크로마토그래피
컬럼 크로마토그래피에서는 물질의 혼합물이 이동상으로 용해되어 컬럼 내의 정지상 위를 통과한다.선택성 계수는 분포 계수의 비율로 정의되며, 이는 정지상과 이동상 사이의 분석물질의 평형 분포를 기술한다.선택성 계수는 정적 위상(이 경우 기판)의 활동이 순수 [9]위상에 대한 표준 가정인 1과 같다는 추가 가정과 함께 선택성 계수와 같다.크로마토그래피 컬럼의 분해능S R은 다음과 같이 선택성 인자와 관련된다.
여기서 α는 선택성 인자, N은 이론판A k의B 수, k는 두 분석물질의 유지 계수이다.보존 요인은 분포 계수에 비례합니다.실제로 선택성 계수가 1에 매우 가까운 물질을 분리할 수 있다.이것은 특히 60m까지 컬럼 길이가 가능한 기액 크로마토그래피에서 매우 많은 이론적인 플레이트를 제공한다.
이온 교환 크로마토그래피에서 선택도 계수는 약간 다른[10] 방식으로 정의된다.
용제 추출
용제 추출은[11] 모나자이트와 같은 광석의 자연에서 발견되는 혼합물에서 개별 랜턴 원소를 추출하기 위해 사용됩니다.하나의 공정에서 수용액 중의 금속이온을 트리부틸인산(TBP)과 착화체를 형성하고 등유 등의 유기용매로 추출한다.완전한 분리는 역류 교환 방법을 사용하여 이루어집니다.다수의 셀이 캐스케이드로서 배치된다.평형 후 각 셀의 수성분을 이전 셀로 옮기고 유기성분을 다음 셀로 옮긴다.다음 셀은 처음에는 물만 포함한다.이렇게 해서 가장 안정된 착체를 가진 금속 이온은 유기상에서 캐스케이드를 통과하고, 가장 안정적인 착체를 가진 금속은 수상에서 [12]캐스케이드를 통과한다.
유기상에서의 용해도 문제가 되지 않는 경우에는 선택도 계수가 2개의 금속이온의 TBP 착체의 안정성 상수 비율과 같다.주기율표에 인접한 란타노이드 원소의 경우 이 비율이 1보다 크지 않기 때문에 캐스케이드에는 많은 셀이 필요합니다.
화학 센서
전위차 선택성 계수는 특정 이온을 다른 이온과 구별하는 이온 선택성 전극의 능력을 정의한다.선택도 계수 K는B,C 1차 이온 B와 간섭 이온 C(고정 간섭법) 이하의 혼합 용액에서 B와 C(분리 용액법)[13]의 이온 선택 전극의 emf 응답에 의해 평가된다.예를 들어 자연적으로 발생하는 대환상 항생제 발리노마이신을 이용하는 칼륨 이온 선택막 전극.이 경우, 대순환 고리의 공동은 칼륨 이온을 캡슐화하기에 딱 알맞은 크기이지만, 나트륨 이온을 강하게 결합하기에는 너무 큽니다. 가장 가능성이 높은 간섭입니다.
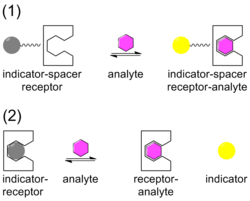
화학적 [14][15]센서는 표적(게스트)이 센서(호스트)와 복합체를 형성하는 특정 표적 분자와 이온을 위해 개발되고 있다.센서는 최대 바인딩 선택성을 제공하기 위해 타깃의 크기와 모양에 있어 최적의 조합이 되도록 설계되었습니다.인디케이터는 타겟이 센서와 콤플렉스를 형성할 때 변경되는 센서와 관련되어 있습니다.인디케이터의 변화는 일반적으로 흡광도 또는 감도가 높은 발광에서 볼 수 있는 색상 변화(그림에서는 회색에서 노란색으로)입니다.표시등은 ISR 배열로 스페이서를 통해 센서에 부착되거나 센서 IDA 배열에서 변위될 수 있습니다.
「 」를 참조해 주세요.
메모들
레퍼런스
- ^ Srinivasan, Bharath (March 2022). "A guide to enzyme kinetics in early drug discovery". The FEBS Journal. doi:10.1111/febs.16404. ISSN 1742-464X.
- ^ Klotz, I.M. (1997). Ligand-Receptor Energetics: A Guide for the Perplexed. Wiley. ISBN 978-0-471-17626-8.
- ^ Foreman, J.C.; Johansen, T., eds. (2003). Textbook of receptor pharmacology (2nd. ed.). Boca Raton, Fla.: CRC Press. ISBN 978-0-8493-1029-4.
- ^ Walker, M.; Shah, H.H. (1997). Everything you should know about chelation therapy (4th ed.). New Canaan, Conn.: Keats Pub. ISBN 978-0-87983-730-3.
- ^ Iron-Selective Chelators 치료적 잠재력으로 Hider, 로버트 C., 홍콩, Xiaole(2013년)에서."8장.아이언:과부하와 Deficiency"에 미치는 영향아스트리드 시겔, 헬무트 시겔과 롤랜드 K.O. 시겔(교육.)에서.필수 금속 이온은 인체에 질병 사이에성.금속 이온은 생명 과학에.Vol13.도르드레흐트:스프링거.를 대신하여 서명함. 229–294. doi:10.1007/978-94-007-7500-8_8.아이 에스비엔 9789400774995.PMID 24470094.
- ^ Miller, Marvin J. (1989). "Syntheses and therapeutic potential of hydroxamic acid-based siderophores and analogs". Chemical Reviews. 89 (7): 1563–1579. doi:10.1021/cr00097a011.
- ^ Ahrland, S.; Chatt, J.; Davies, N.R. (1958). "The relative affinities of ligand atoms for acceptor molecules and ions". Quart. Rev. 12 (3): 265–276. doi:10.1039/QR9581200265.
- ^ Farkas, Etelka; Buglyó, Péter (2017). "Chapter 8. Lead(II) Complexes of Amino Acids, Peptides, and Other Related Ligands of Biological Interest". In Astrid, S.; Helmut, S.; Sigel, R. K. O. (eds.). Lead: Its Effects on Environment and Health. Metal Ions in Life Sciences. Vol. 17. Berlin, Boston: de Gruyter. pp. 201–240. doi:10.1515/9783110434330-008. ISBN 9783110434330. PMID 28731301.
- ^ Skoog, D.A; West, D.M.; Holler, J.F.; Crouch, S.R. (2004). Fundamentals of Analytical Chemistry (8th ed.). Thomson Brooks/Cole. ISBN 978-0-03-035523-3. 섹션 30E
- ^ IUPAC, 화학 용어집, 제2판('골드북') (1997).온라인 수정판: (2006–) "선택성 계수, 이온A/B 교환 크로마토그래피에서 k". doi:10.1351/goldbook.S05566.html
- ^ Rice, N.M.; Irving, H. M. N. H.; Leonard, M.A (1993). "Nomenclature for liquid-liquid distribution (solvent extraction)". Pure Appl. Chem. IUPAC. 65 (11): 2373–2396. doi:10.1351/pac199365112373. S2CID 98514016.
- ^ Rydberg, J.; Musikas, C; Choppin, G.R., eds. (2004). Solvent Extraction Principles and Practice ( (2nd. ed.). Boca Raton, Fla.: CRC Press. ISBN 978-0-8247-5063-3.
- ^ Buck, R. P.; Linder, E. (1994). "Recommendations for nomenclature of ion-selective electrodes". Pure Appl. Chem. IUPAC. 66 (12): 2527–2536. doi:10.1351/Pac199466122527. S2CID 97126225.
- ^ Florinel-Gabriel Bénicha, 화학 센서 및 바이오 센서:Fundamentals and Applications, John Wiley and Sons, Chichester, 2012, ISBN 978-0-470-71066-1 인쇄
- ^ Cattrall, R.W. (1997). Chemical sensors. Oxford University Press. ISBN 978-0-19-850090-2.
![{\displaystyle {\ce {{A}+B<=>AB;{\mathit {K}}_{AB}={\frac {[AB]}{[A][B]}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/66c8b6d30bca33bf83d8b6d3125e0017b14896df)
![{\displaystyle {\ce {{A}+C<=>AC;{\mathit {K}}_{AC}={\frac {[AC]}{[A][C]}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/90f08f540ba07091047ede3f67d93ae37a54c512)

![{\displaystyle {\ce {{AB}+C<=>{AC}+B;{\mathit {K}}_{B,C}={\frac {[AC][B]}{[AB][C]}}={\frac {{\mathit {K}}_{AC}[A][B][C]}{{\mathit {K}}_{AB}[A][B][C]}}={\frac {{\mathit {K}}_{AC}}{{\mathit {K}}_{AB}}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/02cfde6d3068bc904e109ff7d6f181821a4c2b57)