플로우 세포 측정
Flow cytometry 흡착 빨대가 있는 플로우 세포계 튜브 | |
| 분류 | 세포측정학 |
|---|---|
| 분석물 | 세포 또는 입자 |
| 기타 기술 | |
| 관련된 | 콜터 카운터 |
플로우 세포측정법(FC)은 세포 또는 [1][2][3][4]입자의 집단의 물리적 및 화학적 특성을 검출하고 측정하는 데 사용되는 기술입니다.
이 과정에서 세포 또는 입자를 포함한 시료를 유체 중에 부유시켜 플로우 세포계 기기에 주입한다.샘플은 레이저 빔을 통해 한 번에 하나의 셀을 이상적으로 흐르도록 초점이 맞춰져 있습니다. 여기서 산란된 빛은 셀과 그 구성요소에 특징적입니다.세포는 종종 형광 마커로 표시되기 때문에 빛이 흡수되고 파장 대역으로 방출됩니다.수만 개의 세포를 빠르게 검사할 수 있고 수집된 데이터는 컴퓨터로 [citation needed]처리됩니다.
플로우 세포측정법은 기초 연구, 임상 실습 및 임상 시험에서 일상적으로 사용됩니다.흐름 세포 측정에는 다음과 같은 용도가 있습니다.
플로우 세포측정 분석기는 샘플에서 정량 가능한 데이터를 제공하는 기기입니다.플로우 세포측정법을 사용하는 다른 기구로는 광학적 특성에 따라 물리적으로 대상 세포를 분리하여 정화시키는 세포 선별기가 있다.
역사
콜터 원리를 이용한 최초의 임피던스 기반 흐름 세포측정 장치는 1953년 월러스 H. 콜터에게 발행된 미국 특허 2,656,508에서 공개되었다.맥 풀와일러는 오늘날의 흐름 세포계 - 특히 세포 선별기의 [5]선구자였습니다.풀와일러는 이것을 1965년 [6]사이언스에 출판하면서 개발했다.최초의 형광 기반 플로우 세포 측정 장치(ICP 11)는 1968년 몬스터 대학의 볼프강 괴데에 의해 개발되었으며, 1968년 12월[7] 18일 특허를 출원했으며, 1968/69년 괴팅겐의 독일 개발자 및 제조업체인 파르텍에 의해 처음 상용화되었다.당시 흡수법은 [8]형광법보다 다른 과학자들에 의해 여전히 널리 선호되었다.곧이어 Bio/Physics Systems Inc(1971)의 Cytofluorograph(1971년)를 포함한 플로우 세포측정기기가 개발되었다.Ortho Diagnostics), Partec의 PAS 8000(1973), Becton Dickinson(1974), Partec/Phywe의 ICP 22(1975), Coulter의 Epics(1977/78).특허받은 마이크로유체학 "랩온칩"에 기반한 최초의 라벨이 없는 고주파 임피던스 플로우 세포계인 Ampa Z30은 Ampasys(2012)[citation needed]에 의해 도입되었습니다.
테크놀로지명
형광 기반 플로우 세포 측정 기술의 원래 이름은 "펄스 세포 측정"이었습니다(독일어:임펄스지토포토메트리)는 형광 기반 흐름 세포계에 대한 첫 번째 특허 출원에 기초한다.1976년 펜사콜라(플로리다)에서 열린 제5회 미국공학재단 자동화 세포학 컨퍼런스에서 최초의 형광 기반 흐름 세포계(1968년)가 도입된 지 8년 만에 "흐름 세포계"라는 용어를 사용하는 것에 [9]합의하였다.
유동 세포계
현대의 흐름 세포계는 초당 수천 개의 입자를 "실시간"에 분석할 수 있으며, 세포 선별기로 구성되면 유사한 속도로 특정 광학 특성을 가진 입자를 능동적으로 분리 및 분리할 수 있습니다.플로우 세포계는 현미경과 유사하지만, 플로우 세포계는 세포의 이미지를 생성하는 대신 세포별로 지정된 광학 파라미터의 높은 스루풋, 자동화된 정량화를 제공한다.고형 조직을 분석하려면 먼저 단세포 현탁액을 준비해야 [citation needed]한다.
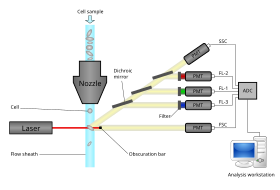
플로우 세포계는 플로우 셀, 측정 시스템, 검출기, 증폭 시스템 및 신호 해석용 컴퓨터의 5가지 주요 부품을 가진다.플로우 셀에는 액체 스트림(시스 유체)이 있어 셀이 광선을 통과하도록 셀을 운반하고 정렬합니다.측정 시스템은 일반적으로 임피던스(또는 전도성) 및 광학 시스템(램프, 제논), 고출력 수냉식 레이저(아르곤, 크립톤, 염료 레이저), 저전력 공랭식 레이저(아르곤(488 nm), 적색-HeNe(633 nm), 녹색-HeNe, 백색(UV), 녹색 레이저(녹색 레이저)를 사용합니다.검출기 및 아날로그-디지털 변환(ADC) 시스템은 전방 산란광(FSC) 및 측면 산란광(SSC) 및 염료 특정 형광 신호의 아날로그 측정을 컴퓨터가 처리할 수 있는 디지털 신호로 변환합니다.증폭 시스템은 선형 또는 [citation needed]로그일 수 있습니다.
흐름 세포계를 사용하여 샘플에서 데이터를 수집하는 과정을 "획득"이라고 합니다.획득은 플로우 세포계에 물리적으로 연결된 컴퓨터와 세포계와의 디지털 인터페이스를 처리하는 소프트웨어에 의해 중재됩니다.소프트웨어는 테스트 중인 샘플에 대한 파라미터(예: 전압, 보상)를 조정할 수 있으며, 파라미터가 올바르게 설정되었는지 확인하기 위해 샘플 데이터를 수집하는 동안 초기 샘플 정보를 표시하는 데도 도움이 됩니다.초기 플로우 세포계는 일반적으로 실험 장치였지만, 기술 발전으로 임상 및 연구 목적 모두에 광범위하게 사용될 수 있게 되었다.이러한 발전으로 계측, 분석 소프트웨어 및 형광표지 항체와 같은 획득에 사용되는 시약의 상당한 시장이 개발되었습니다.
현대의 기기들은 보통 여러 개의 레이저와 형광 검출기를 가지고 있다.현재 상용 기기의 기록은 10개의[10] 레이저와 30개의 형광 [11]검출기입니다.레이저와 검출기의 수를 늘리면 여러 항체 라벨링이 가능하며 표현형 마커로 대상 집단을 보다 정확하게 식별할 수 있습니다.특정 기기는 심지어 개별 셀의 디지털 이미지를 촬영할 수 있기 때문에 세포 내부 또는 표면에서 형광 신호 위치를 분석할 수 있습니다.
하드웨어
유세포계의 유체 소자 시스템
모든 흐름 [12][13][14]세포계에서 세포의 광학 특성을 정확하게 측정하기 위해 세포는 집속 레이저 빔의 중심을 균일하게 통과해야 합니다.유체 시스템의 목적은 레이저 빔을 통해 기기 전체에 걸쳐 하나씩 셀을 이동하는 것입니다.세포 분류 기능이 있는 플로우 세포계의 유체 소자는 또한 스트림을 사용하여 분류된 세포를 채집 튜브나 [12]웰로 운반합니다.
유체 역학적 포커싱
액체 분사 내 셀의 정확한 위치 지정을 위해 대부분의 [12][13][14]셀미터에서 유체 역학적 포커싱이 사용됩니다.현탁 상태의 셀은 외부 칼집 유체로 둘러싸인 기기 안으로 들어갑니다.검체 코어는 시스 유체의 중앙에 유지됩니다.샘플 입력 속도 또는 셀이 레이저 조사까지 흐르는 속도는 샘플 코어에 있는 피복 유체의 압력에 의해 제어될 수 있습니다.최적의 상태에서는 중앙 유체 흐름과 피복액이 [citation needed]혼합되지 않습니다.
음향 보조 유체 역학적 포커싱
음향 포커싱 기술은 유체 역학적 [12][14]포커싱을 지원하기 위해 일부 흐름 세포계에서 사용됩니다.음파(>2MHz)는 시스 유체를 도입하기 전에 시료의 초점을 미리 맞춘다.그런 다음 사전 초점을 맞춘 샘플이 유체역학적 코어로 주입되어 계측기를 통해 흐릅니다.이렇게 하면 높은 샘플 입력 속도에서 데이터 정확도가 향상될 수 있습니다.
광학 및 전자제품
광학 필터
형광체에서 방출되는 빛은 파장의 스펙트럼이기 때문에 여러 형광체를 결합하면 겹칠 수 있습니다.특수성을 추가하기 위해 광학 필터와 다이크로익 미러를 사용하여 광전자 증배관(PMT) 또는 눈사태 포토다이오드(APD)[12]와 같은 검출기로 빛을 필터링하고 이동시킨다.광학 필터는 밴드 패스(BP), 롱 패스(LP) 또는 쇼트 패스(SP) 필터로 설계되어 있습니다.대부분의 흐름 세포계는 광학 스펙트럼의 특정 대역을 선택하기 위해 다이크로익 미러와 밴드 패스 필터를 사용합니다.
프리즘, 격자 및 스펙트럼 흐름 세포 측정
스펙트럼 플로우 세포측정법은 프리즘 또는 회절 격자를 사용하여 검출기 [12][15]어레이 전체에 마커의 방출광을 분산시킨다.이를 통해 각 입자의 전체 스펙트럼을 측정할 수 있다.단일 세포에서 측정된 스펙트럼은 사용된 모든 염료와 자기 형광 스펙트럼의 기준 스펙트럼을 사용하여 혼합되지 않는다.이를 통해 보다 넓은 패널 설계와 새로운 생물학적 [citation needed]마커를 적용할 수 있습니다.
영상 흐름 세포 측정
영상 흐름 세포 측정(IFC)은 세포의 멀티 [12][16]채널 이미지를 캡처합니다.이미징 플랫폼에서 사용되는 검출기는 개별 세포의 이미지를 캡처하기 위해 전하결합소자(CCD) 또는 상보적인 금속산화물반도체(CMOS)를 장착할 수 있다.
데이터 분석
보상
각 형광 색소는 넓은 형광 스펙트럼을 가지고 있다.두 개 이상의 형광 크롬을 사용하면 형광 크롬 간에 중첩이 발생할 수 있습니다.이 상황을 스펙트럼 오버랩이라고 부릅니다.이 상황은 극복되어야 한다.예를 들어 FITC 및 PE의 발광 스펙트럼은 플루오레신이 방출하는 빛이 PE에 사용되는 필터를 통과할 때 동일한 파장과 겹치는 것이다.이 스펙트럼 오버랩은 PE 신호에서 FITC 신호의 일부를 제거함으로써 또는 그 반대로 보정됩니다.이 과정은 색 보정이라고 불리며,[17] 스스로 측정하는 비율로 형광색을 계산합니다.
보정은 다중 매개 변수 흐름 세포 측정 데이터의 스펙트럼 중첩을 보정하는 수학적 과정이다.형광색소는 스펙트럼이 광범위할 수 있기 때문에 중복될 수 있으며, 데이터 분석 시 혼동의 바람직하지 않은 결과를 초래할 수 있다.이러한 오버랩은 스필오버로 알려져 스필오버 계수로 정량화되며, 일반적으로 다른 형광 색소에서 파장의 유의한 피크를 측정하는 특정 형광 색소에 대한 검출기에 의해 발생한다.선형대수는 이러한 [17]보정을 위해 가장 자주 사용된다.
일반적으로 1개 이상의 모수의 그래프가 표시되는 경우 다른 모수가 표시된 분포에 기여하지 않음을 나타냅니다.특히 2배 이상의 파라미터를 사용할 경우 이 문제는 더욱 심각합니다.현재 다차원 매개변수를 효율적으로 표시할 수 있는 도구는 발견되지 않았습니다.세포간의 차이를 알기 위해서는 보상이 매우 중요하다.
[필요한 건]
게이트
흐름 세포계에 의해 생성된 데이터는 단일 차원, 히스토그램, 2차원 점 그림, 또는 3차원으로 플롯할 수 있습니다.이러한 플롯의 영역은 형광 강도에 기초하여 "게이트"라고 불리는 일련의 부분 집합 추출을 만들어 순차적으로 분리할 수 있다.특히 혈액학과 관련하여 진단 및 임상 목적으로 특정 탕구 프로토콜이 존재합니다.개별 단일 셀은 좁게 초점을 맞춘 레이저[18] 빔을 통해 "비행 시간" ("펄스 폭"으로도 표시됨)에 의해 종종 셀 이중점 또는 더 높은 집합체와 구별됩니다.
플롯은 종종 로그 척도로 작성됩니다.서로 다른 형광 염료의 방출 스펙트럼이 [19][20]겹치기 때문에 검출기의 신호는 계산뿐만 아니라 전자적으로도 보정되어야 한다.플로우 세포계를 사용하여 축적된 데이터는 소프트웨어를 사용하여 분석할 수 있습니다.일단 데이터가 수집되면, 유량 세포계에 연결된 상태를 유지할 필요가 없으며, 대부분의 경우 분석은 [citation needed]별도의 컴퓨터에서 수행됩니다.이는 특히 이러한 [citation needed]기계의 사용이 많은 핵심 시설에서 필요합니다.
계산 분석
계산 방법을 사용한 자동화된 모집단 식별에 대한 최근의 발전은 전통적인 게이트 전략에 대한 대안을 제공했다.자동화된 식별 시스템은 희귀하고 숨겨진 모집단의 발견에 잠재적으로 도움을 줄 수 있다.대표적인 자동화 방법으로는 ImmPort의 [22]FLOCK, 바이오컨덕터의 SamSPECral 및 flowCluster[24][25][26], GenePattern의 FLAME 등이 있습니다.T-분산 확률 인접 임베딩(tSNE)은 2차원 "맵"[28]에서 복잡한 다차원 데이터를 시각화할 수 있도록 차원 축소를 수행하도록 설계된 알고리즘입니다.협력적인 노력으로 FlowCAP(Flow Cytometry: Critical Assessment of Population Identification Methods,[29] )라는 이름의 공개 프로젝트가 이루어졌으며, 흐름 세포 측정 데이터 클러스터링 방법을 비교 및 평가하고 이러한 방법의 적절한 사용과 적용에 대한 지침을 확립하기 위한 객관적인 방법을 제공한다.
FMO 제어
형광 마이너스 원(FMO) 컨트롤은 멀티 컬러 패널을 만들 때 데이터 해석에 중요합니다.다색 패널에서는 셀이 여러 개의 형광 색소로 동시에 얼룩집니다.FMO 제어는 특정 채널에서 형광 스필오버를 측정하여 보상을 허용합니다.FMO 컨트롤을 생성하려면 샘플이 테스트 중인 불소크롬을 제외한 모든 불소크롬으로 얼룩집니다. 즉, 4개의 다른 불소크롬을 사용하는 경우 FMO 컨트롤에 포함된 불소크롬은 3개뿐입니다(예: FMO - ABC_, AB_D, A_BC_CD).
플로우 세포측정법에 의한 세포분류
세포 분류는 특정 신체적 [12][14][30]특성의 유무에 따라 세포 집단을 정화시키는 방법이다.분류 기능이 있는 플로우 세포계에서 기기는 세포 크기, 형태학, 단백질 발현 등의 파라미터를 사용하여 세포를 검출한 후 액체 기술을 사용하여 세포를 분류하고 실험 후 사용하기 [12][14]위해 서브셋을 복구합니다.
최초의 시제품 선별기는 1965년 물리학자 맥 풀와일러가 새롭게 발명된 잉크젯 프린터와 [31]콜터 부피 센서를 결합함으로써 로스앨러모스 국립연구소(LANL)에서 만들어졌습니다.살아있는 세포 선별기 또는 형광 활성 세포 선별기(FACS)[a]는 Len Herzenberg에 의해 개발되었으며, 이후 2006년 그의 중요한 [33]업적으로 교토 상을 수상했다.
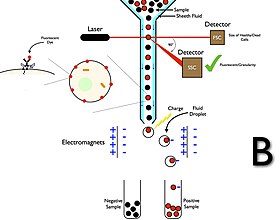
플로우 세포 측정 세포 선별기는 플로우 세포 측정 분석기와 달리 수집 시스템을 가지고 있습니다.채취 과정은 플로우 셀을 통과하는 시스 유체의 스트림에 샘플을 주입하고 레이저를 [34]가로채면 시작됩니다.그런 다음 스트림이 진동 노즐을 통해 셀을 운반하고, 이 노즐은 대부분 셀이 1개 또는 셀이 없는 물방울을 생성합니다.전류가 물방울이 되는 바로 그 지점에 대전링을 배치하고 형광강도를 측정하기 직전에 링에 전하를 재치한다.그 때문에, 물방울이 물방울로부터 끊어질 때에, 반대 전하가 물방울에 포착되어 대전된다.그리고 나서 대전된 물방울은 대전된 물방울을 용기로 전환하는 정전 편향 시스템을 통해 떨어집니다.일부 시스템에서는 전하가 스트림에 직접 인가되며, 액체 파단은 스트림과 동일한 부호의 전하를 유지합니다.물방울이 끊긴 후 스트림이 중립으로 돌아갑니다.수집한 후, 이 세포들은 더욱 배양되고, 조작되고,[citation needed] 연구될 수 있다.
라벨

플로우 세포측정법은 세포나 입자에서 산란된 빛의 성질을 사용하여 물리적 성질을 식별하거나 정량적으로 측정합니다.레이블, 염료 및 얼룩은 다중 모수 분석에 사용할 수 있습니다(셀에 대한 자세한 특성 이해).면역피노타이핑(Immunophetyping)은 염색약이나[35] 염색약과 같은 시약을 포함한 항체 및 기타 불소포자를 사용하여 세포의 이종 집단을 분석하는 것이다.
형광 라벨
플로우 세포 [19]측정에서 광범위한 형광체를 라벨로 사용할 수 있습니다.형광체 또는 단순히 "형광체"[citation needed]는 일반적으로 세포 또는 세포 내의 표적 특성을 인식하는 항체에 부착됩니다. 또한 세포막 또는 다른 세포 구조에 대한 친화력을 가진 화학적 실체에 부착될 수 있습니다.각 형광체는 특징적인 피크 들뜸 파장과 방출 파장을 가지며, 방출 스펙트럼이 겹치는 경우가 많다.따라서 사용할 수 있는 라벨의 조합은 형광색소를 자극하기 위해 사용되는 램프 또는 레이저의 파장과 이용 가능한 [36]검출기에 따라 달라진다.구별 가능한 형광 라벨의 최대 수는 17개 또는 18개로 생각되며,[37] 이 복잡성 수준은 중복 스펙트럼을 분리하기 위한 복잡한 디콘볼루션 알고리즘뿐만 아니라 아티팩트를 제한하기 위한 수고스러운 최적화가 필요하다.플로우 세포 측정에서는 정량적 도구로 형광을 사용합니다. 플로우 세포 측정의 최고 민감도는 공초점 현미경 검사와 같은 다른 형광 검출 플랫폼과 비교할 수 없습니다.절대 형광 감도는 일반적으로 공초점 현미경 검사에서 낮은데, 이는 초점 외 신호가 공초점 광학 시스템에 의해 거부되고 화상이 세포 전체의 모든 위치에서 개별 측정에서 연속적으로 생성되어 신호 [38]수집에 사용할 수 있는 시간이 줄어들기 때문입니다.
양자점
양자점은 때때로 좁은 방출 [citation needed]피크 때문에 전통적인 형광체 대신 사용됩니다.
동위원소 라벨링
질량 세포측정법은 항체에 부착된 랜타니드 동위원소를 이용해 형광 표시 한계를 극복한다.이 방법은 이론적으로 40~60개의 구별 가능한 라벨을 사용할 수 있으며 30개의 [37]라벨에 대해 입증되었다.질량 세포측정법은 기본적으로 흐름 세포측정법과는 다르다. 세포는 플라즈마에 도입되고 이온화되며 관련 동위원소는 비행시간 질량분석법을 통해 정량화된다.이 방법은 다수의 라벨을 사용할 수 있지만 현재 흐름 세포 측정보다 throughput 용량이 낮습니다.또한 분석된 세포를 파괴하여 [37]분류에 의한 회복을 방해한다.
세포계 비드 배열
형광 항체를 통해 개별 세포에 라벨을 붙이고 식별할 수 있는 능력 외에 사이토카인, 단백질 및 기타 인자와 같은 세포 생성물도 측정될 수 있다.ELISA 샌드위치 분석법과 마찬가지로 CBA(cytometric bead array) 분석법은 단일 분석에서 여러 분석물질을 구별하기 위해 크기와 형광 강도에 따라 전형적으로 구별되는 여러 비드 집단을 사용합니다.포착된 분석물의 양은 단백질의 2차 에피토프에 대한 비오티닐화 항체를 통해 검출되며, 이어서 스트렙타비딘-R-피코에리스린 처리가 이루어진다.비드상의 R-피코에리스린의 형광 강도는 488 nm 들뜸원을 갖춘 플로우 세포계에서 정량화된다.시료 중 관심단백질의 농도는 분석물질의 기존 농도의 연속희석으로부터 생성된 형광신호와 표준곡선의 신호를 비교함으로써 얻을 수 있다.일반적으로 Cytokine Bead Array(CBA; 사이토카인 비즈 어레이)라고도 불립니다.
임피던스 플로우 세포 측정
임피던스 기반의 단일 셀 분석 시스템은 일반적으로 콜터 카운터로 알려져 있습니다.그것들은 사실상 모든 종류의 세포와 입자를 세고 크기를 조정하는 잘 확립된 방법을 나타냅니다.라벨 프리 테크놀로지는 최근 "랩 온 어칩" 기반의 접근법 및 정적 직류(DC) 또는 저주파 AC장 [39][40]대신 고주파 교류(AC)를 무선 주파수 범위(100kHz~30MHz)에 적용함으로써 강화되고 있습니다.이 특허 기술은 매우 정확한 세포 분석을 가능하게 하며 멤브레인 캐패시턴스 및 생존 가능성과 같은 추가 정보를 제공합니다.비교적 작은 사이즈와 견고성으로 배터리 전원을 온사이트에서 사용할 수 있습니다.
측정 가능한 파라미터
- 아포토시스(양자화, DNA 분해 측정, 미토콘드리아 막 전위, 투과성 변화, 카스파아제 활성)
- 세포 부착(예를 들어 병원체-호스트 세포 부착)
- 엽록소 또는 피코에리스린과 같은 세포 색소
- 세포표면항원(CD(Cluster of Differency) 마커)
- 세포 생존력
- 순환 종양 세포: 분리 및 정화
- 암세포의 다제내성(MDR) 특성화
- 염색체 분석 및 분류(도서관 구축, 염색체 도료)
- (Flow-FISH 또는 BACs-on-Beads 테크놀로지에 의한) DNA 복사 번호 변화
- 효소 활성
- 글루타치온
- 세포내 항원(다양한 사이토카인, 2차 매개체 등)
- 막유동성
- 세포의 전기투과성 모니터링
- 핵항원
- 산화 버스트
- pH, 세포내 이온화 칼슘, 마그네슘, 막전위
- 단백질 발현 및 국재화
- 단백질 수식, 포스포단백질
- 빛의 산란은 세포나 다른 입자의 부피(전방 산란)와 형태학적 복잡성(측방 산란)을 측정하는 데 사용될 수 있다(비형광성 입자도 마찬가지).이들은 각각 FSC와 SSC로 약칭된다.
- 총 DNA 함량(세포 주기 분석, 세포 속도론, 증식, 배수성, 유배수성, 내복제 등)
- 총 RNA 함량
- 생체내 트랜스제닉 제품, 특히 녹색 형광 단백질 또는 관련 형광 단백질
- 다양한 조합(DNA/표면항원 등)
적용들
이 기술은 분자생물학, 병리학, 면역학, 바이러스학,[41] 식물생물학,[42] 해양생물학 등 다양한 분야에서 응용되고 있습니다.특히 성별 사전 선택을 위한 이식, 혈액학, 종양 면역학 및 화학 치료, 태아 진단, 유전학 및 정자 분류에 광범위하게 응용된다.플로우 세포측정법은 남성 [44]불임측정에서 DNA 조각화와[43] 관련된 정자세포 이상을 검출하기 위해 널리 사용된다.또한 DNA 손상,[45][46] 카스파아제 절단 및 아포토시스 [47]검출을 위한 연구에 광범위하게 사용된다.광음향 흐름 세포측정법은 염색된 [48]박테리오파지로 표시된 혈액 속의 박테리아를 검출, 구별 및 정량화하기 위해 다제내성 박테리아(MRSA) 연구에 사용됩니다.신경과학에서는 세포표면과 세포내 항원의 공발현도 [49]분석할 수 있다.미생물학에서는 GFP 부호화 트랜스포존(TnMHA)[50]으로 구축된 트랜스포존 돌연변이 라이브러리를 스크리닝 및 정렬하거나 [51]생존가능성을 평가하기 위해 사용할 수 있다.단백질 공학에서 플로우 세포측정법은 효모 표시 및 세균 표시와 함께 사용되어 원하는 특성을 가진 세포 표면 표시 단백질 변형을 식별한다.조직학 및 IHC보다 흐름 세포 측정의 주요 장점은 항원의 양을 정밀하게 측정할 수 있는 가능성과 현재 약 10개의 항체를 가진 실험실에서 각 세포를 여러 개의 항체로 염색할 수 있는 가능성이다.이는 현재 최대 40개까지 측정할 수 있는 질량 세포계보다 훨씬 적지만 더 비싸고 느린 속도입니다.
수생 연구
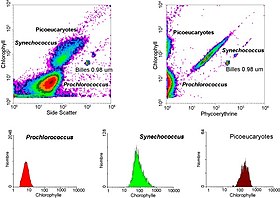
수계통에서 플로우 세포측정법은 자동 형광 세포 또는 형광 표지로 부가된 얼룩이 있는 세포의 분석에 사용된다.이 연구는 1981년 Clarice Yentsch가 적조에서의 형광을 측정하기 위해 유동 세포 측정법을 사용하면서 시작되었다.[52]그 다음 해에 연구자들은 형광 [53]특성에 따라 구별할 수 있는 여러 조류 종들의 흐름 세포 측정 결과를 발표했다.1983년까지 해양 연구원들이나 해수 샘플을 버뮤다에 수집된은phytoplankton 세포 살아 있지 않은 재료에서 청록 색 세균. 여러 인종으로 이뤄진 사회에서, 그 후에 실험실에서 국내 분류될 수 있게 구분할 수 있음을 보여 줄 상업적으로 이용 가능한 흐름 cytometers를 이용하여 그들 자신의 흐름 cytometers[54]을 제조하고 있었다고..[55]플로우 세포측정법은 또한 해양 연구자들이 조광성 프로클로로코쿠스와 현미경 검사를 통한 [56]평가로는 어려운 이종영양성 미생물을 구별할 수 있게 해주었다.기술의 진보로 수생과학자는 연구 순항[57] 중에 흐름 세포계를 계속 사용할 수 있게 되었고 흐름 세포계는 개별 식물성 플랑크톤 [58][59]세포의 이미지를 제공하기 위해 사용됩니다.해양 과학자들은 세포계의 분류 능력을 이용하여 세포 활동과 [60][61]다양성을 이산적으로 측정하고,[62] 가까이 사는 미생물들 간의 상호주의적 관계를 조사하며,[63] 해양에서 여러 과정의 생물 지구 화학적 비율을 측정합니다.
세포 증식 분석
세포 증식은 면역체계의 주요 기능이다.종종 몇 가지 결론을 내리기 위해 세포의 증식 특성을 분석해야 한다.세포 증식을 결정하기 위한 그러한 분석 중 하나는 추적 색소 카르복시플루오레세인 디아세테이트 숙시미딜에스테르(CFSE)이다.증식 세포를 감시하는 데 도움이 됩니다.이 검사는 시계열 [64]실험 중에 정량적 데이터와 정성적 데이터를 제공합니다.이 염료는 세포 안에 존재하는 장수하는 분자와 공유 결합합니다.세포들이 분열할 때, 분자들도 분열하고, 딸 세포들은 부모 집단보다 절반의 염료를 가지고 있다.이러한 강도 감소는 흐름 세포 측정으로 [65]시각화할 수 있습니다.문헌에서, 이 강력한 흐름 세포 측정과 CFSE 기술은 백혈병과 같은 암의 표적 세포를 죽이는 T세포의 효율성을 찾기 위해 사용되어 왔다.표적 세포 사멸을 빠르고 느리게 시각화하기 위해 과학자들은 특정 종류의 세포와 형광으로 표시된 마이크로 비드의 항체 염색과 함께 CFSE 라벨을 사용해 왔다.이것은 또한 특정 사이토카인 [66]치료 시 표적 세포의 증식에 대한 정보를 제공했다.
「 」를 참조해 주세요.
- 아포토시스 진행 중인 세포에 대한 검사인 Annexin A5 친화도 검사는 종종 흐름 세포 측정법을 사용한다.
- 세포주기분석
- 콜터 카운터
- 세포측정학
- 유전영동
- 플로우 세포 측정 표준
- 질량 세포 측정
- 마이크로 형광 측정
- 실행 가능성 분석
메모들
레퍼런스
- ^ Picot J, Guerin CL, Le Van Kim C, Boulanger CM (March 2012). "Flow cytometry: retrospective, fundamentals and recent instrumentation". Cytotechnology. 64 (2): 109–30. doi:10.1007/s10616-011-9415-0. PMC 3279584. PMID 22271369.
- ^ "flow cytometry". TheFreeDictionary.com. Retrieved 2018-09-18.
- ^ Shapiro HM (2003). Practical flow cytometry (4th ed.). New York: Wiley-Liss. ISBN 978-0-471-41125-3.
- ^ Givan AL (2011). "Flow Cytometry: An Introduction". In Hawley T, Hawley R (eds.). Flow Cytometry Protocols. Methods in Molecular Biology. Vol. 699. Humana Press. pp. 1–29. doi:10.1007/978-1-61737-950-5_1. ISBN 978-1-61737-949-9. PMID 21116976.
- ^ US 3380584, Mack Fulwyler, "입자 분리기 06-01 발행
- ^ Fulwyler MJ (November 1965). "Electronic separation of biological cells by volume". Science. 150 (3698): 910–1. Bibcode:1965Sci...150..910F. doi:10.1126/science.150.3698.910. PMID 5891056. S2CID 459342.
- ^ DE 1815352, Dittrich W, Göhde W, "분산 매체 내의 입자를 측정하고 계수하는 광도계용 플로우 스루 챔버", 1977-12-21 출판
- ^ Osborn RA (1970). "Cytology Automation". In Evans DM (ed.). Proceedings of Second Tenovus Symposium. 24–25 October 1968. Edinburgh and London: E. & S. Livingstone (published 1971). doi:10.1016/S0031-3025(16)39506-X. S2CID 58286041.
Kamentsky LA (1973). "Cytology automation". Advances in Biological and Medical Physics. 14: 93–161. doi:10.1016/B978-0-12-005214-1.50007-8. ISBN 9780120052141. PMID 4579761. - ^ Sack U, Tárnok A, Rothe G (2006). Zelluläre Diagnostik [Cellular Diagnostics] (in German). Karger Publishers. ISBN 978-3-318-01217-0.
- ^ "Resources & Equipment". Centenary Institute.
- ^ "BD Biosciences - Special Order Products".
- ^ a b c d e f g h i Cossarizza A, Chang HD, Radbruch A, Akdis M, Andrä I, Annunziato F, et al. (October 2017). "Guidelines for the use of flow cytometry and cell sorting in immunological studies". European Journal of Immunology. 47 (10): 1584–1797. doi:10.1002/eji.201646632. PMC 9165548. PMID 29023707. S2CID 25591889.
- ^ a b "Fluidics System - Flow Cytometry Guide". Bio-Rad. Retrieved 2018-09-18.
- ^ a b c d e "How a Flow Cytometer Works". Thermo Fisher Scientific. Retrieved 2018-09-18.
- ^ Nolan JP, Condello D (January 2013). "Spectral flow cytometry". Current Protocols in Cytometry. Chapter 1 (1): Unit1.27. doi:10.1002/0471142956.cy0127s63. ISBN 978-0471142959. PMC 3556726. PMID 23292705.
- ^ Han Y, Gu Y, Zhang AC, Lo YH (November 2016). "Review: imaging technologies for flow cytometry". Lab on a Chip. 16 (24): 4639–4647. doi:10.1039/c6lc01063f. PMC 5311077. PMID 27830849.
- ^ a b Roederer M (November 2001). "Spectral compensation for flow cytometry: visualization artifacts, limitations, and caveats". Cytometry. 45 (3): 194–205. doi:10.1002/1097-0320(20011101)45:3<194::aid-cyto1163>3.0.co;2-c. PMID 11746088.
- ^ Sharpless T, Traganos F, Darzynkiewicz Z, Melamed MR (1975). "Flow cytofluorimetry: discrimination between single cells and cell aggregates by direct size measurements". Acta Cytologica. 19 (6): 577–81. PMID 1108568.
- ^ a b "Fluorochrome Table (Tools)". Flow Cytometry Network.
- ^ "Table of Fluorochromes". Archived from the original on October 20, 2014.
- ^ Qian Y, Wei C, Eun-Hyung Lee F, Campbell J, Halliley J, Lee JA, et al. (2010). "Elucidation of seventeen human peripheral blood B-cell subsets and quantification of the tetanus response using a density-based method for the automated identification of cell populations in multidimensional flow cytometry data". Cytometry Part B. 78 Suppl 1 (Suppl 1): S69-82. doi:10.1002/cyto.b.20554. PMC 3084630. PMID 20839340.
- ^ "Immunology Database and Analysis Portal". Archived from the original on July 26, 2011. Retrieved 2009-09-03.
- ^ Zare H, Shooshtari P, Gupta A, Brinkman RR (July 2010). "Data reduction for spectral clustering to analyze high throughput flow cytometry data". BMC Bioinformatics. 11: 403. doi:10.1186/1471-2105-11-403. PMC 2923634. PMID 20667133.
- ^ "flowClust". Retrieved 2009-09-03.
- ^ Lo K, Brinkman RR, Gottardo R (April 2008). "Automated gating of flow cytometry data via robust model-based clustering". Cytometry Part A. 73 (4): 321–32. doi:10.1002/cyto.a.20531. PMID 18307272.
- ^ Lo K, Hahne F, Brinkman RR, Gottardo R (May 2009). "flowClust: a Bioconductor package for automated gating of flow cytometry data". BMC Bioinformatics. 10: 145. doi:10.1186/1471-2105-10-145. PMC 2701419. PMID 19442304.
- ^ "FLow analysis with Automated Multivariate Estimation (FLAME)". Archived from the original on August 21, 2009. Retrieved 2009-09-03.
- ^ Wattenberg M, Viégas F, Johnson I (Oct 13, 2016). "How to Use t-SNE Effectively". Distill. 1 (10). doi:10.23915/distill.00002.
- ^ "FlowCAP - Flow Cytometry: Critical Assessment of Population Identification Methods". Retrieved 2009-09-03.
- ^ a b Perkel J (July 19, 2004). "Fluorescence-Activated Cell Sorter". The Scientist. Retrieved 2018-09-18.
- ^ "Record Unit 9554, The History of the Cell Sorter Interviews". Smithsonian Institution Archives. Fulwyler, Mack Jett. interviewee, Herzenberg, Leonard A. interviewee, Bach, Bruce Allen. interviewee, Krasnow, Mark A. interviewee, Mhatre, Nagesh S. interviewee. 1991. Retrieved 2018-09-18.
{{cite web}}: CS1 유지보수: 기타 (링크) - ^ Bushnell T (2016-05-04). "12 Flow Cytometry Terms And Definitions Most Scientists Get Wrong". Expert Cytometry. Retrieved 2018-09-18.
- ^ Julius MH, Masuda T, Herzenberg LA (July 1972). "Demonstration that antigen-binding cells are precursors of antibody-producing cells after purification with a fluorescence-activated cell sorter". Proceedings of the National Academy of Sciences of the United States of America. 69 (7): 1934–8. Bibcode:1972PNAS...69.1934J. doi:10.1073/pnas.69.7.1934. PMC 426835. PMID 4114858.
- ^ "Cell Sorting – Faculty of Medicine Flow Cytometry Facility". flowcytometry.utoronto.ca. Retrieved 2018-09-18.
- ^ "Conjugation of monoclonal antibodies". www.drmr.com. Retrieved 2018-09-18.
- ^ Loken MR (1990). Immunofluorescence Techniques in Flow Cytometry and Sorting (2nd ed.). Wiley. pp. 341–53.
- ^ a b c Ornatsky O, Bandura D, Baranov V, Nitz M, Winnik MA, Tanner S (September 2010). "Highly multiparametric analysis by mass cytometry". Journal of Immunological Methods. 361 (1–2): 1–20. doi:10.1016/j.jim.2010.07.002. PMID 20655312.
- ^ Basiji DA, Ortyn WE, Liang L, Venkatachalam V, Morrissey P (September 2007). "Cellular image analysis and imaging by flow cytometry". Clinics in Laboratory Medicine. 27 (3): 653–70, viii. doi:10.1016/j.cll.2007.05.008. PMC 2034394. PMID 17658411.
- ^ Sun T, Morgan H (April 2010). "Single-cell microfluidic impedance cytometry: a review". Microfluidics Nanofluidics. 8 (4): 423–443. doi:10.1007/s10404-010-0580-9. S2CID 95631023.
- ^ Cheung KC, Di Berardino M, Schade-Kampmann G, Hebeisen M, Pierzchalski A, Bocsi J, et al. (July 2010). "Microfluidic impedance-based flow cytometry". Cytometry Part A. 77 (7): 648–66. doi:10.1002/cyto.a.20910. PMID 20583276.
- ^ Zamora JL, Aguilar HC (February 2018). "Flow virometry as a tool to study viruses". Methods. 134–135: 87–97. doi:10.1016/j.ymeth.2017.12.011. PMC 5815898. PMID 29258922.
- ^ Murphy RW, Lowcock LA, Smith C, Darevsky IS, Orlov N, MacCulloch RD, Upton DE (1997). "Flow cytometry in biodiversity surveys: methods, utility and constraints". Amphibia-Reptilia. 18: 1–13. doi:10.1163/156853897x00260.
- ^ Gorczyca W, Traganos F, Jesionowska H, Darzynkiewicz Z (July 1993). "Presence of DNA strand breaks and increased sensitivity of DNA in situ to denaturation in abnormal human sperm cells: analogy to apoptosis of somatic cells". Experimental Cell Research. 207 (1): 202–5. doi:10.1006/excr.1993.1182. PMID 8391465.
- ^ Evenson DP (September 2017). "Evaluation of sperm chromatin structure and DNA strand breaks is an important part of clinical male fertility assessment". Translational Andrology and Urology. 6 (Suppl 4): S495–S500. doi:10.21037/tau.2017.07.20. PMC 5643675. PMID 29082168.
- ^ Tanaka T, Halicka HD, Huang X, Traganos F, Darzynkiewicz Z (September 2006). "Constitutive histone H2AX phosphorylation and ATM activation, the reporters of DNA damage by endogenous oxidants". Cell Cycle. 5 (17): 1940–5. doi:10.4161/cc.5.17.3191. PMC 3488278. PMID 16940754.
- ^ MacPhail SH, Banáth JP, Yu Y, Chu E, Olive PL (June 2003). "Cell cycle-dependent expression of phosphorylated histone H2AX: reduced expression in unirradiated but not X-irradiated G1-phase cells". Radiation Research. 159 (6): 759–67. Bibcode:2003RadR..159..759M. doi:10.1667/rr3003. PMID 12751958. S2CID 26093456.
- ^ Darzynkiewicz Z, Juan G, Li X, Gorczyca W, Murakami T, Traganos F (January 1997). "Cytometry in cell necrobiology: analysis of apoptosis and accidental cell death (necrosis)". Cytometry. 27 (1): 1–20. doi:10.1002/(SICI)1097-0320(19970101)27:1<1::AID-CYTO2>3.0.CO;2-L. PMID 9000580.
- ^ Edgar RH, Noel C, Minard A, Fernandez R, Fitzpatrick M, Sajewski A, et al. (2019-02-27). Wang L, Oraevsky AA (eds.). "Identification of MRSA infection in blood using photoacoustic flow cytometry". Photons Plus Ultrasound: Imaging and Sensing 2019. International Society for Optics and Photonics. 10878: 1087860. Bibcode:2019SPIE10878E..60E. doi:10.1117/12.2510210. ISBN 9781510623989. S2CID 86428267.
- ^ Menon V, Thomas R, Ghale AR, Reinhard C, Pruszak J (December 2014). "Flow cytometry protocols for surface and intracellular antigen analyses of neural cell types". Journal of Visualized Experiments (94): e52241. doi:10.3791/52241. PMC 4396953. PMID 25549236.
- ^ Antypas H, Veses-Garcia M, Weibull E, Andersson-Svahn H, Richter-Dahlfors A (June 2018). "A universal platform for selection and high-resolution phenotypic screening of bacterial mutants using the nanowell slide". Lab on a Chip. 18 (12): 1767–1777. doi:10.1039/c8lc00190a. PMC 5996734. PMID 29781496.
- ^ Davey HM (August 2011). "Life, death, and in-between: meanings and methods in microbiology". Applied and Environmental Microbiology. 77 (16): 5571–6. doi:10.1128/AEM.00744-11. PMC 3165249. PMID 21705550.
- ^ Yentsch CM (1981). "Flow cytometric analysis of cellular saxitoxin in the dinoflagellate Gonyaulax tamarensis var. excavata". Toxicon. 19 (5): 611–21. doi:10.1016/0041-0101(81)90099-4. PMID 7197816.
- ^ Trask, B. J.; Engh, G. J. van den; Elgershuizen, J. H. B. W. (1982). "Analysis of phytoplankton by flow cytometry". Cytometry. 2 (4): 258–264. doi:10.1002/cyto.990020410. ISSN 1097-0320. PMID 6799265.
- ^ Olson, Robert J.; Frankel, Sheila L.; Chisholm, Sallie W.; Shapiro, Howard M. (1983-04-08). "An inexpensive flow cytometer for the analysis of fluorescence signals in phytoplankton: Chlorophyll and DNA distributions". Journal of Experimental Marine Biology and Ecology. 68 (2): 129–144. doi:10.1016/0022-0981(83)90155-7. ISSN 0022-0981.
- ^ Yentsch CM, Horan PK, Muirhead K, Dortch Q, Haugen E, Legendre L, et al. (1983). "Flow cytometry and cell sorting: A technique for analysis and sorting of aquatic particles1". Limnology and Oceanography. 28 (6): 1275–1280. Bibcode:1983LimOc..28.1275Y. doi:10.4319/lo.1983.28.6.1275. ISSN 1939-5590.
- ^ Chisholm SW, Olson RJ, Zettler ER, Goericke R, Waterbury JB, Welschmeyer NA (July 1988). "A novel free-living prochlorophyte abundant in the oceanic euphotic zone". Nature. 334 (6180): 340–343. Bibcode:1988Natur.334..340C. doi:10.1038/334340a0. S2CID 4373102.
- ^ Swalwell JE, Ribalet F, Armbrust EV (2011). "SeaFlow: A novel underway flow-cytometer for continuous observations of phytoplankton in the ocean". Limnology and Oceanography: Methods. 9 (10): 466–477. doi:10.4319/lom.2011.9.466. ISSN 1541-5856.
- ^ Olson RJ, Sosik HM (2007). "A submersible imaging-in-flow instrument to analyze nano-and microplankton: Imaging FlowCytobot". Limnology and Oceanography: Methods. 5 (6): 195–203. doi:10.4319/lom.2007.5.195.
- ^ Jakobsen HH, Carstensen J (2011). "FlowCAM: Sizing cells and understanding the impact of size distributions on biovolume of planktonic community structure". Aquatic Microbial Ecology. 65 (1): 75–87. doi:10.3354/ame01539. ISSN 0948-3055.
- ^ Longnecker K, Sherr BF, Sherr EB (December 2005). "Activity and phylogenetic diversity of bacterial cells with high and low nucleic acid content and electron transport system activity in an upwelling ecosystem". Applied and Environmental Microbiology. 71 (12): 7737–49. doi:10.1128/AEM.71.12.7737-7749.2005. PMC 1317353. PMID 16332746.
- ^ Stepanauskas R, Sieracki ME (May 2007). "Matching phylogeny and metabolism in the uncultured marine bacteria, one cell at a time". Proceedings of the National Academy of Sciences of the United States of America. 104 (21): 9052–7. Bibcode:2007PNAS..104.9052S. doi:10.1073/pnas.0700496104. PMC 1885626. PMID 17502618.
- ^ Thompson AW, Foster RA, Krupke A, Carter BJ, Musat N, Vaulot D, et al. (September 2012). "Unicellular cyanobacterium symbiotic with a single-celled eukaryotic alga". Science. 337 (6101): 1546–50. Bibcode:2012Sci...337.1546T. doi:10.1126/science.1222700. PMID 22997339. S2CID 7071725.
- ^ Lomas, Michael W.; Bronk, Deborah A.; van den Engh, Ger (2011-01-15). "Use of Flow Cytometry to Measure Biogeochemical Rates and Processes in the Ocean". Annual Review of Marine Science. 3 (1): 537–566. Bibcode:2011ARMS....3..537L. doi:10.1146/annurev-marine-120709-142834. ISSN 1941-1405. PMID 21329216.
- ^ Hawkins ED, Hommel M, Turner ML, Battye FL, Markham JF, Hodgkin PD (2007). "Measuring lymphocyte proliferation, survival and differentiation using CFSE time-series data". Nature Protocols. 2 (9): 2057–67. doi:10.1038/nprot.2007.297. PMID 17853861. S2CID 13550456.
- ^ Quah BJ, Parish CR (October 2010). "The use of carboxyfluorescein diacetate succinimidyl ester (CFSE) to monitor lymphocyte proliferation". Journal of Visualized Experiments (44). doi:10.3791/2259. PMC 3185625. PMID 20972413.
- ^ Jedema I, van der Werff NM, Barge RM, Willemze R, Falkenburg JH (April 2004). "New CFSE-based assay to determine susceptibility to lysis by cytotoxic T cells of leukemic precursor cells within a heterogeneous target cell population". Blood. 103 (7): 2677–82. doi:10.1182/blood-2003-06-2070. PMID 14630824. S2CID 1984056.
추가 정보
- Carey JL, McCoy Jr JP, Keren DF (2007). Flow cytometry in clinical diagnosis (4th ed.). Chicago, IL: American Society for Clinical Pathology (ASCP) Press. ISBN 978-0-89189-548-0.
- Darzynkiewicz Z, Roederer M, Tanke HJ, eds. (2004). Methods in Cell Biology, Cytometry. Vol. 75 (4th ed.). Elsevier /Academic Press. ISBN 0-12-480283-4.
- Darzynkiewicz Z, Robinson JP, Roederer M (2009). Essential cytometry methods (1st ed.). Amsterdam: Elsevier/Academic Press. ISBN 978-0-12-375045-7.
- Darzynkiewicz Z, et al., eds. (2011). Recent Advances in Cytometry. Part A. Methods in Cell Biology. Vol. 102. Elsevier/Academic Press. ISBN 978-0-12-374912-3.
- Darzynkiewicz Z, et al., eds. (2011). Recent Advances in Cytometry. Part B. Methods in Cell Biology. Vol. 103. Elsevier/Academic Press. ISBN 978-0-12-385493-3.
- Lloyd D (1993). Flow cytometry in microbiology. London: Springer-Verlag. ISBN 978-3-540-19796-6.
- Ormerod MG (1999). Flow cytometry (2nd ed.). Oxford, UK: Bios Scientific Publishers. ISBN 978-1-85996-107-0.
- Ormerod MG, ed. (2000). Flow cytometry : a practical approach (3rd ed.). Oxford [England]: Oxford University Press. ISBN 978-0-19-963824-6.
- Ormerod MG (2008). Flow cytometry : a basic introduction. Redhill: M.G. Ormerod. ISBN 978-0-9559812-0-3.
- Robinson JP, et al. (1993). Handbook of flow cytometry methods. New York: Wiley-Liss. ISBN 978-0-471-59634-9.
- Shapiro HM (2003). Practical flow cytometry (4th ed.). New York: Wiley-Liss. ISBN 978-0-471-41125-3.
- Sklar LA (2005). Flow cytometry for biotechnology. New York: Oxford University Press. ISBN 978-0-19-515234-0.
외부 링크
| 라이브러리 리소스 정보 플로우 세포 측정 |