콜로이드
Colloid
| 응축물리학 |
|---|
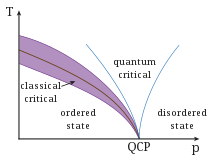 |
| 단계 · 위상 전이 · QCP |
콜로이드는 현미경으로 분산된 불용성 입자로 구성된 한 물질이 다른 물질 전체에 매달려 있는 혼합물이다. 그러나 어떤 정의는 입자가 액체로 분산되어야 한다고 명시하고,[1] 또 어떤 정의는 에어로졸이나 겔과 같은 물질을 포함하도록 정의를 확장한다. 콜로이드 서스펜션이라는 용어는 전체적인 혼합물을 뚜렷하게 나타낸다(일단, 서스펜션이라는 단어의 좁은 감각은 입자의 크기가 더 큰 콜로이드와 구별된다). 콜로이드에는 분산상(일시된 입자)과 연속상(일시 중단의 매개체)이 있다. 분산된 위상 입자의 직경은 약 1나노미터에서 1마이크로미터까지이다.[2][3]
어떤 콜로이드들은 틴달 효과 때문에 반투명하게 되는데, 이것은 콜로이드의 입자에 의한 빛의 산란이다. 다른 콜로이드들은 불투명하거나 약간의 색을 가질 수 있다.
콜로이드 정지는 인터페이스와 콜로이드 과학의 주제다. 이 연구 분야는 1845년 이탈리아의 화학자 프란체스코 셀미(Francesco Selmi[4])에 의해 소개되었고 1861년부터 스코틀랜드의 과학자 토마스 그레이엄(Thomas Graham)에 의해 추가적으로 조사되었다.[5]
콜로이드: 한 매체에 분산된 분자 또는 다분자 입자가 약 1nm에서 1μm 사이의 차원을 가지거나 시스템 불연속부가 그 순서의 거리에서 발견되는 분할 상태.[6][7][8]
분류
콜로이드의 분류는 다음과 같다.
| 중/상 | 분산상 | |||
|---|---|---|---|---|
| 가스 | 액체 | 고체 | ||
| 분산 중간의 | 가스 | 그러한 콜로이드들은 알려져 있지 않다. 헬륨과 제논은 특정 조건에서 불변하는 것으로 알려져 있다.[9][10] | 액체 에어로졸 예: 안개, 구름, 응결, 안개, 증기, 헤어 스프레이 | 고체 에어로졸 예: 연기, 얼음 구름, 대기 먼지 |
| 액체 | 거품 예: 생크림, 면도크림 | 에멀전 또는 액정 예:우유, 마요네즈, 핸드크림, 라텍스, 생물막, 액체 생체분자 응축수 | 솔 예: 색소화 잉크, 침전물, 침전물, 고체 바이오 분자 응축물 | |
| 고체 | 고체 폼 예: 에어로겔, 스티로폼, 푸미스 | 젤 예: 아가르, 젤리, 젤리, 젤리 같은 생체분자 응축수 | 솔리드솔 예: 크랜베리 글라스 | |
이 크기 범위에서 분산된 상이 있는 균질 혼합물을 콜로이드 에어로졸, 콜로이드 유화, 콜로이드 폴, 콜로이드 분산 또는 하이드로솔이라고 할 수 있다.
콜로이드와 용액 비교
콜로이드는 분산된 상과 연속적인 상이 있는 반면, 용액에서는 용액과 용제가 단 하나의 상만을 구성한다. 용액 속의 용액은 개별 분자나 이온인 반면 콜로이드 입자는 더 크다. 예를 들어, 물 속의 소금 용액에서는 염화나트륨(NaCl) 결정이 용해되고, Na와+ Cl− 이온은 물 분자에 둘러싸여 있다. 그러나 우유와 같은 콜로이드에서는 콜로이드 입자가 개별적인 지방 분자라기 보다는 지방의 구상체라고 할 수 있다.
입자 간 상호작용
콜로이드 입자의 상호작용에 있어 다음과 같은 힘이 중요한 역할을 한다.[11][12]
- 제외된 볼륨 반발: 이것은 단단한 입자 사이에 어떤 겹침도 있을 수 없는 것을 가리킨다.
- 정전기 상호작용: 콜로이드 입자는 종종 전하를 운반하므로 서로 끌어당기거나 밀어낸다. 단계 이동성뿐만 아니라 연속적인 단계와 분산된 단계의 전하도 이 상호작용에 영향을 미치는 요인들이다.
- 판 데르 발스 힘: 이것은 영구적이거나 유도된 두 쌍둥이의 상호작용 때문이다. 입자가 영구 쌍극자를 갖고 있지 않더라도 전자 밀도의 변동은 입자에 임시 쌍극자를 발생시킨다. 이 임시 쌍극자는 근처의 입자에 쌍극자를 유도한다. 임시 쌍극자와 유도 쌍극자는 서로 끌어당긴다. 이를 반데르 발스 힘이라고 하며, (분산된 상과 연속적인 상상의 굴절 지수를 일치시키지 않는 한), 항상 존재하는 것으로 단거리로서 매력적이다.
- 폴리머로 덮인 표면 사이의 스테릭 힘 또는 비애도빙 폴리머를 함유한 용액 내에서는 인터피사이드 힘을 조절할 수 있으며, 추가 스테릭 반발력(기원은 대부분 내향성) 또는 그들 사이의 매력적인 고갈력을 발생시킬 수 있다.
침전 속도
지구의 중력장은 콜로이드 입자에 작용한다. 따라서 콜로이드 입자가 서스펜션의 매질보다 밀도가 높으면 침전(아래로 떨어짐), 밀도가 낮으면 크림(위쪽으로 떠 있음)이 된다. 큰 입자는 또한 이러한 움직임에 대항하기 위해 브라운의 움직임이 작기 때문에 침전하는 경향이 더 크다.
침전 또는 크림핑 속도는 스톡스 드래그력을 중력과 동일시함으로써 발견된다.
어디에
은 콜로이드 입자의 아르키메데스 중량이다.
은(는) 서스펜션 매체의 점도,
은 콜로이드 입자의 반지름이며,
은(는) 침전물 또는 크림핑 속도.
콜로이드 입자의 질량은 다음을 사용하여 발견된다.
어디에
은 V= 4 3 V r을(를) 사용하여 계산한 콜로이드 입자의 볼륨이다
그리고 - 2{\}}은 콜로이드 입자와 현수 매체 사이의 질량 밀도 차이다.
재배치를 통해 침전물 또는 크림핑 속도는 다음과 같다.
1μm 이상의 입자는 침전되기 쉬우므로 콜로이드 입자의 지름에는 상단의 크기 제한이 있다. 따라서 그 물질은 더 이상 콜로이드 중단으로 간주되지 않을 것이다.[13]
콜로이드 입자는 침전 속도가 브라운 운동으로부터의 이동 속도와 같을 경우 침전 평형 상태에 있다고 한다.
준비
콜로이드 준비에는 크게 두 가지 방법이 있다.[14]
- 전단을 밀링, 살포 또는 도포하여 콜로이드 치수로 큰 입자나 물방울의 분산(예: 흔들림, 혼합 또는 고 전단 혼합)
- 강우, 응축 또는 리독스 반응에 의해 작은 용해 분자가 더 큰 콜로이드 입자로 응결된다. 이러한 과정은 콜로이드성 실리카나 금을 준비하는 데 사용된다.
안정화
콜로이드 시스템의 안정성은 용액에 매달려 있는 입자에 의해 정의되며 입자 사이의 상호작용 힘에 의존한다. 여기에는 정전기 상호작용과 반 데르 발스 힘이 포함된다. 왜냐하면 둘 다 시스템의 전체 자유 에너지에 기여하기 때문이다.[15]
콜로이드(colorid)는 콜로이드 입자 사이의 매력적인 힘에 의한 상호작용 에너지가 kT보다 작을 경우 안정적이며, 여기서 k는 볼츠만 상수, T는 절대 온도다. 이럴 경우 콜로이드 입자가 밀어내거나 약하게 서로 끌어당길 뿐 물질은 중단상태로 남게 된다.
교호작용 에너지가 kT보다 크면 매력적인 힘이 우세해지고, 콜로이드 입자들이 뭉치기 시작할 것이다. 이 과정은 일반적으로 집적(collection)이라고 부르지만, 편평(flocculation), 응고(coagulation) 또는 강수(vacuation)라고도 한다.[16] 이러한 용어들은 종종 서로 교환하여 사용되지만, 어떤 정의에서는 약간 다른 의미를 갖는다. 예를 들어, 응고는 입자를 함께 고정시키는 힘이 교반 또는 혼합에 의해 야기되는 어떤 외부 힘보다 강한 되돌릴 수 없고 영구적인 집계를 설명하는 데 사용될 수 있다. 플로크레이션은 더 약한 매력적인 힘을 포함하는 가역적 집계를 설명하기 위해 사용될 수 있으며, 그 집계를 보통 플록이라고 부른다. 강수라는 용어는 일반적으로 교란을 받을 때 콜로이드 산포에서 고체로(프리키피테이트)의 위상 변화를 설명하기 위해 사용된다.[13] 집계는 침전이나 크림을 일으키므로 콜로이드는 불안정하다. 이러한 과정 중 하나가 발생하면 콜로이드는 더 이상 중단되지 않는다.
정전기 안정화와 스테릭 안정화는 집적 안정화를 위한 두 가지 주요 메커니즘이다.
- 정전기 안정화는 유사한 전하의 상호 반발에 기초한다. 콜로이드 입자의 전하(charge of coloridal iciple)는 전기적 이중층으로 구성되는데, 이 층은 입자가 표면에서 전하(charge)되지만, 그 다음에는 입자를 둘러싸고 있는 반작용(반전하의 이온)을 끌어들인다. 부유된 콜로이드 입자 사이의 정전기적 반발은 제타 전위의 관점에서 가장 쉽게 정량화된다. 집계에 대한 반 데르 발스 매력과 정전기 반발의 결합 효과는 DLVO 이론에 의해 정량적으로 설명된다.[17] 콜로이드를 안정시키는 일반적인 방법은 전해질로 흔들리는 과정인 펩타이드화다.
- 강직 안정화는 입자들이 매력적인 힘의 범위에서 가까이 접근하지 못하도록 하기 위해 입자에 있는 중합체나 계면활성제의 층을 흡수하는 것이다.[13] 폴리머는 입자 표면에 부착된 체인으로 구성되며, 밖으로 뻗어나가는 체인의 부분은 서스펜션 매체에 용해된다.[18] 이 기법은 유기용제를 포함한 모든 유형의 용매에서 콜로이드 입자를 안정시키기 위해 사용된다.[19]
두 메커니즘의 조합도 가능하다(전기 안정화).
젤 네트워크 안정화라고 불리는 방법은 콜로이드들을 집적과 침전 양쪽에 안정되게 생산하는 주요한 방법을 나타낸다. 그 방법은 젤 네트워크를 형성할 수 있는 폴리머를 콜로이드 서스펜션에 추가하는 것으로 구성된다. 입자 안착은 입자가 갇혀 있는 중합체 행렬의 강성으로 인해 방해되며,[20] 긴 중합체 체인은 분산된 입자에 강직 또는 전기적 안정화를 제공할 수 있다. 그러한 물질의 예로는 크산탄과 구아 껌이 있다.
불안정화
불안정은 다음과 같은 다양한 방법으로 달성할 수 있다.
- 입자의 집적을 방지하는 정전기 차단막 제거. 이는 입자의 데비 스크리닝 길이(전기 이중 층의 폭)를 줄이기 위해 정지에 소금을 첨가함으로써 이루어질 수 있다. 또한 서스펜션의 pH를 변경하여 서스펜션 입자의 표면 전하를 효과적으로 중화시킴으로써 수행된다.[1] 이렇게 하면 콜로이드 입자를 분리해 두는 반발력이 제거되고 반데르발스 세력으로 인해 집결이 가능하다. pH의 사소한 변화는 제타 잠재력에 상당한 변화를 가져올 수 있다. 제타 전위의 크기가 일반적으로 ± 5mV 정도인 특정 임계값 미만이면 급속 응고 또는 집계가 발생하는 경향이 있다.[21]
- 충전된 폴리머 플로크쿨란트 추가. 폴리머 플로쿨러스는 매력적인 정전기적 상호작용에 의해 개별 콜로이드 입자를 연결시킬 수 있다. 예를 들어 음전하 콜로이드 실리카 또는 점토 입자는 양전하 고분자를 추가하여 플록콜링할 수 있다.
- 내향성 효과로 인해 집적을 일으키는 디플렛트라고 불리는 비아드레드 폴리머의 추가.
소량분수의 불안정한 콜로이드성 서스펜션이 군집화된 액체 서스펜션을 형성하는데, 이때 개별 입자 군집에서는 서스펜션 매질보다 밀도가 높으면 침전물이 퇴적되고, 밀도가 낮으면 크림이 퇴적된다. 그러나, 더 큰 부피 분수의 콜로이드 정지는 점탄성의 성질을 가진 콜로이드 겔을 형성한다. 벤토나이트나 치약과 같은 점탄성 콜로이드 젤은 전단 밑의 액체처럼 흐르지만 전단을 제거할 때 그 모양을 유지한다. 치약 튜브에서 치약을 짜낼 수 있지만 칫솔을 바른 후에도 칫솔 위에 그대로 있는 것도 이 때문이다.
모니터링 안정성
제품의 산포 상태를 감시하고 불안화 현상을 식별 및 정량화하기 위해 가장 널리 사용되는 기법은 수직 스캐닝과 결합된 다중 광 산란이다.[22][23][24][25] 탁도법으로 알려진 이 방법은 시료를 통해 보내진 후 콜로이드 입자에 의해 역행하는 빛의 분율을 측정하는 것에 기초한다. 백스캐터링 강도는 분산된 단계의 평균 입자 크기 및 부피 비율에 정비례한다. 따라서 침전물이나 크림핑에 의한 국소농도 변화, 집계에 의한 입자의 뭉침에 의한 국소농도 변화를 감지하여 감시한다.[26] 이러한 현상은 불안정한 콜로이드와 관련이 있다.
동적 빛의 산란은 콜로이드 입자가 얼마나 빠르게 확산되는지를 측정함으로써 콜로이드 입자의 크기를 감지하는 데 사용될 수 있다. 이 방법은 레이저 광선을 콜로이드 쪽으로 유도하는 것이다. 흩어진 빛은 간섭 패턴을 형성할 것이며, 이 패턴에서 빛의 세기의 변동은 입자의 브라운 운동으로 인해 발생한다. 만약 그들이 집계를 통해 뭉쳐서 입자들의 겉보기 크기가 증가한다면, 그것은 더 느린 브라운 운동을 야기할 것이다. 이 기법은 겉보기 입자 크기가 콜로이드 입자의 일반적인 크기 범위를 벗어나는 것으로 결정되는 경우 집계가 발생했음을 확인할 수 있다.[15]
저장 수명 예측을 위한 가속 방법
불안정의 운동 프로세스는 다소 길 수 있으며(일부 제품의 경우 최대 수개월 또는 심지어 수 년까지) 새로운 제품 설계를 위한 합리적인 개발 시간에 도달하기 위해 제조자가 추가 가속 방법을 사용하는 것이 종종 필요하다. 열 방법은 가장 일반적으로 사용되며 불안정을 가속화하기 위한 온도 상승(상위 반전 또는 화학적 분해의 임계 온도 이하)으로 구성된다. 온도는 점성뿐만 아니라 비이온 계면활성제의 경우 또는 시스템 내부의 보다 일반적인 상호작용 힘의 경우 계면 장력에 영향을 미친다. 분산을 고온으로 보관하면 제품의 실제 생활 상태(예: 여름철 자동차에 자외선 차단 크림 튜브)를 시뮬레이션할 수 있을 뿐 아니라 최대 200배까지 불안화 과정을 가속화할 수 있다. 진동, 원심분리 및 동요를 포함한 기계적 가속을 사용하는 경우가 있다. 그들은 입자/방울을 서로 밀어내는 다른 힘에 제품을 노출시켜 필름 배수를 돕는다. 그러나, 어떤 유화들은 인공 중력 하에서 하는 동안, 보통 중력에서는 결코 결합되지 않을 것이다.[27] 또한 원심분리 및 진동 사용 시 다양한 입자 집단의 분리가 강조되었다.[28]
원자의 모델 시스템으로서
물리학에서 콜로이드들은 원자의 흥미로운 모델 시스템이다.[29] 마이크로메트레 스케일 콜로이드 입자는 콘포칼로컬 현미경 등 광학 기법으로 관찰할 수 있을 만큼 크다. 제외된 부피 상호작용이나 정전기력 등 물질의 구조와 행동을 지배하는 힘 중 많은 수가 콜로이드 정지의 구조와 행동을 지배한다. 예를 들어, 이상적인 기체를 모형화하는 데 사용되는 것과 동일한 기법을 적용하여 단단한 구체 콜로이드 서스펜션의 동작을 모형화할 수 있다. 또한 콜로이드 서스펜션의 위상 전환은 광학 기법을 이용하여 실시간으로 연구할 수 있으며,[30] 액체의 위상 전환과 유사하다. 많은 흥미로운 사례에서 광학적 유동성은 콜로이드 서스펜션을 조절하는데 사용된다.[30][31]
크리스털
콜로이드 결정(coloridal crystal)은 매우 긴 범위(일반적으로 몇 밀리미터에서 1 센티미터의 순서로)에 걸쳐 형성될 수 있고 원자 또는 분자 결정과 유사하게 보이는 고도로 정렬된 입자 배열이다.[32] 이 주문 현상의 가장 훌륭한 자연적 예 중 하나는 이산화규소(또는 실리카, SiO2)의 무정형 콜로이드 구가 밀집된 영역에서 순수 스펙트럼 색의 빛나는 영역이 나타나는 귀중한 오팔에서 찾을 수 있다.[33][34] 이 구형 입자들은 호주와 다른 지역의 매우 규소성이 높은 웅덩이에서 침전되어 수년간의 정수압과 중력하에서의 침전 및 압축 후에 고도로 질서 정연한 배열들을 형성한다. 서브크로미터 구형 입자의 주기적인 배열은 특히 간격이 입사 광파와 동일한 크기일 때 가시 광파에 대해 자연적인 회절 격자 역할을 하는 간극의 유사한 배열을 제공한다.[35][36]
따라서 혐오스러운 쿨롱 상호 작용으로 인해 수성 환경에서 전기 충전된 고분자는 종종 개별 입자 직경보다 상당히 큰 인터피사 분리 거리와의 장거리 결정과 같은 상관관계를 나타낼 수 있다는 것은 여러 해 동안 알려져 왔다. 자연에서 이러한 모든 경우에서 같은 찬란한 발광(또는 색채의 놀이)은 결정체 고형물에서 X선이 산란하는 것과 유사한 문제에서 브래그의 법칙을 만족시키는 가시광파의 회절과 건설적인 간섭에 기인할 수 있다.
이러한 이른바 '협착 결정체'의 물리학과 화학을 탐구하는 실험이 많은 것은 지난 20년간 합성 모노디스페르스 콜로이드(중합체와 광물 둘 다)를 준비하고, 다양한 메커니즘을 통해 그 장기를 구현하고 보존하는 비교적 간단한 방법의 결과로 나타났다.천사의 질서 [37]형성
생물학에서
콜로이드 위상 분리는 세포의 세포질과 핵 모두를 생체 분자 응축물로 분할하기 위한 중요한 조직 원리로, 액체 결정의 일종인 지질 빌레이어 막을 통한 구획 분할과 유사하다. 생체분자 응축수라는 용어는 세포 내의 액체-액체 또는 액체-고체 위상 분리를 통해 발생하는 고분자 군집을 지칭하기 위해 사용되어 왔다. 고분자 혼잡은 콜로이드 페이즈 분리 및 생체분자 응축물의 형성을 강하게 강화한다.
환경에서는
또한 콜로이드 입자는 표면 물(해수, 호수, 강, 민물)과 갈라진 암석[39](예: 석회암, 사암, 화강암)에서 순환하는 지하수(예: 석회암, 사암, 화강암)에서 다양한 오염물질의 이동 벡터[38] 역할을 할 수 있다. 방사성핵종과 중금속은 물에 매달린 콜로이드에 쉽게 흡수된다. 다양한 종류의 콜로이드(예: 점토 입자, 규산염, 철옥시-수산화물), 유기 콜로이드(인간 및 풀빅 물질)가 인식된다. 중금속이나 방사성핵종이 자체 순수 콜로이드(pure colorid)를 형성할 때 "유전자콜로이드(eigencoloid)"라는 용어는 순수 단계(즉, 순수 Tc(OH),4 U(OH)4 또는 Am(OH)를 지정하는 데 사용된다.3 콜로이드들은 네바다 핵 실험장에서 플루토늄의 장거리 수송을 의심받아 왔다. 그들은 여러 해 동안 상세한 연구의 대상이 되어 왔다. 그러나 무기질 콜로이드의 이동성은 밀집한 점토막에서 초유입이 일어나는 과정 때문에 압축된 벤토나이트와 깊은 점토형성에서[40] 매우 낮다.[41] 문제는 종종 진정으로 용해된 유기 분자와 공극수에 혼합된 작은 유기 콜로이드에 대해서는 덜 명확하다.[42]
토양 과학에서 토양에 있는 콜로이드 분율은 지름 1μm 미만의 작은 점토 입자와 희석 입자로 구성되며 토양 샘플의 화학적 조건(즉, 토양 pH)에 따라 달라지는 양전하 및/또는 음전하 중 하나를 운반한다.[43]
정맥 요법
정맥주사 치료에 사용되는 콜로이드 용액은 주요 볼륨 확장기에 속하며 정맥주사 교체에 사용할 수 있다. 콜로이드들은 혈액 속에 높은 콜로이드 삼투압력을 보존하므로 이론적으로 혈관 내 부피를 우선적으로 증가시켜야 하는 반면 결정체라 불리는 다른 형태의 볼륨 확장기도 미간 부피와 세포내 부피를 증가시킨다.[44] 그러나 이 차이에 의한 실제 효능 차이에 대해서는 여전히 논란이 있고,[44] 이러한 콜로이드 사용과 관련된 연구의 상당 부분은 요아힘 볼트의 사기 연구에 근거하고 있다.[45] 또 다른 차이점은 결정체가 일반적으로 콜로이드보다 훨씬 싸다는 것이다.[44]
참조
- ^ a b Israelachvili, Jacob N. (2011). Intermolecular and surface forces (3rd ed.). Burlington, MA: Academic Press. ISBN 978-0-08-092363-5. OCLC 706803091.
- ^ International Union of Pure and Applied Chemistry. Subcommittee on Polymer Terminology (2009). Compendium of polymer terminology and nomenclature : IUPAC recommendations, 2008. Richard G. Jones, International Union of Pure and Applied Chemistry. Commission on Macromolecular Nomenclature. Cambridge: Royal Society of Chemistry. ISBN 978-1-84755-942-5. OCLC 406528399.
- ^ Stepto, Robert F. T. (1 January 2009). "Dispersity in polymer science (IUPAC Recommendations 2009)". Pure and Applied Chemistry. 81 (2): 351–353. doi:10.1351/PAC-REC-08-05-02. ISSN 1365-3075. S2CID 95122531.
- ^ 프란체스코 셀미, 스터디술라 디모루루 디 클로루로 다젠토, 누오비 안날리 델레 스시엔제 디 볼로냐, 파시 디 아고스토 1845.
- ^ 그레이엄은 1861년에 "콜로이드"라는 용어를 만들었다. 참고 항목: Graham, Thomas (1861) "분석에 적용되는 유동체 확산", 151 : 183–224 런던 왕립학회 철학적 거래. 183쪽부터: "겔라틴이 그 유형으로 보이므로, 클래스의 물질을 콜로이드로 지정하고, 물질의 콜로이드 조건으로서 그 독특한 형태의 집적 형태를 말하는 것을 제안한다."
- ^ a b Richard G. Jones; Edward S. Wilks; W. Val Metanomski; Jaroslav Kahovec; Michael Hess; Robert Stepto; Tatsuki Kitayama, eds. (2009). Compendium of Polymer Terminology and Nomenclature (IUPAC Recommendations 2008) (2nd ed.). RSC Publ. p. 464. ISBN 978-0-85404-491-7.
- ^ a b Stepto, Robert F. T. (2009). "Dispersity in polymer science (IUPAC Recommendations 2009)" (PDF). Pure and Applied Chemistry. 81 (2): 351–353. doi:10.1351/PAC-REC-08-05-02. S2CID 95122531.
- ^ Slomkowski, Stanislaw; Alemán, José V.; Gilbert, Robert G.; Hess, Michael; Horie, Kazuyuki; Jones, Richard G.; Kubisa, Przemyslaw; Meisel, Ingrid; Mormann, Werner; Penczek, Stanisław; Stepto, Robert F. T. (2011). "Terminology of polymers
and polymerization processes in dispersed systems (IUPAC Recommendations 2011)" (PDF). Pure and Applied Chemistry. 83 (12): 2229–2259. doi:10.1351/PAC-REC-10-06-03. S2CID 96812603. - ^ de Swaan Arons, J.; Diepen, G. A. M. (2010). "Immiscibility of gases. The system He-Xe: (Short communication)". Recueil des Travaux Chimiques des Pays-Bas. 82 (8): 806. doi:10.1002/recl.19630820810. ISSN 0165-0513.
- ^ de Swaan Arons, J.; Diepen, G. A. M. (1966). "Gas—Gas Equilibria". J. Chem. Phys. 44 (6): 2322. Bibcode:1966JChPh..44.2322D. doi:10.1063/1.1727043.
- ^ Lekkerkerker, Henk N.W.; Tuinier, Remco (2011). Colloids and the Depletion Interaction. Heidelberg: Springer. doi:10.1007/978-94-007-1223-2. ISBN 9789400712225. Archived from the original on 14 April 2019. Retrieved 5 September 2018.
- ^ van Anders, Greg; Klotsa, Daphne; Ahmed, N. Khalid; Engel, Michael; Glotzer, Sharon C. (2014). "Understanding shape entropy through local dense packing". Proc Natl Acad Sci USA. 111 (45): E4812–E4821. arXiv:1309.1187. Bibcode:2014PNAS..111E4812V. doi:10.1073/pnas.1418159111. PMC 4234574. PMID 25344532.
- ^ a b c Cosgrove, Terence (2010). Colloid Science: Principles, Methods and Applications. John Wiley & Sons. ISBN 9781444320183.
- ^ 코펠리오비치, 드미트리. 콜로이드 준비. substech.com
- ^ a b Everett, D. H. (1988). Basic principles of colloid science. London: Royal Society of Chemistry. ISBN 978-1-84755-020-0. OCLC 232632488.
- ^ Slomkowski, Stanislaw; Alemán, José V.; Gilbert, Robert G.; Hess, Michael; Horie, Kazuyuki; Jones, Richard G.; Kubisa, Przemyslaw; Meisel, Ingrid; Mormann, Werner; Penczek, Stanisław; Stepto, Robert F. T. (10 September 2011). "Terminology of polymers and polymerization processes in dispersed systems (IUPAC Recommendations 2011)". Pure and Applied Chemistry (in German). 83 (12): 2229–2259. doi:10.1351/PAC-REC-10-06-03. ISSN 1365-3075. S2CID 96812603.
- ^ Park, Soo-Jin; Seo, Min-Kang (1 January 2011). "Intermolecular Force". Interface Science and Technology. 18: 1–57. doi:10.1016/B978-0-12-375049-5.00001-3. ISBN 9780123750495. ISSN 1573-4285.
- ^ Colloid stability : the role of surface forces. Part I. Tharwat F. Tadros. Weinheim: Wiley-VCH. 2007. ISBN 978-3-527-63107-0. OCLC 701308697.CS1 maint: 기타(링크)
- ^ Genz, Ulrike; D'Aguanno, Bruno; Mewis, Jan; Klein, Rudolf (1 July 1994). "Structure of Sterically Stabilized Colloids". Langmuir. 10 (7): 2206–2212. doi:10.1021/la00019a029. ISSN 0743-7463.
- ^ Comba, Silvia; Sethi (August 2009). "Stabilization of highly concentrated suspensions of iron nanoparticles using shear-thinning gels of xanthan gum". Water Research. 43 (15): 3717–3726. doi:10.1016/j.watres.2009.05.046. PMID 19577785.
- ^ Bean, Elwood L.; Campbell, Sylvester J.; Anspach, Frederick R.; Ockershausen, Richard W.; Peterman, Charles J. (1964). "Zeta Potential Measurements in the Control of Coagulation Chemical Doses [with Discussion]". Journal (American Water Works Association). 56 (2): 214–227. doi:10.1002/j.1551-8833.1964.tb01202.x. ISSN 0003-150X. JSTOR 41264141.
- ^ Roland, I; Piel, G; Delattre, L; Evrard, B (2003). "Systematic characterisation of oil-in-water emulsions for formulation design". International Journal of Pharmaceutics. 263 (1–2): 85–94. doi:10.1016/S0378-5173(03)00364-8. PMID 12954183.
- ^ Lemarchand, Caroline; Couvreur, Patrick; Besnard, Madeleine; Costantini, Dominique; Gref, Ruxandra (2003). "Novel polyester-polysaccharide nanoparticles". Pharmaceutical Research. 20 (8): 1284–92. doi:10.1023/A:1025017502379. PMID 12948027. S2CID 24157992.
- ^ Mengual, O (1999). "Characterisation of instability of concentrated dispersions by a new optical analyser: the TURBISCAN MA 1000". Colloids and Surfaces A: Physicochemical and Engineering Aspects. 152 (1–2): 111–123. doi:10.1016/S0927-7757(98)00680-3.
- ^ Bru, P.; et al. (2004). T. Provder; J. Texter (eds.). Particle sizing and characterisation.
- ^ Matusiak, Jakub; Grządka, Elżbieta (8 December 2017). "Stability of colloidal systems - a review of the stability measurements methods". Annales Universitatis Mariae Curie-Sklodowska, sectio AA – Chemia. 72 (1): 33. doi:10.17951/aa.2017.72.1.33. ISSN 2083-358X.
- ^ Salager, J-L (2000). Françoise Nielloud; Gilberte Marti-Mestres (eds.). Pharmaceutical emulsions and suspensions. CRC press. p. 89. ISBN 978-0-8247-0304-2.
- ^ Snabre, Patrick; Pouligny, Bernard (2008). "Size Segregation in a Fluid-like or Gel-like Suspension Settling under Gravity or in a Centrifuge". Langmuir. 24 (23): 13338–47. doi:10.1021/la802459u. PMID 18986182.
- ^ Manoharan, Vinothan N. (2015). "Colloidal matter: Packing, geometry, and entropy" (PDF). Science. 349 (6251): 1253751. doi:10.1126/science.1253751. PMID 26315444. S2CID 5727282.
- ^ a b Greenfield, Elad; Nemirovsky, Jonathan; El-Ganainy, Ramy; Christodoulides, Demetri N; Segev, Mordechai (2013). "Shockwave based nonlinear optical manipulation in densely scattering opaque suspensions". Optics Express. 21 (20): 23785–23802. Bibcode:2013OExpr..2123785G. doi:10.1364/OE.21.023785. PMID 24104290.
- ^ Greenfield, Elad; Rotschild, Carmel; Szameit, Alexander; Nemirovsky, Jonathan; El-Ganainy, Ramy; Christodoulides, Demetrios N; Saraf, Meirav; Lifshitz, Efrat; Segev, Mordechai (2011). "Light-induced self-synchronizing flow patterns". New Journal of Physics. 13 (5): 053021. Bibcode:2011NJPh...13e3021G. doi:10.1088/1367-2630/13/5/053021.
- ^ Pieranski, P. (1983). "Colloidal Crystals". Contemporary Physics. 24: 25–73. Bibcode:1983ConPh..24...25P. doi:10.1080/00107518308227471.
- ^ Sanders, J.V.; Sanders, J. V.; Segnit, E. R. (1964). "Structure of Opal". Nature. 204 (4962): 1151. Bibcode:1964Natur.204..990J. doi:10.1038/204990a0. S2CID 4191566.
- ^ Darragh, P.J.; et al. (1976). "Opals". Scientific American. 234 (4): 84–95. Bibcode:1976SciAm.234d..84D. doi:10.1038/scientificamerican0476-84.
- ^ Luck, Werner; Klier, Manfred; Wesslau, Hermann (1963). "Über Bragg-Reflexe mit sichtbarem Licht an monodispersen Kunststofflatices. II". Berichte der Bunsengesellschaft für Physikalische Chemie. 67 (1): 84–85. doi:10.1002/bbpc.19630670114.
- ^ Hiltner, P.A.; Krieger, I.M. (1969). "Diffraction of light by ordered suspensions". J. Phys. Chem. 73 (7): 2306. doi:10.1021/j100727a049.
- ^ Liu, Xuesong; Li, Zejing; Tang, Jianguo; Yu, Bing; Cong, Hailin (9 September 2013). "Current status and future developments in preparation and application of colloidal crystals". Chemical Society Reviews. 42 (19): 7774–7800. doi:10.1039/C3CS60078E. ISSN 1460-4744. PMID 23836297.
- ^ Frimmel, Fritz H.; Frank von der Kammer; Hans-Curt Flemming (2007). Colloidal transport in porous media (1 ed.). Springer. p. 292. ISBN 978-3-540-71338-8.
- ^ Alonso, U.; T. Missana; A. Patelli; V. Rigato (2007). "Bentonite colloid diffusion through the host rock of a deep geological repository". Physics and Chemistry of the Earth, Parts A/B/C. 32 (1–7): 469–476. Bibcode:2007PCE....32..469A. doi:10.1016/j.pce.2006.04.021. ISSN 1474-7065.
- ^ Voegelin, A.; Kretzschmar, R. (December 2002). "Stability and mobility of colloids in Opalinus Clay" (PDF). Technischer Bericht / NTB. Institute of Terrestrial Ecology, ETH Zürich. Nagra Technical Report 02-14.: 47. ISSN 1015-2636. Archived from the original (PDF) on 9 March 2009. Retrieved 22 February 2009.
- ^ "Diffusion of colloids in compacted bentonite". Archived from the original on 4 March 2009. Retrieved 12 February 2009.
- ^ Wold, Susanna; Trygve Eriksen (2007). "Diffusion of humic colloids in compacted bentonite". Physics and Chemistry of the Earth, Parts A/B/C. 32 (1–7): 477–484. Bibcode:2007PCE....32..477W. doi:10.1016/j.pce.2006.05.002. ISSN 1474-7065.
- ^ R., Weil, Ray (11 October 2018). Elements of the nature and properties of soils. Brady, Nyle C. (Fourth ed.). New York, NY. ISBN 9780133254594. OCLC 1035317420.
- ^ a b c Martin, Gregory S. (19 April 2005). "An Update on Intravenous Fluids". Medscape. Medscape Infectious Diseases. Retrieved 6 July 2016.
- ^ Blake, Heidi (3 March 2011). "Millions of surgery patients at risk in drug research fraud scandal". The Telegraph. UK. Archived from the original on 4 November 2011. Retrieved 4 November 2011.
추가 읽기
- Berg, J.C. 인터페이스 및 콜로이드 소개: 나노과학으로 가는 다리. 2010년 세계과학출판사 ISBN 981-4293-07-5
- Lyklema, J. Interface and Colorid Science의 기초, 2권 3208, 1995
- 헌터, R.J. 콜로이드 사이언스 재단, 옥스퍼드 대학 출판부, 1989년
- 덕힌, S.S. & Derjaguin, B.V. 전자동 현상, J. Wiley and Sons, 1974년
- 러셀, W.B., 사빌, D.A. 및 쇼월터, W.R. 콜로이드 디스패션, 캠브리지, 1989년 캠브리지 대학 출판부
- Kruyt, H.R. Colorid Science, 제1권, 되돌릴 수 없는 시스템, Exvier, 1959년
- A.S. 덕힌과 괴츠, P.J. 콜로이드 특성을 나타내는 초음파, 엘스비에, 2002
- 로딜, 마. 루르드 C. 화학 중앙 과학, 7번 에드. ISBN 0-13-533480-2
- 피에란스키, P, 콜로이드 크리스탈, 컨템포러리. 물리, 24권, 페이지 25 (1983)
- 샌더스, J.V. Opal, Nature, Vol. 204, 페이지 1151, (1964)
- Darragh, P.J. 외, Scientific American, Vol. 234, 페이지 84, (1976년)
- 행운, W. 외, Ber. 부센주 피스 화학, 67권, 페이지 84(1963)
- 힐트너, P.A.와 크리거, 아이엠, 오더드 서스펜션에 의한 빛의 회절, J. Phys. 화학, 제73권, 페이지 2306(1969년)
- 아로라, 에이케이, 타타, B.V.R., 에드. 뉴욕의 유료 콜로이드 와일리에서의 주문 및 위상 전환 (1996)
- 수드, 영국 솔리드 스테이트 물리학, 에드. 에렌레이치, H, 턴불, D, 제45권, 페이지 1(1991)
- 머레이, C.A.와 그리어, D.G., 콜로이드 크리스탈, 아머. 과학자, 제83권, 페이지 238(1995);
- Annu, Monodispers Coloridal Systems의 비디오 현미경. 체육 목사 화학, 제47권, 페이지 421(1996)
- 다나카, T, 반응성 겔에서 볼륨 전환 1, Ed. Karl Dusek, 폴리머 과학의 진보, Vol.109, Springer Berlin(1993)



 콜로이드 입자의
콜로이드 입자의  (는) 서스펜션 매체의
(는) 서스펜션 매체의  콜로이드 입자의
콜로이드 입자의  (는) 침전물 또는 크림핑 속도.
(는) 침전물 또는 크림핑 속도.