에우로피움(Europium)III) 염화물
Europium( | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 에우로피움(Europium)III) 염화물 삼염화 유로피움 | |
| 식별자 | |
| |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.030.025 |
| EC 번호 |
|
펍켐 CID | |
| RTECS 번호 |
|
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| EuCl3 | |
| 어금질량 | 258.323 g/190 366.41 g/㎥(수화물) |
| 녹는점 | 632 °C(1,170 °F, 905 K) 분해 |
| 기타 용매의 용해성 | 수용성 |
| 구조 | |
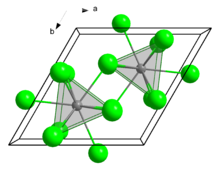
| 육각형(UCl형3), hP8 | |
| P63/m, 176번 | |
| 삼차 프리즘 (9시 15분) | |
| 관련 화합물 | |
기타 음이온 | 에우로피움(Europium)III) 산화물 |
기타 양이온 | 염화 사마륨(III) 염화 가돌리늄(III) |
관련 화합물 | 중염화유로피움 |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
에우로피움(Europium)III) 염화물은 EuCl이라는3 공식을 가진 무기 화합물이다. 무수 화합물은 노란색 고체다. 흡습성이기 때문에 물을 빠르게 흡수하여 하얀 결정인 육수화물, EuCl3/6을 형성한다.HO2, 무색무색. 그 화합물은 연구에 사용된다.
준비
수용성 HCl로 EuO를23 처리하면 수산화 Europium 염화물이 생성된다(EuCl3/6).HO2. 이 소금은 가열하여 무수 상태로 만들 수 없다. 대신 옥시염소화물을 얻는다. 무수 EuCl은3 EuO23[1][2] 또는 수산화 Europium 염화물(EuCl3/6)에서 시작하는 "암모늄 경로"에 의해 준비되는 경우가 많다.HO2) 230 °C까지 조심스럽게 가열한다.[3] 이러한 방법은 다음을 생성한다(NH4[2EuCl5]:
- 10 NHCl4 + EuO23 → 2 (NH4)[2EuCl5] + 6 NH3 + 3 HO2
- EuCl3·6H2O + 2 NH4Cl → (NH4)2[EuCl5] + 6 H2O
오타클로라이드는 다음 식에 따라 열적으로 분해된다.
- (NH4)[2EuCl5] → 2 NHCl4 + EuCl3
열분해 반응은 (NH4)[EuCl27]의 매개체를 통해 진행된다.
반응
에우로피움(Europium)III) 염화물은 다른 유로피언 화합물의 전구체다. 리튬 비스(트리메틸릴)아미드와의 염전계열을 통해 해당 금속 비스(트리메틸실릴)아미드로 변환할 수 있다.[4] 반응은 THF에서 수행되며 환류 시 기간이 필요하다.
- EuCl3 + 3 LiN(SiMe3)2 → Eu(N(SiMe3)23 + 3 LiCl
eu(N(SiMe3))23는 더욱 복잡한 조정 단지의 출발 재료다.
가열된 수소 가스로 감축하면 EuCl이2 나온다. 후자는 europium의 유기측정 화합물을 준비하기 위해 사용되어 왔다.II), 예를 들어 bis(Pentamethylcylopentadienyl)europium()II) 복합체.[5][6] 에우로피움(Europium)III) 염화물을 다른 유로피움 염류 준비의 출발점으로 사용할 수 있다.
구조
고체 상태에서는 UCl3 모티브로 결정된다. EU 센터는 9개의 조정으로 되어 있다.[7]
참고 문헌 목록
- Weast, R. C., ed. (1972). Handbook of Chemistry and Physics (53rd ed.). Cleveland, OH: Chemical Rubber Co.
참조
- ^ Meyer, G. (1989). The Ammonium Chloride Route to Anhydrous Rare Earth Chlorides-The Example of YCl3. Inorganic Syntheses. Vol. 25. pp. 146–150. doi:10.1002/9780470132562.ch35. ISBN 978-0-470-13256-2.
- ^ Edelmann, F. T.; Poremba, P. (1997). Herrmann, W. A. (ed.). Synthetic Methods of Organometallic and Inorganic Chemistry. Vol. VI. Stuttgart: Georg Thieme Verlag. ISBN 3-13-103021-6.
- ^ Taylor, M.D.; Carter, C.P. (1962). "Preparation of anhydrous lanthanide halides, especially iodides". Journal of Inorganic and Nuclear Chemistry. 24 (4): 387–391. doi:10.1016/0022-1902(62)80034-7.
- ^ Bradley, Donald C.; Ghotra, Joginder S.; Hart, F. Alan (1973). "Low co-ordination numbers in lanthanide and actinide compounds. Part I. The preparation and characterization of tris{bis(trimethylsilyl)-amido}lanthanides". Journal of the Chemical Society, Dalton Transactions (10): 1021–1023. doi:10.1039/DT9730001021.
- ^ Tilley, T. Don; Andersen, Richard A.; Spencer, Brock; Ruben, Helena; Zalkin, Allan; Templeton, David H. (1980). "Divalent lanthanide chemistry. Bis (pentamethylcyclopentadienyl) europium(II) and -ytterbium(II) derivatives: crystal structure of bis (pentamethylcyclopentadienyl) (tetrahydrofuran ytterbium(II) -hemitoluene at 176 K". Inorganic Chemistry. 19 (10): 2999. doi:10.1021/ic50212a031.
- ^ Evans, William J.; Hughes, Laura A.; Hanusa, Timothy P. (1986). "Synthesis and x-ray crystal structure of bis(pentamethylcyclopentadienyl) complexes of samarium and europium: (C5Me5)2Sm and (C5Me5)2Eu". Organometallics. 5 (7): 1285. doi:10.1021/om00138a001.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.



