염화 스칸듐
Scandium chloride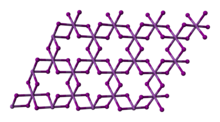 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 염화 스칸듐(III) | |
| 기타 이름 염화 스칸듐 삼염화산 스칸듐 | |
| 식별자 | |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.030.714 |
펍켐 CID | |
| RTECS 번호 |
|
| 유니 | |
CompTox 대시보드 (EPA) | |
| |
| |
| 특성. | |
| ScCl3 | |
| 어금질량 | 151.31 g/190 |
| 외관 | 회백색의 결정체 |
| 밀도 | 2.39 g/mL, 솔리드 |
| 녹는점 | 960°C(1,760°F, 1,230K)[1] 63°C(헥사하이드레이트) |
| 용해성성의 | |
| 기타 용매의 용해성 | EtOH에서 불용성인 |
| 위험 | |
| 산업안전보건(OHS/OSH): | |
주요 위험 | 자극적인 |
| NFPA 704(화재 다이아몬드) | |
| 치사량 또는 농도(LD, LC): | |
LD50(중간 선량) | 3980mg/kg(구강, 구강) |
| 안전 데이터 시트(SDS) | 외부 MSDS |
| 관련 화합물 | |
기타 음이온 | 스칸듐(III) 불소화 브롬화 스칸듐 스칸디움 삼요오드 |
기타 양이온 | 염화 이트리움(III) 루테튬()III) 염화물 |
관련 화합물 | 질산 스칸듐(III) |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
염화스캔듐(III)은 ScCl이라는3 공식을 가진 무기 화합물이다. 그것은 흰색, 고융해 이온 화합물로, 조미료가 풍부하고 수용성이 높다.[2] 이 소금은 주로 연구소에 관심이 많다. 무수 형태와 육수화물(ScCl3•6)HO2)는 상업적으로 이용할 수 있다.
구조
겹겹이 쌓인 BiI3 모티브의 ScCl3 결정체, 팔면체 스칸듐 센터가 특징이다.[3] 모노메릭 ScCl은3 900K의 증기 단계에서 지배적인 종으로, 조광기 ScCl은26 약 8%[4]를 차지한다. 전자 회절 스펙트럼은 모노머가 평면이고 조광기는 각 Sc가 4좌표인 두 개의 가교 Cl 원자를 가지고 있음을 나타낸다.[4]
반응
scCl은3 물을 흡수해 아쿠오 콤플렉스를 주는 루이스 산이다. X선 결정체에 따르면 그러한 수화물 중 하나는 소금 트랜스[ScCl2(HO2)]4Cl·2HO이다2.[5] 덜 기초적인 리간드 테트라하이드로푸란으로, ScCl은3 유도 ScCl3(THF)3을 흰색 결정으로 산출한다. 이 THF 수용성 복합체는 오르가오코스칸듐 화합물의 합성에 사용된다.[6] scCl은3 알돌 유사 반응에서 '루이스산-계면활성제 복합촉매(LASC)'로 조사된 도데실황산염으로 전환됐다.[7]
축소
염화스캔듐(III)은 700-800°C에서 염화스캔듐(III) 및 기타 염류의 황산화물 전기분해로 금속스캔듐을 처음 준비한 피셔 외 연구진에 의해 사용되었다.[8]
ScCl은3 스칸디움 금속과 반응하여 스칸디움이 산화 상태 <+3, ScCl, ScCl710, ScCl23, ScCl58, ScCl, ScCl712 등 여러 가지 염화물을 제공한다.[2][9] 예를 들어, 염화 세슘이 존재하는 상태에서 스칸듐 금속으로 ScCl을3 감소시키면 ScClII6 옥타헤드라 공유면이 포함된 합성물 ScCl이II3− 선형 체인에 포함된 CsScCl이3 생성된다.[10]
사용하다
염화스캔듐(III)은 일부 할로겐화 램프, 광섬유, 전자 세라믹, 레이저에서 발견된다.[11]
참조
- ^ Frederikse, H.P.R.; Lide, David R. (1998년) CRC 화학물리학 핸드북(78판)
- ^ a b Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ 분말 중성자 회절 데이터로부터 정제된 ScCl의3 결정구조, Fjellvgg, H, Karen, P, Acta Chemica Scandinavica, 48, 294-297, doi:10.3891/acta.chem.scand.48-0294
- ^ a b 하랜드 A, 마틴슨 K-G, 쇼로호프 D.J, 기리체프 G.V., 소콜로프 V.I., J. Chem. Soc, Dalton Trans, 1998, 2787 - 2792, doi:10.1039/a803339k
- ^ 희토류 요소, 기초 및 응용 프로그램 David A. 2012년 앳우드, ISBN 9781119950974 존 와일리 & 선스 주식회사
- ^ Manzer, L. E., "선택한 초기 전환 금속의 테트라하이드로푸란 복합체", 무기 합성물, 1982년, 제21권, 135-40.doi:10.1002/9780470132524.ch31권
- ^ Manabe, Kei; Mori, Yuichiro; Kobayashi, Shū (1999). "Effects of Lewis acid-surfactant-combined catalysts on aldol and Diels-Alder reactions in water". Tetrahedron. 55 (37): 11203–11208. doi:10.1016/S0040-4020(99)00642-0.
- ^ Fischer, Werner; Brünger, Karl; Grieneisen, Hans (1937). "Über das metallische Scandium". Zeitschrift für anorganische und allgemeine Chemie. 231 (1–2): 54–62. doi:10.1002/zaac.19372310107.
- ^ Corbett, J.D. (1981). "Extended metal-metal bonding in halides of the early transition metals". Acc. Chem. Res. 14 (8): 239–246. doi:10.1021/ar00068a003.
- ^ Meyer, Gerd.; Corbett, John D. (1981). "Reduced ternary halides of scandium: RbScX3 (X = chlorine, bromine) and CsScX3 (X = chlorine, bromine, iodine)". Inorganic Chemistry. 20 (8): 2627–2631. doi:10.1021/ic50222a047. ISSN 0020-1669.
- ^ 금속 공급업체 온라인. (2000). 염화 스칸듐




