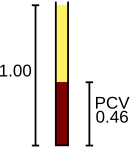완전혈구수
Complete blood count| 완전혈구수 | |
|---|---|
 CBC 및 차등 결과를 표시하는 출력물 앞 CBC 시료 | |
| 동의어 | 완전혈구수,[1] 완전혈구수(FBC),[2] 완전혈구수,[3] 완전혈구검사(FBE),[2] 혈구검사(Hemogram[4]) |
| 메슈 | D001772 |
| 메드라인플러스 | 003642 |
| 로인크 | CBC용 코드(예: 57021-8) |
| HCPCS-L2 | G0306 |
완전혈액수(CBC, Full Blood Count, FBC)라고도 알려진 완전혈액수(Complete Blood Count, CBC)는 사람의 혈액 속 세포에 대한 정보를 제공하는 일련의 의학 실험실 검사다.CBC는 백혈구, 적혈구 및 혈소판의 계수, 헤모글로빈 농도, 헤마토크리트(적혈구의 부피 백분율)를 나타낸다.적혈구의 평균 크기와 헤모글로빈 함량을 나타내는 적혈구 지표도 보고되며, 다른 종류의 백혈구를 세는 백혈구 차이도 포함될 수 있다.
CBC는 종종 의료 평가의 일환으로 수행되며 건강 모니터링이나 질병 진단에 사용될 수 있다.성별과 연령에 따라 달라지는 기준 범위에 비교함으로써 결과를 해석한다.빈혈과 혈소판감소증과 같은 질환은 비정상적인 완전혈구수 결과에 의해 정의된다.적혈구 지수는 철분 결핍, 비타민 B12 결핍 등 사람의 빈혈의 원인에 대한 정보를 제공할 수 있으며, 백혈병 같은 바이러스, 세균, 기생충 감염과 혈액 질환을 진단하는 데 백혈병 등 백혈구 차이의 결과가 도움이 될 수 있다.기준 범위를 벗어나는 모든 결과가 의료 개입을 필요로 하는 것은 아니다.
CBC는 기본 실험실 장비나 자동 혈액학 분석기를 사용하여 수행되며, 이 분석기는 세포의 크기와 구조에 대한 정보를 수집한다.헤모글로빈의 농도를 측정하고 적혈구 지수를 적혈구와 헤모글로빈을 측정하여 계산한다.수동 테스트를 사용하여 비정상적인 결과를 독립적으로 확인할 수 있다.검체의 약 10~25%는 수동 혈액 얼룩 검사를 필요로 하며,[5] 분석기 결과가 세포의 모양과 일치하는지 확인하고 이상을 찾기 위해 혈액을 현미경으로 관찰한다.헤마토크릿은 시료를 원심분리하고 적혈구 비율을 측정해 수작업으로 결정할 수 있으며, 자동화된 기기에 접근하지 못한 실험실에서는 혈모세포계를 이용해 혈구를 현미경으로 계수한다.
1852년 칼 비에로르트는 혈구수를 수행하기 위한 첫 번째 절차를 발표했는데, 여기에는 알려진 양의 혈구를 현미경 슬라이드에 뿌리고 모든 세포를 세는 것이 포함된다.루이찰스 맬러세즈에 의해 1874년 혈모세포계가 발명되면서 혈액세포의 현미경 분석이 단순화되었고, 19세기 후반에는 폴 에를리히와 드미트리 레오니도비치 로마노프스키가 여전히 혈흔을 검사하는 데 사용되는 백혈구와 적혈구를 염색하는 기술을 개발하였다.헤모글로빈 측정에 대한 자동화된 방법이 1920년대에 개발되었고, 맥스웰 윈트로브는 1929년에 윈트로브 헤마토크리트법을 도입하였고, 이 방법을 통해 적혈구 지수를 정의할 수 있게 되었다.혈구 수 자동화의 획기적인 점은 1953년 월리스 H. 콜터가 특허를 낸 쿨터 원칙이다.콜터 원리는 혈액 세포를 세고 그 크기를 결정하기 위해 전기 임피던스 측정을 사용한다; 그것은 많은 자동화된 분석기에서 사용되고 있는 기술이다.1970년대 추가 연구에서는 백혈구 차이의 자동화를 가능케 한 세포의 수를 세고 식별을 위해 광학적 측정을 사용하는 것이 포함되었다.
목적
혈액은 혈장이라고 불리는 액체 부분과 적혈구, 백혈구, 혈소판 등을 포함하는 세포 부분으로 구성된다.[note 1][7]전체 혈액수는 혈액의 세 가지 세포 성분을 평가한다.빈혈이나 혈소판감소증과 같은 일부 의학적 상태는 혈구 수의 현저한 증가 또는 감소에 의해 정의된다.[8]많은 장기 체계의 변화는 혈액에 영향을 미칠 수 있기 때문에 CBC 결과는 광범위한 상태를 조사하는 데 유용하다.그것이 제공하는 정보의 양 때문에, 완전한 혈액수는 가장 일반적으로 수행되는 의학 실험실 시험들 중 하나이다.[9][10][11]
CBC는 종종 의료 평가의 일환으로 질병을 검진하는 데 사용된다.[12]그것은 또한 의료 제공자가 감염, 출혈 장애 또는 일부 암과 같은 혈액 세포에 영향을 미치는 질병이 있다고 의심하는 경우에 요구된다.비정상적인 CBC 결과를 초래할 수 있는 질환을 진단받거나 혈구 수에 영향을 줄 수 있는 치료를 받고 있는 사람은 자신의 건강을 감시하기 위해 정기적으로 CBC를 실시하게 될 수 있으며,[4][12] 입원 중인 사람을 대상으로 매일 검사를 실시하는 경우가 많다.[13]그 결과는 혈액이나 혈소판 수혈의 필요성을 나타낼 수 있다.[14]
전체 혈액수는 많은 의학 전문분야에서 특정한 용도가 있다.빈혈 발견, 혈소판 수치 충분 확인, 감염 여부 선별,[15][16] 수술 후 출혈 감시가 가능하도록 수술 전 시행하는 경우가 많다.[12][17]응급의학에서 CBC는 발열, 복통, 호흡곤란 등 수많은 증상을 조사하고 [18][19][20]출혈과 외상을 평가하는 데 사용된다.[21][22]암에 대한 화학요법이나 방사선치료를 받고 있는 사람들에게서 혈액수는 면밀하게 관찰된다. 이러한 치료법은 골수의 혈구 생산을 억제하고 백혈구, 혈소판, 헤모글로빈을 심각하게 낮은 수준으로 생산할 수 있기 때문이다.[23]정기적인 CBC는 클로자핀이나 카바마제핀과 같은 일부 정신의학적 약물을 복용하는 사람들에게 필요한데, 드물게 백혈구 수의 생명을 위협하는 감소(농약구획증)를 일으킬 수 있다.[24][25]임신 중의 빈혈은 산모와 아기에게 더 나쁜 결과를 초래할 수 있기 때문에, 완전한 혈액 수치는 산전관리의 일상적인 부분이다;[26] 신생아의 경우, 패혈증의 지표가 될 수 있는 백혈구 차이의 미숙한 세포 수를 조사하거나 계산하기 위해 CBC가 필요할 수 있다.[27][28]
완전혈구수는 혈액학에서 필수적인 도구로 혈액과 관련된 질병의 원인, 예후, 치료, 예방을 연구하는 학문이다.[29]CBC와 얼룩 검사의 결과는 혈액 세포의 생산과 발달, 특히 골수에 관여하는 기관과 조직인 조혈모세포의 기능을 반영한다.[9][30]예를 들어 세 가지 세포 유형(판시토페니아)을 모두 적게 세면 혈구 생성에 골수 질환이 영향을 미치고 있음을 나타낼 수 있으며, 골수 검사를 통해 원인을 더욱 자세히 조사할 수 있다.[31]혈액 표지의 비정상적인 세포는 급성 백혈병이나 림프종을 나타낼 수 있는 반면,[30] 비정상적으로 높은 수의 중성미자나 림프구는 지시 증상 및 혈액 표식 결과와 결합하여 골수성 백혈병이나 림프구 질환을 의심하게 할 수 있다.CBC 결과와 혈액의 얼룩을 검사하면 영양결핍, 골수장애, 후천적 용혈성 무감각증, 겸상적혈구 빈혈, 탈라체와 같은 유전적 조건과 같은 빈혈의 원인을 구별하는 데 도움이 될 수 있다.[32][33]
전체 혈액수의 기준 범위는 겉보기에는 건강한 사람의 95%에서 발견된 결과의 범위를 나타낸다.[note 2][35]정의에 따르면, 결과의 5%는 항상 이 범위를 벗어나므로, 일부 비정상적인 결과는 의학적인 문제를 나타내기 보다는 자연적인 변화를 반영할 수 있다.[36]이는 특히 그러한 결과가 기준 범위를 약간 벗어나거나, 이전 결과와 일치하거나, 또는 CBC에 의해 나타난 다른 관련 이상이 없는 경우에 발생할 가능성이 높다.[37]비교적 건강한 모집단에 대해 검사를 수행할 때 임상적으로 경미한 이상 징후 수가 질병을 나타내는 결과 수를 초과할 수 있다.[38]이 때문에 미국, 영국, 캐나다의 전문기관들은 관련 의료조건이 없는 개인의 저위험 수술에 대한 수술 전 CBC 검사에 반대할 것을 권고하고 있다.[15][39][40]입원한 환자의 혈액학 검사를 위해 반복적으로 혈액을 뽑아내는 것은 병원에서 얻은 빈혈의 원인이 될 수 있고 불필요한 수혈을 초래할 수 있다.[38]
절차
이 샘플은 항응고제(일반적으로 EDTA)가 들어 있는 튜브에 혈액을 끌어들여 자연 응고를 멈추게 함으로써 채취된다.[41]혈액은 보통 정맥에서 채취되지만 이것이 어려울 때는 손가락 마디에 의해 모세혈관에서 채취하거나 아기들의 발뒤꿈치로 채취하기도 한다.[42][43]테스트는 일반적으로 자동분석기로 수행되지만 혈액검사와 같은 수동기법이나 수동 헤마토크리트 검사법을 사용하여 비정상적인 결과를 조사할 수 있다.[44]셀 수 및 헤모글로빈 측정은 자동화된 기기에 대한 접근이 부족한 실험실에서 수동으로 수행된다.[45]
자동화된
분석기에 탑승하면 샘플이 동요하여 세포를 균등하게 분포시킨 다음 희석하여 최소 두 개의 채널로 분할하는데, 그 중 하나는 적혈구와 혈소판 수를 세고 다른 하나는 백혈구 수를 세어 헤모글로빈 농도를 결정하는 데 사용된다.일부 계측기는 별도의 채널에서 헤모글로빈을 측정하며, 차등 백혈구 수, 레티쿨로시세포 수, 혈소판의 특화된 측정에 추가 채널을 사용할 수 있다.[46][47][48]이 세포들은 유체 흐름에서 매달려 있으며 흐름 세포측정법이라고 알려진 기법으로 센서들을 지나 흐를 때 그 성질을 측정한다.[note 3][49][52]희석된 샘플이 저압 액의 흐름에 주입되어 샘플의 셀이 층류 흐름을 통해 한 줄로 정렬되도록 하는 등 보다 정확한 결과를 얻을 수 있도록 개별 셀을 격리하는 데 유체역학적 초점을 사용할 수 있다.[53][54]
헤모글로빈 농도를 측정하기 위해 시약 화학물질을 검체에 첨가하여 적혈구 수치에 사용되는 채널과 별개의 채널에서 적혈구를 파괴(lyse)한다.헤모글로빈 측정과 같은 채널에서 백혈구 계수를 수행하는 분석기에서는 이를 통해 백혈구를 보다 쉽게 계량할 수 있다.[55]혈액학 분석기는 분광측정법을 사용하여 헤모글로빈을 측정하며 빛의 흡광도와 존재하는 헤모글로빈 양 사이의 선형 관계에 기초한다.화학 물질은 옥시헤모글로빈, 카복시헤모글로빈과 같은 다른 형태의 헤모글로빈을 하나의 안정된 형태, 보통은 시안메트헤모글로빈으로 전환시키고 영구적인 색 변화를 일으키는데 사용된다.특정 파장(보통 540나노미터)에서 측정했을 때 발생하는 색상의 흡광도는 헤모글로빈 농도와 일치한다.[56][57]
센서는 전기 임피던스와 빛의 산란이라는 두 가지 주요 원리를 사용하여 샘플의 셀을 세고 식별한다.[58]임피던스 기반 셀 카운팅은 쿨터 원리에 따라 동작한다. 셀은 전류를 운반하는 액체로 매달려 있으며, 작은 개구부(구경)를 통과할 때 전기 전도도가 떨어져 전류 감소를 일으킨다.셀이 개구부를 통과할 때 생성되는 전압 펄스의 진폭은 셀에 의해 이동된 유체의 양과 상관관계가 있는 반면,[59][60] 셀의 부피와 전체 펄스 수는 샘플의 셀 수와 상관관계가 있다.셀 볼륨의 분포는 히스토그램에 표시되며, 각 셀 유형의 일반적인 크기를 기준으로 볼륨 임계값을 설정함으로써 서로 다른 셀 모집단을 식별하고 셀 수를 셀 수 있다.[61]
가벼운 산란 기법에서는 레이저나 텅스텐 할로겐 램프의 빛이 세포의 흐름을 향하게 하여 크기와 구조에 대한 정보를 수집한다.세포는 광도계를 이용해 검출되는 빔을 통과할 때 다른 각도로 빛을 산란시킨다.[62]빔의 축을 따라 산란되는 빛의 양을 가리키는 전방 산란(Forward sparant)은 주로 빛의 회절에 의해 발생하며 세포 크기와 상관관계가 있으며, 측면 산란(90도 각도로 산란된 빛)은 반사 및 굴절에 의해 발생하며 세포 복잡성에 대한 정보를 제공한다.[62][63]
무선주파수 기반 방법은 임피던스와 조합하여 사용할 수 있다.이러한 기법은 세포가 개구부를 통과할 때 전류의 방해를 측정하는 것과 같은 원리에 작용하지만 고주파 RF 전류가 세포 안으로 침투하기 때문에 결과 펄스의 진폭은 핵의 상대적 크기, 핵의 구조, 세포핵의 과립의 양과 같은 요인과 관련된다.m.[64][65] 혈소판과 크기가 비슷한 작은 적색세포와 세포 이물질은 혈소판 개수를 방해할 수 있으며, 큰 혈소판은 정확하게 계산되지 않을 수 있으므로, 일부 분석기기는 형광 얼룩, 다각광 산란, 단각 항체 태깅과 같은 혈소판을 측정하기 위해 추가 기법을 사용한다.[48]
대부분의 분석기자는 평균세포량(MCV)이라고 하는 적혈구의 평균 크기를 직접 측정하여 적혈구수를 MCV에 곱하여 헤마토크리트(Hymocrit)를 계산한다. 적혈구의 총 부피를 샘플링한 혈액의 부피와 비교하여 헤마토크리트(Hymocrit)와 적혈구로부터 MCV를 추출한다.혈구 [66]수헤모글로빈 농도, 적혈구 수, 헤마토크릿은 각 적혈구 내 헤모글로빈의 평균 양, 평균 분자 헤모글로빈 농도(MCH)를 계산하는 데 사용된다.[67]또 다른 계산인 적혈구 분포 폭(RDW)은 평균 세포 부피의 표준 편차에서 도출되며 세포 크기의 변화를 반영한다.[68]
시약으로 치료한 후, 백혈구는 히스토그램에 볼륨이 표시되면 세 개의 뚜렷한 피크를 형성한다.이러한 정점들은 대략 과립구, 림프구 및 기타 단핵세포의 모집단에 해당하므로 세포량만을 기준으로 3부 분차를 수행할 수 있다.[69][70]더 나은 고급 분석기seven-part는 미분 빛 산란 또는 고주파 analysis,[70]또는cells—for 예 안에 특정 화학 물질을 염색하 색소를 사용해 같은 5을 제공하기 위해 추가적인 기법들을 사용하는 미숙한 cells[71]또는 myeloperoxidase에 많이 발견된다 핵산, 효소 번째의 세포에서 발견된.emyelo신분 [72][73]혈통바소필은 시약이 다른 백혈구를 파괴하고 바소필을 그대로 두는 별도의 채널에서 계수될 수 있다.이러한 측정에서 수집된 데이터는 분석되고 산점그램에 표시되며, 산점그램은 각 백혈구 유형과 상관관계가 있는 군집을 형성한다.[70][72]미분수 자동화를 위한 또 다른 접근방식은 디지털 현미경 소프트웨어를 사용하는 것인데,[74] 이 소프트웨어는 인공 지능을 사용하여 혈흔의 광자극으로부터 백혈구를 분류한다.셀 이미지는 인간 운영자에게 표시되며, 필요한 경우 수동으로 셀을 다시 분류할 수 있다.[75]
대부분의 분석기자들은 모든 검사를 완전한 혈액수에서 실행하는 데 1분도 걸리지 않는다.[58]분석기자들이 개별 세포를 많이 시료화하고 세기 때문에 그 결과는 매우 정밀하다.[76]그러나 일부 비정상적인 셀은 정확하게 식별되지 않을 수 있으므로 계측기 결과를 수동으로 검토하고 계측기가 분류할 수 없는 다른 비정상적인 셀 수단에 의한 식별이 필요하다.[5][77]
진료지점검사
진료지점시험이란 사람의 침대 옆이나 진료소에서와 같이 실험실 환경 밖에서 실시하는 시험을 말한다.[78][79]이 시험방법은 기존 방법에 비해 속도가 빠르고 혈액을 적게 사용하며, 특별히 훈련된 인력이 필요하지 않기 때문에 응급상황이나 자원에 대한 접근이 제한된 지역에서 유용하다.흔히 진료지점혈액검사에 사용되는 장치로는 분광측정법을 이용해 시료의 헤모글로빈 농도를 측정하는 휴대용 분석기 헤모큐와 혈액의 전도도에서 적혈구 농도를 추정해 헤모글로빈 판독치를 도출하는 i-STAT가 있다.[79]헤모글로빈과 헤마토크릿은 혈액 가스 검사를 위해 설계된 관리 지점에서 측정할 수 있지만, 이러한 측정은 표준 방법을 통해 얻은 측정값과 좋지 않은 상관관계가 있는 경우가 있다.[78]완전한 혈액수와 차이를 제공할 수 있는 진료소에서 사용하도록 설계된 혈액학 분석기의 단순화된 버전이 있다.[80]
수동
시험은 자동화된 장비를 사용할 수 없거나 분석기 결과가 추가 조사가 필요한 것으로 나타날 때 수동으로 수행할 수 있다.[45]자동화된 결과는 분석기가 제대로 계산할 수 없는 비정상적인 세포군,[5] 결과가 부정확할 수 있음을 암시하는 분석기에 의해 생성된 내부 플래그 [81]또는 설정된 임계값을 벗어나는 수치적 결과일 수 있다.[77]이러한 문제를 조사하기 위해 현미경 슬라이드에 피를 뿌리고 로마노프스키 얼룩으로 얼룩져 현미경으로 검사한다.[82]적혈구와 백혈구, 혈소판의 외관을 평가하고, 존재하는 경우 질적 이상을 보고한다.[83]적혈구의 외관 변화는 상당한 진단적 의미를 가질 수 있는데, 예를 들어 낫 세포의 존재는 낫 세포 질환을 나타내며, 분열된 적혈구(슈이스트모세포)의 수가 많으면 미세항진성 용혈성 빈혈을 암시할 수 있기 때문에 긴급한 조사가 필요하다.[84]일부 염증 조건과 다발성 골수종과 같은 파라프로테인 장애에서는 혈중 단백질의 수치가 높으면 홍혈구가 얼룩덜룩하게 나타나게 되는데, 이를 루루라고 한다.[85]말라리아, 개병 등 일부 기생충 질환은 혈흔에 있는 원인균을 찾아내어 검출할 수 있으며 [86]혈소판 수치는 혈흔에서 추정할 수 있어 자동 혈소판 수치가 부정확할 경우 유용하다.[77]
수동 백혈구 차이를 수행하기 위해 현미경 분석가는 혈액에 있는 100개의 세포를 세어 그들의 외모를 기준으로 분류한다; 때때로 200개의 세포가 계수된다.[87]이는 백혈구 유형별 비율을 부여하며, 이러한 비율을 백혈구 총수에 곱함으로써 백혈구 유형별 절대수를 얻을 수 있다.[88]수동계수는 자동분석과 비교했을 때 셀이 거의 집계되지 않아 표본오차가 발생하지만 급성백혈병에서 볼 수 있는 송풍세포 [72][77]등 분석기자가 할 수 없는 비정상세포를 확인할 수 있다.[76][89]독성 과립과 같은 임상적으로 중요한 특징도 백혈구의 현미경 검사에서 확인할 수 있다.[90]
헤마토크릿은 모세관에 혈액을 채워 원심분리하고 적혈구로 구성된 혈중 비율을 측정하는 방식으로 수작업으로 수행할 수 있다.[66]이는 다혈구(고도로 높은 적혈구 수)[66]나 심각한 백혈구 수(고도로 높은 백혈구 수)와 같이 자동화된 헤마토크리트 결과가 부정확하게 될 수 있는 일부 조건에서 유용하다.[91]
적혈구와 백혈구 및 혈소판은 지정된 양의 희석혈액을 보관하는 챔버가 들어 있는 현미경 슬라이드인 혈모시계를 사용하여 계산할 수 있다.혈소판 측정기의 챔버는 셀 카운팅을 돕기 위해 보정된 그리드로 식각된다.격자 안에 보이는 세포들을 세어서 검사한 혈액의 부피로 나누는데, 이는 격자 상에 계수된 정사각의 수에서 결정되어 시료 속의 세포의 농도를 얻는다.[45][92]수동 셀 카운트는 자동화된 방법에 비해 노동 집약적이고 부정확하기 때문에 자동화된 분석기에 접근할 수 없는 실험실을 제외하고는 거의 사용되지 않는다.[45][92]백혈구를 세려면 옥살산 암모늄, 아세트산, 염산 등 적혈구를 침윤하는 화합물이 포함된 액체를 사용해 시료를 희석한다.[93]간혹 백혈구의 핵을 부각시키는 희석액에 얼룩이 더해져 식별이 쉬워지기도 한다.수동 혈소판 수치는 유사한 방식으로 수행되지만, 일부 방법은 적혈구를 그대로 유지한다.가벼운 현미경보다는 위상 대비 현미경을 사용하면 혈소판을 쉽게 식별할 수 있다.[94]적혈구 수치 수동은 적혈구 측정이 부정확하고 적혈구 측정에 헤모글로빈측정법, 수작업 헤마토크리트법 등 다른 방법을 이용할 수 있지만, 필요한 경우 염분으로 희석된 혈액에서 적혈구를 계량할 수 있다.[95]
헤모글로빈은 분광도계나 색도계를 사용하여 수동으로 측정할 수 있다.헤모글로빈을 수동으로 측정하기 위해 적혈구를 파괴하는 시약을 사용하여 검체를 희석하여 헤모글로빈을 방출한다.다른 종류의 헤모글로빈을 한 형태로 변환하기 위해 다른 화학물질이 사용되어 쉽게 측정할 수 있다.그런 다음 용액을 측정 큐벳에 놓고 흡광도를 특정 파장에서 측정하는데, 이는 사용되는 시약의 종류에 따라 달라진다.알려진 양의 헤모글로빈을 포함하는 기준 표준은 흡광도와 헤모글로빈 농도 사이의 관계를 결정하기 위해 사용되어 표본의 헤모글로빈 수준을 측정할 수 있다.[96]
시골지역과 경제적 취약지역에서는 장비 및 인력에 대한 접근에 의해 이용 가능한 시험이 제한된다.이러한 지역의 1차 치료 시설에서 시험은 적혈구 형태학 검사와 헤모글로빈의 수동 측정에 국한될 수 있으며, 수동 셀 수 및 차등, 때로는 자동화된 셀 수 등과 같은 보다 복잡한 기법이 지역 연구소에서 수행된다.지역 및 지방 병원과 학술 센터는 일반적으로 자동 분석기에 접근할 수 있다.실험실 시설을 이용할 수 없는 경우, 표준화된 형태의 흡수성 용지에 혈액을 떨어뜨려 색척도와 비교함으로써 헤모글로빈 농도의 추정치를 얻을 수 있다.[97]
품질관리
자동 분석기는 정기적으로 보정해야 한다.대부분의 제조업체는 정의된 매개 변수를 사용하여 보존 혈액을 제공하고 결과가 정의된 임계값을 벗어날 경우 분석기를 조정한다.[98]결과가 계속 정확하도록 하기 위해, 일반적으로 계기 제조업체가 제공하는 품질관리 시료를 적어도 하루에 한 번 이상 시험한다.샘플은 특정 결과를 제공하도록 제조되며, 실험실은 그 결과를 알려진 값과 비교하여 기기가 올바르게 작동하는지 확인한다.[99][100]상업적 품질 관리 재료에 접근할 수 없는 실험실의 경우 인도 규제 기관은 환자 샘플을 중복하여 실행하고 결과를 비교할 것을 권고한다.[101]환자 검체의 평균 결과를 정해진 간격으로 측정하는 이동 평균 측정을 추가 품질 관리 기법으로 사용할 수 있다.시간이 지남에 따라 환자 모집단의 특성이 거의 동일하다고 가정하면 평균은 일정하게 유지되어야 한다. 평균 값의 큰 변화는 계측기 문제를 나타낼 수 있다.[99][100]이 점에서 MCHC 값은 특히 유용하다.[102]
실험실은 결과가 알려진 내부 품질 관리 샘플을 분석하는 것 외에도 규제 기관으로부터 외부 품질 평가 샘플을 받을 수 있다.내부 품질 관리의 목적은 분석기 결과가 주어진 실험실에서 재현 가능한지 확인하는 것이지만, 외부 품질 평가는 서로 다른 실험실의 결과가 서로 일치하고 목표값과 일치하는지 검증한다.[103]외부품질평가 표본에 대한 예상 결과는 실험실에 공개되지 않는다.[104]외부 품질 평가 프로그램은 북미와 서유럽에서 널리 채택되어 왔으며,[99] 인가를 유지하기 위해 실험실이 이러한 프로그램에 참여해야 하는 경우가 많다.[105]물류상의 문제로 인해 지원 수준이 낮은 분야의 실험실이 외부 품질 평가 계획을 구현하기가 어려울 수 있다.[106]
포함 테스트
CBC는 혈소판과 적혈구 및 백혈구의 양을 헤모글로빈 및 헤마토크리트 값과 함께 측정한다.적혈구 지수 -적혈구의 크기와 그 헤모글로빈 함량을 설명하는 MCV, MCH, MCHC는 적혈구 크기의 변화량을 측정하는 적혈구 분포폭(RDW)과 함께 보고된다.다른 종류의 백혈구를 열거하는 백혈구 차등을 실시할 수도 있고, 미성숙 적혈구(소모세포)의 카운트가 포함되는 경우도 있다.[4][107]
적혈구, 헤모글로빈, 헤마토크리트
| 분석 물질 | 결과 | 정상범위 |
|---|---|---|
| 적세포수 | 5.5 x 1012/L | 4.5–5.7 |
| 백혈구수 | 9.8 x 109/L | 4.0–10.0 |
| 헤모글로빈 | 123 g/L | 133–167 |
| 헤마토크리트 | 0.42 | 0.35–0.53 |
| MCV | 76 fL | 77–98 |
| MCH | 22.4 페이지 | 26–33 |
| MCHC | 293 g/L | 330–370 |
| RDW | 14.5% | 10.3–15.3 |
적혈구는 폐에서 조직으로 산소를 전달하고, 그들이 돌아오면 이산화탄소를 폐에서 배출되는 곳으로 다시 운반한다.이 기능들은 세포의 헤모글로빈에 의해 매개된다.[109]분석기는 적혈구를 세어 혈액(× 10/μL6) 마이크로리터 당 10개6 또는 리터 당12 10개12 세포 단위로 결과를 보고하고, 평균 크기를 측정하는데, 이를 평균 세포량이라고 하며 펨톨리트 또는 입방 마이크로미터로 표현한다.[4]적혈구의 수, 그 혈구(헤마토 크리트)또는 포장된 혈구 용적(PCV)에 의해 평균 혈구 용적, 또한 multiplying한 것까지, 혈액은 적혈구로 이루어졌습니다. 그러나 그 비율의 측정되고 혈구를 직접 수행된다[66]과 세계의 평균 혈구 용적은 혈구와 적혈구 수로 계산할 수 파생될 수 있다.[110][111]적혈구를 라이스 처리한 후 측정되는 헤모글로빈은 보통 리터당 그램(g/L) 또는 데틸리트르당 그램 단위로 보고된다.[112]적혈구가 정상이라고 가정하면 헤모글로빈과 헤마토크리트 사이에는 일정한 관계가 있는데, 헤마토크리트 퍼센트가 g/dL의 헤모글로빈 값보다 약 3배 더 크며, 플러스 마이너스 3이다.3의 법칙이라고 불리는 이 관계는 CBC 결과가 정확한지 확인하는 데 사용될 수 있다.[113]
다른 두 가지 측정은 적혈구 수, 헤모글로빈 농도, 헤마토크리트, 즉 평균 말뭉치 헤모글로빈 농도로부터 계산된다.[114][115]이 매개변수들은 각 적혈구의 헤모글로빈 함량을 설명한다.MCH와 MCHC는 혼동될 수 있다. 본질적으로 MCH는 적혈구당 평균 헤모글로빈 양을 측정하는 것이다.MCHC는 헤모글로빈인 세포의 평균 비율을 제공한다.MCH는 적혈구의 크기를 고려하지 않는 반면 MCHC는 적혈구의 크기를 고려하지 않는다.[116]종합하여 MCV, MCH, MCHC를 적혈구 지수라고 한다.[114][115]이러한 지수의 변화는 혈액 얼룩에 나타나는데, 비정상적으로 크거나 작은 적혈구는 백혈구의 크기에 비해 식별이 가능하며 헤모글로빈 농도가 낮은 세포는 창백하게 나타난다.[117]또 다른 파라미터는 적혈구 세포의 초기 측정치인 적혈구 분포 폭 또는 RDW로부터 계산되는데, 이는 세포 크기의 변화 정도를 반영한다.[118]

헤모글로빈, 헤마토크리트, 적혈구 수치가 비정상적으로 낮으면 빈혈이 나타난다.[119]빈혈은 그 자체로 진단되는 것이 아니라 그 사람의 적혈구에 영향을 미치는 근본적인 상태를 가리킨다.[88]빈혈의 일반적인 원인은 출혈, 결함 있는 적혈구 생산(불효성 적혈구 생성), 적혈구 생산 감소(불충분한 적혈구 생성), 적혈구 파괴 증가(혈액성 빈혈) 등이다.[120]빈혈은 혈액의 산소 운반 능력을 떨어뜨려 피로감, 호흡곤란 등의 증상을 일으킨다.[121]사람의 임상 상태에 따라 헤모글로빈 수치가 한계치 이하로 떨어지면 수혈이 필요할 수 있다.[122]
적혈구의 증가는 보통 헤모글로빈과 헤마토크릿의 증가로 이어지는 다혈구증이라고 한다.[note 4][126]탈수나 이뇨제를 사용하면 적색세포에 비해 혈장의 양을 줄임으로써 '상대적' 다성체질을 유발할 수 있다.절대다혈구라고 불리는 적혈구의 수의 진정한 증가는 신체가 폐나 심장질환과 같은 조건에서 만성적으로 낮은 산소 농도를 보상하기 위해 적혈구를 더 많이 생산하거나, 적혈구의 생성을 촉진하는 호르몬인 에리트로포이에틴(EPO)의 수치가 비정상적으로 높을 때 발생할 수 있다.다혈질 베라에서, 골수는 과도하게 높은 속도로 적혈구와 다른 혈액세포를 생산한다.[127]
적혈구 지수의 평가는 빈혈의 원인을 파악하는 데 도움이 된다.MCV가 낮을 경우 빈혈은 미세혈성이라고 하는 반면, MCV가 높은 빈혈은 거시적 빈혈이라고 한다.MCHC가 낮은 빈혈은 저자극성 빈혈이라고 불린다.빈혈이 있지만 적혈구 지수가 정상인 경우, 빈혈은 노르만색성, 노르모피성으로 간주된다.[117]높은 MCHC를 가리키는 하이퍼크로미아라는 용어는 일반적으로 사용되지 않는다.참조 상한 값 이상의 MCHC 상승은 드물며, 주로 척추측만증, 겸상세포질환, 헤모글로빈 C질환과 같은 조건에서 발생한다.[115][128]또한 MCHC 상승은 적혈구 응고(적혈구 수를 거짓으로 감소시켜 MCHC를 상승시킨다)[129][130]와 같은 조건이나 혈액 내 지질의 높은 증가(헤모글로빈 결과의 잘못된 증가를 야기한다)[128][131]에서 오는 잘못된 결과일 수 있다.
미세혈성 빈혈은 일반적으로 철분결핍, 탈라세혈증, 만성질환의 빈혈과 관련이 있는 반면, 거시적 빈혈은 알코올중독, 엽산, B12결핍증, 일부 약물의 사용, 일부 골수질환과 관련이 있다.급성 출혈, 용혈성 빈혈, 골수 장애, 각종 만성 질환으로 인해 노르모시성 혈액 사진으로 빈혈이 발생할 수 있다.[115][132]MCV는 실험실 품질 관리에서 추가적인 목적을 제공한다.다른 CBC 파라미터에 비해 시간이 지남에 따라 비교적 안정적이므로 MCV의 큰 변화는 잘못된 환자로부터 샘플을 추출했음을 나타낼 수 있다.[133]
낮은 RDW는 임상적인 의미는 없지만, 높은 RDW는 항산화증이라고 알려진 질환인 적혈구 크기의 증가하는 변화를 나타낸다.[118]Anisocytosis 철 결핍성 빈혈증과 빈혈 영양 anemias에 비타민 B12나 엽산 결핍 때문에, 지중해 빈혈을 가진 사람들의 결과에 근거한 정상 RDW.[118]을 미칠 수 있는 추가 단계를 효과적이며. 페리틴 시험 철 결핍증, 또는 헤모글로빈 당선자의 존재를 확인하기 위해 같은 빈혈, 조사하기 위해 취할 수 있습니다.roph탈라세미아나 겸상세포질환과 같은 혈색소병증을 진단하기 위한 [134]광석
백혈구
|
|
백혈구는 감염으로부터 방어하고 염증 반응에 관여한다.[136]백혈구증이라고 불리는 백혈구 수치가 높으면 감염, 염증, 생리학적 스트레스 상태 등에서 자주 발생한다.골수종, 림프종 장애 등 혈액세포의 비정상적인 생성을 수반하는 질병에 의해서도 발생할 수 있다.[137]백혈구 수 감소는 백혈구감소증이라고 불리며 감염의 위험을 증가시킬 수 있으며,[138] 화학요법이나 방사선 치료와 같은 치료법과 혈액 세포의 생성을 억제하는 많은 조건들에서 발생한다.[139]패혈증은 백혈구와 백혈구 모두와 관련이 있다.[140]총 백혈구 수는 대개 혈액의 마이크로리터당 세포(/μL) 또는 리터당 세포9 10개(× 109/L)로 보고된다.[4]
백혈구 차등에서는 서로 다른 종류의 백혈구를 식별하여 세어 본다.결과는 단위 부피당 백분율과 절대수로 보고된다.중성자, 림프구, 단세포, eosinophils, basophils 등 5가지 유형의 백혈구가 일반적으로 측정된다.[141]일부 기구는 미숙한 과립세포의 수를 보고하는데, 이는 중성미자의 전구체, 특히 프로밀세포, 골모세포, 변성세포로 구성된 분류다.[note 5][144]다른 셀 유형은 수동 차등에서 식별될 경우 보고된다.[145]
차이점 결과는 많은 의학적 상태를 진단하고 모니터링하는 데 유용하다.예를 들어 중성미자 수가 증가하면 세균감염, 염증, 골수성 질환과 관련이 있는 반면 감소하는 수(중성소모증)는 항암치료를 받고 있거나 특정 약물을 복용하고 있거나 골수에 영향을 주는 질병을 가지고 있는 개인에서 발생할 수 있다.[146][147][148][149]중성미자 역시 일부 선천성 질환에 의해 발생할 수 있으며 어린이들의 바이러스나 박테리아 감염 후에 일시적으로 발생할 수 있다.[150]심각한 중성미자와 감염의 임상적 징후를 가진 사람들은 잠재적으로 생명을 위협하는 질병을 예방하기 위해 항생제로 치료된다.[151]
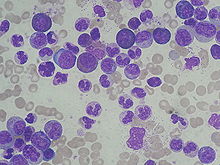
분절핵이 부족한 젊은 중성미자, 또는 미성숙 과립세포는 좌변위라고 불리며 패혈증과 일부 혈액 장애에서 발생하지만 임신에서는 정상이다.[152][153]높아진 림프구 수(림프구 증가증)바이러스 infection[6]과 만성 임파성 백혈병 같은 림프 증식성 질환,(단구 증가증)만성 염증성 국가들과 관련된[154] 높은 monocyte건,[155]과 호산성는 것은 종종 기생충 감염과 알레르기가 사기 행각에(호산구 증가증)가 증가 관련이 있다.전통과 난해한 규정들.[156]만성 골수성 백혈병이나 다혈성 베라와 같은 골수성 백혈병에서 바소필리아라고 불리는 기저귀의 수가 증가할 수 있다.[147]신소성 특징을 가진 발파 세포나 림프구와 같은 비정상적인 세포의 일부 유형은 혈액학적 악성 종양을 암시한다.[89][157]
혈소판

혈소판은 응고에 필수적인 역할을 한다.혈관벽이 손상되면 혈소판이 부상 부위의 노출된 표면에 달라붙어 틈새를 막는다.응고 캐스케이드가 동시에 활성화되면 피브린이 형성되어 혈소판 플러그를 보강하여 안정된 응고를 만들어 낸다.[158]혈소판 감소증이라고 알려진 혈소판 수치가 낮으면 심한 경우 출혈을 일으킬 수 있다.[159]항암화학요법이나 방사선요법 등 골수를 억제하는 치료를 받고 있거나, 헤파린 등 특정 약물을 복용하는 경우 면역체계가 혈소판을 파괴하도록 유도할 수 있는 사람에게서 발생할 수 있다.혈소판감소증은 급성 백혈병, 재생불량성 빈혈과 같은 많은 혈액 질환과 일부 자가면역 질환의 특징이다.[160][161]혈소판 개수가 극히 낮은 경우 혈소판 수혈을 실시할 수 있다.[162]혈소판 수치가 높다는 뜻의 혈소판 감소증은 철분 결핍증뿐 [163]아니라 염증이나 외상 상태에서도 발생할 수 있으며 혈소판 수치는 희귀한 혈액질환인 필수 혈소판 감소증 환자에서 예외적으로 높은 수준에 도달할 수 있다.[164][163]혈소판 수치는 혈액의 마이크로리터(/μL),[165] 마이크로리터당 10개3(× 103/μL), 리터당 10개9(× 109/L) 단위로 보고할 수 있다.[4]
평균 혈소판 부피(MPV)는 혈소판의 평균 크기를 펨톨리트 단위로 측정한다.혈소판감소증의 원인을 파악하는 데 도움이 될 수 있다. 혈소판의 파괴 증가를 보상하기 위해 혈류로 어린 혈소판이 방출될 때 MPV가 상승할 수 있는 반면, 골수 기능 장애로 인한 혈소판 생산 감소는 낮은 MPV를 초래할 수 있다.또한 MPV는 혈소판감소를 유발하는 선천성 질환을 구별하는데 유용하다.[118][166]미성숙 혈소판 분율(IPF) 또는 망연 혈소판 계수는 일부 분석기자에 의해 보고되며 혈액 내 미성숙 혈소판 수를 측정하여 혈소판 생성 속도에 대한 정보를 제공한다.[167]
기타 시험
레티쿨로시 수

레티쿨로세포는 미성숙 적혈구로서 성숙한 세포와는 달리 RNA를 포함하고 있다. 레티쿨로시세포 카운트는 완전한 혈액수의 일부로서 수행되기도 하는데, 보통은 사람의 빈혈의 원인을 조사하거나 치료에 대한 반응을 평가하기 위해 이루어진다.레티쿨로시세포 수가 많은 빈혈은 골수가 출혈이나 용혈에 대한 보상으로 더 높은 비율로 적혈구를 생산하고 있음을 나타낼 [74]수 있는 반면, 레티쿨로시세포 수가 적은 빈혈은 인체의 적혈구 생성 능력을 떨어뜨리는 질환을 가지고 있음을 나타낼 수 있다.[168]영양빈혈이 있는 사람에게 영양 보충제를 투여할 때, 망막세포의 수가 증가하면 적혈구를 더 많이 생산하여 신체가 치료에 반응하고 있다는 것을 나타낸다.[169]혈액학 분석기는 RNA에 결합하는 염료로 적혈구를 얼룩지게 하고 가벼운 산란이나 형광 분석 등을 통해 레티쿨로세포의 수를 측정하는 방식으로 레티쿨로세포 수를 측정한다.검사는 새 메틸렌 블루로 혈액을 얼룩지게 하고 현미경 아래 RNA가 들어 있는 적혈구 비율을 세어 수작업으로 할 수 있다.망막세포 수는 절대수 또는[168] 적혈구의 백분율로 표현된다.[170]
일부 기구는 각 망막세포에서 헤모글로빈의 평균 양을 측정하는데, 이는 표준 검사에 간섭하는 조건을 가진 사람들의 철분 결핍을 나타내는 지표로 연구되어 온 매개 변수다.[171]미성숙 레티쿨로피 분율(IRF)은 일부 분석기자가 생산한 또 다른 측정치로, 레티쿨로피세포의 성숙도를 정량화하는 것으로, 성숙도가 낮은 세포는 더 많은 RNA를 포함하고 있어 더 강한 형광신호를 생성한다.이 정보는 빈혈 치료나 골수 이식에 따른 항미 진단과 적혈구 생성을 평가하는 데 유용할 수 있다.[172]
핵 적혈구
골수에서 형성되는 동안, 그리고 태아의 간과 비장에서는 적혈구가 세포핵을 포함하고 있는데,[173] 적혈구는 대개 혈류에서 순환하는 성숙한 세포에 존재하지 않는다.[174]발견되었을 때, 특히 어린이와 성인의 핵 적색 세포의 존재는 출혈, 일부 암, 빈혈에 의해 야기될 수 있는 적혈구에 대한 수요가 증가했음을 나타낸다.[118]대부분의 분석기기는 이 세포들을 미분 세포수의 일부로 검출할 수 있다.많은 수의 핵 적색 세포는 잘못된 높은 백혈구 수를 유발할 수 있으며, 이것은 조정이 필요할 것이다.[175]
기타 매개변수
첨단 혈액학 분석기는 연구 연구에서 진단적 중요성을 보여주었지만 아직 광범위한 임상적 용도를 발견하지 못한 혈액 세포의 새로운 측정을 생성한다.[171]예를 들어, 일부 유형의 분석기는 각 백혈구 군집의 크기와 위치를 나타내는 좌표계를 생성한다.이러한 파라미터(단어 세포 집단 데이터)[176]는 혈액 장애, 세균 감염 및 말라리아에 대한 잠재적 지표로 연구되어 왔다.미엘로페록시디아제 얼룩을 사용하여 미분수를 생성하는 분석기는 백혈구의 효소 발현을 측정할 수 있는데, 이 효소는 다양한 질환에서 변형된다.[75]일부 기구는 평균 MCHC 값을 보고하는 것 외에 저혈색인 적혈구의 비율을 보고하거나,[171] 일부 유형의 용혈성 빈혈에서 발생하는 단편화된 적혈구(슈이스트모세포)의 카운트를 제공할 수 있다.[177]이러한 매개변수는 종종 특정 분석기 브랜드에 특정되기 때문에 실험실이 결과를 해석하고 비교하는 것은 어렵다.[171]
기준 범위
| 테스트 | 단위 | 성인 | 소아과 (4~7세) | 신생아 (0–1일) |
|---|---|---|---|---|
| WBC | × 109/L | 3.6–10.6 | 5.0–17.0 | 9.0–37.0 |
| RBC | × 1012/L |
| 4.00–5.20 | 4.10–6.10 |
| HGB | g/L |
| 102–152 | 165–215 |
| HCT | 신용장 |
| 0.36–0.46 | 0.48–0.68 |
| MCV | fL | 80–100 | 78–94 | 95–125 |
| MCH | pg | 26–34 | 23–31 | 30–42 |
| MCHC | g/L | 320–360 | 320–360 | 300–340 |
| RDW | % | 11.5–14.5 | 11.5–14.5 | 고상한[note 6] |
| PLT | × 109/L | 150–450 | 150–450 | 150–450 |
| 중성미자 | × 109/L | 1.7–7.5 | 1.5–11.0 | 3.7–30.0 |
| 림프구 | × 109/L | 1.0–3.2 | 1.5–11.1 | 1.6–14.1 |
| 단세포 | × 109/L | 0.1–1.3 | 0.1–1.9 | 0.1–4.4 |
| 어시노필스 | × 109/L | 0.0–0.3 | 0.0–0.7 | 0.0–1.5 |
| 바소필스 | × 109/L | 0.0–0.2 | 0.0–0.3 | 0.0–0.7 |
전체 혈액수는 겉보기에 건강한 사람들의 95%에서 발견된 결과를 나타내는 기준 범위와 출력을 비교함으로써 해석된다.[35]통계적 정규 분포를 바탕으로 테스트한 표본의 범위는 성별과 연령에 따라 다양하다.평균적으로 성인 암컷은 남성보다 헤모글로빈, 헤마토크리트, 적혈구 수치 값이 낮으며, 그 차이는 줄어들지만 폐경 후에도 여전히 존재한다.[179]
갓난아기의 피는 나이 든 아이와 많이 달라서 다시 어른의 피와 다르다.신생아의 헤모글로빈, 헤마토크리트, 적혈구 수치가 극히 높아 자궁 내 산소 농도가 낮으며, 태아 헤모글로빈의 비율이 높아 적혈구 내에서는 성숙한 형태의 헤모글로빈보다 조직에 산소를 전달하는 효과가 떨어진다.[180][181]MCV도 증가하고, 백혈구 수치는 중성미자의 우세함과 함께 높아진다.[180][182]적혈구 수 및 관련 값은 출생 직후부터 감소하기 시작하여 생후 약 2개월에 최저점에 도달하고 그 이후 증가하게 된다.[183][184]나이가 많은 유아와 어린이의 적혈구는 성인에 비해 MCH가 낮아 더 작다.소아 백혈구 차이에서 림프구가 중성미자보다 많은 반면 성인의 중성미자에서는 림프구가 우세하다.[180]
모집단 간의 다른 차이는 기준 범위에 영향을 미칠 수 있다. 예를 들어, 고도에 사는 사람들은 헤모글로빈, 헤마토크리트, RBC 결과가 더 높고, 아프리카 유산의 사람들은 평균적으로 백혈구 수치가 더 낮다.[185]CBC를 실행하는 데 사용되는 분석기의 유형은 기준 범위에도 영향을 미친다.따라서 기준 범위는 개별 실험실이 자체 환자 모집단과 장비에 기초하여 설정한다.[186][187]
제한 사항
일부 의학적 조건이나 혈액 샘플의 문제는 부정확한 결과를 초래할 수 있다.검체가 눈에 띄게 응고된 경우, 이는 혈소판 개수가 잘못 감소하고 다른 결과가 비정상적일 수 있기 때문에 시험하기에 부적합하다.[188][189]시료를 실온에서 몇 시간 동안 보관하면 혈장으로부터 수분을 흡수하면서 적혈구가 부풀어 오르기 때문에 MCV에 대한 잘못된 판독값을 얻을 수 있으며, 혈소판과 백혈구 차이 결과는 세포가 시간이 지남에 따라 저하되기 때문에 오래된 시료에서 부정확할 수 있다.[190][91]

혈장 내 빌리루빈 또는 지질 수치가 매우 높은 개인에서 추출한 샘플(각각 난해성 샘플 또는 지방성 샘플로 칭함)[191]은 헤모글로빈에 대한 잘못된 판독값을 나타낼 수 있는데, 이러한 물질들은 헤모글로빈 측정을 방해하는 샘플의 색상과 불투명도를 변경하기 때문이다.[192]이러한 효과는 혈장을 식염수로 대체함으로써 완화될 수 있다.[91]
일부 개인은 혈액이 CBC 시료를 채취하는 데 일반적으로 사용되는 항응고제인 EDTA가 함유된 관으로 빨려 들어갈 때 혈소판이 덩어리를 형성하도록 하는 항체를 생성하기도 한다.혈소판 덩어리는 자동 분석기에 의해 단일 혈소판으로 계산될 수 있으며, 이는 혈소판 수를 거짓으로 감소시키는 결과를 초래할 수 있다.이것은 구연산나트륨이나 헤파린과 같은 대체 항응고제를 사용하면 피할 수 있다.[193]
완전한 혈액수 결과에 영향을 미칠 수 있는 또 다른 항체 매개 질환은 적혈구 응고다.이 현상은 세포 표면에 묶인 항체 때문에 적혈구가 뭉치게 한다.[194]적혈구 골재는 분석기에 의해 단일 세포로 계수되어 적혈구 수와 헤마토크리트 수가 현저하게 감소하고 MCV와 MCHC가 현저하게 상승한다.[53]흔히 이러한 항체는 상온(이 경우 콜드 아글루틴이라고 함)에서만 활성하며, 시료를 37°C(99°F)로 가열하면 응고 효과를 역전시킬 수 있다.따뜻한 자가면역 용혈성 빈혈이 있는 사람들의 표본은 온난화를 해결하지 못하는 적혈구 응고 현상을 보일 수 있다.[130]
송풍과 림프종 세포는 수동 미분에서 확인할 수 있지만 현미경 검사로는 세포의 조혈 혈통을 신뢰성 있게 판단할 수 없다.이 정보는 종종 혈액암을 진단하는데 필요하다.비정상적인 세포가 식별된 후에는 흐름 세포계에 의한 면역항진술과 같은 추가 기술을 사용하여 세포에 대한 추가 정보를 제공하는 표지를 식별할 수 있다.[195][196]
역사

자동화된 세포 카운터가 도입되기 전에, 완전한 혈액 계수 테스트를 수동으로 수행했다: 백혈구와 적혈구, 혈소판은 현미경을 사용하여 계수되었다.[198]혈액 세포에 대한 현미경 관찰 결과를 최초로 발표한 사람은 안토니 판 루웬후크(Antonie van Leeuwenhoek)인데,[199] 그는 런던 왕립 협회(Royal Society of London)에 1674년 서한에서 적세포의 출현에 대해 보고했다.[200]Jan Swimmerdam은 몇 년 전에 적혈구를 설명했지만, 그 당시에는 그의 연구 결과를 발표하지 않았다.18세기와 19세기에 걸쳐 무채색 렌즈와 같은 현미경 기술의 향상은 백혈구와 혈소판을 무균 샘플로 셀 수 있게 했다.[201]
생리학자인 칼 비에로르트는 첫 번째 혈구 수치를 수행한 공로를 인정받았다.[8][202][203]1852년에 출판된 그의 기술은 조심스럽게 측정된 양의 혈액을 모세관 안에 흡인하여 달걀 흰자로 코팅된 현미경 슬라이드에 뿌리는 것을 포함한다.피가 마른 후, 그는 미끄럼틀에 있는 모든 세포들을 세어 보았다. 이 과정을 완료하는 데 3시간 이상이 걸릴 수 있었다.[204]루이찰스 맬러세즈가 1874년 도입한 혈모세포계는 혈액세포의 미세한 계수를 단순화했다.[205]맬라세즈의 혈구측정기는 납작해진 모세관(capillary tube)이 들어 있는 현미경 슬라이드로 구성되었다.희석된 혈액은 한쪽 끝에 부착된 고무관을 이용하여 모세관에 유입되었고, 현미경에 눈금 격자가 달린 아이피스를 부착하여 현미경학자가 혈액의 부피당 세포 수를 셀 수 있게 하였다.1877년 윌리엄 고워스는 계수 그리드가 내장된 혈모시계를 발명하여 각 현미경에 대해 특별히 보정된 안료를 생산할 필요가 없게 되었다.[206]

1870년대에 폴 에를리히는 다른 종류의 백혈구를 구별할 수 있고 적혈구 형태학이 검사될 수 있는 산성염료와 기본 염료를 결합하여 염색기술을 개발하였다.[201]드미트리 레오니도비치 로마노프스키는 1890년대에 이 기법을 개선하여, 에오신과 노화된 메틸렌 블루를 혼합하여 두 가지 얼룩을 단독으로 사용할 때는 존재하지 않는 광범위한 색조를 만들어냈다.이것이 로마노프스키 얼룩의 기초가 되었는데, 이 기술은 여전히 수동 검토를 위해 피를 얼룩지게 하는데 사용된다.[207]
헤모글로빈 측정의 첫 번째 기법은 19세기 후반에 고안되었고, 알려진 기준과 비교하여 희석된 혈액의 색상을 시각적으로 비교하였다.[203]분광측정법과 색소측정법을 이용하여 이 과정을 자동화하려는 시도는 헤모글로빈이 여러 가지 형태로 혈액 속에 존재한다는 사실, 즉 하나의 파장으로 측정할 수 없다는 사실 때문에 제한되었다.1920년에는 서로 다른 형태의 헤모글로빈을 하나의 안정적인 형태(사이안메트헤모글로빈 또는 헤미글로빈시아니드)로 변환하는 방법이 도입되어 헤모글로빈 수치를 자동으로 측정할 수 있게 되었다.시안메트헤모글로빈 방법은 헤모글로빈 측정의 기준법으로 남아 있으며, 여전히 많은 자동화된 혈액학 분석기에 사용되고 있다.[57][208][209]
맥스웰 윈트로브는 헤마토크리트 테스트의 발명으로 인정받고 있다.[66][210]1929년, 그는 튤레인 대학에서 적혈구 매개 변수의 정상 범위를 결정하기 위한 박사 프로젝트에 착수했고, 윈트로브 헤마토크리트라고 알려진 방법을 발명했다.헤마토크리트 측정이 앞서 문헌에 기술된 바 있지만, 윈트로브의 방식은 스케일이 내장된 정밀한 사양에 맞춰 대량 생산이 가능한 대형 관을 사용했다는 점에서 차이가 있었다.관내의 적혈구 분율은 원심분리 후 측정하여 헤마토크리트(Hymocrit)를 결정한다.헤마토크리트 값을 결정하는 재현 가능한 방법의 발명은 윈트로브가 적혈구 지수를 정의할 수 있게 했다.[203]
자동화된 세포 개수에 대한 연구는 20세기 초에 시작되었다.[209]1928년에 개발된 방법은 적혈구 수를 추정하기 위해 광도계에 의해 측정된 희석된 혈액 샘플을 통해 전달되는 빛의 양을 사용했지만, 이는 적혈구가 비정상적인 샘플의 경우 부정확한 것으로 판명되었다.[8]1930년대와 1940년대에 실패한 다른 시도들은 현미경에 부착된 광전자 탐지기를 포함했는데, 현미경은 스캔했을 때 세포를 계산하게 된다.[209]1940년대 후반, 히로시마와 나가사키의 폭격 이후 더 나은 적혈구 계수 방법이 필요하다는 동기에서 월리스 H. 쿨터는 광전지의 계수 기법을 개선하려고 시도했다.[211][note 7]그의 연구는 그의 형인 조셉 R의 도움을 받았다.콜터,[60] 시카고의 지하 실험실에 있어그 결과들은 광전 메서드를 사용하여, 그리고 1948년에, 종이는 적혈구 농도는 피의 전도도 관련된 읽은 후에, 월리스는 콜터 principle—the 이론는 구멍을 통과한 세포는 전도성 매체에 매달려 그것의 사이즈를 현재 proportional에 한 방울 생성을 고안했다 실망스러웠다.[211]
그해 10월 월리스는 그 원칙을 증명하기 위해 카운터를 만들었다.재정적인 제약 때문에, 그 조리개는 담배 꾸러미의 셀로판 조각을 통해 구멍을 내는 것으로 만들어졌다.[60][211]월러스는 1949년에 이 기술에 대한 특허를 출원했고, 1951년에 콜터 카운터의 개발에 자금을 대기 위해 해군 연구소에 신청했다.[211]월리스의 특허 출원은 1953년에 허가되었고, 검체 크기에 대한 정밀한 제어를 제공하기 위해 조리개 개선과 수은 측정기의 도입에 따라, 형제는 1958년에 콜터 일렉트로닉스 주식회사를 설립하여 그들의 상품들을 판매했다.콜터 카운터는 처음에는 적혈구 수를 세도록 설계되었지만, 나중에 수정함으로써 백혈구 수를 세는데 효과적이었다.[60]콜터 카운터는 의학 연구소에 의해 널리 채택되었다.[209]
다수의 셀 카운트를 동시에 생산할 수 있는 최초의 분석기는 1965년에 출시된 테크니콘 SMA 4A-7A이다.혈액샘플을 적혈구와 백혈구 계수용과 헤모글로빈 측정용 두 채널로 분할해 이를 달성했다.그러나 그 기구는 믿을 수 없고 유지하기가 어려웠다.1968년에 Coulter Model S 분석기가 출시되어 널리 이용되었다.테크니콘 기기와 유사하게 두 개의 서로 다른 반응실을 사용했는데, 그 중 하나는 적혈구 카운트에 사용되었고, 그 중 하나는 백혈구 카운트와 헤모글로빈 결정에 사용되었다.또한 모델 S는 임피던스 측정을 사용하여 평균 세포량을 결정하였고, 이를 통해 적혈구 지수와 헤마토크릿을 도출할 수 있었다.자동 혈소판 개수는 1970년에 테크니콘의 헤몰로그-8 기기와 함께 도입되었고 1980년에 콜터의 S Plus 시리즈 분석기에 의해 채택되었다.[212]
기본 세포 계산이 자동화된 후에도 백혈구 차이는 과제로 남았다.1970년대 내내 연구원들은 차등 계산 자동화를 위한 두 가지 방법인 디지털 이미지 처리와 흐름 사이토메트릭을 탐구했다.1950년대와 60년대에 개발된 기술을 사용하여 Pap smear의 판독을 자동화함으로써, 이미지 처리 분석기의 여러 모델이 생산되었다.[213]이 기구들은 세포핵을 찾기 위해 얼룩진 혈액을 스캔한 다음, 밀도측정법을 통해 분석하기 위해 세포의 고해상도 스냅숏을 찍을 것이다.[214]그것들은 값비싸고 느리고 실험실에서 작업량을 줄이는 데 거의 도움이 되지 않았다. 왜냐하면 그들은 여전히 혈흔을 준비하고 얼룩을 지워야 하기 때문이다.[215][216] 그래서 흐름 세포측정기 기반 시스템이 더 인기를 끌게 되었고 1990년경에는 미국이나 서유럽에서 상업적으로 사용할 수 있는 디지털 이미지 분석기가 없었다.[217]이러한 기법들은 2000년대에 인공 신경망을 이용한 보다 진보된 영상 분석 플랫폼이 도입되면서 부활을 누렸다.[218][219][220]
초기 흐름 세포측정기기는 특정 파장의 세포에 빛의 빔을 쏘고 그 결과 흡광도, 형광도 또는 빛 산란도를 측정하여 세포의 특징에 대한 정보를 수집하고 DNA와 같은 세포 내용을 정량화할 수 있게 했다.[221]그러한 도구 중 하나인 Louis Kamentsky가 1965년에 자궁경부 세포학을 자동화하기 위해 개발한 Rapid Cell Spectrophotometer는 세포 화학적 얼룩 기술을 사용하여 혈구 산란을 발생시킬 수 있었다.Rapid Cell Spectrophotometer의 Staining 시스템 개발을 도왔던 Leonard Ornstein과 그의 동료들은 후에 최초의 상업적 흐름 세포 세포 차등 분석기인 Hemalog D를 만들었다.[222][223]1974년에 도입된 이 분석기는 보통 비정형 림프구나 발파세포로 구성된 분류인 "큰 정체불명의 세포" 외에 5가지 정상 백혈구 유형을 식별하기 위해 빛 산란, 흡광도, 세포 얼룩을 사용했다.[224][225]Hemalog D는 한 번의 실행으로 10,000개의 셀을 셀 수 있으며, 이는 수동 차이에 비해 현저한 개선이다.[223][226]1981년 테크니콘은 헤말로그 D를 헤말로그-8 분석기와 결합하여 최초의 완전한 혈액수와 미분 분석기인 테크니콘 H6000을 생산하였다.이 분석기는 조작이 노동집약적이어서 혈액학 실험실에서 인기가 없었지만, 1980년대 후반부터 1990년대 초반까지 유사한 시스템이 시스멕스, 애보트, 로슈, 벡만 쿨터 등 다른 제조사에 의해 널리 생산되었다.[227]
주석
- ^ 흔히 그렇게 일컬어지지만 혈소판은 엄밀히 말하면 세포가 아니다. 혈소판은 골수에 있는 메가카리세포의 세포질에서 형성된 세포 조각이다.[6]
- ^ 기준 범위를 구성하는 데 사용되는 데이터는 대개 "정상적인" 과목에서 도출되지만, 이들 개인이 무증상 질환을 가질 가능성도 있다.[34]
- ^ 가장 넓은 의미에서 flow cytometry라는 용어는 유체 흐름에서 개별 세포의 성질을 측정하는 것을 말하며,[49][50] 이 점에서 모든 혈액학 분석기(디지털 이미지 처리를 사용하는 것을 제외)는 flow cytometer이다.그러나 이 용어는 일반적으로 빛 산란 및 형광 방법, 특히 세포 표면 표지에 결합하는 라벨링 항체를 사용한 세포 식별(면역헤노티핑)과 관련된 용어로 사용된다.[49][51]
- ^ 항상 그렇지는 않다.예를 들어, 탈라세아의 일부 유형에서는 적혈구가 매우 작기 때문에 적혈구 수치가 낮거나 정상적인 헤모글로빈과 함께 발생한다.[123][124]MCV를 RBC 카운트에 비교한 멘처지수는 철분결핍 빈혈과 탈라세미아를 구분하는 데 활용할 수 있다.[125]
- ^ 자동화된 계측기는 이 세 가지 유형의 세포를 "불멸성 과립세포" 분류에 따라 함께 분류하지만,[142] 그것들은 수동 미분류에 별도로 계산된다.[143]
- ^ RDW는 출생시 매우 높아지며 생후 약 6개월이 될 때까지 점차 감소한다.[178]
- ^ 미국 해군 함정에 사용된 페인트의 입자를 연구하기 위해 월리스가 콜터 카운터를 발명했다는 사실이 알려진 사실, 다른 진술들은 그것이 원래 플랑크톤을 세기 위해 제2차 세계대전 중에 고안되었다고 주장한다.그러나 월러스는 해군에서 일한 적이 없으며, 이 장치에 대한 그의 초기 저술은 그것이 처음으로 혈액을 분석하는 데 사용되었다고 말한다.그림 이야기는 결국 월리스 H. 콜터 재단이 제작한 문서에서 철회되었다.[211]
참조
인용구
- ^ Tefferi, A; Hanson, CA; Inwards, DJ (2005). "How to interpret and pursue an abnormal complete blood cell count in adults". Mayo Clinic Proceedings. 80 (7): 923–936. doi:10.4065/80.7.923. ISSN 0025-6196. PMC 7127472. PMID 16212155.
- ^ a b HealthDirect (August 2018). "Full blood count". HealthDirect.gov.au. Archived from the original on 2 April 2019. Retrieved 8 September 2020.
- ^ "Blood tests: Chronic lymphocytic leukaemia (CLL)". Cancer Research UK. 18 September 2020. Archived from the original on 23 October 2020. Retrieved 23 October 2020.
- ^ a b c d e f American Association for Clinical Chemistry (12 August 2020). "Complete Blood Count (CBC)". Lab Tests Online. Archived from the original on 18 August 2020. Retrieved 8 September 2020.
- ^ a b c Smock, KJ. Greer, JP et al., ed.(2018), sec. "자동 혈액학으로 인한 장점과 오류 원인".
- ^ a b 터건, ML (2016년)페이지 309.
- ^ 해크닝, DM(2009)2-3 페이지
- ^ a b c Green, R; Wachsmann-Hogiu, S (2015). "Development, history, and future of automated cell counters". Clinics in Laboratory Medicine. 35 (1): 1–10. doi:10.1016/j.cll.2014.11.003. ISSN 0272-2712. PMID 25676368.
- ^ a b Keohane, E et al. (2015).244 페이지
- ^ Leach, M (2014). "Interpretation of the full blood count in systemic disease – a guide for the physician". The Journal of the Royal College of Physicians of Edinburgh. 44 (1): 36–41. doi:10.4997/JRCPE.2014.109. ISSN 1478-2715. PMID 24995446.
- ^ 마샬, WJ 외 (2014년)페이지 497.
- ^ a b c 반 리우웬, AM; 블라드, ML (2019)377 페이지
- ^ 르완드로스키, K 등 (2016년)페이지 96.
- ^ American Association of Blood Banks (24 April 2014). "Five Things Physicians and Patients Should Question". Choosing Wisely: an initiative of the ABIM Foundation. American Association of Blood Banks. Archived from the original on 24 September 2014. Retrieved 12 July 2020.
- ^ a b 르완드로스키, K 등 (2016년)페이지 97.
- ^ 하르트만, CJ, 카부시, LR (2017)4-5 페이지
- ^ Dewan, M (2016). "Reducing unnecessary postoperative complete blood count testing in the pediatric intensive care unit". The Permanente Journal. 21: 16–051. doi:10.7812/TPP/16-051. ISSN 1552-5767. PMC 5283785. PMID 28241909.
- ^ 벽, R 외 (2017). 페이지 130.
- ^ 벽, R 외 (2017). 페이지 219.
- ^ 벽, R 외 (2017). 페이지 199.
- ^ 벽, R 외 (2017). 페이지 1464.
- ^ 무어, EE 외 (2017). 페이지 162.
- ^ Lewis, SL 외 (2015).페이지 280.
- ^ Wiciński, M; Węclewicz, MM (2018). "Clozapine-induced agranulocytosis/granulocytopenia". Current Opinion in Hematology. 25 (1): 22–28. doi:10.1097/MOH.0000000000000391. ISSN 1065-6251. PMID 28984748. S2CID 20375973.
- ^ Patemi, SH; Clayton, PJ. (2016). 페이지 666.
- ^ 둘리, EK, 링글러, RL. (2012)20-21 페이지
- ^ Keohane, E et al. (2015).페이지 834–835.
- ^ 샤퍼마이어, RW 외(2018).페이지 467–468.
- ^ Smock, Greer의 KJ. 1장 JP 외, ed.(2018), sec. "소개서"
- ^ a b Kaushansky, K 등 (2015). 페이지 11.
- ^ Kaushansky, K 등(2015년).페이지 43.
- ^ Kaushansky, K 등(2015년).42-44 페이지
- ^ 맥퍼슨, RA; 핀커스, MR (2017). 페이지 574.
- ^ 베인, BJ 외 (2017). 페이지 8.
- ^ a b 베인, BJ 외 (2017). 페이지 10.
- ^ 베인, BJ(2015).213 페이지
- ^ Keohane, E et al. (2015).245 페이지
- ^ a b 르완드로스키, K 등 (2016년)96-97 페이지
- ^ "Routine Preoperative Tests for Elective Surgery (NG45)". National Institute for Health and Care Excellence. 5 April 2016. Archived from the original on 28 July 2020. Retrieved 8 September 2020.
- ^ 커크햄, KR 외 (2016)805 페이지
- ^ Smock, Greer의 KJ. 1장 JP 외, ed.(2018), sec. "사양 컬렉션".
- ^ Keohane, E et al. (2015).페이지 28.
- ^ 베인, BJ 외 (2017). 페이지 1.
- ^ Smock, KJ. Greer, JP et al., ed. (2018), sec. "Cell counts", "compacked red cells (hematocrit)", "Leukocyte differents".
- ^ a b c d 베인, BJ 외 (2017).551-555 페이지
- ^ 베인, BJ(2015).페이지 29.
- ^ Dasgupta, A; Sepulveda, JL (2013).305 페이지
- ^ a b D’Souza, C; Briggs, C; Machin, SJ (2015). "Platelets: the few, the young and the active". Clinics in Laboratory Medicine. 35 (1): 123–131. doi:10.1016/j.cll.2014.11.002. ISSN 0272-2712. PMID 25676376.
- ^ a b c Kotke-Marchant, K; Davis, B(2012).8페이지
- ^ HM(2003)의 샤피로.페이지 1
- ^ Bakke, AC (2001). "The principles of flow cytometry". Laboratory Medicine. 32 (4): 207–211. doi:10.1309/2H43-5EC2-K22U-YC6T. ISSN 1943-7730.
- ^ Kaushansky, K 등 (2015). 페이지 12.
- ^ a b 베인, BJ 외 (2017).32~33 페이지
- ^ 맥퍼슨, RA; 핀커스, MR (2017).페이지 44.
- ^ 베인, BJ(2015).29~30쪽
- ^ Whitehead, RD; Mei, Z; Mapango, C; Jefferds, MED (August 2019). "Methods and analyzers for hemoglobin measurement in clinical laboratories and field settings". Annals of the New York Academy of Sciences. 1450 (1): 147–171. Bibcode:2019NYASA1450..147W. doi:10.1111/nyas.14124. PMC 6709845. PMID 31162693.
- ^ a b 스팍, KJ 그리어 1장 JP 외 에드(2018), sec. "헤모글로빈 농도"
- ^ a b Keohane, E et al. (2015).페이지 208.
- ^ 베인, BJ(2015).30~31페이지
- ^ a b c d Graham, MD (2003). "The Coulter principle: foundation of an industry". Journal of the Association for Laboratory Automation. 8 (6): 72–81. doi:10.1016/S1535-5535(03)00023-6. ISSN 1535-5535.
- ^ Keohane, E et al. (2015).208–190 페이지
- ^ a b 베인, BJ 외 (2017). 페이지 32.
- ^ Keohane, E et al. (2015).210-211 페이지
- ^ Keohane, E et al. (2015).페이지 210.
- ^ Kotke-Marchant, K; Davis, B(2012). 페이지 27.
- ^ a b c d e Smock, KJ. Greer, JP 외, ed.(2018), sec. "포장된 적색 세포의 볼륨(hematocrit)"
- ^ Smock, KJ. Greer JP 외 연구진, Ed. (2018) 제1장 "근육 부피", "근육 헤모글로빈 농도", "근육 헤모글로빈 농도", "적세포 분포 폭"
- ^ Keohane, E et al. (2015).페이지 2
- ^ Keohane, E et al. (2015).페이지 209.
- ^ a b c 베인, BJ 외 (2017). 페이지 37.
- ^ 에르네스, BM, Menschikowki, M. (2015)페이지 3
- ^ a b c Smock, KJ. Greer JP 외, ed.(2018), sec. "유전세포 미분"
- ^ 내임, F 등(2009).페이지 210.
- ^ a b 터건, ML (2016년)페이지 318.
- ^ a b 베인, BJ 외 (2017). 페이지 39.
- ^ a b Smock, KJ. Greer, JP et al., ed.(2018), sec. "소개"; "셀 카운트"
- ^ a b c d Gulati, G; Song, J; Dulau Florea, A; Gong, J (2013). "Purpose and criteria for blood smear scan, blood smear examination, and blood smear review". Annals of Laboratory Medicine. 33 (1): 1–7. doi:10.3343/alm.2013.33.1.1. ISSN 2234-3806. PMC 3535191. PMID 23301216.
- ^ a b Mooney, C; Byrne, M; Kapuya, P; Pentony, L; De la Salle, B; Cambridge, T; Foley, D (2019). "Point of care testing in general haematology". British Journal of Haematology. 187 (3): 296–306. doi:10.1111/bjh.16208. ISSN 0007-1048. PMID 31578729.
- ^ a b Sireci, AN (2015). "Hematology testing in urgent care and resource-poor settings: an overview of point of care and satellite testing". Clinics in Laboratory Medicine. 35 (1): 197–207. doi:10.1016/j.cll.2014.10.009. ISSN 0272-2712. PMID 25676380.
- ^ 베인, BJ 외 (2017).페이지 43.
- ^ Keohane, E et al. (2015).225 페이지
- ^ 베인, BJ(2015).9-11 페이지
- ^ 파머, L 외 (2015).288–289 페이지
- ^ 터건, ML (2016년)페이지 325–326.
- ^ 베인, BJ(2015).페이지 98.
- ^ 베인, BJ (2015). 페이지 154.
- ^ 왕, SA; 하세르지안, RP(2018). 페이지 10.
- ^ a b 터건, ML (2016년)페이지 329.
- ^ a b D'Onofrio, G; Zini, G. (2014). 페이지 289.
- ^ 파머, L 외 (2015).페이지 296–297
- ^ a b c Keohane, E et al. (2015).226 페이지
- ^ a b Smock, Greer, JP 외, Ed.(2018), sec. "Cell counts"
- ^ Keohane, E 외 (2017) 페이지 189.
- ^ 베인, BJ(2015).22-23 페이지
- ^ Keohane, E et al. (2017).190-191 페이지
- ^ 베인, BJ 외 (2017).19-22 페이지
- ^ 베인, BJ 외 (2017).548-552 페이지
- ^ Keohane, E et al. (2015).페이지 46.
- ^ a b c Vis, JY; Huisman, A (2016). "Verification and quality control of routine hematology analyzers". International Journal of Laboratory Hematology. 38: 100–109. doi:10.1111/ijlh.12503. ISSN 1751-5521. PMID 27161194.
- ^ a b Kotke-Marchant, K; Davis, B(2012).697-698 페이지
- ^ Pai, S; Frater, JL (2019). "Quality management and accreditation in laboratory hematology: Perspectives from India". International Journal of Laboratory Hematology. 41 (S1): 177–183. doi:10.1111/ijlh.13017. ISSN 1751-5521. PMID 31069974.
- ^ 그리어, JP(2008).4 페이지
- ^ Kotke-Marchant, K; Davis, B(2012).페이지 438.
- ^ 베인, BJ 외 (2017).페이지 539-540.
- ^ Favaloro, EJ; Jennings, I; Olson, J; Van Cott, EM; Bonar, R; Gosselin, R; Meijer, P (2018). "Towards harmonization of external quality assessment/proficiency testing in hemostasis". Clinical Chemistry and Laboratory Medicine (CCLM). 57 (1): 115–126. doi:10.1515/cclm-2018-0077. ISSN 1437-4331. PMID 29668440. S2CID 4978828.
- ^ 베인, BJ 외 (2017). 페이지 551.
- ^ Keohane, E et al. (2015).4-5 페이지
- ^ 블랜, A; 아흐메드, N (2014). 페이지 106.
- ^ 터건, ML (2016). 페이지 293.
- ^ 베인, BJ 외 (2017).33-34 페이지
- ^ 터건, ML (2016년)319-320 페이지
- ^ Brereton, M; McCafferty, R; Marsden, K; Kawai, Y; Etzell, J; Ermens, A (2016). "Recommendation for standardization of haematology reporting units used in the extended blood count". International Journal of Laboratory Hematology. 38 (5): 472–482. doi:10.1111/ijlh.12563. ISSN 1751-5521. PMID 27565952.
- ^ Keohane, E 외 (2015). 페이지 195.
- ^ a b 베인, BJ(2015).22 페이지
- ^ a b c d Keohane, E et al. (2015. 페이지 196).
- ^ 슈마이어, AH; 레자로스, HM(2012). 페이지 25.
- ^ a b 베인, BJ(2015).73-75 페이지
- ^ a b c d e May, JE; Marques, MB; Reddy, VVB; Gangaraju, R (2019). "Three neglected numbers in the CBC: The RDW, MPV, and NRBC count". Cleveland Clinic Journal of Medicine. 86 (3): 167–172. doi:10.3949/ccjm.86a.18072. ISSN 0891-1150. PMID 30849034.
- ^ Keohane, E et al. (2015).285 페이지
- ^ Keohane, E et al. (2015).286 페이지
- ^ Kaushansky, K 등 (2015). 페이지 503.
- ^ Vieth, JT; Lane, DR(2014).11-12페이지
- ^ 베인, BJ(2015).297 페이지
- ^ DiGregorio, RV 등(2014년).페이지 491-493
- ^ 아이작스, C 외 (2017). 페이지 331.
- ^ 베인, BJ(2015).232 페이지
- ^ 맥퍼슨, RA; 핀커스, MR (2017).600-601 페이지
- ^ a b Smock, Greer, JP 외, ed.(2018), sec. "Mean orcular hemoglobin 농도".
- ^ Keohane, E 외 (2015). 197 페이지.
- ^ a b Kotke-Marchant, K; Davis, B(2012).88 페이지
- ^ 베인, BJ (2015). 페이지 193.
- ^ 베인, BJ 외 (2017).501-502 페이지
- ^ 씨슬라, B(2018). 페이지 26.
- ^ 파월, DJ, 아체베, MO. (2016)530 페이지, 537–539.
- ^ 해크닝, DM(2009)페이지 380.
- ^ Pagana, TJ 등(2014년).992 페이지
- ^ 벽, R 등 (2017).1480–1481 페이지
- ^ Territo, M (January 2020). "Overview of White Blood Cell Disorders". Merck Manuals Consumer Version. Archived from the original on 23 June 2020. Retrieved 8 September 2020.
- ^ Pagana, TJ 등(2014년).991 페이지
- ^ 맥컬로, RJ; 오팔, SM. 오로펠로의 42장 JM 외, 에드. (2016), 초. "백혈구 수 및 차등"
- ^ American Association for Clinical Chemistry (29 July 2020). "WBC Differential". Lab Tests Online. Archived from the original on 19 August 2020. Retrieved 8 September 2020.
- ^ 왕, SA; 하세르지안, RP(2018). 페이지 8.
- ^ 파머, L 외 (2015).294-295 페이지
- ^ Chabot-Richards, DS; George, TI(2015). 페이지 10.
- ^ 파머, L 외 (2015).294 페이지
- ^ 터건, ML (2016년)306 페이지
- ^ a b Kaushansky, K 등(2015년).페이지 44.
- ^ 호프만, EJ 외 연구진(2013). 페이지 644.
- ^ 포르위트, A 외(2011년).247–252 페이지
- ^ 벽, R 외 (2017). 페이지 1483.
- ^ 벽, R 등 (2017).1497-1498 페이지
- ^ 베인, BJ(2015).페이지 99.
- ^ 베인, BJ 외 (2017). 페이지 85.
- ^ 베인, BJ 외 (2017).페이지 498.
- ^ 베인, BJ(2015).243 페이지
- ^ 포르위트, A 외(2011. 페이지 256).
- ^ 파머, L 외 (2015).298 페이지
- ^ 터건, ML (2016년)358-360 페이지
- ^ Kaushansky, K 등 (2015). 페이지 1993.
- ^ 터건, ML (2016년)315 페이지
- ^ 벽, R 등 (2017).1486–1488 페이지
- ^ Kaufman, RM; Djulbegovic, B; Gernsheimer, T; Kleinman, S; Tinmouth, A T.; Capocelli, KE; et al. (2015). "Platelet transfusion: a clinical practice guideline from the AABB". Annals of Internal Medicine. 162 (3): 205–213. doi:10.7326/M14-1589. ISSN 0003-4819. PMID 25383671.
- ^ a b Keohane, E et al. (2015).4 페이지
- ^ 벽, R 외 (2017). 페이지 1489.
- ^ Gersten, T (25 August 2020). "Platelet count: MedlinePlus Medical Encyclopedia". MedlinePlus. United States National Library of Medicine. Archived from the original on 9 September 2020. Retrieved 9 September 2020.
- ^ 왕, SA; 하세르지안, RP(2018). 7페이지.
- ^ Kaushansky, K 등(2015년).18~19페이지
- ^ a b Kaushansky, K 등 (2015). 페이지 14.
- ^ 터건, ML (2016년)318-319 페이지
- ^ 터건, ML (2016년)페이지 319.
- ^ a b c d Kaushansky, K 등 (2015). 페이지 16.
- ^ 베인, BJ 외 (2017).42-43 페이지
- ^ 해크닝, DM(2009)8-10 페이지
- ^ Constantino, B; Cogionis, B (2000). "Nucleated RBCs – significance in the peripheral blood film". Laboratory Medicine. 31 (4): 223–229. doi:10.1309/D70F-HCC1-XX1T-4ETE.
- ^ 잔데키, M 등(2007).24-25 페이지
- ^ Virk, H; Varma, N; Naseem, S; Bihana, I; Sukhachev, D (2019). "Utility of cell population data (VCS parameters) as a rapid screening tool for acute myeloid leukemia (AML) in resource-constrained laboratories". Journal of Clinical Laboratory Analysis. 33 (2): e22679. doi:10.1002/jcla.22679. ISSN 0887-8013. PMC 6818587. PMID 30267430.
- ^ 베인, BJ(2015).페이지 90.
- ^ a b Keohane, E et al. (2015).앞물.
- ^ 베인, BJ(2015).211-213 페이지
- ^ a b c 베인, BJ (2015). 페이지 143.
- ^ Lanzkowsky, P 등 (2016). 페이지 197.
- ^ Kaushansky, K 등(2015년).페이지 99.
- ^ 카우산스키, K 외 (2015). 페이지 103.
- ^ 베인, BJ(2015).페이지 220.
- ^ 베인, BJ(2015).214 페이지
- ^ 베인, BJ 외 (2017).8-10 페이지
- ^ 파머, L 외 (2015).296 페이지
- ^ 베인, BJ (2015). 페이지 195.
- ^ Kotke-Marchant, K; Davis, B(2012). 페이지 67.
- ^ 베인, BJ (2015). 페이지 194.
- ^ 터건, ML (2016년)페이지 91.
- ^ Kotke-Marchant, K; Davis, B(2012) 페이지 80, 86–87.
- ^ 베인, BJ(2015).196-180쪽
- ^ 로닥, BF, 카, JH(2013). 페이지 109.
- ^ 왕, SA; 하세르지안, RP(2018).페이지 9.
- ^ Kotke-Marchant, K; Davis, B(2012).페이지 19-20
- ^ Science Museum, London. "Haemoglobinometer, United Kingdom, 1850–1950". Wellcome Collection. Archived from the original on 29 March 2020. Retrieved 29 March 2020.
- ^ Keohane, E et al. (2015).1-4 페이지
- ^ Kotke-Marchant, K; Davis, B. (2012). 페이지 1.
- ^ 윈트로브, MM(1985) 페이지 10.
- ^ a b Kotke-Marchant, K; Davis, B.(2012).3-4 페이지
- ^ Verso, ML (May 1962). "The evolution of blood counting techniques". Read at a Meeting of the Section of the History of Medicine, First Australian Medical Congress. 8 (2): 149–158. doi:10.1017/s0025727300029392. PMC 1033366. PMID 14139094.
- ^ a b c Means, RT (2011). "It all started in New Orleans: Wintrobe, the hematocrit and the definition of normal". The American Journal of the Medical Sciences. 341 (1): 64–65. doi:10.1097/MAJ.0b013e3181e2eb09. ISSN 0002-9629. PMID 21191263.
- ^ 데이비스, JD(1995) 페이지 167.
- ^ Kotke-Marchant, K; Davis, B(2012).4 페이지
- ^ 데이비스, JD(1995)168–168 페이지
- ^ Bezrukov, AV (2017). "Romanowsky staining, the Romanowsky effect and thoughts on the question of scientific priority". Biotechnic & Histochemistry. 92 (1): 29–35. doi:10.1080/10520295.2016.1250285. ISSN 1052-0295. PMID 28098484. S2CID 37401579.
- ^ Keohane, E 외 (2015). 페이지 134.
- ^ a b c d Kotke-Marchant, K; Davis, B(2012). 페이지 5.
- ^ Robinson, JP (2013). "Wallace H. Coulter: decades of invention and discovery". Cytometry Part A. 83A (5): 424–438. doi:10.1002/cyto.a.22296. ISSN 1552-4922. PMID 23596093.
- ^ a b c d e Graham, MD (2013). "The Coulter principle: Imaginary origins". Cytometry Part A. 83 (12): 1057–1061. doi:10.1002/cyto.a.22398. ISSN 1552-4922. PMC 4237176. PMID 24151220.
- ^ Kotke-Marchant, K; Davis, B(2012). 페이지 6.
- ^ Groner, W (1995)12-14 페이지
- ^ Lewis, SM (1981). "Automated differential leucocyte counting: Present status and future trends". Blut. 43 (1): 1–6. doi:10.1007/BF00319925. ISSN 0006-5242. PMID 7260399. S2CID 31055044.
- ^ 다 코스타, L (2015). 페이지 5
- ^ Groner, W (1995)12-15 페이지
- ^ Bentley, SA (1990). "Automated differential white cell counts: a critical appraisal". Baillière's Clinical Haematology. 3 (4): 851–869. doi:10.1016/S0950-3536(05)80138-6. ISSN 0950-3536. PMID 2271793.
- ^ Kratz, A; Lee, S; Zini, G; Riedl, JA; Hur, M; Machin, S (2019). "Digital morphology analyzers in hematology: ICSH review and recommendations". International Journal of Laboratory Hematology. 41 (4): 437–447. doi:10.1111/ijlh.13042. ISSN 1751-5521. PMID 31046197.
- ^ 다 코스타, L(2015년).5-6페이지
- ^ 맥캔, SR (2016). 193 페이지.
- ^ 멜라메드, M(2001)5-6페이지
- ^ HM(2003)의 샤피로.84-85 페이지
- ^ a b 멜라메드, M. (2001)8페이지
- ^ 피콧, J 외 (2012). 페이지 110.
- ^ Mansberg, HP; Saunders, AM; Groner, W (1974). "The Hemalog D white cell differential system". Journal of Histochemistry & Cytochemistry. 22 (7): 711–724. doi:10.1177/22.7.711. ISSN 0022-1554. PMID 4137312.
- ^ 피에르, RV(2002년).281 페이지
- ^ Kotke-Marchant, K; Davis, B(2012).8~9페이지
일반 참고 문헌 목록
- Arneth, BM; Menschikowki, M (2015). "Technology and new fluorescence flow cytometry parameters in hematological analyzers". Journal of Clinical Laboratory Analysis. 29 (3): 175–183. doi:10.1002/jcla.21747. ISSN 0887-8013. PMC 6807107. PMID 24797912.
- Bain, BJ (2015). Blood Cells: A Practical Guide (5 ed.). John Wiley & Sons. ISBN 978-1-118-81733-9.
- Bain, BJ; Bates, I; Laffan, MA (2017). Dacie and Lewis Practical Haematology (12 ed.). Elsevier Health Sciences. ISBN 978-0-7020-6925-3.
- Blann, A; Ahmed, N (2014). Blood Science (1 ed.). Institute of Biomedical Science. p. 106. ISBN 978-1-118-35146-8.
- Chabot-Richards, DS; George, TI (2015). "White blood cell counts". Clinics in Laboratory Medicine. 35 (1): 11–24. doi:10.1016/j.cll.2014.10.007. ISSN 0272-2712. PMID 25676369.
- Ciesla, B (2018). Hematology in Practice (3 ed.). F. A. Davis Company. ISBN 978-0-8036-6825-6.
- Da Costa, L (2015). "Digital image analysis of blood cells". Clinics in Laboratory Medicine. 35 (1): 105–122. doi:10.1016/j.cll.2014.10.005. ISSN 0272-2712. PMID 25676375.
- Dasgupta, A; Sepulveda, JL (2013). Accurate Results in the Clinical Laboratory: A Guide to Error Detection and Correction. Elsevier. ISBN 978-0-12-415858-0.
- Davis, JD (1995). "The evolution of the progressive-era hemocytometer". Caduceus: A Humanities Journal for Medicine and the Health Sciences. 11 (3): 164–183. PMID 8680947.
- DiGregorio, RV; Green-Hernandez, C; Holzemer, SP (2014). Primary Care: An Interprofessional Perspective (2 ed.). Springer Publishing Company. ISBN 978-0-8261-7148-1.
- Dooley, EK; Ringler, RL (2012). "Prenatal care: touching the future". Primary Care: Clinics in Office Practice. 39 (1): 17–37. doi:10.1016/j.pop.2011.11.002. ISSN 0095-4543. PMID 22309579.
- Fatemi, SH; Clayton, PJ (2016). The Medical Basis of Psychiatry (4 ed.). Springer. ISBN 978-1-4939-2528-5.
- Greer, JP (2008). Wintrobe's Clinical Hematology (12 ed.). Lippincott Williams & Wilkins. ISBN 978-0-7817-6507-7.
- Greer, JP; Arber, DA; Glader, BE; List, AF; Means, RM; Rodgers, GM (2018). Wintrobe's Clinical Hematology (14 ed.). Wolters Kluwer Health. ISBN 978-1-4963-6713-6.
- Groner, W (1995). Practical Guide to Modern Hematology Analyzers. Wiley. ISBN 978-0-471-95712-6.
- Harmening, D (2009). Clinical Hematology and Fundamentals of Hemostasis (5 ed.). F. A. Davis Company. ISBN 978-0-8036-1732-2.
- Hartman, CJ; Kavoussi, LR (2017). Handbook of Surgical Technique: A True Surgeon's Guide to Navigating the Operating Room. Elsevier Health Sciences. ISBN 978-0-323-51222-0.
- Hoffman, R; Benz, Jr., EJ; Silberstein, LE; Heslop, H; Anastasi, J; Weitz, J (2013). Hematology: Basic Principles and Practice (6 ed.). Elsevier Health Sciences. ISBN 978-1-4377-2928-3.
- Isaacs, C; Agarwala, S; Cheson, B (2017). Hoffman and Abeloff's Hematology-Oncology Review (1 ed.). Elsevier Health Sciences. ISBN 978-0-323-44318-0.
- Kaushansky, K; Lichtman, MA; Prchal, J; Levi, MM; Press, OW; Burns, LJ; Caligiuri, M (2015). Williams Hematology (9 ed.). McGraw-Hill Education. ISBN 978-0-07-183301-1.
- Keohane, E; Smith, L; Walenga, J (2015). Rodak's Hematology: Clinical Principles and Applications (5 ed.). Elsevier Health Sciences. ISBN 978-0-323-23906-6.
- Kirkham, KR; Wijeysundera, DN; Pendrith, C; Ng, R; Tu, JV; Boozary, AS; et al. (2016). "Preoperative laboratory investigations". Anesthesiology. 124 (4): 804–814. doi:10.1097/ALN.0000000000001013. ISSN 0003-3022. PMID 26825151. S2CID 35916964.
- Kottke-Marchant, K; Davis, B (2012). Laboratory Hematology Practice (1 ed.). John Wiley & Sons. ISBN 978-1-4443-9857-1.
- Lanzkowsky, P; Lipton, JM; Fish, JD (2016). Lanzkowsky's Manual of Pediatric Hematology and Oncology. Elsevier Science. ISBN 978-0-12-801674-9.
- Lewandrowski, K; Rudolf, J (2016). "Utilization Management in the Routine Hematology Laboratory". In Lewandrowski J, Sluss PM (ed.). Utilization Management in the Clinical Laboratory and Other Ancillary Services. Springer. doi:10.1007/978-3-319-34199-6_10. ISBN 978-3-319-34199-6.
- Lewis, SL; Dirksen, SR; Heitkempet, MM; Bucher, L; Camera, I (2015). Medical-Surgical Nursing: Assessment and Management of Clinical Problems, Single Volume (8 ed.). Elsevier Health Sciences. ISBN 978-0-323-29033-3.
- Marshall, WJ; Lapsley, M; Day, A; Ayling, R (2014). Clinical Biochemistry E-Book: Metabolic and Clinical Aspects (3 ed.). Elsevier Health Sciences. ISBN 978-0-7020-5478-5.
- McCann, SR (2016). A History of Haematology: From Herodotus to HIV. OUP Oxford. ISBN 978-0-19-102713-0.
- McPherson, RA; Pincus, MR (2017). Henry's Clinical Diagnosis and Management by Laboratory Methods (23 ed.). Elsevier Health Sciences. ISBN 978-0-323-41315-2.
- Melamed, M (2001). "Chapter 1 a brief history of flow cytometry and sorting". Methods in Cell Biology. Vol. 63 part A. Elsevier. pp. 3–17. doi:10.1016/S0091-679X(01)63005-X. ISBN 978-0-12-544166-7. PMID 11060834.
- Moore, EE; Feliciano, DV; Mattox, KL (2017). Trauma (8 ed.). McGraw-Hill Education. ISBN 978-1-260-12860-4.
- Naeim, F; Rao, PN; Grody, WW (2009). Hematopathology: Morphology, Immunophenotype, Cytogenetics, and Molecular Approaches (1 ed.). Academic Press. ISBN 978-0-08-091948-5.
- d'Onofrio, G; Zini, G (2014). Morphology of Blood Disorders (2 ed.). Wiley. ISBN 978-1-118-44258-6.
- Oropello, JM; Kvetan, V; Pastores, SM (2016). Lange Critical Care. McGraw-Hill Education. ISBN 978-0-07-181726-4.
- Pagana, KD; Pagana, TJ; Pagana, TN (2014). Mosby's Diagnostic and Laboratory Test Reference. Elsevier Health Sciences. ISBN 978-0-323-22592-2.
- Palmer, L; Briggs, C; McFadden, S; Zini, G; Burthem, J; Rozenberg, G; Proytcheva, M; Machin, SJ (2015). "ICSH recommendations for the standardization of nomenclature and grading of peripheral blood cell morphological features". International Journal of Laboratory Hematology. 37 (3): 287–303. doi:10.1111/ijlh.12327. ISSN 1751-5521. PMID 25728865.
- Picot, J; Guerin, CL; Le Van Kim, C; Boulanger, C (2012). "Flow cytometry: retrospective, fundamentals and recent instrumentation". Cytotechnology. 64 (2): 109–130. doi:10.1007/s10616-011-9415-0. ISSN 0920-9069. PMC 3279584. PMID 22271369.
- Porwit, A; McCullough, J; Erber, WN (2011). Blood and Bone Marrow Pathology (2 ed.). Elsevier Health Sciences. ISBN 978-0-7020-4535-6.
- Pierre, RV (2002). "Peripheral blood film review: the demise of the eyecount leukocyte differential". Clinics in Laboratory Medicine. 22 (1): 279–297. doi:10.1016/S0272-2712(03)00075-1. ISSN 0272-2712. PMID 11933579.
- Powell, DJ; Achebe, MO (2016). "Anemia for the primary care physician". Primary Care: Clinics in Office Practice. 43 (4): 527–542. doi:10.1016/j.pop.2016.07.006. ISSN 0095-4543. PMID 27866575.
- Rodak, BF; Carr, JH (2013). Clinical Hematology Atlas (4 ed.). Elsevier Health Sciences. ISBN 978-1-4557-0830-7.
- Schafermeyer, RW; Tenenbein, M; Macias, CJ (2018). Strange and Schafermeyer's Pediatric Emergency Medicine (5 ed.). McGraw-Hill Education. ISBN 978-1-259-86076-8.
- Shapiro, HM (2003). Practical Flow Cytometry (4 ed.). John Wiley & Sons. ISBN 978-0-471-43403-0.
- Schmaier, AH; Lazarus, HM (2012). Concise guide to hematology (1 ed.). Wiley-Blackwell. ISBN 978-1-4051-9666-6.
- Turgeon, ML (2016). Linné & Ringsrud's Clinical Laboratory Science: Concepts, Procedures, and Clinical Applications (7 ed.). Elsevier Mosby. ISBN 978-0-323-22545-8.
- Van Leeuwen, AM; Bladh, ML (2019). Davis's Comprehensive Manual of Laboratory and Diagnostic Tests with Nursing Implications (8 ed.). F. A. Davis Company. ISBN 978-0-8036-9448-4.
- Vieth, JT; Lane, DR (2014). "Anemia". Emergency Medicine Clinics of North America. 32 (3): 613–628. doi:10.1016/j.emc.2014.04.007. ISSN 0733-8627. PMID 25060253.
- Walls, R; Hockberger, R; Gausche-Hill, M (2017). Rosen's Emergency Medicine - Concepts and Clinical Practice (9 ed.). Elsevier Health Sciences. ISBN 978-0-323-39016-3.
- Wang, SA; Hasserjian, RP (2018). Diagnosis of Blood and Bone Marrow Disorders. Springer. ISBN 978-3-319-20279-2.
- Wintrobe, MM (1985). Hematology, the Blossoming of a Science: A Story of Inspiration and Effort. Lea & Febiger. ISBN 978-0-8121-0961-0.
- Zandecki, M; Genevieve, F; Gerard, J; Godon, A (February 2007). "Spurious counts and spurious results on haematology analysers: a review. Part II: white blood cells, red blood cells, haemoglobin, red cell indices and reticulocytes". International Journal of Laboratory Hematology. 29 (1): 21–41. doi:10.1111/j.1365-2257.2006.00871.x. PMID 17224005.