탄산마그네슘
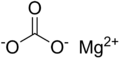
Magnesium carbonate
 | |
 | |
| 이름 | |
|---|---|
| 기타 이름 | |
| 식별자 | |
| |
3D 모델(JSmol) | |
| 체비 | |
| 첸블 | |
| 켐스파이더 | |
| ECHA 정보 카드 | 100.008.106 |
| E번호 | E504(i)(산도 조절기, ...) |
PubChem CID | |
| RTECS 번호 |
|
| 유니 |
|
CompTox 대시보드 (EPA ) | |
| |
| |
| 특성. | |
| MgCO3 | |
| 몰 질량 | 84.3139 g/g (무수) |
| 외모 | 무색 결정체 또는 백색 고체 흡습성 |
| 냄새 | 무취 |
| 밀도 | 2.958 g/cm3 (무수) 2.825g/cm3(수화물) 1.837g/cm3(3수화물) 1.73 g/cm3 (펜타수화물) |
| 녹는점 | 350°C(662°F, 623K) 분해(무수) 165 °C (329 °F, 438 K) (삼수화물) |
| 무수: 0.0139g/100ml(25°C) 0.0063g/100ml(100°C)[1] | |
용해도 제품(Ksp) | 10개−7.8[2] |
| 용해성 | 산, 수성2 CO에 용해됨 아세톤, 암모니아에 용해되지 않음 |
자화율(δ) | - 32.4 · 10−6 cm3 / 세로 |
굴절률(nD) | 1.717 (무수) 1.458(수화물) 1.412 (3수화물) |
| 구조. | |
| 삼각형의 | |
| 열화학 | |
열용량 (C) | 75.6 J/mol·K[1] |
표준 어금니 엔트로피 (S | 65.7 J/mol/K[1][3] |
표준 엔탈피/ 형성 (δHf⦵298) | - 1113 kJ/mol[3] |
깁스 자유 에너지 ( (Gf)) | - 1029.3 kJ/mol[1] |
| 약리학 | |
| A02AA01(WHO) A06AD01(WHO) | |
| 위험 요소 | |
| NFPA 704(파이어 다이아몬드) | |
| 플래시 포인트 | 불연성 |
| NIOSH(미국 건강 노출 제한): | |
PEL(허용) |
|
| 안전 데이터 시트(SDS) | ICSC 0969 |
| 관련 화합물 | |
기타 음이온 | 중탄산 마그네슘 |
기타 캐티온 | 탄산 베릴륨 탄산칼슘 탄산 스트론튬 탄산바륨 탄산라듐 |
관련 화합물 | 아르티네이트 하이드로마그네사이트 다이핑가이트 |
달리 명시되지 않은 한 표준 상태(25°C[77°F], 100kPa)의 재료에 대한 데이터가 제공됩니다. | |
|
탄산마그네슘(MgCO)은3 무색 또는 흰색 고체인 무기염이다.수화된 탄산 마그네슘의 기본 형태도 광물로 존재한다.
폼
탄산마그네슘의 가장 일반적인 형태는 마그네사이트(MgCO3)라고 불리는 무수염과 바링토나이트로 알려진3 di, tri, 펜타히드레이트(MgCO·2)입니다.HO2), nesquehonite(MgCO3·3)HO2) 및 랜스포다이트(MgCO3·5)HO)[5]를2 참조해 주세요.Artinite(MgCO23(OH)·23 등 일부 기본 형태HO2), 하이드로마그네사이트(Mg5(CO3)(4OH)·24HO2) 및 다이핑라이트(Mg5(CO3)(4OH)·25HO2)는 미네랄로도 발생합니다.그 모든 미네랄은 컬러리스나 흰색입니다.
마그네사이트는 무색 또는 흰색 삼각 결정으로 구성되어 있습니다.무수염은 물, 아세톤, 암모니아에 실질적으로 용해되지 않는다.모든 형태의 탄산 마그네슘은 산과 반응한다.마그네사이트는 Mg가 6개의 산소원자로 둘러싸인2+ 칼사이트 구조로 결정화된다.이수화물은 삼사정 구조를 가지고 있는 반면, 삼수화물은 단사정 구조를 가지고 있다.
"가볍다"와 "무거운" 마그네슘 탄산염에 대한 언급은 각각 마그네슘 하이드록시 탄산염과 다이핑라이트를 의미합니다.[6]
준비
탄산마그네슘은 일반적으로 마그네사이트 광산에 의해 얻어진다.세계 물량의 70%가 중국에서 [7]채굴되고 준비된다.
탄산마그네슘은 수용성 마그네슘 소금과 중탄산나트륨의 반응을 통해 실험실에서 제조할 수 있다.
- MgCl2(aq) + 2 NaHCO3(aq) → MgCO3(s) + 2 NaCl(aq) + HO(l) + CO22(g)
염화마그네슘(또는 황산나트륨)을 수성 탄산나트륨으로 처리하면 탄산마그네슘이 아닌 염기성 탄산마그네슘(탄산마그네슘과 수산화마그네슘의 수화복합체)의 침전이 형성됩니다.
- 52 MgCl(aq) + 5 NaCO23(aq) + 52 HO(l) → Mg4(CO3)(3OH)/23HO2(s) + Mg(HCO3)(2aq) + 10 NaCl(aq)
고순도 산업 루트에는 수산화마그네슘과 이산화탄소를 고압 및 적당한 온도에서 혼합하여 [5]형성할 수 있는 중탄산마그네슘을 통과하는 경로가 포함됩니다.중탄산염은 진공 건조되어 이산화탄소와 물 분자를 잃게 됩니다.
- Mg(OH)2 + 2 CO2 → Mg(HCO3)2
- Mg(HCO3)2 → MgCO3 + CO22 + HO
화학적 성질
산포함
많은 일반적인 2족 금속 탄산염과 마찬가지로 탄산 마그네슘은 수산과 반응하여 이산화탄소와 물을 방출합니다.
- MgCO3 + 2 HCl → MgCl2 + CO22 + HO
- MgCO3 + HSO24 → MgSO4 + CO22 + HO
분해
고온에서3 MgCO는 산화마그네슘과 이산화탄소로 분해됩니다.이 과정은 [5]산화마그네슘 생산에 중요하다.이 과정을 소성이라고 합니다.
- MgCO3 → MgO + CO2 (δH = +160 kJ/mol)
분해 온도는 350°C(662°F)[8][9]입니다.그러나 산화물에 대한 소성은 방출된 이산화탄소의 판독을 방해하기 때문에 일반적으로 900°C 이하에서는 완전한 것으로 간주되지 않습니다.
소금의 하이드레이트는 [10]분해하는 동안 다른 온도에서 수분을 잃습니다.예를 들어, 3수화물3 MgCO·3은분자식이2 Mg(HCO3)(OH)·2HO로2 표기될 수 있는 HO는 다음과 [10]같이 157°C와 179°C에서 탈수 단계가 발생한다.
- Mg(HCO3)(OH)·2(HO2) → Mg(HCO3)(OH)·(HO2) + 1572°C에서의 HO
- Mg(HCO3)(OH)·(HO2) → Mg(HCO3)(OH) + 1792 °C에서의 HO
사용하다
탄산마그네슘의 주요 용도는 소성하여 산화마그네슘을 생산하는 것입니다.마그네사이트와 돌로마이트 광물은 내화 [5]벽돌을 만드는데 사용된다.MgCO는3 바닥재, 방화, 소화, 화장품, 먼지 분말, 치약에도 사용된다.그 외의 용도에는 필러재, 플라스틱의 연기 억제제, 네오프렌 고무의 강화제, 건조제, 식품의 색 유지 등이 있습니다.
물에3 대한 낮은 용해성과 흡습성 특성 때문에, MgCO는 1911년에 소금이 더 자유롭게 흐를 수 있도록 처음 첨가되었다.Morton Salt사는 "When the3 rains it pours"라는 슬로건을 채택했는데, 이는 MgCO가 함유된 소금이 습한 [11]날씨에는 서로 달라붙지 않는다는 것을 의미한다.탄산마그네슘은 암벽 등반, 체조, 역도 등 꽉 잡아야 하는 [7]종목에서 선수들의 손 건조제로도 사용된다.
식품첨가물로서 탄산마그네슘은 E504로 알려져 있다.그것의 유일한 부작용은 [12]고농도에서는 설사약으로 작용할 수 있다는 것이다.
탄산마그네슘은 두개골 미백을 위한 박제술에 사용된다.그것은 과산화수소와 섞여서 반죽을 만들 수 있고, 그것은 하얀색 마무리를 하기 위해 두개골에 펴 발라진다.
투사 [13]스크린의 매트 화이트 코팅으로 탄산마그네슘을 사용한다.
의료용
또한 식탁용 소금에 고순도 탄산마그네슘을 제산제 및 첨가제로 사용하여 유동성을 유지한다.탄산마그네슘은 물 속에서 녹지 않고, [14]거품을 내기 위한 산성에서만 녹기 때문에 이것을 할 수 있다.
안전.
탄산마그네슘은 무독성과 불연성이다.
보충 상태
「 」를 참조해 주세요.
- 아세트산칼슘/탄산마그네슘
- 탄산마그네슘의 비정질 형태인 우살라이트
주 및 참고 자료
- ^ a b c d "Magnesium carbonate".
- ^ Bénézeth, Pascale; Saldi, Giuseppe D.; Dandurand, Jean-Louis; Schott, Jacques (2011). "Experimental determination of the solubility product of magnesite at 50 to 200 °C". Chemical Geology. 286 (1–2): 21–31. Bibcode:2011ChGeo.286...21B. doi:10.1016/j.chemgeo.2011.04.016.
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A22. ISBN 978-0-618-94690-7.
- ^ NIOSH Pocket Guide to Chemical Hazards. "#0373". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b c d Margarete Seeger; Walter Otto; Wilhelm Flick; Friedrich Bickelhaupt; Otto S. Akkerman. "Magnesium Compounds". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a15_595.pub2.
- ^ Botha, A.; Strydom, C.A. (2001). "Preparation of a magnesium hydroxy carbonate from magnesium hydroxide". Hydrometallurgy. 62 (3): 175. doi:10.1016/S0304-386X(01)00197-9.
- ^ a b Allf, Bradley (21 May 2018). "The Hidden Environmental Cost of Climbing Chalk". Climbing Magazine. Cruz Bay Publishing. Retrieved 22 May 2018.
In fact, China produces 70 percent of the world’s magnesite. Most of that production—both mining and processing—is concentrated in a small corner of Liaoning, a hilly industrial province in northeast China between Beijing and North Korea.
- ^ "IAState MSDS".
- ^ Weast, Robert C.; et al. (1978). CRC Handbook of Chemistry and Physics (59th ed.). West Palm Beach, FL: CRC Press. p. B-133. ISBN 0-8493-0549-8.
- ^ a b "Conventional and Controlled Rate Thermal analysis of nesquehonite Mg(HCO3)(OH)·2(H2O)" (PDF).
- ^ "Her Debut - Morton Salt". Retrieved 27 December 2017.
- ^ "Food-Info.net : E-numbers : E504: Magnesium carbonates". 080419 food-info.net
- ^ Noronha, Shonan (2015). Certified Technology Specialist-Installation. McGraw Hill Education. p. 256. ISBN 978-0071835657.
- ^ "What Is Magnesium Carbonate?". Sciencing. Retrieved 15 April 2018.
- ^ British Pharmacopoeia Commission Secretariat (2009). "Index, BP 2009" (PDF). Archived from the original (PDF) on 11 April 2009. Retrieved 31 January 2010.
- ^ "Japanese Pharmacopoeia, Fifteenth Edition" (PDF). 2006. Archived from the original (PDF) on 22 July 2011. Retrieved 31 January 2010.