갈륨(III)산화물
Gallium(III) oxide β-GaO23 결정체 | |
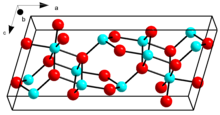 β-GaO의23 결정구조 | |
| 이름 | |
|---|---|
| 기타 이름 삼산화 갈륨, 세스키오사이드 갈륨 | |
| 식별자 | |
| |
3D 모델(JSmol) | |
| 켐스파이더 | |
| ECHA InfoCard | 100.031.525 |
펍켐 CID | |
| RTECS 번호 |
|
| 유니 | |
CompTox 대시보드 (EPA) | |
| 특성. | |
| 가오23 | |
| 어금질량 | 187.444 g/190[1] |
| 외관 | 백색 결정 가루 |
| 밀도 | 6.44 g/cm3, 알파 5.88 g/cm3, 베타 |
| 녹는점 | 1,900 °C(3,450 °F, 2,170 K) 알파 1725°C, 베타 |
| 불용성인 | |
| 용해성 | 대부분의 산에서 용해되는 |
| 밴드 갭 | 4.7-4.9 eV(β-GaO23) |
| 구조 | |
| α: 삼각, hR30, 우주군 = R3c, 번호 167[3] | |
a = 0.49835 / 1.222247nm, b = 0.49835 / 0.30403nm, c = 0.53286/0.58088nm | |
공식 단위(Z) | 6 / 4 |
| 열화학 | |
열 용량 (C) | 92.1 J/몰·K[5] |
성 어금니 엔트로피 (S | 85.0 J/mol·K[5] |
의 성 엔탈피 대형화 (ΔfH⦵298) | −1089.1 kJ/mol[5] |
기브스 자유 에너지 (ΔfG˚) | -998.3 kJ/mol[5] |
| 위험 | |
| 나열되지 않음 | |
달리 명시된 경우를 제외하고, 표준 상태(25°C [77°F], 100 kPa)의 재료에 대한 데이터가 제공된다. | |
| Infobox 참조 자료 | |
삼산화 갈륨은 GaO라는 공식을 가진23 무기 화합물이다. 그것은 여러 개의 다형체로 존재하며, 모두 백색, 수용성 고체다. 상업적 응용은 존재하지 않지만, GaO는23 갈륨의 정화의 매개체로서 갈륨 비소로 거의 독점적으로 소비되고 있다.[6] β-GaO의23 열전도도는 GaN, SiC와 같은 다른 와이드 밴드갭 반도체보다 최소 한 자릿수 낮다.[7] 주로 전자기기에 사용되는 관련 나노구조물에 대해서는 더욱 감소한다.[7] 다이아몬드, SiC와 같은 높은 열전도성 기판과의 이질적인 통합은 β-GaO23 전자기의 열 방출을 돕는다.[8][9]
준비
삼산화 갈륨은 갈륨 소금의 산성 용액이나 기본 용액의 중성화에 따라 수화 형태로 침전된다. 또한 공기 중의 갈륨을 가열하거나 질산 갈륨을 200–250 ˚C에서 열분해하여 형성된다. α, β, β, Δ, Δ, ε의 다섯 가지 다른 변형에서 발생할 수 있다. 이러한 변형 중 β-GaO가23 가장 안정된 형태다.[10]
- β-GaO는23 질산염, 아세테이트, 옥살레이트 또는 기타 유기파생물을 1000 °C 이상 가열하여 제조한다. β-GaO의23 상피 박막은 190 °C에서 550 °C 사이의 온도에서 사파이어 기질에 침전될 수 있다.[11]
- α-GaO는23 65 kbars 및23 1100 °C에서 가열하면 얻을 수 있다. 수화 형태는 500 °C에서 침전된 갈륨과 "숙성된" 갈륨을 분해하여 준비할 수 있다.
- γ-GaO는23 수산화 겔을 400~500℃에서 빠르게 가열하여 제조한다. 이 다형체의 보다 결정적인 형태는 용온 합성에 의해 갈륨 금속으로부터 직접 준비될 수 있다.[12]
- Δ-GaO는23 250 °C에서 가(NO3)3를 가열하여 얻는다.
- ε-GaO는23 Δ-GaO를23 550 °C에서 가열하여 준비한다.[10] ε-GaO의23 박막은 550~650°C의 온도에서 사파이어 기판에 트리메틸갈륨과 물을 사용하여 금속 유기 증기상 에피택스에 의해 침전된다.
반응
삼산화 갈륨은 암페리히 입니다.[14] 고온에서 알칼리 금속 산화물과 반응하여 예를 들어 NaGaO를2 형성하고 Mg, Zn, Co, Ni, Cu 산화물 등과 반응하여 스피넬을 형성한다(예: MgGaO24).[15] 강한 알칼리에 용해되어 용액인 가(OH)를 형성한다.−
4
HCl로 갈륨 트리클로로이드 GaCl을3 형성한다.[16]
- Ga2O3 + 6 HCl → 2 GaCl3 + 3 H2O
H에2 의해 또는 갈륨 금속과의 반응에 의해 아산화 갈륨(갈륨(I) 산화물) GaO로2 감소될 수 있다.[17][18]
- GaO23 + 2H2 → GaO2 + 2 HO2
- Ga2O3 + 4 Ga → 3 Ga2O
구조
β-GaO는23 1900 pointC의 녹는점을 가진 것으로 가장 안정적인 결정체 변형이다. 산화 이온은 왜곡된 입방체 가장 가까운 패킹 배열 안에 있으며 갈륨(III) 이온은 왜곡된 사면체 및 팔면체 부위를 차지하고 있으며, 각각 Ga-O 결합 거리는 1.83 00과 2.00 å이다.[19]
α-GaO는23 α-AlO와23 동일한 구조(코런덤)를 가지며, 여기서 Ga 이온은 6개 좌표로 되어 있다. γ-GaO는23 γ-AlO와23 유사한 결함 스피넬 구조를 가지고 있다.[20]
ε-GaO23 필름은 금속유기성 증기상피막으로 퇴적되어 직교합체 결정 대칭이 있는 주상 구조를 보여준다. 거시적으로 이 구조는 X선 결정학에 의해 육각형 근접 포장된 것으로 보인다.[21]
잠재적 응용 프로그램
갈륨(III) 산화물은 레이저, 인광 및 발광 물질의 사용으로 연구되었다.[10] 그것은 또한 촘촘한 접합부의 절연 장벽으로 사용되어 왔다.[22] 모노클린 β-GaO는23 가스 센서와 발광 인광에 사용되며 태양 전지의 유전체 코팅에 적용할 수 있다. 이 안정적인 산화물은 또한 극자외선 투명 전도성 산화물 [23]및 트랜지스터 용도에 대한 가능성을 보여주었다.[24][25]
사파이어에 예치된 ε-GaO23 박막은 태양맹 UV 광검출기로서의 잠재적인 응용을 보여준다.[26]
얇은 가오23 필름은 가스감응 소재와 가오(GaO23)로 상업적 관심이 높다. 타원측정법은 β-GaO의23 광학적 기능을 결정하는 데 사용할 수 있는 절차다.[11][23]
β-GaO는23 GaO-AlO2323 촉매의 생산에 사용된다.[27]
참조
- ^ Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton, FL: CRC Press. p. 4.64. ISBN 1-4398-5511-0.
- ^ Patnaik, Pradiot(2002) 무기 화학 지침서. 맥그로힐 ISBN 0-07-049439-8
- ^ Eckert, L. J.; Bradt, R. C. (1973). "Thermal Expansion of Alpha Ga2O3". Journal of the American Ceramic Society. 56 (4): 229. doi:10.1111/j.1151-2916.1973.tb12471.x.
- ^ Dohy, D.; Gavarri, J.R. (1983). "Oxyde β-Ga2O3: Champ de force, dilatation thermique, et rigidité anisotropes". Journal of Solid State Chemistry. 49 (1): 107–117. Bibcode:1983JSSCh..49..107D. doi:10.1016/0022-4596(83)90222-0.
- ^ Jump up to: a b c d Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton, FL: CRC Press. p. 5.12. ISBN 1-4398-5511-0.
- ^ 그레버, J. F. (2012) 울만의 산업 화학 백과사전 Wiley-VCH, Weinheim의 "갈륨과 갈륨 화합물" 도이:10.1002/14356007.a12_163.
- ^ Jump up to: a b Cheng, Zhe; Tanen, Nicholas; Chang, Celesta; Shi, Jingjing; McCandless, Jonathan; Muller, David; Jena, Debdeep; Xing, Huili Grace; Graham, Samuel (26 August 2019). "Significantly reduced thermal conductivity in β-(Al0.1Ga0.9)2O3/Ga2O3 superlattices". Applied Physics Letters. 115 (9): 092105. arXiv:1905.00139. doi:10.1063/1.5108757. ISSN 0003-6951.
- ^ Cheng, Zhe; Yates, Luke; Shi, Jingjing; Tadjer, Marko J.; Hobart, Karl D.; Graham, Samuel (1 March 2019). "Thermal conductance across β-Ga2O3-diamond van der Waals heterogeneous interfaces". APL Materials. 7 (3): 031118. doi:10.1063/1.5089559.
- ^ Cheng, Zhe; Mu, Fengwen; You, Tiangui; Xu, Wenhui; Shi, Jingjing; Liao, Michael E.; Wang, Yekan; Huynh, Kenny; Suga, Tadatomo; Goorsky, Mark S.; Ou, Xin (7 October 2020). "Thermal Transport across Ion-Cut Monocrystalline β-Ga2O3 Thin Films and Bonded β-Ga2O3–SiC Interfaces". ACS Applied Materials & Interfaces. 12 (40): 44943–44951. doi:10.1021/acsami.0c11672. ISSN 1944-8244.
- ^ Jump up to: a b c 바야르, J; 에멜레우스, H; 니홀름, R; 트로트만 디킨슨, A. F. (1973) 종합 무기 화학. 제1권 1091호
- ^ Jump up to: a b Rafie Borujeny, E.; Sendetskyi, O.; Fleischauer, M. D.; Cadien, K. C. (2020). "Low Thermal Budget Heteroepitaxial Gallium Oxide Thin Films Enabled by Atomic Layer Deposition". ACS Applied Materials & Interfaces. 12 (39). doi:10.1021/acsami.0c08477. PMID 32865966.
- ^ Playford, Helen Y.; Hannon, Alex C.; Barney, Emma R.; Walton, Richard I. (2013). "Structures of Uncharacterised Polymorphs of Gallium triOxide from Total Neutron Diffraction". Chemistry – A European Journal. 19 (8): 2803–13. doi:10.1002/chem.201203359. PMID 23307528.
- ^ Boschi, F.; Bosi, M.; Berzina, T.; Buffagni, E.; Ferrari, C.; Fornari, R. (2015). "Hetero-epitaxy of ε-Ga2O3 layers by MOCVD and ALD". Journal of Crystal Growth. 44: 25–30. doi:10.1016/j.jcrysgro.2016.03.013.
- ^ 에빙, 다렐 D.; 감몬, 스티븐 D. (2010) 제너럴 케미스트리, 9번 에드, 톰슨 브룩스/콜레. ISBN 0538497521
- ^ 다운스, 앤서니 존(1993) 알루미늄, 갈륨, 인듐 및 탈륨의 화학. 스프링거 . ISBN 075140103X
- ^ Jukerman, JJ 및 Hagen, A P eds. (2009) 무기반응 및 방법, 할로겐에 대한 채권 형성(2부), Wiley-VCH Verlag GmbH, ISBN 9780470145395
- ^ Koch, H. F.; Girard, L. A.; Roundhill, D. M. (1999). "Determination of Gallium in a Cerium Surrogate and in Drops from a Copper Collector by ICP as Model Studies for the Removal of Gallium from Plutonium". Atomic Spectroscopy. 20 (1): 30.
- ^ 그린우드, N.N.; 에밀레우스, H. J.와 샤프, A. G. (1963) 무기화학 및 방사화학 분야의 진보에 있어서의 갈륨의 화학, 제5권, 엘스비에르, 학술언론
- ^ 킹, R. B. (1994) 무기화학 백과사전 제3권 페이지 1256. ISBN 978-0-470-86078-6
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. p. 247. ISBN 978-0-08-037941-8.
- ^ Cora, I (2017). "The real structure of ε-Ga2O3 and its relation to κ-phase". CrystEngComm. 19 (11): 1509–1516. doi:10.1039/C7CE00123A.
- ^ Dai, Z. R.; Pan, Z. W.; Wang, Z. L. (2002). "Gallium Oxide Nanoribbons and Nanosheets". The Journal of Physical Chemistry B. 106 (5): 902. CiteSeerX 10.1.1.655.6068. doi:10.1021/jp013228x.
- ^ Jump up to: a b Rebien, M; Henrion, W; Hong, M; Mannaerts, J; Fleischer, M (2002). "Optical properties of gallium oxide thin films". Applied Physics Letters. 81 (2): 250. Bibcode:2002ApPhL..81..250R. doi:10.1063/1.1491613.
- ^ Thomas, Stuart R.; Adamopoulos, George; Lin, Yen-Hung; Faber, Hendrik; Sygellou, Labrini; Stratakis, Emmanuel; Pliatsikas, Nikos; Patsalas, Panos A.; Anthopoulos, Thomas D. (2014). "High electron mobility thin-film transistors based on Ga2O3 grown by atmospheric ultrasonic spray pyrolysis at low temperatures". Applied Physics Letters. 105 (9): 092105. Bibcode:2014ApPhL.105i2105T. doi:10.1063/1.4894643.
- ^ Higashiwaki, M.; Jessen, G. H. (2018). "The dawn of gallium oxide microelectronics". Applied Physics Letters. 112 (6): 060401. doi:10.1063/1.5017845.
- ^ Pavesi, M. (2018). "ε-Ga2O3 epilayers as a material for solar-blind UV photodetectors". Materials Chemistry and Physics. 205: 502–507. doi:10.1016/j.matchemphys.2017.11.023.
- ^ Shimizu, Ken-Ichi; Takamatsu, Mikio; Nishi, Koji; Yoshida, Hisao; Satsuma, Atsushi; Tanaka, Tsunehiro; Yoshida, Satohiro; Hattori, Tadashi (1999). "Alumina-Supported Gallium trixide Catalysts for NO Selective Reduction: Influence of the Local Structure of Surface Gallium trioxide Species on the Catalytic Activity". The Journal of Physical Chemistry B. 103 (9): 1542. doi:10.1021/jp983790w.
