산화물
Oxide
산화물(/ ˈɒka ɪd/)은 적어도 하나의 산소 원자와 하나의 다른 원소를 포함하는 화학 화합물입니다.산화물 자체가 산소의 음이온( –2의2– 순전하를 갖는 음이온)이며, 산화 상태가 -2인 산화 상태가 -2인 산소의 O 이온입니다.지구의 지각의 대부분은 산화물로 이루어져 있습니다.순수 원소로 간주되는 물질조차도 종종 산화물 코팅이 발생합니다.예를 들어 알루미늄 포일은 다음과 같은 얇은 피부를 형성합니다.추가적인 산화로부터 호일을 보호하는 AlO23(패시베이션 층이라고 함)[2]
화학양론
산화물은 화학양론적 관점(반응물과 반응물의 화학 방정식 사이의 측정 가능한 관계)과 각 화학양론적 관점에서 매우 다양합니다.대부분의 원소는 하나 이상의 화학양론적 산화물을 형성합니다.잘 알려진 예로는 일산화탄소와 이산화탄소가 있습니다.[2]이것은 2진 산화물, 즉 산화물과 다른 원소만을 포함하는 화합물에 적용됩니다.이진 산화물보다 훨씬 더 일반적인 것은 더 복잡한 화학양론적 구조의 산화물입니다.이러한 복잡성은 다른 양이온(양으로 대전된 이온, 즉 전기 분해에서 음극으로 끌어당길 수 있는 이온) 또는 다른 음이온(음으로 대전된 이온)의 도입에 의해 발생할 수 있습니다.철 규산염, FeSiO24, 광물 파얄라이트는 삼원계 산화물의 많은 예들 중 하나입니다.많은 금속 산화물의 경우 다형성과 비화학양론의 가능성도 존재합니다.[3]상업적으로 중요한 티타늄의 다이옥사이드는 예를 들어 세 가지의 별개의 구조로 존재합니다.많은 금속 산화물들이 다양한 비양론적 상태로 존재합니다.다양한 리간드를 가진 많은 분자 산화물들이 또한 존재합니다.[4]
단순화를 위해 이 기사의 대부분은 이진 산화물에 초점을 맞추고 있습니다.
형성
산화물은 몇 가지 희가스를 제외한 모든 요소와 관련이 있습니다.이와 같이 다양한 종류의 화합물이 형성되는 경로는 그만큼 많습니다.
금속산화물
많은 금속 산화물은 탄산염, 수산화물 및 질산염과 같은 다른 금속 화합물의 분해에 의해 발생합니다.칼슘 산화물을 만드는 과정에서 탄산칼슘(석회석)은 가열할 때 분해되어 이산화탄소를 방출합니다.[2]
공기 중의 산소와 요소의 반응은 특히 철의 상업적 사용과 관련된 부식의 핵심 단계입니다.거의 모든 원소들은 산소 분위기로 가열할 때 산화물을 형성합니다.예를 들어, 아연 분말은 공기 중에서 연소되어 산화 아연을 제공합니다.[5]
광석으로부터 금속을 생산하는 것은 종종 금속 황화물 광물을 공기 중에서 로스팅(가열)함으로써 산화물을 생산하는 것을 수반합니다.이러한 방식으로, MoS2(몰리브덴나이트)는 사실상 모든 몰리브덴 화합물의 전구체인 삼산화몰리브덴으로 변환됩니다.[6]
금과 백금과 같은 귀금속은 산소와 직접적인 화학적 결합에 저항하기 때문에 귀하게 여겨집니다.[2]
비금속산화물
중요하고 널리 사용되는 비금속 산화물은 이산화탄소와 일산화탄소입니다.이 종들은 탄소 또는 탄화수소의 완전한 또는 부분적인 산화에 의해 형성됩니다.산소가 부족한 상태에서 일산화탄소가 생성됩니다.[2]
산소가 과잉일 경우 이산화탄소가 생성되며, 일산화탄소의 매개에 의해 경로가 진행됩니다.
질소 원소(N2)는 산화물로 변환하기 어렵지만 암모니아의 연소로 산화 질소가 생성되어 산소와 더 반응합니다.
이러한 반응은 상품 화학물질인 질산의 생산에서 실행됩니다.[7]
산업적으로 가장 큰 규모로 생산되는 화학물질은 황산입니다.이산화황으로 황이 산화되어 삼산화황으로 따로 산화됩니다.[8]
마지막으로 삼산화물은 수화 반응에 의해 황산으로 전환됩니다.
구조.
산화물은 개별 분자에서 고분자 및 결정 구조에 이르기까지 다양한 구조를 가지고 있습니다.표준 조건에서 산화물의 범위는 고체에서 기체에 이르기까지 다양합니다.금속의 고체 산화물은 일반적으로 주변 조건에서 고분자 구조를 갖습니다.[9]
분자산화물
- 일부 중요한 기체 산화물
-
이산화탄소는 화석 연료 연소의 주요 생성물입니다.
-
일산화탄소는 탄소 기반 연료의 불완전 연소의 산물이며 많은 유용한 화학물질의 전구물질입니다.
-
이산화질소는 내연기관에서 발생하는 문제가 되는 오염물질입니다.
-
아산화질소("웃는 가스")는 토양 박테리아에 의해 생성되는 강력한 온실가스입니다.
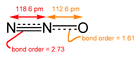
대부분의 금속 산화물은 결정성 고체이지만 일부 산화물은 분자입니다.분자 산화물의 예로는 이산화탄소와 일산화탄소가 있습니다.질소의 모든 단순 산화물은 분자입니다. 예를 들어 NO, NO2, NO2 및 NO24.오산화인은 기만적인 이름을 가진 더 복잡한 분자 산화물이며, 실제 공식은 PO입니다410.테트로옥사이드는 희귀하며, 몇 가지 더 일반적인 예로는 이리듐 테트로옥사이드,[10] 루테늄 테트로옥사이드, 오스뮴 테트로옥사이드, 제논 테트로옥사이드가 있습니다.[2]
반응
축소
금속 산화물을 금속으로 환원하는 것은 일부 금속 생산에서 대규모로 실행됩니다.많은 금속 산화물이 가열만으로 금속으로 변환됩니다(열분해 참조).예를 들어 산화은은 200 °C에서 분해됩니다.[11]
그러나 대부분의 경우 금속 산화물은 화학 시약에 의해 환원됩니다.일반적이고 저렴한 환원제는 콜라 형태의 탄소입니다.가장 눈에 띄는 예는 철광석 제련입니다.많은 반응이 관련되어 있지만, 단순화된 방정식은 보통 다음과 같이 나타납니다.[2]
일부 금속 산화물은 유기 화합물을 포함할 수 있는 환원제의 존재 하에서 용해됩니다.산화철의 환원 용해는 철의 순환과 같은 지구화학 현상에 필수적입니다.[12]
가수분해 및 용해
일반적으로 M-O 결합이 강하기 때문에 금속 산화물은 수성 산과 염기에 의해 공격을 받을 수 있지만 용매에 불용성인 경향이 있습니다.[2]
산화물의 용해는 종종 옥시아니온을 제공합니다.수성 염기를 PO에410 첨가하면 다양한 인산염을 얻을 수 있습니다.수성 염기를 MoO에3 첨가하면 폴리옥소메탈레이트가 생성됩니다.옥시케이션은 더 드물며, 일부 예로는 니트로소늄(NO+), 바나딜(VO2+), 우라닐(UO2+2)이 있습니다.물론 많은 화합물들이 산화물과 다른 그룹 모두에 알려져 있습니다.유기 화학에서, 이것들은 케톤과 많은 관련된 카보닐 화합물을 포함합니다.전이 금속의 경우, 옥시할라이드 뿐만 아니라 많은 옥소 복합체가 알려져 있습니다.[2]
명명법 및 수식
가장 높은 산화 상태의 화학 원소 산화물의 화학 공식은 예측 가능하며 해당 원소에 대한 원자가 전자의 수에서 유도됩니다.16족4 원소로는 O의 화학식인 테트라산소도 예측 가능합니다.한 가지 예외는 구리이며, 이 경우 가장 높은 산화 상태의 산화물은 구리)입니다.II) 구리(I) 산화물이 아닌 산화물.불소는 FO로 예상되는 것처럼27 존재하지 않지만 OF로2 존재합니다.[13]
참고 항목
- 기타 산소이온 오조나이드, O-3, 슈퍼옥사이드, O-2, 과산화물, O2-2 및 다이옥시게닐, O+2
- 아산화물
- 옥소할라이드
- 옥사니온
- 복합산화물
- 카테고리 참조:산화물 목록을 위한 산화물.
- 소금.
- 습전자
참고문헌
- ^ Hein, Morris; Arena, Susan (2006). Foundations of College Chemistry (12th ed.). Wiley. ISBN 978-0-471-74153-4.
- ^ a b c d e f g h i 그린우드, N. N. & Earnshaw, A. (1997)원소의 화학 (제2판), 옥스포드:버터워스-하이네만.ISBN 0-7506-3365-4.
- ^ C. N. R. Rao, B. Raveau (1995). Transition Metal Oxides. New York: VCH. ISBN 1-56081-647-3.
- ^ Roesky, Herbert W.; Haiduc, Ionel; Hosmane, Narayan S. (2003). "Organometallic Oxides of Main Group and Transition Elements Downsizing Inorganic Solids to Small Molecular Fragments". Chem. Rev. 103 (7): 2579–2596. doi:10.1021/cr020376q. PMID 12848580.
- ^ Graf, Günter G. (2000). "Zinc". Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1002/14356007.a28_509. ISBN 3-527-30673-0.
- ^ Roger F. Sebenik; et al. (2005). "Molybdenum and Molybdenum Compounds". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a16_655.
- ^ Thiemann, Michael; Scheibler, Erich; Wiegand, Karl Wilhelm. "Nitric Acid, Nitrous Acid, and Nitrogen Oxides". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a17_293.
- ^ Müller, Hermann (2000). "Sulfuric Acid and Sulfur Trioxide". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a25_635.
- ^ P.A. Cox (2010). Transition Metal Oxides. An Introduction to Their Electronic Structure and Properties. Oxford University Press. ISBN 978-0-19-958894-7.
- ^ Gong, Yu; Zhou, Mingfei; Kaupp, Martin; Riedel, Sebastian (2009). "Formation and Characterization of the Iridium Tetroxide Molecule with Iridium in the Oxidation State +VIII". Angewandte Chemie International Edition. 48 (42): 7879–7883. doi:10.1002/anie.200902733. PMID 19593837.
- ^ "Silver oxide".
- ^ Cornell, R. M.; Schwertmann, U. (2003). The Iron Oxides: Structure, Properties, Reactions, Occurrences and Uses, Second Edition. p. 323. doi:10.1002/3527602097. ISBN 978-3-527-30274-1.
- ^ Schultz, Emeric (2005). "Fully Exploiting the Potential of the Periodic Table through Pattern Recognition". J. Chem. Educ. 82 (11): 1649. Bibcode:2005JChEd..82.1649S. doi:10.1021/ed082p1649.