간세포
Hepatocyte| 간세포 | |
|---|---|
 | |
 | |
| 세부 사항 | |
| 위치 | 간 |
| 식별자 | |
| 메쉬 | D022781 |
| TH | H3.04.05.00006 |
| FMA | 14515 |
| 미세해부술의 해부학적 용어 | |
간세포는 간의 주요 실질 조직의 세포이다.간세포는 간 덩어리의 80%를 차지한다.이러한 셀은 다음 작업에 관여합니다.
구조.
전형적인 간세포는 입방체형이며 변은 20~30μm이다(비교적으로 사람의 털은 직경이 17~180μm이다).[1]간세포의 일반적인 부피는 3.4 x 10−93 [2]cm이다.
부드러운 소포체는 간세포에 풍부하지만, 대부분의 체내 세포는 소량만을 가지고 있다.
미세해부술
간세포는 다수의 미토콘드리아를 반사하는 호산성 세포질 및 대량의 매끄러운 소포체 및 유리 리보솜에 의한 호염기성 스티플링을 나타낸다.갈색 리포푸신 과립은 또한 불규칙한 세포질 비조직 영역과 함께 관찰됩니다. 이것들은 조직학적 준비 과정에서 제거된 세포질 글리코겐 및 지질 저장에 해당합니다.간세포의 평균 수명은 5개월이다; 그들은 재생이 가능하다.
간세포 핵은 분산된 염색질과 두드러진 핵으로 둥글다.이소카리오시스(또는 핵의 크기 변화)는 흔하며 종종 성인 [3]간에서 간세포의 30-40%의 정상 특징인 사배체 및 다른 정도의 다배체를 반영한다.2핵 세포 또한 흔하다.
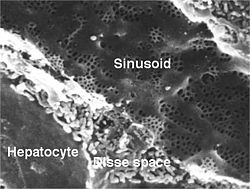
간세포는 레티쿨린(콜라겐 타입 III) 네트워크에 의해 지지되는 배치인 혈관 채널(시누소이드)에 의해 분리된 판으로 조직된다.간세포 판은 포유류의 경우 1개의 세포 두께이고 닭의 경우 2개의 세포 두께입니다.정현파에는 불연속적인 펜스트레이트된 내피세포 라이닝이 나타납니다.내피세포는 기저막이 없고 간세포에서 디세(Disse)의 공간에 의해 분리되며, 디세(Disse)는 림프를 문관 림프관으로 배출한다.
쿠퍼 세포는 내피 세포 사이에 산재한다; 그들은 망상 내피 시스템과 식세포 사용 후 적혈구의 일부이다.성상 세포는 비타민 A를 저장하고 세포 외 기질과 콜라겐을 생성한다; 그것들은 또한 내피 세포에 분포하지만 빛 현미경 검사로는 시각화하기 어렵다.
기능.
단백질 합성
간세포는 혈청 알부민, 피브리노겐 및 프로트롬빈 그룹의 응고 인자를 생산하는 체내 세포이다(인자 3 및 4 제외).
이것은 리포단백질, 셀룰로플라스민, 트랜스페린, 보체 및 당단백질 합성을 위한 주요 장소이다.간세포는 그들만의 구조단백질과 세포내 효소를 생산한다.
단백질의 합성은 거친 소포체(RER)에 의해 이루어지며, 거친 소포체(SER)와 매끄러운 소포체(SER) 모두 형성된 단백질의 분비에 관여한다.
소포체(ER)는 간세포에 의해 합성되거나 변형된 지질 및 탄수화물 부분에 대한 단백질의 결합에 관여한다.
호르몬으로 기능하는 간세포에 의해 생성된 단백질은 간염으로 알려져 있다.
탄수화물 대사
간은 탄수화물로부터 지방산을 형성하고 지방산과 [4]글리세롤로부터 트리글리세리드를 합성한다.간세포는 또한 아포단백질을 합성하여 리포단백질(VLDL, HDL)을 조립하고 수출한다.
간은 또한 알라닌, 글리세롤, 옥살로아세테이트와 같은 전구체로부터 탄수화물을 형성하는 글루코네제네시스(gluconeogenesis)의 주요 부위이다.
지질대사
간은 전신 순환으로부터 많은 지질들을 공급받아 카이로미크론 잔존물을 대사한다.또한 아세테이트로부터 콜레스테롤을 합성하고 담즙염을 추가로 합성합니다.간은 담즙염이 형성되는 유일한 장소이다.
해독
간세포는 약물, 살충제, 스테로이드와 같은 내인성 화합물을 대사, 해독, 비활성화하는 능력을 가지고 있다.
장내 정맥혈을 간으로 배출하려면 다양한 흡수 물질을 효율적으로 해독하여 항상성을 유지하고 섭취한 독소로부터 몸을 보호해야 합니다.
간세포의 해독 기능 중 하나는 암모니아를 배설하기 위해 요소로 변형시키는 것이다.
간세포에서 가장 풍부한 세포는 매끄러운 소포체이다.
사회와 문화
연구에 사용
1차 간세포는 세포 생물학 및 생약 연구에 일반적으로 사용된다.간세포에 기반한 시험관내 모델 시스템은 간의 (파토)생리학적 과정에서 간세포의 역할을 더 잘 이해하는 데 큰 도움이 되었다.또한 제약업계는 약물 대사 메커니즘을 탐색하고 생체 내 약물 대사를 예측하기 위해 현탁액 또는 배양액에서 간세포의 사용에 크게 의존해왔다.이러한 목적을 위해 간세포는 보통 2단계 과정인 콜라게나아제 소화에 의해 동물이나 사람의[5] 전체 간 또는 간 조직으로부터 분리된다.첫 번째 단계에서는 간을 칼슘 킬레이트제를 사용하여 칼슘을 제거하고 세포 밀착을 교란시키는 등방성 용액에 넣는다.다음으로 콜라게나아제를 포함한 용액을 첨가하여 간세포와 간 스트로마 사이를 분리한다.이 과정은 간세포의 현탁액을 생성하며, 여러 웰 플레이트에 씨앗을 심고 며칠 또는 몇 주 동안 배양할 수 있습니다.최적의 결과를 얻으려면 먼저 배양판을 세포외 매트릭스(예: 콜라겐, 매트리겔)로 코팅하여 간세포 부착(일반적으로 파종 후 1-3시간 이내)과 간 표현형 유지를 촉진해야 합니다.또한 간세포의 샌드위치 배양을 확립하기 위해 세포외 매트릭스의 추가 층과의 오버레이를 자주 실시한다.샌드위치 구성의 적용은 [6][7]배양에서 간세포의 장기 유지를 지원한다.즉시 사용되지 않는 갓 분리된 간세포는 저온 보존 [8]및 저장될 수 있다.그들은 배양에서 증식하지 않는다.간세포는 동결과 해동을 포함한 저온 보존 주기 동안 손상에 매우 민감하다.고전적인 저온 보호제를 첨가한 후에도 [9]저온 보존 중에 여전히 손상이 있습니다.그럼에도 불구하고, 최근의 저온 보존 및 소생 프로토콜은 대부분의 바이오 의약품 애플리케이션에 [10]대해 저온 보존 간세포 적용을 지원한다.
기타 이미지
「 」를 참조해 주세요.
레퍼런스
- ^ 사람 머리카락의 지름은 17에서 181 μm이다. Ley, Brian (1999). Elert, Glenn (ed.). "Diameter of a human hair". The Physics Factbook. Retrieved 2018-12-08.
- ^ Lodish, H., Berk, A., Zipursky, S. L., Matsdaira, P., Baltimore, D., D., Darnell, J. E. 분자 세포 생물학 (제5판)W. H. Freeman & Company뉴욕, 2000, 페이지 10
- ^ Celton-Morizur, S; Merlen, G; Couton, D; Desdouets, C (1 February 2010). "Polyploidy and liver proliferation: central role of insulin signaling" (PDF). Cell Cycle. 9 (3): 460–6. doi:10.4161/cc.9.3.10542. PMID 20090410. S2CID 22708555. Archived from the original (PDF) on 2012-04-25.
- ^ Ali ES, Hua J, Wilson CH, Tallis GA, Zhou FH, Rychkov GY, Barritt GJ (2016). "The glucagon-like peptide-1 analogue exendin-4 reverses impaired intracellular Ca2+ signalling in steatotic hepatocytes". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1863 (9): 2135–46. doi:10.1016/j.bbamcr.2016.05.006. PMID 27178543.
- ^ Lecluyse EL, Alexandre E (2010). "Isolation and culture of primary hepatocytes from resected human liver tissue". Hepatocytes. Methods Mol. Biol. Vol. 640. pp. 57–82. doi:10.1007/978-1-60761-688-7_3. ISBN 978-1-60761-687-0. PMID 20645046.
- ^ Dunn JC, Yarmush ML, Koebe HG, Tompkins RG (Feb 1989). "Hepatocyte function and extracellular matrix geometry: long-term culture in a sandwich configuration". FASEB J. 3 (2): 174–7. doi:10.1096/fasebj.3.2.2914628. PMID 2914628. S2CID 449420. 에라타 입력: FASEB J 1989년 5월; 3(7): 1873.
- ^ De Bruyn T, Chatterjee S, Fattah S, Keemink J, Nicolaï J, Augustijns P, Annaert P (May 2013). "Sandwich-cultured hepatocytes: utility for in vitro exploration of hepatobiliary drug disposition and drug-induced hepatotoxicity". Expert Opin Drug Metab Toxicol. 9 (5): 589–616. doi:10.1517/17425255.2013.773973. PMID 23452081. S2CID 27593521.
- ^ Li Albert P (2001). "Screening for human ADME/Tox drug properties in Drug Discovery". Drug Discovery Today. 6 (7): 357–366. doi:10.1016/s1359-6446(01)01712-3. PMID 11267922.
- ^ Hamel, F.; Grondin, M. L.; Denizeau, F.; Averill-Bates, D. A.; Sarhan, F. (2006). "Wheat extracts as an efficient cryoprotective agent for primary cultures of rat hepatocytes". Biotechnology and Bioengineering. 95 (4): 661–670. doi:10.1002/bit.20953. PMID 16927246. S2CID 4981423.
- ^ De Bruyn T, Ye ZW, Peeters A, Sahi J, Baes M, Augustijns PF, Annaert PP (Jul 2011). "Determination of OATP-, NTCP- and OCT-mediated substrate uptake activities in individual and pooled batches of cryopreserved human hepatocytes". Eur J Pharm Sci. 43 (4): 297–307. doi:10.1016/j.ejps.2011.05.002. PMID 21605667.
외부 링크
- 조직학 이미지: 22101ooa – 보스턴 대학의 조직학 학습 시스템 - "세포의 초미세 구조: 간세포와 정현동체"
- 간조직학:간세포(콜로라도 주립 대학교)



