이소펜테닐-이인산 델타 이성질화효소
Isopentenyl-diphosphate delta isomerase| 이소펜테닐디인산II 이성질화효소 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 이소펜테닐2인산델타 이성질가수분해효소옥타머, 테르무스 서모필러스 | |||||||||
| 식별자 | |||||||||
| EC 번호 | 5.3.3.2 | ||||||||
| CAS 번호 | 9033-27-6 | ||||||||
| 데이터베이스 | |||||||||
| 인텐츠 | IntEnz 뷰 | ||||||||
| 브렌다 | 브렌다 엔트리 | ||||||||
| ExPASy | NiceZyme 뷰 | ||||||||
| 케그 | KEGG 엔트리 | ||||||||
| 메타사이크 | 대사 경로 | ||||||||
| 프라이머리 | 프로필 | ||||||||
| PDB 구조 | RCSB PDB PDBe PDBum | ||||||||
| 진 온톨로지 | AmiGO / QuickGO | ||||||||
| |||||||||
| 이소펜테닐피로인산II 이성질화효소1 | |||||||
|---|---|---|---|---|---|---|---|
| 식별자 | |||||||
| 기호. | IDI1 | ||||||
| NCBI유전자 | 3422 | ||||||
| HGNC | 5387 | ||||||
| 옴 | 604055 | ||||||
| 참조 | NM_004508 | ||||||
| 유니프로트 | 문제 13907 | ||||||
| 기타 데이터 | |||||||
| EC 번호 | 5.3.3.2 | ||||||
| 궤적 | 성서 10절 페이지 15.3 | ||||||
| |||||||
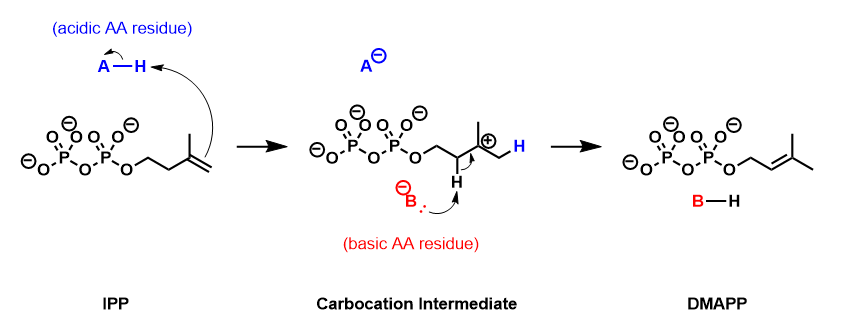
이소펜테닐 피로인산염 이성질화효소(EC 5.3.3.2, IPP 이성질화효소)[1]는 이소펜테닐-디인산 델타 이성질화효소라고도 하며 상대적으로 반응성이 낮은 이소펜테닐 피로인산염(IPP)을 보다 반응성이 높은 이소펜테닐로프로필로인산염으로 전환하는 것을 촉매하는 이성질화효소이다.이러한 이성질화는 메발론산 경로와 MEP 경로를 통한 이소프레노이드의 생합성에 있어 핵심 단계이다.
- 이소펜테닐이인산γ(\ 디메틸알릴이인산
이 효소는 이성질체, 특히 C=C 결합을 전이하는 분자내 산화환원효소에 속한다.이 효소 클래스의 계통명은 이소펜테닐-이인산 델타3-Delta2-이성체화효소이다.일반적으로 사용되는 다른 명칭으로는 이소펜테닐피로인산델타-이소머라아제, 메틸부테닐피로인산이소머라아제 [2][3][4]및 이소펜테닐피로인산이소머라아제가 있다.
효소 메커니즘
IPP 이성질화효소는 [5][6]수소의 남극 표면 전이에 의해 DMAPP에 대한 IPP의 이성질화를 촉매한다.경험적 증거는 이러한 반응이 양성자화/탈양성자 메커니즘에 의해 진행되며, 불활성화된34 C-C 이중 결합의 표면에 양성자가 추가되어 과도적 카르보케이션 [7][8]중간체가 발생한다는 것을 시사한다.C에서2 Pro-R 양성자를 제거하면 DMAPP의 C-C23 이중 결합이 형성된다.
효소구조
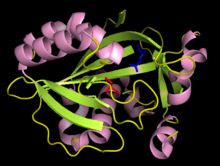
결정학 연구는 IPP 이성질화효소의 활성 형태가 α-헬리체와 β-시트가 [9][10]번갈아 존재하는 단량체라는 것을 관찰했다.IPP 이성질화효소의 활성 부위는 효소 내에 깊숙이 매장되어 있으며, 이성질화의 [9][11]남극 표면 입체 화학과 일관되게 IPP 기질의 반대쪽과 상호작용하는 글루탐산 잔기와 시스테인 잔기로 구성되어 있다.초기 양성자화 단계의 기원은 결정적으로 확립되지 않았다.최근의 증거는 글루탐산 잔기가 카르본산 곁사슬이 카르본산 [12]형태로 안정화된다는 관찰에도 불구하고 양성자화 단계에 관여한다는 것을 시사한다.이러한 차이는 인간 IPP 이성질화효소의 활성 부위에서 물 분자의 발견으로 해결되었으며, 글루타민 잔류물이 IPP의 이중 결합을 분극시키고 [13]물에 의한 양성자화에 더 민감하게 만드는 메커니즘을 제시한다.
또한 IPP 이성질화효소는 활성 배합으로 접히는 2가의 양이온을 필요로 한다.이 효소는 Mg 또는2+ [9][14]Mn과의 조정에2+ 관여하는 촉매 글루탐산염을 포함한 여러 개의 아미노산을 포함합니다.글루탐산염 잔기에 대한 금속 양이온의 배위는 양성자화 후 중간 카르바이오케이션을 안정화시킨다.
구조 연구
2007년 말 현재 이 종류의 효소에 대해 25개의 구조가 해결되었으며 PDB 가입 코드 1HX3, 1HZT, 1I9A, 1NFS, 1NFZ, 1OW2, 1P0K, 1P0N, 1PPV, 1PW, 1PQ54가 있다.
생물학적 기능
불활성 이중 결합의 양성자화는 자연에서 거의 보이지 않으며, IPP 이성질화효소의 독특한 촉매 메커니즘을 강조한다.DMAPP에 대한 IPP의 이성화는 모든 [15]생물의 생합성 경로에서 중요한 역할을 하는 화합물인 이소프레노이드와 이소프레노이드 유도체의 합성에 있어 중요한 단계이다.이소프레노이드 생합성에서 멜라본산 경로의 중요성 때문에 IPP 이성질화효소는 플라스티드와 포유류 미토콘드리아를 [16]포함한 다양한 세포 구획에서 발견된다.
질병 관련성
IPP 이성질화효소 1을 코드하는 유전자인 IDI1의 돌연변이는 효모 사카로미세스 세레비시아, 선충 케노하브디티스 엘레강스, 아라비도시스 탈리아나를 [17][18][19]포함한 많은 생물에서 생존력 감소와 관련이 있다.인간 질병에서 IDI1 돌연변이를 직접적으로 수반하는 증거는 없지만, 게놈 분석은 산발성 근위축성 측삭경화증 환자의 상당 비율에서 2개의 IPP 이성질체 유전자 근처에서 복사 번호 증가를 확인했으며, 이는 이성질체 효소가 이 [20]질환에 영향을 미칠 수 있음을 시사한다.
레퍼런스
- ^ "IDI1 - Isopentenyl-diphosphate Delta-isomerase - Saccharomyces cerevisiae (strain ATCC 204508 / S288c) (Baker's yeast) - IDI1 gene & protein". UniProt. Retrieved 6 June 2016.
- ^ Kaneda K, Kuzuyama T, Takagi M, Hayakawa Y, Seto H (2001). "An unusual isopentenyl diphosphate isomerase found in the mevalonate pathway gene cluster from Streptomyces sp. strain CL190". Proc. Natl. Acad. Sci. U.S.A. 98 (3): 932–7. doi:10.1073/pnas.020472198. PMC 14687. PMID 11158573.
- ^ Bishop JM (1983). "Cellular oncogenes and retroviruses". Annu. Rev. Biochem. 52: 301–54. doi:10.1146/annurev.bi.52.070183.001505. PMID 6351725.
- ^ Agranoff BW, Eggerer H, Henning U, Lynen F (1960). "Biosynthesis of terpenes. VII. Isopentenyl pyrophosphate isomerase". J. Biol. Chem. 235 (2): 326–32. doi:10.1016/S0021-9258(18)69523-7. PMID 13792054.
- ^ Cornforth JW, Cornforth RH, Popják G, Yengoyan L (Sep 1966). "Studies on the biosynthesis of cholesterol. XX. Steric course of decarboxylation of 5-pyrophosphomevalonate and of the carbon to carbon bond formation in the biosynthesis of farnesyl pyrophosphate". The Journal of Biological Chemistry. 241 (17): 3970–3987. doi:10.1016/S0021-9258(18)99800-5. PMID 4288360.
- ^ Cornforth RH, Popják G (1969). "Chemical syntheses of substrates of sterol biosynthesis". In Raymond BC (ed.). Methods in Enzymology. Vol. 15. Academic Press. pp. 359–390.
- ^ Reardon JE, Abeles RH (Sep 1986). "Mechanism of action of isopentenyl pyrophosphate isomerase: evidence for a carbonium ion intermediate". Biochemistry. 25 (19): 5609–5616. doi:10.1021/bi00367a040. PMID 3022798.
- ^ Street IP, Christensen DJ, Poulter CD (1990). "Hydrogen exchange during the enzyme-catalyzed isomerization of isopentenyl diphosphate and dimethylallyl diphosphate". Journal of the American Chemical Society. 112 (23): 8577–8578. doi:10.1021/ja00179a049.
- ^ a b c Hall NR, Fish DE, Hunt N, Goldin RD, Guillou PJ, Monson JR (Jun 1992). "Is the relationship between angiogenesis and metastasis in breast cancer real?". Surgical Oncology. 1 (3): 223–229. doi:10.1016/0960-7404(92)90068-v. PMID 1285217.
- ^ Zheng W, Sun F, Bartlam M, Li X, Li R, Rao Z (Mar 2007). "The crystal structure of human isopentenyl diphosphate isomerase at 1.7 A resolution reveals its catalytic mechanism in isoprenoid biosynthesis". Journal of Molecular Biology. 366 (5): 1447–1458. doi:10.1016/j.jmb.2006.12.055. PMID 17250851.
- ^ Street IP, Coffman HR, Baker JA, Poulter CD (Apr 1994). "Identification of Cys139 and Glu207 as catalytically important groups in the active site of isopentenyl diphosphate:dimethylallyl diphosphate isomerase". Biochemistry. 33 (14): 4212–4217. doi:10.1021/bi00180a014. PMID 7908830.
- ^ Wouters J, Oudjama Y, Barkley SJ, Tricot C, Stalon V, Droogmans L, Poulter CD (Apr 2003). "Catalytic mechanism of Escherichia coli isopentenyl diphosphate isomerase involves Cys-67, Glu-116, and Tyr-104 as suggested by crystal structures of complexes with transition state analogues and irreversible inhibitors". The Journal of Biological Chemistry. 278 (14): 11903–11908. doi:10.1074/jbc.M212823200. PMID 12540835.
- ^ Zhang C, Liu L, Xu H, Wei Z, Wang Y, Lin Y, Gong W (Mar 2007). "Crystal structures of human IPP isomerase: new insights into the catalytic mechanism". Journal of Molecular Biology. 366 (5): 1437–1446. doi:10.1016/j.jmb.2006.10.092. PMID 17137593.
- ^ Bonanno JB, Edo C, Eswar N, Pieper U, Romanowski MJ, Ilyin V, Gerchman SE, Kycia H, Studier FW, Sali A, Burley SK (Nov 2001). "Structural genomics of enzymes involved in sterol/isoprenoid biosynthesis". Proceedings of the National Academy of Sciences of the United States of America. 98 (23): 12896–12901. Bibcode:2001PNAS...9812896B. doi:10.1073/pnas.181466998. PMC 60796. PMID 11698677.
- ^ Bach TJ (Mar 1995). "Some new aspects of isoprenoid biosynthesis in plants--a review". Lipids. 30 (3): 191–202. doi:10.1007/BF02537822. PMID 7791527. S2CID 3999323.
- ^ Ramos-Valdivia AC, van der Heijden R, Verpoorte R (Dec 1997). "Isopentenyl diphosphate isomerase: a core enzyme in isoprenoid biosynthesis. A review of its biochemistry and function". Natural Product Reports. 14 (6): 591–603. doi:10.1039/np9971400591. PMID 9418296.
- ^ Mayer MP, Hahn FM, Stillman DJ, Poulter CD (Sep 1992). "Disruption and mapping of IDI1, the gene for isopentenyl diphosphate isomerase in Saccharomyces cerevisiae". Yeast. 8 (9): 743–748. doi:10.1002/yea.320080907. PMID 1441751. S2CID 19430360.
- ^ Yochem J, Hall DH, Bell LR, Hedgecock EM, Herman RK (Apr 2005). "Isopentenyl-diphosphate isomerase is essential for viability of Caenorhabditis elegans". Molecular Genetics and Genomics. 273 (2): 158–166. doi:10.1007/s00438-004-1101-x. PMID 15765206. S2CID 1637634.
- ^ Okada K, Kasahara H, Yamaguchi S, Kawaide H, Kamiya Y, Nojiri H, Yamane H (Apr 2008). "Genetic evidence for the role of isopentenyl diphosphate isomerases in the mevalonate pathway and plant development in Arabidopsis". Plant & Cell Physiology. 49 (4): 604–616. doi:10.1093/pcp/pcn032. PMID 18303110.
- ^ Kato T, Emi M, Sato H, Arawaka S, Wada M, Kawanami T, Katagiri T, Tsuburaya K, Toyoshima I, Tanaka F, Sobue G, Matsubara K (Nov 2010). "Segmental copy-number gain within the region of isopentenyl diphosphate isomerase genes in sporadic amyotrophic lateral sclerosis". Biochemical and Biophysical Research Communications. 402 (2): 438–442. doi:10.1016/j.bbrc.2010.10.056. PMID 20955688.
외부 링크
- 미국 국립의학도서관 의학주제표제(MeSH)의 이소펜텐일디인산염+델타이성질화효소