캔 – 잉골드 – 사전 로그 우선 순위 규칙
Cahn–Ingold–Prelog priority rules
유기화학에서 CIP(Cahn–Ingold) 서열 규칙(Robert Sydney Cahn, Christopher Kelk Ingold, 그리고 Vladimir Prelog의 이름을 따서 명명된 CIP 우선 규칙)은 분자의 입체이성질체를 완전하고 명확하게 명명하는 표준 과정입니다.[1][2]: 26 CIP 시스템의 목적은 각 입체 센터에 R 또는 S 디스크립터를 할당하고 각 이중 결합에 E 또는 Z 디스크립터를 할당하여 전체 분자의 구성을 시스템 이름에 포함시켜 고유하게 지정할 수 있도록 하는 것입니다. 분자는 임의의 수의 입체 중심과 임의의 수의 이중 결합을 포함할 수 있으며, 각각은 일반적으로 두 개의 가능한 이성질체를 생성합니다. 입체 중심의 수를 나타내는 정수 n을 가진 분자는 일반적으로 2개의n 입체 이성질체를 가지고 2개의n−1 입체 이성질체는 각각 관련된 거울상 이성질체 쌍을 가지고 있습니다.[3][4] CIP 서열 규칙은 모든 유기 분자의 모든 입체 이성질체의 정확한 명명에 기여합니다(그러나 6개의 연결을 포함하여 이 용어는 중심에 결합된 "인접 원자의 수"를 나타냅니다).[2]: 26f [4]
CIP 서열 규칙을 규정하는 주요 기사는 1966년에 발표되었고,[5] 이후 추가적인 개선 작업이 뒤따랐고,[6] 1974년 유기 명명법을 정의하는 공식 기관인 국제 순수 응용 화학 연합(IUPAC)의 규칙에 통합되었습니다.[2]: 26ff 이 규칙은 이후 개정되었으며, 가장 최근에는 2013년 IUPAC 책 유기 화학 명명법의 일부로 [7]개정되었습니다. 규칙의 IUPAC 프레젠테이션은 공식적이고 공식적인 사용 표준을 구성하며, "이 방법은 최대 4개의 결찰성을 가진 모든 화합물을 포함하도록 개발되었습니다..."라고 언급합니다. 이러한 화합물의 모든 구성과 형태에 대한 ligancy 6의 경우에도 마찬가지로 extended합니다." 그럼에도 불구하고, IUPAC 문서는 철저한 소개를 제시하고 있지만, "비교적 단순한 경우가 아닌 경우에 시퀀스 규칙을 사용하기 전에 원본 논문, 특히 1966년 논문을 연구하는 것이 필수적"이라는 주의를 포함하고 있습니다.[2]: 26f
최근 논문은 올바른 기술자가 불분명한 특정 분자를 다루기 위해 일부 규칙(서열 규칙 1b 및 2)을 변경할 것을 주장합니다.[8] 그러나 다른 문제가 남아 있습니다: 드물게, 같은 분자의 두 개의 다른 입체 이성질체가 같은 CIP 기술자를 가질 수 있으므로 CIP 시스템이 입체 이성질체에 명확하게 이름을 붙이지 못할 수 있으며 다른 시스템이 더 바람직할 수 있습니다.[9]: 27
이름 짓기 단계
CIP 시스템을 사용하여 분자를 명명하는 단계는 종종 다음과 같이 제시됩니다.
우선순위배정
R/S 및 E/Z 기술자는 각 스테레오 센터에 부착된 그룹의 순위 우선 순위를 정하는 시스템을 사용하여 할당됩니다. 시퀀스 규칙이라고도 하는 이 절차는 CIP 시스템의 핵심입니다. 이 섹션의 개요에서는 드문 경우에만 필요한 일부 규칙을 생략합니다.
- 스테레오 센터에 직접 부착된 원자의 원자 번호(Z)를 비교합니다. 높은 원자 번호 Z의 원자를 가진 그룹은 높은 우선 순위(즉, 1번)를 받습니다.
- 동점일 경우, 스테레오 센터에서 거리 2에 있는 원자를 고려해야 합니다. 스테레오 센터에 직접 연결된 원자에 결합된 추가 원자 그룹별로 목록이 작성됩니다. 각 목록은 원자 번호 Z가 감소하는 순서로 배열됩니다. 그런 다음 원자별로 목록을 비교합니다. 가장 빠른 차이는 원자 번호 Z가 더 높은 원자를 포함하는 그룹이 더 높은 우선 순위를 받습니다.
- 여전히 동점일 경우, 두 개의 목록에 있는 각 원자는 다른 원자의 하위 목록으로 대체되고(스테레오 센터에서 거리 3), 하위 목록은 원자 번호 Z의 내림차순으로 배열되며, 전체 구조는 다시 원자별로 비교됩니다. 이 과정은 고리가 끊어질 때까지 원자와 한 번씩 입체 중심에서 더 멀리 결합하는 재귀적으로 반복됩니다.
동위 원소
두 그룹이 동위원소에서만 다른 경우에는 더 큰 원자 질량을 사용하여 우선 순위를 설정합니다.[10]
이중결합과 삼중결합

원자 A가 다른 원자에 이중 결합되어 있다면, 원자 A는 "같은 원자에 두 번 연결된" 것처럼 취급되어야 합니다.[11] 이중결합을 한 원자는 단일결합을 한 원자보다 우선순위가 높습니다.[11] 이중 결합된 우선순위 그룹을 처리할 때 아크를 생성할 때 동일한 원자를 두 번 방문할 수 있습니다.[12]
B가 부착된 원자 목록으로 대체될 때 A 자체는 제외되지만 "팬텀"은 제외됩니다. 방금 따라온 결합을 따라 두 배로 돌아가지 않는다는 일반적인 원칙에 따라. 삼중 결합은 A와 B가 각각 다른 두 개의 유령 원자에 연결되어 있다는 것을 제외하고는 동일하게 취급됩니다.[2]: 28
기하학적 이성질체
원자의 두 치환기가 서로 기하학적 이성질체인 경우, Z-이성질체가 E-이성질체보다 우선순위가 높습니다. 이중결합(cis)의 같은 면에 우선순위가 높은 두 개의 그룹이 있는 입체이성질체는 "Z"로 분류됩니다. 탄소-탄소 이중결합(trans)의 반대쪽에 우선순위가 높은 두 개의 그룹이 있는 입체이성질체는 "E"로 분류됩니다.[13]
순환 분자
하나 이상의 사이클을 포함하는 분자를 처리하려면 먼저 스테레오 센터에서 시작하는 모든 가능한 경로의 결합을 통과하여 트리(계층적 디그래프라고 함)로 확장해야 합니다. 현재 경로가 이미 통과한 원자를 횡단할 때 트리를 유한하게 유지하기 위해 팬텀 원자가 생성됩니다. 원래 분자의 단일 원자는 나무의 많은 곳에 나타날 수 있습니다(어떤 곳은 유령으로, 어떤 곳은 그렇지 않습니다).[14]: 572
설명자 할당
스테레오 센터: R/S

카이랄 스플라이싱된3 이성질체는 4개의 다른 치환기를 포함합니다. 4개의 치환기는 모두 원자 번호에 따라 양성자를 할당합니다. 스테레오 센터의 대체자들이 우선순위를 지정한 후, 분자는 가장 낮은 우선순위를 가진 그룹이 관찰자로부터 멀어지도록 공간에서 배향됩니다. 대체물에 1(최우선순위)부터 4(최우선순위)까지의 번호가 매겨지면 1, 2, 3을 통과하는 곡선의 회전 감각이 입체 이성질체를 구별합니다. 구성 이성질체에서 가장 낮은 우선 순위 그룹(대부분 수소)은 판독기에서 멀어지는 평면 또는 해칭 결합 뒤에 위치합니다. 가장 우선순위가 높은 그룹은 나머지 그룹과 연결되는 호를 그리며 3순위 그룹에서 마무리됩니다. 시계 방향으로 그려진 호는 직근(R)이 할당되어 있습니다. 시계 반대 방향으로 그려진 호에는 불길한(S) 할당이 있습니다. 이름은 각각 '오른쪽'과 '왼쪽'을 뜻하는 라틴어에서 유래되었습니다.[15][16] 유기 이성질체를 명명할 때, 직근 또는 사악한 할당의 약어는 괄호 안의 이름 앞에 배치됩니다. 예를 들어, 직장이 할당된 3-메틸-1-펜텐은 (R)-3-메틸-1-펜텐으로 포맷됩니다.[12]

거울상이성질체가 R인지 S인지 판단하는 방법은 오른손 규칙으로 분자를 1→2→3 방향으로 감는다. 엄지가 네 번째 치환기 방향을 가리키면 거울상이성질체는 R이고, 그렇지 않으면 S입니다.
원자의 두 치환기가 절대적인 구성(R 또는 S)만 다른 경우도 드물게 있습니다. 이러한 치환기의 상대적 우선순위를 설정해야 하는 경우 R이 S보다 우선합니다. 이 경우, 스테레오 센터의 설명자는 일반적으로 사용되는 대문자 대신 소문자(r 또는 s)[17]입니다.
이중본드 : E/Z
이중 결합 분자의 경우 이중 결합의 치환기 우선 순위를 결정하기 위해 Can-Ingold-Prelog 우선 순위 규칙(CIP 규칙)을 따릅니다. 우선 순위가 높은 두 그룹이 이중 결합(cis 구성)의 같은 쪽에 있으면 입체 이성질체에 구성 Z(zusammen, "함께"를 의미하는 독일어 단어)가 할당됩니다. 높은 우선순위의 그룹이 이중 결합의 반대쪽에 있는 경우(트랜스 구성), 입체 이성질체에는 구성 E(엔테겐, "반대되는"[18] 의미의 독일어)가 할당됩니다.
배위화합물
입체 중심이 형성되는 경우에는 구성을 지정해야 합니다. 비공유 상호작용이 없으면 화합물은 카이랄입니다. 일부 전문가들은 이를 설명하기 위해 새로운 규칙을 제안했습니다. 이 규칙은 우선 순위를 지정할 때 "비공유 상호 작용은 0과 1 사이의 허구적인 수를 갖는다"고 명시합니다.[19] 이런 현상이 일어나는 화합물을 배위화합물이라고 합니다.
스피로 화합물
스피로 구조는 비대칭 중심이 없는 카이랄 분자를 포함합니다. 스피로 구조의 고리는 서로 직각으로 놓여 있습니다. 스피로 구조의 거울 이미지는 중첩되지 않으며 거울상이성질체라는 점에 유의해야 합니다.[12]
광학 이성질화
광학 이성질체는 중심 탄소에 4개의 다른 치환기가 부착된 화합물입니다. 광학 이성질체는 생물학적 활동에 중요한 역할을 합니다. 광학 이성질체는 평면 편광 시계방향(R) 또는 반시계방향(S)으로 회전할 수 있습니다. 광학 이성질체가 두 개의 이성질체를 만들 때, 하나는 시계 방향으로 회전하고 다른 하나는 반시계 방향으로 회전합니다. 그러나 두 이성질체의 혼합물은 평면 편광 빛을 회전시키지 않습니다. 이 두 이성질체는 화학적으로 동일할 수 있지만 구별할 수 없습니다.[12]
예
다음은 명명법의 적용 예입니다.[20]
여러 화합물에 대한 R/S 할당 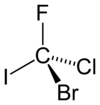
(R)-구성에 나타난 가상 분자 브로모클로로플루오로아이오도메탄은 매우 단순한 카이랄 화합물일 것입니다. 우선 순위는 원자 번호(Z)에 따라 지정됩니다: 요오드(Z = 53) > 브롬(Z = 35) > 염소(Z = 17) > 불소(Z = 9). 불소(최저 우선순위, 숫자 4)가 관찰자로부터 멀어지는 것을 허용하면 회전이 시계방향으로 진행되므로 R 할당이 이루어집니다. 
L-세린의 할당에서 가장 높은 우선순위(즉, 1번)는 아미노기(NH)의 질소 원자(Z = 7)에 부여됩니다. 히드록시메틸기(CHOH)와 카르복실산기(COOH)는 모두 탄소 원자(Z = 6)를 가지고 있으나, COOH기의 탄소 원자는 제2 산소(Z = 8)에 연결되어 있고, CHOH기의 탄소는 수소 원자(Z = 1)에 연결되어 있으므로, 후자에 우선 순위를 부여하는 것을 특징으로 하는 탄소 원자. 수소 원자에 가장 낮은 우선순위(즉, 숫자 4)가 주어지고, 이 원자가 관찰자로부터 멀어질 때, 나머지 3개의 치환기에 대한 우선순위의 반시계 방향 감소는 S로서 할당을 완료합니다. 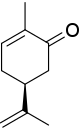
(S)-카본의 입체 센터는 하나의 수소 원자(도시되지 않음, 우선순위 4)와 3개의 탄소 원자에 연결됩니다. 이소프로필기는 우선순위 1(탄소 원자만 해당)을 가지며, 나머지 2개의 탄소 원자에 대해서는 탄소 원자가 2개의 결합을 제거하고, 케토기 1개 부분(O, O, C, 우선순위 2번) 및 알켄 1개 부분(C, C, H, 우선순위 3번)을 제거하여 우선순위를 결정하는 것을 특징으로 하는 탄소 원자. 결과적으로 반시계 방향으로 회전하면 S가 됩니다.
다중 중심 설명
화합물에 두 개 이상의 카이랄 입체 중심이 있는 경우, 각 중심은 R 또는 S로 표시됩니다. 예를 들어, 에페드린은 서로 다른 거울상 형태인 (1R,2S) 및 (1S,2R) 입체 이성질체에 존재하여 거울상 이성질체를 만듭니다. 이 화합물은 또한 에페드린이 아닌 슈도에페드린으로 명명되는 (1R,2R)과 (1S,2S)라고 쓰여진 두 개의 거울상이성질체로서 존재합니다. 이 네 가지 이성질체는 모두 계통 명명법으로 2-메틸아미노-1-페닐-1-프로판올로 명명됩니다. 그러나 에페드린과 슈도에페드린은 거울상 복사물과 관련이 없기 때문에 이성질체가 아닌 디아스테레오머, 즉 입체이성질체입니다. 슈도에페드린과 에페드린은 각각의 라세미 혼합물에 대해서도 디아스테레오머로서 화학적 성질이 다르기 때문에 다른 이름이 붙여졌습니다.
더 일반적으로, 어떤 거울상이성질체 쌍의 경우, 모든 설명자는 반대입니다: (R,R)과 (S,S)는 거울상이성질체이고 (R,S)와 (S,R)도 마찬가지입니다. 디아스테레오머는 적어도 하나의 디스크립터를 공통으로 갖는데, 예를 들어 (R,S) 및 (R,R)은 디아스테레오머이고 (S,R) 및 (S,S)도 마찬가지입니다. 이것은 2개 이상의 입체 중심을 갖는 화합물에 대해서도 마찬가지입니다: 두 입체 이성질체가 적어도 하나의 기술자를 공통으로 가지고 있다면, 그들은 디아스테레오 이성질체입니다. 모든 설명자가 반대인 경우 거울상이성질체입니다.
메소 화합물은 2개 이상의 입체 중심을 가지고 있음에도 불구하고 카이랄 분자입니다. 메조 화합물은 거울상에서 "중첩가능"하므로 2법칙에n 의해 예측되는 입체 이성질체의 수를 줄입니다. 이것은 분자가 중심 탄소-탄소 결합을 중심으로 회전하도록 하는 대칭 평면을 얻기 때문에 발생합니다.[12] 한 예는 (R,S)가 (S,R) 형태와 동일한 메조-타르산입니다. 메조 화합물에서 R과 S 입체 중심은 대칭적으로 위치한 쌍으로 발생합니다.[21]
상대구성
2개의 입체 이성질체의 상대적인 구성은 별표(*)로 기술자(R, S)에 의해 표시될 수 있습니다. (R*,R*)는 동일한 구성을 갖는 2개의 중심, (R,R) 또는 (S,S); (R*,S*)는 반대 구성을 갖는 2개의 중심, (R,S) 또는 (S,R)을 의미합니다. 우선, (IUPAC의 체계적인 번호 부여에 따라) 가장 낮은 숫자의 입체 중심에는 R* 기술자가 부여됩니다.
두 개의 아노머를 지정하기 위해 상대 입체 스크립트 알파(α) 및 베타(β)가 사용됩니다. α 아노머에서 아노머 탄소 원자와 참조 원자는 반대의 구성(R,S) 또는 (S,R)을 갖는 반면, β 아노머에서는 동일한(R,R) 또는 (S,S).[22]
얼굴들

입체화학은 케톤과 같은 삼각형 분자에 얼굴을 할당하는 역할도 합니다. 친핵성 첨가물에 포함된 친핵체는 마주보는 두 면 또는 면에서 카르보닐기에 접근할 수 있습니다. 카이랄성 친핵체가 아세톤을 공격할 때, 양쪽 얼굴은 같고 반응 생성물은 하나뿐입니다. 핵형성체가 부탄을 공격할 때, 얼굴이 동일하지 않고(생리학적) 라세미 생성물이 생성됩니다. 친핵체가 카이랄 분자일 때 디아스테레오이성질체가 형성됩니다. 분자의 한 면이 다른 면과 비교하여 치환기나 기하학적 제약에 의해 가려질 때, 그 면을 디아스테레오토픽(diastereotopic)이라고 합니다. 입체 센터의 입체 화학을 결정하는 동일한 규칙은 분자 그룹의 면을 지정할 때에도 적용됩니다. 그런 다음 얼굴을 Re-face 및 Si-face라고 합니다.[23][24] 오른쪽에 표시된 예에서는 화합물 아세토페논을 Re-face에서 봅니다. 환원 과정에서와 같이 이 쪽에서 수소화물을 추가하면 (S)-이성질체가 형성되고 반대쪽 Si-면에서 공격하면 (R)-이성질체가 생성됩니다. 그러나 화학 그룹의 우선 순위를 고려해야 하므로 Re-face에서 프로카이랄 중심에 화학 그룹을 추가하는 것이 항상 (S)-스테레오 중심으로 이어지지는 않는다는 점에 유의해야 합니다. 즉, 제품의 절대 입체화학은 어떤 면에서 공격을 받았는지를 고려하지 않고 스스로 결정됩니다. 상기 예에서, Re-face에서 프로키랄 중심에 염화물(Z = 17)을 첨가하면, (R)-이성질체가 생성됩니다.
참고 항목
참고문헌
- ^ March, Jerry; Michael B., Smith (2007). March's advanced organic chemistry : reactions, mechanisms, and structure (6. ed.). Hoboken, NJ: Wiley-Interscience. pp. 155–162. ISBN 978-0-471-72091-1.
- ^ a b c d e f Cross, L.C; Klyne, W. (1974). Rules for the Nomenclature of Organic Chemistry: Section E: Stereochemistry (Recommendations 1974) (PDF). ISBN 978-0-08-021019-3. Archived from the original (PDF) on 2016-04-07.
- ^ Clayden, Jonathan; Greeves, Nick & Warren, Stuart (2012). Organic Chemistry (2nd ed.). Oxford, UK: Oxford University Press. pp. 316f. ISBN 978-0199270293. Retrieved 2 February 2016.
- ^ a b "보통"은 그럼에도 불구하고 카이랄 중심을 가진 분자들이 대칭의 거울 평면들, 예를 들어 메소 화합물들을 가지고 있을 수 있으며, 이는 입체 이성질체들 중 일부를 "퇴화"(동일)하게 만들어 이 수학적 표현이 그 수를 과대평가한다는 사실에 근거를 두고 있습니다. 클레이든, op. cit., 317쪽 참조.
- ^ Cahn, R.S.; Ingold, C.K.; Prelog, V. (1966). "Specification of Molecular Chirality". Angewandte Chemie International Edition. 5 (4): 385–415. doi:10.1002/anie.196603851.
- ^ Prelog, V. & Helmchen, G. (1982). "Basic Principles of the CIP-System and Proposals for a Revision". Angewandte Chemie International Edition. 21 (8): 567–58. doi:10.1002/anie.198205671.
- ^ IUPAC Chemical Nomenclature and Structure Representation Division (2013). "P-9". In Favre, Henri A.; Powell, Warren H. (eds.). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. IUPAC–RSC. ISBN 978-0-85404-182-4.
- ^ Hanson, Robert M.; Mayfield, John; Vainio, Mikko; Yerin, Andrey; Redkin, Dmitry Vladimirovich; Musacchio, Sophia (30 July 2018). "Algorithmic Analysis of Cahn-Ingold-Prelog Rules of Stereochemistry: Proposals for Revised Rules and a Guide for Machine Implementation". Journal of Chemical Information and Modeling. 58 (9): 1755–1765. doi:10.1021/acs.jcim.8b00324. PMID 30059222. S2CID 51876996.
- ^ Mayfield, John; Lowe, Daniel; Sayle, Roger (2017). Comparing CIP implementations: The need for an open CIP. Abstracts of papers of the American Chemical Society. Vol. 254. Retrieved 2020-07-22. 게시자 웹 사이트의 추상화[영구적 데드링크]

- ^ Ashenhurst, James (2017-01-17). "Assigning Cahn-Ingold-Prelog (CIP) Priorities (2) - The Method of Dots". Master Organic Chemistry. Retrieved 2022-11-18.
- ^ a b "3.6 Cahn-Ingold Prelog Rules". Chemistry LibreTexts. 2014-08-05. Retrieved 2022-11-18.
- ^ a b c d e Patrick, Graham (2004). Instant Notes Organic Chemistry (2nd ed.). Garland Science. pp. 52–61. ISBN 0203427610.
- ^ Okuyama, Tadashi; Maskill, Howard (2014). Organic Chemistry, A Mechanistic Approach. Oxford University Press. pp. 38–39. ISBN 9780199693276.
- ^ Prelog, Vladlmir; Helmchen, Guenter (August 1982). "Basic Principles of the CIP-System and Proposals for a Revision". Angewandte Chemie International Edition in English. 21 (8): 567–583. doi:10.1002/anie.198205671.
- ^ Klein, David R. (2013-12-31). Organic Chemistry (2nd ed.). Wiley. p. 203. ISBN 978-1118454312.
- ^ Cahn, R. S. (March 1964). "An introduction to the sequence rule: A system for the specification of absolute configuration". Journal of Chemical Education. 41 (3): 116. Bibcode:1964JChEd..41..116C. doi:10.1021/ed041p116.
- ^ IUPAC, 화학 용어 해설서, 2ded. ("Gold Book") (1997). 온라인 수정 버전: (2006–) "가칭 탄소 원자". doi:10.1351/goldbook.P04921
- ^ International Union of Pure and Applied Chemistry. Commission on the Nomenclature of Organic Chemistry (1993). A guide to IUPAC nomenclature of organic compounds : recommendations 1993. Robert Panico, Warren H. Powell, Jean-Claude Richer. Oxford: Blackwell Scientific Publications. ISBN 0-632-03702-4. OCLC 27431284.
- ^ Elguero, José (2016-12-01). "Is it possible to extend the Cahn-Ingold-Prelog priority rules to supramolecular structures and coordination compounds using lone pairs?". Chemistry International (in German). 38 (6): 30–31. doi:10.1515/ci-2016-0633. ISSN 1365-2192. S2CID 99300397.
- ^ Harold Hart; Christopher M. Hadad; Leslie E. Craine; David J. Hart (1 January 2011). Organic Chemistry: A Short Course. Cengage Learning. pp. 177–. ISBN 978-1-133-17283-3.
- ^ Bruice, Paula Yurkanis (2007). Organic chemistry. Pearson Prentice Hall. ISBN 978-0-13-199631-1. OCLC 1046519135.
- ^ IUPAC, 화학 용어 해설서, 2ded. ("Gold Book") (1997). 온라인 수정 버전: (2006–) "상대 구성". doi:10.1351/goldbook.R05260
- ^ Moss, G. P. (1996). "Basic terminology of stereochemistry (IUPAC Recommendations 1996)". Pure and Applied Chemistry. 68 (12): 2193–2222. doi:10.1351/pac199668122193. S2CID 98272391.
- ^ IUPAC, 화학 용어 해설서, 2ded. ("Gold Book") (1997). 온라인 수정 버전: (2006–) "Re, Si". doi:10.1351/goldbook.R05308




