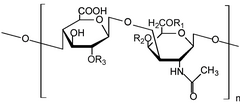
글리코사미노글리칸
Glycosaminoglycan이 글은 대부분의 독자들이 이해하기에는 너무 기술적인 것일 수도 있다. (2015년 7월)(이과 시기 |
글리코사미노글리칸[1](GAG) 또는 점막다당류는[2] 반복 이당류 단위(즉, 2당 단위)로 구성된 긴 선형 다당류다. 반복적인 2당 단위는 요당( ur sugar)과 아미노당으로 구성되는데, 요당 대신 갈락토스가 있는 케라탄을 제외한다.keratan)을 제외한다.[3] GAG는 극성이 높고 수분을 끌어들이기 때문에 몸 안에서 윤활유나 쇼크 업소버로 사용된다. 무코폴리스당류는 효소 결핍으로 글리코사미노글리칸이 비정상적으로 축적되는 대사장애의 집단이다.
생산
글리코사미노글리칸은 분자질량, 이당체 구성, 황화작용 등에서 매우 다양하다. GAG 합성은 단백질이나 핵산처럼 추진되는 템플릿이 아니라 효소를 가공해 지속적으로 변형되기 때문이다.[4]
GAG는 핵심 이당 구조를 기준으로 4개 그룹으로 분류된다.[5] 골기 장치에서는 헤파린/헤파란 황산염(HSGAGs)과 콘드로이틴 황산염/데르마탄 황산염(CSGAGs)이 합성되는데, 거친 내포체성 망막에서 만들어진 단백질 코어는 단백질을 형성하는 글리코실전달에 의해 O-연계 글리코실화 후 변형된다. 케라탄 황산염은 프로테오글리칸의 N연계 글리코실화 또는 O연계 글리코실화를 통해 핵심 단백질을 변형시킬 수 있다. GAG의 네 번째 등급인 히알루론산은 동적으로 긴 이당류 사슬을 즉시 분비하는 적분막 시네타스에 의해 합성된다.
HSGAG와 CSGAG
HSGAG와 CSGAG 수정 프로테오글리칸은 먼저 핵심 단백질에서 Ser-Gly/Ala-X-Gly 모티브로 시작한다. -GlcAβ1–3Galβ1–3Galβ1–3Galβ1–4Xylβ1-O-(Ser)-로 구성된 사트라사카리드 링커의 구성(여기서 xylosyl transferase, β4-galactosyl transferase (Gal)TI),β3-갈락토실전달효소(GalT-II), β3-GlcA전달효소(GlcAT-I)가 4개의 단당류를 전달하며, GAG 변형 단백질의 합성을 시작한다. 사타당체 링커의 첫 번째 수정은 HSGAGs 또는 CSGAGs의 추가 여부를 결정한다. GlcNAc의 추가는 HSGAG의 추가를 촉진하는 반면, 4차 당류 링커에 GalNAc를 추가하는 것은 CSGAG 개발을 촉진한다.[5] GlcNAcT-I transfers GlcNAc to the tetrasaccahride linker, which is distinct from glycosyltransferase GlcNAcT-II, the enzyme that is utilized to build HSGAGs. EXTL2 and EXTL3, two genes in the EXT tumor suppressor family, have been shown to have GlcNAcT-I activity. 반대로, GalNAc는 CsGAGs의 합성을 시작하기 위해 효소 GalNAc에 의해 링커로 전달된다. CSGAGs는 콘드로이틴 싱타아제의 GalNAc 전달효소 활성과 비교하여 뚜렷한 활동을 가질 수도 있고 아닐 수도 있다.[5]
HSGAGs에 관해서, EXT1과 EXT2 유전자 계열의 인코딩된 복합 효소인 HSGAGs는 HSGAG 체인 연장을 위해 GlcNAc와 GlcA를 모두 전달한다. 길어지는 동안 HSGAG는 동적으로 변형되는데, 첫째는 N-deacetylase, N-sulfotransferase(NDST1)에 의해 N-acetyl 그룹을 GlcNAc로부터 분리하고 그 다음 N-position을 황화시키는 이분 효소다. 다음으로 C-5 뇨닐 에피메라제가 d-GlcA를 l-IdoA에 커버한 후 2-O 슐포트란스페라제(Heparan sulfate 2-O-술포트란스페라제)에 의한 요론산당 2-O 황화효소(Heparan sulfotransferase)를 2-O로 처리한다. 마지막으로 GlcNAc moities의 6-O 및 3-O 위치는 6-O(Heparan sulfotransperase)와 3-O(3-OST) sulfotransperase에 의해 황화된다.
CSGAG를 구성하는 콘드로이틴 황산염과 피부염 황산은 각각 GlcA와 IdoA 에피머가 존재해 서로 차별화된다. C-5 뇨닐 에피메라제는 HSGAGs의 생산과 유사하게 d-GlcA를 l-IdoA로 변환하여 피부염 황산염을 합성한다. CSGAG 체인의 세 가지 황화 이벤트가 발생한다: GalNAc의 4-O 및/또는 6-O 황화 및 요산 2-O 황화. Four isoforms of the 4-O GalNAc sulfotransferases (C4ST-1, C4ST-2, C4ST-3, and D4ST-1) and three isoforms of the GalNAc 6-O sulfotransferases (C6ST, C6ST-2, and GalNAc4S-6ST) are responsible for the sulfation of GalNAc.[6]
케라탄황산염종
HSGAGs나 CSGAGs와는 달리, 케라탄 황산염 타입에 속하는 GAG의 세 번째 등급은 특정 단백질 시퀀스 모티브를 통해 생합성을 향해 추진된다. 예를 들어 빛은 각막과 연골에 EᆩPFPS.[7]Additionally의 합의를 서열과 다른 세keratansulfated proteoglycans,lumican,keratocan,mimecan(OGN), 공통 배열 NX(T/S)단백질 2차 structur와 더불어 tandemly 반복 hexapeptides 일련의,,aggrecan의 케라탄 황산 도메인 구성되어 있다.e 각질 황산염을 포함한 N-연계 올리고당 확장에 관여하기로 결정되었다.[7] 케라탄 황산염 연장은 세 종류의 케라탄 황산염을 정의하는 세 가지 연결과당류의 비절감 끝에서 시작한다. 케라탄 황산염 I(KSI)는 높은 마노오스형 전구체 올리고당을 통해 N-연계된다. Keratan sulfate II(KSII)와 Keratan sulfate III(KSIII)는 O-linked이며, KSII는 뮤신 코어 구조와 동일한 KSII 연결, KSIII는 2-O mannose와 연결된다. 각질 황산염 중합체의 연장은 Gal과 GlcNAc의 글리코실전달효소를 첨가하여 발생한다. 갈락토오스 첨가는 주로 β-1,4-갈락토실전달효소(β4Gal-T1)를 통해 발생하며, β-3-나세틸글루코사민을 담당하는 효소는 명확하게 식별되지 않았다. 마지막으로, 중합체의 황화는 두 설탕 잔류물의 6개 위치에서 발생한다. 효소 KS-Gal6ST(CHST1)는 황산염을 갈락토스로, N-acetyllucosammini-6-sulfotransferase(GlcNAc6)는 황산염을 갈락토오스(galactose)로 전달한다.ST) (CHST2)는 황산염 그룹을 각질 황산염의 단자 GlcNAc로 전송한다.[8]
히알루론산급

GAG의 네 번째 등급인 히알루론산(HA)은 황화되지 않으며, 3개의 트랜섬브레인 싱타아제 단백질인 HAS1, HAS2, HAS3에 의해 합성된다. 선형 다당류인 HA는 →4)GlcAβ(1→3)GlcNAcβ(1→)의 반복적인 이당류 단위로 구성되며 105~10Da의7 분자량이 매우 높다. 각 HAS 효소는 UDP-GlcA와 UDP-GlcNAc와 함께 공급될 때 트랜스글리코실화가 가능하다.[9][10] HAS2는 매우 큰 히알루론산 중합체를 담당하는 반면, HA의 작은 크기는 HA1과 HA3으로 합성된다. 각 HAS ISO폼이 동일한 생합성 반응을 촉진하는 반면, 각 HAS ISO폼은 독립적으로 활성화된다. 또한 HAS ISO 폼은 UDP-GlcA 및 UDPGlcNAc에 대한 Km 값이 서로 다른 것으로 나타났다.[11] 효소 활성도와 발현상의 차이를 통해 HA가 매개하는 광범위한 생물학적 함수의 스펙트럼을 조절할 수 있다고 믿으며, 이는 뇌의 하위영역에서 신경줄기세포 조절에 관여하는 것과 같다.
함수
- CSGAGs
- 내생성 헤파린은 국소화되어 돛대 세포의 분비물 과립에 저장된다. 과립 내에 존재하는 히스타민은 과립(5.2~6.0) 내에서 pH에서 양성자(HA22+)되기 때문에 음전하가 심한 헤파린은 히스타민을 정전기적으로 보존·저장하는 기능을 하는 것으로 판단된다.[12] 이 클리닉에서 헤파린은 항응고제로 투여되며 혈전증 질환의 첫 번째 선 선택이기도 하다.[13][14] 헤파란 황산염(HS)은 세포 접착, 세포 성장과 증식의 조절, 발달 과정, 지단백질 지질 및 기타 단백질의 세포 표면 결합, 혈관신생, 바이러스 침입, 종양 전이 등 수많은 생물학적 활동과 기능을 가지고 있다.[12]
CSGAGs interact with heparin binding proteins, specifically dermatan sulfate interactions with fibroblast growth factor FGF-2 and FGF-7 have been implicated in cellular proliferation and wound repair[15] while interactions with hepatic growth factor/scatter factor (HGF/SF) activate the HGF/SF signaling pathway (c-Met) through its receptor. CASGAG는 뼈, 피부, 연골에서 지지력과 접착력을 제공하는 데 중요하다. CSGAG가 CNS 발달에서 축 성장과 재생의 억제, 뇌 발달에서의 역할, 신경 유발 활동, 병원체 감염 등이 중요한 기능을 하는 것으로 알려진 다른 생물학적 기능이다.[16]
- 케라탄황산염
- 제3종 GAG의 주요 기능 중 하나인 케라탄 황산염은 조직 수화 유지다.[17] 케라탄 황산염은 눈의 뼈, 연골, 각막에 있다.[18] 정상 각막 내에서 황산피부는 완전하게 수분을 공급하고 각막 황산은 부분적으로만 수분을 공급하므로 각막 황산은 동적으로 제어되는 수분 완충제 역할을 할 수 있다.[17] KS와 같은 GAG의 수치가 변하는 황반변성증 등의 질환 상태에서는 각막 스트로마 내 수화 상실이 각막 연무의 원인이라고 여겨져 각막 투명성이 적절한 각막 황산염의 수준에 의존한다는 오랜 가설을 뒷받침한다. 케라탄 황산염 GAG는 각막을 제외한 다른 많은 조직에서 발견되는데, 이 조직들은 대식세포 접착을 조절하고, 뉴런 생장에 장벽을 형성하며, 생리주기 동안 자궁내막 자궁 안벽에 배아 이식을 조절하며, 각막 내피세포의 운동성에 영향을 미치는 것으로 알려져 있다.[17] 요약하면 KS는 세포 운동성 및 부착력뿐만 아니라 다른 잠재적인 생물학적 과정에서도 KS의 매우 중요한 기능을 제안하는 반접착 역할을 한다.
피부염황산염
피부염 황산염은 피부, 힘줄, 혈관, 심장 판막에서 기능한다.[18]
- 히알루론산
- 히알루론산은 다른 결합조직의 지반 물질뿐만 아니라 시노브 조직과 액체의 주요 성분이다. 히알루론산은 세포들을 하나로 묶고 관절을 윤활하며 안구의 모양을 유지하는데 도움을 준다.[18]히알루론산의 점탄성은 연골과 같이 서로 움직이는 관절과 표면에 윤활에 이상적이다. 낮은 전단 응력 하에서 히알루론산 용액은 높은 전단 응력 하에서보다 점도가 훨씬 높다.[19] 백혈구, 정자세포, 일부 박테리아에서 생성되는 효소인 히알루론디아제는 히알루론산을 분해하여 용액이 더 액체화되도록 한다.[18]
- 체내에서는 히알루론산이 무작위로 꼬인 코일을 형성하여 히알루론산 네트워크를 형성하여 확산 속도를 늦추고 세포간 물질의 이동을 조절하는 확산 장벽을 형성한다. 예를 들어 히알루로난은 혈장 단백질을 혈관 공간과 외혈관 공간 사이에 분할하는 데 도움을 주는데, 이는 중간체 내 고분자의 용해도에 영향을 미치고, 화학적 평형성을 변화시키며, 콜라겐 섬유의 구조를 안정화시킨다.[19]
- 기타 기능으로는 히알루론ectin, 글릴 히알루론 결합 단백질, 뇌농축 히알루론 결합 단백질, 콜라겐 VI, TSG-6, 알파간-트립신 억제제 등의 히알루론 결합 단백질과의 매트릭스 상호작용이 있다. 히알루로난과 관련된 세포 표면 상호작용은 종양 진행과 관련이 있을 수 있는 CD44와의 잘 알려진 결합이며, 또한 발달 과정, 종양 전이, 병리학적 회복 과정에 관여된 RHAMM(Hyaluronan-mediated motility receptor)과도 관련이 있다. 섬유질, 중피세포, 그리고 특정한 종류의 줄기세포는 박테리아, 적혈구 또는 다른 기질 분자로부터 자신을 보호하기 위해 히알루로난으로 구성된 심피세포 "코트"로 그들 자신을 둘러싸고 있다. 예를 들어, 줄기세포와 관련하여, 히알루로난 황산염과 함께, 줄기세포 틈새의 형성에 도움을 준다. 줄기세포는 히알루로난과 최소 황화 연두로틴 황산염의 차폐에 의해 성장 인자의 영향으로부터 보호된다. 유전자 분열을 하는 동안, 딸 세포는 성장 인자의 영향을 받아 훨씬 더 멀리 구별될 수 있는 이 심막 보호막 밖으로 이동한다.
분류
글리코사미노글리칸 계열의 구성원은 그들이 포함하는 헥소사민, 헥소오스 또는 헥수론산 단위(예: 글루코사민, 이두론산, 갈락토사민, 글루코사민)의 종류에 따라 다양하다.
그들은 또한 글리코시드 연결의 기하학에서 다양하다.
GAG의 예는 다음과 같다.
| 이름 | 헥수론산 또는 육각(케라탄의 경우) | 헥소사민 | 주요 단수체 단위 사이의 연결 기하학 | 고유 기능 |
|---|---|---|---|---|
| 콘드로이틴황산염 | GlcUA 또는 GlcUA(2S) | GalNAc 또는 GalNAc(4S) 또는 GalNAc(6S) 또는 GalNAc(4S,6S) | GlcUAβ(1→3)GalNAcβ(1→4) | 가장 널리 퍼진 GAG |
| 피부염황산염 | GlcUA 또는 IdoUA 또는 이도UA(2S) | GalNAc 또는 GalNAc(4S) 또는 GalNAc(6S) 또는 GalNAc(4S,6S) | '이도UAβ1-3'갈NAcβ1-4 | 일부 헥수론산 모노사카라이드는 글루쿠론산일 수 있지만 이두론산이 있어 콘드로이틴 황산과는 구별된다.[15] |
| 케라탄황산염 | 갈 또는 갈(6S) | GlcNAc 또는 GlcNAc(6S) | -Gal(6S)β1-4GlcNAc(6S)β1-3 | 케라탄 황산염 타입 II는 fucosylated일 수 있다.[20] |
| 헤파린 | GlcUA 또는 이도UA(2S) | GlcNAc 또는 GlcNS 또는 GlcNAc(6S) 또는 GlcNS(6S) | -이도UA(2S)α1-4GlcNS(6S)α1-4 | 알려진 생물학적 분자의 최고 음전하 밀도 |
| 황산헤파란산 | GlcUA 또는 IdoUA 또는 이도UA(2S) | GlcNAc 또는 GlcNS 또는 GlcNAc(6S) 또는 GlcNS(6S) | -GlcUAβ1-4GlcNAcα1-4 | 헤파린과 구조가 매우 유사하지만 헤파란 황산염의 이당류 단위는 황화 및 비황화 영역으로 구분된다.[21] |
| 히알루로난 주 | 글큐아 | GlcNAc | -GlcUAβ1-3GlcNAcβ1-4 | 독점적으로 비황산인 유일한 GAG |
약어
- GlcUA = β-D-글루쿠론산
- GlcUA(2S) = 2-O-술포-β-D-글루쿠론산
- 이도UA = α-L-iduronic acid
- 이도UA(2S) = 2-O-술포-α-L-이두론산
- 갈 = β-D-갈락토스
- 갈(6S) = 6-O-술포-β-D-갈락토스
- GalNAc = β-D-N-아세틸갈락토사민
- 갈나크(4S) = β-D-N-아세틸갈락토사민-4-O-황산염
- 갈나크(6S) = β-D-N-아세틸갈락토사민-6-O-황산염
- GalNAc(4S,6S) = β-D-N-아세틸갈락토사민-4-O, 6-O-황산염
- GlcNAc = α-D-N-아세틸글루코사민
- GlcNS = α-D-N-술포글루코사민
- GlcNS(6S) = α-D-N-술포글루코사민-6-O-술프산염
참고 항목
참조
- ^ 도랜드 의학 사전의 "글리코사미노글리칸"
- ^ 도랜드 의학 사전의 "무코폴리사당"
- ^ Esko, Jeffrey D; Kimata, Koji; Lindahl, Ulf (2009). "Chapter 16: Proteoglycans and Sulfated Glycosaminoglycans". Essentials of Glycobiology. Cold Spring Harbor Laboratory Press. ISBN 978-0879695590.
- ^ Caligur, Vicki (2008). "Glycosaminoglycan Sulfation and Signaling". Retrieved 25 November 2012.
- ^ Jump up to: a b c Sasisekharan, Ram; Raman, Rahul; Prabhakar, Vikas (August 2006). "Glycomics Approach to Structure-Function Relationships of Glycosaminoglycans". Annual Review of Biomedical Engineering. 8 (1): 181–231. doi:10.1146/annurev.bioeng.8.061505.095745. PMID 16834555.
- ^ Kusche-Gullberg M, Kjellén L (2003). "Sulfotransferases in glycosaminoglycan biosynthesis". Current Opinion in Structural Biology. 13 (5): 605–11. doi:10.1016/j.sbi.2003.08.002. PMID 14568616.
- ^ Jump up to: a b Funderburgh JL. (2002). "Keratan sulfate biosynthesis". IUBMB Life. 54 (4): 187–94. doi:10.1080/15216540214932. PMC 2874674. PMID 12512857.
- ^ Yamamoto Y, Takahashi I, Ogata N, Nakazawa K (2001). "Purification and characterization of N-acetylglucosaminyl sulfotransferase from chick corneas". Archives of Biochemistry and Biophysics. 392 (1): 87–92. doi:10.1006/abbi.2001.2422. PMID 11469798.
- ^ Yoshida M, Itano N, Yamada Y, Kimata K (2000). "In vitro synthesis of hyaluronan by a single protein derived from mouse HAS1 gene and characterization of amino acid residues essential for the activity". The Journal of Biological Chemistry. 275 (1): 497–506. doi:10.1074/jbc.275.1.497. PMID 10617644.
- ^ DeAngelis PL, Weigel PH (1994). "Immunochemical confirmation of the primary structure of streptococcal hyaluronan synthase and synthesis of high molecular weight product by the recombinant enzyme". Biochemistry. 33 (31): 9033–39. doi:10.1021/bi00197a001. PMID 8049203.
- ^ Itano N; Sawai T; Yoshida M; Lenas P; Yamada Y; Imagawa M; Shinomura T; Hamaguchi M; Yoshida Y; Ohnuki Y; Miyauchi S; Spicer AP; McDonald JA; Kimata K (1999). "Three isoforms of mammalian hyaluronan synthases have distinct enzymatic properties". Journal of Biological Chemistry. 274 (35): 25085–92. doi:10.1074/jbc.274.35.25085. PMID 10455188.
- ^ Jump up to: a b Rabenstein DL. (2002). "Heparin and heparan sulfate: structure and function". Natural Product Reports. 19 (3): 312–31. doi:10.1039/B100916H. PMID 12137280.
- ^ Jin L, Abrahams JP, Skinner R, Petitou M, Pike RN, Carrell RW (1997). "The anticoagulant activation of antithrombin by heparin". Proceedings of the National Academy of Sciences of the United States of America. 94 (26): 14683–88. Bibcode:1997PNAS...9414683J. doi:10.1073/pnas.94.26.14683. PMC 25092. PMID 9405673.
- ^ Rodén, L. (1989). Lane, DA (ed.). Heparin: Chemical and Biological Properties, Clinical Applications. CRC Press, Inc. p. 1.
- ^ Jump up to: a b Trowbridge JM, Gallo RL (2002). "Dermatan sulfate: new functions from an old glycosaminoglycan". Glycobiology. 12 (9): 117R–125R. doi:10.1093/glycob/cwf066. PMID 12213784.
- ^ Sugahara K, Mikami T, Uyama T, Mizuguchi S, Nomura K, Kitagawa H (2003). "Recent advances in the structural biology of chondroitin sulfate and dermatan sulfate". Current Opinion in Structural Biology. 13 (5): 612–20. doi:10.1016/j.sbi.2003.09.011. PMID 14568617.
- ^ Jump up to: a b c Funderburgh, JL. (2000). "Keratan sulfate: structure, biosynthesis, and function". Glycobiology. 10 (10): 951–58. doi:10.1093/glycob/10.10.951. PMID 11030741.
- ^ Jump up to: a b c d Tortora, Gerard J. (2013-12-31). Principles of anatomy & physiology. Derrickson, Bryan (14th ed.). Danvers, MA. ISBN 978-1-118-34500-9. OCLC 871018672.
- ^ Jump up to: a b Laurent TC, Laurent UB, Fraser JR (1996). "The structure and function of hyaluronan: An overview". Immunology and Cell Biology. 74 (2): A1-7. doi:10.1038/icb.1996.32. PMID 8724014.
- ^ Funderburgh JL. (2000). "Keratan sulfate: structure, biosynthesis, and function". Glycobiology. 10 (10): 951–58. doi:10.1093/glycob/10.10.951. PMID 11030741.
- ^ Gallagher, J.T., Lyon, M. (2000). "Molecular structure of Heparan Sulfate and interactions with growth factors and morphogens". In Iozzo, M, V. (ed.). Proteoglycans: structure, biology and molecular interactions. New York: Marcel Dekker Inc. pp. 27–59. ISBN 978-0-8247-0334-9.CS1 maint: 여러 이름: 작성자 목록(링크)
외부 링크
- 킹 M. 2005. 글리코사미노글리칸스. 2006년 12월 31일 인디아나 의과대학에 접속했다.
- 미국 국립 의학 도서관의 글리코사미노글리칸스 (MesH)
- 글리코사미노글리칸 손실의 MRI 평가(dGEMRIC 평가)